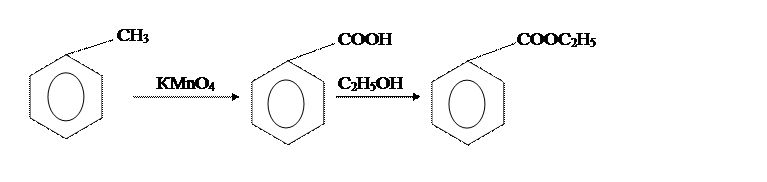
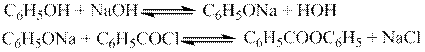Этиловый эфир бензойной кислоты ”. Бензойноэтиловый эфир
Бензойноэтиловый эфир
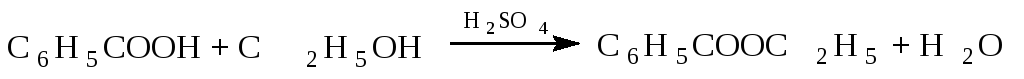
Реактивы:
Бензойная кислота 12,2 г
Этиловый спирт 35 см3
Серная кислота (конц.) 4 см 3
Углекислый натрий
Хлороформ
Хлористый кальций
В круглодонную колбу вместимостью 100 или 150 см3 помещают 12,2 г бензойной кислоты (надо помнить, что бензойная кислота раздражает кожу и дыхательные пути), 35 см3 этилового спирта, 4 см3 концентрированной серной кислоты и несколько кусочков фарфора. Смесь нагревают на водяной бане в течение трех часов с обратным холодильником. Затем заменяют холодильник нисходящим и по возможности полно отгоняют избыток спирта. Остаток после охлаждения выливают в 80 см3 холодной воды и нейтрализуют твердым углекислым натрием. Выделившееся масло извлекают хлороформом, отделяют при
29


Реактивы:
Сульфаниловая кислота 10,5 г
Нитрит натрия 4,0 г
Диметиланилин 6,0 г
Гидроксид натрия
Серная кислота (конц.)
Соляная кислота
Растворяют 2,0 г гидроксида натрия в 25 см3 воды и при нагревании в полученный раствор вносят сульфаниловую кислоту. После растворения всей кислоты жидкость должна иметь щелочную реакцию. К полученному раствору прибавляют азотистокислый натрий, охлаждают до 10 0С. Далее готовят раствор серной кислоты, добавляя к 40 см3 воды 6 см3 серной кислоты. Раствор охлаждают в бане с холодной водой, к нему добавляют 50 г толченого льда. Затем к нему в один прием добавляют раствор сульфаниловой кислоты. Начинается интенсивное образование осадка диазобензолсульфокислоты.
После этого готовят раствор диметиланилина в 50 см3 раствора соляной кислоты концентрации С(HCl)=1моль/дм3(1н.). Охлаждают полученный раствор льдом и приливают его к суспензии диазобензолсульфоновой кислоты. Жидкость начинает окрашивается в интенсивный красно-фиолетовый цвет. Затем к смеси прибавляют до ясно щелочной реакции концентрированный раствор гидроксида натрия. Раствор необходимо добавлять постепенно, не за один прием. Вскоре начинают выделяться кристаллы красителя. Под конец добавления раствора гидроксида натрия смесь застывает в сплошную массу, а цвет постепенно меняется до оранжево-желтого. Через несколько часов выделившуюся в виде красивых оранжево-красных листочков натриевую соль красителя отфильтровывают на воронке Бюхнера и перекристаллизовывают из небольшого количества воды.
Выход около 14 г.
28
Растворяют 2,0 г гидроксида натрия в 25 см3 воды и при нагревании в полученный раствор вносят сульфаниловую кислоту. После растворения всей кислоты жидкость должна иметь щелочную реакцию. К полученному раствору прибавляют азотистокислый натрий, охлаждают до 10 0С. Далее готовят раствор серной кислоты, добавляя к 40 см3 воды 6 см3 серной кислоты. Раствор охлаждают в бане с холодной водой, к нему добавляют 50 г толченого льда. Затем к нему в один прием добавляют раствор сульфаниловой кислоты. Начинается интенсивное образование осадка диазобензолсульфокислоты.
Раствор 2-нафтола в едком натре готовят следующим образом. В стакане растворяют 2,0 г гидроксида натрия в 40 см3 воды, в полученный раствор вносят 3,6 г 2-нафтола и перемешивают до растворения. Затем полученный раствор приливают при перемешивании к взвеси диазобензолсульфокислоты. Смесь перемешивают в продолжение 30 мин. Затем для уменьшения растворимости красителя прибавляют 25 г хлористого натрия и оставляют стоять стакан на льду один час, время от времени перемешивая смесь. Выпавший краситель отфильтровывают на воронке Бюхнера, промывают небольшим количеством холодной воды, тщательно отфильтровывают, снимают с фильтра и сушат на воздухе.
Выход 2- нафтолоранжа около 8 г.
studfiles.net
Бензойноэтиловый эфир - Справочник химика 21
Опыт 4. Получение бензойноэтилового эфира [c.233]Образование бензойноэтилового эфира протекает согласно уравнению [c.83]
Гидролиз бензойноэтилового эфира [c.178]
Этилбензоат (бензойноэтиловый эфир). . . . . [c.152]
Бензойноэтиловый эфир (синтез дан на с. 215, 216)...... 9,5 г [c.324]
Для бензойноэтилового эфира, как и для всех сложных эфиров, характерна реакция омыления [c.84]
Выход бензойноэтилового эфира 10-12 г. Ткип. 210 °С. [c.77]
Этилбензоат см. Бензойноэтиловый эфир. [c.294]
Бензойноэтиловый эфир 2,1 г (2 мл) Круглодонная колба на 50 мл Едкое кали 0,8 г Холодильник Либиха [c.178]Бензойноэтиловый эфир 2,1 г (2 мл) Круглодонная колба на 50 жл [c.166]
Как и в случае получения уксусноэтилового эфира, для ускорения реакции прибавляют серную кислоту. Так как бензойноэтиловый эфир труднолетуч, то для смещения равновесия вправо приходится прибавлять большой избыток спирта. [c.83]
Налейте в пробирку 3—4 мл этилового спирта и растворите в нем 1 г бензойной кислоты, после чего прилейте 7—8 капель концентрированной серной кислоты (пл. 1,84 г см ). Осторожно нагрейте иробирку на газовой горелке отметьте появление характерного мятного запаха об )азующегося бензойноэтилового эфира. [c.245]
Охладите содержимое пробирки до комнатной температуры и осторожно перелейте раствор в пробирку с водой. Перемешайте полученную смесь стеклянной палочкой и дайте отстояться в течение нескольких секунд. Какова растворимость бензойноэтилового эфира в воде [c.245]
Синтез проводят в приборе, изображенном на рис. 31, в. Получение магнийбромфенила производят по методике, описанной в предыдущем синтезе (вначале приливая 20 мл абсолютного эфира и для приготовления раствора бромбензола затрачивая 30 мл абсолютного эфира). После прибавления всего бромбензола и получасового нагревания на водяной бане до полного растворения магния, колбу охлаждают водой со льдом и приливают по каплям (при охлаждении и периодическом встряхивании колбы) раствор 9,5 г свежеперегнанного бензойноэтилового эфира в 30 мл абсолютного эфира при этом выделяется белый осадок. Затем нагревают реакционную смесь на водяной бане образуется густая кашеобразная масса. Снова охлаждают колбу льдом и постепенно вносят в нее 100 г льда, а затем по каплям раствор [c.324]
Выделившееся масло извлекают эфиром, отделяют при помощи делительной воронки эфирный слой и сушат его в течение нескольких часов хлористым кальцием. Затем переливают раствор в небольшую перегонную колбу, бросают в нее несколько стеклянных капилляров и отгоняют эфир на водяной бане. Оставшийся в колбе бензойноэтиловый эфир перегоняют на небольшом пламени (без сетки) с воздушным холодильником. [c.84]
Трифенилкарбинол получается в результате взаимодействия магнийбромфенила с этиловым эфиром бензойной кислоты, причем с молекулой эфира последовательно реагируют 2 молекулы магнийорганического соединения. Приведенные ниже уравнения иллюстрируют путь получения трифенилкарбинола из бромбензола и бензойноэтилового эфира [c.172]
К охлажденному раствору фенилмагнийбромида через капельную воронку прибавляют по каплям раствор бензойноэтилового эфира в 10 ж л абсолютного эфира и затем нагревают на водяной бане в течение 1 часа (эфир должен слабо кипеть). Охлаждают колбу, погружая ее в баню с ледяной водой, и разлагают продукт присоединения насыщенным раствором 15 г хлористого аммония. Раствор хлористого аммония постепенно приливают через капельную воронку при перемешивании жидкости. [c.173]
В круглодонную колбу емкостью 150 мл, снабженную обратным холодильником закрытым хлоркальциевой трубкой, помещают 12,2 г бензойной кислоты, 100 мл абсолютного этилового спирта и 3 мл концентрированной серной кислоты. Смесь нагревают в течение 6 ч. По окончании реакции основную массу спирта отгоняют, к остатку добавляют 100 мл воды и органическое вещество извлекают эфиром. Эфирную вытяжку взбалтывают с раствором соды (для удаления кислоты), промывают водой и сушат в течение ночи безводным сернокислым натрием. После отгонки эфира остаток перегоняют. Выход бензойноэтилового эфира 10— 12 г (68—80% теоретического), т. кип. 212° С , Ид 1,5057. [c.215]
Этшювый эфир бензоилуксусной кислоты был получен конденсацией (в присутствии этилата натрия) уксусноэтилового эфира с бензойноэтиловым эфиром ацетофенона с угольным эфиром и ацетофенона с щавелевым эфиром с последующим нагреванием действием концентрированной серной кислоты на этиловый эфир фенилпропиоловой кислотыили на а-бромкоричную кислоту взаимодействием диазоуксусного эфира с бензальдегидом , конденсацией бензола с моноэтиловым эфиром хлорангидрида малоновой кислоты в присутствии хлористого алюминия , или [c.585]
Поскольку реакция этерификации является обратимой, выход эфира тем больше, чем в большем избытке взят спирт или кислота и чем полнее удаляются из реакционной смеси сложный эфир и вода. Так, например, при получении бензойноэтилового эфира берется избыток спирта при получении уксусноэтилового эфира отгоняется эфир, так как он кипит при температуре, которая ниже температуры кипения воды при получении уксусноизоамилового эфира отгоняется вода, так как ее температура кипения ниже температуры кипения образовавшегося эфира. В последнем случае вода отгоняется в виде азеотропной смеси с темп. кип. 94° С. Такой способ получения эфира называют азеотропной этерификацией. Иногда связывают воду с помощью водоотнимающих средств (И2864, гпСЦ, СаС , А12(804)3 и др.). [c.166]
В пробирку налейте пять капель 2 н. раствора гидроксида натрия, 2—3 каили фенолфталеина и 2—3 мл уксусноэтилового эфира СН3СООС2Н5, полученного н опыте 1, а или бензойноэтилового эфира С6Н5СООС2Н5, полученного в опыте 1, б. [c.245]
В пробирку налейте 4 мл этилового спирта, 3—4 мл 10%-ного раствора NaOH и 1 мл хлористого бензоила. Содержимое пробирки нагрейте до кипения жидкость расслаивается. Верхний маслянистый слой, пахнущий мятой, представляет собой бензойноэтиловый эфир. Напишите уравнение реакции. [c.233]
chem21.info
Бензойноэтиловый эфир

Реактивы:
Бензойная кислота 12,2 г
Этиловый спирт 35 см3
Серная кислота (конц.) 4 см 3
Углекислый натрий
Хлороформ
Хлористый кальций
В круглодонную колбу вместимостью 100 или 150 см3 помещают 12,2 г бензойной кислоты (надо помнить, что бензойная кислота раздражает кожу и дыхательные пути), 35 см3 этилового спирта, 4 см3 концентрированной серной кислоты и несколько кусочков фарфора. Смесь нагревают на водяной бане в течение трех часов с обратным холодильником. Затем заменяют холодильник нисходящим и по возможности полно отгоняют избыток спирта. Остаток после охлаждения выливают в 80 см3 холодной воды и нейтрализуют твердым углекислым натрием. Выделившееся масло извлекают хлороформом, отделяют при
29


Реактивы:
Сульфаниловая кислота 10,5 г
Нитрит натрия 4,0 г
Диметиланилин 6,0 г
Гидроксид натрия
Серная кислота (конц.)
Соляная кислота
Растворяют 2,0 г гидроксида натрия в 25 см3 воды и при нагревании в полученный раствор вносят сульфаниловую кислоту. После растворения всей кислоты жидкость должна иметь щелочную реакцию. К полученному раствору прибавляют азотистокислый натрий, охлаждают до 10 оС. Далее готовят раствор серной кислоты, добавляя к 40 см3 воды 6 см3 серной кислоты. Раствор охлаждают в бане с холодной водой, к нему добавляют 50 г толченого льда. Затем к нему в один прием добавляют раствор сульфаниловой кислоты. Начинается интенсивное образование осадка диазобензолсульфокислоты.
После этого готовят раствор диметиланилина в 5 см3 раствора соляной кислоты концентрации С(HCl)=1моль/дм3(1н.). Охлаждают полученный раствор льдом и приливают его к суспензии диазобензолсульфоновой кислоты. Жидкость начинает окрашивается в интенсивный красно-фиолетовый цвет. Затем к смеси прибавляют до ясно щелочной реакции концентрированный раствор гидроксида натрия. Раствор необходимо добавлять постепенно, не за один прием. Вскоре начинают выделяться кристаллы красителя. Под конец добавления раствора гидроксида натрия смесь застывает в сплошную массу, а цвет постепенно меняется до оранжево-желтого. Через несколько часов выделившуюся в виде красивых оранжево-красных листочков натриевую соль красителя отфильтровывают на воронке Бюхнера и перекристаллизовывают из небольшого количества воды.
Выход около 14 г.
28
Растворяют 2,0 г гидроксида натрия в 25 см3 воды и при нагревании в полученный раствор вносят сульфаниловую кислоту. После растворения всей кислоты жидкость должна иметь щелочную реакцию. К полученному раствору прибавляют азотистокислый натрий, охлаждают до 10 оС. Далее готовят раствор серной кислоты, добавляя к 40 см3 воды 6 см3 серной кислоты. Раствор охлаждают в бане с холодной водой, к нему добавляют 50 г толченого льда. Затем к нему в один прием добавляют раствор сульфаниловой кислоты. Начинается интенсивное образование осадка диазобензолсульфокислоты.
Раствор 2-нафтола в едком натре готовят следующим образом. В стакане растворяют 2,0 г гидроксида натрия в 40 см3 воды, в полученный раствор вносят 3,6 г 2-нафтола и перемешивают до растворения. Затем полученный раствор приливают при перемешивании к взвеси диазобензолсульфокислоты. Смесь перемешивают в продолжение 30 мин. Затем для уменьшения растворимости красителя прибавляют 25 г хлористого натрия и оставляют стоять стакан на льду один час, время от времени перемешивая смесь. Выпавший краситель отфильтровывают на воронке Бюхнера, промывают небольшим количеством холодной воды, тщательно отфильтровывают, снимают с фильтра и сушат на воздухе.
Выход 2- нафтолоранжа около 8 г.
studfiles.net
Этиловый эфир бензойной кислоты ”
РОССИЙСКИЙ ГОСУДАРСТВЕННЫЙУНИВЕРСИТЕТ НЕФТИ И ГАЗА имени И.М.ГУБКИНА

КАФЕДРА ОРГАНИЧЕСКОЙ ХИМИИ И ХИМИИ НЕФТИ
КУРСОВАЯ РАБОТА
в практикуме по синтетическим методам органической химии
(Литературный синтез)
на тему:
“Этиловый эфир бензойной кислоты ”
Студент: Группа: ХТ-05-3
Ананьев С.С.
Преподаватель: профессор
Рябов В.Д.
Москва 2007
- ВВЕДЕНИЕ
Цель работы:
В данной работе рассмотрены физические, химические свойства и методы получения этилового эфира бензойной кислоты. В работе также была синтезирована бензойная кислота окисление бензилового спирта азотной кислотой.
- ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
- Формула соединения и его названия

Брутто-формула (система Хилла) С9Н10О2
Формула в виде текста: С6Н5СООС2Н5
Это соединение известно как этиловый эфир бензойной кислоты, этилбензоат и бензойноэтиловый эфир.
- Физические свойства соединения [5],[6]
Этиловый эфир бензойной кислоты – высококипящее, бесцветное, с фруктовым запахом.
Молекулярная масса 150,17
Плотность: 1,047 (20°C, г/см3)
Температура затвердевания -34,6°С
Температура кипения 212,6°С, 95 °С/17 мм рт. ст.;
d204 1,047;
nD20 1,5058;
Бесцветная жидкость, немного тяжелее воды, нерастворима в воде, растворима в бензоле, этаноле, диэтиловом эфире, хлороформе.
- Химические свойства соединения [7],[8]
- Как и все сложные эфиры, этиловый эфир бензойной кислоты подвержен реакциям нуклеофильного замещения(гидролиз, переэтерификация, аминолиз, гидразинолиз):

где X= OH, Nh3, RNH, R2N и др.
- В случае с третичными аминами этиловый эфир бензойной кислоты является алкилирующим агентом:

- В сложноэфирную конденсацию этиловый эфир бензойной кислоты вступает только в роли карбонильной компоненты, т.к. не имеет α-водородного атома:

- Методы получения соединения [8]
C6H5 COOR, получены впервые в 1835 г. Дюма и Пелиго действием сернометилового эфира (Ch4)2SO4 на бензойную кислоту.
Кроме того, бензойные эфиры получаются:
- Этерификация карбоновых кислот спиртами (главным образом первичными) в присутствии кислотных катализаторов.

- Ацилирование спиртов и фенолов хлорангидридами карбоновых кислот. Чаще всего, эту операцию проводят в присутствии оснований для нейтрализации выделяющегося HCl.

Ароматические ацилгалогениды реагируют медленнее, чем алифатические. По методу Шоттена-Баумана реакции ацилирования хлорангидридами проводят в водных растворах щелочей.

Ацилирование легко гидролизующимися хлорангидридами алифатических карбоновых кислот следует проводить в инертных растворителях и при охлаждении. Этот метод ацилирования часто применяют в промышленных и препаративных лабораторных синтезах.
- Ацилирование спиртов и фенолов ангидридами карбоновых кислот.

- Присоединение спиртов и фенолов к кетенам.

- ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
- Получение бензойной кислоты 10г.
Уравнение первой стадии синтеза:

Характеристики и количества вещества.
| N | Название | Формула | Характеристики | Колличества | ||||||||
| М, г/моль | Ткип, ⁰С | Тпл, ⁰С | nD20 | d420 | Теоретически | По прописи | ||||||
| м,г | ν,моль | м,г | ν, моль | V, мл | ||||||||
| 1 | Бензиловый спирт | С7Н8О | 108 | 205,4 | - | 1,5396 | 1,045 | 8,64 | 0,08 | 10,5 | 0,1 | 10 |
| 2 | Азотная кислота | HNO3 | 63 | - | - | - | 1,504 | 20,16 | 0,32 | 45 | 0,4 | 30 |
| 3 | Бензойная кислота | С7Н8О2 | 122 | - | 120 | - | - | Задано 10г. | ||||
Описание работы:

Рисунок 1 Прибор для получения бензойной кислоты
В трехгорлую колбу на 50 мл. с механической мешалкой, капельной воронкой и обратным холодильником помеместили бензиловый спирт. При нагревании на кипящей водяной бане добавили в течении 20 мин азотную кислоту. Нагревание вели до исчезновения бензилового спирта. Затем охладили смесь и отсасали кислоту на фильтре. Колба сполоснули фильтратом для большего переноса кислоты из колбы на фильтр. Перекристаллизовали из минимального количества воды. Высушили на воздухе.
Тпл=120-121⁰С.
Выход бензойной кислоты 7г.
а) Выход теоретический (ожидаемый):
108 (бензиловый спирт) – 122 (бензойная кислота) х=11,9г
10,5г (бензиловый спирт) – хг (бензойная кислота)
б) Выход в % от теоретического:
7/11,9*100=58,8%
- Получение этилбензоата исходя из 10г бензойной кислоты.
Уравнение второй стадии синтеза:

Характеристики и количества вещества.
| N | Название | Формула | Характеристики | Колличества | ||||||||
| М, г/моль | Ткип, ⁰С | Тпл, ⁰С | nD20 | d420 | Теоретически | По прописи | ||||||
| м,г | ν,моль | м,г | ν, моль | V, мл | ||||||||
| 1 | Бензойная кислота | С7Н8О2 | 122 | - | 120 | - | - | 10 | 0,08 | 10 | 0,08 | - |
| 2 | Этиловый спирт | С2Н5ОН | 46 | - | - | 1,3611 | 0,79 | 3,68 | 0,08 | 6,5 | 0,14 | 5 |
| 3 | Этил-бензоат | С9Н10О2 | 150 | 212 | - | 1,5058 | 1,047 | 12 | 0,08 | 11 | 0,07 | 0,07 |

Рисунок 2 Прибор для получения этилбензоата
Описание работы:
В круглодонную колбу поместили бензойную кислоту, 5мл бензола, 0,5 мл концентрированной серной кислоты. Реакционную смесь нагревал с обратным холодильником на кипящей водяной бане. Об окончании реакции судил по прекращению выделения воды. Суммарное количество воды, выделившейся в результете реакции 5 мл, включая азеотроп воды и бензола.
После окончания реакции перенес смесь продуктов реакции и воду из ловушки Дина-Старка в делительную воронку, где была произведена нейтрализация непрореагировавшей бензойной кислоты 5% раствором Na2CO3.
Затем после отделения водного слоя, проверили его кислотность – среда была щелочная. Промыли эфирный слой дополнительным количеством воды до нейтральной реакции.
Раствор этилбензоата поместили в перегонную колбу и бензол отгонали на песочной бане. Остаток, представляющий собой этилбензоат, перегоняли под вакуумом водоструйного насоса. Перегнаный эфир кипел при 210-212⁰С
Выход этилбензоата 7,5г. Ткип=210-212⁰С, nd20=1,5057.
а) Выход теоретический (ожидаемый):
122 (бензойная кислота) – 150 (этилбензоат) х=12,3г
10г (бензойная кислота ) – хг (этилбензоат)
б) Выход в % от теоретического:
7,5/12,3*100=61%
- Выводы:
- Список литературы:
- О.Ф.Гинзбург, «Лабораторные работы по органической химии», 1969г, стр.138.
- Справочник Бейльштейна (на немецком языке) Т.9. стр. 110-111.
- Х.Гильман, «Синтезы органических препаратов т.1», ИЛ, 1949, с.522.
- В.Н.Кошелев, В.И.Келарев, О.А.Борисова,“Основные принципы номенклатуры органических соединений”,Москва,РГУ нефти и газа им. И.М.Губкина,2002
- “Свойства органических соединений”, Под ред. А.А.Потехина Ленинград,“Химия”,1984
- “Справочник химика” в 7 томах. Том 2 – “Свойства неорганических и органических соединений”, Под ред. Б.Н.Никольского, Ленинград, “Химия”,1964.
- О.Я.Нейланд, “Органическая химия”, Москва,“Высшая школа”,1990, стр. 573–582
- В.Ф.Травень, «Ограническая химия», Москва, «Академкнига», 2005
- М.Н.Храмкина, «Практикум по органическому синтезу»,Ленинград, «Химия», 1977г, стр. 163-164.
add.coolreferat.com
Бензойный этиловый эфир - Справочник химика 21
При достаточном количестве кокаина (не менее 0,2 г),— при открытии его в порошках, напитках и т. д. — кокаин растворяют в алкоголе и прибавляют концентрированной серной кислоты. Нагревают 5 минут на кипящей водяной бане, охлаждают и осторожно разбавляют водой при этом ощущается характерный запах бензойно-этилового эфира. Реакция сводится к отщеплению от кокаина бензойной кислоты и ее открытию. [c.238] В круглодонную колбу помещают 10 г бензойной кислоты, 26 г (33 мл) абсолютного этилового спирта, 1 мл серной кислоты и тщательно перемешивают. Колбу соединяют с обратным холодильником, к которому присоединена хлоркальциевая трубка, и кипятят на водяной бане 4 ч. После окончания реакции обратный холодильник заменяют на прямой, основную массу спирта отгоняют, остаток переносят в делительную воронку, в которую наливают 100 мл воды. Бензойно-этиловый эфир извлекают 3—4 порциями эфира (по 15—20 мл). [c.169]Номенклатура сложных эфиров. Обычно сложные эфиры называют по тем кислотам и спиртам, из которых они образованы. Наиболее краткое и часто применяемое название сложных эфиров выводят из корня латинского наименования кислоты с добавлением к нему окончания аг и с указанием названия того радикала, который соответствует спирту, входящему в состав сложного эфира. Но иногда применяют и более подробные наименования. Так, например, сложные эфиры нижеследующего строения называют (а) — метилацетат, метиловый эфир уксусной кислоты, или уксуснометиловый эфир (б)—этилбензоат этиловый эфир бензойной кислоты, или бензойно-этиловый эфир [c.342]
Получение гидроперекиси бензоила. В 5-литровую круглодопную колбу Помещают 1,5 л сухого толуола и 121 г мелко растертой перекиси бензоила,, после чего суопензию охлаждаюг смесью льда с солью до —5°. Затем при энергичном перемешивании ирибавляют охлажденный ледяной водой раствор этилата натрия, полученный растворением 23 г натрия в 500 см абсолютного ширта. По прибавлении всего количества этилата натрии приливают 2 л ледяной поды, иричем перемешивание продолжают до тех пор пока практически не растворится вся перекись бензоила. Смесь переносят в охлажденную делительную воронку, толуольный раствор отделяют и вол-ньш слой экстрагируют эфиром для удаления последних следов бензойно-этилового эфира. [c.303]
Смотреть страницы где упоминается термин Бензойный этиловый эфир: [c.177] [c.198] [c.195] [c.196] [c.82] [c.95] [c.95] [c.95] [c.123] [c.301] [c.266] [c.531] Курс органической химии (0) -- [ c.421 ]Смотрите так же термины и статьи:
Анестезин Амино бензойная кислота этиловый эфир
Бензоилирование ацетоуксусного эфира этиловым эфиром бензойной кислоты
Бензойная кислота этиловый эфир
Бензойная кислота этиловый эфир, спектр
Бензойная кислота, получение этиловый эфир, реакция с треххлористым фосфором
Гидролиз этилового эфира бензойной кислоты
Получение этилового эфира бензойной кислоты
Фенилмагний бромистый этиловым эфиром бензойной кислоты
Фосфор галоидные соединения с этиловым эфиром бензойной
Этилбензоат Бензойно-этиловый эфир
Этиловый эфир бензоилацетоуксусной кислоты бензойной кислоты
Этиловый эфир бензойной кислоты (этилбензоат)
Этиловый эфир бензойной кислоты, растворимость
Этиловый эфир бензойной кислоты. Бензонафтол. Салол. Диметилфталат. Диэтилфталат. Дибутилфталат. Метиловый эфир паратолуолсульфокислоты Нитро-, диазо- и аминосоединения Алифатические нитросоединения Нитропарафины
Этиловый эфир реакция с ангидридом бензойной
хлорбутиловый эфир из тетрагидрофурана этиловый эфир нз бензойной кислоты
chem21.info
Гидразобензол

Реактивы:
Нитробензол 6,0 г
Цинковая пыль 20,0 г
Гидроксид натрия 8,0 г
Этиловый спирт
Круглодонную колбу вместимостью 250 см3 плотно соединяют двурогой насадкой; боковой отросток последней при помощи короткой (около 10 см) резиновой трубки соединяют с обратным холодильником. Такое соединение помогает энергично взбалтывать содержимое колбы. Другой (вертикальный) отрезок насадки закрывают пробкой. В колбу наливают теплый раствор гидроксида натрия в 25 см3 воды и добавляют раствор нитробензола в 12,5 см3 спирта. После этого через вертикальную трубку форштоса небольшими порциями (от 2 до 3 г) вносят цинковую пыль.
В течение всей реакции необходимо энергичное встряхивание реакционной массы. Новую порцию цинковой пыли вносят только после того, как реакция несколько замедлится. Жидкость в колбе сначала окрашивается в красный цвет, а затем становится светло-желтой. Тогда прибавляют еще 40 см3 спирта, нагревают до кипения на водяной бане и тотчас же фильтруют на воронке Бюхнера. Осадок на фильтре промывают теплым спиртом. Фильтрат охлаждают в смеси льда и соли, и после стояния в течение одного часа выпавшие кристаллы отфильтровывают на воронке Бюхнера.
Выход около 4 г.
Фенилгидроксиламин

Реактивы:
Нитробензол 17,0 г
Цинковая пыль 25,0 г
Хлористый аммоний 9,0 г
Хлористый натрий
В фарфоровый стакан вместимостью 500 см3 наливают 270 см3 воды, добавляют 9 г хлористого аммония и 17 г нитробензола. Массу энергично перемешивают механической мешалкой и в течение 30 мин. в стакан прибавляют небольшими порциями 25 г цинковой пыли.
По мере того, как идет восстановление, температура самопроизвольно повышается до 600С. В тех случаях, когда разогревания не происходит, реакционную массу нагревают до этой температуры на водяной бане.
После добавления последней порции цинковой пыли раствор перемешивают еще 45 мин.
Теплый раствор отфильтровывают на воронке Бюхнера. Осадок промывают 40 см3 горячей воды. Затем фильтрат насыщают поваренной солью (100 г) при перемешивании и помещают в охлаждающую смесь на 1 час (смесь льда и соли). Фенилгидроксиламин выделяется в виде длинных светло-желтых игл, которые отфильтровывают на воронке Бюхнера и сушат.
Выход около 8 г.
Антрон из антрахинона

Реактивы:
Антрахинон 5,0 г
Олово 5,0 г
Уксусная кислота (конц.)
Соляная кислота (конц.)
В круглодонную колбу вместимостью 200 см3, снабженную обратным холодильником, помещают 5 г антрахинона, 5 г олова и 40 см3 уксусной кислоты. (Работа в очках). Смесь нагревают на закрытой плитке и каждые 5 мин. прибавляют по 10 капель концентрированной соляной кислоты через обратный холодильник. Если через час все олово растворится, то прибавляют еще 2 г олова. Кипячение продолжают до тех пор, пока не будет прибавлено 12 см3 соляной кислоты. Если же не весь антрахинон растворится, то прибавляют еще 1 г олова и соляную кислоту до растворения антрахинона. После этого раствор фильтруют, прибавляют 50 см3 воды и охлаждают на льду. Осадок отфильтровывают, промывают водой до исчезновения запаха уксусной кислоты и высушивают на воздухе.
Выход около 4,5 г.
Примечание. Во время нагревания необходимо пользоваться экраном. Соблюдайте осторожность при работе с ледяной уксусной кислотой - она вызывает ожоги.
ФЕНОЛ


Реактивы:
Анилин 9,3 г
Серная кислота (конц.) 10 см3
Нитрит натрия 7,3 г
Эфир 60 см3
Натрий хлористый
Кальций хлористый
В толстостенный стакан наливают 50 см3 воды, при тщательном перемешивании осторожно приливают 10 см3 концентрированной серной кислоты и добавляют 9,3 г свежеперегнанного анилина. Раствор охлаждают до 00С, постепенно добавляя к нему 75 г мелко раздробленного льда при сильном перемешивании, чтобы частично выделяющийся сернокислый анилин был мелкокристаллическим.
К охлажденной смеси из капельной воронки медленно, по каплям, при сильном перемешивании приливают охлажденный до 50С раствор 7,3 г нитрита натрия в 30 см3 воды. Температура реакционной смеси при этом не должна превышать 80С.
После окончания прибавления нитрита натрия раствор соли диазония переносят в колбу вместимостью 500 см3 и нагревают на водяной бане (температура бани от 50 до 600С) до прекращения выделения азота (от 15 до 20 мин.). Полученный фенол отгоняют с водяным паром до тех пор, пока проба дистиллята не перестанет давать помутнение с бромной водой.
Дистиллят насыщают поваренной солью, переливают в делительную воронку и фенол извлекают эфиром (3 раза порциями по 20 см3). Эфирные вытяжки сушат хлористым кальцием, и эфир отгоняют на водяной бане.
Заменив водяной холодильник коротким воздушным, перегоняют фенол, собирая фракцию при температуре от 179 до 1830С в фарфоровую чашку. После охлаждения фенол должен закристаллизоваться.
Выход фенола около 6 г.
Примечание. Фенол вызывает при попадании на кожу ожоги, поэтому при работе с ним следует соблюдать осторожность. Взвешивание фенола проводить в очках и перчатках.
studfiles.net
Этиловый эфир бензойной кислоты. Формула соединения и его названия. Основание выбора схемы синтеза соединения
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
РОССИЙСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ НЕФТИ И ГАЗА им. И.М. ГУБКИНА
КАФЕДРА ОРГАНИЧЕСКОЙ ХИМИИ И ХИМИИ НЕФТИ
КУРСОВАЯ РАБОТА
по синтетическим методам органической химии
на тему:
«Этиловый эфир бензойной кислоты»
Выполнил: студент группы ХТ-06-3
Проверил: преподаватель
МОСКВА 2008 г.
Содержание
1. Введение. 3
2.Теоретическая часть. 3
2.1. Формула соединения и его названия. 3
2.2. Физические свойства соединения. 3
2.3. Химические свойства соединения. 4
2.4. Применение соединения. 6
2.5. Методы получения этилбензоата. 6
2.6. Основание выбора схемы синтеза соединения. 7
3. Экспериментальная часть. 8
3.1. Расчет количеств исходных веществ по второй стадии. 8
3.1.1. Уравнение основной и побочной реакции. 8
3.1.2. Расчет и таблица характеристик и количеств исходных реагентов и продуктов реакции. 8
3.1.3. Описание синтеза [2] 9
3.1.4 Константы полученного соединения. 10
3.2. Расчет количеств исходных веществ по первой стадии. 10
3.2.1. Уравнение основной и побочной реакции. 10
3.2.2. Расчет и таблица характеристик и количеств исходных реагентов и продуктов реакции. 10
3.2.3. Описание синтеза [2] 11
3.2.5. Схема установки. 13
4. Вывод. 14
5. Используемая литература. 15
1. Введение
По окончанию лабораторного практикума по органической химии проводится литературный анализ. Целью литературного анализа является нахождение литературы по данному веществу, проведение синтеза вещества и анализ полученных результатов.
Целью нашего синтеза является получение этилового эфира бензойной кислоты (6 г). Синтез проводится в две стадии (получение бензойной кислоты – первая стадия, получение этилового эфира бензойной кислоты – вторая стадия).
2. Теоретическая часть
2.1. Формула соединения и его названия
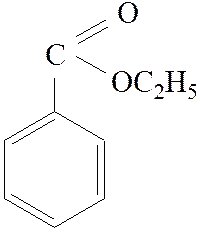
Этиловый эфир бензойной кислоты (этилбензоат)
2.2. Физические свойства соединения
- Бесцветная жидкость [7];
- Хорошо растворим в этаноле, диэтиловом эфире, плохо растворим в воде, бензоле [7];
- Температура плавления -35°С [7];
- Температура кипения 213°С [7];
- Плотность d415 1,0509 [7];
- Показатель преломления ηD15 1,5080 [7];
- Обладает характерным запахом (запах иланг-илангового масла) [7];
2.3. Химические свойства соединения
Эфиры – нейтральные и малоактивные соединения. Разбавленные кислоты, щелочи, металлический натрий и PCl5 на холоду на них не действует. [3]
I. Реакции с участием эфирного кислорода:
1.1. Образование оксониевых соединений. Эфиры присоединяют кислоты к кислороду эфира за счет его неподеленных электронов:
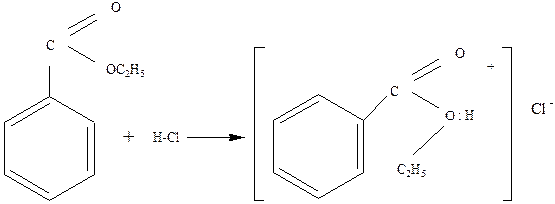
Образующиеся комплексные соли напоминают соли аммония. Оксониевые соли эфиров – обычные промежуточные продукты в их реакциях в присутствии кислот. [3]
1.2. Образование комплексных солей с различными солями:
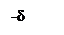
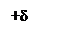
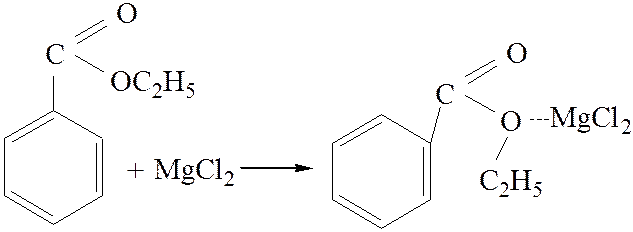 [4]
[4]
II. Реакции сопровождающиеся гомолизом α- С-Н связи:
2.1. Взаимодействие с хлором:
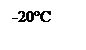
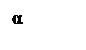
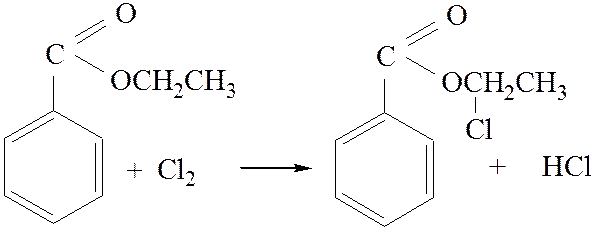 [4]
[4]
2.2. Взаимодействие с нитрилами:
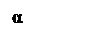
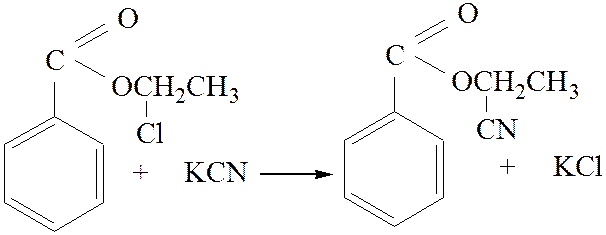 [4]
[4]
2.3. Взаимодействие с магний органическими соединениями:
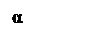
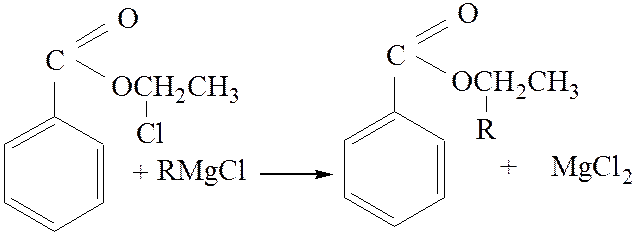 [4]
[4]
2.4. Образование гидроперекиси:
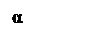
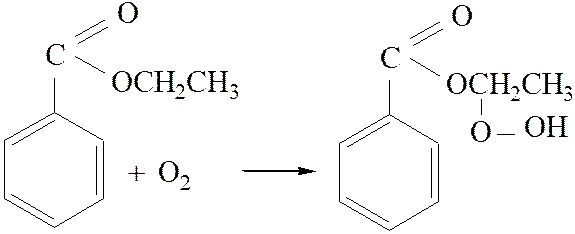 [4]
[4]
III. Реакции расщепления по эфирному кислороду:
3.1. Металлический натрий при нагревании расщепляет эфиры:
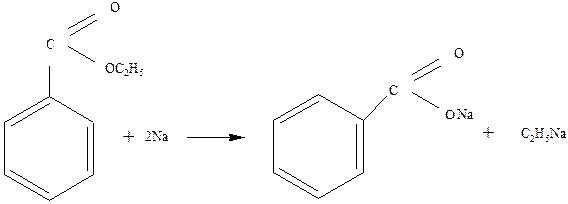
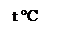
[3]
3.2. Ацидолиз. Концентрированные кислоты (серная, йодистоводородная), а также некоторые другие реагенты (хлорное железо в уксусном ангидриде, ацетилтозилаты) расщепляют эфиры по механизму SN1 или SN2:
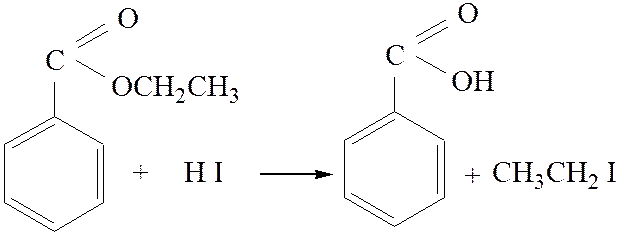 [3]
[3]
2.4. Применение соединения
Этилбензоат применяют в парфюмерии. Используют как растворитель эфиров целлюлозы. В медицине его употребляют для усиления сердечной деятельности. [4]
2.5. Методы получения этилбензоата
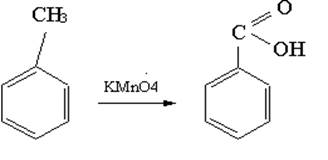
Методы получения этилбензоата отличаются только различными способами получения бензойной кислоты и условиями провидения синтеза. Так, в [6] бензойную кислоту получают из толуола и КМnО4, по реакции:
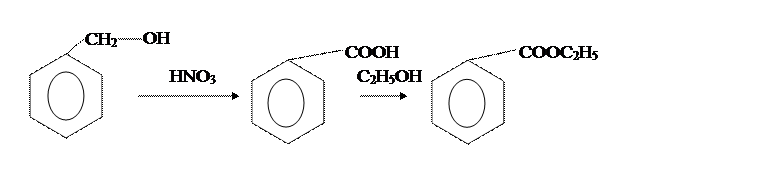
В [2] бензойную кислоту получают из бензилового спирта и концентрированной НNO3,
по реакции: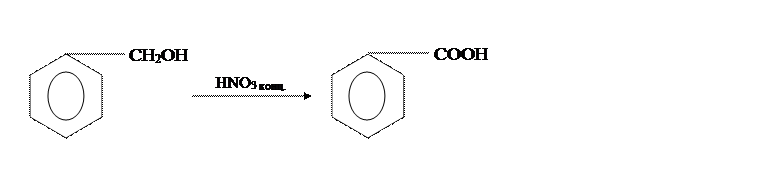
Вторая стадия отличается только способами провидения аппаративного оформления этерификации бензойной кислоты этиловым спиртом.
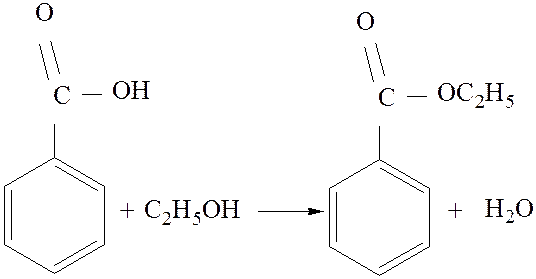 |
2.6. Основание выбора схемы синтеза соединения
Из приведенных методик наиболее оптимальна вторая. [2]
1) С учетом ограниченности времени, эта методика меньше времени занимает при ее проведении.
2) В лаборатории имеются все необходимые реактивы и приборы для проведения данной методики.
3. Экспериментальная часть
По условию нужно получить 6 г этилбензоата. Расчет по обеим стадиям начинаем с конца.
3.1. Расчет количеств исходных веществ по второй стадии.
3.1.1. Уравнение основной и побочной реакции.
Уравнение основной реакции
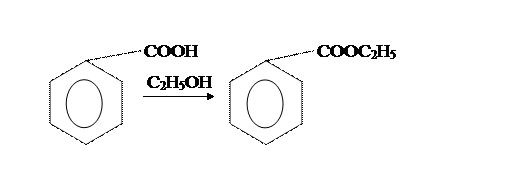
Уравнение побочной реакции
2C2H5ОН ↔ C2H5ОC2H5 + h3O
3.1.2. Расчет и таблица характеристик и количеств исходных реагентов и продуктов реакции.
А. Расчет по уравнению реакции (для получения 6 г этилбензоата):
6 г этилбензоата соответствует количество вещества:
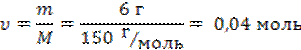
1) По уравнению: υ(C6H5-COOC2H5) : υ(C6H5-COOH) = 1 : 1
По условию: υ(C6H5-COOC2H5) : υ(C6H5-COOH) = 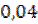 : X
: X
ð υ(C6H5-COOH) = 0,04 моль;
m(C6H5-COOH) = 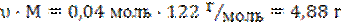
2) По уравнению: υ(C6H5-COOC2H5) : υ(C2H5-OH) = 1 : 1
По условию: υ(C6H5-COOC2H5) : υ(C2H5-OH) = 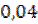 : X
: X
ð υ(C2H5-OH) = 0, 04 моль;
m(C2H5-OH) = 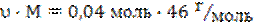 = 1,84
г
= 1,84
г
Б. Расчет количеств веществ по практикуму:
В практикуме Агрономова для получения 10 г этилбензоата используется 10 г бензойной кислоты, 26 г (33мл) этилового спирта, 1 мл h3SO4 (d=1,84):
Для синтеза 6 г этилбензоата требуется бензойной кислоты:
10 г ~ 10 г
=> х = 6 г
6 г ~ х г
Для синтеза 6 г этилбензоата требуется этилового спирта:
vunivere.ru