Диэтиловый эфир. Диэтиловый эфир o2
Диэтиловый эфир
| Диэтиловый эфир | |
| 1,1-Окси-бис-этан | |
| C 4 H 10 O | |
| 74,12 г/ моль | |
| 0,714 г/см³ | |
| 9,53 ± 0,01 эВ [1] | |
| -116,3 °C | |
| 34,65 °C | |
| 193,4 °C | |
| −49 ± 1 °F [1] | |
| 1,9 ± 0,1 об.% [1] | |
| 440 ± 1 мм рт.ст. [1] | |
| 60-29-7 | |
| 3283 | |
| 200-467-2 | |
| KI5775000 | |
| 35702 | |
| 1155 | |
| 3168 | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа) , если не указано иного. | |
Диэтиловый эфир (этиловый эфир, серный эфир, этоксиэтан). По химическим свойствам — типичный алифатический простой эфир . Широко используется в качестве растворителя . Впервые получен в Средние века.
История
Возможно, что впервые диэтиловый эфир был получен в IX веке алхимиком Джабир ибн Хайяном [2] либо алхимиком Раймундом Луллием в 1275 году [2] [3] . Достоверно известно, что он был синтезирован в 1540 году Валерием Кордусом , который назвал его «сладким купоросным маслом» ( лат. oleum dulce vitrioli ), поскольку получил его перегонкой смеси этилового спирта и серной кислоты , которая тогда называлась « купоросным маслом» [2] . Кордус также отметил его анестезирующие свойства.В 1680 г. Роберт Бойль вторично синтезировал эфир. Затем, в 1704 г. Исаак Ньютон открыл эфир в третий раз, в поисках синтеза искусственного золота. [4]
Название «эфир» было дано этому веществу в 1729 году Фробениусом [en] [5] .
В 1794 г. эфир был испытан для вдыханий с целью уменьшения болей, а в 1795 г. Беддос создал Медицинский пневматический институт для лечения различных легочных заболеваний газами. Такие газы тогда называли "искусственным воздухом". [6]
Синтез
Получают действием на этиловый спирт кислотных катализаторов при нагревании, например, перегонкой смеси этилового спирта и серной кислоты при температуре порядка 140—150 °C. Также получается как побочный продукт в производстве этилового спирта гидратацией этилена в присутствии фосфорной кислоты или 96—98 % серной кислоты при 65—75 °С и давлении 2,5 МПа. Основная часть диэтилового эфира образуется на стадии гидролиза этилсульфатов (95—100 °C, 0,2 МПа)
Свойства
- Бесцветная, прозрачная, очень подвижная, летучая жидкость со своеобразным запахом и жгучим вкусом.
- Растворимость в воде 6,5 % при 20 °C. Образует азеотропную смесь с водой (т. кип. 34,15 °C; 98,74 % диэтилового эфира). Смешивается с этанолом , бензолом , эфирными и жирными маслами во всех соотношениях.
- Легко воспламеняется, в том числе пары; в определённом соотношении с кислородом или воздухом пары эфира для наркоза взрывоопасны.
- Разлагается под действием света, тепла, воздуха и влаги с образованием токсичных альдегидов , пероксидов и кетонов , раздражающих дыхательные пути.
- Образующиеся пероксиды нестойки и взрывоопасны, они могут быть причиной самовоспламенения диэтилового эфира при хранении и взрыве при его перегонке «досуха»
По химическим свойствам диэтиловый эфир обладает всеми свойствами, характерными для простых эфиров, например, образует нестойкие оксониевые соли с сильными кислотами:
( C 2 H 5 ) 2 O + H B r → [ ( C 2 H 5 ) 2 O H ] + B r − {\displaystyle {\mathsf {(C_{2}H_{5})_{2}O+HBr\rightarrow [(C_{2}H_{5})_{2}OH]^{+}Br^{-}}}}Образует сравнительно стабильные комплексные соединения с кислотами Льюиса: (C 2 H 5 ) 2 O·BF 3
Применение
Фармакология
В медицине используется в качестве лекарственного средства общеанестезирующего действия , так как его влияние на нейронные мембраны и свойство «обездвиживать» ЦНС очень специфично и полностью обратимо. Применяется в хирургической практике для ингаляционного наркоза , а в стоматологической практике — местно, для обработки кариозных полостей и корневых каналов зуба при подготовке к пломбированию.
В связи с медленным разложением диэтилового эфира, должны строго выдерживаться установленные сроки хранения. Для наркоза можно применять эфир только из склянок, открытых непосредственно перед операцией. По истечении каждых 6 месяцев хранения эфир для наркоза проверяют на соответствие требованиям. Использование технического эфира в этих целях не допускается.
Выдающийся отечественный хирург Н.И. Пирогов , первым в истории медицины, начал оперировать раненых с эфирным обезболиванием в полевых условиях, проведя около десяти тысяч операций под эфирным наркозом.
Техника
Диэтиловый эфир — аэрозоль для быстрого запуска. Инструкция утверждает, что возможен запуск при температуре −55 °F (−48,3 °C)В СССР выпускалась пусковая жидкость «Арктика», небольшое количество заливалось во впускной коллектор через карбюратор при снятом воздушном фильтре . Для армии выпускался эфир в алюминиевой запечатанной гильзе, перед использованием гильза протыкалась штык-ножом или отвёрткой. За рубежом выпускается «жидкость для запуска в холодные дни» в аэрозольном баллоне . Состав: диэтиловый эфир, индустриальное масло , пропеллент.
Механизм запуска ДВС в этом случае по большей мере компрессионный: смесь эфира с воздухом воспламеняется от сжатия уже при степени сжатия порядка 5-6. Потерявшие компрессию по разным причинам двигатели могут делать несколько оборотов на эфире, но на бензине, тем не менее, не работают.
Примечания для "Диэтиловый эфир"
- ↑ 1 2 3 4 http://www.cdc.gov/niosh/npg/npgd0277.html
- ↑ 1 2 3 Toski, A; Bacon, DR; Calverley, RK. The history of Anesthesiology // Clinical Anesthesia / Barash, Paul G; Cullen, Bruce F; Stoelting, Robert K.. — 4th ed. — Lippincott Williams & Wilkins, 2001. — P. 3. — ISBN 978-0-7817-2268-1 .
- ↑ Hademenos, George J.; Murphree, Shaun; Zahler, Kathy; Warner, Jennifer M. McGraw-Hill's PCAT . — McGraw-Hill. — P. 39. — ISBN 978-0-07-160045-3 .
- ↑ П.Ю.Столяренко История обезболивания в стоматологии (часть 1)
- ↑ Dr. Frobenius (1729) "An account of a spiritus vini æthereus, together with several experiments tried therewith, " (недоступная ссылка) Philosophical Transactions of the Royal Society (London), 36 : 283—289.
- ↑ П.Ю.Столяренко История обезболивания в стоматологии (часть 1)
Литература
- Бабаян Э. А., Гаевский А. В., Бардин Е. В. «Правовые аспекты оборота наркотических, психотропных, сильнодействующих, ядовитых веществ и прекурсоров» М.: МЦФЭР , 2000 стр. 148
- Гурвич Я. А. «Справочник молодого аппаратчика-химика» М.: Химия , 1991 стр. 229
- Девяткин В. В., Ляхова Ю. М. «Химия для любознательных, или о чём не узнаешь на уроке» Ярославль: Академия Холдинг, 2000 стр. 48
- Рабинович В. А., Хавин З. Я. «Краткий химический справочник» Л.: Химия, 1977 стр. 148
- Гауптман 3., Органическая химия, пер. с нем., М.: Химия, 1979, с. 332-40;
- Грефе Ю., Общая органическая химия, пер. с англ., т. 2, М., 1982, с. 289—353;
- Ремане X.,Kirk-Othmer encyclopedia, v. 9, N. Y., 1980, p. 381-92.
www.cruer.com
| Диэтиловый эфир | |
| 1,1-Окси-бис-этан | |
| C4h20O | |
| 74,12 г/моль | |
| 0,714 г/см³ | |
| 9,53 ± 0,01 эВ[1] | |
| -116,3 °C | |
| 34,65 °C | |
| 193,4 °C | |
| −49 ± 1 °F[1] | |
| 1,9 ± 0,1 об.%[1] | |
| 440 ± 1 мм рт.ст.[1] | |
| 60-29-7 | |
| 3283 | |
| 200-467-2 | |
| KI5775000 | |
| 35702 | |
| 1155 | |
| 3168 | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
www.wikizero.com
Диэтиловый эфир Вики
| Диэтиловый эфир | |
| 1,1-Окси-бис-этан | |
| C4h20O | |
| 74,12 г/моль | |
| 0,714 г/см³ | |
| 9,53 ± 0,01 эВ[1] | |
| -116,3 °C | |
| 34,65 °C | |
| 193,4 °C | |
| −49 ± 1 °F[1] | |
| 1,9 ± 0,1 об.%[1] | |
| 440 ± 1 мм рт.ст.[1] | |
| 60-29-7 | |
| 3283 | |
| 200-467-2 | |
| KI5775000 | |
| 35702 | |
| 1155 | |
| 3168 | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Диэтиловый эфир (этиловый эфир, серный эфир, этоксиэтан). По химическим свойствам — типичный алифатический простой эфир. Широко используется в качестве растворителя. Впервые получен в Средние века.
История[ | код]
Возможно, что впервые диэтиловый эфир был получен в IX веке алхимиком Джабир ибн Хайяном[2] либо алхимиком Раймундом Луллием в 1275 году[2][3]. Достоверно известно, что он был синтезирован в 1540 году Валерием Кордусом, который назвал его «сладким купоросным маслом» (лат. oleum dulce vitrioli), поскольку получил его перегонкой смеси этилового спирта и серной кислоты, которая тогда называлась «купоросным маслом»[2]. Кордус также отметил его анестезирующие свойства. В 1680 г. Роберт Бойль вторично синтезировал эфир. Затем, в 1704 г. Исаак Ньютон открыл эфир в третий раз, в поисках синтеза искусственного золота.[4]
Название «эфир» было дано этому веществу в 1729 году Фробениусом[en][5].
В 1794 г. эфир был испытан для вдыханий с целью уменьшения болей, а в 1795 г. Беддос создал Медицинский пневматический институт для лечения различных легочных заболеваний газами. Такие газы тогда называли "искусственным воздухом".[6]
Синтез[ | код]
Получают действием на этиловый спирт кислотных катализаторов при нагревании, например, перегонкой смеси этилового спирта и серной кислоты при температуре порядка 140—150 °C. Также получается как побочный продукт в производстве этилового спирта гидратацией этилена в присутствии фосфорной кислоты или 96—98 % серной кислоты при 65—75 °С и давлении 2,5 МПа. Основная часть диэтилового эфира образуется на стадии гидролиза этилсульфатов (95—100 °C, 0,2 МПа)
Свойства[ | код]
- Бесцветная, прозрачная, очень подвижная, летучая жидкость со своеобразным запахом и жгучим вкусом.
- Растворимость в воде 6,5 % при 20 °C. Образует азеотропную смесь с водой (т. кип. 34,15 °C; 98,74 % диэтилового эфира). Смешивается с этанолом, бензолом, эфирными и жирными маслами во всех соотношениях.
- Легко воспламеняется, в том числе пары; в определённом соотношении с кислородом или воздухом пары эфира для наркоза взрывоопасны.
- Разлагается под действием света, тепла, воздуха и влаги с образованием токсичных альдегидов, пероксидов и кетонов, раздражающих дыхательные пути.
- Образующиеся пероксиды нестойки и взрывоопасны, они могут быть причиной самовоспламенения диэтилового эфира при хранении и взрыве при его перегонке «досуха»
По химическим свойствам диэтиловый эфир обладает всеми свойствами, характерными для простых эфиров, например, образует нестойкие оксониевые соли с сильными кислотами:
(C2H5)2O+HBr→[(C2H5)2OH]+Br−{\displaystyle {\mathsf {(C_{2}H_{5})_{2}O+HBr\rightarrow [(C_{2}H_{5})_{2}OH]^{+}Br^{-}}}}Образует сравнительно стабильные комплексные соединения с кислотами Льюиса: (C2H5)2O·BF3
Применение[ | код]
Фармакология[ | код]
В медицине используется в качестве лекарственного средства общеанестезирующего действия, так как его влияние на нейронные мембраны и свойство «обездвиживать» ЦНС очень специфично и полностью обратимо. Применяется в хирургической практике для ингаляционного наркоза, а в стоматологической практике — местно, для обработки кариозных полостей и корневых каналов зуба при подготовке к пломбированию.
В связи с медленным разложением диэтилового эфира, должны строго выдерживаться установленные сроки хранения. Для наркоза можно применять эфир только из склянок, открытых непосредственно перед операцией. По истечении каждых 6 месяцев хранения эфир для наркоза проверяют на соответствие требованиям. Использование технического эфира в этих целях не допускается.
Выдающийся отечественный хирург Н.И. Пирогов, первым в истории медицины, начал оперировать раненых с эфирным обезболиванием в полевых условиях, проведя около десяти тысяч операций под эфирным наркозом.
Техника[ | код]
Диэтиловый эфир — аэрозоль для быстрого запуска.Инструкция утверждает, что возможен запуск при температуре −55 °F (−48,3 °C)В СССР выпускалась пусковая жидкость «Арктика», небольшое количество заливалось во впускной коллектор через карбюратор при снятом воздушном фильтре. Для армии выпускался эфир в алюминиевой запечатанной гильзе, перед использованием гильза протыкалась штык-ножом или отвёрткой. За рубежом выпускается «жидкость для запуска в холодные дни» в аэрозольном баллоне. Состав: диэтиловый эфир, индустриальное масло, пропеллент.
Механизм запуска ДВС в этом случае по большей мере компрессионный: смесь эфира с воздухом воспламеняется от сжатия уже при степени сжатия порядка 5-6. Потерявшие компрессию по разным причинам двигатели могут делать несколько оборотов на эфире, но на бензине, тем не менее, не работают.
Примечания[ | код]
- ↑ 1 2 3 4 http://www.cdc.gov/niosh/npg/npgd0277.html
- ↑ 1 2 3 Toski, A; Bacon, DR; Calverley, RK. The history of Anesthesiology // Clinical Anesthesia / Barash, Paul G; Cullen, Bruce F; Stoelting, Robert K.. — 4th ed. — Lippincott Williams & Wilkins, 2001. — P. 3. — ISBN 978-0-7817-2268-1.
- ↑ Hademenos, George J.; Murphree, Shaun; Zahler, Kathy; Warner, Jennifer M. McGraw-Hill's PCAT. — McGraw-Hill. — P. 39. — ISBN 978-0-07-160045-3.
- ↑ П.Ю.Столяренко История обезболивания в стоматологии (часть 1)
- ↑ Dr. Frobenius (1729) "An account of a spiritus vini æthereus, together with several experiments tried therewith, " (недоступная ссылка) Philosophical Transactions of the Royal Society (London), 36 : 283—289.
- ↑ П.Ю.Столяренко История обезболивания в стоматологии (часть 1)
Литература[ | код]
- Бабаян Э. А., Гаевский А. В., Бардин Е. В. «Правовые аспекты оборота наркотических, психотропных, сильнодействующих, ядовитых веществ и прекурсоров» М.: МЦФЭР, 2000 стр. 148
- Гурвич Я. А. «Справочник молодого аппаратчика-химика» М.: Химия, 1991 стр. 229
- Девяткин В. В., Ляхова Ю. М. «Химия для любознательных, или о чём не узнаешь на уроке» Ярославль: Академия Холдинг, 2000 стр. 48
- Рабинович В. А., Хавин З. Я. «Краткий химический справочник» Л.: Химия, 1977 стр. 148
- Гауптман 3., Органическая химия, пер. с нем., М.: Химия, 1979, с. 332-40;
- Грефе Ю., Общая органическая химия, пер. с англ., т. 2, М., 1982, с. 289—353;
- Ремане X.,Kirk-Othmer encyclopedia, v. 9, N. Y., 1980, p. 381-92.
ru.wikibedia.ru
Диэтиловый эфир — Википедия
Материал из Википедии — свободной энциклопедии
| Диэтиловый эфир | |
| 1,1-Окси-бис-этан | |
| C4h20O | |
| 74,12 г/моль | |
| 0,714 г/см³ | |
| 9,53±0,01 эВ[1] | |
| -116,3 °C | |
| 34,65 °C | |
| 193,4 °C | |
| −49±1 °F[1] | |
| 1,9±0,1 об.%[1] | |
| 440±1 мм рт.ст.[1] | |
| 60-29-7 | |
| 3283 | |
| 200-467-2 | |
| KI5775000 | |
| 35702 | |
| 1155 | |
| 3168 | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Диэтиловый эфир (этиловый эфир, серный эфир, этоксиэтан). По химическим свойствам — типичный алифатический простой эфир. Широко используется в качестве растворителя. Впервые получен в Средние века.
История
Возможно, что впервые диэтиловый эфир был получен в IX веке алхимиком Джабир ибн Хайяном[2] либо алхимиком Раймундом Луллием в 1275 году[2][3]. Достоверно известно, что он был синтезирован в 1540 году Валерием Кордусом, который назвал его «сладким купоросным маслом» (лат. oleum dulce vitrioli), поскольку получил его перегонкой смеси этилового спирта и серной кислоты, которая тогда называлась «купоросным маслом»[2]. Кордус также отметил его анестезирующие свойства. В 1680 г. Роберт Бойль вторично синтезировал эфир. Затем, в 1704 г. Исаак Ньютон открыл эфир в третий раз, в поисках синтеза искусственного золота.[4]
Название «эфир» было дано этому веществу в 1729 году Фробениусом[en][5].
В 1794 г. эфир был испытан для вдыханий с целью уменьшения болей, а в 1795 г. Беддос создал Медицинский пневматический институт для лечения различных легочных заболеваний газами. Такие газы тогда называли "искусственным воздухом".[6]
Видео по теме
Синтез
Получают действием на этиловый спирт кислотных катализаторов при нагревании, например, перегонкой смеси этилового спирта и серной кислоты при температуре порядка 140—150 °C. Также получается как побочный продукт в производстве этилового спирта гидратацией этилена в присутствии фосфорной кислоты или 96—98 % серной кислоты при 65—75 °С и давлении 2,5 МПа. Основная часть диэтилового эфира образуется на стадии гидролиза этилсульфатов (95—100 °C, 0,2 МПа)
Свойства
- Бесцветная, прозрачная, очень подвижная, летучая жидкость со своеобразным запахом и жгучим вкусом.
- Растворимость в воде 6,5 % при 20 °C. Образует азеотропную смесь с водой (т. кип. 34,15 °C; 98,74 % диэтилового эфира). Смешивается с этанолом, бензолом, эфирными и жирными маслами во всех соотношениях.
- Легко воспламеняется, в том числе пары; в определённом соотношении с кислородом или воздухом пары эфира для наркоза взрывоопасны.
- Разлагается под действием света, тепла, воздуха и влаги с образованием токсичных альдегидов, пероксидов и кетонов, раздражающих дыхательные пути.
- Образующиеся пероксиды нестойки и взрывоопасны, они могут быть причиной самовоспламенения диэтилового эфира при хранении и взрыве при его перегонке «досуха»
По химическим свойствам диэтиловый эфир обладает всеми свойствами, характерными для простых эфиров, например, образует нестойкие оксониевые соли с сильными кислотами:
(C2H5)2O+HBr→[(C2H5)2OH]+Br−{\displaystyle {\mathsf {(C_{2}H_{5})_{2}O+HBr\rightarrow [(C_{2}H_{5})_{2}OH]^{+}Br^{-}}}}Образует сравнительно стабильные комплексные соединения с кислотами Льюиса: (C2H5)2O·BF3
Применение
Фармакология
В медицине используется в качестве лекарственного средства общеанестезирующего действия, так как его влияние на нейронные мембраны и свойство «обездвиживать» ЦНС очень специфично и полностью обратимо. Применяется в хирургической практике для ингаляционного наркоза, а в стоматологической практике — местно, для обработки кариозных полостей и корневых каналов зуба при подготовке к пломбированию.
В связи с медленным разложением диэтилового эфира, должны строго выдерживаться установленные сроки хранения. Для наркоза можно применять эфир только из склянок, открытых непосредственно перед операцией. По истечении каждых 6 месяцев хранения эфир для наркоза проверяют на соответствие требованиям. Использование технического эфира в этих целях не допускается.
Выдающийся отечественный хирург Н.И. Пирогов, первым в истории медицины, начал оперировать раненых с эфирным обезболиванием в полевых условиях, проведя около десяти тысяч операций под эфирным наркозом.
Техника
Диэтиловый эфир — аэрозоль для быстрого запуска.Инструкция утверждает, что возможен запуск при температуре −55 °F (−48,3 °C)В СССР выпускалась пусковая жидкость «Арктика», небольшое количество заливалось во впускной коллектор через карбюратор при снятом воздушном фильтре. Для армии выпускался эфир в алюминиевой запечатанной гильзе, перед использованием гильза протыкалась штык-ножом или отвёрткой. За рубежом выпускается «жидкость для запуска в холодные дни» в аэрозольном баллоне. Состав: диэтиловый эфир, индустриальное масло, пропеллент.
Механизм запуска ДВС в этом случае по большей мере компрессионный: смесь эфира с воздухом воспламеняется от сжатия уже при степени сжатия порядка 5-6. Потерявшие компрессию по разным причинам двигатели могут делать несколько оборотов на эфире, но на бензине, тем не менее, не работают.
Примечания
- ↑ 1 2 3 4 http://www.cdc.gov/niosh/npg/npgd0277.html
- ↑ 1 2 3 Toski, A; Bacon, DR; Calverley, RK. The history of Anesthesiology // Clinical Anesthesia / Barash, Paul G; Cullen, Bruce F; Stoelting, Robert K.. — 4th ed. — Lippincott Williams & Wilkins, 2001. — P. 3. — ISBN 978-0-7817-2268-1.
- ↑ Hademenos, George J.; Murphree, Shaun; Zahler, Kathy; Warner, Jennifer M. McGraw-Hill's PCAT. — McGraw-Hill. — P. 39. — ISBN 978-0-07-160045-3.
- ↑ П.Ю.Столяренко История обезболивания в стоматологии (часть 1)
- ↑ Dr. Frobenius (1729) "An account of a spiritus vini æthereus, together with several experiments tried therewith, " (недоступная ссылка) Philosophical Transactions of the Royal Society (London), 36 : 283—289.
- ↑ П.Ю.Столяренко История обезболивания в стоматологии (часть 1)
Литература
- Бабаян Э. А., Гаевский А. В., Бардин Е. В. «Правовые аспекты оборота наркотических, психотропных, сильнодействующих, ядовитых веществ и прекурсоров» М.: МЦФЭР, 2000 стр. 148
- Гурвич Я. А. «Справочник молодого аппаратчика-химика» М.: Химия, 1991 стр. 229
- Девяткин В. В., Ляхова Ю. М. «Химия для любознательных, или о чём не узнаешь на уроке» Ярославль: Академия Холдинг, 2000 стр. 48
- Рабинович В. А., Хавин З. Я. «Краткий химический справочник» Л.: Химия, 1977 стр. 148
- Гауптман 3., Органическая химия, пер. с нем., М.: Химия, 1979, с. 332-40;
- Грефе Ю., Общая органическая химия, пер. с англ., т. 2, М., 1982, с. 289—353;
- Ремане X.,Kirk-Othmer encyclopedia, v. 9, N. Y., 1980, p. 381-92.
www.wikipedia.green
Диэтиловый эфир - Gpedia, Your Encyclopedia
| Диэтиловый эфир | |
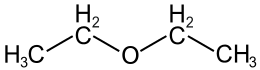 | |
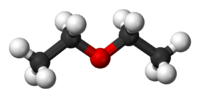 | |
| 1,1-Окси-бис-этан | |
| C4h20O | |
| 74,12 г/моль | |
| 0,714 г/см³ | |
| 9,53 ± 0,01 эВ[1] | |
| -116,3 °C | |
| 34,65 °C | |
| 193,4 °C | |
| −49 ± 1 °F[1] | |
| 1,9 ± 0,1 об.%[1] | |
| 440 ± 1 мм рт.ст.[1] | |
| 60-29-7 | |
| 3283 | |
| 200-467-2 | |
| KI5775000 | |
| 35702 | |
| 1155 | |
| 3168 | |
  | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Диэтиловый эфир (этиловый эфир, серный эфир, этоксиэтан). По химическим свойствам — типичный алифатический простой эфир. Широко используется в качестве растворителя. Впервые получен в Средние века.
История
Возможно, что впервые диэтиловый эфир был получен в IX веке алхимиком Джабир ибн Хайяном[2] либо алхимиком Раймундом Луллием в 1275 году[2][3]. Достоверно известно, что он был синтезирован в 1540 году Валерием Кордусом, который назвал его «сладким купоросным маслом» (лат. oleum dulce vitrioli), поскольку получил его перегонкой смеси этилового спирта и серной кислоты, которая тогда называлась «купоросным маслом»[2]. Кордус также отметил его анестезирующие свойства. В 1680 г. Роберт Бойль вторично синтезировал эфир. Затем, в 1704 г. Исаак Ньютон открыл эфир в третий раз, в поисках синтеза искусственного золота.[4]
Название «эфир» было дано этому веществу в 1729 году Фробениусом[en][5].
В 1794 г. эфир был испытан для вдыханий с целью уменьшения болей, а в 1795 г. Беддос создал Медицинский пневматический институт для лечения различных легочных заболеваний газами. Такие газы тогда называли "искусственным воздухом".[6]
Синтез
Получают действием на этиловый спирт кислотных катализаторов при нагревании, например, перегонкой смеси этилового спирта и серной кислоты при температуре порядка 140—150 °C. Также получается как побочный продукт в производстве этилового спирта гидратацией этилена в присутствии фосфорной кислоты или 96—98 % серной кислоты при 65—75 °С и давлении 2,5 МПа. Основная часть диэтилового эфира образуется на стадии гидролиза этилсульфатов (95—100 °C, 0,2 МПа)
Свойства
- Бесцветная, прозрачная, очень подвижная, летучая жидкость со своеобразным запахом и жгучим вкусом.
- Растворимость в воде 6,5 % при 20 °C. Образует азеотропную смесь с водой (т. кип. 34,15 °C; 98,74 % диэтилового эфира). Смешивается с этанолом, бензолом, эфирными и жирными маслами во всех соотношениях.
- Легко воспламеняется, в том числе пары; в определённом соотношении с кислородом или воздухом пары эфира для наркоза взрывоопасны.
- Разлагается под действием света, тепла, воздуха и влаги с образованием токсичных альдегидов, пероксидов и кетонов, раздражающих дыхательные пути.
- Образующиеся пероксиды нестойки и взрывоопасны, они могут быть причиной самовоспламенения диэтилового эфира при хранении и взрыве при его перегонке «досуха»
По химическим свойствам диэтиловый эфир обладает всеми свойствами, характерными для простых эфиров, например, образует нестойкие оксониевые соли с сильными кислотами:
(C2H5)2O+HBr→[(C2H5)2OH]+Br−{\displaystyle {\mathsf {(C_{2}H_{5})_{2}O+HBr\rightarrow [(C_{2}H_{5})_{2}OH]^{+}Br^{-}}}}Образует сравнительно стабильные комплексные соединения с кислотами Льюиса: (C2H5)2O·BF3
Применение
Фармакология
В медицине используется в качестве лекарственного средства общеанестезирующего действия, так как его влияние на нейронные мембраны и свойство «обездвиживать» ЦНС очень специфично и полностью обратимо. Применяется в хирургической практике для ингаляционного наркоза, а в стоматологической практике — местно, для обработки кариозных полостей и корневых каналов зуба при подготовке к пломбированию.
В связи с медленным разложением диэтилового эфира, должны строго выдерживаться установленные сроки хранения. Для наркоза можно применять эфир только из склянок, открытых непосредственно перед операцией. По истечении каждых 6 месяцев хранения эфир для наркоза проверяют на соответствие требованиям. Использование технического эфира в этих целях не допускается.
Выдающийся отечественный хирург Н.И. Пирогов, первым в истории медицины, начал оперировать раненых с эфирным обезболиванием в полевых условиях, проведя около десяти тысяч операций под эфирным наркозом.
Техника
Диэтиловый эфир — аэрозоль для быстрого запуска.Инструкция утверждает, что возможен запуск при температуре −55 °F (−48,3 °C)В СССР выпускалась пусковая жидкость «Арктика», небольшое количество заливалось во впускной коллектор через карбюратор при снятом воздушном фильтре. Для армии выпускался эфир в алюминиевой запечатанной гильзе, перед использованием гильза протыкалась штык-ножом или отвёрткой. За рубежом выпускается «жидкость для запуска в холодные дни» в аэрозольном баллоне. Состав: диэтиловый эфир, индустриальное масло, пропеллент.
Механизм запуска ДВС в этом случае по большей мере компрессионный: смесь эфира с воздухом воспламеняется от сжатия уже при степени сжатия порядка 5-6. Потерявшие компрессию по разным причинам двигатели могут делать несколько оборотов на эфире, но на бензине, тем не менее, не работают.
Примечания
- ↑ 1 2 3 4 http://www.cdc.gov/niosh/npg/npgd0277.html
- ↑ 1 2 3 Toski, A; Bacon, DR; Calverley, RK. The history of Anesthesiology // Clinical Anesthesia / Barash, Paul G; Cullen, Bruce F; Stoelting, Robert K.. — 4th ed. — Lippincott Williams & Wilkins, 2001. — P. 3. — ISBN 978-0-7817-2268-1.
- ↑ Hademenos, George J.; Murphree, Shaun; Zahler, Kathy; Warner, Jennifer M. McGraw-Hill's PCAT. — McGraw-Hill. — P. 39. — ISBN 978-0-07-160045-3.
- ↑ П.Ю.Столяренко История обезболивания в стоматологии (часть 1)
- ↑ Dr. Frobenius (1729) "An account of a spiritus vini æthereus, together with several experiments tried therewith, " (недоступная ссылка) Philosophical Transactions of the Royal Society (London), 36 : 283—289.
- ↑ П.Ю.Столяренко История обезболивания в стоматологии (часть 1)
Литература
- Бабаян Э. А., Гаевский А. В., Бардин Е. В. «Правовые аспекты оборота наркотических, психотропных, сильнодействующих, ядовитых веществ и прекурсоров» М.: МЦФЭР, 2000 стр. 148
- Гурвич Я. А. «Справочник молодого аппаратчика-химика» М.: Химия, 1991 стр. 229
- Девяткин В. В., Ляхова Ю. М. «Химия для любознательных, или о чём не узнаешь на уроке» Ярославль: Академия Холдинг, 2000 стр. 48
- Рабинович В. А., Хавин З. Я. «Краткий химический справочник» Л.: Химия, 1977 стр. 148
- Гауптман 3., Органическая химия, пер. с нем., М.: Химия, 1979, с. 332-40;
- Грефе Ю., Общая органическая химия, пер. с англ., т. 2, М., 1982, с. 289—353;
- Ремане X.,Kirk-Othmer encyclopedia, v. 9, N. Y., 1980, p. 381-92.
www.gpedia.com
Диэтиловый эфир - это... Что такое Диэтиловый эфир?
Диэтиловый эфир (этиловый эфир, серный эфир).
По химическим свойствам — типичный алифатический простой эфир.Свойства
- Бесцветная, прозрачная, очень подвижная, летучая жидкость со своеобразным запахом и жгучим вкусом.
- Разлагается под действием света, тепла, воздуха и влаги с образованием токсичных альдегидов, пероксидов и кетонов, раздражающих дыхательные пути.
- Растворимость в воде 6,5 % при 20 °C. Образует азеотропную смесь с водой (т. кип. 34,15 °C; 98,74 % диэтилового эфира). Смешивается со спиртом, бензолом, эфирными и жирными маслами во всех соотношениях.
- Легко воспламеняется, в том числе пары; в определённом соотношении с кислородом или воздухом пары эфира для наркоза взрывоопасны.
Синтез
Впервые получен в XIII веке алхимиком Луллием.
Получают действием на этиловый спирт кислотных катализаторов при нагревании, например перегонкой смеси этилового спирта и h3SO4 при температуре порядка 140—150 °C.
Применение
Фармакология
В медицине используется в качестве лекарственного средства общеанестезирующего действия и применяется в хирургической практике для ингаляционного наркоза, а в стоматологической практике — местно, для обработки кариозных полостей и корневых каналов зуба при подготовке к пломбированию.
Техника
Диэтиловый эфир — аэрозоль для быстрого запуска. Инструкция утверждает, что возможен запуск при температуре — 55 °FВ СССР выпускалась пусковая жидкость «Арктика», небольшое количество заливалось во впускной коллектор через карбюратор при снятом воздушном фильтре. За рубежом выпускается «жидкость для запуска в холодные дни» в аэрозольном баллоне. Состав: диэтиловый эфир, индустриальное масло, пропеллент.
Литература
- Бабаян Э. А., Гаевский А. В., Бардин Е. В. «Правовые аспекты оборота наркотических, психотропных, сильнодействующих, ядовитых веществ и прекурсоров» М.: МЦФЭР, 2000 стр. 148
- Гурвич Я. А. «Справочник молодого аппаратчика-химика» М.:Химия, 1991 стр. 229
- Девяткин В. В., Ляхова Ю. М. «Химия для любознательных, или о чем не узнаешь на уроке» Ярославль: Академия Холдинг, 2000 стр. 48
- Рабинович В. А., Хавин З. Я. «Краткий химический справочник» Л.: Химия, 1977 стр. 148
- Гауптман 3., Органическая химия, пер. с нем., М., 1979, с. 332-40;
- Грефе Ю.,Общая органическая химия, пер. с англ., т. 2, М., 1982, с. 289—353;
- Ремане X.,Kirk-Othmer encyclopedia, v. 9, N. Y., 1980, p. 381-92.
ushakov.academic.ru
Эфир диэтиловый - Википедия
Материал из Википедии — свободной энциклопедии
(перенаправлено с «»)Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 11 августа 2017; проверки требует 1 правка. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 11 августа 2017; проверки требует 1 правка.| Диэтиловый эфир | |
| 1,1-Окси-бис-этан | |
| C4h20O | |
| 74,12 г/моль | |
| 0,714 г/см³ | |
| 9,53±0,01 эВ[1] | |
| -116,3 °C | |
| 34,65 °C | |
| 193,4 °C | |
| -49±1 °F[1] | |
| 1,9±0,1 об.%[1] | |
| 440±1 мм рт. ст.[1] | |
| 60-29-7 | |
| 3283 | |
| 200-467-2 | |
| KI5775000 | |
| 35702 | |
| 1155 | |
| 3168 | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Диэтиловый эфир (этиловый эфир, серный эфир). По химическим свойствам — типичный алифатический простой эфир. Широко используется в качестве растворителя. Впервые получен в Средние века.
История[ | ]
Возможно, что впервые диэтиловый эфир был получен в IX веке алхимиком Джабир ибн Хайяном[2] либо алхимиком Раймундом Луллием в 1275 году[2][3]. Достоверно известно, что он был синтезирован в 1540 году Валерием Кордусом, который назвал его «сладким купоросным маслом» (лат. oleum dulce vitrioli), поскольку получил его перегонкой смеси этилового спирта и серной кислоты, которая тогда называлась «купоросным маслом»[2]. Кордус также отметил его анестезирующие свойства.
Название «эфир» было дано этому веществу в 1729 году [en][4].
Синтез[ | ]
Получают действием на этиловый спирт кислотных катализаторов при нагревании, например, перегонкой смеси этилового спирта и серной кислоты при температуре порядка 140—150 °C. Также получается как побочный продукт в производстве этилового спирта гидратацией этилена в присутствии фосфорной кислоты или 96—98 % серной кислоты при 65—75 °С и давлении 2,5 МПа. Основная часть диэтилового эфира образуется на стадии гидролиза этилсульфатов (95—100 °C, 0,2 МПа)
Свойства[ | ]
- Бесцветная, прозрачная, очень подвижная, летучая жидкость со своеобразным запахом и жгучим вкусом.
- Растворимость в воде 6,5 % при 20 °C. Образует азеотропную смесь с водой (т. кип. 34,15 °C; 98,74 % диэтилового эфира). Смешивается с этанолом, бензолом, эфирными и жирными маслами во всех соотношениях.
- Легко воспламеняется, в том числе пары; в определённом соотношении с кислородом или воздухом пары эфира для наркоза взрывоопасны.
- Разлагается под действием света, тепла, воздуха и влаги с образованием токсичных альдегидов, пероксидов и кетонов, раздражающих дыхательные пути.
- Образующиеся пероксиды нестойки и взрывоопасны, они могут быть причиной самовоспламенения диэтилового эфира при хранении и взрыве при его перегонке «досуха»
По химическим свойствам диэтиловый эфир обладает всеми свойствами, характерными для простых эфиров, например, образует нестойкие оксониевые соли с сильными кислотами:
(C2H5)2O+HBr→[(C2H5)2OH]+Br−{\displaystyle {\mathsf {(C_{2}H_{5})_{2}O+HBr\rightarrow [(C_{2}H_{5})_{2}OH]^{+}Br^{-}}}}Образует сравнительно стабильные комплексные соединения с кислотами Льюиса: (C2H5)2O·BF3
Применение[ | ]
Фармакология[ | ]
В медицине используется в качестве лекарственного средства общеанестезирующего действия, так как его влияние на нейронные мембраны и свойство «обездвиживать» ЦНС очень специфично и полностью обратимо. Применяется в хирургической практике для ингаляционного наркоза, а в стоматологической практике — местно, для обработки кариозных полостей и корневых каналов зуба при подготовке к пломбированию.
В связи с медленным разложением диэтилового эфира, должны строго выдерживаться установленные сроки хранения. Для наркоза можно применять эфир только из склянок, открытых непосредственно перед операцией. По истечении каждых 6 месяцев хранения эфир для наркоза проверяют на соответствие требованиям. Использование технического эфира в этих целях не допускается.
Техника[ | ]
Диэтиловый эфир — аэрозоль для быстрого запуска. Инструкция утверждает, что возможен запуск при температуре −55 °F (−48,3 °C)В СССР выпускалась пусковая жидкость «Арктика», небольшое количество заливалось во впускной коллектор через карбюратор при снятом воздушном фильтре. Для армии выпускался эфир в алюминиевой запечатанной гильзе, перед использованием гильза протыкалась штык-ножом или отвёрткой. За рубежом выпускается «жидкость для запуска в холодные дни» в аэрозольном баллоне. Состав: диэтиловый эфир, индустриальное масло, пропеллент.
Механизм запуска ДВС в этом случае по большей мере, дизельный: смесь эфира с воздухом воспламеняется от сжатия уже при степени сжатия порядка 5-6; потерявшие компрессию по разным причинам двигатели могут делать несколько оборотов на эфире, но на бензине, тем не менее, не работают.
Примечания[ | ]
- ↑ 1 2 3 4 5 6 7 8 http://www.cdc.gov/niosh/npg/npgd0277.html
- ↑ 1 2 3 Toski, A; Bacon, DR; Calverley, RK. The history of Anesthesiology // Clinical Anesthesia / Barash, Paul G; Cullen, Bruce F; Stoelting, Robert K.. — 4th ed. — Lippincott Williams & Wilkins, 2001. — P. 3. — ISBN 978-0-7817-2268-1.
- ↑ Hademenos, George J.; Murphree, Shaun; Zahler, Kathy; Warner, Jennifer M. McGraw-Hill's PCAT. — McGraw-Hill. — P. 39. — ISBN 978-0-07-160045-3.
- ↑ Dr. Frobenius (1729) "An account of a spiritus vini æthereus, together with several experiments tried therewith, " Philosophical Transactions of the Royal Society (London), 36 : 283—289.
Литература[ | ]
- Бабаян Э. А., Гаевский А. В., Бардин Е. В. «Правовые аспекты оборота наркотических, психотропных, сильнодействующих, ядовитых веществ и прекурсоров» М.: , 2000 стр. 148
- Гурвич Я. А. «Справочник молодого аппаратчика-химика» М.: Химия, 1991 стр. 229
- Девяткин В. В., Ляхова Ю. М. «Химия для любознательных, или о чём не узнаешь на уроке» Ярославль: Академия Холдинг, 2000 стр. 48
- Рабинович В. А., Хавин З. Я. «Краткий химический справочник» Л.: Химия, 1977 стр. 148
- Гауптман 3., Органическая химия, пер. с нем., М.: Химия, 1979, с. 332-40;
- Грефе Ю., Общая органическая химия, пер. с англ., т. 2, М., 1982, с. 289—353;
- Ремане X.,Kirk-Othmer encyclopedia, v. 9, N. Y., 1980, p. 381-92.
encyclopaedia.bid


















