Реферат: Способы получения сложных эфиров Конденсации формальдегида с изобутиленом Различные способы. Способы синтеза сложных эфиров
Методы синтеза сложных эфиров - Справочник химика 21
Реакции с солями металлов. Алкилсульфонаты легко реагируют с солями минеральных и органических кислот. Некоторые из этих реакций служат удобными методами синтеза сложных эфиров. [c.366]
Современные методы синтеза сложных эфиров основаны на широком [c.1450]Методы синтеза сложных эфиров [c.639]
МЕТОДЫ СИНТЕЗА СЛОЖНЫХ ЭФИРОВ [c.639]
Многочисленные методы синтеза сложных эфиров карбоновых кислот изложены в ряде монографий и учебных пособий [1—3]. Однако не все они пригодны для синтеза пластификаторов. Большинство методов используется для приготовления эфиров низших карбоновых кислот и спиртов с числом углеродных атомов до С4. [c.7]
Основной метод синтеза сложных эфиров заключается в этерификации карбоновых кислот спиртами [c.7]
Одним из широко используемых методов синтеза сложных эфиров является ацилирование спиртов с помощью хлорангидри дов кислот. [c.48]
Для синтеза сложных эфиров и амидов существует три методологических подхода прямая катализируемая кислот.ой реакция спирта с кислотой, предварительное превращение кислоты в реакционноспособное производное и активация спирта или амина по отношению к нуклеофильной атаке карбоксильных ионов. Тетраэдрический интермедиат (32), возникающий при первых двух подходах, интенсивно изучался 199]. Другие менее общие методы синтеза сложных эфиров, такие как реакция Байера — Виллигера или фотохимическое окисление кетонов, рассмотрены в разд. 9.1.1.1. Кетены [200] редко применяют для получения монофункциональных амидов или сложных эфиров. [c.47]
Сложные эфиры образуются при контролируемом гидролизе или алкоголизе ортоэфиров (50, X = 0) или соответствующих тио-аналогов (50, X = S) (см. разд. 9.8.4). Недавно эта реакция использована [91] в общем методе синтеза сложных эфиров из альдегидов по схеме (112). Этот путь позволяет избежать относительно бурных окислительных процессов (см. разд. 9.8.1.3), с которыми обычно ассоциируется такое превращение. [c.312]
Известны и другие методы синтеза сложных эфиров из альдегидов и кетонов или их производных, и некоторые из них потенциально достаточно общи. Так, ацетали альдегидов можно [c.315]
Реакции карбонильных соединений со спиртами очень похожи на соответствуюшие реакции с водой. Реакции спиртов с ацилхлоридами и карбоновыми кислотами широко используются в качестве методов синтеза сложных эфиров (рис. 8.14). Как и [c.180]
Взаимодействие спиртов с ангидридами и хлорангид-ридами протекает легче, чем с карбоновыми кислотами. Метод синтеза сложных эфиров с помощью хлорангидридов имеет широкое применение, поскольку эта реакция необратима. Хлорангидриды ароматических кислот несколько менее активны по сравнению с хлорангидридами кислот алифатического ряда. Выделяющийся при реакции хлороводород можно удалять из сферы реакции или поглощать каким-нибудь основанием — гидроксидом натрия, диметиланилином, пиридином или магнием. Наиболее общим является метод, в котором используют пиридин. Механизм ацилирования спиртов хлор ангидридами кислот можно представить схемой [c.51]
МЕТОДЫ СИНТЕЗА СЛОЖНЫХ ЭФИРОВ ЦЕЛЛЮЛОЗЫ [c.255]
Из методов синтеза сложных эфиров целлюлозы, разработанных в последние годы, существенный интерес представляют реакции нуклеофильного замещения и переэтерификации. Основные лабораторные и промышленные методы синтеза изложены при описании методов получения соответствующих эфиров целлюлозы. Ниже приводятся краткие данные о новых методах этерификации целлюлозы, которые, по-видимому, получат в дальнейшем более широкое применение. [c.256]
В последние годы синтезированы новые эфиры целлюлозы, предложены новые катализаторы для осуществления реакций этерификации. Результаты исследований изложены в различных обзорах и монографиях [7] и поэтому в данном разделе не рассматриваются. Из новых методов синтеза сложных эфиров целлюлозы известный интерес представляют этерификация целлюлозы на поверхности раздела фаз и реакция переэтерификации. [c.16]
Полиэфиракрилаты могут быть получены как методами синтеза сложных эфиров по двухстадийному процессу, так и одностадийным процессом — методом конденсационной теломеризации. [c.132]
УСОВЕРШЕНСТВОВАННЫЙ МЕТОД СИНТЕЗА СЛОЖНЫХ ЭФИРОВ [c.241]
Если R — первичная группа, то RX может быть только винил-или арилгалогенидом, причем винильная группа R взаимодействует с сохранением конфигурации. Следовательно, карбокатион не является интермедиатом в этой реакции. Если R — третичная группа, то R может быть первичной алкильной, а также винильной или арильной группой. Это один из немногих методов синтеза сложных эфиров из третичных спиртов. Наилучшие результаты достигаются при использовании алкилиодидов, немного хуже реакция идет с алкилбромидами. В присутствии амина, по крайней мере в некоторых случаях, возможно непосредственно выделить амид. [c.226]
Практически все методы синтеза сложных эфиров, известные в органической химии, применимы для синтеза полиэфиров. Обычно применяют методы переэтерифика-[щи и иепосредственную реакцию карбоксильных или хлорангндридных групп со спиртами. [c.140]
Спассов [1746] разработал метод синтеза сложных эфиров из алифатических (первичных, вторичных и третичных) и ароматических спиртов, включая фенолы (за исключением трифенил-метанола). Метод является простым и быстрым и позволяет получать эфиры с большими выходами. Он состоит в следующем. Спирт и магний (в порошке) смешивают с эфиром в отношении 0,1 моля спирта и 0,1 атомного веса магния на 10—15 г эфира для некоторых третичных спиртов отношение эфира к спирту должно быть равно 15—25 0,1 моля. В спиртовую смесь при умеренном охлаждении (в случае необходимости) медленно, по каплям, добавляют с небольшим избытком (1,25—1,5 эквивалента) раствор хлорангидрида кислоты в эфире (0,1 моля 5—10 г). Смесь оставляют стоять в течение часа, после чего нагревают в продолжение [c.372]
Образование металл-углеродной связи путем реакции комплекса переходного металла с органическим галогенидом, за которым следует внедрение по этой связи монооксида углерода и алкина, является потенциально ценным методом синтеза сложных эфиров и лактонов. Как и в соответствующих реакциях, приводящих к образованию карбоновых кислот, аллилникелевые комплексы проявляют ярко выраженную тенденцию к тому, чтобы внедрение алкина происходило прежде, чем внедрение СО. Так, из аллилхлорида, ацетилена, монооксида углерода и метанола при обычных условиях [76] был получен 1 ис-метилгексадиеноат [схема (6.87)]. Каталитическая система состоит из хлорида никеля, тиомочевины, оксида магния (для нейтрализации НС1, образующегося в результате реакции) и сплава марганца с железом для предварительного восстановления никеля(II) в никель (0). [c.221]
В 1904 г. Н. Д. Зелинским был открыт новый общий метод синтеза альдегидов из муравьиной кислоты с применением магнийорганических соединений. В этом же году А. Е. Чичибабин открыл новую реакцию получения альдегидов из ортомуравьиного эфира через стадию ацеталей, нашедшую препаративное применение. Им же разработан метод синтеза сложных эфиров из нейтральных угольных эфиров, а также ортоэфиров из ортоугольного эфира. [c.11]
Данное исследование предпринято с целью разработки методов синтеза сложных эфиров дигидропираполов и предварительного определения их фармакологического действия. [c.61]
Один из широко применяемых методов синтеза сложных эфиров состоит в обработке первичных или вторичных (но не третичных) спиртов галоидангидридами карбоновых кислот. Вы-скалепте сообралеения о том, какие побочные реакции протекают Б случае третичных спиртов. [c.68]
Предложен [22] метод синтеза сложных эфиров фенола путем совместного окисления бензола и уксусной, пропионовой, масляной или изомасляной кислот над палладиевым или платиновым катализатором. Указанные металлы (раздельно или в смеси) в количестве 0,1—10% (масс.) наносят на окись алюминия, алюмосиликат, пемзу или другой носитель с развитой поверхностью. В качестве промоторов добавляют золото и соли щелочных металлов. При 130 °С и мольном соотношении СеНв СНз ООН Ог = 1,0 1,0 0,4 на палладиевом катализаторе (2% Р(1 + 2% СНзСООМа на шариках из шпинели лития) получают фенилацетат и фенол. Суммарная селективность образования этих веществ достигает 100%. Окислительная этерификация бензола пропионовой кислотой на палладиевом катализаторе, промотированном добавками золота и пропионата лития, [c.115]
Маккомби, Саундерс и их сотрудники разработали следующие методы синтеза сложных эфиров монофторфосфорной кислоты [c.131]
В этом случае образуется молекула эфира и молекула кис-лоть, тчк что этерификация спирта ппохолит до конца. Оригинальным методом синтеза сложных эфиров является реакция Тищенко под влиянием этилата алюминия (катализатор) две молекулы альдегида превращаются в молекулу соответствующего сложного эфира [c.183]
Другими методами синтеза сложных эфиров являются превращения ангидридов и хлорангадридов карбоновых кислот при их взаимодействии со спиртами, атакже реакция солей карбоновых кислот с арилалкил-галогенидами, например [c.154]
chem21.info
Реферат - Способы получения сложных эфиров Конденсации формальдегида с изобутиленом Различные способы
Способы получения сложных эфиров. Основные продукты и области их применения. Условия проведения реакции этерификации органических кислот со спиртами. Катализаторы процесса. Особенности технологического оформления реакционного узла этерификации.
Взаимодействие кислот со спиртами:
/>
Это наиболее распространенный способ получения сложных эфиров.
Синтез сложных эфиров методом конденсации альдегидов:
/>
Синтез сложных эфиров из альдегидов (реакция Тищенко) осуществляется в присутствии алкоголята алюминия, активированного хлоридом железа или, что лучше, хлоридом алюминия и окисью цинка. Данный метод имеет промышленное значение.
Присоединение органических кислот к алкенам:
/>
Синтез сложных эфиров путем дегидрогенизации спиртов:
/>
Получение сложных эфиров методом переэтерификации.
Данная реакция имеет две разновидности: реакция обмена между эфиром и спиртом спиртовыми радикалами (реакция алкоголиза):
/>
и реакция обмена кислотными радикалами у спиртовой группы эфира:
/>
Синтез эфиров из ангидридов кислот и спиртов:
/>
Взаимодействие кетонов со спиртами:
/>
Взаимодействие между галоидангидридами и спиртами:
/>
Реакция между серебряными или калиевыми солями кислот и алифатическими галоидными производными:
/>
Взаимодействие кислот с алифатическими диазосоединениями (в основном с диазометаном):
/>
Основными продуктами реакции этерификации являются сложные эфиры, используемые в качестве растворителей, пластификаторов, синтетических смазочных масел и гидравлических жидкостей, душистых веществ, мономеров.
Этерификацию спиртов карбоновыми кислотами можно проводить в отсутствии катализатора, но в этом случае она протекает медленно и для достижения достаточной скорости требуется высокая температура (200-300ОС). Но когда примесь катализатора трудно отмывается, применяют именно некаталитический процесс. В присутствии кислотных катализаторов этерификация протекает при температуре 70-150ОС.
Наиболее распространенными катализаторами этерификации являются минеральные кислоты: серная, фосфорная. Могут использоваться бензолсульфокислота, толуолсульфокислота и т.д. Большую группу катализаторов составляют соли органических и неорганических кислот. Могут быть использованы в качестве катализаторов реакции этерификации: перекись титана, молибден на инертном носителе, активный этилат алюминия, алкоголяты титана и др. Все более широкое применение в качестве катализаторов получают ионообменные смолы.
/>
Вариант 18
Реакции гидролиза. Получаемые продукты и области их применения. Основные гидролизующие агенты и катализаторы. Способы регулирования селективности в процессах гидролиза. Обосновать выбор реакторного узла для процесса жидкофазного гидролиза хлорпентана в аллиловые спирты.
Реакциями гидролиза называют процессы замещения или двойного обмена, протекающие под действием воды или щелочей. С помощью гидролиза синтезируют некоторые производные фенолов, служащие основой для получения пестицидов. Для получения спиртов щелочной гидролиз сохраняет значение как путь синтеза аллилового спирта. Гидролиз – одна из стадий получения глицерина. Гидролизом нитрилов получают карбоновые кислоты. Кроме того, гидролиз – одна из стадий получения таких продуктов как: акрилонитрил, поливиниловый спирт, этиловый спирт из древесины, акриламид, высшие жирные спирты (процесс «Алфол»), МХУК, производство капролактама из анилина и т.д.
Вода или водяной пар в отсутствии катализатора – очень слабый гидролизующий агент. В качестве щелочных гидролизующих агентов применяют водные или водно – спиртовые растворы щелочей (для щелочного плавления – твердая щелочь с небольшой добавкой воды). Водные растворы слабых щелочей оказывают более медленное и мягкое гидролизующее действие. Для гидролиза типично каталитическое влияние кислот, которое зависит от их силы. Часто используют серную кислоту, но ее применение нередко ведет к побочным реакциям конденсации и осмоления. Поэтому используют и кислоты более мягкого действия – органические сульфокислоты, которые лучше растворимы в органических средах, и, кроме того, обладают поверхностно – активными свойствами, что облегчает гомогенизацию реакционной массы. Кроме этого часто применяются гетерогенные контакты кислотного типа (катиониты, фосфорная кислота на носителе и т.д.), преимущество которых состоит в малом расходе, меньшей коррозионной активности и снижении количества сточных вод.
При действии щелочей на хлорпроизводные возможны параллельные реакции замещения (гидролиз) и отщепления (дегидрохлорирование) атомов хлора. На их относительную долю влияют температура, среда, но самым эффективным методом регулирования направления этих двух реакций является выбор гидролизующего агента. Для гидролизу требуется слабое основание, обладающее высокой нуклеофильностью (например Na2CO3), а для дегидрохлорирорвания – сильное основание с небольшой нуклеофильностью (NaOH, Ca(OH)2). Эффективный путь подавления побочных реакций – снижение концентрации целевого продукта в реакционной массе путем его непрерывной отгонки. Этому способствует то обстоятельство, что целевой продукт всегда более летучий, чем исходные реагенты. Для повышения селективности реакций гидролиза целесообразно применять реакторы, близкие к модели идеального вытеснения.
При жидкофазном гидролизе хлорпентана в аллиловые спирты в качестве гидролизующих агентов применяют 5-10%-ный раствор Na2CO3 или NaOH, который для обеспечения более высокой интенсивности процесса и повышения степени конверсии хлорпроизводного берут в избытке 10-25% к стехиометрическому количеству. Ввиду наличия двух жидких фаз важное значение имеет увеличение поверхности их контакта. При непрерывных процессах это достигается обычно уже в насосе, во всасывающую линию которого подают оба реагента. Сохранение системы в эмульгированном состоянии обеспечивается турбулизация потока за счет его достаточно большой линейной скорости. Это предопределяет использование реакторов типа змеевиков или многоходовых кожухотрубных аппаратов, что возможно при небольшом времени реакции. Когда ее продолжительность велика и продукт выпускают в небольшом масштабе, процесс осуществляется периодическим способом в автоклаве, перемешивая смесь мешалкой или барботируя через нее пар соответствующего давления. Реакционную массу по окончании процесса дросселируют до атмосферного давления, причем целевой продукт переходит в газовую фазу (аллиловый спирт). После этого спирт чистят ректификацией.
Конденсации формальдегида с изобутиленом
При конденсации формальдегида с изобутиленом можно использовать изобутилен-изобутановую фракцию с содержанием изобутилена до 50%масс и примесями линейных бутенов без предварительного выделения. Изложите химизм процесса и объясните, почему это возможно. Поясните, почему лимитируется содержание бутадиена-1,3 в исходном сырье. Каковы условия и особенности гетерофазного процесса конденсации и оформления реакционного узла.
Конденсация формальдегида с изобутиленом, протекающая в присутствии катализаторов кислотного типа (реакция Принса), приобрела практическое значение для синтеза 4,4 – диметилдиоксана – 1,3. Побочно образуются ненасыщенные одноатомные спирты, триметилкарбинол (продукт гидратации изобутилена) и более сложные кислородсодержащие соединения. Образование всех этих веществ объясняет следующая схема.
Обычно сопутствующие изобутилену непредельные углеводороды С4 нормального строения, также как пропилен и олефины С5, значительно уступают по реакционной способности изобутилену, обладающему активным реакционноспособным атомом водорода при третичном атоме углерода во взаимодействии с формальдегидом. Скорости взаимодействия с формальдегидом 1-бутена и 2-бутена приблизительно на два порядка ниже, чем с изобутиленом. Это означает, что в условиях синтеза диметилдиоксана бутены нормального строения практически не реагирует, и, следовательно, их предварительное выделение из углеводородного сырья не требуется.
Данный вывод неприемлем лишь к бутадиену-1,3, продукт взаимодействия которого с формальдегидом (4-винилдиоксан-1,3), при последующем расщеплении даёт циклопентадиен – сильнейший каталитический яд реакции стереоспецифической полимеризации изопрена. Поэтому на исходную фракцию С4 налагаются жёсткие требования по содержанию бутадиена (≤ 0,3 % мас.).
Конденсация изобутилена с формальдегидом – это гетерофазная жидкофазная каталитическая реакция, в которой взаимодействие осуществляется в пределах одной реакционной фазы (водной), а реакционная масса представляет собой жидкую двухфазную систему. Продукты реакции распределяются между двумя фазами в соответствии с их природой. Присутствие ДМД в водной фазе нежелательно, т.к. в присутствии серной кислоты он гидролизуется, поэтому его экстрагируют в углеводородную фазу парафиновыми углеводородами, содержащимися в сырье. Интенсивность реакции во многом зависит от развития поверхности контакта.
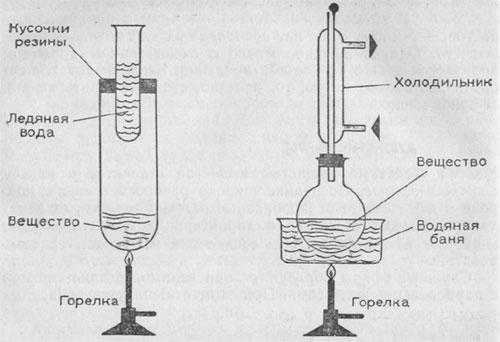
Условия процесса: Т=85-95oC, Р = 1,5-2 МПа, когда все реагенты находятся в жидком состоянии. Конверсия 85-90% по обоим реагентам, мольное соотношение – формальдегид: i-бутилен = 2/1, причем в реакционной массе должен всегда находиться свободный формальдегид, чтобы препятствовать полимеризации изобутилена. Катализатор h3SO4 – 1 – 1,5 % вес. по отношению к изобутилену. Процесс проводится в реакторе идеального вытеснения, работающем по принципу прямо – или противотока. Реактор должен удовлетворять следующим требованиям:
--PAGE_BREAK--интенсивный массообмен между углеводородной и водной фазами;
равномерный съем тепла, t = const;
постоянное время пребывание исходных реагентов в зоне реакции.
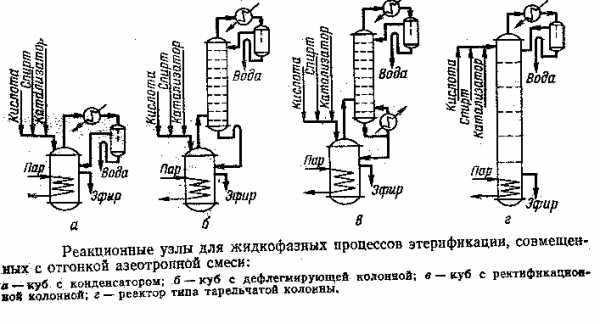
Реакционный узел синтеза ДМД представляет два последовательно соединенных между собой трубчатых аппарата. Каждая трубка реактора снабжена соплом, обеспечивающим высокую скорость подачи изобутиленовой фракции и ее расщепление при соприкосновении с движущей навстречу водной фазой. Отвод тепла реакции осуществляется паровым конденсатом через межтрубное пространство.
/>
Различные способы получения фенола. Для кумольного способа привести принципиальную технологическую схему. Обосновать выбор типа и конструкции реактора окисления изопропилбензола. Перечислить основные побочные продукты кумольного способа, как они образуются и утилизируются.
a) Хлорбензольный:
/>
Сульфирование бензола
/>
Метод Рашига:
/>
Кумольный метод:
/>
Окисление толуола:
/>
Окисление циклогексана:
/>
б) />
в) колонна окислительная – РИВ, противоток; все недостатки гетерофазного процесса
каскад реакторов идеального смешения.
г) разложение гидроперекиси на катионитах
/>
/>
/>
www.ronl.ru
Реферат - Способы получения сложных эфиров. Конденсации формальдегида с изобутиленом. Различные способы получения фенола
Способы получения сложных эфиров. Основные продукты и области их применения. Условия проведения реакции этерификации органических кислот со спиртами. Катализаторы процесса. Особенности технологического оформления реакционного узла этерификации.
1. Взаимодействие кислот со спиртами:
Это наиболее распространенный способ получения сложных эфиров.
2. Синтез сложных эфиров методом конденсации альдегидов:
Синтез сложных эфиров из альдегидов (реакция Тищенко) осуществляется в присутствии алкоголята алюминия, активированного хлоридом железа или, что лучше, хлоридом алюминия и окисью цинка. Данный метод имеет промышленное значение.
3. Присоединение органических кислот к алкенам:
4. Синтез сложных эфиров путем дегидрогенизации спиртов:
5. Получение сложных эфиров методом переэтерификации.
Данная реакция имеет две разновидности: реакция обмена между эфиром и спиртом спиртовыми радикалами (реакция алкоголиза):
и реакция обмена кислотными радикалами у спиртовой группы эфира:
6. Синтез эфиров из ангидридов кислот и спиртов:
7. Взаимодействие кетонов со спиртами:
8. Взаимодействие между галоидангидридами и спиртами:
9. Реакция между серебряными или калиевыми солями кислот и алифатическими галоидными производными:
10. Взаимодействие кислот с алифатическими диазосоединениями (в основном с диазометаном):
Основными продуктами реакции этерификации являются сложные эфиры, используемые в качестве растворителей, пластификаторов, синтетических смазочных масел и гидравлических жидкостей, душистых веществ, мономеров.
Этерификацию спиртов карбоновыми кислотами можно проводить в отсутствии катализатора, но в этом случае она протекает медленно и для достижения достаточной скорости требуется высокая температура (200-300О С). Но когда примесь катализатора трудно отмывается, применяют именно некаталитический процесс. В присутствии кислотных катализаторов этерификация протекает при температуре 70-150О С.
Наиболее распространенными катализаторами этерификации являются минеральные кислоты: серная, фосфорная. Могут использоваться бензолсульфокислота, толуолсульфокислота и т.д. Большую группу катализаторов составляют соли органических и неорганических кислот. Могут быть использованы в качестве катализаторов реакции этерификации: перекись титана, молибден на инертном носителе, активный этилат алюминия, алкоголяты титана и др. Все более широкое применение в качестве катализаторов получают ионообменные смолы.
Вариант 18
Реакции гидролиза. Получаемые продукты и области их применения. Основные гидролизующие агенты и катализаторы. Способы регулирования селективности в процессах гидролиза. Обосновать выбор реакторного узла для процесса жидкофазного гидролиза хлорпентана в аллиловые спирты.
Реакциями гидролиза называют процессы замещения или двойного обмена, протекающие под действием воды или щелочей. С помощью гидролиза синтезируют некоторые производные фенолов, служащие основой для получения пестицидов. Для получения спиртов щелочной гидролиз сохраняет значение как путь синтеза аллилового спирта. Гидролиз – одна из стадий получения глицерина. Гидролизом нитрилов получают карбоновые кислоты. Кроме того, гидролиз – одна из стадий получения таких продуктов как: акрилонитрил, поливиниловый спирт, этиловый спирт из древесины, акриламид, высшие жирные спирты (процесс «Алфол»), МХУК, производство капролактама из анилина и т.д.
Вода или водяной пар в отсутствии катализатора – очень слабый гидролизующий агент. В качестве щелочных гидролизующих агентов применяют водные или водно – спиртовые растворы щелочей (для щелочного плавления – твердая щелочь с небольшой добавкой воды). Водные растворы слабых щелочей оказывают более медленное и мягкое гидролизующее действие. Для гидролиза типично каталитическое влияние кислот, которое зависит от их силы. Часто используют серную кислоту, но ее применение нередко ведет к побочным реакциям конденсации и осмоления. Поэтому используют и кислоты более мягкого действия – органические сульфокислоты, которые лучше растворимы в органических средах, и, кроме того, обладают поверхностно – активными свойствами, что облегчает гомогенизацию реакционной массы. Кроме этого часто применяются гетерогенные контакты кислотного типа (катиониты, фосфорная кислота на носителе и т.д.), преимущество которых состоит в малом расходе, меньшей коррозионной активности и снижении количества сточных вод.
При действии щелочей на хлорпроизводные возможны параллельные реакции замещения (гидролиз) и отщепления (дегидрохлорирование) атомов хлора. На их относительную долю влияют температура, среда, но самым эффективным методом регулирования направления этих двух реакций является выбор гидролизующего агента. Для гидролизу требуется слабое основание, обладающее высокой нуклеофильностью (например Na2 CO3 ), а для дегидрохлорирорвания – сильное основание с небольшой нуклеофильностью (NaOH, Ca(OH)2 ). Эффективный путь подавления побочных реакций – снижение концентрации целевого продукта в реакционной массе путем его непрерывной отгонки. Этому способствует то обстоятельство, что целевой продукт всегда более летучий, чем исходные реагенты. Для повышения селективности реакций гидролиза целесообразно применять реакторы, близкие к модели идеального вытеснения.
При жидкофазном гидролизе хлорпентана в аллиловые спирты в качестве гидролизующих агентов применяют 5-10%-ный раствор Na2 CO3 или NaOH, который для обеспечения более высокой интенсивности процесса и повышения степени конверсии хлорпроизводного берут в избытке 10-25% к стехиометрическому количеству. Ввиду наличия двух жидких фаз важное значение имеет увеличение поверхности их контакта. При непрерывных процессах это достигается обычно уже в насосе, во всасывающую линию которого подают оба реагента. Сохранение системы в эмульгированном состоянии обеспечивается турбулизация потока за счет его достаточно большой линейной скорости. Это предопределяет использование реакторов типа змеевиков или многоходовых кожухотрубных аппаратов, что возможно при небольшом времени реакции. Когда ее продолжительность велика и продукт выпускают в небольшом масштабе, процесс осуществляется периодическим способом в автоклаве, перемешивая смесь мешалкой или барботируя через нее пар соответствующего давления. Реакционную массу по окончании процесса дросселируют до атмосферного давления, причем целевой продукт переходит в газовую фазу (аллиловый спирт). После этого спирт чистят ректификацией.
Конденсации формальдегида с изобутиленом
При конденсации формальдегида с изобутиленом можно использовать изобутилен-изобутановую фракцию с содержанием изобутилена до 50%масс и примесями линейных бутенов без предварительного выделения. Изложите химизм процесса и объясните, почему это возможно. Поясните, почему лимитируется содержание бутадиена-1,3 в исходном сырье. Каковы условия и особенности гетерофазного процесса конденсации и оформления реакционного узла.
Конденсация формальдегида с изобутиленом, протекающая в присутствии катализаторов кислотного типа (реакция Принса), приобрела практическое значение для синтеза 4,4 – диметилдиоксана – 1,3. Побочно образуются ненасыщенные одноатомные спирты, триметилкарбинол (продукт гидратации изобутилена) и более сложные кислородсодержащие соединения. Образование всех этих веществ объясняет следующая схема.
Обычно сопутствующие изобутилену непредельные углеводороды С4 нормального строения, также как пропилен и олефины С5, значительно уступают по реакционной способности изобутилену, обладающему активным реакционноспособным атомом водорода при третичном атоме углерода во взаимодействии с формальдегидом. Скорости взаимодействия с формальдегидом 1-бутена и 2-бутена приблизительно на два порядка ниже, чем с изобутиленом. Это означает, что в условиях синтеза диметилдиоксана бутены нормального строения практически не реагирует, и, следовательно, их предварительное выделение из углеводородного сырья не требуется.
Данный вывод неприемлем лишь к бутадиену-1,3, продукт взаимодействия которого с формальдегидом (4-винилдиоксан-1,3), при последующем расщеплении даёт циклопентадиен – сильнейший каталитический яд реакции стереоспецифической полимеризации изопрена. Поэтому на исходную фракцию С4 налагаются жёсткие требования по содержанию бутадиена (≤ 0,3 % мас.).
Конденсация изобутилена с формальдегидом – это гетерофазная жидкофазная каталитическая реакция, в которой взаимодействие осуществляется в пределах одной реакционной фазы (водной), а реакционная масса представляет собой жидкую двухфазную систему. Продукты реакции распределяются между двумя фазами в соответствии с их природой. Присутствие ДМД в водной фазе нежелательно, т.к. в присутствии серной кислоты он гидролизуется, поэтому его экстрагируют в углеводородную фазу парафиновыми углеводородами, содержащимися в сырье. Интенсивность реакции во многом зависит от развития поверхности контакта.
Условия процесса: Т=85-95o C, Р = 1,5-2 МПа, когда все реагенты находятся в жидком состоянии. Конверсия 85-90% по обоим реагентам, мольное соотношение – формальдегид: i-бутилен = 2/1, причем в реакционной массе должен всегда находиться свободный формальдегид, чтобы препятствовать полимеризации изобутилена. Катализатор h3 SO4 – 1 – 1,5 % вес. по отношению к изобутилену. Процесс проводится в реакторе идеального вытеснения, работающем по принципу прямо – или противотока. Реактор должен удовлетворять следующим требованиям:
1. интенсивный массообмен между углеводородной и водной фазами;
2. равномерный съем тепла, t = const;
3. постоянное время пребывание исходных реагентов в зоне реакции.
Реакционный узел синтеза ДМД представляет два последовательно соединенных между собой трубчатых аппарата. Каждая трубка реактора снабжена соплом, обеспечивающим высокую скорость подачи изобутиленовой фракции и ее расщепление при соприкосновении с движущей навстречу водной фазой. Отвод тепла реакции осуществляется паровым конденсатом через межтрубное пространство.

Различные способы получения фенола. Для кумольного способа привести принципиальную технологическую схему. Обосновать выбор типа и конструкции реактора окисления изопропилбензола. Перечислить основные побочные продукты кумольного способа, как они образуются и утилизируются.
a) Хлорбензольный :
Сульфирование бензола
Метод Рашига :
Кумольный метод :
Окисление толуола :
Окисление циклогексана :
б)
в) колонна окислительная – РИВ, противоток; все недостатки гетерофазного процесса
каскад реакторов идеального смешения.
г) разложение гидроперекиси на катионитах
www.ronl.ru
Способы получения сложных эфиров Конденсации формальдегида с изобутиленом Различные способы
Способы получения сложных эфиров. Основные продукты и области их применения. Условия проведения реакции этерификации органических кислот со спиртами. Катализаторы процесса. Особенности технологического оформления реакционного узла этерификации.
Взаимодействие кислот со спиртами:
Это наиболее распространенный способ получения сложных эфиров.
Синтез сложных эфиров методом конденсации альдегидов:
Синтез сложных эфиров из альдегидов (реакция Тищенко) осуществляется в присутствии алкоголята алюминия, активированного хлоридом железа или, что лучше, хлоридом алюминия и окисью цинка. Данный метод имеет промышленное значение.
Присоединение органических кислот к алкенам:
Синтез сложных эфиров путем дегидрогенизации спиртов:
Получение сложных эфиров методом переэтерификации.
Данная реакция имеет две разновидности: реакция обмена между эфиром и спиртом спиртовыми радикалами (реакция алкоголиза):
и реакция обмена кислотными радикалами у спиртовой группы эфира:
Синтез эфиров из ангидридов кислот и спиртов:
Взаимодействие кетонов со спиртами:
Взаимодействие между галоидангидридами и спиртами:
Реакция между серебряными или калиевыми солями кислот и алифатическими галоидными производными:
Взаимодействие кислот с алифатическими диазосоединениями (в основном с диазометаном):
Основными продуктами реакции этерификации являются сложные эфиры, используемые в качестве растворителей, пластификаторов, синтетических смазочных масел и гидравлических жидкостей, душистых веществ, мономеров.
Этерификацию спиртов карбоновыми кислотами можно проводить в отсутствии катализатора, но в этом случае она протекает медленно и для достижения достаточной скорости требуется высокая температура (200-300ОС). Но когда примесь катализатора трудно отмывается, применяют именно некаталитический процесс. В присутствии кислотных катализаторов этерификация протекает при температуре 70-150ОС.
Наиболее распространенными катализаторами этерификации являются минеральные кислоты: серная, фосфорная. Могут использоваться бензолсульфокислота, толуолсульфокислота и т.д. Большую группу катализаторов составляют соли органических и неорганических кислот. Могут быть использованы в качестве катализаторов реакции этерификации: перекись титана, молибден на инертном носителе, активный этилат алюминия, алкоголяты титана и др. Все более широкое применение в качестве катализаторов получают ионообменные смолы.
Вариант 18
Реакции гидролиза. Получаемые продукты и области их применения. Основные гидролизующие агенты и катализаторы. Способы регулирования селективности в процессах гидролиза. Обосновать выбор реакторного узла для процесса жидкофазного гидролиза хлорпентана в аллиловые спирты.
Реакциями гидролиза называют процессы замещения или двойного обмена, протекающие под действием воды или щелочей. С помощью гидролиза синтезируют некоторые производные фенолов, служащие основой для получения пестицидов. Для получения спиртов щелочной гидролиз сохраняет значение как путь синтеза аллилового спирта. Гидролиз – одна из стадий получения глицерина. Гидролизом нитрилов получают карбоновые кислоты. Кроме того, гидролиз – одна из стадий получения таких продуктов как: акрилонитрил, поливиниловый спирт, этиловый спирт из древесины, акриламид, высшие жирные спирты (процесс «Алфол»), МХУК, производство капролактама из анилина и т.д.
Вода или водяной пар в отсутствии катализатора – очень слабый гидролизующий агент. В качестве щелочных гидролизующих агентов применяют водные или водно – спиртовые растворы щелочей (для щелочного плавления – твердая щелочь с небольшой добавкой воды). Водные растворы слабых щелочей оказывают более медленное и мягкое гидролизующее действие. Для гидролиза типично каталитическое влияние кислот, которое зависит от их силы. Часто используют серную кислоту, но ее применение нередко ведет к побочным реакциям конденсации и осмоления. Поэтому используют и кислоты более мягкого действия – органические сульфокислоты, которые лучше растворимы в органических средах, и, кроме того, обладают поверхностно – активными свойствами, что облегчает гомогенизацию реакционной массы. Кроме этого часто применяются гетерогенные контакты кислотного типа (катиониты, фосфорная кислота на носителе и т.д.), преимущество которых состоит в малом расходе, меньшей коррозионной активности и снижении количества сточных вод.
При действии щелочей на хлорпроизводные возможны параллельные реакции замещения (гидролиз) и отщепления (дегидрохлорирование) атомов хлора. На их относительную долю влияют температура, среда, но самым эффективным методом регулирования направления этих двух реакций является выбор гидролизующего агента. Для гидролизу требуется слабое основание, обладающее высокой нуклеофильностью (например Na2CO3), а для дегидрохлорирорвания – сильное основание с небольшой нуклеофильностью (NaOH, Ca(OH)2). Эффективный путь подавления побочных реакций – снижение концентрации целевого продукта в реакционной массе путем его непрерывной отгонки. Этому способствует то обстоятельство, что целевой продукт всегда более летучий, чем исходные реагенты. Для повышения селективности реакций гидролиза целесообразно применять реакторы, близкие к модели идеального вытеснения.
При жидкофазном гидролизе хлорпентана в аллиловые спирты в качестве гидролизующих агентов применяют 5-10%-ный раствор Na2CO3 или NaOH, который для обеспечения более высокой интенсивности процесса и повышения степени конверсии хлорпроизводного берут в избытке 10-25% к стехиометрическому количеству. Ввиду наличия двух жидких фаз важное значение имеет увеличение поверхности их контакта. При непрерывных процессах это достигается обычно уже в насосе, во всасывающую линию которого подают оба реагента. Сохранение системы в эмульгированном состоянии обеспечивается турбулизация потока за счет его достаточно большой линейной скорости. Это предопределяет использование реакторов типа змеевиков или многоходовых кожухотрубных аппаратов, что возможно при небольшом времени реакции. Когда ее продолжительность велика и продукт выпускают в небольшом масштабе, процесс осуществляется периодическим способом в автоклаве, перемешивая смесь мешалкой или барботируя через нее пар соответствующего давления. Реакционную массу по окончании процесса дросселируют до атмосферного давления, причем целевой продукт переходит в газовую фазу (аллиловый спирт). После этого спирт чистят ректификацией.
Конденсации формальдегида с изобутиленом
При конденсации формальдегида с изобутиленом можно использовать изобутилен-изобутановую фракцию с содержанием изобутилена до 50%масс и примесями линейных бутенов без предварительного выделения. Изложите химизм процесса и объясните, почему это возможно. Поясните, почему лимитируется содержание бутадиена-1,3 в исходном сырье. Каковы условия и особенности гетерофазного процесса конденсации и оформления реакционного узла.
Конденсация формальдегида с изобутиленом, протекающая в присутствии катализаторов кислотного типа (реакция Принса), приобрела практическое значение для синтеза 4,4 – диметилдиоксана – 1,3. Побочно образуются ненасыщенные одноатомные спирты, триметилкарбинол (продукт гидратации изобутилена) и более сложные кислородсодержащие соединения. Образование всех этих веществ объясняет следующая схема.
Обычно сопутствующие изобутилену непредельные углеводороды С4 нормального строения, также как пропилен и олефины С5, значительно уступают по реакционной способности изобутилену, обладающему активным реакционноспособным атомом водорода при третичном атоме углерода во взаимодействии с формальдегидом. Скорости взаимодействия с формальдегидом 1-бутена и 2-бутена приблизительно на два порядка ниже, чем с изобутиленом. Это означает, что в условиях синтеза диметилдиоксана бутены нормального строения практически не реагирует, и, следовательно, их предварительное выделение из углеводородного сырья не требуется.
Данный вывод неприемлем лишь к бутадиену-1,3, продукт взаимодействия которого с формальдегидом (4-винилдиоксан-1,3), при последующем расщеплении даёт циклопентадиен – сильнейший каталитический яд реакции стереоспецифической полимеризации изопрена. Поэтому на исходную фракцию С4 налагаются жёсткие требования по содержанию бутадиена (≤ 0,3 % мас.).
Конденсация изобутилена с формальдегидом – это гетерофазная жидкофазная каталитическая реакция, в которой взаимодействие осуществляется в пределах одной реакционной фазы (водной), а реакционная масса представляет собой жидкую двухфазную систему. Продукты реакции распределяются между двумя фазами в соответствии с их природой. Присутствие ДМД в водной фазе нежелательно, т.к. в присутствии серной кислоты он гидролизуется, поэтому его экстрагируют в углеводородную фазу парафиновыми углеводородами, содержащимися в сырье. Интенсивность реакции во многом зависит от развития поверхности контакта.
Условия процесса: Т=85-95oC, Р = 1,5-2 МПа, когда все реагенты находятся в жидком состоянии. Конверсия 85-90% по обоим реагентам, мольное соотношение – формальдегид: i-бутилен = 2/1, причем в реакционной массе должен всегда находиться свободный формальдегид, чтобы препятствовать полимеризации изобутилена. Катализатор h3SO4 – 1 – 1,5 % вес. по отношению к изобутилену. Процесс проводится в реакторе идеального вытеснения, работающем по принципу прямо – или противотока. Реактор должен удовлетворять следующим требованиям:
coolreferat.com
Способы получения сложных эфиров Конденсации формальдегида с изобутиленом Различные способы - реферат
Способы получения сложных эфиров. Основные продукты и области их применения. Условия проведения реакции этерификации органических кислот со спиртами. Катализаторы процесса. Особенности технологического оформления реакционного узла этерификации. Взаимодействие кислот со спиртами: /> Это наиболее распространенный способ получения сложных эфиров. Синтез сложных эфиров методом конденсации альдегидов: /> Синтез сложных эфиров из альдегидов (реакция Тищенко) осуществляется в присутствии алкоголята алюминия, активированного хлоридом железа или, что лучше, хлоридом алюминия и окисью цинка. Данный метод имеет промышленное значение. Присоединение органических кислот к алкенам: /> Синтез сложных эфиров путем дегидрогенизации спиртов: /> Получение сложных эфиров методом переэтерификации. Данная реакция имеет две разновидности: реакция обмена между эфиром и спиртом спиртовыми радикалами (реакция алкоголиза): /> и реакция обмена кислотными радикалами у спиртовой группы эфира: /> Синтез эфиров из ангидридов кислот и спиртов: /> Взаимодействие кетонов со спиртами: /> Взаимодействие между галоидангидридами и спиртами: /> Реакция между серебряными или калиевыми солями кислот и алифатическими галоидными производными: /> Взаимодействие кислот с алифатическими диазосоединениями (в основном с диазометаном): /> Основными продуктами реакции этерификации являются сложные эфиры, используемые в качестве растворителей, пластификаторов, синтетических смазочных масел и гидравлических жидкостей, душистых веществ, мономеров. Этерификацию спиртов карбоновыми кислотами можно проводить в отсутствии катализатора, но в этом случае она протекает медленно и для достижения достаточной скорости требуется высокая температура (200-300ОС). Но когда примесь катализатора трудно отмывается, применяют именно некаталитический процесс. В присутствии кислотных катализаторов этерификация протекает при температуре 70-150ОС. Наиболее распространенными катализаторами этерификации являются минеральные кислоты: серная, фосфорная. Могут использоваться бензолсульфокислота, толуолсульфокислота и т.д. Большую группу катализаторов составляют соли органических и неорганических кислот. Могут быть использованы в качестве катализаторов реакции этерификации: перекись титана, молибден на инертном носителе, активный этилат алюминия, алкоголяты титана и др. Все более широкое применение в качестве катализаторов получают ионообменные смолы. /> Вариант 18 Реакции гидролиза. Получаемые продукты и области их применения. Основные гидролизующие агенты и катализаторы. Способы регулирования селективности в процессах гидролиза. Обосновать выбор реакторного узла для процесса жидкофазного гидролиза хлорпентана в аллиловые спирты. Реакциями гидролиза называют процессы замещения или двойного обмена, протекающие под действием воды или щелочей. С помощью гидролиза синтезируют некоторые производные фенолов, служащие основой для получения пестицидов. Для получения спиртов щелочной гидролиз сохраняет значение как путь синтеза аллилового спирта. Гидролиз – одна из стадий получения глицерина. Гидролизом нитрилов получают карбоновые кислоты. Кроме того, гидролиз – одна из стадий получения таких продуктов как: акрилонитрил, поливиниловый спирт, этиловый спирт из древесины, акриламид, высшие жирные спирты (процесс «Алфол»), МХУК, производство капролактама из анилина и т.д. Вода или водяной пар в отсутствии катализатора – очень слабый гидролизующий агент. В качестве щелочных гидролизующих агентов применяют водные или водно – спиртовые растворы щелочей (для щелочного плавления – твердая щелочь с небольшой добавкой воды). Водные растворы слабых щелочей оказывают более медленное и мягкое гидролизующее действие. Для гидролиза типично каталитическое влияние кислот, которое зависит от их силы. Часто используют серную кислоту, но ее применение нередко ведет к побочным реакциям конденсации и осмоления. Поэтому используют и кислоты более мягкого действия – органические сульфокислоты, которые лучше растворимы в органических средах, и, кроме того, обладают поверхностно – активными свойствами, что облегчает гомогенизацию реакционной массы. Кроме этого часто применяются гетерогенные контакты кислотного типа (катиониты, фосфорная кислота на носителе и т.д.), преимущество которых состоит в малом расходе, меньшей коррозионной активности и снижении количества сточных вод. При действии щелочей на хлорпроизводные возможны параллельные реакции замещения (гидролиз) и отщепления (дегидрохлорирование) атомов хлора. На их относительную долю влияют температура, среда, но самым эффективным методом регулирования направления этих двух реакций является выбор гидролизующего агента. Для гидролизу требуется слабое основание, обладающее высокой нуклеофильностью (например Na2CO3), а для дегидрохлорирорвания – сильное основание с небольшой нуклеофильностью (NaOH, Ca(OH)2). Эффективный путь подавления побочных реакций – снижение концентрации целевого продукта в реакционной массе путем его непрерывной отгонки. Этому способствует то обстоятельство, что целевой продукт всегда более летучий, чем исходные реагенты. Для повышения селективности реакций гидролиза целесообразно применять реакторы, близкие к модели идеального вытеснения. При жидкофазном гидролизе хлорпентана в аллиловые спирты в качестве гидролизующих агентов применяют 5-10%-ный раствор Na2CO3 или NaOH, который для обеспечения более высокой интенсивности процесса и повышения степени конверсии хлорпроизводного берут в избытке 10-25% к стехиометрическому количеству. Ввиду наличия двух жидких фаз важное значение имеет увеличение поверхности их контакта. При непрерывных процессах это достигается обычно уже в насосе, во всасывающую линию которого подают оба реагента. Сохранение системы в эмульгированном состоянии обеспечивается турбулизация потока за счет его достаточно большой линейной скорости. Это предопределяет использование реакторов типа змеевиков или многоходовых кожухотрубных аппаратов, что возможно при небольшом времени реакции. Когда ее продолжительность велика и продукт выпускают в небольшом масштабе, процесс осуществляется периодическим способом в автоклаве, перемешивая смесь мешалкой или барботируя через нее пар соответствующего давления. Реакционную массу по окончании процесса дросселируют до атмосферного давления, причем целевой продукт переходит в газовую фазу (аллиловый спирт). После этого спирт чистят ректификацией. Конденсации формальдегида с изобутиленом При конденсации формальдегида с изобутиленом можно использовать изобутилен-изобутановую фракцию с содержанием изобутилена до 50%масс и примесями линейных бутенов без предварительного выделения. Изложите химизм процесса и объясните, почему это возможно. Поясните, почему лимитируется содержание бутадиена-1,3 в исходном сырье. Каковы условия и особенности гетерофазного процесса конденсации и оформления реакционного узла. Конденсация формальдегида с изобутиленом, протекающая в присутствии катализаторов кислотного типа (реакция Принса), приобрела практическое значение для синтеза 4,4 – диметилдиоксана – 1,3. Побочно образуются ненасыщенные одноатомные спирты, триметилкарбинол (продукт гидратации изобутилена) и более сложные кислородсодержащие соединения. Образование всех этих веществ объясняет следующая схема. Обычно сопутствующие изобутилену непредельные углеводороды С4 нормального строения, также как пропилен и олефины С5, значительно уступают по реакционной способности изобутилену, обладающему активным реакционноспособным атомом водорода при третичном атоме углерода во взаимодействии с формальдегидом. Скорости взаимодействия с формальдегидом 1-бутена и 2-бутена приблизительно на два порядка ниже, чем с изобутиленом. Это означает, что в условиях синтеза диметилдиоксана бутены нормального строения практически не реагирует, и, следовательно, их предварительное выделение из углеводородного сырья не требуется. Данный вывод неприемлем лишь к бутадиену-1,3, продукт взаимодействия которого с формальдегидом (4-винилдиоксан-1,3), при последующем расщеплении даёт циклопентадиен – сильнейший каталитический яд реакции стереоспецифической полимеризации изопрена. Поэтому на исходную фракцию С4 налагаются жёсткие требования по содержанию бутадиена (≤ 0,3 % мас.). Конденсация изобутилена с формальдегидом – это гетерофазная жидкофазная каталитическая реакция, в которой взаимодействие осуществляется в пределах одной реакционной фазы (водной), а реакционная масса представляет собой жидкую двухфазную систему. Продукты реакции распределяются между двумя фазами в соответствии с их природой. Присутствие ДМД в водной фазе нежелательно, т.к. в присутствии серной кислоты он гидролизуется, поэтому его экстрагируют в углеводородную фазу парафиновыми углеводородами, содержащимися в сырье. Интенсивность реакции во многом зависит от развития поверхности контакта. Условия процесса: Т=85-95oC, Р = 1,5-2 МПа, когда все реагенты находятся в жидком состоянии. Конверсия 85-90% по обоим реагентам, мольное соотношение – формальдегид: i-бутилен = 2/1, причем в реакционной массе должен всегда находиться свободный формальдегид, чтобы препятствовать полимеризации изобутилена. Катализатор h3SO4 – 1 – 1,5 % вес. по отношению к изобутилену. Процесс проводится в реакторе идеального вытеснения, работающем по принципу прямо – или противотока. Реактор должен удовлетворять следующим требованиям:--PAGE_BREAK--интенсивный массообмен между углеводородной и водной фазами; равномерный съем тепла, t = const; постоянное время пребывание исходных реагентов в зоне реакции. Реакционный узел синтеза ДМД представляет два последовательно соединенных между собой трубчатых аппарата. Каждая трубка реактора снабжена соплом, обеспечивающим высокую скорость подачи изобутиленовой фракции и ее расщепление при соприкосновении с движущей навстречу водной фазой. Отвод тепла реакции осуществляется паровым конденсатом через межтрубное пространство. /> Различные способы получения фенола. Для кумольного способа привести принципиальную технологическую схему. Обосновать выбор типа и конструкции реактора окисления изопропилбензола. Перечислить основные побочные продукты кумольного способа, как они образуются и утилизируются. a) Хлорбензольный: /> Сульфирование бензола /> Метод Рашига: /> Кумольный метод: /> Окисление толуола: /> Окисление циклогексана: /> б) /> в) колонна окислительная – РИВ, противоток; все недостатки гетерофазного процесса каскад реакторов идеального смешения. г) разложение гидроперекиси на катионитах /> /> />
2dip.su
Методы синтеза сложных эфиров целлюлозы
Из методов синтеза сложных эфиров целлюлозы, разработанных в последние годы, существенный интерес представляют реакции нуклеофильного замещения и переэтерификации. Основные лабораторные и промышленные методы синтеза изложены при описании методов получения соответствующих эфиров целлюлозы. Ниже приводятся краткие данные о новых методах этерификации целлюлозы, которые, по-видимому, получат в дальнейшем более широкое применение. [c.256]
В последние годы синтезированы новые эфиры целлюлозы, предложены новые катализаторы для осуществления реакций этерификации. Результаты исследований изложены в различных обзорах и монографиях [7] и поэтому в данном разделе не рассматриваются. Из новых методов синтеза сложных эфиров целлюлозы известный интерес представляют этерификация целлюлозы на поверхности раздела фаз и реакция переэтерификации. [c.16]Для получения эфиров целлюлозы и ненасыщенных органических кислот можно использовать обычные методы, применяемые для синтеза сложных эфиров целлюлозы взаимодействие с хлорангидридами кислот в среде различных оснований, с ангидридами кислот в присутствии или в отсутствие катализатора, переэтерификация эфира целлюлозы соответствующей кислотой, непосредственное действие кислот на целлюлозу в присутствии катализаторов, нуклеофильное замещение остатков некоторых кислот в эфирах целлюлозы при действии солей непредельных кислот. Необходимо отметить, что при синтезе непредельных эфиров целлюлозы возникают специфические затруднения, связанные со способностью ненасыщенных кислот к полимеризации. [c.349]
Существенный интерес представляет осуществленный советскими исследователями синтез сложного эфира целлюлозы, содержащего тройные связи Эфир целлюлозы и пропиоловой кислоты был синтезирован тремя методами. [c.352]
Синтез сложных эфиров целлюлозы этерификацией гидроксильных групп действием органических или минеральных кислот или их ангидридов — основной метод, на котором основывается промышленность химической переработки целлюлозы. Достаточно указать на производство нитратов, ксантогенатов и ацетатов целлюлозы, чтобы оценить практическое значение этого метода. [c.16]
Смешанные эфиры целлюлозы, содержащие наряду с остатками уксусной кислоты небольшое количество остатков других кислот (5—15% от суммарной степени замещения эфира целлюлозы), могут быть получены различными методами. Наиболее целесообразным способом синтеза этих производных целлюлозы является добавление в ацетилирующую смесь некоторых количеств кислот, которые должны быть введены в молекулу сложного эфира целлюлозы. Если прямое ацилирование смесью кислот или ангидридов представляет затруднение, смешанные эфиры получают взаимодействием кислоты или ее ангидрида с вторичным ацетатом целлюлозы, обычно растворенным в каком-либо растворителе. В этих условиях ацилирование протекает в более мягких условиях. [c.339]
Реакция нуклеофильного замещения может быть с успехом использована для синтеза сложных эфиров, которые другими методами не могут быть получены (например, эфиры целлюлозы и а-аминокислот) или образуются с большим трудом (эфиры целлюлозы и кислот, содержащих тройные связи). [c.33]
Все эти тенденции, естественно, необходимо было учесть при подготовке данной книги. По сравнению с изданной в 1953 г. книгой 3. А. Роговина и Н. Н. Шорыгиной Химия целлюлозы и ее спутников в этой монографии сокращены разделы, посвященные вопросам взаимодействия целлюлозы с основаниями, гидролизу и окислению целлюлозы, и в известной степени разделы по синтезу и исследованию свойств сложных и простых эфиров целлюлозы. Одновременно введены новые разделы, отражающие современные направления развития химии целлюлозы. Это — новые методы превращений, обеспечивающие введение в макромолекулу целлюлозы разнообразных функциональных групп и, особенно, синтез и исследование свойств привитых сополимеров целлюлозы с различными синтетическими полимерами. Во избежание чрезмерного увеличения объема монографии исключен ряд разделов, относящихся к выделению целлюлозы из растительных материалов, а также все разделы, посвященные спутникам целлюлозы — лигнину и полиозам, которые требуют освещения в специальных монографиях. [c.10]
Триалкилфосфаты были получены по крайней мере 100 лет назад а синтез трифенилфосфатов относится к 1854 г. Однако сложные эфиры фосфорной кислоты не представляли промышленного интереса до начала 20-х годов настоящего столетия, когда была сделана попытка найти заменители пластификатора для нитрата целлюлозы, чтобы ликвидировать монополию Японии в области производства камфоры. В последние годы третичные эфиры фосфорной кислоты нашли широкое применение в качестве пластификаторов, противопенных присадок, присадок к маслам и моторным топливам, а также огнестойких гидравлических жидкостей и синтетических смазочных масел. Методы получения этих соединений могут быть рассмотрены на примерах синтеза трех типов эфиров фосфорной кислоты триа-рил-, триалкил- и алкиларилфосфатов. [c.38]
Сложные и простые эфиры целлюлозы. Описано большое число сложных, простых и смешанных эфиров целлюлозы. Принципы их получения сопоставлены в табл. 6, в которой различные замещенные производные классифицированы ио функциональным группам. Методы синтеза, свойства и применение главных замещенных производных целлюлозы являются предметом отдельной книги и здесь не рассматриваются. [c.114]
Более широкое исцользованпе этого метода для синтеза сложных эфиров целлюлозы зависит от возможности применения в качестве исходных продуктов более доступных эфиров целлюлозы, особенно ее нитратов. [c.35]
Возможности использования этого метода для синтеза сложных эфиров целлюлозы в известной степени ограничены применением в качестве исходных продуктов эфиров целлюлозы и сульфокислот. Они могут быть расширены при использовании более до ступных эфиров целлюлозы, особенно ее нитратов Путем замещения тозилоксигрупп могут быть полу чены также новые типы простых эфиров целлюлозы синтез которых другим методом невозможен. Так после неоднократных неудачных попыток синтеза фениловых эфиров целлюлозы эти эфиры удалось получить Роговину и Владимировой [38] по схеме [c.33]
В результате систематических исследований в этой области, проведенных в течение последних 10— 15 лет в комплексной научной лаборатории кафедры технологии химических волокон Московского текстильного института, был осуществлен синтез сложных эфиров целлюлозы и перфторалкановых кислот 188], простых фторсодержащих эфиров целлюлозы 189, 190], а также фтордезоксипроизводных целлюлозы [191]. Большое внимание было уделено разработке практически приемлемых методов получения привитых сополимеров с фторсодержащими мономерами (подробнее см. с. 151). [c.104]
В результате проведенных до настоящего времени исследований установлен бесспорный факт, не получивший, однако, до сих пор удовлетворительного объяснения, что путем синтеза низкозамешенных производных целлюлозы (простые и сложные эфиры целлюлозы), а также привитых сополимеров целлюлозы удается замедлить, а в ряде случаев почти полностью устранить ферментативное расщепление целлюлозных материалов. Так, например, при содержании в препаратах 2—3% алкоксильных групп (метил-, этил-целлюлоза) рост бактерий, разрушающих целлюлозу, уже не происходит Метод частичной этерификации или 0-алкилирования целлюлозы получил в последние годы практическое применение для повышения устойчивости этих материалов к действию микроорганизмов и к гниению (частичное ацетилирование.цианэтилирова-ние, этилирование и т. д.). [c.196]
Реакции нуклеофильного замещения широко применяются в органической химии низкомолекулярных соединений и, в частности, в химии сахаров для синтеза большого числа разнообразных производных. По механизму нуклеофильного замещения протекают, в частности, все реакции О-алкилирования целлюлозы, т- е. получение различных типов простых эфиров целлюлозы. При этом роль нуклеофильного реагента, атакующего различные 0-алкили-рующие реагенты, играют ионизированные гидроксильные группы целлюлозы. Однако синтез производных целлюлозы по реакции нуклеофильного замещения может быть осуществлен и по принципиально иной схеме — взаимодействием различных низкомолекулярных нуклеофильных реагентов с цёллюлозой (редко) или с некоторыми сложными эфирами целлюлозы. Таким путем можно синтезировать новые классы производных целлюлозы, получение которых другими известными методами до настоящего времени не представлялось возможным. [c.430]
Использование реакций этого типа является перспективным методом синтеза различных производных дезоксицеллюлозы. Выше уже указывалось, что при использовании в качестве нуклеофильных реагентов алкоголятов некоторых спиртов или щелочных солей карбоновых кислот образуются простые или сложные эфиры целлюлозы [c.438]
Эффективность прививки методом передачи цепи от макрорадикала гомополимера может быть повышена введением в молекулу целлюлозы группировок, понижающих энергию активации реакции передачи цепи. С этой целью был осуществлен синтез производных целлюлозы, содержащих бром (смешанный сложный эфир целлюлозы с уксусной и 11-бромундекановой кислотами) или сульфгидрильпые группы (продукт обработки щелочной целлюлозы этиленсульфидом) При введении сульфгидрильных групп (метод, предложенный впервые Глукманом ) эффективность прививки повышается в 4—5 раз. Значительное увеличение расхода мономера на прививку, а не на гомополимеризацию наблюдалось и при прививке на эфир целлюлозы, содержащий N-алкиламино-группы, в частности N-пропиламиногруппы . [c.478]
Впервые реакция переэтерификации была использована для получения бората целлюлозы [10]. При алкоголизе целлюлозной метил- и н-пропнлборатов был получен борат целлюлозы со степенью замещения 2,88, легко гидролизовавшийся водой. Позднее были проведены систематические исследования синтеза фосфорсодержащих эфиров целлюлозы алко-голизом целлюлозой эфиров кислот трехвалентного фосфора. При переэтерификации были использованы моно- [И], ди- [12] и триметилфосфиты [13], а также эфиры фосфонистой кислоты [14]. Проведенные исследования показали, что степень замещения эфира целлюлозы в этих реакциях может быть повышена при проведении их в среде апротонного растворителя (диметилформамида), а снижение температуры реакции может быть достигнуто при использовании вместо диметилфосфитов фенил-Р-хлорэтил- или Р-фторэтилфосфитов [15, 16]. Значительный интерес представляет реакция алкоголиза ОН-группами целлюлозы эфиров арил- и нафталинсульфокислот, приводящая к образованию не сложных, как в рассмотренных выше случаях, а простых эфиров целлюлозы [17, 18]. Как известно, алкоголиз целлюлозой сложных эфиров серной кислоты (диметилсульфата) лежит в основе одного из широко распространенных методов получения метилцеллюлозы. [c.18]
Наконец, в результате сложных химических превращений получен ряд сложных эфиров целлюлозы. Хотя механизм этих реакций недостаточно выяснен [291], известно, что цианаты целлюлозы, например, можно получить нагреванием целлюлозы, пропитанной биуретом [364]. Другим специфическим методом получения является синтез антрапилового эфира целлюлозы действием на целлюлозу ангидрида N-кapбoк иaнтpaнилoвoй кислоты в присутствии щелочи или ацетата калия [322]. [c.303]
Также как и при получении сложных эфиров целлюлозы, свойства и области применения простых эфиров определяются не только степенью алкилирования, но и распределением заместителей в элементарном звене макромолекулы целлюлозы [212]. Эфиры с низкой степенью алкилирования находят применение в текстильной промышленности [101, ИЗ, 143, 144] для модификации свойств целлюлозных волокон и изделий из них, а с более высокой степенью алкилирования — в бумажной промышленности [165, 278, 281, 306, 397, 422, 424]. По-видимому, для ряда целей могут быть использованы и сложные эфиры целлюлозы с низкой степенью этерификации, однако простые эфиры обладают значительно более высокой устойчивостью к гидролизу. Синтез высокозамещенных простых эфиров целлюлозы затруднен и в значительной степени определяется доступностью. Известны методы получения высокоэтерифицированных препаратов метилцеллюлозы [316]. Смешанные простые эфиры целлюлозы, содержащие более одного заместителя, получаются сравнительно легко [160] и имеют практическое значение [212, 213]. [c.303]
chem21.info
Лекция - Способы получения сложных эфиров Конденсации формальдегида с изобутиленом Различные способы
Способы получения сложных эфиров. Основные продукты и области их применения. Условия проведения реакции этерификации органических кислот со спиртами. Катализаторы процесса. Особенности технологического оформления реакционного узла этерификации.
Взаимодействие кислот со спиртами:
/>
Это наиболее распространенный способ получения сложных эфиров.
Синтез сложных эфиров методом конденсации альдегидов:
/>
Синтез сложных эфиров из альдегидов (реакция Тищенко) осуществляется в присутствии алкоголята алюминия, активированного хлоридом железа или, что лучше, хлоридом алюминия и окисью цинка. Данный метод имеет промышленное значение.
Присоединение органических кислот к алкенам:
/>
Синтез сложных эфиров путем дегидрогенизации спиртов:
/>
Получение сложных эфиров методом переэтерификации.
Данная реакция имеет две разновидности: реакция обмена между эфиром и спиртом спиртовыми радикалами (реакция алкоголиза):
/>
и реакция обмена кислотными радикалами у спиртовой группы эфира:
/>
Синтез эфиров из ангидридов кислот и спиртов:
/>
Взаимодействие кетонов со спиртами:
/>
Взаимодействие между галоидангидридами и спиртами:
/>
Реакция между серебряными или калиевыми солями кислот и алифатическими галоидными производными:
/>
Взаимодействие кислот с алифатическими диазосоединениями (в основном с диазометаном):
/>
Основными продуктами реакции этерификации являются сложные эфиры, используемые в качестве растворителей, пластификаторов, синтетических смазочных масел и гидравлических жидкостей, душистых веществ, мономеров.
Этерификацию спиртов карбоновыми кислотами можно проводить в отсутствии катализатора, но в этом случае она протекает медленно и для достижения достаточной скорости требуется высокая температура (200-300ОС). Но когда примесь катализатора трудно отмывается, применяют именно некаталитический процесс. В присутствии кислотных катализаторов этерификация протекает при температуре 70-150ОС.
Наиболее распространенными катализаторами этерификации являются минеральные кислоты: серная, фосфорная. Могут использоваться бензолсульфокислота, толуолсульфокислота и т.д. Большую группу катализаторов составляют соли органических и неорганических кислот. Могут быть использованы в качестве катализаторов реакции этерификации: перекись титана, молибден на инертном носителе, активный этилат алюминия, алкоголяты титана и др. Все более широкое применение в качестве катализаторов получают ионообменные смолы.
/>
Вариант 18
Реакции гидролиза. Получаемые продукты и области их применения. Основные гидролизующие агенты и катализаторы. Способы регулирования селективности в процессах гидролиза. Обосновать выбор реакторного узла для процесса жидкофазного гидролиза хлорпентана в аллиловые спирты.
Реакциями гидролиза называют процессы замещения или двойного обмена, протекающие под действием воды или щелочей. С помощью гидролиза синтезируют некоторые производные фенолов, служащие основой для получения пестицидов. Для получения спиртов щелочной гидролиз сохраняет значение как путь синтеза аллилового спирта. Гидролиз – одна из стадий получения глицерина. Гидролизом нитрилов получают карбоновые кислоты. Кроме того, гидролиз – одна из стадий получения таких продуктов как: акрилонитрил, поливиниловый спирт, этиловый спирт из древесины, акриламид, высшие жирные спирты (процесс «Алфол»), МХУК, производство капролактама из анилина и т.д.
Вода или водяной пар в отсутствии катализатора – очень слабый гидролизующий агент. В качестве щелочных гидролизующих агентов применяют водные или водно – спиртовые растворы щелочей (для щелочного плавления – твердая щелочь с небольшой добавкой воды). Водные растворы слабых щелочей оказывают более медленное и мягкое гидролизующее действие. Для гидролиза типично каталитическое влияние кислот, которое зависит от их силы. Часто используют серную кислоту, но ее применение нередко ведет к побочным реакциям конденсации и осмоления. Поэтому используют и кислоты более мягкого действия – органические сульфокислоты, которые лучше растворимы в органических средах, и, кроме того, обладают поверхностно – активными свойствами, что облегчает гомогенизацию реакционной массы. Кроме этого часто применяются гетерогенные контакты кислотного типа (катиониты, фосфорная кислота на носителе и т.д.), преимущество которых состоит в малом расходе, меньшей коррозионной активности и снижении количества сточных вод.
При действии щелочей на хлорпроизводные возможны параллельные реакции замещения (гидролиз) и отщепления (дегидрохлорирование) атомов хлора. На их относительную долю влияют температура, среда, но самым эффективным методом регулирования направления этих двух реакций является выбор гидролизующего агента. Для гидролизу требуется слабое основание, обладающее высокой нуклеофильностью (например Na2CO3), а для дегидрохлорирорвания – сильное основание с небольшой нуклеофильностью (NaOH, Ca(OH)2). Эффективный путь подавления побочных реакций – снижение концентрации целевого продукта в реакционной массе путем его непрерывной отгонки. Этому способствует то обстоятельство, что целевой продукт всегда более летучий, чем исходные реагенты. Для повышения селективности реакций гидролиза целесообразно применять реакторы, близкие к модели идеального вытеснения.
При жидкофазном гидролизе хлорпентана в аллиловые спирты в качестве гидролизующих агентов применяют 5-10%-ный раствор Na2CO3 или NaOH, который для обеспечения более высокой интенсивности процесса и повышения степени конверсии хлорпроизводного берут в избытке 10-25% к стехиометрическому количеству. Ввиду наличия двух жидких фаз важное значение имеет увеличение поверхности их контакта. При непрерывных процессах это достигается обычно уже в насосе, во всасывающую линию которого подают оба реагента. Сохранение системы в эмульгированном состоянии обеспечивается турбулизация потока за счет его достаточно большой линейной скорости. Это предопределяет использование реакторов типа змеевиков или многоходовых кожухотрубных аппаратов, что возможно при небольшом времени реакции. Когда ее продолжительность велика и продукт выпускают в небольшом масштабе, процесс осуществляется периодическим способом в автоклаве, перемешивая смесь мешалкой или барботируя через нее пар соответствующего давления. Реакционную массу по окончании процесса дросселируют до атмосферного давления, причем целевой продукт переходит в газовую фазу (аллиловый спирт). После этого спирт чистят ректификацией.
Конденсации формальдегида с изобутиленом
При конденсации формальдегида с изобутиленом можно использовать изобутилен-изобутановую фракцию с содержанием изобутилена до 50%масс и примесями линейных бутенов без предварительного выделения. Изложите химизм процесса и объясните, почему это возможно. Поясните, почему лимитируется содержание бутадиена-1,3 в исходном сырье. Каковы условия и особенности гетерофазного процесса конденсации и оформления реакционного узла.
Конденсация формальдегида с изобутиленом, протекающая в присутствии катализаторов кислотного типа (реакция Принса), приобрела практическое значение для синтеза 4,4 – диметилдиоксана – 1,3. Побочно образуются ненасыщенные одноатомные спирты, триметилкарбинол (продукт гидратации изобутилена) и более сложные кислородсодержащие соединения. Образование всех этих веществ объясняет следующая схема.
Обычно сопутствующие изобутилену непредельные углеводороды С4 нормального строения, также как пропилен и олефины С5, значительно уступают по реакционной способности изобутилену, обладающему активным реакционноспособным атомом водорода при третичном атоме углерода во взаимодействии с формальдегидом. Скорости взаимодействия с формальдегидом 1-бутена и 2-бутена приблизительно на два порядка ниже, чем с изобутиленом. Это означает, что в условиях синтеза диметилдиоксана бутены нормального строения практически не реагирует, и, следовательно, их предварительное выделение из углеводородного сырья не требуется.
Данный вывод неприемлем лишь к бутадиену-1,3, продукт взаимодействия которого с формальдегидом (4-винилдиоксан-1,3), при последующем расщеплении даёт циклопентадиен – сильнейший каталитический яд реакции стереоспецифической полимеризации изопрена. Поэтому на исходную фракцию С4 налагаются жёсткие требования по содержанию бутадиена (≤ 0,3 % мас.).
Конденсация изобутилена с формальдегидом – это гетерофазная жидкофазная каталитическая реакция, в которой взаимодействие осуществляется в пределах одной реакционной фазы (водной), а реакционная масса представляет собой жидкую двухфазную систему. Продукты реакции распределяются между двумя фазами в соответствии с их природой. Присутствие ДМД в водной фазе нежелательно, т.к. в присутствии серной кислоты он гидролизуется, поэтому его экстрагируют в углеводородную фазу парафиновыми углеводородами, содержащимися в сырье. Интенсивность реакции во многом зависит от развития поверхности контакта.
Условия процесса: Т=85-95oC, Р = 1,5-2 МПа, когда все реагенты находятся в жидком состоянии. Конверсия 85-90% по обоим реагентам, мольное соотношение – формальдегид: i-бутилен = 2/1, причем в реакционной массе должен всегда находиться свободный формальдегид, чтобы препятствовать полимеризации изобутилена. Катализатор h3SO4 – 1 – 1,5 % вес. по отношению к изобутилену. Процесс проводится в реакторе идеального вытеснения, работающем по принципу прямо – или противотока. Реактор должен удовлетворять следующим требованиям:
--PAGE_BREAK--интенсивный массообмен между углеводородной и водной фазами;
равномерный съем тепла, t = const;
постоянное время пребывание исходных реагентов в зоне реакции.
Реакционный узел синтеза ДМД представляет два последовательно соединенных между собой трубчатых аппарата. Каждая трубка реактора снабжена соплом, обеспечивающим высокую скорость подачи изобутиленовой фракции и ее расщепление при соприкосновении с движущей навстречу водной фазой. Отвод тепла реакции осуществляется паровым конденсатом через межтрубное пространство.
/>
Различные способы получения фенола. Для кумольного способа привести принципиальную технологическую схему. Обосновать выбор типа и конструкции реактора окисления изопропилбензола. Перечислить основные побочные продукты кумольного способа, как они образуются и утилизируются.
a) Хлорбензольный:
/>
Сульфирование бензола
/>
Метод Рашига:
/>
Кумольный метод:
/>
Окисление толуола:
/>
Окисление циклогексана:
/>
б) />
в) колонна окислительная – РИВ, противоток; все недостатки гетерофазного процесса
каскад реакторов идеального смешения.
г) разложение гидроперекиси на катионитах
/>
/>
/>
www.ronl.ru