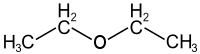Номенклатура и изомерия. Номенклатура эфиров
11.3.Простые эфиры
11.3.1.Номенклатура простых эфиров
Согласно тривиальной номенклатуре, простые эфиры называют по радикалам, связанным с атомом кислорода, добавляя слово «эфир»:
| (Сh4)2CH-OC2H5 изопропилэтиловый эфир | (Ch4)2CH-O-CH(Ch4)2 диизопропиловый эфир |
| Ch4-O-Сh3Ch3Ch3Ch4 н-бутилметиловый эфир |
По номенклатуре ИЮПАК эфиры рассматривают как алкоксиалканы. Корень названия определяет наиболее длинная алкильная группа:
| Сh4OCh3Ch3OCh4 1,2-диметоксиэтан | 3-пропоксигексан |
| 1-этокси-4,4-диметилпентан | |
Простые эфиры имеют ту же геометрию, что и Н2О. Валентный угол С-О-С соответствует 112° для СН3ОСН3, что близко к тетраэдрическому углу и указывает на sp3-характер гибридизации атома кислорода. Простые эфиры относятся к числу малореакционноспособных веществ и стабильны по отношению ко многим реагентам (металлоорганическим соединениям и др.), но они чувствительны по отношению к кислороду и легко образуют взрывчатые гидропероксиды, которые являются причиной взрыва при неосторожном обращении.
11.3.2.Получение простых эфиров
Существует три общих метода получения простых эфиров: межмолекулярная дегидратация спиртов, алкоксимеркурирование алкенов и реакция А.Вильямсона.
11.3.2.А. Межмолекулярная дегидратация спиртов
Этот наиболее старый способ получения простых эфиров описан ранее в этой главе. Он пригоден для получения симметричных простых эфиров из неразветвленных первичных спиртов:

Третичные спирты в этих условиях образуют алкены в результате внутримолекулярной дегидратации. Метод непригоден для получения смешанных эфиров, за исключением такого случая, когда один спирт третичный, а второй - первичный:

Межмолекулярная дегидратация спиртов имеет крайне ограниченное значение в практике органического синтеза. В промышленности этим способом получают диэтиловый, дибутиловый и ряд других простейших эфиров. Гораздо более важными общими методами синтеза простых эфиров являются алкоксимеркурирование алкенов и реакция Вильямсона.
11.3.2.Б.Алкоксимеркурирование алкенов
Алкоксимеркурирование алкенов по существу аналогично оксимеркурированию (гл. 5, ч. 1), единственное различие состоит в том, что роль «внешнего» нуклеофильного агента выполняет спирт, который используется в качестве растворителя. Для получения эфиров, содержащих третичную или вторичную алкильную группу в качестве электрофильного агента, целесообразно использовать трифторацетат ртути:

Последующее демеркурирование осуществляется с помощью боргидрида натрия. Суммарный результат соответствует присоединению спирта по двойной связи алкена в соответствии с правилом Марковникова:


Механизм реакции полностью аналогичен механизму оксимеркурирования алкенов (гл. 5, ч. 1).
11.3.2.В. Синтез простых эфиров по а.Вильямсону
Эта реакция рассматривалась ранее в этой же главе:

Так можно получать как симметричные, так и несимметричные эфиры. Механизм реакции и область ее применения обсуждались ранее. Эта старая реакция неожиданно обрела второе рождение после открытия нового класса простых эфиров, так называемых краун-полиэфиров1. Краун-полиэфирами называют макроциклические полиэфиры, содержащие несколько атомов кислорода в цикле. Все краун-полиэфиры характеризуются регулярной структурой, где каждые два атома кислорода в цикле связаны посредством двух метиленовых звеньев, т.е. формально краун-полиэфиры можно рассматривать как продукты циклоолигомеризации окиси этилена. В названиях краун-полиэфиров первая цифра указывает на размер цикла, а вторая определяет число атомов кислорода в цикле.
| | | | |
| 12-краун-4 | 15-краун-5 | 18-краун-6 | 24-краун-8 |
Первый краун-полиэфир дибензо-18-краун-б был получен К.Педерсеном в 1967 г. с помощью реакции Вильямсона между динатриевой солью пирокатехина и бис-(2-хлорэтиловым) эфиром:

Другие краун-полиэфиры также получают при конденсации дигалогенидов или дисульфонатов с дианионом диолов. В качестве примера приведем синтез 18-краун-6 (Д.Крам) как наиболее важного из краун-полиэфиров и 24-краун-8-полиэфира. Выход циклических краун-полиэфиров очень сильно зависит от природы катиона основания:


Наиболее высокий выход 18-краун-6-полиэфира наблюдается при использовании алкоголятов калия, а для 12-краун-4 - алкоголятов лития. Выходы обоих краун-полиэфиров падают практически до нуля, если в качестве основания берется гидроксид тетраалкиламмония. Это указывает на то, что катион играет роль матрицы при образовании цикла, содержащего определенное число атомов кислорода. Размер цикла определяется координационным числом катиона щелочного металла. Координационное число К+ по отношению к кислородсодержащим лигандам равно шести, поэтому катион калия наиболее эффективен при получении 18-краун-б-полиэфира с шестью атомами кислорода в цикле. Аналогично катион лития с координационным числом четыре способствует замыканию цикла, содержащего столько же атомов кислорода:

Влияние катиона на размер образующего цикла получило название матричного, или «темплатного», эффекта.
Краун-полиэфиры образуют стабильные комплексы с катионами непереходных и переходных металлов. Стабильность этих комплексов зависит от соответствия диаметра катиона размеру полости кольца, а также от координационного числа катиона металла. Катион лития с диаметром иона 1,20 Å образует стабильный комплекс с 12-краун-4-полиэфиром с диаметром полости кольца 1,2—1,5 Å; катион натрия (d = 1,9 Å) даст наиболее стабильный комплекс с 15-краун-5 (d = 1,7-2,2 Å), катион калия (d = 2,66 Å) - с 18-краун-6 (d = 2,6-3,2 Å). Катион цезия с d = 3,38 Å образует прочный комплекс с 24-краун-8-полиэфиром с диаметром полости кольца порядка 4 Å. Комплексообразование краун-полиэфиров, их сернистых и азотных аналогов, а также полициклических краун-соединений - так называемых криптандов - с катионами металлов составляет интересный самостоятельный раздел современной аналитической химии:
 криптанд[2,2,2]
криптанд[2,2,2]
studfiles.net
Номенклатура и изомерия - Сложные эфиры - Сложная эфиры. Жиры. Моющие средства - Органическая химия
Среди функциональных производных карбоновых кислот особое место занимают сложные эфиры — соединения, представляющие карбоновые кислоты, у которых атом водорода в карбоксильной группе заменен углеводородным радикалом. Общая формула сложных эфиров
| R — C — O — R’ |
| || |
| O |
где R и R‘ — углеводородные радикалы (в сложных эфирах муравьиной кислоты R — атом водорода).
Названия сложных эфиров производят от названия, углеводородного радикала и названия кислоты, в котором вместо окончания "-овая кислота" используют суффикс "ат", например:
|
| |||||||||||||||||||||||||
Часто сложные эфиры называют по тем остаткам кислот и спиртов, из которых они состоят. Так, рассмотренные выше сложные эфиры могут быть названы: этановоэтиловый эфир, кротоновометиловый эфир.
Для сложных эфиров характерны три вида изомерии:
1. Изомерия углеродной цепи, начинается по кислотному/> остатку с бутановой кислоты, по спиртовому остатку — с пропилового спирта, например:
|
| |||||||||||||||||||||||||
|
| |||||||||||||||||||||||||
2. Изомерия положения сложноэфирной группировки />-СО-О-. Этот вид изомерии начинается со сложных эфиров, в молекулах которых содержится не менее 4 атомов углерода, например:/>
| СН3-СО-О-С2Н5 | С2Н5-СО-О-СН3 | |
| этилацетат | метилпропионат |
3. Межклассовая изомерия, например:
| СН3-СО-О-СН3 | С2Н5-СО-ОН | |
| метилацетат | пропионовая кислота |
Для сложных эфиров, содержащих непредельную кислоту или непредельный спирт, возможны еще два вида изомерии: изомерия положения кратной связи; цис-транс-изомерия.
Физические свойства сложных эфиров. Сложные эфиры />низших карбоновых кислот и спиртов представляют собой летучие, малорастворимые или практически нерастворимые в воде жидкости. Многие из них имеют приятный запах. Так, например, бутилбутират имеет запах ананаса, изоамилацетат — груши и т.д.
Сложные эфиры имеют, как правило, более низкую температуру кипения, чем соответствующие им кислоты. Например, стеариновая кислота кипит при 232 °С (Р = 15 мм рт. ст.), а метилстеарат— при 215 °С (Р =15 мм рт. ст.). Объясняется это тем, что между молекулами сложных эфиров отсутствуют водородные связи.
Сложные эфиры высших жирных кислот и спиртов — воскообразные вещества, не имеют запаха, в воде не растворимы, хорошо растворимы в органических растворителях. Например, пчелиный воск представляет собой в основном мирицилпальмитат (C15h41COOC31H63).
www.himhelp.ru
Номенклатура эфиров простых - Справочник химика 21
Номенклатура и изомерия. Простые эфиры обычно называют по рациональной номенклатуре. Названия эфиров производят от названий алкильных радикалов [c.115]О)гласно номенклатуре ЮПАК, простые эфиры называют, прибавляя к названию старшего (наиболее длинного) углеводородного радикала в качестве приставки название алкоксигруппы (R — О) или для эфиров фенолов — арилоксигруппы (Аг — О). Например, [c.208]
НОМЕНКЛАТУРА ПРОСТЫХ ЭФИРОВ [c.2322]Номенклатура и изомерия. Названия отдельных простых эфиров производят от названий образующих их радикалов. Например [c.127]
Номенклатура простых эфиров [c.332]
Наиболее последовательным 1ло бы применять к жирам принцип сокращенной номенклатуры сложных эфиров по аналогии с солями кислот. С этой точки зрения жир, образованный, например, тремя молекулами стеариновой кислоты, следует назвать тристеаратом глицерина. Так же просто можно называть и смешанные глицериды, например [c.85]
Согласно номенклатуре ЮПАК простые эфиры называют двумя способами, прибавляя к названию старшего (наиболее длинного) углеводородного радикала в качестве префикса название алкокси-группы (К—О—) пли для эфиров фенолов — арилоксигруппы (Аг—О—), например [c.233]
Номенклатура эфиров не отличается от обычно применяемой в современной мировой литературе. В основе ее лежат простые [c.32]
В названиях альдегидов и в той части сложных эфиров, которая присоединена к атому углерода, используется кислотная номенклатура. В названиях спиртов, простых эфиров, кетонов, аминов и той части сложных эфиров, которая присоединена к атому кислорода, используется номенклатура алканов. [c.295]
Номенклатура простых эфиров. Простые эфиры называют по радикалам. Так, например [c.137]
Задание 5.27. Назовите по заместительной и радикально-функци-ональной номенклатуре следующие простые эфиры С,Н,ОСН,СН,СН, [c.192]
Номенклатура циклических простых эфиров 364 [c.6]
НОМЕНКЛАТУРА ЦИКЛИЧЕСКИХ ПРОСТЫХ ЭФИРОВ [c.364]
Простые эфиры рассматриваются как углеводороды, в которых один или несколько атомов водорода замещены алкоксигруппами. Для симметричных эфиров может быть сохранена ныне принятая номенклатура. [c.295]
НОМЕНКЛАТУРА ПРОСТЫХ ЭФИРОВ 70 [c.847]
В применяемой СА заместительной номенклатуре для простой эфирной группы КО нет суффикса, и эта группа должна фигурировать только в префиксе. Даже самые простые эфиры при этом получают довольно необычные названия, например С2Н5ОС2Н5 1-этоксиэтан. Однако алкокси-префиксные названия становятся удобнее названий с использованием слова эфир, когда один из составляющих радикалов много больше другого или имеется несколько алкоксигрупп. В качестве примера приведем названия Зр-метокси-5а-холестан и 2,3,5-триметоксихино-лин. [c.131]
Резюме номенклатура простых эфиров [c.184]
Номенклатура алифатических и ароматических галогенпроизвод-ных углеводородов, спиртов, одно- и двухосновных фенолов, простых эфиров, тиолов, тиоэфиров, нитросоединений и аминов. [c.193]
Простые эфиры обычно называют по радикально-функциональной номенклатуре [c.178]
В рассмотренном случае изомеры принадлежат к одному классу органических соединений - алканам, но часто бывает, что изомерами с одной молекулярной формулой являются вещества из разных классов. Например, одной молекулярной формуле С Н 0 соответствуют семь разных соединений из классов спиртов и простых эфиров. Они изображены ниже, а Вы назовите их по правилам систематической номенклатуры. [c.203]
Номенклатура простых эфиров.........................................................293 [c.229]
Номенклатура. Для более легкого нахождения соединений в таблице их наименования представлены так, что в начале указывается кислота, производными которой они являются. Так, например, вместо этиловый эфир бензойной кислоты в таблице стоит бензойной кислоты эфир . Этиловые эфиры кислоты именуются просто эфирами для всех остальных эфиров указывается спиртовый радикал. Циклические ангидриды, лактоны и азлактоны помещены как производные соответствующих кислот, а не в числе гетероциклических соединений. [c.369]
Номенклатура простых эфиров. Обычно названия простых эфиров строят из названий углеводородных радикалов, связанных с атомом кислорода, с добавлением слова эфир [c.218]
Эфиры простые — Называют всегда по заместительной номенклатуре, используя префиксы R-окси или Аг-окси все радикало-функциональные названия исключены, например С2Н5ОС2Н5 этоксиэтан, с. 130, 131. [c.210]
Составьте структурные формулы изомерных простых эфиров, имеющих эмпирическую формулу 4h20O. Назовите их по рациональной номенклатуре и номенклатуре ШРАС. Каким веществам с иной функциональной группой соответствует такая же молекулярная формула Какие виды изомерии характерны для простых эфиров [c.52]
Напишите формулы а ) дипропилового эфира б) этилбутнлового эфира в ) этил-трет-изобутилового эфира г) ди-бтор-бутилового эфира. Какие из них называются смешанными простыми эфирами . Назовите все эфиры по заместительной номенклатуре. [c.40]
Изомерия и номенклатура простых,эфиров. Способы получения. Физические и химические свойства. Применение. Циклические окиси. Способы полуения. ишчесше свойства. Применение в органическом синтезе. Органические перекиси. Номенклатура,получение, свойства. [c.191]
Используемая для краун-эфиров сокращенная номенклатура довольно проста первое число означает общее число атомов в кольце, а второе — общее число гетероатомов. Легко усмотреть аналогию между такими комплексами, имеющими полость для связывания лиганда Ь, и активным центром фермента, специфически узнающим свой субстрат. Размер макроцикла может меняться и тем самым обеспечивать связывание лигандов разных размеров. Циклические полиэфиры типа краун сравнительно легко можно получить и подвергнуть разнообразным структурным модификациям. Эту область химии Крам предложил назвать химией до-норно-акцепторного комплексообразования [134—136]. Напомним также о гипотезе замка и ключа , предложенной Фишером в 1894 г. для описания структурного соответствия между ферментом и его субстратом в ферментсубстратном комплексе. Помимо ферментативного катализа и ингибирования комплексообразование играет первостепенную роль в таких биологических процессах, как репликация, хранение и передача генетической информации, иммунный ответ и транспорт ионов. В настоящее время накоплено уже достаточно сведений о структуре таких комплексов, чтобы подтолкнуть химиков-органиков к созданию высокоструктурированных молекулярных комплексов и к изучению специфического химизма процессов комплексообразования. [c.266]
Назовите ио радика.яьно-функциональной и по заместительной номенклатурам следующие простые эфиры [c.39]
Согласно номенклатуре ИЮПАК, простые эфиры называ-двумя способами, прибавляя к названию старшего (наибо-длинного) углеводородного радикала в качестве префикса звание алкоксигруппы (К—О—) или для эфиров фенолов — илоксигруппы (Аг—О—), например [c.305]
В этом разделе изучаются номенклатура, строение и свойства большой группы производных углевс1Доро-дов, содержащих кислородсодержащие функциональные группы. Простейшими представителями этой группы являются спирты, поэтому они открывают настс ящий раздел. Далее в нем последовательно рассматриваются фенолы, содержащие такую же функциональную группу, как и спирты, альдегиды, карбоновые кислоты, сложные эфиры, в частности, жиры-триглицериды, углеводы [c.526]
Приведите структурные формулы симметричных эфиров состава СеНиО и назовите их по номенклатуре ШРАС. Чем объясняется хорошая растворимость простых эфиров в воде [c.52]
Простые эфиры можно рассматривать как продукты замещения водорода в гидроксильной группе спирта на какой-либо радикал. Общая формула эфиров К—О—К. По рациональной номенклатуре называют радикалы простых эфиров в порядке усложнения, к последнему радикалу добавляя окончание -овый, и заканчивают название словом эфир. По международной номенклатуре за основу принимают название углеводорода с длинной неразветвленной цепью, а к названию второго радикала эфира добавляют окончание -окси, обычно отбрасывая окончание радикалов -мл (СН3О — метокси, С2Н5О — этокси, РО — ал-кокси) [c.38]
Термин сложные эфиры (в отличие от простых эфиров) — одна из неудачных традиций русской номенклатуры название длинное, вызывает путаницу со смешанными простыми эфирами. Однако попытки ввести в обиход термин эстеры (по аналогии с английским и немецким esters) не увенчались успехом, хотя и предпринимались рядом авторов. — Прим. переводчика. [c.170]
Сульфиды являются сернистыми аналогами простых эфиров и имеют общую формулу R—S—R. Их номенклатура аналогична номенклатуре простых эфиров. По правилам ШРАС их называют сульфидами, однако в hem. Abstr. этот термин не применяется. Вот несколько примеров [c.207]
Наиболее употребительные органические соединения сохраняют исторически сложившиеся тривиальные названия, указывающие ибо на происхождение данного вещества (молочная кислота, масляная кислота, мочевина и т. д.), либо на его свойства (эфир, антифебрин, скатол и т. д.). С развитием органического синтеза количество органических соединений стало возрастать с такой быстротой, что, пользуясь прежней системой обозначения, оказалось чрезвычайно трудным придумывать тысячи различных новых названий. Решение было найдено в заместительной, или так называемой рациональной, номенклатуре (PH). Эта номенклатура рассматривает химические соединения к к производные более простых и хорошо известных соединений — прототипов, в которых один или несколько атомов водорода замещены радикалами (остатками углеводородов), другими элементами или функциональными группами (—ОН, —Nh3, —ТМОг и т. д.). В качестве прототипов используются, например, метан, этилен, ацетилен, метиловый спирт, уксусная кислота и другие простейшие соединения. Рациональная номенклатура, очень удобная для обозначения сравнительно простых соединений, теряет свои преимущества при переходе к более сложным соединениям. В связи с этим возникла потребность в создании новой, универсальной международной номенклатуры (МН). [c.36]
Сульфиды являются сернистыми аналогами простых эфиров, поэтому их называли раньше также тиоэфирами. По правилам номенклатуры 1иРАС их называют диалкил-, алкил арил-, диарил- и т.д. -сульфидами, например [c.471]
chem21.info
Заместительная номенклатура простых эфиров - Справочник химика 21
Радикально-функциональная номенклатура используется реже, чем заместительная. В основном она применяется для некоторых классов органических соединений — спиртов, кетонов, простых эфиров и др. [c.28]Кроме заместительной номенклатуры, в меньшей степени продолжает использоваться радикально-функциональная номенклатура, являющаяся также вариантом систематической номенклатуры ИЮПАК. Чаще она применяется для галогенопроизводных, спиртов, аминов и простых эфиров. Для некоторых классов соединений, например карбоновых кислот и альдегидов, эта номенклатура неприменима. [c.33]
При составлении названия простого эфира по заместительной номенклатуре за основу берут старший (наиболее длинный или наиболее разветвленный) радикал, к названию которого прибавляют приставку алкокси- (для алифатических) или арилокси- (для ароматических) групп. Названия эфиров часто составляют по радикально-функциональ-ной номенклатуре, перечисляя в алфавитном порядке радикалы и добавляя название класса — эфир (приведены в скобках). [c.191]Задание 5.27. Назовите по заместительной и радикально-функци-ональной номенклатуре следующие простые эфиры С,Н,ОСН,СН,СН, [c.192]
Соединения типа R—О—R принято называть простыми эфирами, причем название их может строиться различными способами [1] с применением либо радикало-функциональной, либо заместительной номенклатуры. Здесь будут даны пояснения различным способам наименования простых эфиров, после чего будут приведены примеры (табл. 4.3.1, в скобках условной символикой указана использованная система номенклатуры). [c.289]
В применяемой СА заместительной номенклатуре для простой эфирной группы КО нет суффикса, и эта группа должна фигурировать только в префиксе. Даже самые простые эфиры при этом получают довольно необычные названия, например С2Н5ОС2Н5 1-этоксиэтан. Однако алкокси-префиксные названия становятся удобнее названий с использованием слова эфир, когда один из составляющих радикалов много больше другого или имеется несколько алкоксигрупп. В качестве примера приведем названия Зр-метокси-5а-холестан и 2,3,5-триметоксихино-лин. [c.131]
Эфиры простые — Называют всегда по заместительной номенклатуре, используя префиксы R-окси или Аг-окси все радикало-функциональные названия исключены, например С2Н5ОС2Н5 этоксиэтан, с. 130, 131. [c.210]
Назовите ио радика.яьно-функциональной и по заместительной номенклатурам следующие простые эфиры [c.39]
Напишите формулы а ) дипропилового эфира б) этилбутнлового эфира в ) этил-трет-изобутилового эфира г) ди-бтор-бутилового эфира. Какие из них называются смешанными простыми эфирами . Назовите все эфиры по заместительной номенклатуре. [c.40]
Названия простых эфиров, а также их S-, Se- и Те-аналогов формирзтот, используя одну из трех номенклатур радикало-функ-щюнальную, заместительную или заменительную (см. разд. 1.2). [c.138]
Эта форма номенклатуры применяется в Правилах IUPA реже, чем заместительная, но все же занимает немалое место. В Правилах ШРАС радикало-функцио-нальная номенклатура иллюстрируется примерами названий спиртов (метиловый спирт), кетонов (метилэтилкетон, дипропилкетон), галогенпроизводных (метилхлорид, или хлористый метил), нитрилов (бутилцианид), простых эфиров (диэтиловый эфир) и их S-аналогов, азидов. Привьга-ную карбинольную номенклатуру спиртов Правила ШРАС относят к числу нерекомендуемых, так называемые рациональные названия углеводородов, спиртов, ьси-слот (имеются в виду названия типа диметилэтилен, три-фенилкарбинол, метилэтилуксусная кислота — все это по существу радикало-функциональные названия) вообще не упоминаются. [c.369]
Их частные названия образуют аналогично иазваииям простых эфиров по заместительной номенклатуре, используя приставки алкилтио-, или арилтио- и т. д., вместо алкилокси- и т. д. по радикально-функциоиальиой номенклатуре — применяя слово сул1 )ид вместо эфир или оксид , а для ансамблей идентичных структурных компонентов--тио- вместо -окси-. [c.235]
Наиболее употребительные органические соединения сохраняют исторически сложившиеся тривиальные названия, указывающие ибо на происхождение данного вещества (молочная кислота, масляная кислота, мочевина и т. д.), либо на его свойства (эфир, антифебрин, скатол и т. д.). С развитием органического синтеза количество органических соединений стало возрастать с такой быстротой, что, пользуясь прежней системой обозначения, оказалось чрезвычайно трудным придумывать тысячи различных новых названий. Решение было найдено в заместительной, или так называемой рациональной, номенклатуре (PH). Эта номенклатура рассматривает химические соединения к к производные более простых и хорошо известных соединений — прототипов, в которых один или несколько атомов водорода замещены радикалами (остатками углеводородов), другими элементами или функциональными группами (—ОН, —Nh3, —ТМОг и т. д.). В качестве прототипов используются, например, метан, этилен, ацетилен, метиловый спирт, уксусная кислота и другие простейшие соединения. Рациональная номенклатура, очень удобная для обозначения сравнительно простых соединений, теряет свои преимущества при переходе к более сложным соединениям. В связи с этим возникла потребность в создании новой, универсальной международной номенклатуры (МН). [c.36]
chem21.info
Номенклатура, физические свойства сложных эфиров
Сложными эфирами называются органические соединения, молекулы которых состоят из углеводородных радикалов (остатков спирта) и кислотных остатков, соединенных атомом кислорода.
Сложные эфиры можно рассматривать как производные кислот, у которых атом водорода в карбоксиле замещен радикалом:
R – C – O – R/ || O
Общая формула сложных эфиров такая же, как и у карбоновых кислот С n H 2n O 2.
Сложные эфиры могут быть образованы как органическими, так и неорганическими кислотами:

Номенклатура сложных эфиров
Сложные эфиры в большинстве своем называют по тем кислотам и спиртам, остатки которых участвуют в их образовании. По систематической номенклатуре сложные эфиры называют, прибавляя в качестве приставки название спиртового радикала к названию кислоты, в котором окончание “- овая” заменяется на “- оат”.

Изомерия сложных эфиров
Изомерия сложных эфиров определяется изомерией радикалов кислот и спиртов, участвующих в их образовании.
Сложные эфиры являются межклассовыми изомерами с карбоновыми кислотами, имея одинаковую общую формулу.
Физические свойства сложных эфиров
Сложные эфиры простейших и средних представителей кислот и спиртов - жидкости, легче воды, летучие, в большинстве случаев обладающие приятным запахом фруктов. Температуры кипения и плавления сложных эфиров ниже температур кипения и плавления исходных органических кислот. В воде растворимы лишь сложные эфиры с наименьшим числом углеродных атомов. Большинство сложных эфиров плохо растворяется в воде, но хорошо растворяется в органических растворителях.
Таблица 1. Показатели пожарной опасности сложных эфиров
|
Кислоты |
Плотность r, кг/м3 |
tкип |
tвспышки |
tсамовосп |
НТПР |
ВТПР |
| Метилацетат СН3СООСН3 |
927 |
57,3 |
– 15 |
470 |
– 15 |
10 |
| Этилацетат СН3СООС2Н5 |
884 |
77,1 |
2 |
400 |
1 |
31 |
| Бутилацетат СН3СООС4Н9 |
870 |
126,1 |
29 |
421 |
25 |
57 |
| Амилацетат СН3СООС5Н11 |
877 |
148,4 |
25 |
360 |
20 |
58 |
Этилацетат – жидкость с приятным запахом, легко испаряется, плохо растворяется в воде. С воздухом этилацетат образует взрывоопасные смеси. Эфир способен к электризации. При контакте с сильными окислителями (перманганатом калия КMnO4, хромовым ангидридом CrO3, перекисью натрия Na2O2) самовозгорается.
biofile.ru