Простые эфиры этиленгликоля. Монобутиловый эфир
Монобутиловый эфир - Справочник химика 21
Монобутиловый эфир диэтиленгликоля [c.331]Дипропиленгликоля монобутиловый эфир см. Монобутиловый эфир дипропиленгликоля [c.189]
Монобутиловый эфир этиленгликоля Днэтиловый эфир [c.319]
Бутилгликоль см. Монобутиловый эфир этилен- [c.99]
Монобутиловый эфир диэтиленгли- [c.650]
Алфавит. Расположение соединений по алфавиту подчинено общепринятым правилам. При этом отсутствие буквы условно принимается за нулевую букву. Например, Дифенил приводится до Дифениламина . Приставки моно , ди , три , би , бис и т. п., которые не отделяются дефисом, включены в алфавит напрнмер, дибутиловый эфир помещен до монобутилового эфира . В некоторых случаях приставки бис- и т. п. по каким-либо причинам не должны включаться в алфавит (например, Дифениламин, п, ч -бис-диметиламино-), тогда они набраны курсивом и отделены от названия дефисом. Приставки пере-, втор-, ана-, цис-, симм- и т. п. или символы м-, п-. о- и другие, набираемые курсивом и отделяемые от слова дефисом, не включаются в алфавит. [c.394]
Монобутиловый эфир дипропиленгликоля [c.331]На нижней части рисунка показаны результаты азеотропной перегонки смеси монобутилового эфира этиленгликоля со смесью углеводородов при 770 мм рт. ст. Азеотропная смесь содержит около 60% объемн. углеводородов. [c.247]
Эфир уксусной кислоты и 1-оксиаценафтена вводят по каплям в вертикально установленную колонку из нержавеющей стали, нагретую до 520° и наполненную шариками диаметром 3 мм, состоящими из окиси алюминия 90%) и борнокислой меди (10%) в системе поддерживают остаточное давление, равное 2 мм. Продукты реакции собирают в приемнике, охлаждаемом водой. Выходящие из приемника газы пропускают через промывную склянку, содержащую какой-либо растворитель, например, монобутиловый эфир диэтиленгликоля, для растворения сублимированных частиц. Из [c.189]
Монобутиловый эфир триэтиленгликоля [c.331]
Бутокси этанол см. Монобутиловый эфир этиленгликоля [c.109]
Бутоксиэтокси)-этанол см. Монобутиловый эфир диэтиленгликоля [c.109]
Гидрохинона монобутиловый эфир см. Монобутиловый эфир гидрохинона [c.131]
Диэтиленгликоля монобутиловый эфир см. Монобутиловый эфир диэтиленгликоля [c.211]
Монобутиловый эфир гидрохинона [c.331]
Бутилдигликоль 2-(2-Бутоксиэтокси)-этанол Диэтиленгликоля монобутиловый эфир [c.331]
Монобутиловый эфир пропиленгликоля [c.331]
Монобутиловый эфир этиленгликоля [c.331]
Триэтиленгликоля монобутиловый эфир см. Монобутиловый эфир триэтиленгликоля [c.488]
Противообледенительные присадки. К таким присадкам относятся изопропиловый спирт, монобутиловый эфир этиленгликоля, глицеринмоноолеат, некоторые амины. [c.205]
Противообледенительные присадки добавляются к автомобильным бензинам с целью предотвращения обледенения карбюраторов. Присадки предотвращают также замерзание воды в топливных насосах и резервуарах. В качестве нротивообледенительных присадок применяются изопропиловый спирт, монобутиловый эфир этиленгликоля (концентрацией [c.335]
Пирокатехин, диметало-вый эфнр дипропиловый эфир —, диэтиловый эфир моноамиловый эфир —, монобутиловый эфир —, монометиловый эфир монопропиловый эфир [c.892]
Этиловый эфнр 2-метил-пентен 3-овой-5 к-ты Метиловый эфир гндрак-риловой к-ты Метиловый эфир Р, 3-ди-метилакриловой к-ты Монобутиловый эфир диэтиленгликоля бутил-карбнтол) [c.835]
В качестве противообледенительных присадок первого типа, действующих посредством образования с водой низкозамерзающих смесей, известны соединения из класса спиртов, гликолей, формамидов и их производных. Эти присадки действуют в довольно большой концентрации— до 0,5 и даже до 2% например монобутиловый эфир диэтиленгликоля добавляют к бензину в концентрации 0,05—0,5%. Эффективной противообледенительной присадкой этого типа является диметилформамид применяют также гексилен- и дипропиленгликоли, диметил-карбинол, 2-метилпентадиол-2,4-диметилформамид, мо-ноолеат глицерина и др. [8, 9, И, 12]. [c.207]
Пропиленгликоля 1-монобутиловый эфир см. 1-Мо-нобутиловый эфир пропиленгликоля [c.417]
chem21.info
Монобутиловый эфир этиленгликоля - Справочник химика 21
Монобутиловый эфир этиленгликоля Днэтиловый эфир [c.319]На нижней части рисунка показаны результаты азеотропной перегонки смеси монобутилового эфира этиленгликоля со смесью углеводородов при 770 мм рт. ст. Азеотропная смесь содержит около 60% объемн. углеводородов. [c.247]
Бутокси этанол см. Монобутиловый эфир этиленгликоля [c.109]
Монобутиловый эфир этиленгликоля [c.331]
Этиленгликоля монобутиловый эфир см. Монобутиловый эфир этиленгликоля [c.556]
Монометиловый эфир этиленгликоля Моноэтиловый эфир этиленгликоля Монобутиловый эфир этиленгликоля [c.112]Противообледенительные присадки добавляются к автомобильным бензинам с целью предотвращения обледенения карбюраторов. Присадки предотвращают также замерзание воды в топливных насосах и резервуарах. В качестве противообледенительных присадок применяются изопропиловый спирт, монобутиловый эфир этиленгликоля (концентрацией [c.335]
Бутилцеллозольв (монобутиловый эфир этиленгликоля) 171 7.85 А 0.74 6.3 0.77 [c.20]
Остановимся для примера на методе теплот смешения. Теплота смешения простого монобутилового эфира этиленгликоля и воды ири различных темиературах составляет (в кал/ыоль ) [11, с. 77] [c.291]
СбН Ог Монобутиловый эфир этиленгликоля 171,15 166,95 43 [c.522]
Фурфуриловый спирт Пентановая кислота 3 -Метилбутановая кислота Монобутиловый эфир этиленгликоля Бензилметиловый эфир [c.526]
СбН.А Монобутиловый эфир этиленгликоля 171,15 161,2 88 [c.552]
СбН 02 Монобутиловый эфир этиленгликоля 171,25 186,35 63 [c.566]
СбН]402 Монобутиловый эфир этиленгликоля 171,15 166,7 64 [c.570]
Монобутиловый эфир этиленгликоля 171,25 [c.574]
БУТИЛОВЫЙ СПИРТ—МОНОБУТИЛОВЫЙ ЭФИР ЭТИЛЕНГЛИКОЛЯ [c.87]
Монобутиловый эфир этиленгликоля. . . 171,2 [c.85]
Бутилцеллозольв (монобутиловый эфир этиленгликоля)— прозрачная жидкость, обладающая слабым приятным запахом и низкой летучестью. Получают путем оксиэтилирования нормального бутанола. Бутилцеллозольв — растворитель, многих смол и окисленного масла, а в смеси с бутанолом (38 62) применяется в производстве водоразбавляемых лаков и красок. [c.451]
ТУ 38-10269-73) Бутилцеллозольв (монобутиловый эфир этиленгликоля) [c.464]
Эпоксиэфиры могут быть использованы для изготовления водоразбавляемых лакокрасочных материалов . С этой целью их переводят в водорастворимую форму присоединением малеинового -ангидрида к остаткам жирных кислот эпоксиэфира по месту двойных связей либо взаимодействием фталевого ангидрида с остаточными гидроксильными группами эпоксиэфира. Полученные таким образом эпоксиэфиры разбавляют монобутиловым эфиром этиленгликоля, нейтрализуют аммиаком или аминами и разбавляют водой. [c.154]
Противообледенительные присадки. К таким присадкам относятся изопропиловый спирт, монобутиловый эфир этиленгликоля, глицеринмоноолеат, некоторые амины. [c.205]
БУТИЛЦЕЛЛОЗОЛЬВАЦЕТАТ СНзСОО(СН2)20С4Н9, -63,5°С, i 192,3 °С 0,9424, 1,4138 раств. в орг. р-рителях, плохо — в воде (1,5%) (нс,1 71 °С. Получ. взанмод. монобутилового эфира этиленгликоля с уксусной к-той. Р-рите.ль цеЛлюло.зы, эпоксидных смол, по.ливинил-ацетата. [c.89]
Для обнаружения урана может быть использован роданид калия или аммония, дающий с уранилом желтое окрашивание. По данным Арланд [305], образуются комплексные ионы вида [U02S N] , [и02(8СМ)2], [и02(ЗСМ)з1 с константами равновесия 5,7 5,5 и 15 соответственно. Реакция выполняется как в водных растворах, так и в смесях, содержащих ацетон, спирт или монобутиловый эфир этиленгликоля [426]. При определении в среде смешивающихся с водой органических растворителей избирательность метода увеличивается 2г, ТЬ, 5п, Мп, а также ацетаты, сульфаты и фосфаты определению не мешают [437]. Ре (III) предварительно восстанавливают аскорбиновой кислотой [990] или хлористым оловом [633]. Одним из достоинств метода является то обстоятельство, что окраска устойчива в широких пределах кислотности — от 0,1 до 2,0Л/ по НС1 или НМОз, поэтому поддержание точного значения pH не обязательно. Роданидный метод является особенно удобным при определении урана на фоне больших количеств тория. При соотношении и ТЬ=--1 10000 торий не мешает [440]. Но чувствительность роданидного метода невысока — 20—40 мкг мл урана. [c.38]
СбНнОг 2-Бутоксиэтанол (бутилцеллозольв, монобутиловый эфир этиленгликоля) 1 [c.552]
СбНнОг Монобутиловый эфир этиленгликоля 171,15 170,85 25 [c.540]
СбНнОг Монобутиловый эфир этиленгликоля 171,25 170,75 55 [c.573]
Пример. Для получения глиоксалидиновой композиции использовали, части (по массе) аминоэтилэтаноламин 30 и жирную кислоту таллового масла 70. Получившееся в этой реакции вещество (88,5 частей) взаимодействовало с азелаиновой (1,7-гептандикарбоновой) кислотой (11,5 частей). Полученную композицию (35 частей) смешивали с поли-пропиленгликолем молекулярной массой 3800 (25 частей), бутиловым целлозольвом (монобутиловым эфиром этиленгликоля) (20 частей) и водой (20 частей по массе). [c.255]
Для стабилизации комплексного соединения молибдена с роданидом рекомендуют вводить в раствор некоторые водорастворимые органические жидкости, как, например, гликолевый эфир, бутилкарбитол (моно-бутиловый эфир диэтиленгликоля) и бутилцеллозольв (монобутиловый эфир этиленгликоля). В присутствии этих жидкостей интенсивность окраски роданида молибдена нарастает в продолжение 10 мин и затем остается постоянной 24 ч. Способ применяют главным образом в массо- вых анализах стали, так как он исключает необходимость экстрагирования, но в этом-случае следует устранять влияние хрома, который дает окрашенныр ионы, и меди,, которая образует нерастворимые соединения с роданидом. [c.369]
Часть II показывает результаты азеотропной перегонки смеси монобутилового эфира этиленгликоля со смесью ароматических, циклопарафиновых и парафиновых углеводородов при 770 лш Hg, обычно встречающихся в узкокппящей фракции (166—169° С) керосина оклахомской нефти. Азеотропная смесь содержит около 60 % (по объему) углеводородов, причем содержание их увеличивается от ароматических к циклопарафиновым и к парафиновым. [c.86]
Моноэтиловый эфир этиленгликоля. ... Монобутиловый эфир этиленгликоля. . . Ацетат моноэтилового эфира этиленгликоля Монометиловьтй эфир этиленгликоля. . . Диэтиловый эфир этиленгликоля. Сосновое масло Окись мезитила Фурфурол. . . Бёнзальдегид. Моноэтиловый [c.221]
Бутиленгликоль см. Монобутиловый эфир этиленгликоля. ....... С4Н10О2 Жид- кость Г орючий Б [c.229]
Более неблагоприятным является количественное извлечение и фотометрическое определение кальция в виде ЯЫНз(СаОхз) [17]. Однако этот метод вполне сравним с экстракцией магния по Льюку [10] и превосходит, с другой стороны, предложенный Янковским и Фрейзером [8], вероятно, по аналогии с методом Льюка, способ извлечения СаОхг в присутствии монобутилового эфира этиленгликоля. [c.131]
chem21.info
Диэтиленгликоль эфир ди и монобутиловые
Монобутиловый эфир диэтиленгликоля [c.331]Эфир монобутиловый диэтиленгликоля [c.773]
Эфир уксусной кислоты и 1-оксиаценафтена вводят по каплям в вертикально установленную колонку из нержавеющей стали, нагретую до 520° и наполненную шариками диаметром 3 мм, состоящими из окиси алюминия 90%) и борнокислой меди (10%) в системе поддерживают остаточное давление, равное 2 мм. Продукты реакции собирают в приемнике, охлаждаемом водой. Выходящие из приемника газы пропускают через промывную склянку, содержащую какой-либо растворитель, например, монобутиловый эфир диэтиленгликоля, для растворения сублимированных частиц. Из [c.189]
ООО О - - эфиры этиленгликоля или диэтиленгликоля простые монометиловые 2909 43 ООО О - - эфиры этиленгликоля или диэтиленгликоля простые монобутиловые 2909 44 ООО О - - эфиры этиленгликоля или диэтиленгликоля простые моноалкиловые, прочие 2909 49 - - прочие [c.169]Бутоксиэтокси)-этанол см. Монобутиловый эфир диэтиленгликоля [c.109]
Диэтиленгликоля монобутиловый эфир см. Монобутиловый эфир диэтиленгликоля [c.211]
ДИЭТИЛЕНГЛИКОЛЯ МОНОБУТИЛОВЫЙ ЭФИР [c.194]
Бутилдигликоль 2-(2-Бутоксиэтокси)-этанол Диэтиленгликоля монобутиловый эфир [c.331]
Монобутиловый эфир 230,8 диэтиленгликоля [c.569]
С8Н,80з Монобутиловый эфир диэтиленгликоля 230,4 196,2 72,5 [c.520]
С8Н, Оз Монобутиловый эфир диэтиленгликоля 231,2 [c.587]
Диоксибензойная кислота Трихлор-трет-бутиловый спирт Монобутиловый эфир диэтиленгликоля [c.515]
Эфир метиловый этиленгликоль-ацетата Эфир миристиновометиловый Эфир миристиновометиловый Эфир монобутиловый диэтиленгликоля [c.773]
ЭФИР МОНОБУТИЛОВЫЙ ДИЭТИЛЕНГЛИКОЛЯ ЭФИР МОНОМЕТИЛОВЫЙ ДИЭТИЛЕНГЛИКОЛЯ ЭФИР МОНОУКСУСНЫЙ ЭТИЛЕНГЛИКОЛЯ ЭФИР МОНОХЛОРДИМЕТИЛО-ВЫЙ [c.194]
Этиловый эфнр 2-метил-пентен 3-овой-5 к-ты Метиловый эфир гндрак-риловой к-ты Метиловый эфир Р, 3-ди-метилакриловой к-ты Монобутиловый эфир диэтиленгликоля бутил-карбнтол) [c.835]
В качестве противообледенительных присадок первого типа, действующих посредством образования с водой низкозамерзающих смесей, известны соединения из класса спиртов, гликолей, формамидов и их производных. Эти присадки действуют в довольно большой концентрации— до 0,5 и даже до 2% например монобутиловый эфир диэтиленгликоля добавляют к бензину в концентрации 0,05—0,5%. Эффективной противообледенительной присадкой этого типа является диметилформамид применяют также гексилен- и дипропиленгликоли, диметил-карбинол, 2-метилпентадиол-2,4-диметилформамид, мо-ноолеат глицерина и др. [8, 9, И, 12]. [c.207]
h28O3 2-(2-Бутоксиэтокси)этанол (монобутиловый эфир диэтиленгликоля) [c.640]
Монобутиловый эфир диэтиленгликоля sHig b. См. 2-(2-Бутоксиэтокси)-этанол [c.821]
МОНОБУТИЛОВЫИ ЭФИР ЭТИЛЕНГЛИКОЛЯ— МОНОБУТИЛОВЫЙ ЭФИР ДИЭТИЛЕНГЛИКОЛЯ СеН О -СвН зОз [c.205]
В качестве антиобледенительных присадок первого типа применяют различные спдрты, гликоли, фррмамиды и их производные. Присадки добавляют в количестве до 0,5—2%, [23, 1]. Например, монобутиловый эфир диэтиленгликоля добавляют к бензину в концентрации 0,05—0,5% вес. [50]. [c.324]
Монобутиловый эфир диэтиленгликоля (товарное название Бутилкарбитол ) представляет собой жидкость со слабым запахом, кипящую при 222°. Эфир растворяет нитроцеллюлозу и различные смолы, но не a цeтилцeлJ юлoзy. Это соединение смешивается с водой и углеводородами. [c.573]
Для стабилизации комплексного соединения молибдена с роданидом рекомендуют вводить в раствор некоторые водорастворимые органические жидкости, как, например, гликолевый эфир, бутилкарбитол (моно-бутиловый эфир диэтиленгликоля) и бутилцеллозольв (монобутиловый эфир этиленгликоля). В присутствии этих жидкостей интенсивность окраски роданида молибдена нарастает в продолжение 10 мин и затем остается постоянной 24 ч. Способ применяют главным образом в массо- вых анализах стали, так как он исключает необходимость экстрагирования, но в этом-случае следует устранять влияние хрома, который дает окрашенныр ионы, и меди,, которая образует нерастворимые соединения с роданидом. [c.369]
Бутокси)этокси]этанол (бутилкарбитол монобутиловый эфир диэтиленгликоля) 112-34-5 С8Н)80з 10 а, 4 1,3 [c.109]
Для выделения метанола из реакционной смеси восстановление удобнее всего проводить в высококипящем эфире, а разлагать комплекс — высшими спиртами. При проведении этой реакции в диэтилкарбитоле с последующим разложением комплекса бутилкарбитолом (монобутиловым эфиром диэтиленгликоля) образуется метанол с выходом 81% [2160]. [c.204]
Повышение электропроводности наблюдается при введении в состав эпоксидных клеев, содержащих мелкодисперсное серебро, 2,5% (масс.) монобутилового эфира диэтиленгликоля или моноэтилового эфира диэтиленгликольацетата. Такие добавки позволяют снизить электрическое сопротивление клеев в [c.111]
Карбитол (монобутиловый эфир диэтиленгликоля). Бесцветная жидкость промышленного производства. [c.39]
chem21.info
Простые эфиры этиленгликоля - Отравления промышленными ядами - Неотложная помощь при острых отравлениях - Библиотека доктора - Медкурсор
16 апреля 2009
Метилцеллосольв (метилгликоль, монометиловый эфир этиленгликоля)
СН3–О–СН2СН2ОН
Жидкость, температура кипения 124,6° С. Ядовитое вещество, оказывает очень сильное угнетающее действие на центральную нервную систему, обладает высокой поражающей активностью в отношении печени и почек, вызывает гемолиз. Пары метилцеллосольва раздражают слизистые оболочки глаз и верхних дыхательных путей. Смертельная доза при поступлении внутрь 10 г.
Метилгликольацетат (метнлцеллосольвацетат) СН3ОСН2СН2ОСОСН3
Наркотик с заметным раздражающим действием на слизистые оболочки. Достаточно сильно поражает печень и почки. Вызывает гематурию. Смертельная доза 10 г.
Этилгликольацетат (целлосольвацетат)
С2Н5ОСН2СН2ОСОСН3
По действию сходен с метилцеллосольвацетатом.
Этилцеллосольв (моноэтиловый эфир этиленгликоля)С2Н5–О–СН2СН2ОН
Жидкость, температура кипения 134,8° С. Пары этилцеллосольва оказывают слабое раздражающее действие, обладают заметным наркотическим свойством. Сильно повреждают печень и почки, вызывают гематурию. Смертельная доза 10 г.
Монобутиловый эфир этиленгликоля (бутилцеллосольв) С4Н9–О–СН2СН2ОН
Жидкость, температура кипения 170° С. Оказывает заметное раздражающее и наркотическое действие, сильно повреждает печень и почки, вызывает гематурию. Смертельная доза при попадании внутрь 10 г.
Карбитол (этилдигликолевый эфир)
C2H5–О–(СН2)2–О–(СН2)ОН
Бесцветная гигроскопическая жидкость. Применяется в качестве растворителя. Оказывает нерезко выраженное раздражающее действие, способен поражать печень и почки. Смертельная доза 30 г.
β-Нафтол Твердое вещество, температура плавления 122–123° С. Применяется в производстве органических красителей. Ядовитое вещество. В парообразном состоянии оказывает сильное раздражающее действие на слизистые оболочки глаз и органов дыхания. Довольно сильно угнетает центральную нервную систему и повреждает печень и почки, вызывает гемолиз. У отравленных отмечаются желтуха, гемоглобинурия, анемия, судороги, кома. Отравления возможны, при вдыхании паров и пыли, а также при всасывании нафтола с кожи. Примерная смертельная доза 5 г.
При отравлении гликолями в результате их приема внутрь необходимо срочно промыть желудок через зонд и дать солевое слабительное. В дальнейшем назначают поддерживающую и симптоматическую терапию. В случае необходимости проводят искусственное дыхание, применяют кислород. По показаниям используют сердечно-сосудистые препараты и др. При отравлении (3-нафтолом могут потребоваться специальные мероприятия по борьбе с недостаточностью печени.
«Неотложная помощь при острых отравлениях», С.Н.Голиков
Читайте далее:Азобензол Кристаллическое вещество красного цвета, температура кипения 293° С, температура плавления 68° С. В воде не растворяется, растворяется в органических растворителях. Ядовит: смертельная доза для человека при поступлении внутрь 1 г. Проникая в организм, вызывает острую дистрофию печени и почек. Акридин (дибензопиридин) Бесцветные кристаллы со своеобразным запахом, температура кипения 346° С, температура плавления 111° С….
Трихлорбензол (существуют три изомера) С6Н3Cl3 Жидкость, температура кипения 208,5–219° С. По характеру действия на организм напоминает дихлорбензол. Пары оказывают заметное раздражающее действие на слизистые оболочки глаз и органов дыхания. Примерная смертельная доза при поступлении внутрь 25 г. Трихлорпропан (трихлоргидрин) ClСН2СНClСН2Cl Жидкость. По действию на организм похож на хлороформ: вызывает наркотическое состояние. Довольно сильно угнетает дыхание….
Ацетальдегид (уксусный альдегид, этаналь) Высоколетучая жидкость, температура кипения 20,2° С. Паральдегид (СН3СНО)3 Жидкость с острым вкусом и запахом, хорошо растворяется в воде, температура кипения 124° С. Метальдегид (СН3СНО)4 Твердое вещество. Под действием кислот происходит быстрое разложение паральдегида и медленное – метальдегида с выделением ацетальдегида. Паральдегид медленно разлагается с образованием ацетальдегида и уксусной кислоты в присутствии…
Бесцветная маслянистая легколетучая жидкость с ароматическим запахом, температура кипения 200° С, температура плавления 130,2° С. Пары ТЭС в 11,2 раза тяжелее воздуха. Нерастворим в воде, но хорошо растворяется в органических растворителях и животных жирах. ТЭС в качестве антидетонатора входит в состав этиловой жидкости, которая применяется для этилирования бензина. ТЭС – опасный нервно-сосудистый яд. Он легко…
NO, NO2, N2O4Окись азота (NO) – нестойкое соединение и уже через 30 c после выделения в атмосферу практически полностью переходит в двуокись (NO2). Четырехокись азота (N2O4) представляет собой бесцветную жидкость с температурой кипения +21,2°С. При нагревании разлагается с образованием двуокиси. Последняя в концентрации 0,2–0,3 мг/л опасна для жизни, а в концентрации 0,4–0,5 мг/л вызывает быструю…
www.medkursor.ru
Моноэтиловый эфир этиленгликоля - Справочник химика 21
Состав этилкарбитола следующий, % карбитол — 55,0 этилен-гликоль — 44,5 моноэтиловый эфир этиленгликоля — 0,04 диэти-ленгликоль — 0,11 вода — 0,35. Этилкарбитол — прозрачная, бесцветная или слегка темноватая жидкость, малолетучая. Поэтому пары его в зоне дыхания не могут создать опасной для человека концентрации. [c.134]Используя этилен, напишите схему получения моноэтилового эфира этиленгликоля (этилцеллозольва). [c.31]
Из простых эфиров этиленгликоля большое техническое применение нашли моноэтиловый эфир этиленгликоля, известный под названием целло-зольв , метиловый эфир этиленгликоля или метилцеллозольв и бутиловый эфир этиленгликоля или бутилцеллозольв . [c.271]Поточная схема получения моноэтилового эфира этиленгликоля приведена па рис. 9. [c.157]
Одной из наиболее эффективных присадок оказался этилцеллозольв — моноэтиловый эфир этиленгликоля (ГОСТ 8313—60), физико-химические свойства которого приведены ниже [c.337]
Моноэтиловый эфир этиленгликоля..... [c.246]
Этилгликоль см. Моноэтиловый эфир этиленгликоля [c.555]
Этиленгликоля моноэтиловый эфир см. Моноэтиловый эфир этиленгликоля [c.556]
Моноэтиловый эфир этиленгликоля 135 [c.343]
В — метанол Г — этиленгликоль Д — моноэтиловый эфир этиленгликоля Е — уксусная кислота. [c.197]
Моноэтиловый эфир этиленгликоля , 3635 3 605 30 [c.204]
Этоксиэтанол (моноэтиловый эфир этиленгликоля, этилцеллозольв) С2Н5ОСН2СН2ОН [c.425]
Моноэтиловый эфир этиленгликоля см. Этилцелло-зольв. [c.171]
Имеются рекомендации по применению экстракционной депарафинизации для обезмасливания гачей и петролатумов. Так, в патенте одной американской фирмы [58] предлагается обезмасливать гачи путем их обработки нитробензолом с добавкой ацетона и моноэтилового эфира этиленгликоля. По опубликованным данным, нри такой обработке гача (температура плавления 45° и содержание масла 24,2%) был получен парафин с температурой плавления 53,5° и содержанием масла 0,3%. Имеется предложение [59] по обезмасливанию гачей в мелкогранулированном состоянии путем экстракционной обработки дихлорэтаном. На одном из отечественных заводов С. И. Степуро и Н. А. Тарасовым успешно осуществлено в опытных масштабах обезмасливание остаточного петролатума в твердом распыленном состоянии экстрагированием его дихлорэтан-бензоловой смесью. [c.154]
Примечание. Вместо безводного метанола Р при изготовлении реактива можно применять моноэтиловый эфир этиленгликоля Р. [c.237]
Монометиловый эфир этиленгликоля Моноэтиловый эфир этиленгликоля Монобутиловый эфир этиленгликоля [c.112]
Моноэтиловый эфир этиленгликоля. .... [c.160]
Гидрирование окиси этилена над никелем, осажденным на окиси бария > дает с удовлетворительным выходом этиловый спирт при значительном избытке водорода, повышенном давлении и температуре не выше 80 °С. При 130—150 °С и избытке окиси этилена преимущественно образуется моноэтиловый эфир этиленгликоля. [c.79]
Как правило, перхлораты полностью растворимы в воде и во многих органических растворителях. Чени и Манн определили примерные растворимости (табл. 21) ряда перхлоратов в фурфуроле, целлозольве (моноэтиловом эфире этиленгликоля) ив воде. [c.51]
Собственно целолольфом называется моноэтиловый эфир этиленгликоля. Другие представители ряда целозольфов называются в соответствии с названием спирта, образующего эфир с этиленгликолем, например, метил-пропил-, бутилцелозольф. [c.192]
Физико-химические методы предотвращения образования кристаллов льда в топливе и обмерзания топливных фильтров основаны на устранении обратимой гигроскопичности нефтяных топлив и перевода их в гигроскопичность необратимую. Практически это достигается путем введения в топливо различных присадок, растворяющихся в топливе и обладающих высокой необратимой гигроскопичностью. Такими присадками могут быть Некоторые спирты, эфиры и другие соединения. Наиболее эффективным из них оказался этилцеллозольв — моноэтиловый эфир этиленгликоля, предложенный Б. А. Энглиным. [c.51]
Этилцеллозольв СН20НСН2(ОС2Нд) — это моноэтиловый эфир этиленгликоля, бесцветная прозрачная жидкость, имеющая плотность 0.,930—0,935 г см и показатель преломления 1,4070—1,4090. Исследования показали, что в концентрации до 0,3% этилцеллозольв не оказывает влияния на физико-химические и эксплуатационные свойства топлив. В связи с тем, что этилцеллозольв может извлекаться из топлив водой, вводить его в топлива следует непосредственно перед их применением. В зарубежной практике для предотвращения образования кристаллов льда в топливах применяется метилцеллозольв [8]. [c.317]
При применении авиационных топлив в зимнее время, а также при длительных полетах самолетов на больших высотах в топливо добавляют моноэтиловый эфир этиленгликоля (жидкость И ) и тетрагидрофуриловый спирт с целью предотвращения образования кристаллов льда при охлаждении. Топливо смешивают с присадками на аэродромны) складах в одну или две стадии. Количество присадки (м ) для добавления в топлию определяют по формуле [c.139]
Со спиртами и фенолами окись этилена образует моноалкплэфиры соответствующих гликолей. Так, нанример, при нагревании окпси этилена с этиловым спиртом образуется моноэтиловый эфир этиленгликоля [c.288]
Присадки позволяют повысить растворимость воды в нефтепродуктах за счет образования гомогенной тройной системы нефтепродукт—присадка—вода. В результате вода не выпадает из нефтепродуктов при низких температурах. Этим достигается необходимый положительный эффект, поскольку с эксплуатационной точки зрения опасна не растворенная, а выпадающая из топлив и масел вода. Присадки, предотвращающие выделение воды при низких температурах, применаются в настоящее время к авиационным топливам. В качестве таких присадок исследована большая группа соединений. Эффективными и пригодными для промышленного применения оказались моноэтиловый эфир этиленгликоля (этил-целлозольв, жидкость И ), монометиловый эфир этиленгликоля (метилцеллозольв) и тетрагидрофурфуриловый спирт. Добавление 0,1—0,3 % этилцеллозольва предотвращает выделение воды нз топлив при низких температурах. В присутствии присадки и при уреличении ее концентрации с 0,1 до 0,3 % скорость растворения кристаллов льда в топливе значительно увеличивается (табл. 63). С понижением температуры скорость растворения кристаллов льда уменьшается. В присутствии этилцеллозольва температура образования кристаллов значительно понижается. В топливах с 0,3 % этилцеллозольва и максимальным содержанием воды 0,013 % образования кристаллов льда не происходит даже при —60 °С. Без этилцеллозольва образование кристаллов льда в топливе наблюдается уже при содержании воды 0,003 %. [c.150]
Винилэтиловый эфир этиленгликоля — легкоподвижная, бесцветная, прозрачная, Летучая жидкость с своеобразным эфирным запахом. Смешивается во всех отношениях с обычвыми органическими растворителями. Плохо растворим в воде. Энергично реагирует с бромом. Обесцвечивает раствор перманганата. Гидролизуется слабым водным раствором серной кислоты с образованием ацетальдегида и моноэтилового эфира этиленгликоля. Под влиянием хлорного железа превращается в маслообразный, нерастворимый в воде светлый полимер. С концентрированной серной кислотой реагирует со взрывом. С металлическим натрием, едкими щелочами и углекислыми солями щелочных металлов не реагирует. При хранении устойчив. Т. Кип. 123,7—123°,9 при 755 мм 0,8760, 1,4125 [7]. [c.52]
Б. 2-Бром-З-метилбензойная кислота. Внимание Этот синтез следует проводить в хорошо действующем вытяжном шкафу, так как при синтезе выделяется ядовитый газ — цианистый водород. В 5-литровую круглодонную колбу помещают90г цианистого калия, 900 мл моноэтилового эфира этиленгликоля (примечание 3), 850 мл воды и полученный выше 2-бром-4-нит-ротолуол во влажном состоянии, К колбе присоединяют обратный холодильник и смесь кипятят в течение 16 час. (примечание 4). Затем к горячему раствору темно-красного цвета прибавляют 1,5 л воды и смесь подкисляют концентрированной соляной кислотой. (Внимание При этом происходит выделение цианистого водорода.) Для удаления цианистого водорода подкисленную смесь кипятят в течение 15 мин., а затем охлаждают до 35—40°. Прибавляют 5 г диатомита, смесь перемешивают и фильтруют через воронку Бюхнера, дно которой предварительно покрывают небольшим слоем диатомита. Осадок отбрасывают, а фильтрат экстрагируют трем I порциями хлороформа по 200 мл. Хлороформные вытяжки сг диняют вместе и экстрагируют тремя порциями 5%-ного растьора углекислого аммония по 100 мл. Щелочные вытяжки соединяют, подкисляют концентрированной соляной кислотой и охлаждают в бане со льдом. Выделившееся вначале маслянистое вещество вскоре закристаллизовывается. [c.15]
Амид 9-антраценкарбоновой-О кислоты. Смесь 18,8 г нитрила 9-антраценкарбоновой кислоты, 17 г едкого кали, 10 мл воды и 75 мл моноэтилового эфира этиленгликоля кипятят с обратным холодильником в течёние 2,5 час., после чего разбавляют водой и отделяют выпавший амид. Выход 20,5 г, т. пл. 212—215°. Полученный амид очищают перекристаллизацией из спирта, т. пл. 215—216°. [c.68]
Н0С2Н40Н, где Н — низшая алкильная группа [451]. Однако, как утверждалось, золи, получаемые в простом моноэтиловом эфире этиленгликоля, из которых вода удалялась в вакууме при невысокой температуре, не содержали этерифицированного кремнезема [452]. Если это так, то устойчивость золя должна быть следствием стерической стабилизации , вызванной образованием водородных связей между силанольными группами поверхности кремнезема и атомами кислорода эфирных и гидроксильных групп органического вещества. В более раннем патенте описано, что такой тип золя подвергался нагреванию с целью его стабилизации, причем подобное воздействие, вероятно, оказывала этерификация [453]. [c.570]
Моноэтиловый эфир этиленгликоля, моноэтиловый эфир гликоля, 2-этоксиэтанол, целлосольв [c.17]
Ароматические альдегидокнслоты, например опиановая кислота, и сложные альдегиды, например гидрастинин, также дают реакцию Канниццаро. Алифатические альдегиды при действии щелочей в большинстве случаев осмоляются, но под влиянием алкоголятов алю.миния, например алюмината моноэтилового эфира этиленгликоля они прев-ращантгся в сложные эфиры, которые после омыления дают кислоту и спирт, молекулы которых содержат то же число атомов углерода, что и исходный альдегид (реакция Тищенко) [c.383]
Образовавшийся моноэтиловый эфир этиленгликоля реагирует со следующей молекулой окиси этилена с образованием моноэти-лового эфира диэтиленгликоля [c.155]
Моноэтиловый эфир этиленгликоля СН3—О—СН2—СНдОН прекрасно растворяет ацетилцеллюлозу, нитроцеллюлозу, смолы. Наибольшее. зиачение как растворитель имеет моноэтиловый эфир этиленгликоля, называемый целлозольв С2Н5ОСН2—СН2ОН. Он применяется не только как чистый растворитель, но и как добавка к другим растворителям. Прекрасными растворяющими способностями обладает также и карбитол, этиловый эфир диэтиленгликоля. [c.158]
Для обнаружения кобальта (и некоторых других элементов) в частицах весом Ю- о—10- г, находящихся в атмосферном воздухе [1297], наносят на предметное стекло желатино-глицериновые пленки, импрегнированные растворами рубеановодородной кислоты и ацетата аммония в моноэтиловом эфире этиленгликоля. Окрашенные зоны рассматривают под микроскопом в отраженном свете. [c.51]
chem21.info
Процессы получения простых эфиров
10
Простые эфиры являются производными спиртов, диолов, фенолов и т.п., у которых атом водорода гидроксильной группы замещен углеводородным остатком. Рассмотрим способы получения диалкиловых (симметричных и несимметричных), циклических, алкилариловых эфиров - продуктов основного органического синтеза:
Наиболее распространенные представители простых эфироов:
1. Диалкиловые эфиры:
Симметричные эфиры:
- диметиловый эфир (метоксиметан) tкип = -23,7С
- диэтиловый эфир (серный эфир) tкип = 34,6С
- диизопропиловый эфир tкип = 67,5С
Несимметричные эфиры:
- метил-третбутиловый эфир tкип = 53-56С
азеотроп с МеОН tкип = ???С
- метил-третамиловый эфир tкип =
ди-, три-, тетра- и полиэтиленгликоли:
- диэтиленгликоль tкип = 245С
- триэтиленгликоль tкип = 284С
- тетраэтиленгликоль tкип = 313-314С
- полиэтиленгликоль (ПЭГ-13)
- полиэтиленгликоль (ПЭГ-35)
- полиэтиленгликоль (ПЭГ-115)
и их моноалкиловые эфиры:
моноалкиловые эфиры этиленгликоля, пропиленгликоля - целлозольвы:
- монометиловый эфир этиленгликоля
(метоксиэтанол, метилцеллозольв) tкип = 124,3С
- моноэтиловый эфир этиленгликоля
(этоксиэтанол, этилцеллозольв) tкип = 135,1С
- монобутиловый эфир этиленгликоля
(бутоксиэтанол, бутилцеллозольв) tкип = 171С
- монометиловый эфир пропиленгликоля
моноалкиловые эфиры диэтиленгликоля- карбитолы:
- монометиловый эфир диэтиленгликоля (метилкарбитол) tкип = 194С
- моноэтиловый эфир диэтиленгликоля (этилкарбитол) tкип = 201-202С
- монобутиловый эфир диэтиленгликоля (бутилкарбитол) tкип =
моноалкиловые эфиры полиэтиленгликолей, у которых число
оксиэтильных звеньев n = 3-20 и алкильный радикал R = C10-C20
- синтанолы (ДС-3, ДС-6, ДС-10, ДС-20 - R = C10-C18)
- и диалкиловые эфиры:
- диметиловый эфир этиленгликоля (глим) tкип = 84,5С
- диметиловый эфир диэтиленгликоля (диглим) tкип = 61-62С
(11 мм рт ст)
2. Циклические эфиры:
эпоксиды:
- этиленоксид tкип = 10С
- пропиленоксид tкип = 36С
- глицидол tкип =56C (11 мм рт ст)
- оксид стирола tкип =
- оксиды олефинов С10-С16 tкип =
тетрагидрофуран (аз. tкип = 64С, 6% Н2О, ) tкип = 65,7С
1,3-диоксолан -ОСН2СН2ОСН2 tкип = 75С
2-метил-1,3-диоксолан -ОСН2СН2ОСН-СН3 tкип = 82,5С
1,3-диоксан -ОСН2СН2СН2ОСН2 - tкип = 105С
4,4-диметил-1,3-диоксан (СН3)2-С-СН2СН2ОСН2О- tкип =
1,4-диоксан (аз. tкип = 87,8, 18,4% Н2О, ) tкип = 101,3С
3. Алкилариловые эфиры
- метилфениловый эфир (анизол) (н.р.) tкип = 155С
азеотроп с Н2О tкип = 95,5С
- монофениловый эфир этиленгликоля (феноксиэтанол) tкип = 236-238С
- моноалкилфениловые эфиры полиэтиленгликолей
(неонолы АФ9 3-12)
В основе промышленных способов получения простых эфиров лежат следующие химические превращения:
1. Межмолекулярная и внутримолекулярная дегидратация спиртов и диолов.
Данный процесс используется главным образом для получения симметричных диалкиловых эфиров, циклических эфиров (ТГФ, 1,4-диоксан) и алкилариловых эфиров (анизол). В некоторых случаях данный процесс может быть использован для синтеза несимметричных эфиров:
| 1 | 2ROH ROR + h3O | |
| 2 | ROH + ROH ROR + h3O | Слабоэкзотермические |
| 3 | HOCh3Ch3Ch3Ch3OH ТГФ + h3 | реакции |
| 4 | HOCh3Ch3OCh3Ch3OH диоксан + h3O | -H20 kДж/моль |
| 5 | СН3ОН + С6Н5ОН СН3ОС6Н + Н2О |
Все эти реакции относятся к числу кислотно-каталитических процессов. В качестве катализаторов используют:
гетерогенные контакты:
- AL2O3
- Н3РО4/на носителе (AL2O3, силикагель и др)
- цеолиты
- фосфаты кальция (CaHPO4)
- сульфокатиониты:
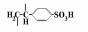
гомогенные катализаторы:
-серная кислота.
Основные побочные реакции:
а). Реакция внутримолекулярной дегидратации с образованием олефина с последующей его кислотной полимеризацией:
Ch4Ch3Ch3Ch3OH Ch4Ch3CH=Ch3 + h3O (энд) H 40-48 kДж/моль
n Ch4Ch3CH=CH (Ch3Ch3CH-CH)n
б). Реакция дегидрирования спирта с образованием альдегида или кетона:
Ch4Ch3Ch3Ch3OH Ch4Ch3Ch3COH + h3
Данная реакция протекает в присутствии гетерогенных контактов, содержащих металлы.
в). Реакция изомеризации циклических эфиров
| Ch3Ch3 H+ Ch3O Ch3OH O O | CHCh4 | + Ch4COH Ch3Ch3 Ch3O Ch3OH |
г). При получении анизола реакции межмолекулярной дегидратации метанола с образованием диметилового эфира, фенола с образованием дифенилового эфира, а также продукты реакции алкилирования фенола и анизола в ароматическое ядро с образованием крезолов и т.п.
Все целевые реакции и основная побочная являются равновесными (обратимыми) при этом Кр целевых реакций с увеличением температуры падает, а Кр основной побочной реакции растет. В газовой фазе при 200-400С основная и побочная конкурируют друг с другом. В связи с этим для повышения степени превращения спиртов в целевые продукты необходимо проводить процесс при умеренных температурах.
Для селективного получения циклических эфиров (тетрагидрофуран, диоксан и др.), также диалкиловых эфиров (кроме диметилового и диэтилового) процесс обычно проводят в жидкой фазе при температуре 80-200С при обычном или небольшом давлении.
Учитывая тот факт, что, как правило, образующиеся продукты более летучи, чем спирты, для повышения выхода процесса в жидкой фазе также используют прием удаления продуктов из зоны реакции, снижая текущую концентрация целевого продукта в реакционной смеси и тем самым снижая скорость его (целевого эфира) превращения по реакции изомеризации (в).
В связи с низкой реакционной способностью метанола и этанола при получении диметилового и диэтилового эфиров процесс следует осуществлять в газовой фазе при температуре 200-250С в присутствии гетерогенного катализатора - фосфорная кислота на носителе (Al2O3).
Аналогично, для увеличения селективности образования анизола и исключения образования продуктов алкилирования в ароматическое ядро процесс осуществляют в газовой фазе в присутствии цеолитов при 300-320С и при соотношении фенол : метанол 1 : 2.
При проведении процесса в газовой фазе для повышения селективности образования целевого эфира используют принцип Лешателье. Для смещения равновесия побочной реакции внутримолекулярной дегидратации влево процесс осуществляют при повышенном давлении 1-2 МПа. При этом поскольку тепловой эффект невелик процесс можно проводить в адиабатических условиях.
Для повышения селективности образования анизола процесс осуществляют в избытке метанола в присутствии селективных катализаторов - цеолитов, при этом образующийся по реакции диметиловый эфир возвращают в реакцию (циркулируют на вход реактора).
Аппаратурное оформление процесса:
1. Агрегатное состояние реагентов и катализатора-
Ж-Ж- (Ж)kt-гомогенный
Ж-Ж- (Т)kt-гетерогенный
Г - Г - (Т)kt-гетерогенный
2. Непрерывные и периодические реактора
3. Реактора смешения и вытеснения
4. Движется одна фаза (жидкость или газ)
5. Адиабатический, изотермический или политропический
6. Все виды подвода и отвода тепла реакции
7. Внешнее и внутреннее
8. Выбор оптимального зерна гетерогенного катализатора
9. Реакционная камера, колонны, реже - теплообменник
См. Рис.I – IV
studfiles.net
Моно бутиловый эфир - Справочник химика 21
Метилизобутилкетон Моно-бутиловый эфир этиленгликоля (бутилцеллозольв) [c.421]Амидофосфорные кислоты. Помимо самого амида фосфорной кислоты, соединения этого типа мало изучены. Очевидно, они менее устойчивы в кислой среде, чем моноэфиры, и лучше всего могут быть получены гидрированием дибензилового эфира и замещенных дибензиловых эфиров над палладием [142, 217, 321] или дифенилового эфира над платиной [142, 152]. От амидодифенилфос-фата при щелочном гидролизе в жестких условиях отщепляются оба фенильных остатка [281, 3211. Некоторые N-ариламиды фосфорной кислоты были получены нагреванием ариламмониевых солей N-ариламидов моно-тре/п-бутилового эфира фосфорной кислоты,, которые образуются непосредственно при реакции ариламина с ди-/прв/п-бутилхлорфосфатом [154]. Кроме того, амиды фосфорной кислоты можно получать фосфорилированием аминов хлорокисью фосфора в водном растворе щелочи или гидролизом амино-дигалогено( сфатов [210, 313]. [c.127]
Бутоксиэтокси)-этокси]-этанол см. Моно бутиловый эфир триэтиленгликоля [c.109]Окись пропилена, окись этилена, моно-бутиловый эфир этиленгликоля Полимер КОН жидкая фаза, 4,2 бар, [c.83]
В качестве флотореагентов-пенообразователей можно применять вещества, способные к адсорбции на границе раздела вода — воздух и умеренно стабилизирующие пену. Для этих целей используют продукты, содержащие терпеновые спирты, одноатомные алифатические спирты с шестью — восьмью атомами углерода, крезолы и ксиленолы, монометиловые и моно-бутиловые эфиры полипропиленгликолей и др. Для регулирования щелочности воды применяют такие реагенты, как известь, соду, серную и соляную кислоты [33]. [c.166]
Патент РФ № 2159224. Бахтина И.А., Комарова Л.Ф., Полякова Л.В. и др. Способ выделения бутиловых эфиров моно- и диэтиленгликолей из продуктов оксиэтилирования бутилового спирта. Заявл. 02.02.99. Опубл. 23.05. 2000. [c.40]
Фуриловый. ........ Моно-н-бутиловый эфир эти- 170 129 i 45 80 [c.222]
Уксусный эфир моно-н-бутилового эфира диэтиленгликоля Изобутиловый фенилуксусной 246 247 0,9871 20/20 0,999 18/4 [c.245]
Моно-н-бутиловый эфир диэтилен гликоля. ......... [c.276]
Для стабилизации комплексного соединения молибдена с роданидом рекомендуют вводить в раствор некоторые водорастворимые органические жидкости, как, например, гликолевый эфир, бутилкарбитол (моно-бутиловый эфир диэтиленгликоля) и бутилцеллозольв (монобутиловый эфир этиленгликоля). В присутствии этих жидкостей интенсивность окраски роданида молибдена нарастает в продолжение 10 мин и затем остается постоянной 24 ч. Способ применяют главным образом в массо- вых анализах стали, так как он исключает необходимость экстрагирования, но в этом-случае следует устранять влияние хрома, который дает окрашенныр ионы, и меди,, которая образует нерастворимые соединения с роданидом. [c.369]
Так, например, при экстракции диэтиловым эфиром в качестве высаливающего агента применяются нитраты кальция или магния успещно используется нитрат алюминия при экстракции такими растворителями, как метил-изо-бутилкетон (гексон), моно-бутиловый эфир этиленгликоля (целлосольв), ди-изо-пропило-вый эфир (ДИПЭ) [1]. [c.129]
Из высококипящих растворителей используют метиламилацетат, моно-бутиловый эфир этиленгликоля и ацетат моноэтилового эфира этиленгликоля. Амилацетат, широко применявшийся раньше в лакокрасочных композициях, слу/кит в настоящее время для экстракции пенициллина. Важнейшими вспомогательными растворителями для нитролаков, наносимых краскопультами, являются этиловый, изопропиловы11 и / -бутиловый спирты. Кроме них, применяют еще метплизобутилкарбинол. Большие количества этилового и изопропилового спирта расходуют при транспортировке нитроцеллюлозы, которую для безопасности смешивают с 30—35% вес. этих спиртов. Многочисленные возможности применения органических растворителей в основном кислородных производных в области нанесения красочных покрытий, в фармацевтической и косметической промышленности, в пищевой и нефтяной промышленности, в производстве текстильных вспомогательных продуктов, взрывчатых веществ, флотореагентов, в экстракционном деле и для многих других технических целей делают их одними из важнейших продуктов современной химической промышленности. [c.442]
Определение моно- -бутилового эфира эти-ленгликоля в реакционной смеси окиси этилена с м-бутанолом методом газо-жидкостной хроматографии. (НФ ДС-703 и смесь его с диметиловым эфиром тетраэтиленгли-коля.) [c.34]
В ледяной уксусной кислоте, содержащей 0,25 М раствор ацетата аммония, потенциалы полуволны для алифатических моно- и а,ш-динадкислот с длинной углеродной цепью практически одинаковы (в области от О до —0,1 в), однако диффузион ный ток для последних лишь в 1,6 раза больше, чем для мононадкислот [198, 199]. Исследование mpm-бутиловых эфиров надкислот, диацилперекисей и алкилгидроперекисей алифатических одноосновных кислот, содержащих пять или более атомов углерода (при этом в качестве фона использовали 0,3 М раствор Li l в смеси бензола с абсолютным метанолом 1 1), показывает, что потенциалы полуволны трет-бути-ловых эфиров надкислот (от —0,96 до —0,82 в относительно НКЭ) с увеличением длины цепи уменьшаются, а для диацилперекисей возрастающего молекулярного веса эти потенциалы остаются постоянными (от —0,08 до —0,12 в) [236]. Потенциал полуволны наиболее отрицателен для перекиси трет-бутила и уменьшается в ряду /прет-бутиловый эфир надкислоты > гидроперекись > диацилперекись > надкислота. [c.389]
Во многих патентах и других работах [16,68,69,81,82,87,89] предлагается использовать в качестве компонентов ангиобледенительных присадок к бензинам и водорастворяющих агентов, предотвращающих замерзание воды, метиловые, этиловые, изопропиловые и бутиловые эфиры моно-, ди-, и триэтиленгликоля (целлозольвы), эфиры дипропиленгликоли, ацетаты гликолевых эфиров, а также кетоны (ацетон, метилэтилкетон). Предлагается использовать и смеси этих эфиров с низшими спиртами и гликолями. Производство большин--ства предлагаемых сложных эфиров базируется на органических кислотах и спиртах различного строения с использованием реакции эте-рификации [30,90] [c.33]
Экстракция циркония ди-и-бутилфосфатом. Скадден и Баллов [717] показали, что из 1 N раствора азотной, соляной, серной и хлорной кислот, содержащего 2,5 М (N1 4)2564 и 0,04 М Н2С2О4, цирконий количественно экстрагируется за 15 мин. 0,06 М раствором ди-н-бутилфосфата (ДБФ) в ди-н-бутиловом эфире. Экстракция была подробно изучена Роль юм [696] и использована для отделения и определения микрограммовых количеств циркония в алюминиево-магниевых сплавах (см. стр. 156). Для экстракции циркония авторы применяли продажный препарат, содержащий 55% ДБФ и 45% моно-н-бутилфосфата, растворенный в хлороформе. Экстракцию циркония с ДБФ изучали при помощи 2г . Цирконий хорошо экстрагируется в присутствии фторидных ионов (фтор-борной кислоты). В отсутствие фторидных ионов цирконий экстрагируется неполностью, с неустойчивыми результатами, вероятно, вследствие гидролиза. Цирконий экстрагируется количественно из растворов в 1—10 М НЫОз. Начиная от pH 0,65 и выше, полнота экстракции циркония быстро уменьшается, при, pH 1,4 экстраги- [c.87]
Склонность к деацилированию у ацилзамещенных 0-, S-, дополнительных NHj, имидазольной и гуанидиновой групп намного выше, чем у сс-КНг-групп, причем ТФА-производные в этом отношении намного чувствительнее соответствующих ацетильных соединений. Эти свойства имеют решающее значение при выборе жидкой фазы и носителя для ГХ. Было показано, что в водной среде ди-ТФА-серин быстро превращается в moho (Ы)-ацильное производное [144]. При достаточно длительном воздействии N-ТФА-серин в конце концов снова превращается в нативную аминокислоту, что, как полагают, связано с N—>0 ацильной миграцией. Дй-ТФА-производные оксипролина, серина, треонина, тирозина и цистеина тоже быстро разлагаются до. N-ТФА-соединенип в метаноле, воде и даже в некоторых тщательно высушенных растворителях (бензол, хлористый этилен и н-амилтрифторацетат) [28, 84, 99]. При этом наиболее лабильны производные тирозина, а наиболее устойчивы -0-ТФА-группировка треонина и производное по индольному атому азота триптофана. Наблюдаемые в ГХ метанольных растворов метиловых эфиров ТФА-аминокислот большие времена удерживания для серина и тирозина согласуются с их разложением до свободных ОН -форм. Еще одним доказательством лабильности О- и S-ТФА-тирозина и цистеина служит их способность к ацилированию н-амилового эфира изолейцина. Треонин, серин и оксипролин в этом отношении были неактивны [28]. н-Бутиловый эфир ди-ТФА-гистидина оказалось целесообразным хроматографировать, полностью разлагая его бутано лом на газохроматографической колонке до моно-ТФА-произ-водного [43] (см. также разд. 2.7.3). [c.114]
Аналогичным действием обладает и B I3 — метанол, но он более стабилен, чем его фторированный аналог. BF3 — бутанол, который используют для быстрого получения бутиловых эфиров жирных кислот, особенно эффективен для синтеза производных низкомолекулярных кислот, так как бутиловые эфиры менее летучи, чем соответствующие метиловые эфиры. Последний реагент можно применять и для синтеза н-бугиловых эфиров гербицидных хлорфеноксиуксусных кислот. BF3 — н-буганол используют как для приготовления н-бутиловых эфиров насыщенных кислот с длинной цепочкой, так и для дериватизации короткоцепочечных ( i—Сю) моно- и ди-карбоновых кислот. Это важно, так как метиловые эфиры этих кислот очень летучи и их трудно количественно извлечь из такой реакционной среды, как вода [38]. [c.294]
По имеющимся данным, перекись трет-бутила является эффективным инициатором реакции диаллилового эфира с сероводородом, в результате чего образуется полимер [205], а использование этой перекиси вместе с железом весьма эффективно при реакции присоединения к 2,5-диметилгексадиену-2,4, которая приводит к моно-идитиолам [193]. Перекись бензоила применяли при присоединении к ди-н-бутиловому эфиру а-метил-а -метиленадипиновой кислоты [206]. Следы кислорода инициируют присоединение сероводорода к виниловым эфирам [196] и винилсульфидам [179], но большие количества кислорода (например, 0,05% в случае бутилвини-лового эфира) являются уже ингибиторами [196]. Из всех изученных инициаторов свободнорадикальных реакций, по-видимому, азонитрилы дают наиболее удовлетворительные результаты в реакциях присоединения сероводорода [190, 200]. [c.214]
При анализе эквимолярпого раствора аминокислот колебание значений отношений площадей пиков к соответствующим молярным концентрациям аминокислоты для моноацильного производного гистидина составляло 0,36—0,45. Метод определения гистидина в виде бутилового эфира моно-ТФАпроизводного не давал возможности точно определить для него значение коэффициента чувствительности. [c.71]
Уиллеме [696] предпринял широкое исследование синтеза пропансультона, получив шесть моноалкил-, четыре диалкил- и три триалкилпроизводных, а также одно арилалкилпроизводное были применены три различных варианта метода термической дегидратации. По первому из этих методов реакцию проводили без растворителя, по второму — использовали гидрофильный растворитель (моно-н-бутиловый эфир этиленгликоля), а по третьему — гидрофобный растворитель (ксилол). Выходы пропансультона по всем трем методам составляли 40—60%, но в случае некоторых его замещенных первые два метода не привели к получению желаемых продуктов. Третий метод дает хорошие результаты во всех случаях. [c.250]
Если дегидратацию проводить в присутствии моно-н-бутилового эфира этиленгликоля или ксилола [696], выход сультона повышается до 89%. Данный сультон был также получен перегонкой 4-хлорбутансульфокислоты [299]. В небольших количествах он производится промышленностью [11]. [c.260]
Явления, происхос]ящие при испарении растворителей. Поглощение из окружающей ат.мосферы энергии, необходимой для испарения растворителей, может вызвать конденсацию влаги на поверхности пленки и ее помутнение. Для предотвращения этого в лакокрасочный материал добавляют высококипящие водорастворимые растворители, например моно-н-бутиловый эфир этилен-гликоля. [c.26]
Получение. При реакции хлорметилового производной) дигидросафрола с натрнево ) солью моно-н-бутилового эфира диэтиленгликоля (патент США 2550737). [c.196]
Мочевино-формальдегидные смолы, модифицированные феноло-альдегидными смолами, и прочие модифицированные смолы. Известно, что формальдегид реагирует с фенолами по реакциям, аналогичным реакциям мочевины. В щелочной среде подвижный атом водорода принимает участие в образовании радикала —СН2ОН и получается моно- или диметилолфенол. Эти фенолоспирты в присутствии диметилолмочевины или ее бутилового эфира вступают в реакции внутримолекулярной конденсации, приводящие в конце концов к образованию комплексных смол. Твердость таких смол обусловливается участием мочевины, а водостойкость — участием фенолов. [c.339]
Г ераниол.......... Моно-к-бутиловый эфир диэти- 229 47 62 [c.223]
chem21.info