/ Наглядная химия. Фенолы и Простые эфиры (pdf). Метилфениловый эфир
Метилфениловый эфир - Большая Энциклопедия Нефти и Газа, статья, страница 1
Метилфениловый эфир
Cтраница 1
Метилфениловый эфир 173, 175 Метилфосфин 200, 201 Метилфосфиновая кислота 201 а - Метилфуран 207; см. Сильван Метилхолантрен 127, 129 Метилэтилкетон 229, 230, 234, 270 Метан 33 Метинон 409 Меченый азот 378 Меченый иод 398 Мечников И. [1]
Анизол ( метоксибензол, метилфениловый эфир) - бесцветная жидкость с характерным запахом; нерастворим в воде, легко растворяется в спирте, эфире, бензоле; легко перегоняется с водяным паром. [2]
Ан изол ( метоксибензол; метилфениловый эфир) С6Н5ОСНз; М 108 14; бц. [3]
ПКФ; 5 - 2 6-ди-грет - бутил-4 - метилфениловый эфир ПКФ; 7 - Ы - фенил - Ы - циклогексил-л-фени-лендиамин; S - М - изопропил - М - фениленди-амин; 9 - неозон Д; 10 - ДНФДА. [5]
Анейрин 401; см. Витамин В ] Анизол 175; см. Метилфениловый эфир. [6]
Обычно название образуется так, как показано на двух следующих примерах: димети-ловый эфир, метилфениловый эфир. [7]
В работе [63] на примере торможения окисления полипропилена показано, что из фосфитов наибольшей эффективностью обладают эфиры пирокатехинфосфористой кислоты, такие, как 2 6-ди-трет - бутил-4 - метилфениловый эфир пирокатехинфосфористой кислоты и фосфит а-нафтола и пирокатехина. Простые эфиры фосфористой кислоты ( например, тринонилфенилфосфит ( полигард) или три-я - / пре / п-бутилфенилфосфит) всегда менее эффективны, чем смешанные эфиры. Как показал один из авторов, хорошими ингибирующими свойствами обладает фосфит продукта реакции фенола со стиролом. Это - густая жидкость соломенно-желтого цвета, в концентрации 0 5 % по весу обеспечивает сохранение физико-механических характеристик различного типа полиолефинов в различных условиях переработки. Продукт не окрашивает полимеры, не токсичен, вследствие чего может быть использован при стабилизации пластиков, применяемых для бытовых целей. [8]
Защита от светостарения может осуществляться введением анти-оксидантов, подавляющих процессы фотосенсибилизированного окисления. Так, например, эффективными светостабилизаторами полиамидной пленки являются 2 6-ди-тре / и-бутил-4 - метилфениловый эфир пирокатехинфосфористой кислоты, 2 6-ди-трт - бутилгидро-хинон и смесь йодистого калия с нафтенатом меди. [9]
Несколько антиоксидантов были исследованы путем однократного введения спиртовых растворов антиоксидантов на метаноле в желудок белым мышам. В этих опытах были исследованы: 2 6 - р и-трет-бутил - 4-метилфенол, фенил-а-нафтиламин, ТЧД - ди-р-нафтил-га - фе-нилендиамин и 2 6-ди - / тгрет-бутил-4 - метилфениловый эфир пирока-техинфосфористой кислоты. [10]
Но эта заметка очень хорошо показывает, в каком темном лесу блуждали химики, в том числе и сам Канниццаро, до создания теории строения ароматических соединений. Так, Канниццаро уже склоняется к совершенно верному мнению Кольбе о том, что анисовый спирт не аналогичен гликолям Вюрца, но в то же время Канниццаро, не считая фенол спиртом, полагает, что низший гомолог бензилового спирта будет не тождествен, а изомерен с фенолом. Это подтверждается, по Канниццаро, тем, что как в описанных ранее основаниях, так и в гомоанисовой кислоте кислородосодержащий остаток - бвНдв играет роль одноатомного радикала. Это подтверждается и свойствами ( ссылка на работу Каура) анизола и его гомолога. Канниццаро надеется, что, исходя из гомологов фенола, можно получить гомологи анисовой кислоты и соответствующие им спирты. Вся проблема их конституции сводится к изучению конституции фенола, служащей отправной точкой для этой серии спиртов. Впервые полученный Канниццаро и Бертаныши анисовый спирт представлял собою новый класс спиртов с кислородосодержащим радикалом. Высказанное ранее предположение о его аналогии с гликолями и о том, что истинным радикалом анисового спирта является стирол, не подтвердилось, так как из двубромированного стирола анисовый спирт получить не удалось. После того как различными путями было установлено, что в анисовом спирте имеется лишь одна оксигидрильпая группа Н0, необходимо было установить, как и с чем связан второй атом кислорода в анисовом спирте. Из различных предположений осталось одно, когда обнаружилось, что анисовая кислота распадается на углекислоту и метилфениловый эфир. Формула анисового спирта будет, по Канниццаро, 7Н7 ( - СНгО) О. [11]
Страницы: 1
www.ngpedia.ru
Анизол - это... Что такое Анизол?
| Анизол | |
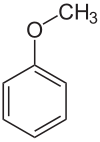 | |
| Систематическое наименование | Метоксибензол, метилфениловый эфир |
| Традиционные названия | Анизол |
| Химическая формула | C6H5OCh4 |
| Состояние (ст. усл.) | бесцветная жидкость |
| Молярная масса | 108,13 г/моль |
| Плотность | 0,9954 г/см³ |
| Температура плавления | -37,5 °C |
| Температура кипения | 153,8 °C |
| Температура вспышки | 41 °C °C |
| Критическая точка | 4,04 МПа, 369 °C |
| Удельная теплота испарения | 36,81 кДж/моль |
| Растворимость в воде | 0,15 г/100 мл |
| Показатель преломления | 1,5178 |
Анизол (метоксибензол, метилфениловый эфир) C6H5OCh4 — бесцветная жидкость с приятным запахом.
Получение
- В промышленности анизол получают взаимодействием фенолята натрия с Ch4OSO2ONa:


- В лабораторных условиях анизол получают взаимодействием фенола и диметилсульфата в водно-щелочной среде:

Физические свойства
Анизол — бесцветная жидкость с приятным запахом.
Легко растворим в этаноле, эфире, бензоле. Плохо растворим в воде (0,15 г/100 г воды).Химические свойства
- Анизол, как и все простые эфиры, устойчив и гидролизуется только при особых условиях:


- При действии хлора на анизол образуется смесь 4-хлор- (пара-), 2,4-дихлор- и 2,4,6-трихлоранизолов.
- При хлорировании с помощью PCl5 образуется только 4-хлоранизол.
Применение
Анизол используется как растворитель и как промежуточный продукт в производстве красителей, лекарств и душистых веществ.
Токсические свойства
ЛД50 3,5÷4 г/кг при подкожном введении.
Безопасность
Температура вспышки анизола 41 °C, температура самовоспламенения 485 °C, КПВ 0,34÷6,3%.
Литература
Примечания
dic.academic.ru
Анизол — Википедия (с комментариями)
Материал из Википедии — свободной энциклопедии
| Анизол | |
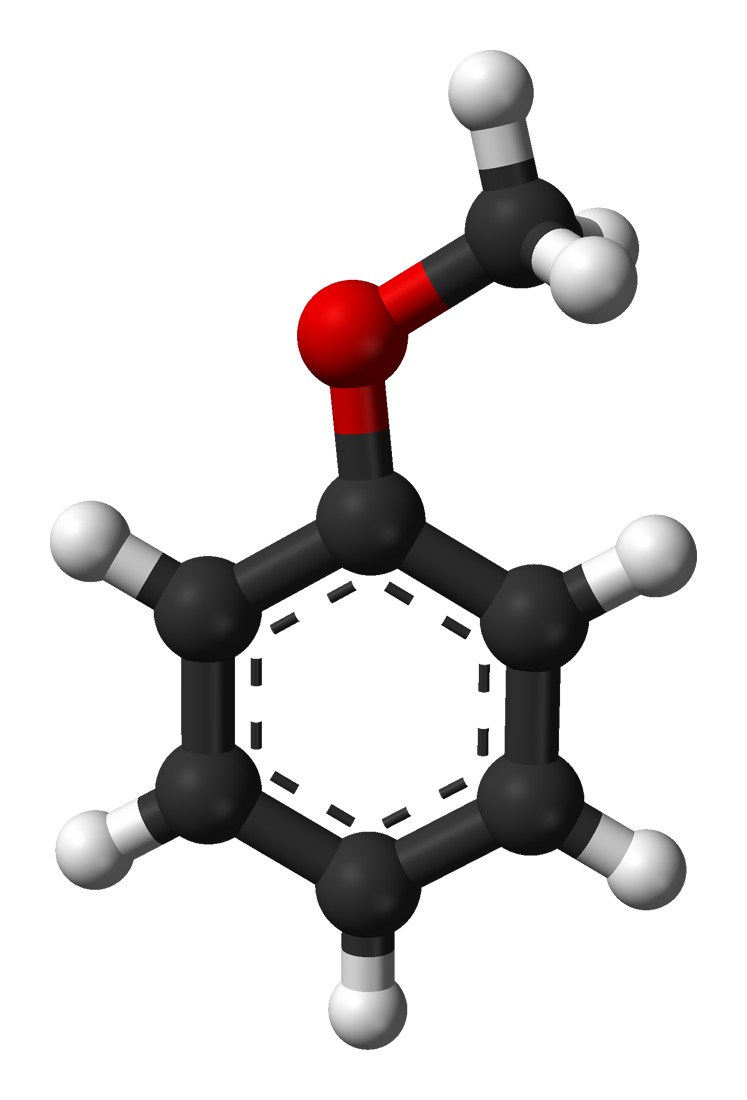 | |
| Систематическоенаименование | Метоксибензол, метилфениловый эфир |
| Традиционные названия | Анизол |
| Хим. формула | C6H5OCh4 |
| Состояние | бесцветная жидкость |
| Молярная масса | 108,13 г/моль |
| Плотность | 0,9954 г/см³ |
| Т. плав. | -37,5 °C |
| Т. кип. | 153,8 °C |
| Т. всп. | 41 °C °C |
| Кр. точка | 4,04 МПа, 369 °C |
| Растворимость в воде | 0,15 г/100 мл |
| Показатель преломления | 1,5178 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Анизóл (метоксибензол, метилфениловый эфир) C6H5OCh4 — метиловый эфир фенола, органическое вещество относится к простым эфирам.
Получение
В промышленности анизол получают взаимодействием фенолята натрия с метилсульфатом натрия:
<math>\mathsf{C_6H_5ONa + CH_3OSO_2ONa \ \xrightarrow{\ \ \ }\ C_6H_5OCH_3 + Na_2SO_4}</math>Взаимодействием фенола и метанола:
<math>\mathsf{C_6H_5OH + CH_3OH \ \xrightarrow{175-225^oC,\ Al_2O_3}\ C_6H_5OCH_3 + H_2O}</math>Также можно получить анизол при взаимодействии фенолята натрия с хлористым метилом[1]:
<math>\mathsf{C_6H_5ONa + CH_3Cl \rightarrow C_6H_5OCH_3 + NaCl}</math>В лабораторных условиях анизол получают взаимодействием фенола и диметилсульфата в водно-щелочной среде:
<math>\mathsf{C_6H_5OH + (CH_3O)_2SO_2 \xrightarrow{100^oC,\ OH^-}\ C_6H_5OCH_3 + H_2SO_4}</math>Физические свойства
Анизол — бесцветная жидкость с приятным запахом. Легко растворим в этаноле, диэтиловом эфире, бензоле. Плохо растворим в воде (0,15 г/100 г воды).
Химические свойства
- Анизол, как и все простые эфиры, устойчив и гидролизуется только при особых условиях:
- При действии хлора на анизол образуется смесь 4-хлор- (пара-), 2,4-дихлор- и 2,4,6-трихлоранизолов.
- При хлорировании с помощью PCl5 образуется только 4-хлоранизол.
Применение
Анизол используется как растворитель и как промежуточный продукт в производстве красителей, лекарств и душистых веществ.
Токсические свойства
Слаботоксичен, ЛД50 3,5÷4 г/кг (крысы, подкожно) и 10 г/кг (крысы, внутрижелудочно). Оказывает очень слабое раздражение кожи[1].
Безопасность
Температура вспышки анизола 41 °C, температура самовоспламенения 485 °C, КПВ 0,34÷6,3%.
Напишите отзыв о статье "Анизол"
Литература
См. также
Примечания
- ↑ 1 2 Вредные вещества в промышленности. Справочник для химиков, инженеров и врачей. Изд. 7-е, пер. и доп. В трех томах. Том I. Органические вещества. Под ред. засл. деят. науки проф. Н. В. Лазарева и докт. мед. наук Э. Н. Левиной. Л., «Химия», 1976. 592 стр., 27 табл., библиография —1850 названий.
Отрывок, характеризующий Анизол
«Je serais maudit par la posterite si l'on me regardait comme le premier moteur d'un accommodement quelconque. Tel est l'esprit actuel de ma nation», [Я бы был проклят, если бы на меня смотрели как на первого зачинщика какой бы то ни было сделки; такова воля нашего народа. ] – отвечал Кутузов и продолжал употреблять все свои силы на то, чтобы удерживать войска от наступления. В месяц грабежа французского войска в Москве и спокойной стоянки русского войска под Тарутиным совершилось изменение в отношении силы обоих войск (духа и численности), вследствие которого преимущество силы оказалось на стороне русских. Несмотря на то, что положение французского войска и его численность были неизвестны русским, как скоро изменилось отношение, необходимость наступления тотчас же выразилась в бесчисленном количестве признаков. Признаками этими были: и присылка Лористона, и изобилие провианта в Тарутине, и сведения, приходившие со всех сторон о бездействии и беспорядке французов, и комплектование наших полков рекрутами, и хорошая погода, и продолжительный отдых русских солдат, и обыкновенно возникающее в войсках вследствие отдыха нетерпение исполнять то дело, для которого все собраны, и любопытство о том, что делалось во французской армии, так давно потерянной из виду, и смелость, с которою теперь шныряли русские аванпосты около стоявших в Тарутине французов, и известия о легких победах над французами мужиков и партизанов, и зависть, возбуждаемая этим, и чувство мести, лежавшее в душе каждого человека до тех пор, пока французы были в Москве, и (главное) неясное, но возникшее в душе каждого солдата сознание того, что отношение силы изменилось теперь и преимущество находится на нашей стороне. Существенное отношение сил изменилось, и наступление стало необходимым. И тотчас же, так же верно, как начинают бить и играть в часах куранты, когда стрелка совершила полный круг, в высших сферах, соответственно существенному изменению сил, отразилось усиленное движение, шипение и игра курантов.Русская армия управлялась Кутузовым с его штабом и государем из Петербурга. В Петербурге, еще до получения известия об оставлении Москвы, был составлен подробный план всей войны и прислан Кутузову для руководства. Несмотря на то, что план этот был составлен в предположении того, что Москва еще в наших руках, план этот был одобрен штабом и принят к исполнению. Кутузов писал только, что дальние диверсии всегда трудно исполнимы. И для разрешения встречавшихся трудностей присылались новые наставления и лица, долженствовавшие следить за его действиями и доносить о них. Кроме того, теперь в русской армии преобразовался весь штаб. Замещались места убитого Багратиона и обиженного, удалившегося Барклая. Весьма серьезно обдумывали, что будет лучше: А. поместить на место Б., а Б. на место Д., или, напротив, Д. на место А. и т. д., как будто что нибудь, кроме удовольствия А. и Б., могло зависеть от этого. В штабе армии, по случаю враждебности Кутузова с своим начальником штаба, Бенигсеном, и присутствия доверенных лиц государя и этих перемещений, шла более, чем обыкновенно, сложная игра партий: А. подкапывался под Б., Д. под С. и т. д., во всех возможных перемещениях и сочетаниях. При всех этих подкапываниях предметом интриг большей частью было то военное дело, которым думали руководить все эти люди; но это военное дело шло независимо от них, именно так, как оно должно было идти, то есть никогда не совпадая с тем, что придумывали люди, а вытекая из сущности отношения масс. Все эти придумыванья, скрещиваясь, перепутываясь, представляли в высших сферах только верное отражение того, что должно было совершиться. «Князь Михаил Иларионович! – писал государь от 2 го октября в письме, полученном после Тарутинского сражения. – С 2 го сентября Москва в руках неприятельских. Последние ваши рапорты от 20 го; и в течение всего сего времени не только что ничего не предпринято для действия противу неприятеля и освобождения первопрестольной столицы, но даже, по последним рапортам вашим, вы еще отступили назад. Серпухов уже занят отрядом неприятельским, и Тула, с знаменитым и столь для армии необходимым своим заводом, в опасности. По рапортам от генерала Винцингероде вижу я, что неприятельский 10000 й корпус подвигается по Петербургской дороге. Другой, в нескольких тысячах, также подается к Дмитрову. Третий подвинулся вперед по Владимирской дороге. Четвертый, довольно значительный, стоит между Рузою и Можайском. Наполеон же сам по 25 е число находился в Москве. По всем сим сведениям, когда неприятель сильными отрядами раздробил свои силы, когда Наполеон еще в Москве сам, с своею гвардией, возможно ли, чтобы силы неприятельские, находящиеся перед вами, были значительны и не позволяли вам действовать наступательно? С вероятностию, напротив того, должно полагать, что он вас преследует отрядами или, по крайней мере, корпусом, гораздо слабее армии, вам вверенной. Казалось, что, пользуясь сими обстоятельствами, могли бы вы с выгодою атаковать неприятеля слабее вас и истребить оного или, по меньшей мере, заставя его отступить, сохранить в наших руках знатную часть губерний, ныне неприятелем занимаемых, и тем самым отвратить опасность от Тулы и прочих внутренних наших городов. На вашей ответственности останется, если неприятель в состоянии будет отрядить значительный корпус на Петербург для угрожания сей столице, в которой не могло остаться много войска, ибо с вверенною вам армиею, действуя с решительностию и деятельностию, вы имеете все средства отвратить сие новое несчастие. Вспомните, что вы еще обязаны ответом оскорбленному отечеству в потере Москвы. Вы имели опыты моей готовности вас награждать. Сия готовность не ослабнет во мне, но я и Россия вправе ожидать с вашей стороны всего усердия, твердости и успехов, которые ум ваш, воинские таланты ваши и храбрость войск, вами предводительствуемых, нам предвещают».
wiki-org.ru
Наглядная химия. Фенолы и Простые эфиры (pdf)

23
Химические свойства
Основные свойства
.. | .. | .. |
Ch4 O Ch4 | Ch4 O | O |
диметиловый эфир | метилфениловый эфир | дифениловый эфир |
| Убывание основности |
|
|
|
|
|
|
|
|
|
|
|
|
| ||
Ch4OCh4 + HCl |
|
| Ch4 |
|
|
|
|
|
| Ch4 Cl- | |||
|
|
| O |
| |||||||||
| |||||||||||||
|
|
|
| ||||||||||
| |||||||||||||
диметиловый эфир
H
диметилоксонийхлорид
Расщепление простых эфиров
| Ch4OCh3Ch4 + HI |
|
|
| CH I | + CH CH OH | |||||||||||||||||
|
|
| |||||||||||||||||||||
| метилэтиловый | 3 |
| 3 | 2 |
|
|
| |||||||||||||||
|
| иодметан |
|
|
|
|
| этанол |
|
|
| ||||||||||||
|
|
| эфир |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||
Ch4OCh3Ch4 + 2HI |
|
| CH I + | CH CH I + H O | |||||||||||||||||||
|
| ||||||||||||||||||||||
метоксиэтан | 3 |
| 3 | 2 | 2 |
| |||||||||||||||||
иодметан |
| иодэтан |
|
|
| ||||||||||||||||||
CH |
| O |
| Ch3Ch4 + H+ |
|
|
|
|
| δ + |
|
|
|
|
| `δ + |
|
|
| ||||
|
|
|
|
|
| CH |
|
| O |
| CH |
| CH | ||||||||||
|
|
|
|
|
|
|
|
| |||||||||||||||
3 | метоксиэтан |
| 3 |
|
|
|
|
|
|
| 2 | 3 | |||||||||||
|
|
|
|
|
|
| |||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||
|
|
|
|
|
|
|
|
| H |
|
|
|
| ||||||||||
метилэтоксоний-ион

|
|
|
|
|
|
|
| 24 |
|
|
|
| нуклеофил |
|
|
| уходящая |
|
|
|
|
|
|
|
| группа |
CH |
| O | CH | CH + I- | δ - | CH | δ + |
|
3 | I | OCH CH | ICh4 + C2H5OH | |||||
|
| 2 | 3 |
| 3 | 2 3 | ||
|
| H |
|
|
|
| H | иодметан этанол |
переходное состояние
|
|
|
|
нуклеофил | уходящая | ||
|
|
| группа |
|
| ||
|
|
|
|
Ch4Ch3OH + HI | δ + |
| O | H | C H I + H O | ||
CH CH | 2 | + I- | |||||
| 3 |
| H | 2 | 5 | 2 | |
этанол |
|
|
| иодэтан |
| ||
|
|
|
|
| |||
C6H5OCh4 + HI |
| C6H5OH + Ch4I | ||
| ||||
анизол |
| фенол иодметан | ||
Ch4Ch3OCh3Ch4 + HOSO3H |
|
| C2H5OSO3H + C2H5OH | |
|
| |||
диэтиловый эфир |
| этилгидросульфат этанол | ||
Окисление простых эфиров
• Пероксидами называются соединения, содержащие в молекуле группировку из двух атомов кислорода —О—О—.

25
• Гидропероксидами называются соединения, содержащие в молекуле группировку —О—ОН.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| R |
|
|
| O |
|
|
| O |
|
|
|
| H |
|
|
|
|
|
|
|
|
|
| |||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||
Ch4Ch3 |
|
| O |
|
| Ch3Ch4 | [O] |
| Ch4 | CH |
|
|
|
| O |
| O |
|
|
|
|
| CHCh4 | h3O | |||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||||||||||||||||||||
|
|
| диэтиловый эфир |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||||||||||
|
|
|
|
|
|
|
|
| OH |
|
|
|
|
|
|
|
|
|
| OH | |||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| пероксид дигидроксиэтила | ||||||||||||||||||||||||
|
|
|
| Ch4 | CH |
|
| O |
|
| OH + Ch4 | CH |
| OH |
|
|
|
|
|
|
|
|
|
| |||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||
|
|
|
|
|
| OH |
|
|
|
|
|
|
|
|
| OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||
|
|
| гидропероксид |
|
|
|
| гидрат ацетальдегида |
|
|
|
|
|
| |||||||||||||||||||||||||||||||||||
|
| гидроксиэтилена |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| O |
|
|
|
|
|
| |||
|
|
|
|
|
| Ch4 | CH |
|
| OH |
|
|
|
|
|
|
| Ch4 |
|
|
|
| C | + |
| H O | |||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| H | 2 |
|
| ||||||
|
|
|
|
|
|
|
|
|
|
| OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||
Отдельные представители |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||||
HC |
| CH + HOCh3Ch3Ch3Ch4 |
|
|
|
|
|
| Ch3 |
| CH |
|
| O |
|
|
|
| Ch3Ch3Ch3Ch4 | ||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
| ||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
| ||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
| ||||||||||||||||||||||||||||||||||||||||||
ацетилен |
|
|
|
|
|
|
| бутанол-1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| бутилвиниловый эфир | |||||||||||||||||||||
Винилин, или бальзам Шостаковского
nCh3 CH
CH
 Ch3 CH
Ch3 CH
OC4H9 OC4H9
n
studfiles.net
Наглядная химия. Фенолы и Простые эфиры (pdf)

13
ФЕНОЛЫ
• Фенолами называются производные ароматических углеводородов, в которых один или несколько атомов водорода, непосредственно связанных с ароматическим кольцом, заменены на гидроксильные группы.
ФЕНОЛЫ
Одноатомные
| C2H5 |
фенол | этилфенол |
Двухатомные
OH |
| HO |
| OH |
|
1,2- | 1,3- | 1,4-дигидроксибензол |
дигидроксибензол | дигидроксибензол | (гидрохинон) |
(пирокатехин) | (резорцин) |
|

15
Способы получения
Получение из бензола
+ Ch3 CH Ch4 AlCl3, HCl, 100°C
Ch4 CH Ch4
кумол
O2,95-130°C | h3SO4,50-90°C | + CH |
| C |
| CH |
| |||
|
|
|
|
|
| |||||
|
|
| 3 |
|
|
|
|
|
| 3 |
|
|
|
|
|
|
|
|
| ||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| O |
| ||||
Ch4 C | Ch4 | OH |
|
|
|
|
|
|
| |
| O | OH |
|
|
|
|
|
|
|
|
гидропероксид кумола | фенол | ацетон |
| |||||||
Получение из ароматических сульфокислот
SO3Na | ONa |
| OH |
|
|
| |
| NaOH, тв. | HCl |
|
|
| -NaCl |
|
| SO3Na | ONa | OH |
|
|
|
натриевая соль | натриевая соль | резорцин | |
м-бензолсульфокислоты | резорцина | ||
|

16
Химические свойства
| OH |
|
δ - | δ - | +M > –I |
|
| |
| δ - |
|
Кислотные свойства
C6H5OH + KOH C6H5OK + h3O
C6H5OK + h3O
C6H5OK + CO2 + h3O C6H5OH + KHCO3
C6H5OH + KHCO3
| OH | OH | NO2 |
| OH | OH | |
|
|
| |
Ch4 |
| O2N | NO2 |
|
| ||
|
| O2N | |
п-крезол | фенол | п-нитрофенол | пикриновая |
pKa |
|
| кислота |
10.2 | 10.0 | 7.8 | ~1 |
Увеличение кислотности

17
Реакции нуклеофильного замещения
Взаимодействие с галогенопроизводными
C6H5O-K+ | δ + | Br | C6H5OCh4 + KBr |
+ Ch4 | |||
феноксид | бромметан | метилфениловый | |
калия |
|
| эфир |
C6H5O-Na+ + C6H5I | C6H5OC6H5 + NaI | ||
феноксид | иодбензол | дифениловый | |
натрия |
|
| эфир |
Реакции углеводородного радикала
Галогенирование
|
| Br |
|
OH |
|
| OH |
+ | 3Br2 |
| + 3HBr |
|
| Br | Br |
OH |
|
| O |
Br | Br | Br | Br |
| + | h3O |
|
| Br2 |
|
не растворим в воде

19
Сульфирование
OH | OH | OH |
|
| SO3H |
| h3SO4 | + |
|
|
|
| SO3H |
фенол | 2-гидроксибензол- | 4-гидроксибензол- |
| сульфокислота | сульфокислота |
Окисление
фенол | O | OH |
п-хинон | гидрохинон | |
| OH | O |
[O]
пирокатехин | о-хинон |

20
Отдельные представители
OH
OH
OH
|
|
| OH |
|
| OH |
|
|
|
фенол | гидрохинон |
| пирокатехин |
|
| (1,4-дигидроксибензол)(1,2-дигидроксибензол) | |||
OH | OCh4 Ch4 |
| OH | |
|
| NH | OH |
|
OCh4 | OCh4 | Ch3 | CH | OH |
|
|
| ||
гваякол | вератрол |
| адреналин |
|
OH
OH
OH
| NO2 |
резорцин | пикриновая кислота |
1,3-дигидроксибензол | (2,4,6-тринитрофенол) |

21
Простые эфиры
• Простыми эфирами называются производные спиртов и фенолов, в которых атом водорода гидроксильной группы заменен на углеводородный радикал.
R O R'
СИММЕТРИЧНЫЙ | НЕСИММЕТРИЧНЫЙ | ||||
|
|
|
|
|
|
| C2H5OC2H5 |
|
| Ch4OC2H5 |
|
|
|
|
|
|
|
диэтиловый эфир | метилэтиловый эфир | ||||
Номенклатура
Ch4OCh3Ch3Ch3Ch4 Ch4Ch3OCh3Ch3Ch4 | Ch4Ch3OC6H5 | |
метоксибутан | этоксипропан | этоксибензол |
(бутилметиловый эфир) | (пропилэтиловый эфир) | (фенилэтиловый эфир) |

22
метоксибензол | этоксибензол |
(анизол) | (фенетол) |
Способы получения
Получение из галогенопроизводных.
нуклеофил |
|
|
Ch4Ch3Ch3O- K+ + | δ + |
|
Ch4 Cl | Ch4Ch3Ch3OCh4 + KCl | |
пропоксид калия | хлорметан | метилпропиловый эфир |
нуклеофил |
|
|
C6H5O- K+ + | δ + | C6H5OCh3Ch3Ch4 + KBr |
Ch4Ch3Ch3 Br | ||
феноксид калия | 1-бромпропан | пропилфениловый эфир |
Получение из спиртов
2Ch4Ch3Ch3OHH+  Ch4Ch3Ch3OCh3Ch3Ch4 + h3O
Ch4Ch3Ch3OCh3Ch3Ch4 + h3O
пропанол-1 | дипропиловый эфир |
studfiles.net



















