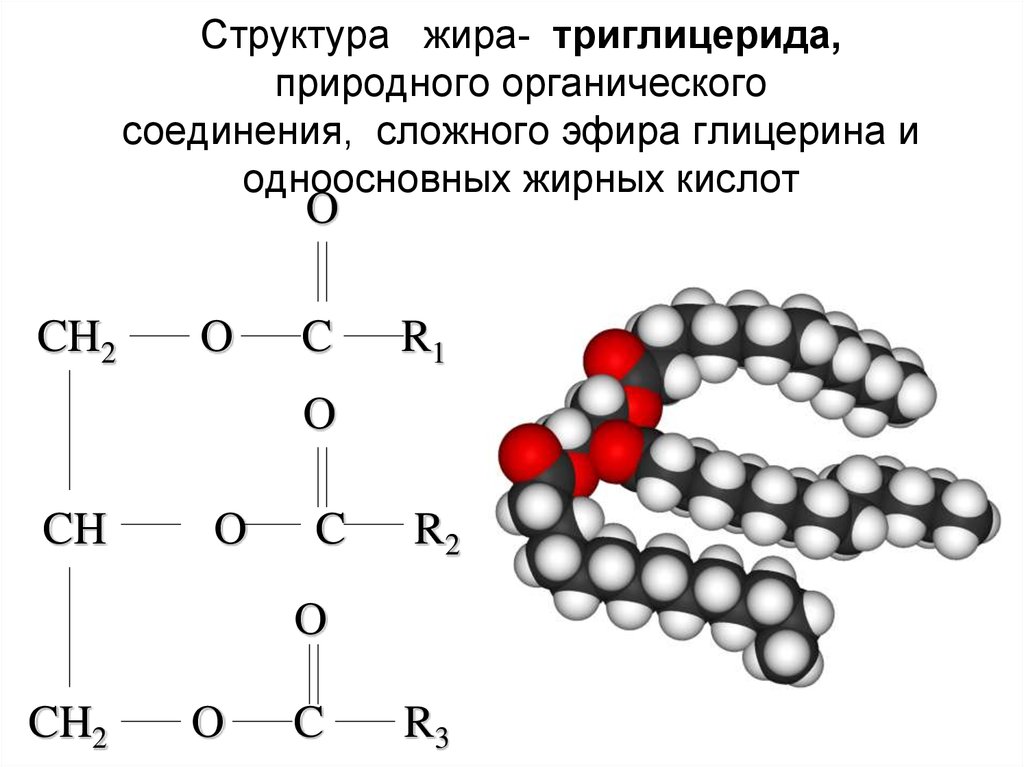
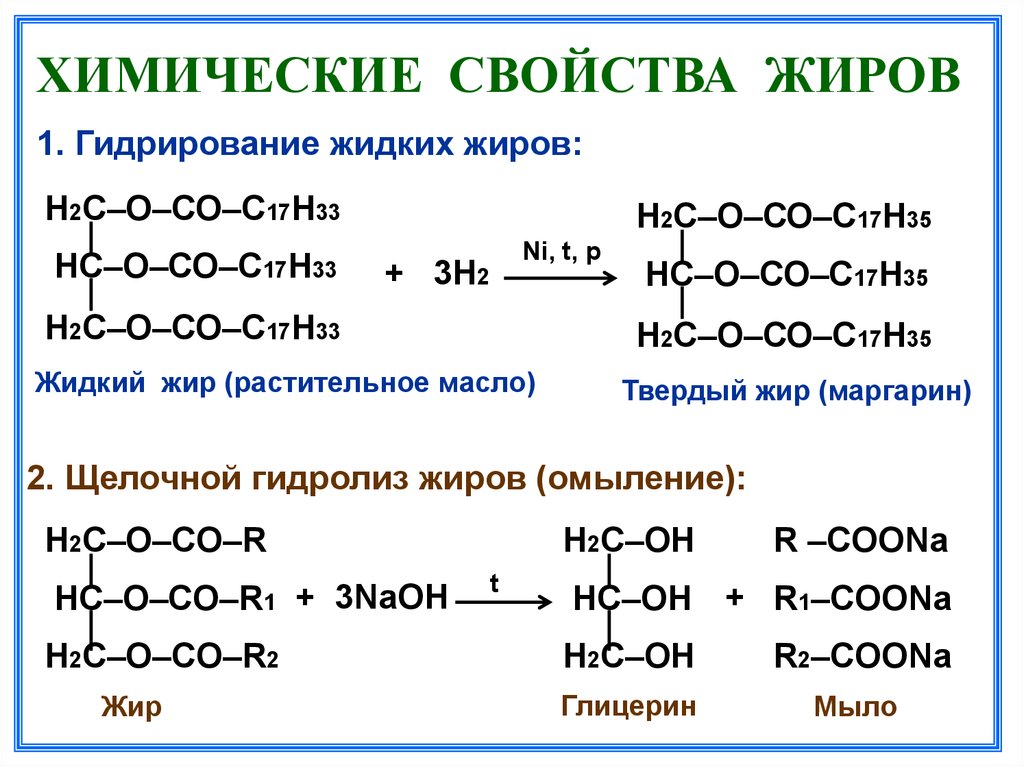
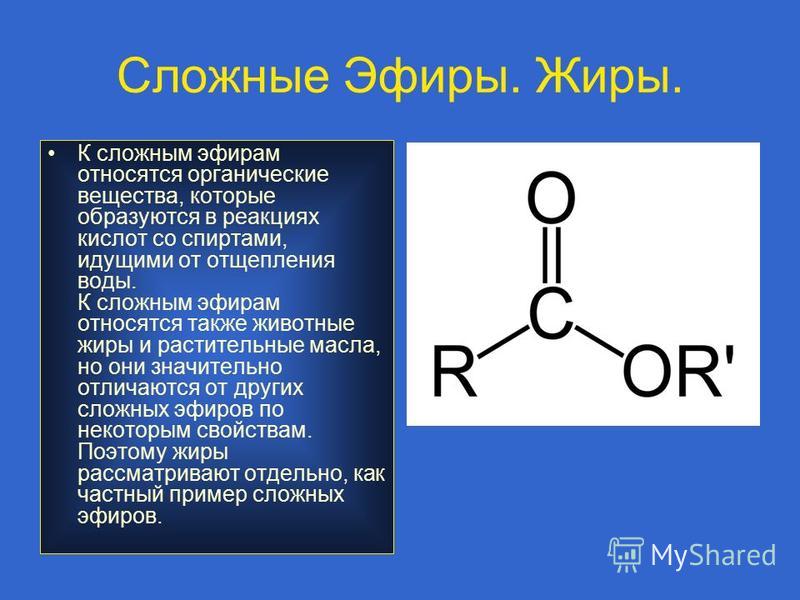
Содержание
Строение и свойства сложных эфиров, их применение
На данном уроке будет рассмотрена тема «Производные карбоновых кислот. Сложные эфиры». Благодаря этой теме, вы сможете познакомиться с производными карбоновых кислот. Также вы изучите самые важные функциональные производные карбоновых кислот – сложные эфиры. Рассмотрите их состав, некоторые свойства, формирование названий и сферы их применения в жизни.
I. Состав и строение сложных эфиров
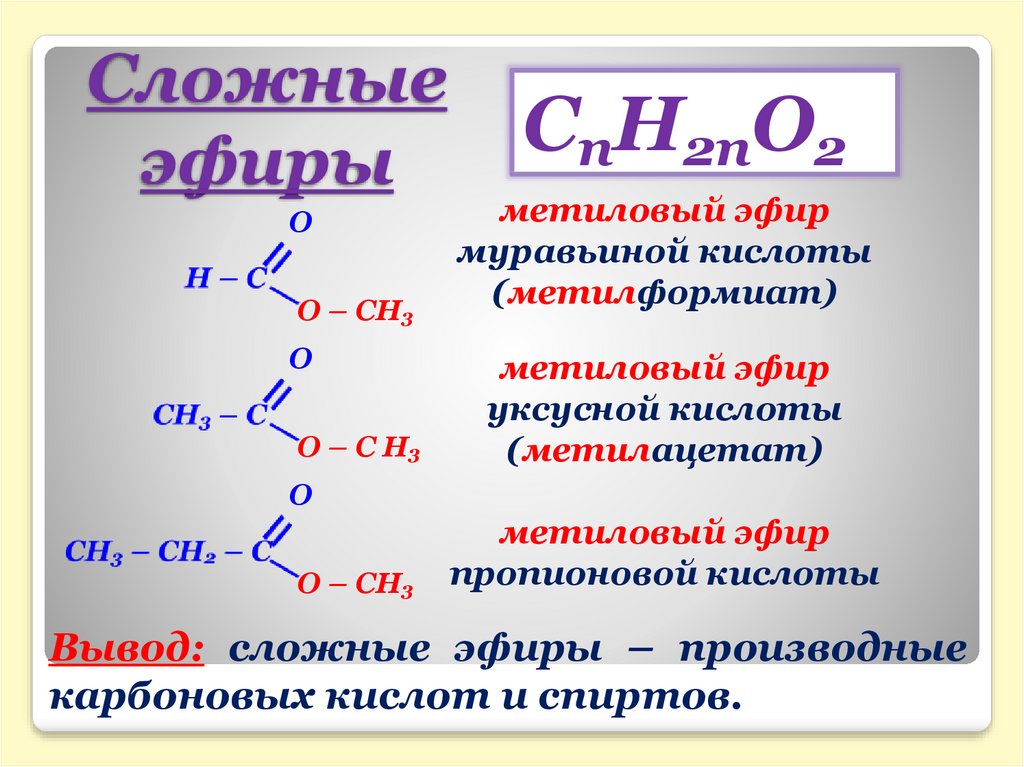
Сложные эфиры – функциональные производные карбоновых кислот, в молекулах которых гидроксильная группа (-ОН) замещена на остаток спирта (-OR).
Сложные эфиры карбоновых кислот – соединения с общей формулой R–COOR’, где R и R’ – углеводородные радикалы.
II. Физические свойства и нахождение сложных эфиров в природе
- Летучие, бесцветные жидкости
- Плохо растворимы в воде
- Чаще с приятным запахом
- Легче воды
Сложные эфиры содержатся в цветах, фруктах, ягодах.
Они определяют их специфический запах.
Являются составной частью эфирных масел (известно около 3000 эф.м. – апельсиновое, лавандовое, розовое и т. д.)
Эфиры низших карбоновых кислот и низших одноатомных спиртов имеют приятный запах цветов, ягод и фруктов. Эфиры высших одноосновных кислот и высших одноатомных спиртов – основа природных восков. Например, пчелиный воск содержит сложный эфир пальмитиновой кислоты и мирицилового спирта (мирицилпальмитат):
CH3(CH2)14–CO–O–(CH2)29CH3
|
Аромат.
Структурная формула.
|
Название сложного эфира
|
|
Яблоко
|
Этиловый эфир
2-метилбутановой кислоты
|
|
Вишня
|
Амиловый эфир муравьиной кислоты
|
|
Груша
|
Изоамиловый эфир уксусной кислоты
|
|
Ананас
|
Этиловый эфир масляной кислоты
(этилбутират)
|
|
Банан
|
Изобутиловый эфир уксусной кислоты
(у изоамилацетата так же напоминает запах банана)
|
|
Жасмин
|
Бензиловый эфир уксусной (бензилацетат)
|
Запахи эфиров:
Рис.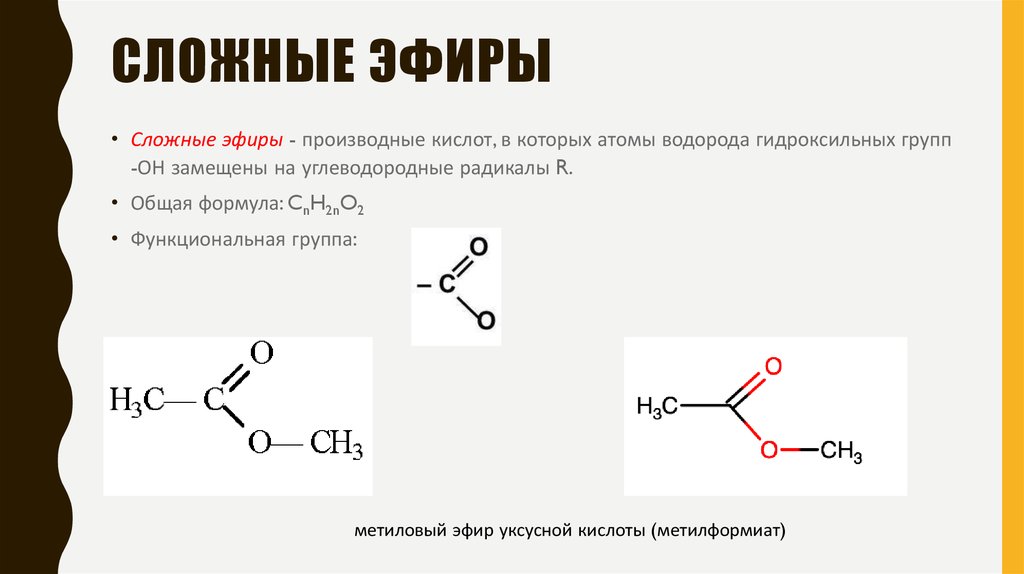 1.
1.
Сложные эфиры нерастворимы в воде, но хорошо смешиваются со многими органическими веществами. Именно поэтому они используются как растворители для лаков и красок. Рис. 1. Этилацетат и метил ацетат – основа растворителя – жидкости для снятия лака с ногтей.
Температуры кипения сложных эфиров меньше, чем температуры кипения кислот и спиртов с близкой молярной массой. Почему? Сложные эфиры, в отличие от кислот и спиртов, не способны образовывать водородные связи между молекулами.
Сравнение температуры кипения эфиров
III. Номенклатура сложных эфиров
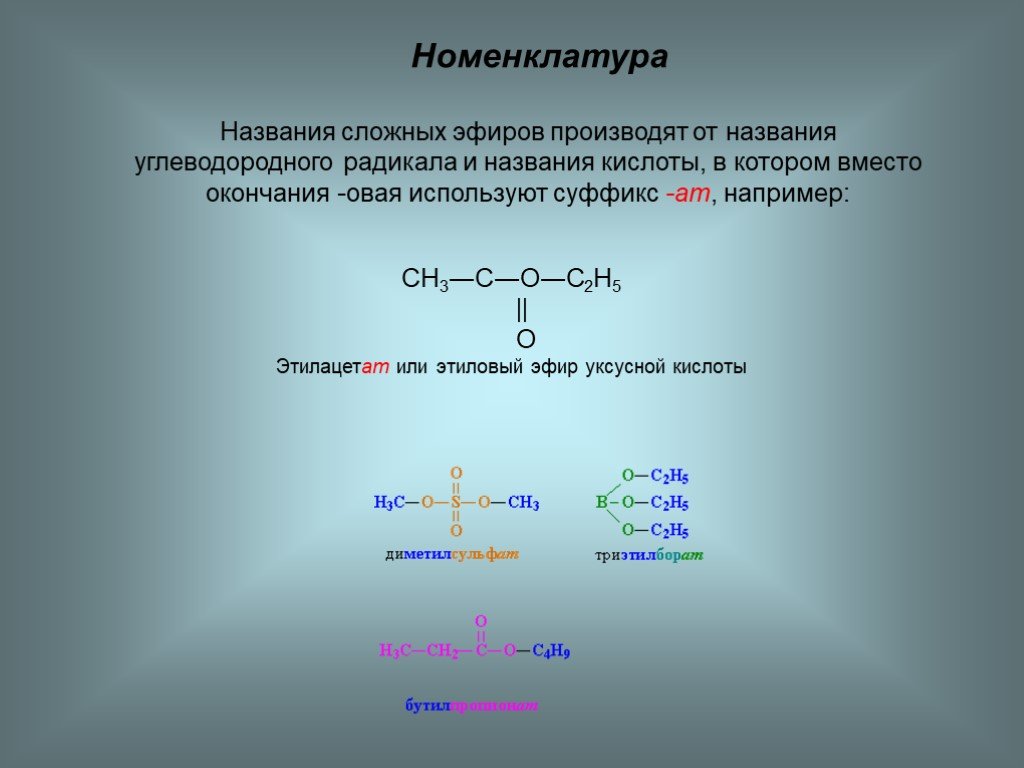
Краткие названия сложных эфиров строятся по названию радикала (R’) в остатке спирта и названию группы RCOO— в остатке кислоты. Например, этиловый эфир уксусной кислоты CH3COOC2H5 называется этилацетат.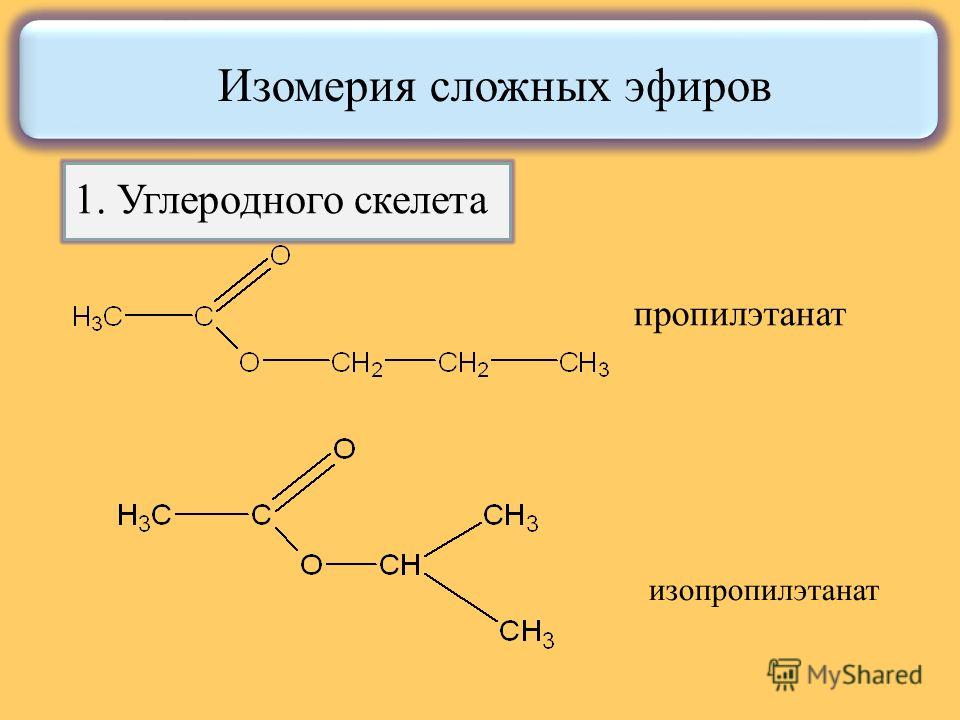
Названия по ИЮПАК выделены жирным шрифтом:
|
H–COO–C2H5
|
Ch4–COO–Ch4–Ch4
|
Ch3Ch3–COO–C2H5
|
|
Этилформиат, этилметаноат;
этиловый эфир муравьиной кислоты
|
Метилацетат, метилэтаноат;
метиловый эфир уксусной кислоты
|
Этилбутират, этилбутаноат;
этиловый эфир бутановой кислоты
|
IV. Применение
- В качестве отдушек и усилителей запаха в пищевой и парфюмерной (изготовление мыла, духов, кремов) промышленности;
- В производстве пластмасс, резины в качестве пластификаторов.
Пластификаторы – вещества, которые вводят в состав полимерных материалов для придания (или повышения) эластичности и (или) пластичности при переработке и эксплуатации.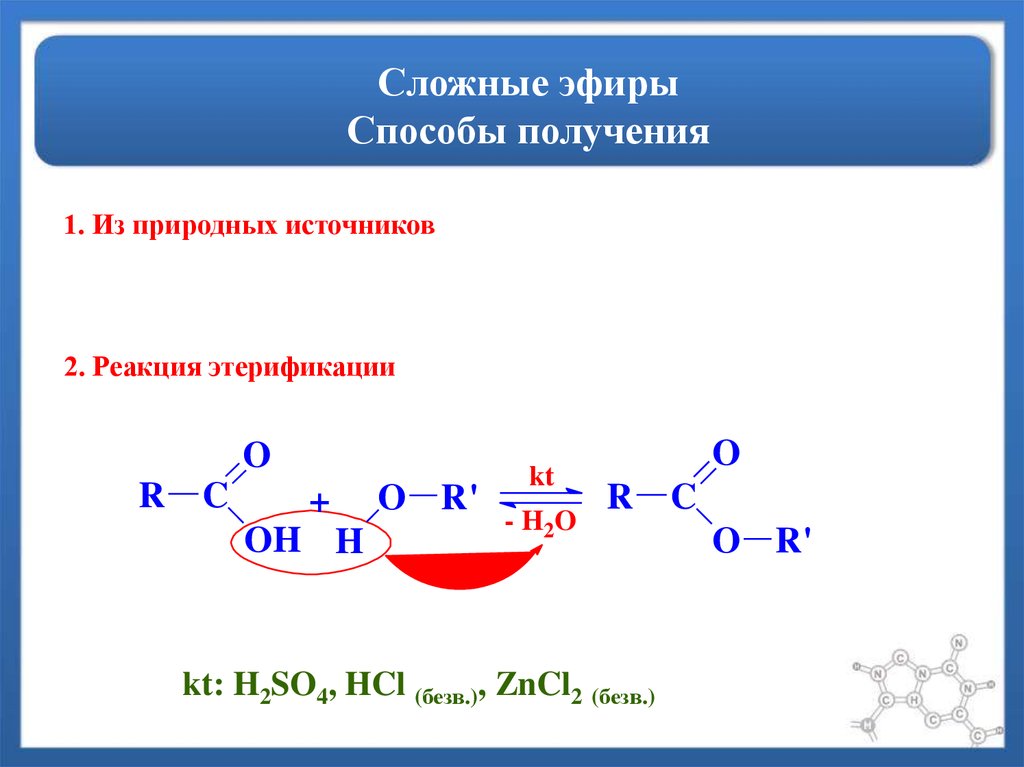
Применение в медицине
В конце XIX — начале ХХ века, когда органический синтез делал свои первые шаги, было синтезировано и испытано фармакологами множество сложных эфиров. Они стали основой таких лекарственных средств, как салол, валидол и др. Как местнораздражающее и обезболивающее средство широко использовался метилсалицилат, в настоящее время практически вытесненный более эффективными средствами.
V. Получение сложных эфиров
Cложные эфиры могут быть получены при взаимодействии карбоновых кислот со спиртами (реакция этерификации). Катализаторами являются минеральные кислоты.
Видео-опыт: «Получение уксусноэтилового эфира»
Видео-опыт: «Получение борноэтилового эфира»
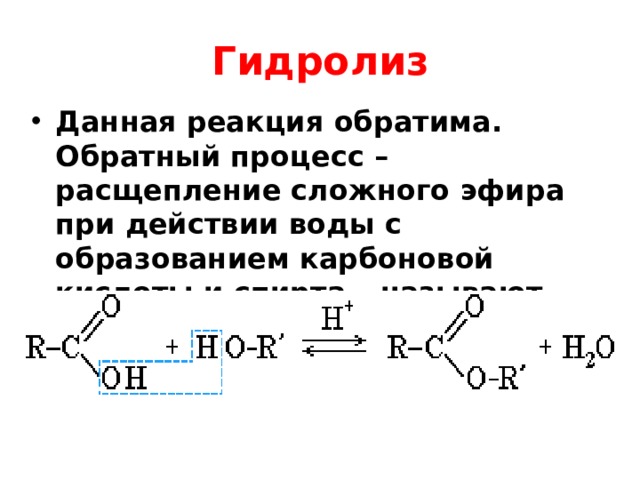
Реакция этерификации в условиях кислотного катализа обратима. Обратный процесс – расщепление сложного эфира при действии воды с образованием карбоновой кислоты и спирта – называют гидролизом сложного эфира.
RCOOR’ + H2O (H+)↔ RCOOH + R’OH
Гидролиз в присутствии щелочи протекает необратимо (т.к. образующийся отрицательно заряженный карбоксилат-анион RCOO– не вступает в реакцию с нуклеофильным реагентом – спиртом).
Эта реакция называется омылением сложных эфиров (по аналогии со щелочным гидролизом сложноэфирных связей в жирах при получении мыла).
VI. Тренажеры
Тренажер №1: “Реакция этерификации”
ЦОРы
Видео-опыт: «Получение уксусноэтилового эфира»
Видео-опыт: «Получение борноэтилового эфира»
Сложные эфиры
Цели:
- Рассмотреть строение и виды изомерии сложных
эфиров. - Познакомить учащихся с номенклатурой этого
класса соединений. - Изучить особенности реакций этерификации и
гидролиза сложных эфиров.
- Рассказать о распространенности сложных эфиров
в природе.
Использованные ЦОР:
- Флеш-анимации:
- реакция этерификации. http://files.school-collection.edu.ru/dlrstore/d777bfac-8cff-11db-b606-0800200c9a66/ch20_21_02.swf
- Иллюстрации ЕК ЦОР:
- нахождение сложных эфиров в природе. http://files.school-collection.edu.ru/dlrstore/d777bfad-8cff-11db-b606-0800200c9a66/ch20_21_03.jpg
- применение сложных эфиров. http://files.school-collection.edu.ru/dlrstore/d777bfae-8cff-11db-b606-0800200c9a66/ch20_21_04.jpg
- Видео-опыты:
- получение уксусноэтилового эфира. http://files.school-collection.edu.ru/dlrstore/2638df79-e8e5-0109-e2e2-cd2fa153a7bb/index.htm
ХОД УРОКА
I. Оргмомент
II. Проверка знаний учащихся
Работа с модульными карточками: «Химические
свойства карбоновых кислот» (1 вариант работает с
реагентами А, 2 вариант – с реагентами Б, 3 вариант
– в реагентами В)
Реагент | 1 вариант | 2 вариант | 3 вариант |
| Муравьиная кислота | Уксусная кислота | Пропионовая кислота | |
1. Взаимодействие с металлами Взаимодействие с металлами
| |||
2. Взаимодействие с оксидами
| |||
3. Взаимодействие с основаниями
| |||
4. Взаимодействие с солями
| |||
5. Взаимодействие со спиртами Взаимодействие со спиртами
|
III. Новая тема
Актуализация знаний
Невозможно представить нашу жизнь без запахов.
И окружающая нас природа, и вкусная свежая еда
или выпечка дарят нам естественные, всеми
любимые ароматы.
Звучит «Вальс цветов» П. И. Чайковского.
Демонстрируется видеофильм с кадрами
распускающихся цветов.
Сейчас вы посмотрели фрагмент фильма,
показывающий красоту и многообразие цветов —
этих удивительно красивых и необыкновенно
ароматных созданий природы и человека. Они
излучают нежные ароматы, которые в жизни
растений имеют большое значение.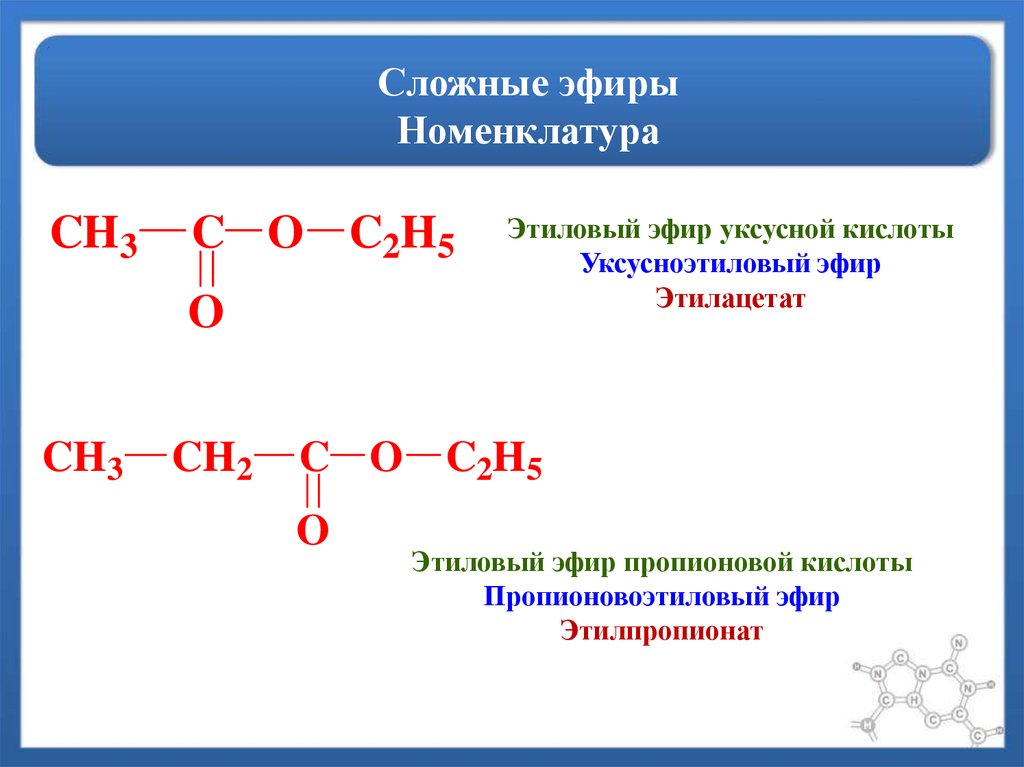 Ароматы цветов
Ароматы цветов
привлекают насекомых для опыления, а фруктовые
запахи притягивают животных и способствуют
распространению семян.
Под чарующие звуки этой мелодии представьте
себе розу. Можно долго любоваться её красотой,
вслушиваться в дыхание её лепестков и листьев, но
впечатление будет неполным, если не ощущать
аромат царственного цветка.
Куст алых роз опять заполнил утро ароматом,
Зимой он стыл в тоске усталых грез, зовя весну.
Расцвел улыбчивый рассвет на лепестке крылатом,
Луч солнца пробудился вновь у певчих птиц в
плену.
У каждого из нас есть любимые ароматы.
? Скажите, какие ароматы всплывают в вашей памяти?
В природе большое количество веществ, имеющих
запах, относятся к химическому классу сложных
эфиров. Все они имеют свой уникальный запах.
Многие эфиры имеют запахи, напоминающие
тропические цветы или фрукты. Сегодня вы
Сегодня вы
познакомитесь со строением сложных эфиров,
способами их получения и применением.
История открытия
Много веков назад арабы уже знали различные
способы получения душистых веществ из растений и
выделений животных. Душистые вещества
содержатся обычно в виде капелек в особых
клетках. Они встречаются в цветах, листьях,
кожуре плодов и даже в древесине. Их называют
эфирными маслами. Они представляют собой сложные
смеси душистых органических веществ.
В 1759 г. Л. де Лаурагваис перегонял крепкую
уксусную кислоту с винным спиртом и получил
некоторое количество жидкости, запах которой
отличался от запаха исходных веществ. Так
впервые был получен сложный эфир — продукт
взаимодействия карбоновой кислоты и спирт СН3
– СООН + С2Н5ОН = СН3СООС2Н5
+ Н2О.
Определение сложных эфиров
Сложные эфиры – функциональные
производные карбоновых кислот,
в молекулах которых гидроксильная группа (– ОН)
замещена на остаток спирта (–OR)
Сложные эфиры карбоновых кислот –
соединения с общей формулой
R–COOR’, где R и R’ –
углеводородные радикалы.
Общая формула сложных эфиров, образованных
предельными одноосновными кислотами и
предельными одноосновными спиртами: СnH2nO2
Такую же формулу имеют предельные одноосновные
карбоновые кислоты.
Номенклатура сложных эфиров
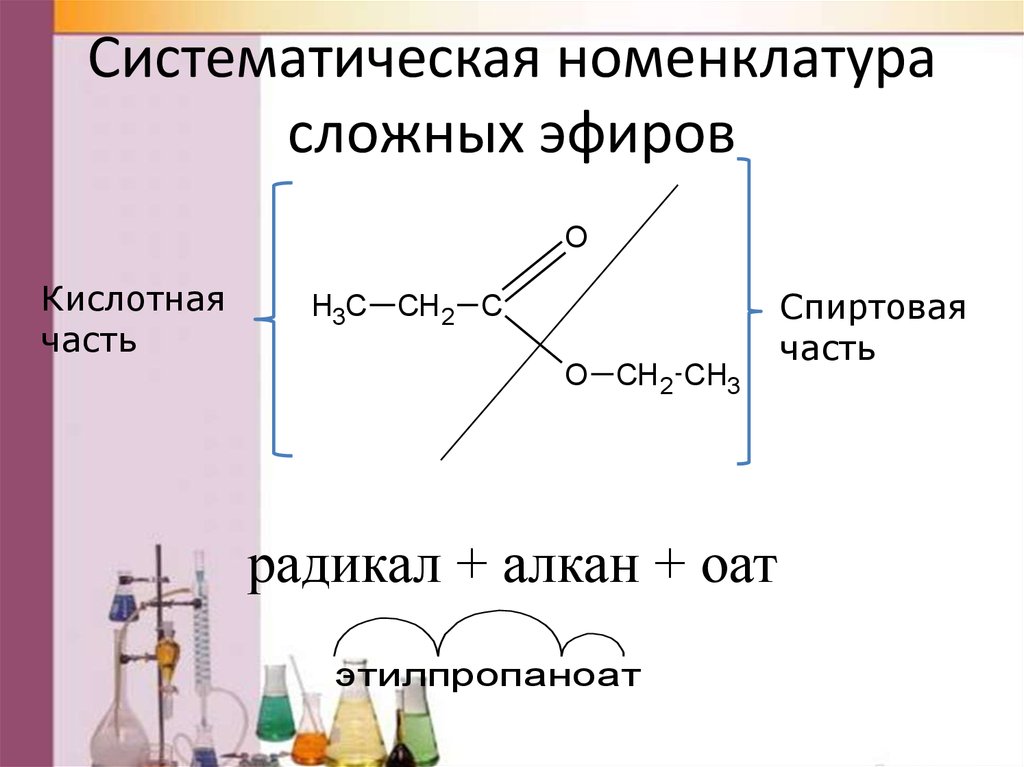
По систематической номенклатуре названия
сложных эфиров образуются путем прибавления к
названию аниона кислоты приставки, с названием
УВ радикала спирта. Название аниона кислоты
заканчивается на -ат или -оат.
Широко используется и другой способ, по
которому название сложного эфира отражают,
перечисляя название спиртового радикала и
кислоты. Например: метиловый эфир уксусной
кислоты или метиловый эфир этановой кислоты.
Назвать сложные эфиры:
Изомерия сложных эфиров
Изомерия сложных эфиров связана с изомерией УВ
радикалов кислот и спиртов, входящих в состав
эфиров.
Напишем изомеры для пропилбутаната: С3Н7
– СО – О – СН2 – СН2 – СН3
- Изомерия углеродного скелета: С2Н7 –
СО – О – СН – СН3
СН2 (изопропилбутанат) - Изомерия положения ФГ: СН3 – СН2 – СН2
– СН2 – СО – О – СН2 – СН3 - Межклассовая изомерия (с карбоновыми
кислотами): СН3 – (СН2)5 – СООН
Получение сложных эфиров
? По какой реакции могут быть получены
сложные эфиры? (При взаимодействии карбоновых
кислот со спиртами).
1. Такие реакции называются реакциями
этерификации:
R1 – COOH + HO – R2 <––H+––> R1
– CO – O – R2 + H2O
Реакция протекает в присутствии катализатора
– сильных минеральных кислот (в основном серной
к-ты) и является обратимой. Катализатор ускоряет
Катализатор ускоряет
как прямую так и обратную реакции.
2. Взаимодействием галогеноангидрида кислоты с
алкаголятом щелочного металла: R1 –
COCl + R2ONa = R1 – COO – R2 + NaCl
Как называется процесс, противоположный
реакции этерификации? (Гидролиз СЭ)
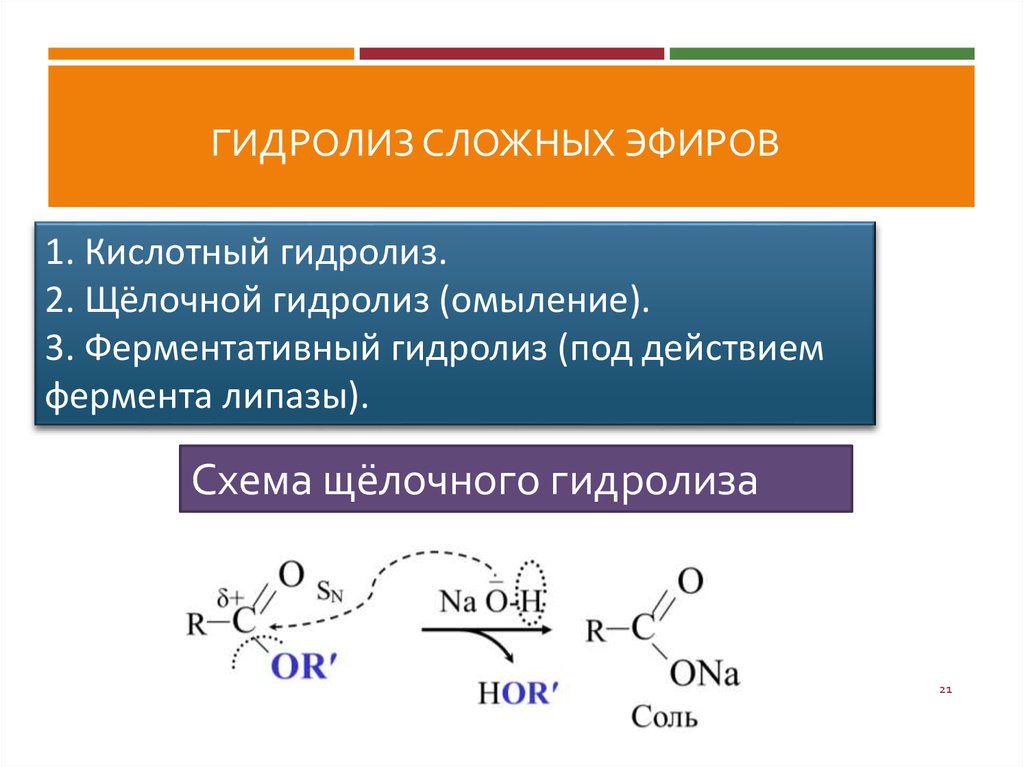
Химические свойства сложных эфиров
1. Гидролиз сложных эфиров расщепление сложного
эфира при действии воды с образованием
карбоновой кислоты и спирта:
RCOOR’ + H2O <––(H+)––> RCOOH + R’OH
2. Гидролиз в присутствии щелочи протекает
необратимо (т.к. образующийся отрицательно
заряженный карбоксилат-анион RCOO– не вступает
в реакцию с нуклеофильным реагентом – спиртом).
Эта реакция называется омылением сложных
эфиров (по аналогии со щелочным гидролизом
сложноэфирных связей в жирах при получении мыла).
3. Горение сложных эфиров:
Горение сложных эфиров:
2CH3 – COO – CH3 + 7O2 = 6CO2 + 6H2O
Сложные эфиры в природе.
Сложные эфиры содержатся в цветах, фруктах,
ягодах. Они определяют их специфический
запах.
Являются составной частью эфирных масел
(известно около 3000 эф.м. – апельсиновое,
лавандовое, розовое и т. д.)
Эфиры низших карбоновых кислот и низших
одноатомных спиртов имеют приятный запах цветов,
ягод и фруктов. Эфиры высших одноосновных кислот
и высших одноатомных спиртов – основа природных
восков.
Физические свойства этих эфиров различны:
| Эфиры | Сложные эфиры, образованные низшими КК
и спиртами | Сложные эфиры, образованные высшими КК
и спиртами (воски) |
| Свойства | Летучие жидкости | Твердые вещества |
| Запах | Приятный фруктовый запах | Не имеют запаха |
| Растворимость | Плохо растворимы в воде, хорошо – в
органических растворителях | Не растворимы в воде |
Применение сложных эфиров
Сложные эфиры широко используются в качестве
растворителей и ароматизаторов в пищевой
промышленности.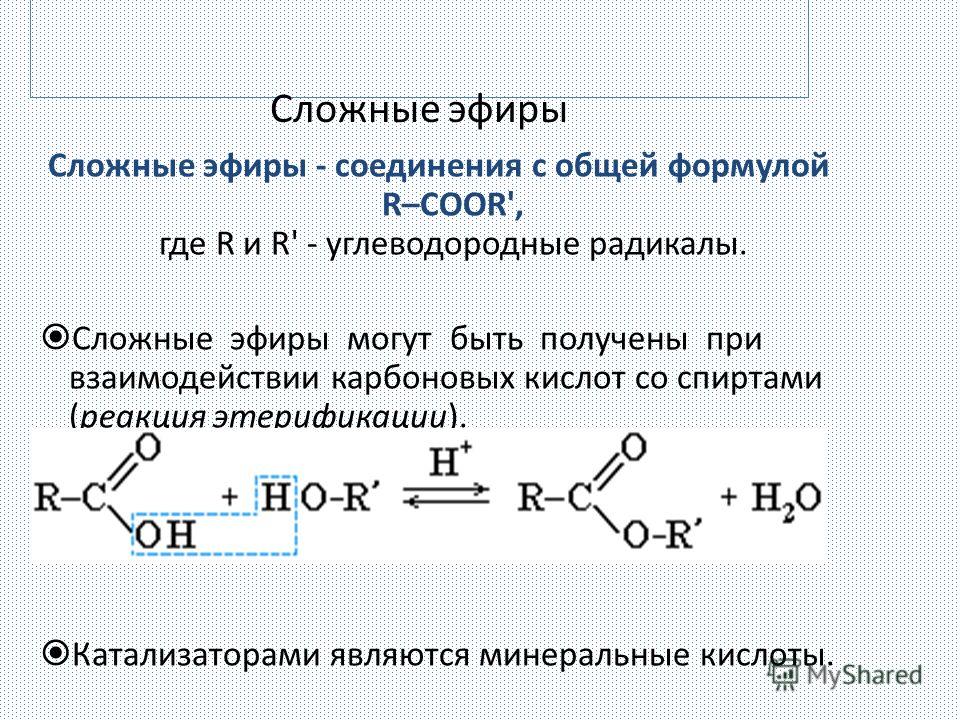
IV. Закрепление
А. Выберите правильные ответы:
1. В соответствии со схемой реакции происходит взаимодействие
между:
1) азотной кислотой и этанолом
2) метанолом и этанолом
3) муравьиной кислотой и пентанолом-2
4) бутанолом-2 и уксусной кислотой
5) метилацетатом и масляной кислотой
6) пальмитиновой кислотой и пропиловым спиртом
2. Сложные эфиры образуются при взаимодействии
уксусной кислоты с:
1) метанолом
2) фенолом
3) глицерином
4) пропанолом
5) пропаналем
6) этилатом натрия
Б. Составьте формулы и названия сложных эфиров,
образованных следующими веществами:
– СН3СООН и С2Н5ОН;
– С2Н5СООН и С3Н7ОН;
–С3Н7СООН и С4Н9ОН;
–С4Н9СООН и С5Н11ОН.
V. Домашнее задание: § 21 с. 196 – 197
Подготовить сообщения по темам:
– «Медицина и ароматерапия»
– «Применение восков»
VI. Итоги урока
Использованная литература:
- М.Ю. Горковенко Поурочные разработки по
химии к учебным комплектам О.С. Габриеляна и др. 10
класс. М.: «ВАКО», 2005 - В.Г. Денисова Химия. 10 класс: Поурочные
планы. – Волгоград: Учитель, 2003 - https://www.google.ru/url?sa=t&rct=j&q=&esrc=s&source=web&cd=6&cad=rja&uact=8&ved=0CEAQFjAF&url=http%3A%2F%2Fwiki.saripkro.ru%2Fimages%2FV-mire-aromatov..doc&ei=BZUdU4LfItTE4gSf04DQDg&usg=AFQjCNEIRSQSd8NQ2h5jPX6cbKVFXDY_fQ&sig2=Dwa2ad-v-9L-id156-9Jrw&bvm=bv.62578216,d.bGE
Функциональная группа сложных эфиров и этерификация
Учебные пособия по органической химии
- Сообщение от
Анжелика Девицки
15
Jul
Основные понятия функциональных групп сложного эфира
В этом руководстве вы узнаете об основных свойствах и структуре функциональной группы сложного эфира . Вы также узнаете о этерификации и ее механизме.
Темы, освещенные в других статьях
- Функциональные группы в органической химии
- Нуклеофил – что это такое?
- Реакция Sn1
- Реакция Sn2
Что такое сложноэфирная функциональная группа?
В органической химии сложные эфиры являются распространенной функциональной группой. Основная структура сложного эфира состоит из углерода, одинарно связанного с углеродом, двойной связи с кислородом и одинарной связи с кислородом. Для молекулы ниже показана простая структура сложноэфирной группы.
Структура основного эфира с неподеленными электронными парами
Основная химическая формула сложного эфира – R-COOR’. Группы R обозначают остальную часть молекулы, не входящую в функциональную группу.
Группы R обозначают остальную часть молекулы, не входящую в функциональную группу.
Что такое сложноэфирная связь?
Сложноэфирная связь представляет собой связь между атомом, имеющим двойную связь, с атомом кислорода, несущим любую алкильную или арильную группу. Эфирные связи находятся в сложноэфирных функциональных группах. Кроме того, связь обычно ковалентная и необходима для образования липидов.
Пример сложноэфирной связки. Источник изображения: что такое сложноэфирная связь?
Эти сложноэфирные связи важны, когда речь идет о липидах в нашем организме. Когда глицерин (спирт) соединяется с молекулами жирных кислот, это позволяет получить три сложных эфира. Этот процесс является причиной образования сложноэфирных связей.
Свойства сложных эфиров
По сравнению со спиртами и карбоновыми кислотами сложные эфиры, как правило, менее полярны, что позволяет им иметь более низкие температуры кипения. Из-за полярности сложных эфиров они могут участвовать в образовании водородных связей в качестве акцепторов водородных связей. Их способность участвовать в образовании водородных связей зависит от длины алкильных цепей, присоединенных к функциональной группе сложного эфира.
Их способность участвовать в образовании водородных связей зависит от длины алкильных цепей, присоединенных к функциональной группе сложного эфира.
Название сложного эфира
Название сложного эфира происходит от исходного спирта и исходной кислоты. В то время как простые эфиры могут быть названы в соответствии с их общими именами, все сложные эфиры могут быть названы с использованием их систематического названия IUPAC. Название основано на кислоте, за которой следует суффикс «-оат».
Примеры наименования IUPAC для простых эфиров
Когда сложный эфир образуется из обычной карбоновой кислоты, существуют замены для названия сложного эфира IPUAC.
- «этаноат» = «ацетат»
- «метаноат» = «формиат»
- «пропаноат» = «пропионат»
- «бутаноат» = «бутират»
Примеры сложных эфирных групп
Сложные эфиры широко распространены в природе. Сложные эфиры обычно имеют приятный запах и отвечают за характерные ароматы фруктов и цветов. Ароматизаторы и отдушки содержат натуральные и синтетические эфиры.
Ароматизаторы и отдушки содержат натуральные и синтетические эфиры.
Фруктовые запахи, связанные с эфирами. Источник изображения: Fragrance Chemicals in Fruits
Жиры и растительные масла представляют собой жирные кислоты с длинной цепью и глицерин, которые имеют сложные эфиры. Кроме того, крайне важное значение для жизни имеют эфиры фосфорных кислот. Некоторые распространенные примеры сложных эфиров и их названия приведены в списке ниже.
- methyl methanoate/formate (HCOOCH 3 )
- methyl ethanoate/acetate (CH 3 COOCH 3 )
- ethyl ethanoate/acetate (CH 3 COOCH 2 CH 3 )
Этерификация
Что такое этерификация?
Этерификация по Фишеру является наиболее распространенной реакцией для получения простых эфиров и включает смешивание карбоновой кислоты и спирта с небольшим количеством каталитической кислоты. Реакцию можно довести до конца кипячением с обратным холодильником (при наличии большого количества энергии).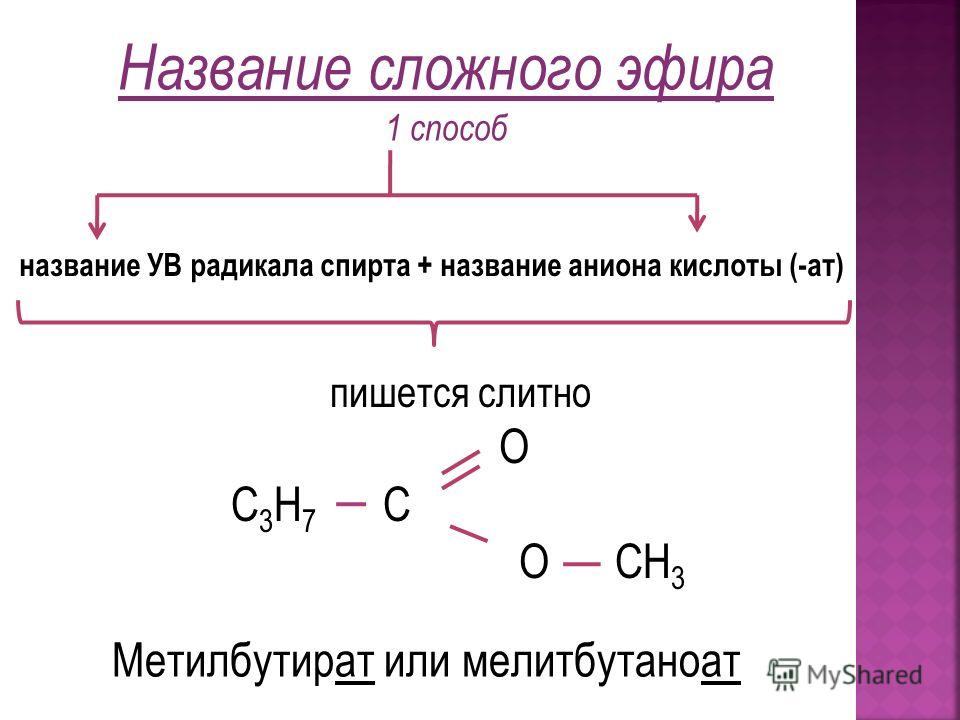 Чрезмерное тепло необходимо для этерификации, поскольку требуется много энергии для удаления группы «-OH» из карбоновой кислоты с образованием сложного эфира.
Чрезмерное тепло необходимо для этерификации, поскольку требуется много энергии для удаления группы «-OH» из карбоновой кислоты с образованием сложного эфира.
Простая реакция этерификации (H+ обозначает кислоту)
Механизм этерификации
- Во-первых, реакция этерификации начинается с протонирования карбонильного кислорода карбоновой кислоты. Созданный ион оксония стабилизируется резонансом (способностью перемещать электроны к другому атому).
- Затем спирт атакует карбонильный углерод, выталкивая электроны на кислород. В результате происходит образование тетраэдрического интермедиата.
- После этого ион оксония тетраэдрического промежуточного соединения теряет протон с образованием нейтрального тетраэдрического промежуточного соединения.
Стадии 1-3 этерификации. Источник изображения: Michael Leonard
- В любой из гидроксильных групп происходит протонирование и образуется хорошая уходящая группа (H 2 O).
- Следовательно, вода диссоциирует как хорошая уходящая группа по мере повторного образования карбонила.

- Наконец, протон теряется с образованием нейтрального эфира в качестве продукта реакции.
Стадии 4-6 этерификации. Источник изображения: Майкл Леонард
Дальнейшее чтение
- Функциональная группа карбоновой кислоты
- Реакция конденсации Aldol
- Реакция ацилирования фриделя
- Williamson Ether Synthes
Перейти к содержимому
Эфиры
Сложные эфиры представляют собой один из видов карбонильных соединений, описываемых как производные карбоновых кислот. В этой группе группа «-ОН» карбоновой кислоты была заменена группой, содержащей углеродсодержащую группу «-OR». Например:
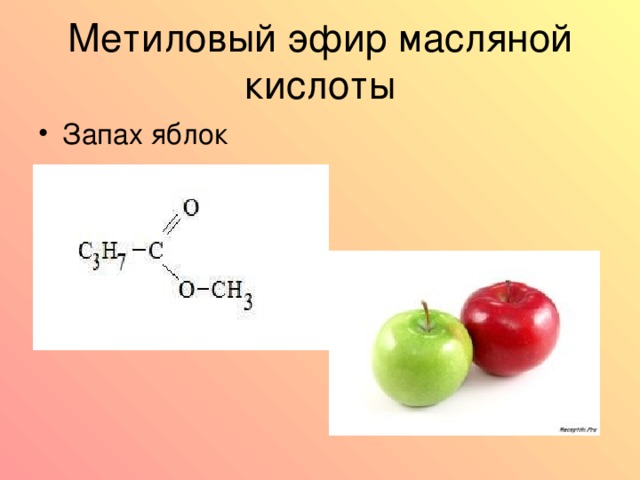
Этот сложный эфир представляет собой 3-метилбутилэтаноат. Он также известен под своим общим названием изоамилацетат. Это вещество является одним из немногих соединений аромата/вкуса, которые отличают вкус банана, хотя оно также содержится в некоторых других фруктах. Искусственный банановый ароматизатор, который используется для изготовления популярных конфет, в основном состоит из этого вещества.

Обратите внимание на карбонил здесь и второй атом кислорода, соединенный непосредственно с карбонильным углеродом. Эти структуры очень похожи на структуры карбоновых кислот, но свойства сложных эфиров не включают кислотность. Таким образом, сложные эфиры не могут ионизироваться, что делает их менее растворимыми в воде, чем карбоновые кислоты. И хотя неионизированные карбоновые кислоты способны образовывать межмолекулярные водородные связи, сложные эфиры этого не делают. Таким образом, сложные эфиры также менее полярны и имеют более низкие температуры плавления и кипения, чем их аналоги карбоновые кислоты.
Ванилин — это ароматический эфир, который является доминирующим ароматом/вкусом в обработанных ванильных бобах.
Многие вкусовые и ароматические соединения цветов и фруктов представляют собой сложные эфиры. Растительный материал чрезвычайно сложен, но отдельные эфиры, выделенные из растительных экстрактов, могут быть настолько характерными для растительных запахов, что люди должны конкретно определять их источники.
 Растительные ароматы в природе часто вырабатываются как аттрактанты животных, и, будучи животными, мы развили органы чувств, которые могут определять присутствие этих веществ и получать удовольствие от многих из них.
Растительные ароматы в природе часто вырабатываются как аттрактанты животных, и, будучи животными, мы развили органы чувств, которые могут определять присутствие этих веществ и получать удовольствие от многих из них.Промежуточная полярность сложных эфиров в сочетании с их несколько небольшим (для органического химического вещества) размером означает, что многие из них имеют достаточно низкие температуры кипения, чтобы некоторые из этих молекул улетучивались в газовую фазу вблизи их источника. Там, где они образуются — из цветка или фрукта — эти молекулы могут попасть в наш нос.
Сложные эфиры, как правило, в некоторой степени реактивны, разлагаясь на другие вещества при нагревании или воздействии резких колебаний pH. Приготовление пищи может изменить вкус продуктов, способствуя разрушению этих соединений.
Бензилэтаноат — сложный эфир, придающий аромат клубники. Rbreidbrown — собственная работа, CC BY-SA 4.0, https://commons.wikimedia.org/w/index.php?curid=92505251
Названия сложных эфиров основаны на двух отдельных частях этих молекул и, в отличие от большинства названий IUPAC, даются как два отдельных слова.
 Первый основан на органической структуре за пределами карбонила, «-метила» или «-этила» и т. д. В случае нашего соединения бананового масла это «3-метилбутиловая» часть названия. Второе слово в названии происходит от карбоновой кислоты, которая существовала бы, если бы мы удалили углероды за карбонилом и заменили их водородом. В приведенном здесь примере у нас есть «-этаноат», который происходит от «этановой кислоты», двухуглеродной карбоновой кислоты.
Первый основан на органической структуре за пределами карбонила, «-метила» или «-этила» и т. д. В случае нашего соединения бананового масла это «3-метилбутиловая» часть названия. Второе слово в названии происходит от карбоновой кислоты, которая существовала бы, если бы мы удалили углероды за карбонилом и заменили их водородом. В приведенном здесь примере у нас есть «-этаноат», который происходит от «этановой кислоты», двухуглеродной карбоновой кислоты.Упражнение 7.4.1
Амиды
Амиды также являются производными карбоновых кислот. Эти соединения имеют карбонил, непосредственно связанный с азотом. Этот азот может быть связан с атомами водорода или дополнительными атомами углерода. Связь между этой группой и аминами предполагается в названии «амид».
Названия амидов могут быть довольно сложными, но самые простые амиды названы на основе карбоновой кислоты, на которую они больше всего похожи, причем «-овая кислота» в названии карбоновой кислоты преобразуется в «-амид».

Например, этанамид выглядит так:
К сожалению для студентов, система ИЮПАК часто отбрасывается в сторону из-за знакомых названий, когда химики обсуждают амиды. Это вещество обычно называют ацетамидом, несистематическим, общим названием.
Амиды имеют электроотрицательные атомы азота, а их неподеленные пары электронов находятся в положении, близком к карбонильной группе. Такое расположение дает молекулы с некоторой полярностью, но на степень полярности амида также влияет то, что соединяется с самим азотом. Короче говоря, полярность может сильно варьироваться в пределах этого семейства соединений. Этанамид, показанный выше, может вступать во взаимодействие с водородными связями и обладает свойствами, отражающими это. Но более высокозамещенные амиды с дополнительными атомами углерода, присоединенными к атому азота, не способны на это и обладают соответствующими свойствами:
Лидокаин является местным анестетиком. Это ароматическое соединение, которое содержит амид, а также амин.

Устойчивость к вращению вокруг амидной связи
Амиды имеют тенденцию иметь некоторую общую электронную плотность с самим карбонильным звеном, в результате чего связь C-N проявляет некоторый характер двойной связи. В частности, для амидов, расположенных в средней части более крупных молекул, эти группы фиксируются в конформации, показанной ниже, сопротивляясь вращению вокруг связи углерод-азот. Это похоже на отсутствие вращения, о котором мы узнали в двойной связи углерод-углерод (например, в цис-транс-геометрических изомерах).
В трехмерных молекулах и моделях амид принимает планарную (плоскую) конфигурацию, и гибкость всей молекулы значительно снижается. Эта заблокированная структура встречается в белках в нескольких местах, где аминокислоты, которые связаны друг с другом, делают это через амидные связи, также известные как пептидные связи. Более крупные структурные особенности белков, такие как единицы вторичной структуры «альфа-спираль» и «бета-лист», часто обсуждаемые в биохимии, частично формируются из-за этой особенности амидных связей в этих белках.




 Растительные ароматы в природе часто вырабатываются как аттрактанты животных, и, будучи животными, мы развили органы чувств, которые могут определять присутствие этих веществ и получать удовольствие от многих из них.
Растительные ароматы в природе часто вырабатываются как аттрактанты животных, и, будучи животными, мы развили органы чувств, которые могут определять присутствие этих веществ и получать удовольствие от многих из них.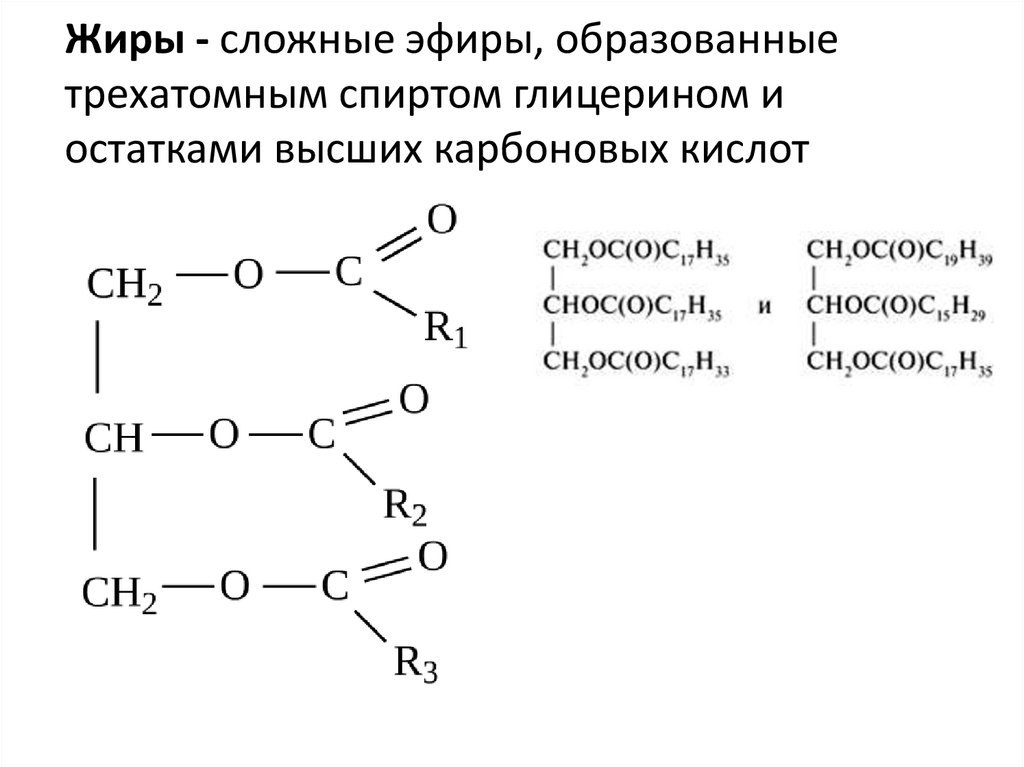 Первый основан на органической структуре за пределами карбонила, «-метила» или «-этила» и т. д. В случае нашего соединения бананового масла это «3-метилбутиловая» часть названия. Второе слово в названии происходит от карбоновой кислоты, которая существовала бы, если бы мы удалили углероды за карбонилом и заменили их водородом. В приведенном здесь примере у нас есть «-этаноат», который происходит от «этановой кислоты», двухуглеродной карбоновой кислоты.
Первый основан на органической структуре за пределами карбонила, «-метила» или «-этила» и т. д. В случае нашего соединения бананового масла это «3-метилбутиловая» часть названия. Второе слово в названии происходит от карбоновой кислоты, которая существовала бы, если бы мы удалили углероды за карбонилом и заменили их водородом. В приведенном здесь примере у нас есть «-этаноат», который происходит от «этановой кислоты», двухуглеродной карбоновой кислоты.