Краткий конспект подготовки к ЗНО по химии №34 Сложные эфиры. Жиры. Сложные эфиры конспект
Краткий конспект подготовки к ЗНО по химии №34 Сложные эфиры. Жиры
Конспект 34. Сложные эфиры. Жиры
Сложные эфиры
В присутствии сильных неорганических кислот гидроксильная группа обратимо обменивается на остаток спирта:
Сложные эфиры RCOOR’ – производные карбоновых кислот, у которых гидроксил карбоксильной группы замещен на остаток спирта.
Номенклатура сложных эфиров
Названия по ИЮПАК выделены жирным цветом:
|
|
|
|
|
Этилформиат, этилметаноат; этиловый эфир муравьиной кислоты |
Метилацетат, метилэтаноат; метиловый эфир уксусной кислоты |
Этилбутират, этилбутаноат; этиловый эфир бутановой кислоты |
Физические свойства эфиров
Сложные эфиры нерастворимы в воде, но хорошо смешиваются со многими органическими веществами. Именно поэтому они используются как растворители для лаков и красок. Этилацетат и метил ацетат – основа растворителя – жидкости для снятия лака с ногтей.
Температуры кипения сложных эфиров меньше, чем температуры кипения кислот и спиртов с близкой молярной массой. Почему? Сложные эфиры, в отличие от кислот и спиртов, неспособны образовывать водородные связи между молекулами.
Химические свойства сложных эфиров
Главное химическое свойство сложных эфиров – способность к гидролизу: Жиры – сложные эфиры глицерина и жирных (неразветвленных одноосновных карбоновых) кислот.Сложные эфиры RCOOR’ – производные карбоновых кислот, у которых гидроксил карбоксильной группы замещен на остаток спирта.Жиры – строительный материал и запас энергии организма. В теле человека массой 70кг в среднем содержится около 11кг жира.В животных жирах обычно содержатся остатки предельных (насыщенных) углеводородов. Эти жиры твердые.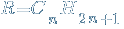 Растительные жиры (масла) обычно жидкие при комнатной температуре. В состав растительных масел обычно входят остатки непредельных (ненасыщенных) кислот. Растительные масла жидкие потому, что окружение каждой двойной связи – жесткая плоская конструкция из 6 атомов, и такие молекулы плохо укладываются в кристаллическую решетку.
Растительные жиры (масла) обычно жидкие при комнатной температуре. В состав растительных масел обычно входят остатки непредельных (ненасыщенных) кислот. Растительные масла жидкие потому, что окружение каждой двойной связи – жесткая плоская конструкция из 6 атомов, и такие молекулы плохо укладываются в кристаллическую решетку.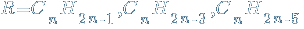 …
…
Гидрирование жиров
Из дешевых сортов растительных масел, непригодных для употребления в пищу, получают с помощью неполного гидрирования маргарин, а при глубоком гидрировании образуется саломас – твердая масса, которую используют для производства мыла:
Гидролиз жиров
В организме под действием ферментов жиры разлагаются на глицерин и жирные кислоты:В промышленности проводят щелочной гидролиз жиров, при этом образуется глицерин и смесь солей жирных кислот – мыло.
vneshkoly.com.ua
doc4web.ru
Конспект урока по химии "Сложные эфиры" (10 класс)
Цели урока.
Продолжить формирование системы знаний о классах органических соединений и генетической связи между ними; способствовать закреплению понимания взаимосвязи химического строения веществ, свойств и применения на примере сложных эфиров.
Задачи урока.
1. Закрепить знания о механизме реакции этерификации.
2. Дать понятия о физических свойствах сложных эфиров, их номенклатуре.
3. Развить понятие о водородной связи, взаимном влиянии атомов, воздействии этих явлений на свойства веществ.
4. Способствовать развитию эрудиции, логического и ассоциативного мышления учащихся.
5. Развитие социальной активности учащихся через установление межпредметных связей химии с историей, биологией, медициной, литературой.
Методы и приемы: словесные, наглядные, практические – в логической взаимосвязи.
Оборудование и реактивы: Для демонстрации: пластиковая бутылка, лучина, спиртовка, спирт, спички, фрукты.
Для лабораторной работы: спиртовки, спирт, спички, пробирки, держатели, газоотводные трубки, уксусная кислота, изоамиловый спирт, вода.
ХОД УРОКА
I. Оргмомент.
II. Подготовка к изучению нового материала.
Одним из химических свойств карбоновых (и минеральных) кислот является их способность вступать в реакцию этерификации. Что это за реакция? Приведите пример такой реакции. Разберите механизм реакции этерификации. Какое вещество образуется в результате реакции этерификации? Тема нашего урока «Сложные эфиры, их строение, получение, изомерия, физические свойства и применение». Оксана Кожевникова (стихотворение о сложных эфирах).
III Изучение нового материала.
Сложные эфиры – производные кислородсодержащих кислот (карбоновых и минеральных), в которых атом водорода гидроксильной группы замещен на углеводородный радикал.
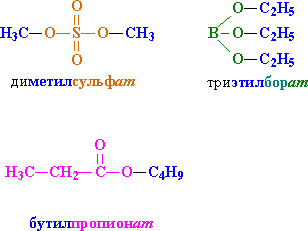
Бутиловый эфир пропионовой кислоты
Пропионовобутиловый эфир
Мы подробно изучим сложные эфиры, являющиеся производными карбоновых кислот.
Выведем общую формулу сложных эфиров, образованных остатками предельных карбоновой кислоты и спирта. Сnh3nO2
Какие виды изомерии характерны для сложных эфиров? (Углеродного скелета, положения, межклассовая с карбоновыми кислотами.)
Задание по группам: Запишите изомерные вещества состава:
С6Н12О2
С5Н10О2
С7Н14О2
С4Н8О2
С8Н16О2
С9Н18О2
относящиеся к разным классам. Назовите все вещества.
Получение сложных эфиров:
1. Реакция этерификации
Задание по группам: Запишите уравнения реакций этерификации между следующими веществами:
масляной кислотой и этиловым спиртом (ананас)
масляной кислотой и бутиловым спиртом (персик)
масляной кислотой и метиловым спиртом (яблоко)
муравьиной кислотой и амиловым спиртом (пентанолом) (вишня)
бензойной кислотой и этиловым спиртом (жасмин)
уксусной кислотой и изобутиловым спиртом (банан)
уксусной кислотой и октиловым спиртом (апельсин)
уксусной кислотой и изоамиловым спиртом (груша)
Назовите получившиеся сложные эфиры разными способами (по международной и тривиальной номенклатуре).
О
Взаимодействие хлорангидридов карбоновых кислот и спиртов СН3С-Сl+НО-С2Н5
О
СН3С-О-С2Н5+НСl
3. Взаимодействие хлорангидридов карбоновых кислот и алкоголятов щелочных металлов
О О
СН3С-Сl+NaО-С2Н5 СН3С-О-С2Н5+NaСl
О О
4. Взаимодействие ангидридов карбоновых кислот и спиртов СН3СОССН3+НОСН3
О О
СН3СОСН3+СН3СОН
5. Если в реакцию вступают двухосновные карбоновые кислоты и двухатомные спирты, то они могут друг с другом вступать в реакции поликонденсации (Что это за реакция?) с получением полиэфиров. Например, реакция между терефталевой (1,4-бензолдикарбоновой) кислотой и этиленгликолем (записать реакцию на доске).
Полученное вещество – полиэтилентерефталат (ПЭТ).
Давайте сами получим сложный эфир. Для этого проведем лабораторную работу по получению уксусноизоамилового эфира (изоамилацетата, изоамилового эфира уксусной кислоты)
Прежде всего нужно вспомнить правила техники безопасности при работе с кислотами и спиртовкой.
Правила техники безопасности при работе с концентрированной серной кислотой:
Наливать кислоту с помощью стеклянной палочки, остерегаться попадания кислоты на кожу, одежду, в глаза.
В случае ожога немедленно сообщить учителю, промыть большим количеством проточной воды, затем обработать раствором питьевой соды.
Правила техники безопасности при работе со спиртовкой:
Зажигать спиртовку спичкой, а не от другой спиртовки.
Не переносить горящую спиртовку с места на место.
Пробирку в держателе закреплять не слишком туго.
Вначале нагревать всю пробирку, а затем ту часть, где находится вещество.
Пробирку направлять не на себя и не на других людей.
Пламя спиртовки гасить колпачком.
Физические свойства сложных эфиров.
Сложные эфиры низших спиртов и низших карбоновых кислот – летучие жидкости с приятным фруктовым или цветочным ароматом, нерастворимые или плохо растворимые в воде с температурами кипения ниже, чем у изомерных карбоновых кислот. Почему? (Между молекулами сложных эфиров и молекулами сложных эфиров и воды не образуются водородные связи.)
Сообщение учащегося об ароматах.
Сложные эфиры высших карбоновых кислот и высших спиртов называются воски. Это твердые, пластичные, легко размягчающиеся вещества, чаще без запаха, обладают водоотталкивающим, смягчающим действием.
Сообщение учащегося о восках.
Применение сложных эфиров:
Из ПЭТ изготовляют пластиковые бутылки, прозрачные пленки, предметы быта. Это термопластичный полимер, который при 1700С переходит в вязкотекучее состояние. Из нитей ПЭТ получают синтетическое волокно – лавсан. Он не подвергается усадке, не боится влаги, устойчив против щелочей, кислот, бактерий, света, имеет высокую прочность на разрыв. Применяется для производства фильтров, войлока, технического сукна, брезентов, транспортерных лент, электроизоляции, тканей, в том числе тюли. Для изготовления тканей его сочетают с хлопком, льном, шерстью. Такие ткани не выгорают, стойки к истиранию и смятию, быстро высыхают. Их нельзя гладить горячим утюгом.
Так как сложные эфиры обладают приятным запахом, они используются в косметической и пищевой промышленности в качестве ароматизаторов.
Многие сложные эфиры применяются в качестве растворителей лаков и красок.
Из восков изготавливают политуры, смазки, пропиточные составы для бумаги (вощеная бумага) и кожи, они входят и в состав косметических кремов и лекарственных мазей.
IV. Рефлексивный тест.
Я узнал(а) много нового.
Мне это пригодится в жизни.
На уроке было над чем подумать.
На все возникшие у меня в ходе урока вопросы я получил(а) ответы.
На уроке я поработал(а) добросовестно и цели урока достиг(ла).
V. Домашнее задание. п.21, упр.3,9,10,11 (учебник О.С.Габриелян. Химия. Профиль. 10 класс.)
infourok.ru
Конспект урока для 11 класса на тему "Сложные эфиры"
Тема урока: «Сложные эфиры. Жиры. Мыла и мыломоющие средства»
Цели урока:
Образовательные - дать учащимся понятие о составе и строении сложных эфиров; отработать умение выделять общие существенные свойства, на основе которых вещества объединяются в класс сложных эфиров, рассмотреть получение и применение сложных эфиров; дать понятие о реакции этерификации.
Развивающие - формирование умений составлять формулы сложных эфиров и называть их, умений составлять уравнения реакций гидролиза и этерификации, развить знания учащихся о закономерностях химических реакций, об условиях смещения химического равновесия; развитие логического мышления, внимания, памяти.
Воспитательные - воспитание познавательной активности, доброжелательности, уважения друг к другу, умения слушать и верно оценивать ответы товарищей, воспитание культуры общения, самостоятельности в приобретении знаний.
Тип урока: изучение нового материала.
Метод урока: словесный и сопутствующий ему наглядный.
Ход урока
I. Организационной момент:
Сообщение темы и плана урока, постановка цели.
Цель: подготовка обучающихся к восприятию нового материала.
Тема и цели урока сообщаются устно, план урока также сообщается устно.
II. Контроль и актуализация опорных знаний обучающихся:
Цель: выяснение уровня знаний, умений навыков, необходимых для восприятия нового материала. Предварительная проверка знаний учащихся об кислородосодержащих соединениях в органической химии.
? Перечислите классы органических веществ, содержащих кислород или кислородсодержащие органические вещества. С какими из них вы знакомы? Приведите примеры.
? Составьте уравнение химической реакции, протекающей при низких температурах, если в реакции участвует избыток этилового спирта. Назовите полученное вещество.
? Какие соединения получаются при взаимодействии спиртов с карбоновыми кислотами? Составьте уравнение химической реакции и назовите полученное вещество.
III. Изучение и усвоение нового материала:
Цель: сообщение обучающимся нового материала.
Изучение нового материала проводится по плану:
Определение сложных эфиров
Номенклатура и изомерия сложных эфиров
Нахождение в природе
Химические свойства сложных эфиров
Области применения сложных эфиров
IV. Закрепление пройденного материала
V. Итоги урока
Сложными эфирами называются органические вещества, которые образуются при взаимодействии кислот со спиртами, идущими с отщеплением воды.
Общая формула: R – C = O
 O – R1, где R, R1 – одинаковые или разные
O – R1, где R, R1 – одинаковые или разные
радикалы углеводородов
Метод меченых атомов:
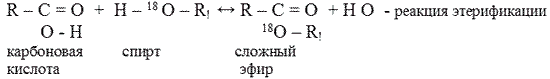
Реакция образования сложных эфиров при взаимодействии кислот и спиртов называется реакцией этерификации.
Этерификации сопутствует обратный процесс – гидролиз сложных эфиров. Он состоит в том, что при взаимодействии сложного эфира с водой снова образуется кислота и спирт. Т. о., данная реакция является обратимой. И, чтобы сместить равновесие в сторону получения сложного эфира, необходимо из реакционной смеси удалять воду. Реакция этерификации, также ускоряется при действии катализаторов – минеральных кислот, например серной.
Номенклатура, изомерия сложных эфиров:
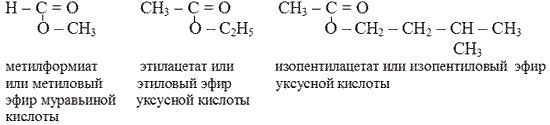
Для сложных эфиров характерна только структурная изомерия (3 её вида):
– изомерия углеродного скелета
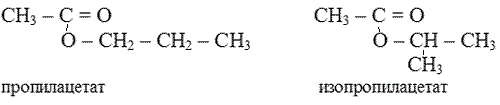
– изомерия положения сложноэфирной группировки

- межклассовая изомерия
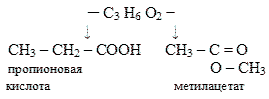
Сложные эфиры – вещества, широко распространенные в природе. Приятные ароматы цветов, плодов и ягод в значительной степени обусловлены присутствующими в них сложными эфирами.
Химические свойства
Характерное химическое свойство сложных эфиров – взаимодействие их с водой (гидролиз). При гидролизе сложных эфиров образуется равновесная смесь эфира и воды с продуктами гидролиза:
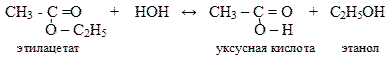
Установление этого равновесия катализируется кислотами.
В щелочной среде реакция также идет быстрее. Гидроксид-ионы не только катализируют гидролиз, но и сдвигают равновесие в сторону образования кислоты и спирта, поскольку образующаяся кислота превращается в соль и выводится из равновесной смеси:
RCO2R1 + h3O 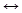 RCO2H + R1OH
RCO2H + R1OH
RCO2H + OH- —> RCO2- + h3O
Таким образом, в присутствии основания реакция гидролиза сложных эфиров доходит до конца:
RCO2R1 + NaOH —> RCO2Na + R1OH
Области применения сложных эфиров
Сложные эфиры применяют для изготовления приятно пахнущих так называемых искусственных фруктовых эссенций.
Их широко используют в производстве фруктовых вод и шипучих фруктовых порошков, кондитерских изделий, а также в парфюмерии.
Многие сложные эфиры используются в производстве пластмасс, взрывчатых веществ, лекарственных препаратов, лаков и синтетических волокон – лавсана и т. д.
Сложные эфиры широко распространены в природе, находят применение в технике и различных отраслях промышленности. Они являются хорошими растворителями органических веществ, их плотность меньше плотности воды, и они практически не растворяются в ней.
Схема. Применение сложных эфиров:
Сложные эфиры с относительно небольшой молекулярной массой представляют собой легковоспламеняющиеся жидкости с невысокими температурами кипения, имеют запахи различных фруктов. Их применяют как растворители лаков и красок, ароматизаторы изделий пищевой промышленности.
Например, метиловый эфир масляной кислоты имеет запах яблок, этиловый эфир этой кислоты — запах ананасов, изобутиловый эфир уксусной кислоты запах бананов.
Сложные эфиры высших карбоновых кислот и высших одноосновных спиртов называют во скажи.
Так, пчелиный воск состоит, главным образом, из эфира пальмитиновой кислоты и мирицилового спирта С15Н31СООС31Н63;
Кашалотовый воск — спермацет – сложный эфир той же пальмитиновой кислоты и ацетилового спирта
С15Н31СООС16Н33.Сложные эфиры часто служат исходными веществами в производстве многих фармацевтических препаратов.
В завершение урока для закрепления изученного материала предлагается осуществить несколько заданий:
Составить уравнения реакций, при помощи которых можно осуществить следующие превращения:
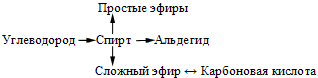
Приведите уравнения реакций получения:
а) этилового эфира муравьиной кислоты;
б) пентилового эфира уксусной кислоты;
в) метилового эфира азотной кислоты.
Итоги урока:
Общая характеристика работы группы, анализ урока: успешность и недостатки, пути их устранения.
Выставление оценок за работу наиболее активных обучающихся.
Задание на дом.
infourok.ru
Конспект лекции по теме "Сложные эфиры, их получение, свойства, номенклатура"
Химия
Лекция
Тема: Сложные эфиры и жиры. Мыла.
Сложные эфиры карбоновых кислот — это соединения, образующиеся при взаимодействии органических кислот со спиртами.
Сложные эфиры, образованные карбоновыми кислотами и одноатомными спиртами, имеют общую формулу:
O
R – C R – COO – R1
O R1
где R и R1 — углеводородные радикалы, одинаковые или разные (исключение — эфиры муравьиной кислоты).
Нахождение в природе и получение. Сложные эфиры широко распространены в природе. Аромат цветов, ягод, фруктов обусловлен присутствием в них тех или иных сложных эфиров:
Запах
Этиловый эфир масляной кислоты
ананаса
Изоамиловый эфир уксусной кислоты
груши
Изобутиловый эфир уксусной кислоты
банана
Метиловый эфир масляной кислоты
яблока
Несмотря на это, сложные эфиры в виде фруктовых эссенций получают путем синтеза, так как выделение их из фруктов цветов сложно в технологическом отношении. В лаборатории получают известной вам реакцией этерификации. Например, при легком нагревании смеси уксусной кислоты и этанола в присутствии небольшого количества концентрированной серной кислоты появляется приятный запах этилацетата — сложного эфира этанола и уксусной кислоты:
О О
СН3 – С + НО – С2Н5 Н2 SO4 t СН3 - С + Н2О
ОН О – С2Н5
этилацетат
Реакция этерификации обратима. Чтобы сместить равновесие этой реакции в сторону образования сложного эфира, согласно принципу Jle Шателье нужно удалять из реакционной смеси один из продуктов реакции (отгонять эфир или связывать воду водоотнимающими средствами). Серная кислота в этой реакции связывает воду и является катализатором.
Физические свойства. Сложные эфиры простейших кислот и спиртов — бесцветные летучие жидкости, малорастворимые в воде, обладают приятным запахом; кипят при более низких температурах, чем соответствующие им кислоты. Это обусловлено отсутствием гидроксильных групп в молекулах сложного эфира, поэтому между молекулами не образуются водородные связи.
Сложные эфиры высших кислот и одноатомных спиртов — воскообразные вещества, например пчелиный воск.
Применение. Благодаря аромату некоторые сложные эфиры используют для приготовления освежающих напитков и фруктовых вод, кондитерских изделий, духов и одеколонов. Этиловый эфир уксусной кислоты и некоторые другие сложные эфиры применяют в качестве растворителей. Некоторые из них используют в медицине (лекарственные вещества — аспирин, салол и др.), в производстве пластмасс (полиметилметакрилат и др.).
infourok.ru
Сложные эфиры
Сложные эфиры – это функциональные производные карбоновых кислот, в которых гидроксильная группа замещена остатком спирта или фенола.
Так, сложный эфир этилэтаноат состоит из остатка карбоновой кислоты – этановой и остатка спирта – этанола. Пропилэтаноат состоит из остатка карбоновой кислоты – этановой и остатка спирта – пропанола.
Сложные эфиры содержат сложноэфирную группу. Для сложных эфиров, как и для карбоновых кислот? можно использовать формулу Cnh3nO2, которая отражает молекулярный состав.
По правилам номенклатуры ИЮПАК при названии сложных эфиров сначала указывают алкильную группу спирта, а потом кислоту, заменяя суффикс -овая- на суффикс -оат-. Кроме этого, допускаются и названия сложных эфиров, когда сначала называется спирт, затем записывают слово «эфир» и далее название кислоты.
Назовём следующие сложные эфиры. Первый эфир называется пропилэтаноат, или пропиловый эфир уксусной кислоты. Второй эфир называется этилметаноат, или этиловый эфир муравьиной кислоты.
Для сложных эфиров возможно существование структурных изомеров. Например, составим структурные изомеры состава С5Н10О2. Это метилбутаноат, припилэтаноат, метил-2-метилпропаноат.
Кроме того, для сложных эфиров характерна межклассовая изомерия с карбоновыми кислотами.
Сложные эфиры, в составе которых низшие карбоновые кислоты и спирты, − летучие, малорастворимые и практически нерастворимые в воде жидкости. Они хорошо растворимы в органических растворителях.
Многие эфиры имеют приятный запах: запах ананаса имеет бутиловый эфир бутановой кислоты, запах груш – изоамиловый эфир этановой кислоты, абрикосами пахнет пентиловый эфир бутановой кислоты, запах жасмина напоминает бензиловый эфир этановой кислоты, запах хризантенм – бензиловый эфир метановой кислоты.
Получить сложные эфиры можно несколькими способами. Например, в реакции карбоновых кислот и спиртов в присутствии минеральных кислот. Так, в реакции уксусной кислоты с этанолом образуется сложный эфир – этилэтаноат, или этиловый эфир уксусной кислоты.
Реакцию образования сложного эфира, как известно, называют реакцией этерификации. Термин «эфир» впервые использовал К. Шееле в конце 18 века.
Сложный эфир можно получить и в реакции глицерина и азотной кислоты, в результате данной реакции образуется тринитроглицерин.
Для сложных эфиров характерны реакции горения. Например, составим реакцию горения метилформиата. При горении образуется углекислый газ и вода.
HCOOCh4 + 2O2 → 2CO2↑ + 2h3O
Важная реакция сложных эфиров – это реакция их с водой в присутствии кислоты или щёлочи. Эта реакция называется гидролизом. Гидролиз – реакция обратная реакции этерификации. Так, в результате гидролиза этилэтаноата в присутствии сильной минеральной кислоты, образуется этановая кислота и этанол. Эта реакция является обратимой.
Ch4COOC2H5 + HOH ↔ Ch4COOH + C2H5OH
В результате щелочного гидролиза этилэтаноата образуется этаноат натрия и этанол. Этот гидролиз необратим и называется омылением.
Сложные эфиры встречаются в виде эфирных масел, жиров, восков.
Воски – это сложные эфиры высших карбоновых кислот и высших спиртов. Пчелиный воск на 70 % состоит из сложного эфира, главным образом, из пальмитиновой кислоты и миристилового спирта. Из воска изготавливают политуры, смазки, пропиточные составы для бумаги и кожи, они входят в состав косметических кремов и мазей.
Сложные эфиры применяют в парфюмерии при производстве духов, в производстве бытовой химии, сложные эфиры составляют основу эссенций для приготовления фруктовых вод, кондитерских изделий, сложные эфиры применяют как растворители органических веществ, при производстве полимерных материалов, в частности пластификаторов, в лакокрасочной промышленности, в производстве искусственных волокон, при производстве лекарственных средств (валидола, аспирина). Сложные эфиры – основа органического стекла.
Таким образом, сложные эфиры – это функциональные производные карбоновых кислот, у которых гидроксильная группа замещена на остаток спирта. Сложные эфиры широко распространены в природе. Сложные эфиры образуются в реакциях между спиртами и кислородсодержащими кислотами. Сложные эфиры гидролизуются растворами минеральных кислот и щелочей. Сложные эфиры применяются во многих областях промышленности.
videouroki.net
Конспект урока по химии "Сложные Эфиры"
Муниципальное бюджетное общеобразовательное учреждение
средняя общеобразовательная школа №8



Подготовила и провела:
Жукова Е.К.
Тема урока: «Сложные эфиры»
Цели урока:
Образовательные - дать учащимся понятие о составе и строении сложных эфиров; отработать умение выделять общие существенные свойства, на основе которых вещества объединяются в класс сложных эфиров, рассмотреть получение и применение сложных эфиров; дать понятие о реакции этерификации.
Развивающие - формирование умений составлять формулы сложных эфиров и называть их, умений составлять уравнения реакций гидролиза и этерификации, развить знания учащихся о закономерностях химических реакций, об условиях смещения химического равновесия; развитие логического мышления, внимания, памяти.
Воспитательные - воспитание познавательной активности, доброже-
лательности, уважения друг к другу, умения слушать и верно оценивать ответы товарищей, воспитание культуры общения, самостоятельности в приобретении знаний.
Оборудование: Образцы сложных эфиров, образцы фруктовых эссенций, карточки для самостоятельной работы учащихся
Тип урока: изучение нового материала.
Метод урока: словесный и сопутствующий ему наглядный.
Дидактическое оснащение: Рудзитис Г.Е., Фельдман Ф.Г., Химия: Органическая химия: Учебник для 10 класса средней школы. М.: Просвещение.

Ход урока
I. Организационной момент:
Сообщение темы и плана урока, постановка цели.
Цель: подготовка обучающихся к восприятию нового материала.
Тема и цели урока сообщаются устно, план урока также сообщается устно.
II. Контроль и актуализация опорных знаний обучающихся:
Цель: выяснение уровня знаний, умений навыков, необходимых для восприятия нового материала.
Предварительная проверка знаний учащихся об кислородосодержащих соединениях в органической химии.
? Перечислите классы органических веществ, содержащих кислород или кислородсодержащие органические вещества. С какими из них вы знакомы? Приведите примеры.
| ? Составьте уравнение химической реакции, протекающей при низких температурах, если в реакции участвует избыток этилового спирта. Назовите полученное вещество. ? Какие соединения получаются при взаимодействии спиртов с карбоновыми кислотами? Составьте уравнение химической реакции и назовите полученное вещество. III. Изучение и усвоение нового материала:Цель: сообщение обучающимся нового материала. Изучение нового материала проводится по плану:
Сложными эфирами называются органические вещества, которые образуются при взаимодействии кислот со спиртами, идущими с отщеплением воды. Общая формула: R – C = O радикалы углеводородов Метод меченых атомов:
Реакция образования сложных эфиров при взаимодействии кислот и спиртов называется реакцией этерификации. Этерификации сопутствует обратный процесс – гидролиз сложных эфиров. Он состоит в том, что при взаимодействии сложного эфира с водой снова образуется кислота и спирт. Т. о., данная реакция является обратимой. И, чтобы сместить равновесие в сторону получения сложного эфира, необходимо из реакционной смеси удалять воду. Реакция этерификации, также ускоряется при действии катализаторов – минеральных кислот, например серной. Номенклатура, изомерия сложных эфиров:
Для сложных эфиров характерна только структурная изомерия (3 её вида): – изомерия углеродного скелета – изомерия положения сложноэфирной группировки
- межклассовая изомерия
Сложные эфиры – вещества, широко распространенные в природе. Приятные ароматы цветов, плодов и ягод в значительной степени обусловлены присутствующими в них сложными эфирами. Химические свойства Характерное химическое свойство сложных эфиров – взаимодействие их с водой (гидролиз). При гидролизе сложных эфиров образуется равновесная смесь эфира и воды с продуктами гидролиза: Установление этого равновесия катализируется кислотами. В щелочной среде реакция также идет быстрее. Гидроксид-ионы не только катализируют гидролиз, но и сдвигают равновесие в сторону образования кислоты и спирта, поскольку образующаяся кислота превращается в соль и выводится из равновесной смеси: RCO2R1+ h3O RCO2H + OH- — RCO2- + h3O Таким образом, в присутствии основания реакция гидролиза сложных эфиров доходит до конца: RCO2R1 + NaOH — RCO2Na + R1OH |
Области применения сложных эфиров

Сложные эфиры применяют для изготовления приятно пахнущих так называемых искусственных фруктовых эссенций.

Их широко используют в производстве фруктовых вод и шипучих фруктовых порошков, кондитерских изделий, а также в парфюмерии.
 Многие сложные эфиры используются в производстве пластмасс, взрывчатых веществ, лекарственных препаратов, лаков и синтетических волокон – лавсана и т. д.
Многие сложные эфиры используются в производстве пластмасс, взрывчатых веществ, лекарственных препаратов, лаков и синтетических волокон – лавсана и т. д.

Сложные эфиры широко распространены в природе, находят применение в технике и различных отраслях промышленности. Они являются хорошими растворителями органических веществ, их плотность меньше плотности воды, и они практически не растворяются в ней.
Схема. Применение сложных эфиров:

Сложные эфиры с относительно небольшой молекулярной массой представляют собой легковоспламеняющиеся жидкости с невысокими температурами кипения, имеют запахи различных фруктов. Их применяют как растворители лаков и красок, ароматизаторы изделий пищевой промышленности.

Например, метиловый эфир масляной кислоты имеет запах яблок, этиловый эфир этой кислоты — запах ананасов, изобутиловый эфир уксусной кислоты запах бананов.


Сложные эфиры высших карбоновых кислот и высших одноосновных спиртов называют во скажи.
Так, пчелиный воск состоит, главным образом, из эфира пальмитиновой кислоты и мирицилового спирта С15Н31СООС31Н63;

Кашалотовый воск —
спермацет – сложный
эфир той же пальмити-
новой кислоты и
цетилового спирта
С15Н31СООС16Н33.
Сложные эфиры часто служат исходными веществами в производстве многих фармацевтических препаратов.


В завершение урока для закрепления изученного материала предлагается осуществить несколько заданий:
Составить уравнения реакций, при помощи которых можно осуществить следующие превращения:

Приведите уравнения реакций получения:
а) этилового эфира муравьиной кислоты;
б) пентилового эфира уксусной кислоты;
в) метилового эфира азотной кислоты.
Итоги урока:Общая характеристика работы группы, анализ урока: успешность и недостатки, пути их устранения.
Выставление оценок за работу наиболее активных обучающихся.
Задание на дом.
kopilkaurokov.ru




 O – R1, где R, R1 – одинаковые или разные
O – R1, где R, R1 – одинаковые или разные







 RCO2H + R1OH
RCO2H + R1OH