Определение - сложный эфир. Определение сложные эфиры
Урок на тему "Сложные эфиры"
Тема урока: Сложные эфирыЦель урока: расширение знаний о кислородосодержащих органических соединениях.
Задачи урока:
Образовательные: дать учащимся понятие о составе и строении сложных эфиров; отработать умение выделять общие существенные свойства, на основе которых вещества объединяются в класс сложных эфиров, рассмотреть получение и применение сложных эфиров; дать понятие о реакции этерификации.
Развивающие: формирование умений составлять формулы сложных эфиров и называть их, умений составлять уравнения реакций гидролиза и этерификации, развить знания учащихся о закономерностях химических реакций, об условиях смещения химического равновесия; развитие логического мышления, внимания, памяти.
Воспитательные: воспитание познавательной активности, доброжелательности, уважения друг к другу, умения слушать и верно оценивать ответы товарищей, воспитание культуры общения, самостоятельности в приобретении знаний.
Оборудование: уксусная кислота, этиловый спирт, спиртовка, химическая посуда, пищевые ароматизирующие добавки, фрукты, цветы, пробники духов, компьютер, проектор, ноутбук.
Ход урока
1. Организационный момент.
Звучит «Вальс цветов» П.И.Чайковского. Демонстрируются слайды с кадрами весны, пробуждения природы.
Учитель. Ребята! Под чарующие звуки этой мелодии представьте себе розу. Можно долго любоваться её красотой, вслушиваться в дыхание её лепестков и листьев, но впечатление будет неполным, если не ощущать аромат царственного цветка.
И только аромат цветущих роз,
Летучий пленник, запертый в стекле,
Напоминает в стужу и мороз
О том, что было лето на земле.
Роза говорила о страстной любви, лилия – о своей непорочности, пышная магнолия втихомолку поведала о чистых радостях святой гордости, а крошечная маргаритка шептала о прелестях простой, укромной жизни.
…Так писала о запахах Жорж Санд в романе «Консуэло»
Мы живем в мире разнообразных запахов и ароматов, они будоражат наше воображение, напоминают о благоухающем саде, цветущем луге и свежести фруктов.
Сейчас вы посмотрели кадры, показывающие красоту и многообразие цветов – этих удивительно красивых и необыкновенно ароматных созданий природы и человека. Они излучают нежные ароматы, которые в жизни растений имеют большое значение. Ароматы цветов привлекают насекомых для опыления, а фруктовые запахи притягивают животных и способствуют распространению семян. У многих из нас самые яркие воспоминания связаны с определенными ароматами. Представьте весну, пробуждение природы. Какие ароматы всплывают в вашей памяти? (ароматы цветущей черемухи, смолянистых тополиных почек, первых весенних цветов).
А что такое запах с химической точки зрения?
Тысячи ароматов дарит нам природа. В школьной лаборатории можно
получить в пробирках вещества, запахи которых напоминают запахи
фруктов и цветов.
Учитель знакомит учащихся с целями урока.
Лабораторный опыт «Определение запаха пищевых добавок и сравнение их с запахом соответствующих фруктов»
На столах у учащихся находятся вещества с различными фруктовыми ароматами. Учащиеся определяют предложенные ароматы, а затем сравнивают их с запахами аналогичных фруктов и ягод. Делают вывод, что ароматы фруктов и предложенные вещества имеют сходные запахи.
Учитель. Ароматические вещества в выданных флаконах получены синтетическим способом, а ароматы фруктов и ягод созданы природой. Несмотря на разное происхождение, они обладают одинаковыми свойствами, а, следовательно, и строением. Цветочно-фруктовые запахи излучают сложные эфиры.
Вы познакомитесь со строением сложных эфиров, способами их получения и применением.
2. Сложные эфиры в природе. История открытия.
Учитель. Много веков назад арабы уже знали различные способы получения душистых веществ из растений и выделений животных. Душистые вещества содержатся обычно в виде капелек в особых клетках. Они встречаются в цветах, листьях, кожуре плодов и даже в древесине. Их называют эфирными маслами. Они представляют собой смеси душистых органических веществ.
В 1759г. Л. Де Лаурагваис перегонял крепкую уксусную кислоту с винным спиртом и получил некоторое количество жидкости, запах которой отличался от запаха исходных веществ. Так впервые был получен сложный эфир. Термин «эфир» впервые применил к синтетическим веществам К.В. Шееле в 1782г.
3. Получение сложных эфиров.
Учитель. Прошло более 200 лет, а способ получения сложных эфиров в принципе не изменился. Сейчас мы с вами получим этиловый эфир уксусной кислоты.
Практическая работа. (Работа по инструктивной карте)
В пробирку нальем 2 мл этилового спирта, 2 мл уксусной кислоты и 1 мл концентрированной серной кислоты. Смесь перемешаем и нагреем не очень сильно в течение 4-5 минут, не доводя до кипения. Затем дадим остыть смеси и выльем ее в пробирку с водой.
Произошла реакция между уксусной кислотой и этиловым спиртом, в результате которой образовались сложный эфир и вода. Такая реакция имеет свое название.
Найдите в учебнике, как называется такая реакция? (этерификации) стр.190
Методом меченых атомов был доказан механизм протекания данной реакции. Оказалось, что молекула кислоты отдает гидроксильную группу, а молекула спирта – атом водорода. Я запишу эту реакцию в общем виде:
R- COOH +R- OH→ R1 – COO – R2 + h3O
А вы запишите реакцию этерификации для уксусной кислоты и этилового спирта.
Следовательно, общая формула сложных эфиров:
R1 – COO – R2
Cn h3nO2
Сложные эфиры предельных одноосновных карбоновых кислот имеют общую формулу:
O
║
Cnh3n+1 – C – O - Cnh3n+1
Сложные эфиры – функциональные производные карбоновых кислот, в молекулах которых гидроксильная группа (-ОН) замещена на остаток спирта (-OR)
4. Номенклатура сложных эфиров.
Учитель. Существуют несколько способов названия сложных эфиров. Наиболее распространены названия, состоящие из четырех слов, например: этиловый эфир уксусной кислоты.
По систематической номенклатуре названия сложных эфиров образуется путем прибавления к названию аниона кислоты приставки с названием УВ радикала спирта. Название аниона кислоты оканчивается на –ат или –оат.
Название сложного эфира

название УВ радикала спирта + название аниона кислоты (-ат)
н-р: C3H7 –COO –Ch4 метилбутират или метилбутаноат
? Составьте формулы и названия сложных эфиров, образованных следующими веществами:
HCOOH и Ch4OH
Ch4COOH и C2H5OH
C2H5COOH и C3H7OH
5.Изомерия и номенклатура.
Для сложных эфиров характерна только структурная изомерия (3 её вида).
1-й вид – изомерия углеродного скелета
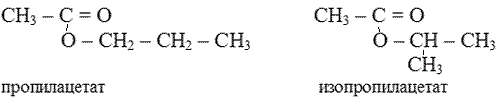
2-й вид – изомерия положения сложноэфирной группировки

3-й вид - межклассовая изомерия:
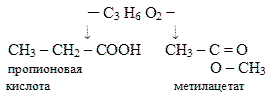
Задание: одинаковые ли формулы изображены?
Ch4-COO-Ch3-Ch3-Ch4 -? Назвать сложный эфир.
Ch4 –COO-CH-Ch4 – назвать сложный эфир.
I
Ch4
Вывод: для сложных эфиров характерна изомерия
углеродного скелета.
Б) Ch4COOC2H5 -? C2H5-COOCh4 -?
Вывод: изомерия положения сложной эфирной группы.
В) Ch4- Ch3 – COOH à C3H6O2 <-- Ch4 –COO- Ch4
Вывод: межклассовая изомерия.
Задание. Напишите формулу сложного эфира изомерного по составу пропионовой кислоте и дайте название:
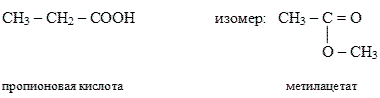
6. Физические свойства
Сложные эфиры низших кислот и низших спиртов – летучие жидкости с приятным запахом, плохо растворимые в воде, но хорошо растворимые в органических растворителях;
Сложные эфиры высших кислот и высших одноатомных спиртов - твердые вещества без запаха
7. Химические свойства эфиров.
? На основании строения сложных эфиров спрогнозируйте, какими свойствами они обладают. (Гидролизуются).
Реакция этерификации в условиях кислотного катализа обратима. Обратный процесс – расщепление сложного эфира при действии воды с образованием карбоновой кислоты и спирта – называют гидролизом сложного эфира.
RCOOR' + h3O (H+)↔ RCOOH + R'OH
Гидролиз в присутствии щелочи протекает необратимо (т.к. образующийся отрицательно заряженный карбоксилат-анион RCOO– не вступает в реакцию с нуклеофильным реагентом – спиртом).
Эта реакция называется омылением сложных эфиров (по аналогии со щелочным гидролизом сложноэфирных связей в жирах при получении мыла).
Учитель. При взаимодействии эфиров с водой образуются исходные вещества – кислота и спирт. Следовательно, гидролиз эфиров – реакция, обратная реакции этерификации.
Резко сожмите кусочек свежей апельсиновой корочки и «выстрелите» капельки клеточного сока на огонь горелки – они ярко вспыхнут.
? Что можно сказать о горючести сложных эфиров.
Генетическая связь.
С2Н4→С2Н5ОН→СН3СОН→СН3СООН→СН3СООСН3
8. Применение сложных эфиров. Из истории сложных эфиров.
(Сообщения учащихся)
Эфирные масла известны с древних времен. 6000 лет до нашей эры в Египте умели получать из растений скипидар и некоторые эфирные масла. Они применялись в основном для УМАСЛИВАНИЯ кожи тела, волос, для религиозных целей, а для запаха - в самую последнюю очередь. Масла стоили дорого и были, естественно, привилегией знати. В Японии более 2000 лет назад не только получали мятное масло, но и выделяли из него ментол. Эфирные масла применяли для благовонных курений, как косметические и лекарственные средства, при Бальзамировании. Масла считались символом божественного проявления и не даром именно маслом мирры "помазывали на царство". Мирра - один из наиболее древних ароматических ингредиентов, которое являет собой желто-коричневую смолу деревьев, произрастающих в Восточной Африке. В отличие от жирных растительных масел эфирные представляют собой многокомпонентные смеси летучих органических соединений (ароматических, алициклических и алифатических карбонильных соединений, спиртов, кислот, эфиров и т.д.), вырабатываемых в особых клетках различных растений и обусловливающих их запах. Конечно, маслами нужно пользоваться очень аккуратно, тем более что практически все масла обладают лечебными свойствами. Масла производились и производятся до сих пор. Они положили начало непосредственно изобретению ТУАЛЕТНОЙ ВОДЫ. Первой ароматической водой на основе спирта и эфирных масел стала "Вода Королевы Венгрии". Создана она была в 1380 году и подарена 70-ти летней королеве неизвестным монахом. Дело в том, что королева была очень больна, но попробовав воду (а ароматические воды еще и пили!) вылечилась от болезни, помолодела и, даже, была просватана королем Польши. Если учесть, что продолжительность жизни в XIV веке составляла в среднем 50 лет, то ароматическая вода совершила поистине великое чудо. Эпоха Просвещения подарила миру новые возможности использования ароматических вод. И если в начале ароматизированные воды и масла использовались в основном как средств гигиены и служения религиозного культа, то с XVII века ароматизация стала самоцелью. До сих пор существуют разные версии происхождения КЁЛЬНСКОЙ ВОДЫ. В XIV веке в монастыре Санта Мария Новелла, что во Флоренции готовили прекрасную лечебную ароматизированную воду "ACQUA REGINA" ("Королевская вода"). Успех ее так велик, что в XIV веке итальянец Джованни Пауло Фемини пускается во все тяжкие лишь бы узнать рецепт этого аромата. Получив рецепт, он начал изготовление воды в Кёльне, где был аптекарем. По началу он дал воде название "Eau de Admirable" ("Чудесная вода"), а несколько позже "Eau de Cologne". Тут-то он и пригласил к себе на службу племянника Джан Мария Фарина, продолжившего дело дяди, и начавшего эпоху "Войны за патент" между семьями Фемини и Фарина. Хотя никакая "война" не помешала им пользоваться славой и популярностью, которую принесла им "Кёльнская вода". Так Жан-Мари Фарина, открыв свое дело в Париже, являлся поставщиком "Кёльнской воды" для Наполеона.
Эфирные масла - бесценный дар природы!
Эфирные масла - бесценный дар природы! Они раздвигают привычные рамки окружающего нас мира, приоткрывают дверь в таинственную страну воображения и фантазии, создают совершенно неповторимое настроение! С букетом чудодейственных свойств ароматных растений человек познакомился уже много тысяч лет назад. Именно они были первыми косметическими средствами, лекарствами, а также снадобьями, которые люди использовали для создания определённой эмоциональной атмосферы, например, праздника или медитации.
Эфирные масла - душистые, легко летучие вещества, содержащиеся в различных частях растений, главным образом в цветах, листьях, плодах, корнях; Эфирные масла легко перегоняются из растительного сырья паром. В настоящее время известно более 2000 эфиромасличных растений. Содержание эфирных масел в растениях зависит от ряда причин и колеблется от 4% до 0,1%
9.Обобщение и выводы.
Синквейн к понятию сложные эфиры
1. Сложные эфиры
2. жидкие, твердые
3. гидролизуются, сгорают, растворяются
4. вещества, обладающие приятным запахом
5. эфирные масла
Домашнее задание.
§ 21 упр. 1,2,3 (упр.11)
А) Задача. При анализе вещества определили, что в его состав
входят: W(C) =40%; W(H) =6.66%; W(O) = 53,34%.
D(в-ва)возд=2.07. Определить молекулярную формулу этого вещества.
Б) С6Н12О2. Составить всевозможные изомеры и назвать по систематической номенклатуре.
.
infourok.ru
Определение сложных эфиров органических кислот
Пластификаторы вводятся в резиновую смесь для уменьшения внутреннего трения в процессе ее переработки (смешения, формования) и для повышения морозостойкости резины. В первом случае они выполняют роль мягчи-телей. В качестве таковых используют нефтяные смолы и масла, каменноугольные смолы, канифоль, сосновую смолу и т. п. вещества. Для повышения морозостойкости вводят сложные эфиры органических кислот (дибутилфталат, дибутилсебацинат и др.). В определенной стенени они одновременно служат и мягчителями. [c.319] Б. Определение сложных эфиров органических кислот [c.166]Комплексный эфир пентаэритрита, дикарбоновой и монокарбоно-вой кислот нашел применение в качестве быстродействующего кои-понента комбинированного ингибитора коррозии для рабоче-консер-вационных масел. Наличие в молекуле органического соединения слоянозфирных групп придает ей быстродействующие свойства - способность вытеснять коррозионно-агрессивный электролит с поверхности металла, предотвращая тем самый коррозию. Введение гидроксильных групп в молекулу сложного эфира повышает его защитные свойства 1.5]. Синтез комплексного эфира пентаэритрита, дикарбоновой и монокарбоновой кислот осуществляется таким образом, чтобы конечный продукт содержал определенное количество гидроксильных групп. Это позволяет использовать его в качестве компонента комбинированного ингибитора коррозии для рабоче-консервационных масел. [c.45]
Анализ углистого остатка после пиролиза показал наличие в нем значительных количеств связанных в виде сложных эфиров органических кислот состава, близкого приведенному в таблице. Определение в этом остатке содержания ароматических веществ не дало положительных результатов. [c.423]
Примером массопередачи, для которой скорость не зависит от интенсивности перемешивания, но зависит от размера поверхности раздела фаз, является взаимодействие некоторых сложных эфиров органических кислот, например этилформиата в I смеси с органическими растворителями, с водным раствором щелочи. Эти реакции используют для определения изменения поверхности эмульсии при изменении интенсивности перемешивания, конструкции аппаратов [9—11]. Их применяют и для оценки влияния интенсивности перемешивания на поверхность раздела фаз в результате волнообразования. Для определения зависимости скорости от размера поверхности целесообразно сравнивать время, за которое перейдет из одной фазы в другую одинаковое количество вещества, но не количество вещества, которое перейдет из одной фазы в другую за одинаковое время. Это следует, например, из уравнения массопередачи в диффузионном режиме с постоянным коэффициентом распределения 1п(С1—С )ЦС —С1р) =—а/, где а — =[KlS Q + )] vq, так как при одинаковом знач и ч приведенного логарифма, но разных значениях 5(8 и 8"), аГ=а"1", откуда 8 Г=8"Г или 8 18"=Г Ц, т. е. время обратно пропорционально поверхности [c.14]
Ассоциация молекул в водной фазе вызывает уменьшение коэффициента распределения при увеличении концентрации металла, ассоциация же в органической фазе—увеличение этого коэффициента. Комплексы металла, имеющего хорошо ассоциирующие частицы, отличаются очень слабой растворимостью в воде, большой—в неполярных растворителях (бензол, четыреххлористый углерод, хлороформ и метилизобутилкетон) и слабой в полярных (спирты, эфиры). Металлы со слабо ассоциированными молекулами особенно хорошо экстрагируются кетонами, простыми и сложными эфирами и другими растворителями типа доноров при добавлении кислот. В таких системах коэффициент распределения увеличивается с повышением количества свободной кислоты, а в некоторых системах имеет максимум при известных ее концентрациях, так как при низких концентрациях из частиц кислоты и экстрагируемого вещества образуется мало комплексов, а при высоких концентрациях количество комплексов сильно увеличивается. Нов некоторых системах при определенной кислотности одновременно начинает расти взаимная растворимость фаз, что может ухудшить коэффициент распределения. [c.425]
Спирты при определенных условиях реагируют как с органическими, так и с неорганическими кислотами с выделением воды, образуя сложные эфиры [c.330]
Производные можно получать для многих классов органических соединений, если предварительно проводить химическое превращение интересующих нас веществ в соединения, способные давать производные. Например, гидролиз сложных эфиров приводит к получению кислот и спиртов. Уменьшение полярности производных по сравнению с таковой в исходном образце приводит к двум важным следствиям менее полярные вещества регистрируются в виде более острых пиков с большим числом теоретических тарелок, у них уменьшается разброс значений к и появляется возможность разделения в изократическом режиме вместо градиентного. У полученных производных выше значения а для выбранных пар веществ. Описаны производные, чувствительность определения которых на электрохимическом детекторе очень высока. Некоторые реагенты, применяемые для получения производных, приведены в табл. 3.2. [c.69]
Сложные эфиры и ангидриды органических кислот мешают определению [c.101]
Наиболее распространенным принципом, лежащим в основе определения органических кислот и ряда их производных, является образование гидроксамовых комплексов железа. В число определяемых соединении входят галогенангидриды и ангидриды кислот, сложные эфиры, нитрилы и др. [c.118]
Летучие кислоты жирного (алифатического) ряда попадают в сточные воды от пирогенного разложения топлива, от производства уксусной кислоты и сложных эфиров, синтетического каучука и т. п. Кроме того, они образуются в сточных водах в результате процесса брожения органических веществ. Метод определения этих кислот состоит в отгонке их из сточной воды после подкисления последней фосфорной кислотой и в титровании отгона едкой щелочью в присутствии фенолфталеина в качестве индикатора. [c.195]
В ре зультате реакции окисления могут образовываться малоустойчивые соединения, являющиеся источниками радикалов, которые в дальнейшем ускоряют эту реакцию. Поэтому при бесконтрольном течении процесса может получиться сложная смесь органических соединений (сложные эфиры, оксикислоты, различные MOHO- и дикарбоновые кислоты и т. д.) и даже продукты горения с образованием двуокиси углерода и воды. Учитывая это, процесс окисления высших алканов проводят при температуре около 150°С в присутствии солей марганца (катализатор). При этом можно добиться получения только одного определенного продукта (с небольшими примесями). Например, при каталитическом окислении высших парафинов нормального строения ( 12 — С25) получают высшие л ирные кислоты (ВЖК) и высшие жирные спирты (ВЖС), представляющие собой весьма ценные продукты, применяемые для производства поверхностно-активных веществ (ПАВ). [c.54]
В случае сильного загрязнения почвы, содержащей помимо ПАУ циклогексанон, ацетофенон, трихлорацетофенон, фталаты, варфарин, 2,4-дихлор-феноксиуксусную кислоту, линдан и другие высокотоксичные ЛОС [63], оптимальным экстрагентом для сложных эфиров и кетонов являются полярные смеси растворителей (вода — ацетон или ацетон — метиленхлорид), обеспечивающие при трехкратной экстракции эффективность извлечения, большую, чем 95%. При этом наилучшее извлечение достигается в системе почва — вода — метиленхлорид (1 2) с использованием вибрационной методики. Последний способ универсален при определении в почвах сложных эфиров, органических кислот и хлоруглеводородов. [c.258]
Взаимодействие аминогрупп кислот с арилсульфокислотами и сложными эфирами органических кислот широко применяется для аналитических и синтетических целей. В частности, как уже указывалось выше, для определения Ы-концевых аминокислот используют реакцию аминогруппы с производным йодфенил-сульфокислоты — п-йодфенилсульфонилхлоридом. При синтезе пептидов для прикрытия свободной аминогруппы очень полезными оказались бензиловые эфиры хлоругольной кислоты (кар-бобензоксихлориды) [c.56]
Новыми восстановителями в органической химии являются нат-рийалкоксигидриды [например, ЫаА1(ОС2Н5)зН], которые восстанавливают многие альдегиды, хлорангидриды, сложные эфиры, ангидриды кислот, нитропроизводные и галогениды. При определенных условиях ароматические нитрилы восстанавливаются до соответствующих альдегидов. [c.188]
Групповой состав нефтяных КС весьма разнообразен в различных нефтях и нрямогонных нефтяных дистиллятах обнаружены карбоновые кислоты, фенолы, простые и сложные эфиры, кетоны, лактопы, амиды, ангидриды и некоторые другие классы кислородсодержащих веществ. Наиболее распространенными в сыры нефтях считаются КС кислого характера, в первую очередь кислоты и фенолы, общее содержание которых принято косвенно выражать в форме так называемого кислотного числа (количества мг КОН, расходуемого на титрование 1 г вещества). Обобщение приведенных в работах [410—413, 416 и др.] результатов определения кислотных чисел (более 460 анализов) показывает, что средняя органическая кислотность сырых нефтей закономерно сни- жается о увеличением возраста и глубины залегания (табл. 3.3 [c.87]
Фторсодержащие полимеры, например политрифторхлорэтилен, ограниченно растворяются и набухают в хлорированных и особенно фторированных соединениях. Для определения вязкости и других свойств этих полимеров используются 1,1,3-трифториентахлорпропан, хлорбен-зотрифторид, дихлорбензотрифторид и другие соединения. Для политетрафторэтилена долгое время не могли найти сколько-нибудь подходящего органического растворителя. Недавно была показана возможность частичного растворения этого прочнейшего пластика во фторированных керосинах при высокой температуре и под давлением. Некоторые фторпласты, например сополимер трифторхлорэтилена и винилиденфторида, растворяются в ацетоне и в сложных эфирах карбоновых кислот. [c.52]
Область двойной связи 1430-1950 см (5,1-7 мкм). Самыми распространенными и характеристичными группами с двойной связью являются карбонильные. Вероятно, они наиболее изученный класс групп, поглощающих в ИК-области. В то время как некоторые структуры можно отличить просто по положению полосы валентного колебания С=0, другие в силу совпадения частот однозначно можно отнести, только прибегая к помощи других областей спектра. Как уже отмечалось, органические кислоты и обычно альдегиды легко идентифицируются по полосе поглощения карбонильной группы и по поглощению групп ОН или СН. Сложные эфиры кроме полосы валентных колебаний С=0 имеют сильное поглощение С—О—Я около 1200 СМ . В кетонах также проявляются полосы средней интенсивности около 1000-1370 см . Сильное поглощение в интервале 1540-1650 см (6,1—6,5 мкм) может указьшать на ионизированную карбонильную группу (например, в металлосодержащих солях органических кислот), на плоскостные деформационные колебания НН в аминах, валентные колебания N=0 в нитратах или валентные колебания С=0 в амидах. Для определения природы поглощения здесь опять необходимо рассмотреть другие спектральные области. Поглощение, обусловленное валентными колебаниями С=С в алифатических соединениях, находится в области 1630—1690 см (5,9 —6,1 мкм), если только к одному или обоим атомам углерода не присоединен атом фтора. В этом случае поглощение смещается в область более высоких частот и число атомов фтора коррелирует с положением полосы. Более тяжелые галогены понижают эту частоту, так как в валентном колебании С = С участвует также некоторая доля деформационного колебания СН. Ценная структурная информация может бьггь получена из положения этой полосы и полосы внеплоскостных деформационных колебаний в области 800-1000 см (10-12,5 мкм) [217]. В ароматических соединениях с малой степенью замещения наблюдаются три (а при лучшем разрешении четыре) резкие полосы в области 1450 — 1650 см (6—7 мкм). Этим полосам сопутствует более слабое поглощение около 1000 — 1200 см (8,3 — 10 мкм) и характеристические внеплоскостные деформационные колебания С—И около 670-900 см (11-15 мкм). Высокозамещенные ароматические соединения имеют [c.188]
Большой интерес представляют работы, в которых было показано, что в определенных условиях может проявляться взаимное усиление смазочного действия полиорганосилоксанов, с одной стороны, и низкомолекулярных углеводородов [2], сложных эфиров двухосновных кислот [23—25] и нефтяных масел [26, 27], с другой. Эти смеси отличаются высокой приемистостью по отношению к противоизносным присадкам [26]. Для объяснения резко выраженного синергизма смазочного действия полиоргано-хилоксанов и органических соединений, в частности углеводородов, была высказана следующая точка зрения [28]. Под влиянием полиорганосилоксанов происходит такое модифицирование поверхности стали, при котором на ней образуется слой повышенной твердости, в результате чего при отсутствии мягкого покрытия условия трения ухудшаются. При определенных концентрациях полиорганосилоксанов в органических соединениях и при прочих благоприятных условиях на поверхности стали при граничном трении может образовываться твердый подслой, насыщенный кремнием с мягким покрытием (например, из РеО), что обусловливает высокие антифрикционные и противоизносные характеристики данного сочетания пары трения со смазочным материалом. [c.156]
Таким образом, вода и водные растворы непригодны как растворители для двуокиси селена при определении этого соединения в пылях свинцового производства. В этом случае необходимо применить органический реагент, который не взаимодействовал бы с другими компонентами пыли. Таким растворителем является метиловый спирт, который дает сложный эфир селенистой кислоты — диметилселенит [c.218]
Фтористый водород обладает способностью катализировать органические реакции различного типа. Поэтому известные в настоящее время реакции, катализируемые фтористым водородом, распределены по отдельным группам. Отнесение данной реакции к определенной группе не всегда может быть решено однозначно. Поэтому некоторые реакции читатель неожиданно для себя сможет найти не под тем заголовком, под которым он будет их искать. Фтористый водород катализирует многие реакции, в которых реагентом являются углеводороды. Под действием фтористого водорода целый ряд веществ вступает в реакцию с ароматическими углеводородами к таким веществам относятся олефины, галоидные алкилы, спирты, меркаптаны, эфиры, карбоновые кислоты, галоидангидриды кислот, сложные эфиры, серная кислота, азотная кислота, окись углерода и кислород. Алифатические углеводороды также служат реагентами в некоторых реакциях. Изопарафины являются более реак-ционноснособными соединениями, чем насыщенные парафины с прямой цепью, но даже последние реагируют при некоторых условиях. [c.229]
Представляет также интерес известный метод колориметрического определения липолитической активности ферментов по расщеплению сложных эфиров фенола и различных органических кислот (фенилбен-зоата, фенилацетата и др.). Фенол, освобождающийся при ферментативном гидролизе, легко можно определить колориметрически. Этот метод отличается исключительно высокой чувствительностью и позволяет вести определение липаз в микроколичествах. [c.76]
Более простым, а в ряде случаев, видимо, и более точным является гравиметрический метод определения суммарного содержания фенолов. Последние в данном методе выделяют раствором щелочи и после подкисления экстрагируют эфиром. После сушки и отгонки эфира фенолы взвешивают. Содержащиеся в пробе органические кислоты предварительно удаляют действием бикарбоната натрия. Метод предпочтителен для анализа сложных фенольных смесей, так как бромометрический и колориметрические методы в этом случае дают значительные ошибки первый — в результате протекания побочных реакций присоединения брома и образования высокозамещенных продуктов второй — в результате зависимости интенсивности окраски не только от количества, но и от строения фенолов. Это подтверждают недавно полученные Тилеманном данные [55] по анализу смесей ксиленолов. [c.49]
За последние годы достигнуты определенные успехи в синтезе особо специфичных ионитов, в структуре которых содержатся функциональные группы комплексообразователей или оса-дителей, а также жидких ионитов, представляющих собой растворы электролитов в органическом растворителе. Так, растворы аминов с достаточно длинной цепью (обычно 18—27 атомов С) в хлороформе, бензоле, нитробензоле и других органических растворителях обладают анионообменными свойствами. Кислоты, нерастворимые в воде, но растворимые в органических растворителях, не смешивающихся с водой, могут быть исходным материалом для изготовления жидких катионитов. Пример тому —сложные диалкиловые эфиры фосфорной кислоты и мо-ноалкиловые эфиры алканфосфоновых кислот (с общим числом атомов С 10—17). [c.670]
Мочевппа образует комплексы только с соединениями нормального или весьма слабо разветвленного строения [88]. Эти соединения включают парафиновые углеводороды, органические кислоты, сложные эфиры, кетоны и ненасыщенные углеводороды. В зависимости от типа или физического состояния соединений для образования комплексов требуется определенная минимальная длина цепи. Для образования комплексов с углеводородами (по крайней мере при атмосферном давлении) последние должны содержать не менее шести углеродных атомов в молекуле. Из карбоновых кислот способны образовать комплексы только кислоты среднего и высокого молекулярного веса, начиная с масляной. В то же время даже низший кетон (ацетон) легко образует комплекс с мочевиной. По мере увеличения длины цени связываемого соединения образование комплексов облегчается, а стабильность их возрастает. Так, если количество раствора мочевины недостаточно для реакции со всем цетаном и гептаном, содержащимися в смеси, то мочевина избирательно взаимодействует с цетаном, в результате чего содержание цетана в комплексе выше, чем н-гептана. Это позволяет фракционировать соединения нормального строения при помощи мочевины [84]. [c.63]
Соли четырехвалентного церия, например желтый концентрированный раствор гексанитроцерата, при добавлении этиленгликоля окрашиваются в красный цвет. Но метод малочувствителен и неселективен, так как такую же реакцию дают алифатические спирты п простые эфиры гликолей. Альдегиды, кетоны, органические кислоты и сложные эфиры не мешают определению [2, с. 291]. Этот колориметрический метод применяют для определения в реактивном топливе метилового эфира этиленгликоля, являюш,егося присадкой, предотвраш,аюш,ей образование льда [3]. [c.335]
Душистые вещества — органические соединения, обладающие характерным приятным запахом, применяют в производстве различных парфюмерных и косметических изделий, мыла, пищевых и других продуктов для придания им определенного запаха. Д. в. широко распространены в природе. Они находятся в эфирных маслах, душистых смолах и других сложных смесях органических веществ, выделяемых из природных продуктов как растительного, так и животного происхождения. Многие Д. в. получают синтетически. Первыми были синтезированы ванилин, индол и др. Практическое применение нашли эфиры уксусной, валериановой, салициловой, антраниловой, коричной и других кислот. [c.50]
Сложные эфиры, ангидриды и лактоны предварительно гидролизуют на холоду или при кипячении известным количеством щелочи, после чего избыток щелочи оттитровывают стандартным раствором кислоты. Подробное обсуждение метода можно найти в соответствующих главах книги Митчелла и др. Органический анализ [165]. Об определении аминокислот см. раздел, написанный Ротом в книге Губен — Вейля Методы органической химии [166]. [c.45]
Число гидроксильных групп, содержащихся в органическом соединении, может быть установлено путем количественно го элементарного анализа тех же производных, которые применялись при качественном определении для этого наиболее пригодны сложные эфиры (стр. 17). Если эфиры содержат азот, как напри.мер уретаны (стр. 28) и их производные, или эфиры нитробензойной кислоты, то часто можно ограничиться только определением азота точно так же достаточно определить содержание галоида в галоидосодержащих соединениях, как например зфирах бромбензойной кислоты или серы в содержащих серу сложных эфирах (стр. 22). В уретанах, полученных с помощью хлорангадрида карбаминовой кислоты, можно определить азот в виде аммиака путем отщепления его щелочью [c.58]
На основании сказанного выше перхлораты можно разделить на две группы 1) более чувствительные и 2) менее чувствительные к нагреванию и удару. В группу менее чувствитатьных (качественное определение) включают чистый перхлорат аммония, перхлораты щаточных и щелочноземельных металлов и перхлорилфторид. К более чувствительным соединениям относятся чистые неорганические азотсодержащие перхлораты, перхлораты тяжелых металлов, перхлораты фтора, органические перхлораты, сложные эфиры перхлоратов, смеси перхлоратов с органическими веществами, тонко раздробленными металлами или серой. Попытка создать более точную классификацию перхлоратов по степени их опасности не может увенчаться успехом на основе имеющихся немногочисленных данных. Каждую систему перхлоратов нужно оценить отдельно е[ тщательно. Однако интересно подумать над возможностью создания по крайней мере полуколичественно зависимости между стабильностью чистых перхлоратов и их строением, как было предложено для хлорной кислоты . [c.214]
Было установлено, что органические соединения многих классов, именно кислоты, высшие спирты, амины, высшие сложные эфиры, простые эфиры, углеводороды, насыщенные кетоны и нитрилы, не оказывают влияния на анализ а-эпоксидов методами, основанными на гидрохлорироваиии. Можно ожидать, что нерастворимые в воде вещества будут снижать результаты определения гидрохлорированием в водном растворе хлорида магния тех эпоксипроизводных, которые трудно переходят в водный слой. [c.248]
Кулькес [56] использовал реакцию ацетиленовой тройной связи с ацетатом ртути для определения некоторых двузамещенных ацетиленовых соединений. Ацетат ртути предпочтительно присоединяется к тройной связи, и избыток ацетата определяют, прибавляя хлорид натрия и титруя высвободившуюся уксусную кислоту. Этот метод достаточно быстрый, однако анализу мешают примеси, реагирующие с ацетатом ртути этиленовые соединения и неорганические и некоторые органические галогениды, комплексно связывающие ион ртути. Ряд органических соединений, например сложные эфиры и сульфонаты, образует выпадающие в осадок вещества, другие же окисляются ионом ртути. [c.362]
Из сложных эфиров а, Р-непредельных кислот определенное значение в качестве мономера имеет метиловый эфир метакри-ловой кислоты (метилметакрилат). Он полимеризуется по той же схеме, что и акролеин и акрилонитрил. Получаемый из него полимер-плексигласс К[—СНз—(СНз)С(СООСНз)—] находит самое разнообразное применение, начиная с консервирования биологических препаратов и кончая изготовлением покрытий, органических стекол, а также бытовых и промышленных изделий. [c.387]
К классу неионогенных ПАВ относятся группы сложных по химическому составу и с широкой областью изменения молекулярных масс соединений, такие, как оксиалкилированные жирные спирты, кислоты, амины, алкилфенолы, алкилтиоэфиры, смешанные оксиэти-лен-оксипропиленовые соединения, а также алканоламиды жирных кислот, сложные эфиры многоатомных спиртов и жирных кислот и др. В связи с этим кроме характерных для анионоактивных и катионоактивных ПАВ качественных и количественных определений основных групп органических соединений, побочных продуктов, пепрореа-тировавших веществ и фракционного состава углеводородных частей для неионогенных ПАВ на основе продуктов оксиалкилирования важную роль играют и некоторые другие определения. К ним относятся определения молекулярно-массового распределения, соотношения и количества присоединенных оксиэтильных и оксипропильных групп в основных продуктах и продуктах побочных превращений (полигликоли). [c.209]
Практическое применение метода к определению воды. Реактив Фишера может быть применен непосредственно для определения воды в самых разнообразных органических соединениях в том числе в предельных и непредельных углеводородах, спиртах, галоидных соединениях, в кислотах и ангидридах кислот, в простых и сложных эфирах, аминах, амидах, нитрозо-и нитросоединениях, в сульфидах, гидроперекисях, диалкилпере-кисных соединениях и т. д. [c.460]
Пептен-2 образуется при производстве дивинила по способу Лебедева в качестве побочного продукта [70] и пока не нашел рационального использования. Поэтому изучение реакции алкилирования им органических кислот представляло не только определенный теоретический интерес, но и имело целью выяснить возможность практического использования его для получения сложных эфиров. [c.333]
Органическое соединение диспергировалось в агаровой питательной среде с добавкой минеральных солен. Содержание углерода в питательной среде было у каждого соединения 0,8%, pH = 6,4 и заметно не изменялось при добавлении сложных эфиров или спиртов. Однако органические кислоты значительно снижали pH питательной среды. Органические кислоты определялись также в питательной среде и корректировались едким натром до pH = 6,4. Питательная среда (налитая в чашки Петри), содержащая испытуемое органическое соединение, засевалась суспензией спор и инкубировалась при 29 1° С в течение 2 недель, не менее. Для каждого соединения определялась его устойчивость к 24 индивидуальным видам плесеней родов Aspergillus, Peni illium и др. Для каждого соединения была рассчитана средняя величина из 24 диаметров колоний, найденных для каждого индивидуального испытываемого организма. Определенные таким путем средние размеры диаметров для всех соединений лежат в пределах О—6,8 см. Эти величины не были включены непосредственно в табл. 31, но оценивались следующим образом. Диаметр колонии О оценивался как степень роста 0 0,1—1 см — как 1 1,1 — 4,0 см — как 2 4,1 — 6,8 см — как 3 а свыше 6,8 см — как 4. [c.112]
chem21.info
Эфиры сложные гликолей, определение - Справочник химика 21
Преимуществом метода является его специфичность на первичные и вторичные ОН-группы и применимость к водным растворам. Кетоны, альдегиды, сложные эфиры и фенолы не мешают определению. Точность определения + 1% (отн.) при содержании гликоля до 0,3%. Гликоли, содержащие третичные ОН-группы, количественно этим методом не определяются. Амины, меркаптаны, эпоксиды и легко гидролизующиеся сложные эфиры (например, формиаты) определению мешают. [c.338] Для обнаружения и количественного определения всех этих соединений используют свойства группировки сложного эфира. Эта группировка придает всем соединениям этого класса, и в особенности некоторым из них, своеобразный характерный запах, который легко отличить от запахов соединений всех остальных классов. По запаху можно часто установить присутствие и приблизительное количество отдельных эфиров в смесях со многими другими растворителями. Только сложные эфиры простых эфиров гликолей не всегда удается обнаружить из-за их слабого запаха, который иногда маскируется запахом сильно пахнущих кетонов и загрязненных углеводородов, маскирующих запах даже более пахучих сложных эфиров. Сложные эфиры определяют прежде всего по их способности к омылению щелочами. Эта реакция настолько надежно доказывает их присутствие (включая лактоны) в смесях растворителей, что можно отказаться от более сложных способов обнаружения сложных эфиров. [c.947]Существует определенная связь между химическим строением и свойствами поверхностно-активных веществ — эмульгаторов. Так, соли карбоновых кислот (растворимые в воде) со щелочными металлами, аммиаком или аминами обычно способствуют образованию эмульсий типа масло в воде, а их кальциевые, магниевые или алюминиевые соли — эмульсий типа вода в масле. Сложные эфиры жирных кислот с полиспиртами (гликолями) также способствуют образованию эмульсий типа вода в масле. [c.336]
На основании изучения кинетических закономерностей термического разложения, а также определения механизма этого процесса для сложных эфиров алифатических моно- и дикарбоновых кислот и спиртов или гликолей, ароматических дикарбоновых кислот и спиртов установлено, что до 200 °С разложение сложных эфиров незначительно [51—53, 57]. [c.103]
Специфические реакции на эфиры гликолей, по-впдимому, отсутствуют. Простейшей качественной пробой на эфир гликоля, а именно на ОН-группу, является реакция с металлическим натрием. Определению мешают вода, спирты и сложные эфпры оксикислот. В случае сложной смеси рекомендуется вначале провести разделение на индивидуальные компоненты, например, ректификацией. Выделенные простые моноэфиры гликолей можно идентифицировать по температурам плавления соответствующих эфиров аллофановой кислоты или инструментальными методами [5, с. 941]. Эта реакция используется для определения простых моноэфиров гликолей колориметрическим методом, например метилового эфпра этиленгликоля, применяемого в качестве присадки, предотвращающей образование льда [5]. [c.336]
В простейших реакциях конденсации, рассмотренных в гл. П, две молекулы реагируют с отщеплением небольшой молекулы, например молекулы воды. Для простых реакций конденсации между одноосновными кислотами и одноатомными основаниями типичным является образование сложного эфира НСООН. Если реагирующие молекулы бифункциональны или содержат большее число групп, то в молекуле продукта сохраняются активные группы и оп может подвергаться дальнейшей конденсации. В результате часто получается линейный полимер, как в случае полиэфиров двухосновных кислот и гликолей, который имеет определенную повторяющуюся группу и характерную связь —СО—О— между группами. Для соединений с большим числом функциональных групп, например полиэфиров глицерина или фенол-формальдегидных полимеров, продукты реакции часто представляют нелинейные полимеры. При поверхностном рассмотрении эти повторяющиеся линейные и нелинейные процессы конденсации напоминают соответственно неразветвленные и разветвленные цепные реакции, но они таковыми не являются. Они протекают как непрерывный ряд аналогичных взаимодействий между исходными реагентами и по мере протекания реакции с продуктами реакции. Сначала образуется некоторое количество димеров , затем эти димеры реагируют с мономерами и другими молекулами димера , образуя большие молекулы, и т. д. Средняя степень полимеризации возрастает со временем сначала медленно, а затем очень быстро, пока не образуется несколько [c.393]
Этим методом можно обнаружить минимум 2 мг воды. Для того чтобы можно было открыть таким образом 0,02% влаги, при анализе инертных растворителей (как углеводороды, простые и сложные эфиры и кетоны) допускается брать для определения пробы величиной до 10 г. При анализе спирта или какого-нибудь другого активного материала нельзя брать больше 1 е пробы, а в тех случаях, когда анализируют метиловый спирт, гликоль или глицерин, величина навески не должна превышать 0,5 г. [c.265]
Помимо остаточных мономеров, определенное значение в механизме сенсибилизирующего действия полимерных материалов могут иметь и вспомогательные химические соединения, выполняющие различную функциональную роль на стадиях их синтеза и переработки — сложные эфиры на основе гликолей, фталевый и малеиновый ангидрид, триэтаноламин, канифоль, различные эмульгаторы и т. д. [И9]. [c.135]
Нитроцеллюлоза выпускается нескольких сортов с различным содержанием азота, что и предопределяет ее растворимость. Сорта с низким содержанием азота растворимы в спирте или в смеси спирта с углеводородами, в то время как сорта с высоким содержанием азота растворяются лишь в кетонах, сложных эфирах и простых эфирах гликолей. Каждый сорт нитроцеллюлозы с определенным содержанием азота может быть нескольких типов, различающихся по молекулярному весу и вязкости в стандартных растворах, причем с увеличением вязкости свойства получаемой пленки улучшаются. [c.287]
Нитроцеллюлозные лаки (нитролаки) готовят на обезвоженном коллоксилине, содержащем около 30% спирта. Наиболее употребительными растворителями являются кетоны (ацетон, метилэтилкетон), сложные эфиры (этилацетат, бутилацетат, эфиры гликоля), спирты (этиловый, бутиловый). Для снижения стоимости лаков в состав их вводят так называемые разбавители (бензол, толуол, ксилол), которые хотя и не растворяют коллоксилин, но при определенных соотношениях с растворителем не вызывают высаживания нитроцеллюлозы из раствора. [c.781]
Свойства смазок проявлять эффективность при высоких нагрузках обычно обусловлены наличием присадок осерненных масел, причем, как известно из практики, в различных типах смазочных составов этот эффект в определенных пределах пропорционален содержанию связанной с маслом серы. Были разработаны различные приемы повышения содержания серы в режущих жидкостях без уменьшения устойчивости смесей [87], в частности использовались тиофосфаты и сходные с ними другие соединения фосфора и серы [88]. Смазочное действие некоторых эмульсионных смазочно-охлаждающих жидкостей зависит от присутствующих в них некомпаундированных масел или специальных эмульгаторов. Большинство рецептур, в которых не используются осерненные или хлорированные масла, включают ряд других веществ, также модифицирующих поверхность раздела металл—жидкость. К ним относятся высшие жирные спирты [891, сложные эфиры высших жирных кислот и гликолей и смешанные эфиры, содержащие низшие оксикарбоновые кислоты [901. Консистентные смазки на основе бентона, длинноцепочечные амины или комплексы четвертичных аммониевых соединений с бентонитом, [c.445]
Соли четырехвалентного церия, например желтый концентрированный раствор гексанитроцерата, при добавлении этиленгликоля окрашиваются в красный цвет. Но метод малочувствителен и неселективен, так как такую же реакцию дают алифатические спирты п простые эфиры гликолей. Альдегиды, кетоны, органические кислоты и сложные эфиры не мешают определению [2, с. 291]. Этот колориметрический метод применяют для определения в реактивном топливе метилового эфира этиленгликоля, являюш,егося присадкой, предотвраш,аюш,ей образование льда [3]. [c.335]
Сабете 116] предложил для характеристики спиртов так называемое число тритилирования , которое указывает количество спирта в процентах, превращающегося в эфир трифенилкарбинола в известных условиях. Реакция осуществляется в обычном приборе Цейзеля, из которого изъят ненужный в данном случае поглотитель с фосфором. Степень тритилирования вычисляется по количеству выделяющегося при реакции хлористого водорода. Было найдено, что в среднем первичные спирты тритилируются на 90—95%, вторичные— на 2—40% и третичные—на 1—5%. Фенолы вступают в реакцию на 10—25%. Гликоли тритилируются в первую очередь по первичной спиртовой группе. Сложные эфиры не мешают определению. [c.58]
Смесь цис- п /гаракс-изомеров циклических диолов проанализирована на основе реакции с борной кислотой — последняя реагирует только с цис-гидроксильными группами [17]. Количественное определение простых моноэфиров гликолей основано главным образом на реакциях ацилирования и осуществляется так же, как и анализ гликолей. Сложные эфиры гликолей определяют качественно и количественно гидролизо.м щелочалш. После гидродиза раствор титруют соляной кислотой в присутствии фенолфталеина уменьшение содержания щелочи пропорционально количеству сложного эфира в пробе. Параллельно проводят холостой опыт [4, р. 981]. [c.340]
Было найдено, что карбоновые кислоты, сложные эфиры и одноатомные спирты не оказывают влияния на определение альдегидов (табл. 2.11). Полигидроксильные соединения мешают анализу, однако это затруднение можно обойти, отделяя альдегид от гликоля перегонкой с водяным паром и затем определяя альдегид в дистилляте. Присутствие ацеталей вызывает завышенный результат на 0,04—2,2% (в пересчете на ацетальдегид). а-Эпоксидь>1 были исследованы на примере пропиленоксида, помех не наблюдалось. [c.105]
Определение анилина служит примером анализа с химическим превращением анализируемого компонента в определяемую форму. В этом случае сначала титрованием находят общее содержание оснований, затем в отдельную пробу вводят салициловый альдегид, который с анилином образует нетитрующееся в смеси гликоля и изопропанола основание Шиффа, и определяют остаточную основность. По разности между суммарным содержанием оснований и остаточной основности находят содержание анилина. Определение этанола в смеси с анилином, этиланилииом и диэтил-анилином является примером анализа с химическим превращением и анализируемого компонента, и примеси, причем продукт превращения основного компонента определяется в присутствии продукта превращения примеси. Этанол можно определять ацетилированием, но мешают анилин и моноэтиланилин. Пробу обрабатывают уксусным ангидридом. Спирт превращается в сложный эфир, а оба амина — в соответствующие анилиды. Затем эфир количественно омыляют щелочью, при этом анилиды заметно не реагируют. [c.619]
Несульфированные образцы обычно определяют экстракцией, гравиметрически или газовой хроматографией по внутренним стандартам. Примеси сульфированного этиленгликоля могут быть определены последовательным анионным и катионным обменом для удаления сульфат- и хлоридионов, помимо сульфированного полиэтилен-гликоля. Для определения уровня содержания сульфированного полиэтиленгликоля сульфат- и хлоридионы вычитаются из общего объема титрования [24]. В случае сложных эфиров сульфосукцинатов содержание их может быть определено растворимой в спирте фракцией или по титрованию сульфонатов. [c.127]
Амиды и эфиры определяют омылением (кипячение или выдерживание с р-рами КОН в воде или диэтилен-гликоле) с последующим титрованием избытка КОН. Для повышения растворимости эфиров и амидов к воде можно добавлять изопропиловый спирт. При определении этим методом сложных ви1шловых эфиров рекомендуется добавлять фенилгидразин во избежание побочной реакции между образующимся альдегидом и едким кали. Амиды, сложные эфиры и др. производные м. б. также гидролизованы к-тами. [c.511]
Таким образом, в исследованных условиях второй компонент лактона не подвергается гидрированию. Этот факт, отрицательный с точки зрения препаративной цели данной работы, позволяет сделать уточнение структуры второго компонента. Исходя из общих представлений о каталитическом гидрировании сложных эфиров [7—9] и предположения, что затруднения гидрированию вызываются экранированием группировки С = 0 заместителями кольца, можно заключить, что негидри-рующийся изомер имеет структуру 1в, т. е. является 2,4-г мс-диэтил-З-7 раис-м-пропилпентанолидом-5. lia рис. представлен выход гликоля в зависимости от объемной скорости гидрирования. Если экстраполировать выход гликоля на нулевую объемную скорость (пунктиром), то можно ориентировочно оценить количество иегндрнрующегося изомера при бесконечно большом времени контакта. Оно составляет около 25%, что соответствует определению методом ГЖХ [2]. [c.53]
Они могуг быть получены в результате взаимодействия жирной кислоты с окисью этилена, окисью пропилена или их смесью [13] при повышенном давлении тем же способом, как и полиоксиэтиленовые эфиры. Обычно их получают посредством этерификации жирной кислотой предварительно полученного полиэтиленгликоля. В США для этого используют полиэтиленгликоли определенного молекулярного веса [14]. При этой реакции, наряду с нужным моноацилированным соединением, в качестве примеси образуется некоторое количество диацилировапного полигликоля, тогда как взаимодействие с жирной кислотой окиси этилена приводит к образованию исключительно моно-ацилированных соединений. Сложные эфиры жирных кислот и поли-гликолей ведут себя аналогично соответствующим простым эфирам [c.204]
Другая группа синтанов—на основе сульфохлоридов—была получена прямым сульфохлорированием насыщенных углеводородов, образовавшихся при гидрировании одной из фракций синтетического топлива. Подобные продукты, полученные из определенной фракции неочищенной пенсильванской нефти методом Рида, оказались вполне пригодными для производства замши и белой кожи [11]. Механизм взаимодействия алкилсульфонилхлорида с гольевым порошком изучал Паттерсон [121. Дубильные свойства синтанов, содержащих алкилсульфокислотные радикалы или радикалы сульфохлорида, могут быть улучшены путем обработки продуктом конденсации гликоля и окиси этилена. Аналогичные вещества были получены из продукта взаимодействия формальдегида с нафталинсульфокислотой путем превращения его в соответствующий сульфохлорид, образующий затем сложный эфир с полигликолем. Известно, что такие синтаны особенно пригодны для обработки голья с целью получения белой, мягкой, плотной и прочной замшевой кожи [13]. [c.467]
Другим типом металлооргапического производного, способного в определенных условиях разлагаться на свободные радикалы, является тетраацетат свинца . Хорошо известная реакция, в которой тетраацетат свинца на холоду разрушает вицинальные гликоли, представляет, но-видимому, полярный процесс паиболее 1 ороятным промежуточным продуктом этой реакции является циклическни сложный эфир [315]. С другой стороны, Фи.зер установил, что нафтохиноны [316] и нитробензо.лы ]317] метилируются при кипячении с тетраацетатом свинца в уксусной кислоте. Наиболее вероятным сле- [c.421]
chem21.info
Определение - сложный эфир - Технический словарь Том III
Определение сложных эфиров по стандартам разных стран основано на реакции омыления их едким натром. Сложные эфиры представляют собой соединения, в которых атом кислорода связан с одним спиртовым остатком ( алкилом) и одним кислотным остатком. По внешнему виду формулы их строение имеет сходство со строением солей, в которых место металла занимает углеводородный радикал. Определение сложных эфиров в присутствии альдегидов, Отч. Определение сложных эфиров бензодиазепина для изучения фар-макокинетики при использовании электронно-захватного детектора и детектора с многоканальной регистрацией ионов. Определение сложных эфиров карбоновых к-т основано на их гидролизе р-ром щелочи, избыток к-рой оттитровывают р-ром к-ты. Малые кол-ва сложных эфиров обычно определяют спектрофотометрически в виде Ре ( Ш) - солей гидрокса-мовых к-т, образующихся при взаимод. Для определения сложных эфиров особенно часто рекомендуется реакция с гидроксиламином. Для определения сложных эфиров [113] к 5 мл 10 - 3 - 10 - 2М раствора сложного эфира в безводном этиловом спирте прибавляют 3 мл смеси равных объемов 12 5 % - ных растворов гидрохлорида гидроксиламина и едкого натра в метиловом спирте и нагревают 5 мин с обратным холодильником при 100 С. Охлаждают до комнатной температуры, переносят в мерную колбу емкостью 100 мл, смывают 50 мл реактива и разбавляют этиловым спиртом до метки. Для определения сложных эфиров в ту же колбу, после определения кислот, добавляют 25 мл 0 1 н раствора едкого натра и содержимое колбы вновь кипятят с обратным холодильником; на водяной бане в течение часа. Для определения сложных эфиров в ту же колбу, после определения кислот, добавляют 25 мл 0 1 н раствора едкого натра и содержимое колбы вновь кипятят с обратным холодильником на водяной бане в течение часа. Для определения сложных эфиров в биосубстратах могут быть использованы методы определения активности холинэсте-разы. Эти методы, как правило, неспецифичны. Оценка количества сложного эфира в связи с этим может быть произведена на фоне эндогенных эфиров самого субстрата. Для определения сложных эфиров фенолов известен метод, основанный на образовании гидроксамовых кислот при действии на эти эфиры солянокислого гидроксиламина. При определении сложных эфиров, наиболее часто используемых в качестве пластификаторов, аналитической полосой в ИК-спектрах обычно является полоса поглощения валентных колебаний связи СО ( 1725 - 1735 см -) сложноэфирной группы. При определении сложных эфиров фенолов предложено для омыления применять растворы щелочи в 50 % - ном водном растворе диоксана [26] / Растворы щелочи в смеси воды и диоксана имеют более высокую температуру кипения, чем в этиловом спирте, устойчивы при хранении и нагревании. Отношение между растворами щелочи и титрованным раствором кислоты устанавливается предварительно; это отношение не изменяется в течение долгого времени. Отпадает необходимость в повторном контрольном опыте. Как общий метод определения сложных эфиров применяется омыление растворами щелочей ( едкого натра или едкого кали) в этиловом спирте. Содержание сложного эфира вычисляют по расходу щелочи, идущей на омыление навески сложного эфира. Малые количества альдегидов определению сложных эфиров не мешают. Если альдегиды присутствуют в большом количестве, следует предварительно проверить их поведение на чистых образцах в условиях определения сложных эфиров и выяснить возможную ошибку определения. Влияние продолжительности реакции и температуры на образование гидроксамовой кислоты.Ход анализа аналогичен ходу определения сложных эфиров, за исключением того, что раствор пробы с гидроксиламином кипятят с обратным холодильником 10 мин. Калибровочные кривые строят по известным концентрациям ангидрида или лактона; обычно получаемые калибровочные кривые не всегда оказываются прямыми линиями. Омыление является наилучшим способом для определения сложных эфиров. Однако следует помнить, что горячая концентрированная щелочь действует также и на другие функциональные группы. Например, альдегиды, имеющие в а - Ио-ложении атомы водорода, подвергаются альдольной конденсации и осмолению. Определение простых эфиров в двух - и трехкомпонентных смесях. Пожалуй, ни один метод определения сложных эфиров не распространен так сильно и не применяется столь часто, как количественное омыление сложных эфиров, тем не менее многим неизвестно, что в смесях растворителей сложные эфиры могут полностью омыляться избытком раствора едкого натра за 1 - 2 ч при энергичном взбалтывании при комнатной температуре, а низшие эфиры иногда омыляются даже в течение 10 мин. При отсутствии альдегидов в анализируемом спирте определение сложных эфиров проводится без добавления гидроксиламина. Метод, положенный в основу технических условий на определение сложных эфиров, пригоден для суммарного определения фталатов. Калибровочные кривые для колориметрического определения уксусного ангидрида в бензоле.| Результаты анализа некоторых смесей ангидридов и сложных эфиров по реакциям образования гидроксамовой кислоты и ее комплекса с. Кислоты, большинство амидов и нитрилы не мешают определению сложных эфиров описанным колориметрическим методом. Условия гидроксиламинолиза недостаточно жестки и реакция с амидами и нитрилами в этих условиях не протекает. Наоборот, хлорангидриды активно участвуют в обоих реакциях. Карбонильные соединения в высоких концентрациях также реагируют с гидроксиламином. Переходные металлы, например медь, никель и ванадий, реагируют с гидроксамовыми кислотами, образуя окрашенные комплексы, которые мешают определению. Ионы, комплексно связывающие Fe3, например хлорид, тартрат, ацетат, а также вода могут оказывать значительное влияние на интенсивность окраски при определении как сложных эфиров, так и ангидридов. Лактоны можно рассматривать как - внутренние сложные эфиры, и методы определения сложных эфиров можно распространить и на лактонную функцию. Результаты анализа смесей кислот и ангидридов титрованием. Метод Годду, Леблана и Райта, описанный в разделе, посвященном определению сложных эфиров, пригоден и для определения ангидридов, а также ангидридов в присутствии сложных эфиров. Результаты определения циклопропиламидов. Следы амидов можно определять колориметрически двумя методами: по окраске железогидроксаматных комплексов аналогично определению сложных эфиров и путем гидролиза и колориметрического определения образующихся аммиака или аминов. При оксимировании альдегидов надо тщательным образом избегать избытка гидроксиламина, который может в условиях определения сложных эфиров омылением превратить последние в гидроксамовые кислоты. Эта реакция используется для количественного определения ал-коксильных групп по методу Цейзеля и может быть применена для определения сложных эфиров.Если спирт содержит много альдегидов ( более 500 мг в 1 л, например, сульфитного спирта), то при определении сложных эфиров омыление их ведут с предварительным связыванием карбонильных групп солянокислым гидроксиламином.Зависимость степени окисления муравьиной ( 1 и н-масляной ( 2 кислот от концентрации серной кислоты. Следует заметить, что метод окисления, использованный нами в работе [16] и давший хорошие результаты для определения этилацетата, оказался совершенно непригодным для определения сложных эфиров муравьиной и к-масляной кислот вследствие их окисления серной кислотой.Зависимость степени окисления муравьиной ( 1 и н-масляной ( 2 кислот от концентрации серной кислоты. Следует заметить, что метод окисления, использованный нами в работе [16] и давший хорошие результаты для определения этилацетата, оказался совершенно непригодным для определения сложных эфиров муравьиной и н-масляной кислот вследствие их окисления серной кислотой.L Влияние времени реакции на степень взаимодействия между эфиром.| Влияние концентрации Fe3 ( а и Н ( б на чувствительность определения эфира уксусной кислоты. Если в смеси ангидрида и сложного эфира необходимо определить оба компонента, калибровочную кривую для ангидрида строят, проводя анализ при тех же условиях, что и при определении сложного эфира. Для определения концентрации ангидрида реакцию образования гидроксамовой кислоты проводят с применением нейтрального реактива - основания гидроксиламина.Для определения сложных эфиров высших жирных спиртов разработана методика, основанная на омылении эфиров до соответствующих спиртов и колориметрическом определении последних по реакции конденсации с п-диметиламинобензальдегидом в присутствии серной кислоты.Общий метод количественного определения сложных эфиров основан на реакции омыления их растворами щелочей. Для открытия и определения сложных эфиров фенолов при малом их содержании применяется реакция образования гидроксамовых кислот.Этот метод пригоден для низкомолекулярных незамещенных жирных кислот, содержащих от 1 до 6 атомов углерода. Он также применим при определении сложных эфиров этих кислот, так как последние могут быть получены из эфиров гидролизом.Некоторые вопросы, относящиеся к определению сложных эфиров путем их омыления, были подробно разобраны в I томе ( стр. Когда производят анализ жиров и других нерастворимых в воде веществ, для омыления применяют спиртовые растворы едкого кали или едкого натра.Для удобства вычисления следует при предварительном определении содержания альдегидов и при определении сложных эфиров применять равные объемы анализируемой смеси, измеренные микробюреткой. Для выражения результатов в процентах по массе этот объем может быть однократно взвешен. С в течение Vs - 1 ч - Параллельно проводят контрольный опыт с тем же объемом щелочи, но без добавления гидроксиламина.Малые количества альдегидов определению сложных эфиров не мешают. Если альдегиды присутствуют в большом количестве, следует предварительно проверить их поведение на чистых образцах в условиях определения сложных эфиров и выяснить возможную ошибку определения.Если в анализируемой смеси присутствуют карболовые кислоты, их количество устанавливается предварительным титрованием раствора спиртовой щелочи в присутствии фенолфталеина в отдельной навеске или, что значительно удобнее, в навеске, предназначенной для определения сложных эфиров.После отделения альдегидов и кетонов смесь исследуют на присутствие сложных эфиров; для этого к пробе прибавляют нормальный раствор едкого натра, нагревают в течение получаса с обратным холодильником до кипения и оттитровывают едкий натр соляной к-той; уменьшение количества щелочи указывает на присутствие сложного эфира. При наличии сложных эфиров спирты выделяют в другой порции смеси помощью фталевого ангидрида ( см. стр. Иногда можно вести определение сложных эфиров высаливанием их из водного раствора хлористым кальцием; спирты при этом остаются в растворе.
Сложные эфиры легко превращаются в алкилиодиды, однако их растворимость в водной иодистоводородной кислоте может быть низкой. Обычно в качестве растворителя рекомендуется фенол, но он может влиять на результат титрования, так как небольшие количества его, извлекаемые бензолом, титруются, как кислота. Подходящими растворителями, не мешающими определению сложных эфиров, являются уксусный и пропионовый ангидриды.Однако при спектральном определении кетона необходимо учитывать присутствие эфиров. Полученные значения коэффициентов погашения в максимуме и ширин полос позволяют оценить степень ыгого наложения: 1 % сложного эфира завышает примерно на 0 15 % найденное содержание кетона. На основании полученных нами данных по параметрам полос разработан и проверен метод определения сложных эфиров и кетонов по ИК-спектрам.Реакция протекает в щелочной среде при кипячении реагирующей жидкости. После омыления эфиров в щелочной среде пробу титруют кислотой в присутствии фенолфталеина или лакмуса. Затем находят количество щелочи, взятое на омыление, которое эквивалентно количеству омыленных эфиров, и вычисляют содержание эфиров в пробе в пересчете на уксусноэтило-вый эфир. Определению сложных эфиров мешают альдегиды, присутствующие в пробе. При со держании альдегидов более 0 5 % их удаляют, обрабатывая пробу солянокислым гидроксила-мином.При расщеплении указанных эфиров в организме накапливается соответствующий спирт. Определение количества этого спирта может быть произведено с помощью методов, описанных выше, - метилового на стр. Однако следует учесть, что эти методы обнаруживают весь спирт - как накопившийся в биосубстрате в результате биотрансформации сложного эфира, так и образующийся из еще не разложившегося эфира в процессе анализа. Таким образом, для суждения об истинном содержании спирта в подобных образцах, помимо определения спирта, следует произвести определение сложного эфира. Найденное в последнем анализе количество стехиометрически пересчитать на спирт, что даст долю спирта в общем его содержании, образующуюся в результате анализа из ранее не разложившегося эфира. Разность между общим содержанием спирта и его количеством, образующимся из неразложившегося эфира, соответствует истинному содержанию спирта в образце в момент анализа.Крепость этилового спирта замеряется спиртомером, отградуированным в объемных процентах спирта при 20 С. Если измерения делаются при другой температуре, то концентрацию находят по специальной таблице. Массовая концентрация кислот определяется титрованием щелочью. Расчет ведется на уксусную кислоту. Для определения альдегидов в этиловом спирте применяют метод, основанный на реакции с гидроксила-мином. Определение сложных эфиров основано на реакции омыления их гидроксидом натрия с последующим титрованием кислотой в присутствии фенолфталеина или лакмуса. Вычисляют содержание эфиров в пересчете на уксусно-этиловый эфир. Определению сложных эфиров в спирте мешают альдегиды, присутствующие в пробе. При содержании альдегидов более 0 5 %, их удаляют, обрабатывая пробу соляно-кислым гидроксила-мином.
www.ai08.org