Большая Энциклопедия Нефти и Газа. Омыление сложных эфиров
Омыление сложных эфиров - Справочник химика 21
XIX.2. ОПРЕДЕЛЕНИЕ КОНСТАНТЫ СКОРОСТИ РЕАКЦИИ ОМЫЛЕНИЯ СЛОЖНОГО ЭФИРА [c.253]В качестве примера реакции омыления сложного эфира рассмотрим реакцию [c.253]
Гидролиз (омыление) сложных эфиров (см. с. 168). [c.105]
Реакции второго порядка. Примером такой реакции может служить омыление сложного эфира щелочью. Реакцию второго порядка представим схемой [c.323]
Гидролиз (омыление) сложных эфиров [c.92]
Таким образом, порядок этой реакции в указанных условиях оказывается псевдопервым. По той же причине порядок реакции омыления сложных эфиров в избытке воды оказывается псевдопервым. Это свойство часто используют при исследовании кинетики химических процессов. [c.157]
Реакции второго порядка. К ним принадлежит больпшнстио бимолекулярных реакцш и некоторые тримолекулярпые реакции. Примером реакции второго порядка может служить реакция омыления сложного эфира щелочью. [c.330]Омыление сложных эфиров [c.246]
Еще Якобсен в свое время [25] выделил из каменноугольной смолы углеводород, кипящий при 170—171°, который он принял за н-декан. После хлорирования его, обработки монохлорида ацетатом калия в ледяной уксусной кислоте, омыления сложного эфира и окисления получившегося спирта перманганатом калия до полного растворения продуктов реакции в воде он получил, обрабатывая соляной кислотой, маслянистую, резко пахнущую жидкость. Это была карбоновая кислота. Она не плавилась при 31°, как каприновая кислота, а при охлаждении до —10° становилась только вязкой. [c.539]
Сырой алкилат промывается 5% раствором едкого натра и затем в присутствии этого раствора отгоняется пропан (170 °С, 14 кгс/см ). Для омыления сложных эфиров серной кислотой (из пропилена и серной кислоты) требуется высокая температура. Во второй колонне под давлением 1,7 кгс/см отгоняется бензол и, наконец, в третьей колонне получают чистые фракции кумола. Ниже приведены результаты, полученные на промышленной установке [241 [c.265]
Омыление сложных эфиров катализируется как кислотой, так и щелочью. В последнем случае оно протекает по уравнению второго порядка и может быть описано уравнением [c.286]
Число омыления определяют обработкой навески продукта спиртовым раствором, едкого кали, последующим подкислением спиртовым раствором соляной кислоты и потенциометрическим титрованием избытка соляной кислоты спиртовой щелочью до pH 10. Число омыления выражается количеством мг едкого кали, необходимым для омыления сложных эфиров и нейтрализации свободных кислот, содержащихся в 1 г исследуемого образца. Эфирное число находят по разнице значений числа омыления и кислотного числа. [c.145]
Гомогенных каталитических реакций в растворах, ускоряем мых ионами гидроксила и водорода, довольно много. К реакциям этого типа относятся этерификации кислот и спиртов, инверсия сахаров, галоидирование соединений, содержащих карбонильную группу, омыление сложных эфиров и др. [c.286]
Сложные эфиры обнаруживают по их способности омыляться щелочами. Растворяют 0,1 г вещества в 3—5 мл спирта. Добавляют несколько капель раствора фенолфталеина и по каплям такое количество 0,1 н. раствора едкого натра в метиловом спирте, чтобы стало заметно красное окрашивание. Пробирку 5 мин нагревают на водяной бане при 40 С. Исчезновение красного окрашивания указывает на образование кислоты в результате омыления сложного эфира. [c.125]
Обратная реакция — гидролиз (омыление) сложных эфиров. Реакционная способность спиртов понижается в ряду первичный > вторичный > третичный. [c.96]
| Таблица 3.12. МФК-омыление сложных эфиров с использованием | 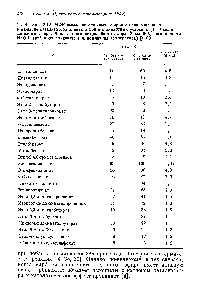 |
Химические свойства. Реакция гидролиза (омыления) сложных эфиров является обратной реакции этерификации. Процесс может проходить как в кислой, так и щелочной среде. В присутствии кислот реакция обратима, так как образующиеся при этом кислота и спирт вновь реагируют с образованием сложного эфира [c.346]
Химические свойства. Гидролиз (омыление) сложных эфиров. Под действием воды, особенно в кислой или щелочной среде, сложные эфиры разлагаются (гидролизуются) с образованием кислоты и [c.180]
Эфирное число — масса КОН (в миллиграммах), необходимая для омыления сложных эфиров, содержащихся в 1 г органического вещества. Характеризует содержание сложноэфирпых групп, главным образом в жирах, мас тах, липидах. Оно равно разности между числом омыления и К1ГСЛ0ТИЫМ числом. [c.252]
В гомогенных системах порядок реакции также снижается, если один из реагентов присутствует в большом избытке и его концентрация практически не уменьшается. Например, в разбавленном водном растворе омыление сложного эфира водой является реакцией первого порядка, так как расход воды не отражается на ее концентрации [c.133]
Масса КОН (мг), затраченного на титрование 1 г органического вещества Масса КОН (мг), затраченного на омыление сложных эфиров, содержащихся в 1 г органического вещества [c.215]
Важнейшей химической особенностью сложных эфиров является их способность распадаться при действии воды на исходные вещества — кислоту и спирт. Это превращение, обратное процессу этерификации, называется гидролизом или омылением сложных эфиров. Как и этерификация, гидролиз катализируется протонами, а кроме того (отличие от этерификации ), гидролиз ускоряется и под действием оснований, катализаторами в этом случае служат гидроксильные ионы. Схема щелочного гидролиза [c.195]
К бимолекулярным реакциям относятся такие, в элементарном акте которых принимают участие две молекулы одинаковой или различной природы. Например, реакция омыления сложного эфира [c.89]
Примером гомогенного катализа могут служить процессы окисления ЗОа в 50з при помощи газообразных окислов азота или омыления сложных эфиров, а также гидролиз дисахаридов прн участии небольших количеств сильных кислот или щелочей и др. [c.97]
Содержание эфиров в практике, как правило, характеризуют эфирным числом. Эфирное число — это масса едкого кали (мг), которая затрачивается на омыление сложных эфиров, содержащихся в 1 г анализируемого продукта. [c.49]
При какой концентрации воды омыление сложного эфира [c.47]
Параметры реакций омыления сложных эфиров уксусной кислоты (СНзСООР + ОН —> СНзСОО"-1-НОН) [c.287]
Реакциями нулевого порядка называют процессы, в которых скорость процесса сохраняется постоянной во времени. Это встречается в некоторых гетерогенных системах. Так, если в предыдущем примере — омыление сложного эфира водой в разбавленном водном растворе — применять эфир, малорастворимый в воде, и взять его в избытке, чтобы в системе присутствовал эфирный слой, то расход эфира будет постоянно восполняться из эфирного слоя. Таким образом, концентрация его в водном слое будет постоянной и, следовательно, постоянной будет скорость процесса у = сопз1, [c.468]
Упрощенная схема процесса изображена на рис. 114. Окисление ведут в каскаде барботажных колонн 1 с последовательным перетоком жидкости и подачей воздуха в каждую колонну. Тепло реакции снимается за счет испарения избыточного циклогексана, который коь денсируется в общем для всех колонн холодильнике 2, отделяется от газа в сепараторе 3 и поступает в линию оборотного циклогексана. Оксидат из последней колонны промывают водой (для выделения низших кислот) в смесителе 4 и отделяют от водного слоя в сепараторе 5. Затем из оксидата в колонне 6 отгоняют основную массу циклогексана, оставляя в кубе такое его количество, чтэбы концентрация гидропероксида не превысила безопасного уровня (3—4%). Кубовую жидкость обрабатывают затем при нагревании и каскаде аппаратов 7 с мешалками (на рисунке изображен один) водной щелочью. При этом происходит омыление сложных эфиров и лактонов, а также разложение гидропероксида. Органический слой отде- [c.389]
Технологическая схема разделения сырых спиртов, полученных прямой гидрогенизацией кислот, представлена на рис. 1.10. Схема включает нейтрализацию свободных кислот и омыление сложных эфиров. Сырые спирты (гидрогенизат) и 20—40%-ная щелочь непрерывно подаются в аппарат 3 с мешалкой дл нейтрализации кислот и омыления эфиров при 90—100 °С. Омыленный продукт через подогреватель 4, обогреваемый высокотемпературным органическим тепло носителем (ВОТ), поступает в один из двух вакуумных кубов-испарителей 5 периодического действия. Из верхней части кубов 5 при 300 С и остаточном давлении 666,5—1333 Па (5—10 мм рт. ст.) отбирают пары воды и широкой фракций спиртов. Кубовый остаток (расплавленные соли КИСЛОТ) 0ТВ0.5ИТСЯ в сбор- [c.35]
Возможными в условиях существования нефтяных месторождений могут быть процессы омыления сложных эфиров карбоновых кислот сульфидрильными солями [c.172]
Во многих случаях гомогенный катализ в растворах вызывается ионами водорода и гидроксила. К таким реакциям относятся инверсия тростникового сахара, омыление сложных эфиров, гидролитическое разложение амидов и ацеталей и др. [c.298]
Протолитическая теория была применена к истолкованию закономерностей реакций кислотно-основного катализа разложение нитра-мида, инверсия сахаров, омыление сложных эфиров и т. п. Скорость этих процессов зависит от природы и концентрации кислот и оснований, присутствующих в растворе, причем сами кислоты и основания в ходе реакции не расходуются, т.е. выступают в роли катализаторов. Реагирующее вещество можно рассматривать как слабую кислоту пли слабое основание, которые вступают в реакцию с катализатором основанием или кислотой с образованием некоторого промежуточного комплекса. Последний затем распадается на конечные продукты с регенерацией катализатора. Сила кислот и оснований (константы их ионизации) и их каталитическая активность связаны между собой. Я. Брёнстед установил, что если в качестве катализаторов использовать ряд однотипных слабых кислот, то между константой скорости катализируемого ими процесса и константой ионизации кислот Ка существует следующее соотношение [c.84]
Нуклеофильная атака указанного атома углерода может осуществляться гйдроксил-ионом (щелочной гидролиз сложных эфиров, амидов, хлорангидридов), алкоксил-ионом (получение сложных эфиров из ангидридов или хлорангидридов кислот), аминным азотом (образование амидов из сложных эфиров, хлорангидридов, ангидридов) и другими аналогичными частицами. В этих случаях предполагается первоначальное образование тетраэдрического переходного состояния в частности, оно возникает при бимолекулярном щелочном омылении сложных эфиров, которое завершается разрывом связи кислород — ацил (реакция типа Вдс2, где В — знак щелочного омыления, Ас — характеризует отщепляющуюся группу) [c.220]
Первые теории химического процесса. Первые теории, описывающие. химический процесс, появились одновременно с первыми структурными представлениями на граяи ХУНТ и XIX вв. Спор между Бертолле и Прустом явился результатом борьбы за сущест-воваиие этих двух направлений, противопоставленных друг другу. Структурные теории тогда пустили глубокие корни и послужили началом стройного атомно-молекулярного учения. Ростки же кинетических теории, как было сказано в гл. II, увяли, так как появились преждевременно. И тем ие менее почвой для их произрастания, правда более чем полувеком спустя, явились открытия, подтвердившие химическую статику Бертолле, т. е. его идеи об обратимости реакций и о влиянии на ход реакций действующих масс. В 1861 г. Д. И. Менделеев под влиянием результатов изучения реакций омыления сложных эфиров одним из первых осмелился ввести понятие об обратимости реа кций в свой учебник Органическая химия [5]. При этом он заметил, что при суждении о химических процессах никогда не должно забывать закона масс, указанного Бертоллетом [5, с. 285]. [c.111]
Ввиду обратимости реакции получения сложного эфира последний при взаимодействии с водой подвергается частичному гидролизу с образованием кислоты и спирта. Под действием только воды гидролиз сложных эфиров (называемый обычно их омылением) протекает чрезвычайно медленно, но в присутствии кислот и особенно щелочей он значительно ускоряется. Кипячение с раствором NaOH ведет к быстрому омылению сложного эфира по схеме [c.540]
При действии концентрированных щелочей также происходит омыление сложного эфира, но за счет большого избытка щелочи образуется натриевая соль натриевого производного енольной формы ацетоуксусной кислоты. Присоединяя воду, этот промежуточный продукт распадается на две молекулы натриевой соли уксусной кислоты. [c.271]
Органическая химия (1968) -- [ c.161 , c.162 ]Курс органической химии (1965) -- [ c.174 , c.254 ]
Реакционная способность и пути реакций (1977) -- [ c.12 ]
Равновесие и кинетика реакций в растворах (1975) -- [ c.135 ]
Введение в электронную теорию органических реакций (1965) -- [ c.253 , c.255 , c.257 , c.269 , c.276 , c.308 ]
Руководство по малому практикуму по органической химии (1964) -- [ c.160 ]
Курс органической химии (1967) -- [ c.174 , c.254 ]
Курс органической химии (1979) -- [ c.244 ]
Органическая химия для студентов медицинских институтов (1963) -- [ c.140 ]
Методы эксперимента в органической химии Часть 2 (1950) -- [ c.217 ]
Органическая химия 1971 (1971) -- [ c.100 , c.165 , c.166 ]
Органическая химия 1974 (1974) -- [ c.82 , c.136 , c.137 ]
Объёмный анализ Том 1 (1950) -- [ c.235 ]
Курс органической химии (0) -- [ c.241 , c.262 , c.263 ]
Курс органической химии _1966 (1966) -- [ c.179 ]
Органическая химия Издание 4 (1970) -- [ c.104 ]
chem21.info
Количественное омыление сложных эфиров - Справочник химика 21
Сложные эфиры и лактоны Количественное омыление сложных эфиров [c.981]Пожалуй, ни один метод определения сложных эфиров не распространен так сильно и не применяется столь часто, как количественное омыление сложных эфиров, тем не менее многим неизвестно, что в смесях растворителей сложные эфиры могут полностью омыляться избытком раствора едкого натра за 1—2 ч при энергичном взбалтывании при комнатной температуре, а низшие эфиры иногда омыляются даже в течение 10 мин. [c.981]
Количественное определение сложных эфиров основано на реакции гидролитического расщепления (омыления). [c.114]Нуклеофильная атака гидроксильного аниона по карбонильной группе дает промежуточный анион, который может элиминировать либо гидроксильный анион, образуя исходные вещества, либо алкоксид-анион. Потеря алкоксид-аниона приводит к образованию карбоновой кислоты, которая реагирует с сильным основанием — алкоксид-анионом, давая карбоксилат-анион и молекулу спирта. Хотя завершающая стадия в принципе обратима, фактически равновесие нацело смещено в сторону образования спирта и карбоксилат-аниона. Таким образом, щелочной гидролиз (или омыление ) сложных эфиров в отличие от кислого гидролиза количественно приводит к солям карбоновых кислот. При этом катион металла не играет абсолютно никакой роли и служит только для сохранения электронейтральности. [c.159]
Щелочное омыление сложных эфиров находит применение так-же для определения эквивалентных масс сложных эфиров или чисел омыления (например, в количественном анализе жиров). Числом омыления называют количество едкого кали (в миллиграммах), необходимое для гидролиза 1 г жира или вообще сложного эфира. [c.97]
Число омыления и эфирное число. Количественное определение сложных эфиров основано на реакции гидролитического расщепления (омыления). В результате омыления образуется спирт и соль кислоты [c.250]
Щелочное омыление сложных эфиров находит также применение для определения эквивалентного веса, или так называемого числа омыления сложных эфиров (например, в количественном анализе жиров). Число омыления— это число миллиграммов едкого кали, которое необходимо для омыления одного грамма жира или вообще сложного эфира. [c.403]
Работы вида 4 обычно удобно проводить на первых же занятиях поэтому они сведены в главе IV. Общие методы количественного элементарного анализа в малый практикум обычно не включаются. Опыты по отдельным, более простым (частным) количественным методам анализа (определение эквивалента кислоты, коэффициента омыления сложного эфира и т. п.) приведены в главах, включающих описание соединений данного класса. [c.16]
Количественное определение сложных эфиров. Обычным методом определения сложных эфиров является гидролиз (омыление). При проведении реакции в присутствии щелочи образуются соль соответствующей кислоты и спирт [c.269]
Учитывая, что при омылении на одну сложноэфирную группировку расходуется одна молекула щелочи, омыление сложного эфира можно использовать для количественного определения эквивалентного сложного эфира. [c.269]
Общий метод количественного определения сложных эфиров основан на реакции омыления их растворами щелочей. Для открытия и определения сложных эфиров фенолов при малом их содержании применяется реакция образования гидроксамовых кислот. [c.296]
Принцип метода. Содержание сложного эфира в продукте выражают в условных единицах эфирного числа , которое обозначает количество миллиграмм едкого кали, необходимое для омыления 1 г продукта. Количественное определение сложных эфиров основано на омылении их титрованным спиртовым раствором едкого кали [c.26]
Принцип метода. Количественное определение сложных эфиров основано на омылении их спиртовым раствором едкого кали. По расходу едкого кали рассчитывают содержание эфиров. [c.8]
Нейтральные вещества черного щелока представляют собой многокомпонентную смесь веществ, относящихся к различным классам органических соединений. Качественный и количественный состав нейтральных веществ меняется в зависимости от видовой специфичности сырья. Нейтральные вещества, извлекаемые из сульфатного мыла малополярным растворителем, в основном состоят из неомыляемых, но в них всегда присутствует какое-то количество сложных эфиров, не подвергнувшихся омылению при сульфатной варке древесины. [c.88]
По количеству щелочи, израсходованному на омыление, рассчитывают количество сложного эфира. Для наиболее часто используемых в основном органическом синтезе сложных эфиров наряду с количественным определением содержания эфира определяют различные константы кислотное число, эфирное число, число омыления, бромное число и другие показатели. [c.250]
Сложность строения многих алкалоидов сильно затрудняет определение их структуры. Прежде всего выясняют, содержит ли изучаемый алкалоид кислород или нет, для чего проводят качественный и количественный анализ, определяют молекулярный вес и устанавливают его молекулярную формулу. Если алкалоид оказался кислородсодержащим, устанавливают, в какой форме представлен в нем кислород для этого применяют ряд реакций, характеризующих ту или иную кислородсодержащую группу например, гидроксильную группу открывают с помощью хлорангидридов кислот или уксусным ангидридом, сложные эфиры — путем их омыления, простые эфиры — действием на них иодистого водорода, что приводит к образованию соответствующего галоидоалкила. [c.370]
Определение в воздухе. Метил-этил-пропил-бутил-амил- и винил-ацетаты омыляют количественно при нагревании в среде водно-спиртовых растворов едких щелочей. По количеству затраченной на омыление щелочи определяют содержание У. У. К. Метод не специфичен, так как реакция омыления характерна для многих других сложных эфиров. Органические растворители, как бензол, толуол, ацетон, скипидар, бензин, спирты, не мешают определению. Метилацетат (также и в присутствии с метиловым спиртом) может быть определен колориметрически. Амилацетат по Коренману определяют путем омыления уловленного эфира и дальнейшей колориметрии амилового спирта (см. Амиловый спирт). [c.356]
Более удобным методом выделения кислот и спиртов из сложных эфиров является метод аминолиза, описанный Кайзером и Кларком . Реагентом в данном случае является моноэтаноламин (см. стр. 185). Этот метод имеет ряд преимуществ перед омылением растворами щелочей продолжительность омыления сокращается до 15—30 мин. Спирты количественно выделяются в чистом виде, и одновременно образуются амиды двухосновных кислот, которые легко характеризовать по температурам плавления и содержанию азота (см. стр. 188). Это дает возможность установить природу двухосновной кислоты, входящей в состав пластификатора (см. табл. 13, стр. 186). [c.262]
Полученный сложный эфир уксусной кислоты после нейтрализации избытка ангидрида подвергают омылению, и по расходу щелочи затем рассчитывают содержание спирта. Метод ацетилирования уксусным ангидридом не пригоден для количественных определений легколетучих спиртов, так как процесс идет при нагревании. [c.53]
Вызывает некоторое удивление незначительная область применения в ряде случаев некоторых из этих реакций. Например, реакция омыления обычно не имеет указанных недостатков или побочных реакций, как это наблюдается у реакций нитрования или сульфирования. По-видимому, с помощью щелочи в таких растворителях, как бензиловый спирт, можно при высокой температуре плавно проводить количественный гидролиз огромного числа сложных эфиров, а следовательно, можно осуществить и достаточно быстрое титрование. Опять-таки, хотя и предположительно, что можно легче разорвать связь кремний — хлор, нежели углерод — хлор, можно было бы ожидать случаи определения других галогенидов путем прямого гидролитического титрования. Такие соеди- [c.66]
Большое влияние на ход омыления оказывает характер спирта, применяемого для приготовления раствора щелочи. Растворы щелочи в метиловом спирте омыляют сложные эфиры очень медленно, и даже для легко омыляемых жиров время реакции приходится иногда удлинять до 3—4 час., а количественного омыления трудно омыляемых жиров или носков за практически приемлемый период времени вообще достичь не удается. [c.217]
Для выяснения строения так называемых сложных эфиров и количественного распределения функциональных групп в кислой и нейтральной фракциях образец парафина промышленного окисления был омылен в лабораторных условиях водно-спиртовой щелочью по методике, применяемой для количественного определения сложных эфиров [8]. Зато неомыляемые отделяли от солей кислот многократной экстракцией петролейным эфиром с последующей отгонкой петролейного эфира в вакууме. Водный раствор солей подкисляли 2JV со.тяной кислотой, затем кислоты экстрагировали петролейным эфиром. В табл. 2 приведен весовой процентный выход продуктов после разделения на фракции. Взвешивание производили после сушки, весовые потери произошли за счет водорастворимых фракций (в основном, очевидно, кислот). - [c.311]
При определении количественного и качественного состава кислородсодержащих соединений широко применяется инфракрасная спектроскопия благодаря наличию характеристических полос кислородных функциональных групп 3400—3600 см — валентные колебания атомов водорода гидроксильных групп кислот и фенолов, 1650—1740 см —валентные колебания карбонильной группы кислот, кетонов, сложных эфиров (лактонов), ангидридов кислот, амидов. Показано [49], что с помощью специфических химических реакций возможно провести идентификацию полос поглощения карбонильных групп различных классов соединений. Так, обработка карбоновых кислот бикарбонатом натрия приводит к образованию карбоксилатанионов, для которых характерно поглощение в области 1580—1610 см . Дальнейшая обработка образца гидроксидом натрия при нагревании вызывает омыление сложных эфиров, лактонов, ангидридов и образование карбоксилатанионов. В результате в области 1650— 1740 СМ наблюдается только поглощение кетонов. Пользуясь групповыми интегральными коэффициентами поглощения (для карбоновых кислот 1,24-10 л/(моль-см), сложных эфиров 1,15 10 кетонов 0,72-10 л/(моль-см) [50], можно определить концентрацию соединений каждого типа. Применение методов ИК-спектроскопии в исследованиях состава нефтей 51] позволило обнаружить и количественно оценить наличие карбоновых кислот, фенолов, амидов, 2-хинолонов. Отмечено, что точность анализа значительно снижается вследствие межмолекулярной ассоциации компонентов, что приводит к уменьшению интенсивности поглощения групп и занижению результатов. Повышение точности достигается разбавлением растворов и использованием в качестве растворителей тетрагидрофурана или дихлорметана. Однако более значительные ошибки возникают из-за неверной оценки молекулярных масс определяемых соединений и наличия в молекуле более одного гетероатома. Исправление этого положения возможно препаративным выделением одного класса соединений и установления коэффициента поглощения данной функциональной группы. [c.50]
Правильность введения константы скорости для количественной характеристики реакционной способности органических соединений получила веское подтверждение в цикле исследований кинетики омыления сложных эфиров, проведенном учеником Вант-Гоффа Рейхером [94]. Рассмотрев диссертацию Шваба [c.26]
Щелочное омыление сложных эфиров находит также применение для определения эквивалентной массы или так называемого числа омыления эфиров (например, при количественном анализе жиров). Числом омыления называют количество гидроксида калия (в мг), которое необходимо для омыления (гидролиза) 1 г жира ялеи сложного эфира. [c.104]
Если количественное определение сложных эфиров омылением в смесях, содержащих альдегиды, приводит к неправиль-иым результатам [29], то альдегиды следует предварительно превратить в оксимы, так как в отличие от самих альдегидов их оксимы стойки по отношению к воздействию щелочей. [c.168]
При количественном анализе растворителя определяют его симические константы (число омыления, гидроксильное, эфирное, карбонильное число и т. д.), количественное содержание ароматических углеводородов и т. д. По гидроксильному числу можно эпределить содержание того или иного спирта, по карбонильному— кетона, по числу омыления — сложного эфира. Окончатель-1ое заключение о составе растворителя следует делать после по-зторного спектрального и хроматографического анализа выделен-1ЫХ из растворителя компонентов. [c.407]
Гидролиз сложных эфиров карбоновых кислот относится к числу хорошо изученных реакций. Законо.черности, присущие этим реакциям, достаточно подробно исследованы на примерах гидролиза сложных эфиров монокарбоновых кислот в кислой и щелочной средах. Хорошо известно, что омыление сложных эфиров в щелочных средах протекает с количественным [c.79]
Конденсация фрагмента [Н (1 —2 )-6—8] с ранее описанным пентапептидом (Н 1—5) с помощью карбодиимидного метода привела с выходом 40% к разветвленному декапептиду [I (1 — 2 )-1—8], охарактеризованному количественным аминокислотным анализом и УФ-спектром. Формильную группу отщепляли действием 4 н. метанольного раствора НС1 в трифторуксусной кислоте или диметилсульфоксиде в течение 20 час при 20 [К ( —2 )-1—8] [2392]. Освободившуюся аминогруппу вновь количественно идентифицировали колориметрическим нингидриновым методом. Последующее омыление сложного эфира проводили обработкой 1,5-кратным избытком 1 н. едкого натра в диметилсульфоксиде в течение 20 час [L(l —2 )-1—8] образовавшуюся свободную карбоксильную группу определяли микротитрованием. Циклизацию синтезированного разветвленного декапептида осуществляли путем перемешивания при 20° раствора декапептида с 300-кратным избытком N, N -дициклогексилкарбодиимида в условиях высокого разбавления, причем выход неочищенного продукта реакции составил 20%. Защитные группы отщепляли действием натрия в жидком аммиаке. Полученный циклический пептид был очищен путем противоточного распределения (400 переносов вго/7-бутанол/0,1 н. соляная кислота) и хроматографирования на целлюлозном порошке (н-бутанол/ пиридин/ледяная уксусная кислота/вода, 30 20 6 24 м-бута-нол, содержащий 15% уксусной кислоты) с последующим обессоливанием на амберлите ШС-50 (ХЕ-64) в Н+-форме. [c.566]
Впервые количественные исследования влияния структурных факторов на скорость омыления сложных эфиров в щелочной среде (реакция второго/но-рядка) были проведены Райхером [И], который, начиная с 1885 г., изучал сложные жирные эфиры К СООК с неразветвленными и разветвленными алкильными группами К и К. Эти исследования были расширены результаты изучения жирных эфиров Олсоном [12], Шкрабалом [13] и Киндлером [14] [c.940]
Омыление щелочью наиболее часто применяется для количественного определения содержания большинства сложных эфиров, в том числе и жиров, а также продуктов этерификации фенолов. Наибольшее влияние на реакцию омыления оказывают следующие факторы достаточная концентрация ионов гидроксила в растворе, хорошая растворимость анализируемого вещества во взятом растворителе и высокая температура реакции омыления. Сравнительно легко растворимые в воде сложные эфиры (как, например, этил-формиат, метилформиат, этилацетат и др.) могут быть омылены водными растворами щелочей. Сложные эфиры, плохо растворимые в воде, омыляют в спиртовой среде. Для этого пользуются спиртовыми растворами едкого кали или едкого натра. Можно прямо растворить сложный эфир в этиловом спирте, а затем прилить определенное количество водного раствора титрованной щелочи и омылить эфир. Спиртовые растворы едкого кали более предпочтительны вследствие хорошей растворимости едкого кали в спирте, особенно при получении его концентрированных растворов. Скорость омыления сложных эфиров различна. Она зависит от природы входящих в состав сложного эфира кислоты и спирта. В одних случаях реакция омыления протекает быстро даже при обычной комнатной температуре, в других [c.249]
В отсутствие полярных групп эфиры легко количественно определить методом ГХ. В этих анализах ншроко применяют полиэфирные жидкие фазы, которые позволяют получать симметричные хроматографические пики для простых эфиров и, кроме того, обеспечивают разделение в зависимости от числа ненасыщенных связей. Симметричные пики и хорошие количественные данные можно получить и на неполярных жидких фазах, но они не позволяют разделять насыщенные и ненасыщенные эфиры. Колонки с неполярными фазами можно использовать только для грубого разделения эфиров по их молекулярным весам (например, отделить эфиры H- i6 от эфиров я- is), а колонки с полиэфирами — для дополнительного разделения по числу ненасыщенных связей (О, 1, 2 или большее число двойных связей). Эфиры с высоким молекулярным весом или их нелетучие комплексы (например, фосфолипид) обычно превращают в более летучие производные (по кислотной или спиртовой группе или по обеим этим группам) путем переэтерификации, алкоголиза или омыления с последующим превращением в простые или сложные эфиры. Если эфиры содержат полярные группы, то на одном из этапов определения получают производные по этим группам. Так, например, ацетилирование моно- и диглицеридов обеспечивало полное элюирование этих эфиров в ГХ-анализе в то же время без ацетилирования элюирование может оказаться неполным [41, 42]. Моноглицериды (Сг— is) и диглицериды (С4—Сзб) определяли также и путем превращения их по свободным оксигруппам в триметилсилильные эфиры под действием бис- (триметилсилил) ацетамида [43]. [c.140]
Как уже указывалось ранее, амиды можно определять, используя реакцию омыления. Однако для амидов реакцию омыления не удается применять столь же широко, как для сложных эфиров. Первичные амиды R ONh3 наиболее легко поддаются определению с помощью омыления, но и в этом случае некото-зые первичные амиды оказываются слишком устойчивыми для количественного омыления. Вторичные R ONHR и третичные R ONR R" амиды подвергаются гидролизу с трудом. [c.149]
Еще одна часто встречаемая в неионогенных ПАВ примесь — это полиэтиленгли-коль. Для определения содержания этой примеси образец, как правило, растворяют в водном растворе натрий хлорида, который впоследствии экстрагируют этилацетатом. Слой этилацетата затем еще раз экстрагируют раствором натрий хлорида. Далее раствор натрий хлорида экстрагируется хлороформом. Слой хлороформа упаривают досуха, и сухой остаток экстрагируют ацетоном для удаления проэкстрагированных солей. Остаток после выпаривания ацетона соответствует содержанию полиэтиленгликоля в исходном образце [63]. Также была разработана технология определения сорбита в сложных эфирах сорбита [2], которая заключается в омылении эфиров сорбитана, после чего выделенный сорбит окисляется перйодной кислотой. Результатом является образование четырех молекул муравьиной кислоты и двух молекул формальдегида, которые могут быть измерены количественно. [c.131]
Ли и Кольтгоф 2 пришли к заключению, что если константы скорости реакций двух компонентов отличаются по крайней мере в 4 раза, практически целесообразно количественное онре-деление обоих компонентов. Так, авторы с успехом определяли близкие пары сложных эфиров, например этилацетата и изопро-пилацетата, используя скорости их омыления, которые при 25° С находятся в соотношении 4,2 1. Средняя ошибка составляла 2% (абсолютных). Были проанализированы различные пары карбонильных соединений путем использования разницы в скоростях разложения их бисульфитных соединений. Для формальдегида и ацетальдегида при 25° С и pH 3,4 соотношение скоростей составляло 1 60. [c.501]
Сложные эфиры спиртов дают с гидроксиламином гидроксамовые кислоты в сильно щелочных средах. Для количественного определения пригоден лишь метод, основанный на образовании окрашенного железного комплекса полученной гидроксамовой кислоты, измеряемого спектрофотометрически. Этот метод особенно удобен при определении малых количеств сложных эфиров и для анализа многокомпонентных систем. Все определение состоит из двух стадий реакции сложного эфира с гидроксиламином, протекающей в щелочной среде, и получения окрашенного комплекса с железом (III) в кислой среде Скорость реакции образования гидроксамовой кислоты увеличивается по мере повышения концентрации Н0 в реакционной среде, однако при этом появляется опасность побочной реакции омыления определяемого эфира без образования гидроксамовой кислоты [33. Как протекает реакция для различных сложных эфиров даже одной и той же кислоты, точно сказать 1 ельзя, так как выделение после реакции чистых гидроксамовых кислот представляет большие трудности и реакция образования гидроксамовых кислот мало изучена. Описываемый метод имеет до известной степени условный характер. Достаточно точные данные удается получить только при строгом соблюдении одинаковых условий на обеих стадиях определения как при построении калибровочной кривой, так и при анализе. [c.171]
Сложные эфиры, лактоны, ангидриды кислот, а) Сложные эфиры. Могут присутствовать эфиры, относящиеся к самым разнообразным группам кислот и спиртов (или фенолов). Их кипятят в течение часа с 8—10 -ным раствором NaOH в метиловом спирте, испаряют большую часть метилового спирта и смешивают с водой при наличии выделившихся веществ их извлекают эфиром, взбалтывают для з даления метилового спирта с водой, отгоняют эфир и подвергают перегонке. Если температура кипении после омыления отличается от таковой до омыления, то это означает, что из эфиров образовались спирты групп Л-Л. 1 или Т-Л. 1 нх исследуют по стр. 229 или по п. II. Если температура кипения изменилась очень мало, — это указывает либо на отсутствие сложного эфира, либо на образование такого спирта, который обладает температурой кипения, весьма близкой к темп. кип. сложного эфира. Последнее возможно только в том случае, если омылялся эфир легколетучей кислоты. Кислота определяется следующим образом небольшую пробу щелочного раствора после омыления осторожно обрабатывают на часовом стекле крепкой НгЗО и определяют присутствие легколетучей кислоты по запаху. Другие методы открытия сложных эфиров и количественного их определения по коэффициенту омыления подробно излагаются в руководствах по исследованию минеральных масел, жиров и воска. [c.249]
Определение этилнитритным методом. Этилнитритный метод количественного определения этилового спирта основан на образовании в солянокислом растворе сложного эфира этилового спирта и азотистой кислоты (этилнитрита) с последующим извлечением и омылением его. О количествах связавшейся с этиловым спиртом азотистой кислоты судят по реакции образования азокрасителя. [c.53]
Для определения степени этерификации простых эфиров целлюлозы нельзя применять методы кислотного или щелочного омыления, которыми обычно пользуются при исследовании сложных эфиров целлюлозы. Алкильные группы могут быть количественно отщеплены только при нагревании с концентрированной иодистоводо-родной кислотой. Этот метод применяется для определения степени этерификации простых эфиров целлюлозы (метод Цейзеля). Реакция протекает по схеме [c.470]
chem21.info
Омыление эфиров - Справочник химика 21
Большинство реальных химических процессов протекает через ряд последовательных химических реакций. Каждая из этих последовательных реакций может быть простой, описываться уравнением односторонней реакции первого или второго порядка, или сложной двусторонней реакцией. В качестве примера простой односторонней последовательной реакции можно привести процесс омыления эфиров двухосновных кислот щелочью [c.546] Первичные амины легко образуются при щелочном омылении эфиров изоциановой кислоты именно этим путем они были впервые получены Вюрцем, который установил их отличие от аммиака на основании способности к горению [c.161]Для В. С. Гутыри характерен строго научный подход к решению практических задач. Так, изучив существующие тогда в мировой практике методы синтеза этилового спирта, он остановился на наиболее перспективном методе гидратации олефинов с помощью минеральных кислот (серной кислоты) с последующим омылением эфиров в алкоголи. Экспериментальные исследо- [c.4]
Это и есть кинетическое уравнение реакции второго порядка. Примером подобной реакции может служить омыление эфиров щелочами [c.147]
Экстракт подается в колонну 11 для отпарки метанола. Сконденсировавшиеся пары метанола поступают в приемник 9, а экстракт подается в емкость 12 на смешение с водой. Полученная эмульсия подается в автоклав 13, где при температуре 180° С и давлении 20 ат происходит омыление эфиров. Из автоклава эмульсия подается в термическую печь 15, нагревается до 350° С и направляется в испаритель 16. В испарителе происходит отделение расплавленного мыла от неомыляемых продуктов, представленных, в основном, спиртами, кетонами и углеводородами. Расплавленное мыло перерабатывается далее по общепринятой схеме образование мыльного клея, разложение мыльного клея серной кислотой, отделение раствора сульфата натрия, ректификация синтетических жирных кислот. [c.173]
Примером реакции второго порядка в растворе может служить омыление эфира щелочью [c.23]
Последовательные реакции — это реакции с промежуточными стадиями. Примеров таких реакций можно привести много. Большинство реакций протекает через промежуточные стадии. Правда, характер промежуточных веществ из-за экспериментальных трудностей не всегда удается установить. К последовательным реакциям относятся, в частности, реакции омыления эфиров двухосновных кислот щелочью, например янтарно-этилового эфира едким натром [c.33]
Рассмотрим весьма распространенный случай гомогенного катализа — кислотно-основной катализ, который используется для ускорения многих технически важных реакций, например омыления эфиров, инверсии сахара, конденсации, полимеризации. [c.408]
При определенной температуре 0,01 н. раствор уксусноэтилового эфира омыляется 0,002 н. раствором NaOH за 23 мин на 10%. Через СКОЛ1.КО минут он будет омылен до такой же степени 0,005 н. раствором NaOH, если реакция омыления эфира — реакция второго порядка, а щелочи диссоциированы полностью [c.342]
Вследствие частичного омыления эфира выход спирта при этом никогда ие бывает количественным тем не менее метод представляет известную ценность для превращения карбоновых кислот в спирты с тем же числом атомов углерода. Иногда этот метод видоизменяют таким образом, что вместо эфиров восстановлению подвергают амиды кислот С Н2п+ СОЫН з однако в этом случае реакция обычно проходит менее гладко. [c.110]
Кислотно-основной катализ. В этом случае роль катализатора выполняют кислоты или основания. Сюда относятся большинство реакций в растворах, как, например, омыление эфиров, инверсия сахара, гидролиз крахмала, амидов, ацеталей и др. Чаще всего непосредственный каталитический э4х ект вызывается ионами гидроксония Н3О+ и гидроксила ОН". Примем следующее выражение константы скорости реакции для этого случая [c.268]
Из j ругих продуктов, образующихся при окислении парафина, значительный интерес представляют спирты. Их можно извлечь (после омыления эфиров и экстракции кислот водными щелочами) в виде сложных эфиров борной кислоты, причем количество этих спиртов составляет 8—10% от исходного парафина. Спирты имеют 8—26 углеродных атомов в молекуле и являются преимущественно (на 65--75%) первичными. Их с успехом применяют для синтеза поверхностно-активных веществ типа алкилсульфатов. [c.383]
Константа скорости реакции омыления уксусноэтилового эфира щелочью прн 283 К равна 2,38 мин- Х Xмоль- -л. Рассчитайте время половинног разложения эфира, еслн 1 л 0,05 н. раствора эфира смешать с I л 0,1 н. раствора щелочи. Реакция омыления эфира подчиняется кинетическому уравнению 2-го порядка. [c.69]
К гомогенным каталитическим реакциям относятся реакции, протекающие в газовой фазе и в растворах. Сюда относится катализируемая оксидом азота реакция окисления диоксида серы кислородом, применяющаяся в камерном и башенном способах производства серной кислоты, реакции омыления эфиров и инверсии сахара, ряд реакций разложения и полимеризации. [c.342]
Следовательно, реакция омыления эфира щелочью является реакцией второго порядка. [c.237]
На основании данных о скоростях омыления эфиров в водных растЕорах [М.] сделайте вывод, омыление какого из эфиров при 323 К СН3СООС2Н5, СН3СООС3Н, или СН3СООС4Н9 происходит быстрее. В каком соотношении находятся константы скорости омыления этих эфиров [c.420]
Напишите уравнения реакций окисления глюкозы омыления эфира пентаацетилглюкозы восстановления глюкозы спиртового брожения. [c.91]
Чтобы определить величины 0 -констант (индукционных констант заместителей), необходимо, воспользовавшись уравнением (IV, 16), задаться значением параметра р в эталонной для данного ряда серии. Заместители К в реакционной серии омыления эфиров оказ1з1вают чрезвычайно малое влияние на скорость кислотного гидролиза эфиров, т, е. р нь = О, поэтому величина р в выражении (VI, 16) практически определяется значением реакционной константы щелочного гидролиза эфиров рои-. Для нее было принято то значение, которым характеризуется щелочное омыление м- и п-замещенных бензоатов. Оно примерно равно 2,48. Учитывая это, можно переписать выражение (VI, 16) [c.177]
Если применяют количества щелочи, достаточные для нейтрализации всей образовавшейся карбоновой кислоты, то происходит количественное омыление эфира. [c.263]
Получение 4-оксистирола омылением эфира 4-оксистирола и бензойной кислоты [c.78]
Эфирное число масса КОН (мг), необходимая для омыления эфиров, содержащихся в 1 г анализируемого вещества. [c.205]
Число омыления (Ч. О.) —масса КОН (мг), необходимая для нейтрализации свободных кислот и омыления эфиров, содержащихся в 1 г анализируемого вещества. Число омыления равно сумме кислотного и эфирного чисел. [c.205]
Известные реакции, лишь формально протекающие по уравнению реакции первого порядка, как это было показано для омыления эфира в кислой среде [уравнение (19)]. Вообще, если один из компонентов имеется в большом избытке и вследствие этого его концентрация почти не снижается а ходе реакции, то, хотя эта реакция протекает со скоростью, определяемой уравнением второго порядка, расчет кинетики такой реакции можно проводить на основе уравнений скорости реакции [c.156]
Технологическая схема разделения сырых спиртов, полученных прямой гидрогенизацией кислот, представлена на рис. 1.10. Схема включает нейтрализацию свободных кислот и омыление сложных эфиров. Сырые спирты (гидрогенизат) и 20—40%-ная щелочь непрерывно подаются в аппарат 3 с мешалкой дл нейтрализации кислот и омыления эфиров при 90—100 °С. Омыленный продукт через подогреватель 4, обогреваемый высокотемпературным органическим тепло носителем (ВОТ), поступает в один из двух вакуумных кубов-испарителей 5 периодического действия. Из верхней части кубов 5 при 300 С и остаточном давлении 666,5—1333 Па (5—10 мм рт. ст.) отбирают пары воды и широкой фракций спиртов. Кубовый остаток (расплавленные соли КИСЛОТ) 0ТВ0.5ИТСЯ в сбор- [c.35]
Для многих химических реакций кинетические закономерности подчиняются уравнению скорости реакции второго порядка. К таким реакциям относятся образование И1 и его разложение на исходные вещества. В качестве классического примера реакции второго порядка часто рассматривают омыление эфира в щелочной среде [c.157]
К категории нуклеофильных реакций относятся такие распространенные процессы органической химии, как гидролиз галоидных алкилов, этерификации и омыление эфиров, амидирование, образование простых эфиров, синтез нитрилов по Кольбе, реакция Манниха и т. п. [c.189]
Последовательные (консекутивные) реакции. Реакции, протекающие через образование промежуточных продуктов, называются последовательными или консекутивными. Поскольку подавляющее большинство веществ, участвующих в биологических и химико-технологических процессах, являются не конечными, термодинамически устойчивыми, а промежуточными продуктами в цепи последовательных превращений, такие реакции являются едва ли не наиболее распространенными в природе и технике они имеют огромное практическое значение. К последовательным реакциям относится, например, омыление эфиров двухосновных кислот [c.247]
Широко распространен кислотно-основной катализ. К нему относится, например, катализируемое кислотой омыление эфиров [реакция (19)]. При реакциях окисления анионами различных оксокислот (призводные оксокислот галогенов, хрома, марганца и др.) зачастую заметно, что протонированный анион реагирует значительно быстрее, чем непротонированный. Например, многие органические соединения (спирты, альдегиды) очень медленно окисляются хроматом в нейтральном растворе, в то же время при уменьшении pH раствора скорость окисления резко возрастает. Очевидно, на реакцию окисления влияет про-толитическое равновесие [c.193]
Примером реакции второго порядка может служить омыление эфира в щелочном растворе [c.265]
К реакциям второго порядка относится, например образование Н1 из Нг и Ь, реакции омыления эфиров [c.133]
Частный порядок находится несколькими методами. Наиболее простой метод подртановок заключается в том, что подставляют экспериментальные данные с = / (т) в кинетические уравнения разных порядков и находят, какое из них дает постоянную величину константы скорости. Например, если провести реакцию омыления эфира щелочью и подставить время и концентрации в уравнение первого порядка, то к не будет постоянной величиной (0,089 0,077 0,060 0,050 0,039). Если же эти данные подставить в уравнение второго порядка, то значения к будут практически постоянными (0,0070 [c.237]
На активированном оксиде алюминия некоторые вещества претерпевают химические превращения, например, возможны омыление эфиров, реакции конденсации с альдегидами и кетонами, реакции изомеризации и полимеризации олефинов и т. д. Поэтому оксид алюминия нельзя использовать для разделения таких веществ. [c.57]
Опыт 142. Изменение концентрации ионов водорода при омылении эфира [c.85]
Омыление эфира карбоновой кислоты щелочью, вероятно, протекает по следугон1ен схеме вначале ОН-нон присоединяется к атому углерода карбоксильной группы а, а затем происходит отщепление протона от атома кислорода при действии второй молекулы щелочи б. Из образовавщегося нестабильного промежуточного продукта выделяется в виде аниоиа а,лкоксигруппа, чем и завершается процесс омыления Э( )ира [c.263]
Оксистирол получен омылением эфиров 4-оксистирола с бензойной или 4-толуолсульфокислотой [374]. [c.78]
Это означает, что период полураспада для гомогенных реакций второго порядка, протекающих в растворе, зависит от к о н-де1 1 р ации, а в азовой средеот д а в л е н и Примером 6иш)лекул яркой реакций 11" раствор может служить омыление эфиров щелочами, например [c.219]
Практикум по органической химии (1956) -- [ c.84 , c.202 ]Органическая химия (1979) -- [ c.413 ]
Технология белковых пластических масс (1935) -- [ c.44 , c.45 ]
Практикум по органической химии Издание 3 (1952) -- [ c.85 , c.203 ]
Органическая химия Издание 3 (1963) -- [ c.201 ]
Органическая химия (1956) -- [ c.191 ]
Физическая химия Том 1 Издание 4 (1935) -- [ c.424 , c.425 , c.431 ]
Практикум по органической химии (1950) -- [ c.85 , c.203 ]
Методы органической химии Том 2 Издание 2 (1967) -- [ c.513 , c.515 , c.947 , c.948 , c.981 ]
Методы органической химии Том 2 Методы анализа Издание 4 (1963) -- [ c.513 , c.515 , c.947 , c.948 , c.981 ]
chem21.info
Омыление - сложный эфир - Большая Энциклопедия Нефти и Газа, статья, страница 2
Омыление - сложный эфир
Cтраница 2
При омылении сложного эфира, а также при перегонке кислоты не происходит в заметной степени изомеризации с перемещением двойной углерод-углеродной связи; таким образом, полученная 2-метил - 2-додецсновая кислота будет иметь двойную связь в том же положении, что и образец сложного эфира, из которого она была получена, следовательно, она нацело состоит из а р-непредельного изомера. [16]
При омылении чисто алифатических сложных эфиров, например образованных ос-замещенными уксусными кислотами, резонанс невозможен. [17]
Что такое омыление сложного эфира и как оно производится. [18]
В результате омыления сложного эфира образуются кислота и спирт. [19]
Согласно реакции омыления сложных эфиров одноосновных кислот щелочью, одна молекула эфира требует для омыления одну молекулу щелочи, следовательно, 1 мл щелочи равен молекулярному весу эфира, помноженному на нормальность щелочи или кислоты. [20]
Опыты по омылению сложных эфиров расширяют общее понятие учащихся о химической реакции, так как в весьма наглядной форме дополняют его сведениями об обратимости реакций и роли катализаторов. [21]
Гидроксильные ионы ускоряют омыление сложных эфиров еще сильнее, чем водородные ионы. Поэтому омыление сложных эфиров щелочами протекает в ряде случаев в 1000 и более раз быстрее, чем омыление кислотами. [22]
Метод заключается в омылении сложных эфиров раствором щелочи. [23]
Например, при омылении водой сложного эфира в разбавленном водном растворе изменение концентрации воды весьма незначительно и скорость реакции зависит лишь от изменения концентрации эфира. В результате кинетика этой реакции описывается уравнением первого порядка, несмотря на то, что реакция бимолекулярная. [24]
КОН, необходимое для омыления сложных эфиров, содержащихся в 1 г данного вещества. [25]
КОН, необходимое для омыления сложных эфиров, содержащихся в 1 г данного вещества. [26]
В противоположность кислотно-катализируемому гидролизу омыление сложных эфиров идет необратимо. [27]
Олигосахарнды 237 ел - Омыление сложных эфиров 173 Оптическая активность 186 ел. [28]
Кислый гидролиз позволяет сразу провести омыление сложного эфира и дегидратацию спирта. [29]
При действии разбавленных щелочей происходит омыление сложного эфира. [30]
Страницы: 1 2 3
www.ngpedia.ru
Сложные эфиры. Реакции этерификация и омыления
При взаимодействии обычной бензойной кислоты с метанолом, который содержал повышенное количество (0,379%) О , было установлено образование лишь обычной воды таким образом, кислородный атом образующейся при этерификации воды отщепляется от бензойной кислоты, а не от метанола, и, следовательно, этерификация протекает в соответствии с уравнением (а). При обратной реакции — гидролизе сложных эфиров водой, содержащей О , меченый кислород входит в образовавшуюся кислоту, а не в спирт, и, значит, омыление протекает по схеме [c.262] Взаимодействие кислоты со спиртом, приводящее к образованию сложного эфира, называется этерификацией. Процесс этот обратим обратная реакция называется реакцией гидролиза или омыления [c.121]Сложные эфиры. Реакции этерификации и омыления [c.329]
Наряду е этерификацией протекает и обратная реакция гидролиза (омыления), при которой сложный эфир расщепляется на кислоту и спирт. В зависимости от природы и количества участвующих в реакции этерификации кислоты и спирта равновесие реакции сдвигается в ту или иную сторону. [c.162]
Реакция этерификации обратима сложный эфир, реагируя с водой (гидролизуясь), образует спирт и кислоту. Реакция гидролиза сложного эфира называется омылением. Вследствие обратимости реакция этерификации требует для своего осуществления применения концентрированных кислот. [c.79]
Например, процесс этерификации с образованием сложного эфира связан с противоположной реакцией омыления эфира водой [c.95]
Гомогенных каталитических реакций в растворах, ускоряем мых ионами гидроксила и водорода, довольно много. К реакциям этого типа относятся этерификации кислот и спиртов, инверсия сахаров, галоидирование соединений, содержащих карбонильную группу, омыление сложных эфиров и др. [c.286]
Химические свойства. Реакция гидролиза (омыления) сложных эфиров является обратной реакции этерификации. Процесс может проходить как в кислой, так и щелочной среде. В присутствии кислот реакция обратима, так как образующиеся при этом кислота и спирт вновь реагируют с образованием сложного эфира [c.346]
Процесс обратим, и реакция образования эфира называется реакцией этерификации, а обратная ей - реакцией омыления. Название сложного эфира образуется из названия спирта и кислотного остатка. Например, полученное выше соединение на- [c.423]
Реакция образования простых эфиров целлюлозы необратима. В отличие от сложных эфиров, степень этерификации которых можно регулировать изменением состава этерифицирующей смеси (при нитровании целлюлозы) или последующим омылением продукта реакции (при получении ацетатов или ксантогенатов), для простых эфиров целлюлозы эти методы регулирования степени замещения не могут быть использованы. [c.373]
Ацилирующие средства галогенангидриды, ангидриды, сложные эфиры. Дцилирование спиртов, фенолов, аминов, аммиака. АциТгиро-вание по Фриделю—Крафтсу. Этерификация. Механизм реакции этерификации. Кислотный и щелочной гидролиз. Омыление жиров. [c.92]
Реакция взаимодействия сложного эфира с водой, право-дящая к образованию спирта и кислоты, называется омылением или гидролизом. Она обратна реакции этерификации. [c.393]
Реакция этерификации обратима она не доходит до конца, так как наряду с этерификацией идет и обратная реакция гидролиза (омыление), т. е. расщепление сложного эфира на кислоту и спирт. [c.254]
Химические свойства наличие поляризованного атома кислорода активирует связь С-О-Н и она легко разрывается даже под действием воды Расщепление сложных эфиров ПОД действием воды называется гидролизом или омылением Эта реакция обратна реакции этерификации Реакция катализируется протонами Н и гидроксид-ионами ОН В присутствии щелочи реакция необратима (происходит омыление — образование соли карбоновой кислоты) [c.44]
Сохранение конфигурации, наблюдаемое для некоторых реакций замещения, может быть обусловлено самыми различными причинами. Во-первых, конфигурации молекул не меняются при реакциях, которые не вызывают разрыва связей между асимметрическим атомом углерода и соседними атомами. В качестве примера можно привести реакцию этерификации оптически активных вторичных спиртов (а) (см. стр. 327), протекающую по механизму третьего порядка, или омыление соответствующих сложных эфиров (б) (см. стр. 190) [c.484]
Реакцию, обратную этерификации, — омыление (или гидролиз) сложных эфиров, можно показать на примере омыления жиров. Жиры представляют собой смесь сложных эфиров трехатомного спирта глицерина и высокомолекулярных кислот стеариновой, пальмитиновой и олеиновой. При нагревании с раствором едкого натра сложный эфир гидролизуется образуется натриевая соль высокомолекулярной кислоты (мыло) и глицерин (уравнение реакции ). Эти опыты можно провести с различными жирами говяжьим, свиным или бараньим салом, коровьим маслом. Жир расплавляют в фарфоровой чашке, приливают к нему концентрированный раствор едкого натра и кипятят при размешивании, добавляя дистиллированную воду по мере упаривания раствора. Нагревание продолжают до тех пор, пока проба массы не будет полностью растворяться в воде. По достижении полноты омыления к массе добавляют при перемешивании горячий насыщенный раствор поваренной соли и охлаждают ее. Всплывший наверх слой мыла отделяют, заворачивают в кусочек ткани и отжимают. [c.108]
На основании проведенной работы найдены следующие условия для получения сложных эфиров синтетических кислот и многоатомных спиртов. К навеске кислот добавляют рассчитанное количество гликоля или глицерина, что составляет 5,5—6,5% взятых кислот при перемешивании реакционную смесь нагревают до 150°С. При этой температуре вводят катализатор из расчета 0.2% от кислот и процесс продолжают в течение 6 часов. Затем температуру повышают до 240 С, при которой реакцию продолжают 15 мин., затем процесс считают законченным. Общая продолжительность процесса этерификации 8--10 часов. Нагревание реакционной смеси прекращают в том случае, если продукт застывает при охлаждении на стекле. В случае проведения реакции этерификации со смесью кислот конечный продукт имеет кислотное число 5 и число омыления 173. Реакция этерификации с глицерином протекает с большей скоростью, чем с гликолем. Наряду со смесью кислот, в качестве исходного сырья были применены карбоновые кислоты и оксикислоты. [c.182]
Реакция гидролиза сложных эфиров (или омыления) обрат-на реакции этерификации [c.147]
В результате омыления сложного эфира образуются кислота и спирт. Реакция омыления обратна реакции образования сложного эфира из кислоты и спирта (реакции этерификации). [c.139]
Как реакция этерификации карбоновой кислоты, так и реакция омыления сложного эфира протекает чрезвычайно медленно даже при нагревании. Скорости обеих реакций значительно возрастают в присутствии сильных кислот, действующих каталитически, Щелочи также ускоряют омыление сложных эфиров, [c.139]
Реакции этерификации обратимы, а следовательно, ограничены состоянием равновесия. Реакции, обратные этерификации, состоящие в том, что сложный эфир, присоединяя воду, превращается в спирт и кислоту, называются реакциями омыления или гидролиза. [c.206]
Чрезвычайно важным способом получения сложных эфиров является реакция этерификации (см. стр. 205), т. е. непосредственное взаимодействие спирта с кислотой. Ка уже было указано, процесс этот обратим обратная реакция, дающая спирт и кислоту, называется реакцией омыления. Обе реакции (прямая и обратная) [c.308]
Дается определение реакции омыления реакция, обратная этерификации, т. е. реакция взаимодействия сложного эфира с водой в щелочной или кислой среде с образованием кислоты и эфира [c.114]
Эта реакция обратима. Реакция получения сложных эфиров называется реакцией этерификации, обратная реакция разложения сложного эфира на кислоту и спирт называется реакцией омыления. [c.63]
Способностью легко гидролизоваться сложные эфиры резко отличаются от простых эфиров, которые очень стойки к гидролизу. Ионы водорода, катализирующие реакцию этерификации, ускоряют также и омыление сложных эфиров. [c.244]
Обратим ыереакциивторогопорядка А + В А + + В. Примером реакции подобного типа могут служить реакции омыления сложных эфиров и этерификация. Формула скорости реакции для данного случая будет иметь следующий вид [c.24]
Анализ опытного материала по катализу привел ряд исследователей (С. 3. Рогинский [3], М. И. Темкин и др.) к выводу о том, что кислотному катализу подвержены преимущественно, если не исключительно, гетеролитические реакции. К реакциям, катализируемым кислотами, в частности, относятся образование полимеров и их распад до мономеров омыление простых и сложных эфиров и процессы этерификации , гидратация, изомеризация, полимеризация и гидрогалоидирование оле-фИ Новых углеводородов дегидратация спиртов, оксикислот и других гидроксилсодержащих соединений алкилирование, сульфирование и нитрование ароматических и парафиновых углеводородов декарбонили-рование, декарбоксилирование и дегидратация карбоновых кислот кето-энольные, прототропные и оксотропные превращения гидролиз сахаров и многие другие. [c.256]
Эта реакция (обратная этерификации) носит название реакции омыления. Практически необратимая ре акция омыления сложных эфиров протекает в ирисут ствии щелочей. [c.417]
Наиболее широко распространенный метод получения этилового эфира метилмалоновой кислоты состоит в алкилировании малонового эфира иодистым метилом бромистым метилом или ди.ме-тилсульфатол Отделение конечного продукта от следов не изменившегося исходного продукта и от этилового эфира диметилмалоновой кислоты не может быть достигнуто перегонкой, так как точки кипения всех трех сложных эфиров лежат в пределах 3,5°. Михаэль 1 нашел, что не вступивший в реакцию малоновый эфир может быть полностью отделен, если воспользоваться тем, что он легче омыляется щелочью, а Гэн и Ингольд получили чистый продукт путем омыления, перекристаллизации метилмалоновой кислоты и последующей этерификацией. На основании опытов Сальковского мл. с ацетоуксусным эфиром можно сделать заключение, что в случае применения бромистого метила в качестве алкилирующего агента образование диметильного производного не имеет места. Методика Б, основанная на работе Михаэля описана в литературе [c.591]
Но так как эти последние в отношении методов их получения и в отношении их свойств и реакций отличаются от типичных алкоксильных соединений, простых эфиров, ацеталей и сложных эфиров ортокислот, то в настоящей главе они не описываются. О них говорится в отделе Этерификация и омыление (т. И). [c.163]
Все эти реакции имеют много общего принципы, лежащие в их основе, будут пояснены главным образом на примере реакций сложных эфиров, поскольку такого рода превращения изучены наиболее полно. Катализируемый кислотой гидролиз сложных эфиров является реакцией, обратной катализируемой кислотой этерификации, которая была рассмотрена выше (стр. 351—353 и 463—465). В противоположность этому происходящий под действием щелочи гидролиз (омыление) практически необратим. Начальная стадия последнего заключается в атаке гидроксил-иона на электронодефицитный углерод карбонильной группы в результате образуется промежуточный анион XI, который может либо отщепить ОН и превратиться в исходный эфир, либо отщепить СНзО и перейти в кислоту. В целом реакция необра- [c.479]
Химические свойства. Наиболее важной реакцией сложных эфирвв является реакция омыления, обратная реакции этерификации. Кроме кислот, омыление могут вызывать также и щелочи, с которыми омыление происходит даже лучше, чем с кис-лота.ми, причем в данном случае реакция необратима, так как происходит нейтрализация образовавшейся кислоты. В растительном мире весьма распространены энзимы (так называемые эстеразы), обладающие способностью каталитически расщеплять сложные эфиры. Один из таких энзи.мов — рициназа содержится в семенах клещевины. [c.309]
Реакция получила название реакции этерификации от латинского aether — эфир. Скорость этерификации зависит от силы кислоты н природы спирта с увеличением силы кислоты она возрастает, первичные спирты реагируют быстрее вторичных, последние быстрее третичных. Этерификация спиртов органическими (карбоновыми) кислотами ускоряется добавлением сильных минеральных кислот. Реакция обратима, обратная реакция получила название гидролиза. Гидролиз сложных эфиров, проводимый водными растворами щелочей, называется омылением (стр. 146). [c.97]
Под действием щелочей и кислот сложные эфиры расщепляются и дают сбратио спирт и кислоту. Реакция расщепления эфира под действием воды в присутствии кислоты называется гидролизом, а под действием щелочи—омылением по аналогии с процессом получения мыла из жиров. Последние представляют собой сложные эфиры глицерина и жирных кислот (стеариновой, пальмитиновой и олеиновой). Под действием щелочи эфир расщеп-ляется на глицерин и жирные кислоты, образующие с щелочью мыла. Мыла представляют собою щелочные соли жирных кислот. Процесс этерификации сопровождается одновременно и обратным процессом— расщеплением эфиров, что и отмечено в приведенных формулах двумя стрелками, направленными в противоположные стороны. Такие процессы и реакции называются обратимыми. Поэтому процесс этерификации без добавки, например, серной [c.15]
Изучая реакцию спирт + кислота = сложный эфир -f вода, Бертло и Сен-Жмль (1862) пришли к выводу, что эта реакция никогда не идет полностью в одном направлении (т. е. в сторону этерификации или омыления), а всегда приближается к определенному пределу, соответствующему равновесию. Бертло и Сен-Жиль установили зависимость между скоростью реакции и пределом превращения. Это оказалось возможным потому, что они избрали органические реакции, в которых равновесие устанавливается гораздо медленнее, чем при реакциях неорганических кислот, оснований и солей. Изучив различные комбинации органических кислот и спиртов, авторы пришли к выводу, что если реагенты вступают во взаимодействие в эквивалентных количествах, то почти независимо от их природы, разбавления и температуры равновесное состояние достигается, после того как прореагирует около 60— 70% исходных веществ. [c.118]
chem21.info
Омыление сложного эфира натрия - Справочник химика 21
Сложные эфиры обнаруживают по их способности омыляться щелочами. Растворяют 0,1 г вещества в 3—5 мл спирта. Добавляют несколько капель раствора фенолфталеина и по каплям такое количество 0,1 н. раствора едкого натра в метиловом спирте, чтобы стало заметно красное окрашивание. Пробирку 5 мин нагревают на водяной бане при 40 С. Исчезновение красного окрашивания указывает на образование кислоты в результате омыления сложного эфира. [c.125] Другой способ определения влаги в спирте состоит в применении в качестве реактива раствора этилового эфира муравьиной кислоты и безводного этилата натрия в абсолютном спирте. В присутствии следов воды происходит омыление сложного эфира с образованием муравьинокислого натрия, который, будучи нерастворим в спирте, выпадает в осадок. [c.47]Сырой алкилат промывается 5% раствором едкого натра и затем в присутствии этого раствора отгоняется пропан (170 °С, 14 кгс/см ). Для омыления сложных эфиров серной кислотой (из пропилена и серной кислоты) требуется высокая температура. Во второй колонне под давлением 1,7 кгс/см отгоняется бензол и, наконец, в третьей колонне получают чистые фракции кумола. Ниже приведены результаты, полученные на промышленной установке [241 [c.265]
Омыление. Сложный эфир омыляют кипячением в течение 5 час. с 75 мл 10%-ного раствора едкого натра, к которому прибавлено [c.198]
При щелочном гидролизе применяют водные или спиртовые растворы щелочей. Если образующиеся в результате гидролиза соединения неустойчивы к действию сильных щелочей, то используют растворы карбоната натрия, бикарбоната натрия, поташа. Эфиры первичных спиртов омыляются щелочными агентами легче, чем эфиры вторичных и третичных спиртов. В этом случае действует правило чем легче образуются эфиры, тем легче протекает их гидролиз. Омыление сложных эфиров кислотами используется редко. Скорость гидролиза в этом случае также увеличивается с повышением температуры. [c.250]
Пожалуй, ни один метод определения сложных эфиров не распространен так сильно и не применяется столь часто, как количественное омыление сложных эфиров, тем не менее многим неизвестно, что в смесях растворителей сложные эфиры могут полностью омыляться избытком раствора едкого натра за 1—2 ч при энергичном взбалтывании при комнатной температуре, а низшие эфиры иногда омыляются даже в течение 10 мин. [c.981]
Задача 3. Для омыления 26 г триглицерида потребовалось 49,2 мл 20%-ного раствора гидроксида натрия (пл. 1,22 г/мл). Определите формулу сложного эфира, взятого для реакции. [c.340]
Обратимся к простому примеру, для того чтобы пояснить этот подход. Рассмотрим вначале реакцию омыления сложных эфиров — одну из первых реакций, которая была изучена кинетически. Как установлено химическим анализом, этилбензоат реагирует с гидроокисью натрия в водном растворе по следующему уравнению [c.11]
Для омыления 14,8 г глицерида потребовалось 72 мл 10%-ного раствора едкого натра (пл. 1,12 г см ). Определить формулу сложного эфира, взятого для реакции. [c.435]
Гидроокись калия, едкое кали КОН — белое кристаллическое гигроскопическое вещество. Выпускается в виде кусочков, палочек, гранул или чешуек. Гидроокись калия широко используется в синтетических работах для получения калиевых солей и проведения технологических процессов, обеспечивающих лучшие результаты, чем с едким натром. В аналитической химии КОН применяют для поглощения кислых паров и газов, нейтрализации кислых растворов, омыления сложных эфиров, титриметрических определений кислот, в газовом и органическом анализе и т. д. Едкое кали применяется также в тех случаях, где нежелательно применение едкого натра. [c.24]
Для определения сложных эфиров в ту же колбу, после оиределения кислот, добавляют 25 мл 0,1 и раствора едкого натра и содержимое колбы вновь кипятят с обратным холодильником на водяной бане в течение часа. При этом происходит омыление сложных эфиров [c.172]
При определении кислотности этилового спирта и содержания эфиров в нем, на титрование 100 мл спирта пошло 0,5 мл 0,1 н раствора едкого натра для омыления сложных эфиров было добавлено еще 25 мл 0,1 н раствора едкого натра, после омыления добавлено 25 мл 0,1 н раствора соляной кислоты, избыток которой оттитрован 4 мл 0,1 н раствора едкого натра. Вычислить содержание органических кислот в пересчете на уксусную кислоту и содержание сложных эфиров в пересчете на этилацетат в миллиграммах в литре спирта. (30 352). [c.199]
Реакции омыления сложных эфиров едким натром в разбавленных растворах при эквимолекулярных соотношениях реагентов являются реакциями второго порядка. Скорость необратимой реакции описывается уравнением [c.243]
Сложные эфиры угольной кислоты можно определять непосредственно в смеси растворителей, так как угольная кислота при обычном омылении сложных эфиров едким натром титруется как одноосновная кислота, а при омылении гидроокисью бария и титровании щавелевой кислотой определяется как двухосновная кислота. Разность, полученная при титровании, непосредственно соответствует содержанию угольной кислоты, т. е. количеству сложного эфира, которое можно вычислить, если известна его формула. [c.984]
В рассмотренном примере реакции омыления сложного эфира гидратом окиси натрия (см. табл. 92) мы видели, как, применяя к экспериментальным данным уравнения кинетики реакций первого и второго порядков, можно было заключить, что данная реакция является реакций второго порядка. [c.643]
При нагревании с раствором едкого натра не только нейтрализуются жирные кислоты, но и происходит гидролиз сложных эфиров, лактонов и эстолидов. Как правило, оксидат-сырец нагревают до 150° в автоклавах с мешалкой очень недолго, прибавляя 35%-ный раствор едкого натра в количестве, немного меньшем теоретического, т. е. найденного при определении числа омыления. Недостаток щелочи предупреждает кристаллизацию мыла (растрескивание), вызываемую слишком высоким содержанием соды. [c.457]
Простейший метод — метод Шоттена — Баумана, состоящий во встряхивании хлорангидрида кислоты с водным раствором едкого натра, содержащим соответствующий спирт. Самые высокие выходы получаются тогда, когда хлорангидрид кислоты (и образующийся эфир) нерастворимы в воде, так что реакция протекает на границе раздела между органическим и водным слоем. Нерастворимость образующегося сложного эфира в водной фазе препятствует его омылению. По окончании реакции эфир получается свободным от хлорангидрида кислоты и хлористого водорода и его можно сразу экстрагировать и сушить. В довольно старом и незаслуженно забытом [c.288]
Омыление сложных эфиров пептидов разбавленным водным раствором едкого натра в смеси с метанолом, диоксаном или ацетоном при комнатной температуре в течение 1 час не затрагивает карбобензилоксигрупп, но при увеличении концентрации щелочи, длительности процесса или повышении температуры образуются [c.168]
Для гидроксилсодержащих аминокислот наиболее употребительны бенэильная и трет-бутильная защитные группы. Вое—SeriBzl)—ОН полунаются прямым алкилированием Вое—Ser—ОН бензилбромидом в присутствии натрия в жидком аммиаке или гидрида натрия в диметилформамиде (выход около 50%). Вое—Thr(Bzl)—ОН более труднодоступен, выход его в тех же условиях составляет лишь 10%. С таким же низким выходом О-бензил-треонин получают и при этерификации карбоксильной и гидроксильной групп бензиловым спиртом в присутствии п-толуол-сульфокислоты с последующим щелочным омылением сложного эфира. [c.134]
При определении количественного и качественного состава кислородсодержащих соединений широко применяется инфракрасная спектроскопия благодаря наличию характеристических полос кислородных функциональных групп 3400—3600 см — валентные колебания атомов водорода гидроксильных групп кислот и фенолов, 1650—1740 см —валентные колебания карбонильной группы кислот, кетонов, сложных эфиров (лактонов), ангидридов кислот, амидов. Показано [49], что с помощью специфических химических реакций возможно провести идентификацию полос поглощения карбонильных групп различных классов соединений. Так, обработка карбоновых кислот бикарбонатом натрия приводит к образованию карбоксилатанионов, для которых характерно поглощение в области 1580—1610 см . Дальнейшая обработка образца гидроксидом натрия при нагревании вызывает омыление сложных эфиров, лактонов, ангидридов и образование карбоксилатанионов. В результате в области 1650— 1740 СМ наблюдается только поглощение кетонов. Пользуясь групповыми интегральными коэффициентами поглощения (для карбоновых кислот 1,24-10 л/(моль-см), сложных эфиров 1,15 10 кетонов 0,72-10 л/(моль-см) [50], можно определить концентрацию соединений каждого типа. Применение методов ИК-спектроскопии в исследованиях состава нефтей 51] позволило обнаружить и количественно оценить наличие карбоновых кислот, фенолов, амидов, 2-хинолонов. Отмечено, что точность анализа значительно снижается вследствие межмолекулярной ассоциации компонентов, что приводит к уменьшению интенсивности поглощения групп и занижению результатов. Повышение точности достигается разбавлением растворов и использованием в качестве растворителей тетрагидрофурана или дихлорметана. Однако более значительные ошибки возникают из-за неверной оценки молекулярных масс определяемых соединений и наличия в молекуле более одного гетероатома. Исправление этого положения возможно препаративным выделением одного класса соединений и установления коэффициента поглощения данной функциональной группы. [c.50]
Омыление щелочью наиболее часто применяется для количественного определения содержания большинства сложных эфиров, в том числе и жиров, а также продуктов этерификации фенолов. Наибольшее влияние на реакцию омыления оказывают следующие факторы достаточная концентрация ионов гидроксила в растворе, хорошая растворимость анализируемого вещества во взятом растворителе и высокая температура реакции омыления. Сравнительно легко растворимые в воде сложные эфиры (как, например, этил-формиат, метилформиат, этилацетат и др.) могут быть омылены водными растворами щелочей. Сложные эфиры, плохо растворимые в воде, омыляют в спиртовой среде. Для этого пользуются спиртовыми растворами едкого кали или едкого натра. Можно прямо растворить сложный эфир в этиловом спирте, а затем прилить определенное количество водного раствора титрованной щелочи и омылить эфир. Спиртовые растворы едкого кали более предпочтительны вследствие хорошей растворимости едкого кали в спирте, особенно при получении его концентрированных растворов. Скорость омыления сложных эфиров различна. Она зависит от природы входящих в состав сложного эфира кислоты и спирта. В одних случаях реакция омыления протекает быстро даже при обычной комнатной температуре, в других [c.249]
Фталильную группу можно отщепить только гидразинолизом. Реакцию проводят обычно с помощью гидразингидрата в метаноле или этаноле при кипячении в течение 1—2 час [848, 2060, 2062] или при длительном выдерживании при комнатной температуре [230, 1241, 2055]. Описано также применение в качестве растворителей грет-бутилового спирта [2280], диоксана [230] и водного раствора бикарбоната натрия [1241]. Фталазин, образующийся при гидразинолизе, осаждают подкислением реакционной смеси соляной [2055, 2060, 2062] или уксусной кислотой [848] его можно удалить также в виде натриевой соли обработкой раствором углекислого натрия [2280]. Отщепление фталильной группы проводят обычно после омыления сложных эфиров, чтобы предотвратить одновременный гидразинолиз сложноэфирных связей. Описано несколько случаев гидразинолиза фталильной группы без разрыва сложноэфирных связей [894, 1236, 2055, 2072]. При взаимодействии фениловых эфиров фталиламинокис- [c.39]
Особенно стойкие по отношению к омылению сложные эфиры, в том числе и диборнилфталат, могут быть определены омылением раствором третичнобутоксида натрия [c.163]
Сложные эфиры салициловой кислоты имеют свободную фенольную группу HO 6h5 OOR и дают растворимые в воде салицилаты щелочных металлов. Для отделения салицилатов от эфиров других спиртов предложено обрабатывать смесь, растворенную в петролейном эфире, 5%-ным раствором едкого натра, взятым в избытке, при охлаждении [28]. Натриевое производное мегилсалицилата выпадает в виде осадка. Идентификация салицилатов после омыления сложного эфира выделяют подкислением из щелочного раствора кристаллическую салициловую кислоту, т. пл. 159° С. [c.307]
Можно этерифицировать смесь кислот раствором соляной к-ты в метиловом спирте фенольный гидроксил при этом не этерифицируется поэтому после удаления спирта можно извлечь сложные эфиры фенолкар-боновых кислот двунормальным раствором едкого натра. Смесь остальных сложных эфиров можно разделить фракционной перегонкой (об омылении сложных эфиров см. стр. 249). [c.238]
В конце электролиза ток и воду выключают, пористый сосуд отъединяют и содержимое его выливают в лабораторный стакан объемом 800 мл. Сосуд промывают водой и промывные воды соединяют с католитом в лабораторном стакане. Католит нейтрализуют твердой содой, высаливая при этом слой раствора бензилового спирта в этиловом спирте. Слой отделяют от католита и нагревают с 15 г едкого натра с обратным холодильником в течение одного часа для омыления сложных эфиров. После омыления спиртовую жидкость подвергают перегонке с паром до тех пор, пока не пойдет совершенно прозрачный дестиллат. После этого дестил-лат высаливают и выделившийся слой высушивают поташом и затем перегоняют, пока термометр не покажет 120°. Нейтрализованный католит и остаток от перегонки с паром экстрагируют эфиром, вытяжку высушивают в течение ночп безводным сульфатом магния и соединяют с сырым бензиловым спиртом в перегонной колбе. Эфир отгоняют и оставшийся бензиловый спирт взвешивают. Вес равен 14 г, т. е. выход 79%. Бензиловый спирт получается почти чистым и перегоняется при 200—202° (неиспр.). [c.27]
Омыление сложного эфира. Сложный эфир помещают в скляночку для взвешивания, снабженную небольшой пипеткой. Определяют общий вес скляночки, пипетки и сложного эфира, и пробу сложного эфира в количестве около 0,2—0,4 г с помощью пипетки переносят в коническую колбу емкостью 150 мм скляночку с пипеткой вновь взвешивают и по уменьшению веса определяют навеску сложного эфира. Затем в колбу с эфиром прибавляют из бюретки точно 15 мл титрованного спиртового раствора едкого натра. Колбу соединяют с хорошо действующим обратным холодильником при помощи тщательно очищенной резиновой пробки, и смесь слабо кипятят в течение 1,25—1,5 час. По истечении этого времени смеси дают несколько остыть. Колбу освобождают от холодильника резиновую пробку и трубку холодильника промывают из промывалки струей воды так, чтобы промывная вода стекала в реакционную смесь. Прибавляют 2 капли фенолфталеина и избыток щелочи титруют 0,25 н. раствором соляной кислоты до слаборозовой окраски. Лучше титровать раствор до исчезновения окраски фенотфталеина и затем избыток кислоты оттитровать той же щелочью. [c.139]
Конденсация фрагмента [Н (1 —2 )-6—8] с ранее описанным пентапептидом (Н 1—5) с помощью карбодиимидного метода привела с выходом 40% к разветвленному декапептиду [I (1 — 2 )-1—8], охарактеризованному количественным аминокислотным анализом и УФ-спектром. Формильную группу отщепляли действием 4 н. метанольного раствора НС1 в трифторуксусной кислоте или диметилсульфоксиде в течение 20 час при 20 [К ( —2 )-1—8] [2392]. Освободившуюся аминогруппу вновь количественно идентифицировали колориметрическим нингидриновым методом. Последующее омыление сложного эфира проводили обработкой 1,5-кратным избытком 1 н. едкого натра в диметилсульфоксиде в течение 20 час [L(l —2 )-1—8] образовавшуюся свободную карбоксильную группу определяли микротитрованием. Циклизацию синтезированного разветвленного декапептида осуществляли путем перемешивания при 20° раствора декапептида с 300-кратным избытком N, N -дициклогексилкарбодиимида в условиях высокого разбавления, причем выход неочищенного продукта реакции составил 20%. Защитные группы отщепляли действием натрия в жидком аммиаке. Полученный циклический пептид был очищен путем противоточного распределения (400 переносов вго/7-бутанол/0,1 н. соляная кислота) и хроматографирования на целлюлозном порошке (н-бутанол/ пиридин/ледяная уксусная кислота/вода, 30 20 6 24 м-бута-нол, содержащий 15% уксусной кислоты) с последующим обессоливанием на амберлите ШС-50 (ХЕ-64) в Н+-форме. [c.566]
В метанол-сырец, поступающий на дистилляцию, добавляют раствор едкого натра для омыления сложных эфиров и нейтрализации кислот, которые могут вызывать коррозию аппаратуры. Вначале отгоняют диметиловый эфир, а затем азеотропную смесь побочных продуктов с водой. После этого метанол проходит химическую очистку перманганатом калия, который добавляют в виде 2%-ного водного раствора. Метанол и высщие спирты более стабильны к действию перманганата, чем карбонильные соединения (которые переходят в кислоты, нейтрализуемые едким натром, ранее добавленным к метанолу-сырцу). В этих условиях пентакарбонил железа разрушается полностью, а КМп04 при окислении превращается в МпОг, который отделяют на фильтр-прессах. Окончательную дистилляцию метанола осуществляют в колонке с большим числом тарелок (примерно 75). На нижних тарелках собирается изобутиловое масло — фракция, содержащая изобутиловый и высшие спирты, примесь метанола и воду. Изобутиловый спирт отгоняют в другой колонне и получают в чистом виде как побочный продукт. Диметиловый эфир (т. кип. —23,7°С) используют частичное холодильной технике, а частично как топливный газ. [c.168]
Выполнение реакции. К 1 мл исследуемой смеси приливают при взбалтывании такое количество бромной воды, чтобы жидкость оставалась в течение одной минуты окрашенной в желтый цвет. На это следует израсходовать не более 1 мл бромной воды, иначе результат определения будет ненадежным. Затем обесцвечивают смесь несколькими каплями 40%-ного раствора едкого натра, прибавляют 4—5 мл чистого бес-цветно1 о пиридина и, в случае необходимости, еще столько же щелочи, чтобы образовалось два слоя. При нагревании смеси и взбалтывании в присутствий соединений, содержащих группу СН3СНОН-- или СН3СО—, соединенную с атомами углерода или водорода, пиридиновый слой более или менее быстро и сильно окрашивается в красный цвет. Если вначале появляется желтое окрашивание, то, продолжая кипячение, его обычно можно ослабить настолько, что оно не мешает различать розовую окраску (иногда с несколько коричневатым оттенком). При длительном кипячении в реакцию постепенно вступают и эфиры упомянутых вторичных спиртов, подвергающиеся омылению. Сложные эфиры, не являющиеся производными метилкарбинолов, мешают лишь тогда, когда добавлено слишком мало едкого натра. [c.944]
Амилнитрит отличается своеобразным плодовым запахом, напоминающим запах леденцов. При наличии амилнитрита в дистилляте последний также обладает специфическим запахом леденцов. Вследствие малой растворимости амилнитрита в воде при достаточном количестве его в дистилляте можно наблюдать наличие капель. Капли ВТИ при взаимодействии с раствором дифениламина в концентрированной серной кислоте дают синее окрашивание. Обнаружение амилшттрита, так же как и амилацетата, сводится к омылению сложного эфира едким натром [c.111]
Олеиновокислый натрий, помимо его эмульгирующего действия, выполняет при омылении хлористого амила еще одну функцию. Он участвует в реакции двойного обмена хлористого алкила, приводящей к образованию сложного эфира соответствующей жирной кислоты, которая затем быстро омыляется в щелочной среде с регенерацией олеиново -кислой соли и образованием спирта [c.219]
Для омыления стерически затрудненных сложных эфиров, которые трудно гидролизуются в обычных условиях, оказалось очень полезным использование краун-эфиров и криптатов. Педерсен и сотр. [504, 505] обнаружили, что дициклогексано-18-краун-6 способствует растворению гидроксидов калия и натрия в бензоле. При этом можно приготовить растворы концентра-цпей до 1 моль/л. В большинстве случаев этот комплекс сначала получают в метаноле, который затем замещают на бензол, однако около 1% СН3ОН удалить не удается. Таким образом, хотя в конечном растворе находятся как ионы ОН , так и СНзО [43, 504], этого вполне достаточно для гидролиза эфиров [c.246]
chem21.info
Омыление - сложный эфир - Большая Энциклопедия Нефти и Газа, статья, страница 1
Омыление - сложный эфир
Cтраница 1
Омыление сложного эфира проводят в конической колбочке емкостью 100 - 150 мл. [1]
Омыление сложных эфиров в присутствии минеральных кислот идет по той же схеме, но в обратном направлении. [2]
Омыление сложных эфиров катализируется как кислотой, так и щелочью. [4]
Омыление сложных эфиров - важнейшее их химическое свойство. В присутствии кислот и щелочей оно протекает довольно легко. С наибольшей скоростью реакция омыления протекает в щелочной среде. [5]
Омыление сложных эфиров кислотами i бораторной практике используется реже. [6]
Омыление сложного эфира ведут в конической колбочке емкостью 100 - 150 мл. В горло колбочки вставляют на плотной резиновой пробке обратный водяной холодильник или насадку с висячим холодильником, укрепленным на пробке с вырезом ( см. рис. 3 на стр. [7]
Омыление сложных эфиров карбоновых кислот в щелочной среде протекает быстрее, чем гидролиз в условиях кислотного катализа, так как нуклеофилыюсть гидроксил-аниона выше нуклеофильности молекулы воды. [8]
Омылением сложных эфиров; для практического получения спиртов наибольшее значение имеют эфиры галоидоводород-ных кислот - алкилгалогениды. [9]
Для омыления сложных эфиров серной кислотой ( из пропилена и серной кислоты) требуется высокая температура. Во второй колонне под давлением 1 7 кгс / см2 отгоняется бензол и, наконец, в третьей колонне получают чистые фракции кумола. [10]
После омыления предполагаемого сложного эфира идентифицируют спирт или фенол, а также кислоту, содержащиеся в продукте гидролиза. [11]
Скорость омыления сложных эфиров различна. [12]
Реакции омыления сложных эфиров едким натром в разбавленных растворах при эквимолекулярных соотношениях реагентов являются реакциями второго порядка. [13]
Скорость омыления сложных эфиров увеличивается с повышением температуры. [14]
При омылении сложного эфира, а также при перегонке кислоты не происходит в заметной степени изомеризации с перемещением двойной углерод-углеродной связи; таким образом, полученная 2-метил - 2-додеценовая кислота будет иметь двойную связь в том же положении, что и образец сложного эфира, из которого она была получена, следовательно, она нацело состоит из а, - непредельного изомера. [15]
Страницы: 1 2 3
www.ngpedia.ru




















