Справочник химика 21. Эфиры борной кислоты
Эфиры борной кислоты Бораты - Справочник химика 21
Эфиры борной кислоты. Эфиры борной кислоты — триалкилбораты — легко получаются нагреванием спирта и борной кислоты с добавкой концентрированной серной кислоты. Борнометиловый эфир (триметил-борат) кипит при 65° С, борноэтиловый (триэтилборат) — при 119° С. Эфиры борной кислоты легко гидролизуются водой. [c.115] Эфиры борной кислоты (бораты) получаются взаимодействием спиртов с борным ангидридом или с борной кислотой (обязательным условием успешного применения борной кислоты является удаление воды, выделяющейся в процессе реакции) [c.351]Реакция со спиртами. Реакцию выполняют в фарфоровом тигле или в чашке. Для реакции берут сухое вещество, а если анализируют раствор, то его предварительно выпаривают досуха. К сухому испытуемому веществу прилейте немного спирта и концентрированной серной кислоты, смесь перемешайте стеклянной палочкой и подожгите пламенем горелки. При наличии боратов пламя окрашивается в зеленый цвет. Бораты и борная кислота в сернокислой среде со спиртами образуют эфиры борной кислоты [c.409]
Летучие сложные эфиры борной кислоты окрашивают пламя в зеленый цвет. В присутствии серной кислоты и этанола борат-ионы образуют летучие сложные эфиры [c.232]
Для стерилизации насекомых предложены и некоторые простейшие эфиры борной кислоты. Борат глицерина предложен для борьбы с тараканами [18]. [c.495]
Боратами назьшают эфиры борной кислоты [c.345]
Реакция окрашивания пламени. В присутствии серной кислоты и этилового спирта борат-ионы легко образуют этиловый эфир борной кислоты, который окрашивает пламя горящего спирта в зеленый цвет [c.87]
Выполнены некоторые исследования эфиров борной кислоты 138, 39, 43] и самой борной кислоты [40]. В последнем случае частота валентных колебаний В — О составляет примерно 1400 сж , а частота деформационных колебаний около 810 СЛ1 , но обе они изменяются при изменении структуры соединения. У простых боратов связь В — О проявляется [43] около 1340 10 слг. что позволяет думать о наличии в какой-то мере характера двойной связи. [c.494]
Открытие тетраборат-иона Тстраборат-ион обнаруживают в oi-дельной пробе анализируемого раствора (4—6 капель) по окрашиванию в зеленый цвет пламени горелки сложными эфирами борной кислоты (см. выше Аналитические реакции борат-ионов В О и ВО ). [c.487]
Прм Применяется для отбелки шерсти, шелка и т.п.,д.чя дезинфекции. ЭФИРЫ БОРНОЙ КИСЛОТЫ борно-метиловый эфнр (триметил борат) - В(ОСНз)з, [c.84]
Реакция сильно смещена вправо, поэтому для повышения устойчивости раствора ее проводят в присутствии спирта. Для стабилизации раствора кремниевой кислоты к нему добавляют борную кислоту, бораты или несколько капель концентрированной минеральной кислоты [138]. Устойчивость раствора кремнеэтилового эфира повышают, заменяя спирт ацетоном. Для получения коллоидного раствора кремниевой кислоты используют 85 % этиловый спирт к 100 мл тетраэтилового эфира ортокремниевой кислоты (свежеперегнанного при 167—168 °С) приливают при энергичном перемешивании 45 мл 85 % этилового спирта. К смеси добавляют 15 мл воды и 2 капли концентрированной азотной кислоты. В растворе находятся в равновесии эфир и ортокремниевая кислота. [c.103]
Спирт в смеси с концентрированной серной кислотой при действии на сухое исследуемое вещество, содержащее борат-ионы, образует эфир борной кислоты [c.63]
Опыт 3. Обнаружение борат-ионов. Чувствительная реакция на бор основана на способности его соединений окрашивать пламя в зеленый цвет. Одну-две крупинки буры поместите в тигель, добавьте несколько капель концентрированной серной кислоты и несколько капель метилового или этилового спирта, смесь перемешайте стеклянной палочкой и зажгите. Заметьте зеленую окраску пламени. Пламя окрашивается образующимся при реакции летучим эфиром борной кислоты со спиртом—В(ОСгИ5)з. [c.200]
Одними из практически ценных борорганических соединений являются эфиры борной кислоты —триалкил(арил)бораты. Существует несколько способов получения этих эфиров. [c.312]
Эфиры борной кислоты и ее производных. При взаимодействии моносахаридов и их производных, содержащих ггликольные группировки, с борной кислотой или ее солями образуются устойчивые отрицательно заряженные комплексы. Это свойство нашло широкое применение для разделения сахаров методом распределительной хроматографии и электрофореза на бумаге а также методом ионообменной хроматографии на смолах и угле Борные эфиры сахаров были в свое время успешно использованы для установления конфигурации аномерного центра (см. стр. 34). Несмотря на то что комплексы сахаров с борат-анионом известны давно, строение их было выяснено только недавно Было показано, что существуют два типа боратных комплексов монокомплекс XXVII и дикомплекс XXVIII [c.148]
Советскими учеными А. Н. Башкировым и В. В. Камзолкиным разработан оригинальный метод нолучения спиртов в качестве целевого продукта окнсления парафинов [156—161]. Выход спиртов достигает 60—70% на исходное сырье. Суш,ность способа заключается в проведении процесса окисления в мягких условиях азот-кислородной смеси с содержанием кислорода 3—4,5% и прекращения окисления на стадии образования спиртов путем связывания их в эфиры борной кислоты. Отделение спиртов от углеводородов в данном случае весьма просто, так как бораты выкипают при более высоких температурах, чем непрореагировавшие парафины. Спирты выделяются и ректифицируются так, как это [c.101]
Пирокатехин и его производные реагируют с борной кислотой в щелочном растворе с образованием комплексов, которые устойчивы в щелочной среде, но полностью гидролизуются разбавленными кислотами. Флавоны и флавонолы, содержащие гидроксильные группы в положениях 3 и 4, могут быть превращены в водном растворе в боратные комплексы, причем гидроксильная группа в положении 5, если она имеется, также реагирует с боратом (ср. раздел Эфиры борной кислоты , стр. 238). Другие фенольные и енольные гидроксильные группы могут быть затем подвергнуты избирательному метилированию после подкисления образуется частично метилированный флавон или флавонол. Частичное метилирование кверцетина LXXII в его 3,7-диметиловый эфир уже упоминалось в связи с защитой фенолов (см. раздел Эфиры борной кислоты , стр. 238). Получение частично метилированных флавонов и родственных соединений описано в ряде работ [391—394]. [c.243]
В качестве антинагарных присадок исследовано значительное количество различных соединений, как, например, трибутилфосфит, триметплфосфит или фосфат, хлорпропилтиофосфат, циклический фосфат, триалкилфосфины, алкарилтиофосфаты или тиофосфиты, алкилборные кислоты или их эфиры, полигликолевые эфиры борной кислоты или эфиры низших алкоголей, бораты гликолей и др. [23]. [c.300]
В ЭТОМ методе бор отгоняют из кислого раствора дистилляцией с метиловым спиртом в виде метилового эфира борной кислоты, последний собирают и определяют бор либо весовым, либо объемным методом. При анализе простых боратов, особенно растворимых, этот метод дает удовлетворительные результаты, если были соблюдены все необходимые меры предосторожности удовлетворительные результаты также при анализе трудно разлагаемых боросиликатов были получены Чэпиным [c.1032]
Вариант 2. В маленьком тигле выпарьте 3—4 капли испытуемого раствора. Сухой остаток смочите серной кислотой, обработайте при нагревании 5 каплями этилового эфира кремневой кислоты или смесью, состоящей из равных объемов метилового спирта и концентрированной HgSO . Выделяющиеся пары подожгите. В присутствии боратов образуются летучие эфиры борной кислоты, и пламя окрашивается в зеленый цвет. [c.370]
Из реакционной массы, образующейся при разложении борато-вой руды, борную кислоту можно извлекать спиртами (или фенолами). При этом образуются эфиры борной кислоты (например, при использовании метанола — триметилборат). Эфир отгоняется и при последующем его гидролизе спирт регенеруется. При охлаждении образовавшегося концентрированного водного раствора кристаллизуется борная кислота, а маточный раствор возвращается в процесс. [c.324]
Окрашивание пламени эфирами борной кислоты. При взаимодействии тетраметокси- или тетраэтоксисиланов с борной кислотой или боратами -в сернокислой среде происходит переэте-рификация. При этом образуются летучие эфиры борной кислоты, которые можно обнаружить по окрашиванию пламени горелки [c.223]
Наконец, была исс,иедована возможность применения реакции А. П. Крешкова и С. С. Вильборг [13] на борную кислоту для обнаружепия эфиров кремневой кислоты. Эта реакция основана на образовашш летучих эфиров борной кислоты ири нагревании метилового илп этилового эфиров кремневой кислоты с борной кислотой или боратами. Пары эфиров борной кислоты окрашивают пламя горелки в зеленый цвет. В качестве реактива нами применялась бура. [c.355]
Морис [67] исследовал разделение метиловых эфиров поли-оксикислот и показал, что пропитка слоев силикагеля реактивом, образующим комплексы с гликолем, улучшает разделение. Так, на слоях силикагеля, пропитанного борной кислотой, боратом или арсенитом натрия, можно дифференцировать трео- и эритро-изомеры диоксикислот, а на слоях силикагеля, пропитанного арсенитом натрия, удается разделить три- и тетраоксистеа-раты. [c.416]
Фирмой Шелл разработан способ получения изопрена из изопентана, основанный на использовании боратных эфиров. Принцип способа заключается в том, что эфиры борной кислоты под действием гидроперекисей превращаются в пероксибораты, которые легко взаимодействуют с олефинами и количественно дают соответствующие окиси. Регенерируемые бораты снова используются для окисления [119]. Следует отметить, что этот метод описан в патентах [103, 104], где он предлагается для получения самых разнообразных окисей [c.106]
chem21.info
Борная кислота сложные эфиры - Справочник химика 21
Сравнительно новым прямым методом расщепления простых эфиров с образованием галогенпроизводных является метод образования сложных эфиров борной кислоты по следующей стехиометри-ческой реакции (пример в) [c.389]Летучие сложные эфиры борной кислоты окрашивают пламя в зеленый цвет. В присутствии серной кислоты и этанола борат-ионы образуют летучие сложные эфиры [c.232]
У. Может ли генцианоза образовывать сложные эфиры борной кислоты типа — -0 1 В(ОН) -0-0- а. Да б. Нет [c.201]Процесс с использованием борной кислоты не лишен недостатков Во-первых, он реализуется по более сложной схеме в связи с необходимостью обеспечивать хорошее распределение порошкообразной борной кислоты в циклогексане, разбавлять воздух инертным газом, регенерировать и очищать борную кислоту. Во-вторых, производство капролактама по этому методу потребует значительного увеличения мощности установки дегидрирования циклогексанола Тем не менее, этот процесс уже осуществлен в промышленном масштабе. Борная кислота при этом связывается в соль, а ее эфиры омыляются. [c.64]
ВЗАИМОДЕЙСТВИЕ БОРНЫХ СОЕДИНЕНИЙ С КАРБОНОВЫМИ КИСЛОТАМИ, СЛОЖНЫМИ ЭФИРАМИ И КАРБОНИЛЬНЫМИ СОЕДИНЕНИЯМИ [c.71]
Из j ругих продуктов, образующихся при окислении парафина, значительный интерес представляют спирты. Их можно извлечь (после омыления эфиров и экстракции кислот водными щелочами) в виде сложных эфиров борной кислоты, причем количество этих спиртов составляет 8—10% от исходного парафина. Спирты имеют 8—26 углеродных атомов в молекуле и являются преимущественно (на 65--75%) первичными. Их с успехом применяют для синтеза поверхностно-активных веществ типа алкилсульфатов. [c.383]
Ш. Какие из циклических форм галактозамина способны к образованию сложных эфиров с борной кислотой типа Г° >(0Н) -С-0 а. в -Пиранозная форма б. -Пиранозная форма в. об -Фуранозная форма г. ув -Фуранозная форма д. Не способны [c.223]
Способ, при котором для отделения спиртов от углеводородов используют борную кислоту, основан иа том, что последняя со всеми спиртами легко образует триалкилбораты. Борные эфиры нелетучи и термически весьма устойчивы, поэтому углеводороды можно от них отогнать. Последние остатки нейтрального масла рекомендуется удалять перегретым водяным паром. В заключение сложные эфиры борной кислоты гидролизуют горячей водой, выделяя таким образом спирт и регенерируя кислоту. Этот метод, который после метода перегопки является паиболее распространенным, потому что ои применим во всех случаях, также пригоден для выделения в чистом виде высших спиртов с 12—20 атомами углерода. [c.551]
ВЖС синтезируют, используя металлорганические соединения, например триэтилалюминий (см. с. 177). Однако наиболее экономически выгодным считается непосредственное окисление парафинов (см. с. 54). При этом образуется сложная смесь промежуточных и конечных продуктов, и прежде всего высших спиртов. Но их высокая реакционная способность (гидроксильная группа окисляется в десятки раз быстрее, чем метиленовая группа в молекуле предельного углеводорода) намного снижает возможность получения их в качестве основного продукта. Чтобы предотвратит дальнейшее окисление спиртов до карбоновых кислот, было предложено (А. И. Башкиров) переводить их по мере образования в борные эфиры. Для этого борную кислоту берут в количестве 4— 5 /с от массы окисляемого парафина. Образовавшиеся сложные эфиры борной кислоты — устойчивые к окислению продукты. Борные эфиры затем разлагают водой борную кислоту возвращают в производство, а ВЖС перегоняют. Чтобы уменьшить скорость окисления спиртов, применяют азотно-кислородную смесь (3—4°/с кислорода). На основе этого метода в 1959 г. в г. Шебекино (Белгородская область) был введен в эксплуатацию первый в мире крупнейший химический комбинат, на котором налажено производство синтетических моющих средств. [c.113]
Метод отгонки применяется и в ряде других случаев, когда образуются более сложные соединения, наиример метиловый эфир борной кислоты и т. д. Таким образом, методы, основанные на получении газообразных соединений, имеют большое значение, особенно для отделения и определения неметаллов и близких к ним элементов. [c.113]
У. Способна ли стрептоза к образованию сложного эфира с борной кислотой типа [c.213]
Борная кислота образует с ПВС сложные циклические эфиры (I), растворяющиеся в метаноле [104, с. 74] [c.120]
Открытие тетраборат-иона Тстраборат-ион обнаруживают в oi-дельной пробе анализируемого раствора (4—6 капель) по окрашиванию в зеленый цвет пламени горелки сложными эфирами борной кислоты (см. выше Аналитические реакции борат-ионов В О и ВО ). [c.487]
Традиционными катализаторами этерификации карбоновых кислот оксисоединениями служат минеральные кислоты серная, соляная, ортофосфорная, борная [9, 10]. Серная кислота была первым катализатором, примененным для ускорения реакции этерификации. До настоящего времени она остается одним из самых высокоактивных и широко используемых катализаторов промышленного производства сложных эфиров [И —13]. [c.8]
Этерификация (сложные эфиры). Бора трифторида эфират. Борная кислота. Гексаметилтриамид фосфорной кислоты Ионообменные смолы Метил-грег-бутиловый эфир, Триметилфосфит. Триэтилоксония борфторид [c.672]
Пиролиз а-полиоксиметилена рекомендуется проводить в смешанном растворителе, представляющем собой смесь углеводорода с простыми или сложными эфирами, к которой добавлены такие кислоты, как серная, мышьяковая, борная, себациновая, стеариновая или полифосфорная [21]. Для уменьшения вклада побочных реакций разложение ведут в атмосфере СОг или инертных газов. [c.173]
Обычно сложную структуру целевого вещества разделяют на фрагменты и затем на относительно простые кирпичики , из которых и начинают проектировать схему синтеза, идя в обратном направлении — от простого к сложному ( ретросинтетический анализ ). В будущем для этой цели реально использовать ЭВМ. Нельзя обойти обширную химию элементоорганических соеди-. нений. Например, известно уже более десятка тысяч только органических соединений бора, многие из которых эффективно исполь- зуются в органическом синтезе как реагенты, как промежуточные вещества при построении органических молекул различной сложности. Некоторые борорганические соединения выпускаются химической промышленностью как продукты (эфиры борной кислоты). [c.29]
Одноатомные жирные спирты в промышленном масштабе получают тремя оснбвными методами восстановлением сложных эфиров синтетических жирных кислот, выделением спиртов из промежуточных продуктов производства синтетических жирных кислот (из так называемых вторых неомыляемых), окислением жидких парафинов до спиртов в прщ утствии борной кислоты. По первому методу получают первичные спирты, по второму методу — смеси, состояш,ие примерно на 35—70% из первичных и на 25—30% из вторичных спиртов [238], а по третьему методу — главным образом (на 70—85%) вторичные спирты [239]. [c.100]
Окисление проводили в колонне, внутри которой помещали водяной змеевик для снятия тенла экзотермической реакции (без охлаждения удержать температуру реакционной массы на заданном уровне не удавалось). Над колонной был установлен флорентийский сосуд, котором собиралась вода, выделявшаяся в реакциях окисления и этерификации борной кислоты образующихся спиртов. Сначала окисляли нормальшле алканы в спирты (режим окисления описан в работе [И]). Наряду со спиртами в оксидате образовывались в значительных количествах кислоты, сложные эфиры и смолы. Оксидат имел темно-желтый цвет. [c.293]
Развивая работы в области окисления парафиновых углеводородов, мы констатировали положительное влияние добавок борной кислоты на накопление в оксндате нейтральных соединений с гидроксильной группой в условиях жидкофазного окисления парафиновых углеводородов. Проведение процесса окисления в присутствии борной кислоты борного ангидрида, а также кремневой и сурьмяной кислот всегда приводило к увеличению выхода спиртов.Однако во всех случаях одновременно получались большие количества побочных продуктов кислот, сложных эфиров, оксикислот, кетонов и других кислородсодержащих соединений. [c.413]
Было показано [56], что при жидкофазном окислении парафиновых углеводородов в присутствии борной кислоты образуются гликоли они были получены в виде сложных эфиров уксусной кислоты и выделены хроматографически. [c.59]
Селективным окислением циклододекана в присутствии мета-борной кислоты или ее ангидрида в промышленности получают циклодо дека НОЛ и циклогексанол [32, 33]. Недостатком борной кислоты является необходимость использования сложного процесса для регенерации сухой кислоты. Поэтому предпочтительнее использование ее эфиров, растворимых в углеводородах. Окисление циклододекана осуществляют чистым кислородом или воздухом в течение 1 ч при 168 °С в присутствии борной кислоты, эфиров ме-таборной кислоты. В присутствии 12 % добавок возможно превращение 70—95 % циклододекана в циклододеканол и циклододе-канон. [c.329]
Алкилбораты — сложные эфиры борной кислоты НаВОз [точнее, гидроксида бора В(ОН)з, см. 13.31. Метил- и этилбораты — легколетучие и легковоспламеняющиеся вещества в аналитической химии это их свойство часто используется для открытия соединений бора [c.493]
Признаком конца нейтрализации соляной кислоты является прекращение растворения углекислого кальция. Раствор отфильтровывают от избытка СаСО в фильтрате содержится вся борная кислота, и он насыщен углекислым газом. Для удаления СО раствор кипятят 15—20 мин. с обратным холодильником, затем охлаждают и, после прибавления к нему глюкозы, титруют едким натром. В более сложных случаях борную кислоту сначала отгоняют в виде метилового эфира борной кислоты, а затем тптруют. [c.344]
Метиловый эфир борной кислоты получают нагреванием Н3ВО9 с СН3ОН в присутствии конц. НС1 илй h3SO4 в качестве водоотнимающего средства. Для отделения образовавщегося сложного эфира от избытка исходного спирта реакционную смесь оставляют стоять над СаСЬ. При этом образуются два слоя нижний отбрасывают, а из верхнего путем фракционной перегонки получают чистый В(ОСНз)з. [c.540]
Мягним дегидратирующим средством, которое в некоторых случаях весьма пригодно для отщепления воды не только от первичных, но также от вторичных и третичных спиртов, является борная кислота. Борная кислота вначале образует сх> спиртом гримерный эфир метаборной кислоты, который разлагается до соответствующего олефина с выделением борной кислоты в этом обнаруживается некоторое сходство с механизмом пиролиза сложных афиров, хотя дегидратация борной кислотой проводится при более низких температурах (300—350° С). Нагреванием эквимолекулярных количеств н-гептанола, м-октанола, -гексанола, ментола, циклогенсанола, холестанола-33 с борной кислотой можно легко получить соответствующие оле-фины [26, 27]. [c.674]
У. Может ли генцЬобиоза образовывать сложные эфиры борной кислоты типа [c.202]
При обработке альдегидов, как содержащих, так и не содержащих а-водорода, этилатом алюминия одна молекула окисляется, а вторая — восстанавливается, как и в реакции 19-70, но в этом случае продуктом является сложный эфир. Этот процесс называется реакцией Тищенко. Возможны также перекрестные реакции Тищенко, При действии более основных алкоголятов, например алкоголятов магния или натрия, альдегиды, имеющие атом водорода в а-положении, вступают в аль-дольную конденсацию. Механизм этой реакции, как и в реакции 19-70, включает перенос гидрид-иона [630]. Реакция Тищенко катализируется также комплексами рутения [631], Ь1 У02 [632], борной кислотой [633], а для ароматических альдегидов — тетракарбонилферратом натрия Ка2ре(СО)4 [634]. [c.339]
ИЗ АЛКЕНОВ ЧЕРЕЗ БОРДНЫ И СЛОЖНЫЕ ЭФИРЫ БОРНОЙ КИСЛОТЫ [c.214]
Как и хлорангидриды кислот, ангидриды кислот широко применяют для получения сложных эфиров из соединений, содержащих оксигруппу. Эту реакцию проводят как в отсутствие катализаторов, так и с применением таких катализаторов, как серная кислота [61], хлористый цинк [62, 63), хлорсулы )окислота [64], хлористый ацетил [65], ацетат натрия [66]. борная кислота [67], сульфат железа(П1) [c.291]
Такие методы могут успешно применяться для разделения сложных эфиров холестерина, моно- и диглицеридов после превращения в соответствующие производные, триглицеридов, сложноэфирных ВОСКОВ, а также фосфоглицеридов, гликозилдиглицеридов и сфинголипидов после соответствующей модификации. Рекомендуется предварительно разделять а- и р-моноглицериды, а также а,р- и а,а -диглнцериды на оксиде кремния, импрегнированном борной кислотой. [c.87]
Получение сложных эфиров и аспирто пи ангидридов кислот. Таким путем получают наприл1ер нейтральные эфиры борной кислоты, для чего ангидрид борной кислоты нагревают со спиртами алкилсерные кислоты получают действием трехокиси серы на охлаждаемый раствор спирта жирного ряда в серной кислоте При пепегонке в вакууме из последних прямо получаются нейтральные эфиры [c.159]
Смесь цис- п /гаракс-изомеров циклических диолов проанализирована на основе реакции с борной кислотой — последняя реагирует только с цис-гидроксильными группами [17]. Количественное определение простых моноэфиров гликолей основано главным образом на реакциях ацилирования и осуществляется так же, как и анализ гликолей. Сложные эфиры гликолей определяют качественно и количественно гидролизо.м щелочалш. После гидродиза раствор титруют соляной кислотой в присутствии фенолфталеина уменьшение содержания щелочи пропорционально количеству сложного эфира в пробе. Параллельно проводят холостой опыт [4, р. 981]. [c.340]
Используемые в данном случае стабилизаторы запатентованы. Они могут включать коротко цепные соли карбоновых кислот, такие как соли муравьиной кислоты, ацетаты и сложные эфиры борной кислоты. Их использование может нарушать права патента. Использование в качестве aiiHOiHioro ПАВ NEODOL 25-35 снижает необходимость использования стабилизаторов. [c.77]
При кислотном гидролизе глицеридов наблюдается переме щение р-ацильной группы в а-положение. При использовании борной кислоты для снятия лабильной бензилиденовой защитной группы остаток этой кислоты замещает защитную группу. Этот процесс осуществляют при температуре не выше 100 °С с исполь зованием в качестве растворителя триэтилбората. Так как образо вавшийся сложный эфир борной кислоты гидролизуется с несрав пенно большей скоростью, чем ацильная, то последнюю удается сохранить в Р-положении [183]. [c.50]
В кач стве побочных продуктов реакции жидкофазного окисления циклодод капа молекулярным кислородом в присутствии борной кислоты образуется циклододеканон (8—10%), который концентрируется главным образом в головной фракции, получаемой при разгонке кислородсодержащих продуктов реакции, и смесь высококипящих кислородсодержащих соединений — остаток, количество которого составляет 12—14% от продуктов реакции. Исследование остатка показало, что он состоит приблизительно на 75% из полифункциональных соединений, представляющих собой главным образом смесь диолов и их сложных эфиров с окси- и дикарбоновыми кислотами, и приблизительно на 25% из монофункциональных соединений, в состав которых входит в основном циклододеканол (в виде сложных эфиров). На основании полученных данных можно было предположить, что окисление этого остатка азотной кислотой приведет к образованию дикарбоновых кислот с хорошими выходами. [c.199]
chem21.info
Борная кислота эфиры - Справочник химика 21
Эфиры борной кислоты. Эфиры борной кислоты — триалкилбораты — легко получаются нагреванием спирта и борной кислоты с добавкой концентрированной серной кислоты. Борнометиловый эфир (триметил-борат) кипит при 65° С, борноэтиловый (триэтилборат) — при 119° С. Эфиры борной кислоты легко гидролизуются водой. [c.115] Некоторые неорганические наполнители (триоксид сурьмы) улучшают огнестойкость пенопласта, но при этом увеличивают кажущуюся плотность и теплопроводность материала. Огнестойкость можно повысить также с помощью таких добавок, как борная кислота, эфиры борной кислоты, галогенированные эфиры фосфорной кислоты, карбамид, тиомочевина, дициандиамид, меламин и др. [23, 26]. [c.175]Электрофорез на бумаге. Моносахариды, имеющие соседние гидроксильные группы в положении цис, образуют с борной кислотой эфиры, в результате чего возникают отрицательно заряженные комплексы типа [94] [c.86]
Карбораны — это лишь один из многочисленных классов борорганических соединений. Химия органических соединений бора является обширной и хорошо исследованной областью. Некоторые боралкилы, например, были описаны задолго до открытия гидридов бора. Однако больщинство ранее известных борорганических соединений не содержит электронодефицитных структур и, следовательно, не имеет тесной связи с карборанами. Структуры таких соединений, как борные кислоты, эфиры борных кислот, боралкилы и содержащие бор гетероциклы, в большей или в меньшей степени находятся в соответствии с классической теорией строения органических соединений, и образование связей в них может быть описано с помощью локализованных двухцентровых связей или комбинаций резонансных структур. С другой стороны, алкильные производные гидридов бора, как, например, этилдекаборан, являются, несомненно, электронодефицитными молекулами, но, так как атомы [c.12]
Селективным окислением циклододекана в присутствии мета-борной кислоты или ее ангидрида в промышленности получают циклодо дека НОЛ и циклогексанол [32, 33]. Недостатком борной кислоты является необходимость использования сложного процесса для регенерации сухой кислоты. Поэтому предпочтительнее использование ее эфиров, растворимых в углеводородах. Окисление циклододекана осуществляют чистым кислородом или воздухом в течение 1 ч при 168 °С в присутствии борной кислоты, эфиров ме-таборной кислоты. В присутствии 12 % добавок возможно превращение 70—95 % циклододекана в циклододеканол и циклододе-канон. [c.329]
Англ. пат. 452508 ( hemis he Fabrik Servo). Оксиэтилирование эфиров фосфорной или борной кислот. Эфир фосфорной кислоты, например, получают при нагревании лаурилового спирта с РаОб. [c.56]
Органикум. Практикум по органической химии. Т.2 (1979) -- [ c.260 ]Курс неорганической химии (1963) -- [ c.374 ]
Новые воззрения в органической химии (1960) -- [ c.187 ]
Химия органических соединений бора (1965) -- [ c.18 ]
Качественный химический полумикроанализ (1949) -- [ c.212 ]
Основы общей химии Том 2 (1967) -- [ c.168 ]
Методы элементоорганической химии Бор алюминий галлий индий таллий (1964) -- [ c.248 ]
Курс неорганической химии (1972) -- [ c.335 ]
chem21.info
Эфир - борная кислота - Большая Энциклопедия Нефти и Газа, статья, страница 1
Эфир - борная кислота
Cтраница 1
Эфиры борной кислоты характеризуются по их цвету и флуоресценции. Этерифккаиия гилпоксила борной кислотой, сообщая реакционность определенным местам соединения в реакциях окисления и замещения, имеет, невидимому, значение и в процессе образования гтооизводннх оксиянтпяхинона при реакциях конденсации производных бензо. Так при ст чтезе хиниззрииа:: я-хлорфенолз и фталепого ангидрида в качестве конденсирующего средства применяется серная кислота вместе с борной. [1]
Эфиры борной кислоты летучи, окрашивают бесцветное пламя горелки в характерный зеленый цвет. [2]
Эфиры борной кислоты легко гидролизуются водой. [3]
Эфиры борной кислоты летучи, окрашивают бесцветное пламя горелки в характерный зеленый цвет. [4]
Эфиры борной кислоты легко образуются при нагревании борного ангидрида, хлористого бора или даже борной кислоты ( и HaS04) со спиртом. Они легко гидролизуются в присутствии воды. [5]
Эфиры борной кислоты, кипящие почти на 200 выше, чем исходная смесь, оставались в кубе; при добавлении разбавленного раствора борной кислоты эфиры легко гидролизовались в спирты. Процесс синол в промышленном масштабе не осуществлен. [6]
Эфиры борной кислоты при этом реагируют как ангидриды кислот, связывая анноны растворителя ( спирта) и повышая тем самым концентрацию водородных ионов. [7]
Эфиры борной кислоты, в частности, настолько характерные соединения, важные к толу же для синтеза истинных элементоорганических производных бора, что обойти их молчанием было невозможно. [8]
Эфиры борной кислоты и им подобные соединения способны к комплексообра-зованию, хотя и в меньшей мере, чем триалкилбор или трехгалоидный бор. [9]
Эфиры борной кислоты характеризуются по их цвету и флуоресценции. Этерификация борной кислотой гидроксмла, сообщая реакционность определенным местам соединения в процессе окисления ( например ализарина в пурпурин или в 1.2.3.4 - тетраоксиантрахиион) и в иных замещениях, имеет по видимому значение и в процессе конденсаций оксиаитрахииоиоиых произиодиых из беизэльиых производных. Так, при синтезе хннизарииа из n - хлорфеиола и фталевого ангидрида в качестве конденсирующего средства применяется серная кислота вместе с борной. [10]
Эфиры борной кислоты летучи, окрашивают бесцветное пламя горелки в характерный зеленый цвет. [11]
Эфиры борной кислоты легко образуются при нагревании борного ангидрида, хлористого бора или даже борной кислоты ( и h3S04) со спиртом. Они легко гидролизуются в присутствии воды. [12]
Эфиры борной кислоты, в частности, настолько характерные соединения, важные к тому же с точки зрения синтеза истинных элементоорганических производных бора, что рассмотрение их было необходимо. [13]
Эфиры борной кислоты - триалкилбора - TLI - легко получаются нагреванием спирта и борной кислоты с добавкой концентрированной серной кислоты. Борнометиловый эфир ( три-метилборат) кипит при 65 С, борноэтиловый ( триэтилборат) - при 119 С. Эфиры борной кислоты легко гидролизуются водой. [14]
Эфиры борной кислоты образуют с аммиаком и органическими аминами двойные соединения. Простейшие из них относятся к типу R3N - B ( OR) 3, и их можно считать производными боразана ( см. стр. Это соединение хотя и растворяется в нитробензоле мономолекулярно, но все же очень склонно к полимеризации. Водой оно частично гидро-лизуется. [15]
Страницы: 1 2 3 4
www.ngpedia.ru
Образование эфира борной кислоты - Справочник химика 21
Б. к. в этой реакции состоит в защите гидроксильных групп при образовании эфиров борной кислоты. Такое же действие Б. к. оказывает и в синтезе производных хинизарина [91. [c.120]Способность к образованию эфиров борной кислоты используют при разделении сахаров методом распределительной хроматографии и электрофореза на бумаге, методом ионообменной хроматографии на смолах и угле. [c.53]
Образование эфира борной кислоты [c.118]Образование эфира борной кислоты.........106 [c.6]
ОБРАЗОВАНИЕ ЭФИРА БОРНОЙ КИСЛОТЫ [c.106]
Со спиртами декаборан реагирует с образованием эфиров борной кислоты и водорода [65] [c.387]
Обработка 1-оке и антрахиноиа в среде 100 % -ной серной кислоты борной кислотой при 50° (для образования эфира борной кислот ы см. гл. Х1П) и последующее добавление нитрующей смеси приводят к образованию 1-н и т р о-4-о к с и а и т р а х и н о н а, выделяемого разбавлением водой При дальнейшем нитровании получают 1,3-д и и и т р о-4-о ксн антрахинон. [c.188]
При обработке Ализарина 80%-ной дымящей серной кислотой при 30° не происходит сульфирования, а две гидроксильные группы вступают в ядро, образуя Ализариновый бордо В или Хинализарин (Шмидт, 1890 С1 1045), который красит по алюминиевой протраве в цвет бордо. Первичными продуктами реакции являются, повидимому, сернокислые эфиры, гидролизующиеся затем до оксисоединений. Введение борной кислоты задерживает и регулирует реакцию вследствие образования эфиров борной кислоты (АР—0В=0), а также хелатных соединений, в которых атом бора связан с а-гидроксильной и карбонильной группами. Это позволяет получать промежуточные соединения в частности при получении Ализаринового бордо В реакцию можно остановить на стадии образования Ализаринового яркого бордо К. [c.946]
Опыт 3. Образование и горение эфиров борной кислоты. Поместите Б небольшую фарфоровую чашечку или в тигель 2—3 кристалла буры, 3—4 капли концентрированной серной кислоты и 6—8 капель метилового или этилового спирта. Смесь перемешайте стеклянной палочкой и подожгите образующийся борнометиловый или борноэтиловый эфир горящей лучинкой. Отметьте цвет пламени. Напишите уравнение реакции образования эфира борной кислоты. [c.219]
Интенсивное изучение данного метода началось с 1977 г., после того как выяснилось, что полистирольный сорбент, полученный с применением оптически активного прототипа, позволяет осуществить частичное разделение соответствующих рацематов [76—80]. Один из наиболее удачных методов предусматривает быстрое и обратимое образование эфиров борной кислоты в результате реакции между углеводом и винилзамещенной фенилборной кислотой (рис. 7.8). Этим путем молекулы мономера ковалентно связываются с прототипом (ср. схему 7.5, этап 1). Полимеризация и сшивка Днвинильным компонентом, последующий гидролиз и промывка приводят к хиральному сорбенту. [c.129]
Для аутоокисления характерна атака радикала (генерируемого химическим, термическим или фотохимическим путем) на молекулярный кислорода основном состоянии ( 2). Реакция катализируется одноэлектронными окислительно-восстановительными реагентами (обычно используются соли или комплексы переходных металлов Со, Си, Fe, Мп, Rh и 1г) и протекает с разложением образующегося гидропероксида. Реакции, используемые в промышленности (см. табл. 4.1.1), обычно проводятся в жидкой фазе при умеренных температурах и давлении. В процессе Хал-кона восстановление гидропероксида [схема (2)] сочетается с получением пропеноксида. В реакции Башкирова (аутоокисление в присутствии борной кислоты) образование эфиров борной кислоты, предохраняющее от дальнейшего окисления, дает возможность увеличить выход вторичных спиртов. [c.25]
Взаимодействие В5Н9 и спиртов [75] приводит к образованию эфиров борной кислоты и водорода [c.353]
Борные эфиры, получаемые таким способом, практически свободны от органических примесей неспиртового характера. При нагревании их с водой протекает реакция, обратная образованию эфира борной кислоты (гидролиз эфира) с получением исходного спирта и борной кислоты (см. главу 5) [c.23]
Трехосновные кислоты (борная, фосфорная) образуют уже три ряда эфиров моноэфиры, диэфиры, трпэфиры. Образование эфиров борной кислоты используется как метод очистки высших жирных спиртов от примесей В (ОН)з -Ь ЗКОН В (ОВ)з -Ь ЗН2О [c.38]
Бортриацетат представляет собой красивые, широ кие, очень гигроскопичные бесцветные иглы с температурой плавления 121°С. Со спиртами и фенолами бортриацетат вновь дает уксусную кислоту с образованием эфиров борной кислоты (соответственно алкил-и арилборатов) по уравнению [c.31]
И. Образование эфиров борной кислоты при действии окисей алкиленов [c.67]
Образование эфиров борной кислоты при действии окисей алкиленов на галогениды бора. На примере взаимодействия эфирата трехфтористого бора с эпихлоргидрином, протекающего уже на холоду, Меервейн [108] открыл [c.253]
chem21.info
Кислота борная, метиловый эфир - Справочник химика 21
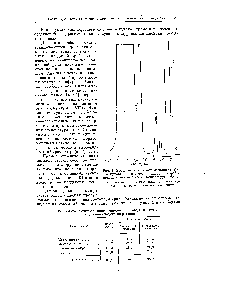
Метиловый эфир борной кислоты (т. кип. 68°) с метиловым спиртом (т. кип. 64°) образует азеотропную смесь (1 1), кипящую при 54,6° Поскольку присутствие даже небольшого количества метилового спирта снижает выход в значительно большей степени, чем этого можно было бы ожидать с учетом стехиометрических соотношений , метиловый эфир борной кислоты перед опытом следует перегнать на хорошей колонке, чтобы удалить в виде головного погона азеотропную смесь метилового эфира борной кислоты с метиловым спиртом, которая могла образоваться при хранении в результате гидролиза. [c.7] Р и с. 1. Прибор для дистилляции бора в виде метилового эфира борной кислоты. [c.412]Прм Применяется для отбелки шерсти, шелка и т.п.,д.чя дезинфекции. ЭФИРЫ БОРНОЙ КИСЛОТЫ борно-метиловый эфнр (триметил борат) - В(ОСНз)з, [c.84]
Метод отгонки применяется и в ряде других случаев, когда образуются более сложные соединения, наиример метиловый эфир борной кислоты и т. д. Таким образом, методы, основанные на получении газообразных соединений, имеют большое значение, особенно для отделения и определения неметаллов и близких к ним элементов. [c.113]
Применяли эфир марки ч. д. а., причем предварительно его сушили над натрием. Применяли продажный метиловый эфир борной кислоты (степень чистоты 99%). Бромистый фенил-магний применяли также продажный, в виде 3,0 М раствора в эфире. [c.7]
При сильном перемешивании из капельных воронок добавляют попеременно, небольшими порциями сначала 10 мл метилового эфира борной кислоты, затем 30 мл бромистого фенилмагния, причем скорость прибавления доля на быть по возможности большой, но в то же время такой, чтобы не допускать разогревания смеси выше температуры минус 60° (см. примечание 4)- [c.210]
Количественный перевод в метиловый эфир борной кислоты, затем омыление с помощью Са(0Н)2 [c.47]
Чистоту препарата определяют по бесцветности и прозрачносводного раствора, pH 1%-ного раствора 3,0—3,2, отсутствию метилового эфира пиридоксина (к 0,1 мл 0,1%-ного раствора прибавляют борную кислоту, аммиачный буферный раствор, 2,6-дихлорхинонхлоримид и бутиловый спирт при встряхивании в слое бутилового спирта не должно возникать голубого окрашивания), влаги (не более 0,5% при высушивании по 100—105°), сульфатной золы (не более 0,1%), тяжелых металлов (не [c.665]
Метилат натрия в метаноле с BFg 0(02115)2 дает метиловый эфир борной кислоты [76[. Этим способом можно получить этиловый эфир борной кислоты и др. [c.29]
Микроколичества бора отделяют от других элементов дистилляцией в виде метилового эфира борной кислоты или экстракцией этанолом. Мешающие катионы удалялись также осаждением в виде гидроокисей или на ртутном катоде. [c.411]
Наиболее часто применяется дистилляция бора из кислых растворов в виде метилового эфира борной кислоты. Этот метод применим к любым пробам. Дистилляция обычно производится из концентрированных растворов кислот, в которых содержится очень небольшое количество свободной воды, например из растворов в концентрированной серной или фосфорной кислоте. Однако Рассел [18] получал удовлетворительные результаты при дистилляции из слабокислого раствора. При дистилляции микроколичеств бора обычно получаются заниженные на 10% результаты, однако при тщательном контроле условий эта ошибка остается постоянной. Большие количества кремневой кислоты мешают дистилляции метилового эфира борной кислоты. [c.411]
Запись данных опыта. Написать уравнения реакций получения борной кислоты, получения борнометилового эфира взаимодействием метилового спирта и борной кислоты, горения борнометилового эфира. [c.206]
Признаком конца нейтрализации соляной кислоты является прекращение растворения углекислого кальция. Раствор отфильтровывают от избытка СаСО в фильтрате содержится вся борная кислота, и он насыщен углекислым газом. Для удаления СО раствор кипятят 15—20 мин. с обратным холодильником, затем охлаждают и, после прибавления к нему глюкозы, титруют едким натром. В более сложных случаях борную кислоту сначала отгоняют в виде метилового эфира борной кислоты, а затем тптруют. [c.344]
Метиловый эфир борной кислоты получают нагреванием Н3ВО9 с СН3ОН в присутствии конц. НС1 илй h3SO4 в качестве водоотнимающего средства. Для отделения образовавщегося сложного эфира от избытка исходного спирта реакционную смесь оставляют стоять над СаСЬ. При этом образуются два слоя нижний отбрасывают, а из верхнего путем фракционной перегонки получают чистый В(ОСНз)з. [c.540]
Бораты меди и натрия между собой образуют легкоплавкие эвтектики. Борная кислота легко образует эфиры, что используется также в машиностроении — газообразные флюсы при пайке и сварке ацетиленокислородной горелкой. Обычно получают борнометиловый эфир, который с метиловым спиртом дает легкокипящий раствор (с постоянной точкой кипения). Этот раствор подают вместе с ацетиленом в горелку, он весь сгорает, а тонкий слой жидкого В2О3 защищает место сварки или пайки от окисления [c.406]
При каталитическом гидрировании перекисной фракции получалась смесь метиловых эфиров оксистеариновых кислот, например IV. Эфиры оксикислот были дегидратированы над борной кислотой до смеси эфиров моноеновых кислот (например, V), которые после омыления, окислительного расщепления перманганатом и перйодатом и удаления низкомолекулярных одноосновных кислот перегонкой с паром приводили к образованию смеси дикарбоновых кислот [c.609]
В общем случае арилгалогениды превращаются в фенолы через магний-органнчесние соединения, а не в результате гидролиза. Сначала на реактив Грппьяра действуют метиловым эфиром борной кислоты [В(ОСНз)з1, а затем окисляют полученную арилборную кислоту разбавленным пероксидом водорода до фенола. [c.289]
В 2-литровой трехгорлой круглодонной колбе, снабженной термометром и холодильником, установленным для перегонки, подвергают дегидратации энергично перемешиваемую смесь (примечания 1 и 2) 740 мл глицерина и 216 з борной кислоты, для чего ее нагревают на масляной бане точно при температуре 170°. Температуру поддерживают па указашюм уровне в течение получаса, а затем дают смеси охладиться. Когда температура упадет до 150°, через горло колбы, в которое вставлен термометр, к ее содержимому прибавляют как можно быстрее смесь 154 г (1 моль) 1,3-ди-метилового эфира пирогаллола и 154 г (1,1 моля) гексаметилентетрамина (примечание 3). Температура падает приблизительно до 125°. Немедленно начинают быстрое нагревание смеси, которое, однако, замедляют при приближении температуры к 145°, а при 148° прекращают. Когда температура достигнет этого предела, следует наблюдать за процессом и регулировать его очень тщательно, так как на указанной стадии реакция становится экзотермичной (примечания 4, 5 и 6). В течение примерно 6 мин. температуру поддерживают при 150—160° (примечание 7). К концу этого времени реакционную смесь как можно быстрее охлаждают до 110° (примечания 6 и 8) и прибавляют к ней заранее приготовленный раствор 184 мл концентрированной серной кислоты в 620 мл воды. Смесь в течение 1 часа перемешивают, а затем охлаждают до 25° в бане со льдом. Борную кислоту, которая выпадает в осадок из раствора, отфильтровывают (примечание 9) и промывают водой (400 мл), чтобы освободить ее от маточного раствора. Фильтрат и промывные воды соединяют вместе и экстрагируют тремя порциями хлороформа по 500 мл (примечания [c.441]
Метиловый эфир борной кислоты (т. кнп. 65—67°) с метиловым спиртом (т. кип. 64") образует азотропиую смесь (1 1), кипящую при 54,6 . Поэтому необходимо перед опытом перегнать его на хорошей колонке, чтобы удалить в виде головного погона азеотропнуго смесь метилового чфира борной КИС.ЛОТЫ с метиловым спиртом, которая могла образоваться при хранении в результате гидролиза. [c.211]
В некоторых случаях, например при исследовании 4-О-метил-глюкуроноксиланов, прежде чем проводить метилирование, восстанавливают карбоксильные группы остатков 4-0-метил-/)-глюкуро-новой кислоты до спиртовых боргидридом натрия или калия [114] или алюмогидридом лития [115]. Высушенный и обеззоленный полисахарид обрабатывают небольшим количеством влажного метанола н карбоксильные группы этерифицируют добавлением раствора диазометана в эфире. Метиловый эфир полисахарида, растворенный в 0,4 М растворе борной кислоты, восстанавливают добавлением раствора боргидрида натрия. После нейтрализации разбавленной кислотой из смеси неорганические ионы удаляют диализом, а затем раствор полисахарида концентрируют и остаток высушивают. Для полного превращения карбоксильных групп в первичные спиртовые требуется провести трехкратную этерификацию и восстановление. [c.92]
Поскольку в метиловом эфире пиридоксина в 5-м положении находится ОСНз-группа, он не способен реагировать, подобно пиридоксину, с борной кислотой и образовывать борный комплекс, не дающий реакции образования индофенола с 2,6-дихлорхинонхлоримидом. На этом свойстве основан способ определения примеси метилового эфира пиридоксина в препарате пиридоксина, предложенный Л. А. Петровой. [c.184]
Метиловый эфир борной кислоты (не являющийся, правда, чисто неорганическим продуктом) получают при реакции борной кислоты с метанолом. Отделение эфира от избытка метанола, с которым он образует азеотропную смесь, осуществляют экстракцией углеводородами. Борную кислоту можно также из-влекать из водных растворов высшими спиртами. Однако вряд ли этот метод может приобрести промышленное значение. [c.651]
Дистилляции мешают только фторид и большие количества кремневой кислоты. Гестель и Юре [7] устраняли мешающее влияние фторида добавлением хлорида алюминия. Сильные окислители необходимо перед дистилляцией восстановить, а легколетучие кислоты должны отсутствовать, чтобы избежать нейтрализации щелочи в приемнике. Если раствор в приемнике во время дистилляции станет кислым, то метиловый эфир борной кислоты будет теряться. [c.413]
Для определения бора в металлах, имеющих важное значение для ядерной технологии, анализируемое вещество растворяют в броме в присутствии метанола, отгоняют метиловый эфир борной кислоты и получают окрашенное соединение с диаминохризазином. Из безводной реакционной смеси следы бора полностью выделяются при частичной дистилляции. Метод применим для многих металлов и дает точные результаты. [c.431]
Карбоксильные группы кислых полисахаридов восстанавливают действием боргидрида на их метиловые эфиры [217]. Высушенный в замороженном состоянии обеззоленнкй полисахарид обрабатывают небольшим количеством влажного метанола, и карбоксильные группы этерифицируют добавлением раствора диазометана в эфире. За короткое время, необходимое для этерификации, не наблюдалось метилирования гидроксильных групп. Метиловый эфир полисахарида, растворенный в 0,4 М борной кислоте, восстанавливают добавлением раствора боргидрида натрия. После нейтрализации разбавленной кислотой смесь диализуют для удаления неорганических ионов, а затем раствор полисахарида концентрируют и лиофилизуют. Для практически полного превращения карбоксильных групп в первичные спиртовые группы обычно требуется провести три цикла этерификации и восстановления. [c.333]
Детальное исследование окисления уточнило эти первоначальные представления. Так, Петри и Верхук сообщили, что в проточной системе (комнатная температура,давление 10— Ъмм, время контакта 2—3 мин) триметилбор количественно реагирует с кислородом с образованием метилового эфира гидроперекиси диметил борной кислоты [81] [c.220]
В ЭТОМ методе бор отгоняют из кислого раствора дистилляцией с метиловым спиртом в виде метилового эфира борной кислоты, последний собирают и определяют бор либо весовым, либо объемным методом. При анализе простых боратов, особенно растворимых, этот метод дает удовлетворительные результаты, если были соблюдены все необходимые меры предосторожности удовлетворительные результаты также при анализе трудно разлагаемых боросиликатов были получены Чэпиным [c.1032]
Из метатиоборной кислоты при взаимодействии с бромидом или хлоридом бора получаются соответствующие галогеноборосульфолы. При взаимодействии с метиловым эфиром борной кислоты получается триметоксиборсуяьфол. Этим же способом удается прийти к аминосоединению, имеющему характер ангидрооснования и образующему с НВг прекрасно кристаллизующиеся соли. Водой борсульфолы гидролизуются, но они растворимы в индиферентных растворителях, таких, как сероуглерод или бензол. По понижению температур замерзания растворов вычислены молекулярные веса, соответствующие следующим формулам [c.369]
chem21.info
бутиловый эфир борной кислоты - Справочник химика 21
Три-язо-бутиловый эфир борной кислоты орто [c.477]H.-БУТИЛОВЫЙ ЭФИР БОРНОЙ КИСЛОТЫ ]33 [c.133]
Основную фракцию н.-бутилового эфира борной кислоты перегоняют вторично из клайзеновской колбы с елочным дефлегматором (примечание 5). Первые 4—б мл дестиллата отбрасывают. Полученный очищенный продукт с т, кип. 103—10578 мм или 114— 115715 мм весит 400—425 г (87—92%теоретич. примечание 6), [c.134]
Так как н.-бутиловый эфир борной кислоты быстро гидролизуется влагой воздуха, необходимо при манипуляциях и переливаниях по мере возможности уменьшить время соприкосновения его с воздухом, [c.134]Н.-БУТИЛОВЫЙ ЭФИР БОРНОЙ КИСЛОТЫ 133 [c.133]
Диборан очень медленно реагирует с простыми эфирами [2275]. Тетрагидрофуран расщепляется им за 64 ч при 60° С, образуя три-бутиловый эфир борной кислоты с выходом 61% [1713] [c.337]
Описанная методика представляет видоизменение метода, разработанного Хотинским и Меламедом , которые первыми сообщили о получении замещенных борных кислот из реактивов Гриньяра и эфиров борной кислоты. Фенилборная кислота и соответствующий ангидрид были также получены при взаимодействии бромистого фенилмагния с трехфтористым бором при реакции фениллития с бутиловым эфиром борной кислоты и реакции дифенилртути с треххлористым бором . [c.8]
Три-изо-бутилортоборат см. Три-изо-бутиловый эфир борной кислоты орто [c.478]
Вышеописанный способ приведен в главных чертах в патенте н.-Бутиловый эфир борной кислоты может быть получен также при действии н.-бутилового спирта на триацетилборную кислоту, или на ангидрид борной кислоты. [c.135]
Впервые о возможности получения замещенных борных кислот из реактива Гриньяра и эфиров борной кислоты было сообщено в работе [I]. о-Фенилборная кислота может быть получена при взаимодействии бромистого фенилмаг-ния с трехфтористым бором [2], фсниллития с бутиловым эфиром борной кислоты [3] и дифенилртути с треххлористым бором [4]. [c.209]
Арилборные кислоты не окисляются кислородом, но ал-килборные кислоты подвержены этому воздействию [36]. Так, например, безводная бутилборная кислота была окислена воздухом и при этом образовался бутиловый эфир борной кислоты, после гидролиза которого были выделены бутиловый спирт и борная кислота. [c.108]
Полиорганоборосилоксан ы были синтезированы Андриановым и Волковой [159] реакцией алкил- или арил-ацетоксисиланов с бутиловым эфиром борной кислоты по схеме [c.386]
Эфиры минеральных кислот и сульфокислот. н-Бутиловый эфир борной кислоты СОП, II—133. к-Амиловый эфир борной кислоты СОП, И—134. Метилнитрат СОП, II—329. Этилнитрат Г—189. Этилнитрит Г—188. н-Бутилнитрит СОП, II—131. Амилнитрнт ПОХ—369. Изоамилнитрит Г—187 Ю, 1/11—183. Диэтил-сульфат Ю, 1/П—183. н-Бутилсульфит СОП, 11—136. н-Бутилфосфат СОП, П—138, Диэтилфосфит ПОХ—381. Метиловый эфир п-толуолсульфокислоты ПОХ—380 СОП, —150. н-Бутиловый эфир п-толуолсульфокислоты СОП, [c.66]
chem21.info