Справочник химика 21. Диметиловый эфир связь
Диметиловый эфир дипольный момент - Справочник химика 21
Пример lV-1. Зная дипольные моменты молекул воды и диметилового эфира (табл. IV-2), рассчитать дипольный момент молекулы метанола. Углы между связями приведены в табл. IV-1. [c.67]В табл. 18 приведены также температуры кипения ряда соединений с близкой молекулярной массой, но отличающихся по своей химической природе и тем самым по характеру нековалентных взаимодействий между молекулами. Видно, что самые низкие температуры кипения у веществ, молекулы которых неполярны, — пропана и пропилена. Это и понятно, если учесть, что в них действуют лишь дисперсионные силы. Заметно выше температуры кипения ме-тилхлорида и диметилового эфира, так как их молекулы полярные, обладаюш,ие постоянным дипольным моментом, а между ними в дополнение к дисперсионным силам действуют силы, обусловленные индукционным и ориентационным взаимодействием. Еще существенно выше температуры кипения у аминов, этилового спирта и муравьиной кислоты, молекулы которых способны образовывать водородные связи. Уместно в этой связи упомянуть воду, температура кипения которой 100°С, притом, что температура кипения близкого к ней по молекулярной массе неполярного метана —162°С [c.126]
Дипольный момент молекулы диметилового эфира = [c.31]Естественно, следует еще считаться и с такими положениями вращающихся групп, когда эти группы не находятся в плоскости бензольного, кольца. Две трет-бутильные группы в положениях 2 и 5 оказывают влияние на расположение эфирных групп эфира гидрохинона и заметно изменяют дипольный момент, который у диметилового эфира 2,5-трет-бУтилгидрохинона составляет всего 1,47 О [236]. [c.92]
Так, например, определение дипольного момента диметилового эфира показывает, что два атома углерода и атом кислорода не расположены на одной прямой, так как в этом случае дипольный момент был бы равен нулю вследствие взаимной компенсации двух одинаковых, противоположно направленных дипольных моментов связей между метильными группами и кислородом. [c.18]
В действительности же дипольный момент молекулы диметилового эфира равен 1,30, и, следовательно, эта молекула имеет изогнутую форму. [c.18]
Дипольный момент диметилового эфира может быть представлен как результат сложения двух векторов а (дипольных моментов связей [c.18]
Окись этилена характеризуется значительным дипольным моментом [1=1,911) (газ) и 1,82 0 (в бензоле). Дипольный момент диметилового эфира 1,29 В (газ). Расчет показывает, что полярность С—О-связей у обоих соединений примерно одинакова (м-с-о в окиси этилена 1,12 О, а в диметиловом эфире 1,08 О). [c.482]
Дипольный момент диметилового эфира может быть представлен как результат сложения двух векторов (а) (дипольных моментов связей СНз—О) по правилу параллелограмма [c.33]
Так, например, определение дипольного момента диметилового эфира сразу же показывает, что два атома углерода и атом кислорода не расположены на одной прямой, так как в этом случае дипольный момент был бы равен нулю [c.90]
Диметиловый эфир — полярный газ с дипольным моментом Р = 1,30- 10 >8. [c.35]
Электростатические силы (их также иногда называют ориентационными силами или диполь-дипольным взаимодействием) возникают между молекулами с постоянными электрическими дипольными моментами, т. е. между молекулами, у которых есть положительный и отрицательный полюса. Электростатические силы стремятся расположить молекулы упорядоченно так, чтобы векторы электрических дипольных моментов были ориентированы вдоль одной прямой (рис. 6.1). Такое взаимное расположение диполей энергетически выгодно. Электростатические силы преобладают в растворах полярных веществ в полярных растворителях, например триметиламина М(СНз)з диметиловом эфире (СНд)20. [c.65]
Водородные связи. Соединения, содержащие кислород-водородные или азот-водородные связи, обнаруживают признаки ассоциации, которая, если судить по молекулярному весу, дипольным моментам и молекулярной поляризуемости этих соединений, превышает все ожидания. К примеру, вода, у которой атомы не обладают высокой поляризуемостью, плавится при 0° и кипит при 100°, между тем как диметиловый эфир, метиловый спирт и ацетон-соединения с более высоким молекулярным весом — кипят при —24, 65 и 57° соответственно и плавятся при очень низких температурах. Нет большой разницы и в дипольных моментах этих веществ. Следовательно, исключительно высокая степень ассоциации воды должна объясняться каким-то коротко дистанционным взаимодействием, которое находит свое отражение не во всех макроскопических свойствах молекул воды. Из сопоставления физических свойств воды, метилового спирта и диметилового эфира следует, что гидроксильная группа имеет резко выраженное специфическое влияние на физические свойства. [c.161]
Найденное-экспериментально значение АсНзОН 1,68 Д хорошо согласуется с расчетным значением дипольного момента молекулы диметилового эфира. [c.68]
Так как экспериментальное значение ц == 1,3-10 Кл-м, то молекула диметилового эфира не может иметь линейное строение ( х = 0) и ей должна быть приписана вторая структура. Учитывая, что дипольный момент группыСН3О равен ij = [д.2 = 1,2-10 Кл-м, и принимая угол между двумя связями С—О равным 111 , получаем путем расчета х = 1,35-10" Кл-м, что практически соответствует опыту. [c.39]
Исследуемое вещество Табличные значения дипольного момента Ш) [2] Дидецил- фталат Диоктил- себацинат Силиконовое масло ВС 200 Диметиловый эфир тетра-этиленгли-коля [c.346]
Соединение (СНз)20ВРз характеризуется следуюш,ими свойствами т. пл. —14° С т. кип. 126,6° С мол. вес (в бензоле) 120 дипольный момент (в бензоле) 4,35 D [77]. Очень большой дипольный момент комплекса подтверждает правильность формулы с трехвалентным положительно заряженным атомом кислорода. Связь между В и О в этом соединении имеет характер координационной связи, причем энергия образования ее значительно меньше энергии образования обычной валентной связи этот вывод может быть сделан на основании относительно малого теплового эффекта реакции взаимодействия диметилового эфира с трехфтористым бором. [c.250]
Окись этилена, так же как простые эфиры, представляет, собо полярное соединение а = 1,88 О. Рассчитанный на основании диполь ного момента окиси этилена дипольный момент связи С—О раве 1,12 О эта величина больше, чем у диметилового эфира (1,08 О] Межядерные расстояния в окиси этилена, определенные электроне графическим методом, незначительно отличаются от расстояний дл соответственно тех же связей в алифатических соединениях [c.418]
Укажите, какое соединение имеет больший дипольный момент диметиловый эфир 1,4-бензолдикарбоновой кислоты (диметилтерефталат) или ее динн-трил л-нитрохлорбензол или ж-нитрохлорбензол. [c.46]
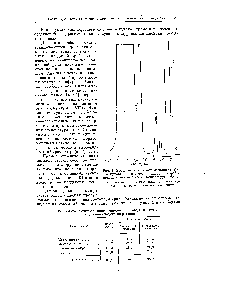
Для подтверждения этих положений и выяснения закономерностей удерживания о-, м- и -изомеров на гидроксилированной поверхности силикагеля были измерены удерживаемые объемы 0-, м- и п-изомеров 16 производных бензола. Из табл. 14.3 видно, что в случаях, когда полярные группы заместителей у ароматического кольца не образуют внутримолекулярных связей (первая группа адсорбатов в этой таблице), изомеры преимущественно удерживаются в порядке пдипольных моментов и увеличению вероятности для обеих полярных групп вступить в специфическое взаимодействие с гидроксильными группами поверхности силикагеля. На рис. 14.3 приведены хроматограммы о-, м- и л-изомеров диметиловых эфиров фталевых кислот, изомеров метилового эфира нитробензойной кислоты, удерживаемых в порядке гкСжСо. Между замещающими группами в этих молекулах сильные внутримолекулярные связи не возникают, поэтому сильнее удерживаются орто-изомеры, молекулы которых имеют наибольшие дипольные моменты и могут наиболее выгодно [c.223]
Изогнутое расположение заместителей принимается уже классической стереохимией в простых органических соединениях кислорода, азота и серы, так как эти элементы могут замещать углерод в циклах (см. т. 1, стр. 82). Доказательство изогнутого расположения заместителей при указанных элементах может быть получено совершенно независимо от этого при помощи дипольных моментов, в том числе и для соединений с открытой цепью. Особенно просто получить его, когда дело идет о таких симметрично построенных соединениях, как диметиловый эфир (СНд)20, диметилсульфид (СНз).,8 и триметиламин ( Hз)зN. Эти вещества обладают дипольным моментом, что указывает на изогнутую структуру, аналогичную той, какая ранее была приведена для воды, сероводорода и аммиака, от которых они и могут быть произведены (см. стр. 65). В связи с этим интересно отметить, что дифе-нилртуть не имеет дипольного момента, что указывает на вытянутое строение ее молекулы [c.89]
chem21.info
Диметиловый эфир Метиловый эфир - Справочник химика 21
Диметиловый эфир (метиловый эфир) [c.407]Нафтеновые кислоты, диметиловый эфир Метиловые эфиры нафтеновых кислот, НгО Алюмосиликат ВТУ 367-54 5 бар, 320° С. Выход 61% [1488] [c.272]
Диметиловый эфир, метиловый эфир, метокси-метан. [c.24]
СНз—О—СНз диметиловый эфир, метиловый эфир, [c.149]
Водородные связи. Соединения, содержащие кислород-водородные или азот-водородные связи, обнаруживают признаки ассоциации, которая, если судить по молекулярному весу, дипольным моментам и молекулярной поляризуемости этих соединений, превышает все ожидания. К примеру, вода, у которой атомы не обладают высокой поляризуемостью, плавится при 0° и кипит при 100°, между тем как диметиловый эфир, метиловый спирт и ацетон-соединения с более высоким молекулярным весом — кипят при —24, 65 и 57° соответственно и плавятся при очень низких температурах. Нет большой разницы и в дипольных моментах этих веществ. Следовательно, исключительно высокая степень ассоциации воды должна объясняться каким-то коротко дистанционным взаимодействием, которое находит свое отражение не во всех макроскопических свойствах молекул воды. Из сопоставления физических свойств воды, метилового спирта и диметилового эфира следует, что гидроксильная группа имеет резко выраженное специфическое влияние на физические свойства. [c.161]
Диметиловый эфир (метиловый [c.734]Диметилоксалат, диметиловый (полный метиловый) эфир щавелевой кислоты. [c.46]
СН3—О—СНз — диметиловый (или метиловый) эфир [c.339]
Диметиловый эфир, метиловый спирт, винилхлорид, хлористый этил. [c.16]
Гидрохлорирование побочных продуктов реакции. Сконденсированные газы, содержащие хлористый метил, диметиловый эфир, метиловый спирт и следы воды, поступают на гидрохлорирование. Установка и метод гидрохлорирования аналогичны гидрохлорированию в производстве этилцеллюлозы (см. стр. 116). [c.140]
Метиловый спирт. . Пропиловый спирт. Диметиловый эфир. Этилпропиловый эфир [c.109]
СНд — О — СНд — диметиловый (или метиловый) эфир, СНз — СНа — О — СН2 — СНз — диэтиловый (или этиловый) эфир. Углеводородные радикалы в простых эфирах могут быть не только одинаковыми, но и различными. Такие простые эфиры называют смешанными, При нагревании метилового и этилового спиртов с серной кислотой получается смешанный метилэтиловый эфир [c.334]
СНз-О-СНз Диметиловый, или метиловый, эфир [c.114]
Рассмотренные представления были развиты без учета участия в процессе растворителя. Фактически же растворитель может играть существенную роль при взаимодействии а-галогенкетона с основанием. На ряде объектов было отмечено различие стереохимического результата при замене протонного растворителя на апротонный. Так, при действии сухого метилата натрия в диметиловом эфире этилепгликоля на любой из стереоизомеров 1-хлор-1-ацетил-2-метилциклогексанона процесс протекает стереоспецифично, а при действии на тот же хлоркетоп метилата натрия в метанольном растворе — нестереоспецифично, т. е. образуются оба стереоизомера метиловых эфиров 1,2-диметилциклогексанкар-боновой кислоты [c.244]
В качестве кислого продукта расщепления а-метилморфиметина образуется монометиловый эфир морфола при других условиях разложения удается выделить родственное ему вещестао — метиловый эфир м о р ф е н о л а. Монометиловый эфир морфола оказался идентичным З-метокеи-4-оксифенантрену при деметилировании он превращается в морфол (3,4-диоксифенантрен), при метилировании— в диметиловый эфир морфола [c.1111]
Реакцию проводят в круглодоиной колбе из термостойкого стекла, соеди-,яенной последовательно промывной склянкой с 30%-ным раствором NaOH для удаления примесей с кислотными свойствами и с двумя осушительными колонками, наполненными соответствеино кусочками твердого едкого натра и пятиокисью фосфора. После высушиваиия газ поступает в конденсатор, охлаждаемый до —78 С где удаляются примеси диметилового эфира, метилового спирта и др., и затем газ конденсируется в коидеисаторе-приемнике, охлаждаемом жидким воздухом. [c.385]
Джонсон исходил из соединений нафталинового ряда, в которых имелась бициклическая система, использованная им для построения колец С и О. Исходное соединение — диметиловый эфир 1,6-диокси-нафталина (XXIX) легко доступен, потому что соответствующие сульфокислоты нафталина являются объектом промышленного производства, а перейти от сульфокислот к фенолам и к их метиловым эфирам не составляет труда. Восстановлением эфира (XXIX) натрием в спирте был получен кетон (XXX), который конденсировали с этилвинилкетоном. В реакцию вводился не сам этилвинилкетон, а продукт присоединения х нему диметиламина и затем иодистого метила. [c.414]
Те же ограничения, что и для эфиров ацетиламинокислот, относятся к метиловым эфирам N-формиламинокислот, полученным и разделенным на газовом хроматографе Лоссе и др. [58]. Эти соединения тоже очень слабо летучи и имеют относительно большие удерживаемые объемы. Их можно приготовить обработкой свободной аминокислоты смесью муравьиной кислоты и уксусного ангидрида с последующей этерификацией диазометаном (см. ниже). Из полифункциональных аминокислот исследовали поведение при ГХ лишь Глу и Асп. Диметиловый эфир N-формил-Глу при нагревании превращается в метиловый эфир пирролидон-карбоновой кислоты, и в таком виде его обнаруживают в газовом хроматографе. Несмотря на то что формильные производные простых аминокислот образуются с высокими выходами, эти соединения до сих пор еще не использовали для аминокислотного анализа [c.321]
Интенсивный характеристический пик иона с массой 149 найден в спектрах всех эфиров фталевой кислоты, начиная с диэти-лового эфира. Этот пик незначителен в диметиловом или метиловом эфире фталевой кислоты, а также в эфирах изофталевой и терефталевой кислот, которые дают ожидаемые ионы М — R, М —2R, М — OOR и Ai —2 00R. [c.73]
I — бензиламин 2 — к-бутиламин 3 — н-пропиламин 4 — диэтиламин 5 — изобутиламин 6 — н-амиламин 7 — изоамиламин 8 — циклогексиламин 9 — анилин 10 — о-толуидин И — К ТОлуидин 12 — о-хлоранилин 13 — ти-хлоранилин 14 — метиловый эфир антраниловой кислоты 15 — N. Ы-диметилацетамид 16 — метил-н-бутиловый эфир 17 — диэтиловый эфир 18 — этил-н-бутиловый эфир 19 — ди-н-пропиЛовый эфир 20 — диизопропиловый эфир 21 — ди-н-бутиловый эфир 22 — диметиловый эфир этиленгликоля 23 — тетрагидрофуран 24 — тетрагидропиран 25 — диоксан 26 — анизол 27 — фенетол 28 — л-метилбензальдегид 29 — бензальдегид 30 — метилбензоат 31 — ацетон 32 — метилэтилкетон 33 — метил-трет-бутилкетон 34 — циклобута-нон 35 — циклопентанон 36 — циклогексанон 37 — циклогептанон 38 — циклооктанон 39 — ацетофенон 40 — п-метилацетофенон 41 — н-бутирофенон 42 — нитробензол. [c.220]
ОСНз КОСНз Диметиловый эфир Метиловый спирт [c.316]
Названия эфиров производятся от названий радикалов. Так, мы имеем метиловый (диметиловый) эфир, метилэтиловый эфир, этиловый (диэтиловый), метилпропиловый, метилизопропиловый эфиры и т. д. [c.212]
В то же время перечисленные трудности в существенной степени устраняются при использовании в качестве исходного продукта диметилового эфира терефталевой кислоты. Поэтому для очистки полученную кислоту превращают в диметиловый эфир, который легко очищают перегонкой в вакууме, перекристаллизацией из растворителя или путем сочетания этих двух процессов. Процесс этерификации осуществляют нагреванием кислоты с метиловым спиртом в присутствии минеральной кислоты [10]. [c.528]
Диметиловый эфир а-дитио-ди-(б-хлорвалериановой) кислоты [378]. К хорошо перемешиваемой смеси 35 г (0,2 моля) 1,1,5-трихлорпентена-1 и 100 мл концентрированной h3SO4 (92%) прибавлено по каплям в течение 40—60 мин. 14 в однохлористой серы. Энергичное выделение хлористого водорода происходит при 15—18° С. После окончания прибавления однохлористой серы полученный темно-коричневый раствор перемешан 15 мин. при 20° и 5 мин. при 40—45° С. Охлажденная реакционная смесь вылита в воду, густо масло проэкстрагировано хлороформом. Хлороформенный экстракт промыт раствором едкого натра. Щелочной раствор подкислен соляной кислотой, выделившееся масло экстрагировано хлороформом. Получено 31 г кислых продуктов реакции. Этерификация проведена метиловым спиртом в присутствии серной кислоты. При перегонке в вакууме получено небольшое количество метилового эфира а-хлорвалериановой кислоты и 20,6 г (выход. 58%) диметилового эфира а-дитио ди-(б-хлорвалериановой) кислоты. [c.88]
chem21.info
Диметиловый эфир, определение вод эфир, определение
Кинетические кривые реакции аминирования хлорметилированного сополимера диметиловым эфиром ИДА приведены на рис 1 1 После достижения определенной степени превращения (60—80%) реакция затормаживается, затем через 3—4 ч выход повышается на 10—15%. Очевидно, на первой стадии в реакцию с диметиловым эфиром иминодиуксусной кислоты вступают атомы хлора, расположенные на поверхности крупных пор, на последней — расположенные в менее доступных гелевых участках [c.94] Экстракция метанолом или диметиловым эфиром и спектрофотометрическое определение [c.329]Примечание. В случае замены в искусственных смесях диметилового эфира диэтиловым эфиром для определения диметилового эфира вводится поправочный коэффициент, равный 1,88 [c.40]
Механизм с участием перекисей требует взаимодействия двух радикалов на каждую молекулу потребленного кислорода, для чего, по-видимому, необходима более высокая концентрация радикалов, чем действительная концентрация их во многих смесях. В том случае, если бы реакция радикал — радикал происходила часто, можно было бы предполагать образование определенных стабильных продуктов, нанример этана или диметилового эфира в качестве основных конечных продуктов реакции. Однако эти соединения почти полностью отсутствуют в продуктах окисления пропана в рассматриваемой области температур. Но если сделать вполне-вероятное допуш ение, что реакция алкильного радикала с кислородом происходит быстро, а реакция образуюш егося радикала перекиси алкила с углеводородом вследствие очень высокой энергии активации медленно, то концентрация радикалов ЛОз-должна достигать большой величины и реакции их с другими радикалами должны играть важную роль. [c.334]
Однако при определенных мерах предосторожности можно приготовить Си—2п-катализатор с довольно высоким содержанием АЬОз, на котором при синтезе метанола получается не более 0,2 масс. % диметилового эфира. [c.215]
В химически чистом образце этого оксида всегда содержится 27,29% С и 72,71% О. Отклонение от указанного состава свидетельствует о присутствии примесей. Утверждение, обратное закону о постоянстве состава веществ каждому определенному составу отвечает только одно химическое соединение, неверно. Действительно, диметиловый эфир и этиловый спирт имеют одинаковый химический состав — СгНбО, но отличаются друг от друга структурой молекул, т. е. порядком соединения в них атомов (изомеры). [c.15]
Двухступенчатое превращение - на первой стадии из метанола получают диметиловый эфир, а на второй - диметиловый эфир на цеолитном катализаторе превращают в углеводороды. Из-за выделения большого количества тепла в системе требуется значительное количество циркуляционного газа, чтобы ограничить рост температуры до определенной величины. [c.128]
Определенный интерес имеет и процесс синтеза диметилового эфира (ДМЭ), который рассматривается в качестве альтернативного дизельного топлива. [c.364]
Кальций дает хорошо измеряемые волны при полярографировании в безводном этилендиамине и диметиловом эфире [1450]. В качестве фона при этом добавляют 0,1 Ж раствор нитрата тетраэтиламмония. Щелочные металлы не мешают определению кальция. Максимумы легко подавляются красителем метиленовым синим. [c.104]
За исключением анализа диметилдисульфида, порядок внесения реагентов в колбу не имеет значения. При смешивании раствора боргидрида натрия с хлоридом алюминия происходит быстрая реакция, и если диметилдисульфид внести в раствор раньше хлорида алюминия, дисульфид частично теряется. При определении диметилдисульфида смешивают раствор боргидрида натрия и хлорид алюминия и выдерживают смесь в ледяной бане несколько минут, при этом берут навеску дисульфида. Можно прибавлять хлорид алюминия в виде раствора и 5 мл диметилового эфира диэтиленгликоля. Этот раствор приливают по каплям к смеси боргидрида и навески пробы. [c.571]
При низкотемпературном синтезе диметиловый эфир практически не образуется. Реакция Будуара (8.15) с термодинамической точки зрения является наиболее благоприятной, пока не достигнута определенная, максимально допустимая температура. [c.313]
Диметиловый эфир и метиловый спирт не мешают определению галогены и некоторые галогенорганические соединения — мешают [c.93]
Диметиловый эфир и метиловый спирт не мешают определению. [c.156]
Определение точки отбора метанола-ректификата. Исследование распределения остаточных легколетучих примесей по высоте колонны показывает, что одна их часть (в основном, диметиловый эфир, изобутилметиловый эфир, легкие углеводороды, диметоксиметан, метилформиат, ацетальдегид, ацетон и др.) имеет максимум концентрации во флегме и частично выводится с предгоном. Другая часть (преимущественно углеводороды, образующие с метанолом азеотропные смеси метилпропионат, 2-метилпропаналь, бутанон-2 и др.) сопутствуют метанолу по всей высоте колонны и выводятся из нее в основном с метанолом-ректификатом. Зонального скопления каких-либо легколетучих углеводородов по высоте колонны не наблюдается. [c.168]
Изучалась возможность определения в воздухе смеси алифатических аминов i—Сб. Накапливание этих веществ из воздуха производилось посредством их поглощения в последовательно соединенные поглотительные сосуды, наполненные раствором, содержащим 14 мл 20% НС1, 1 л воды и 1 л изопропанола. Было найдено, что в первых двух поглотительных сосудах задерживается 95% аминов. Амины экстрагировались изоамиловым спиртом и экстракт анализировался на составной колонке при 70°. Первая колонка длиной 1 м содержала смесь 11,4% диметилового эфира гексаэтиленгликоля и 0,6% триэтаноламина на обработанном щелочью (5% мета-нольного раствора КОН) детергенте Тайд с величиной частиц 0,20—0,25 мм вторая колонка той же длины содержала 20% силикона ДС-703 на обработанной 8% щелочи эмбацеле с величиной частиц 0,125—0,160 мм. Во избежание потерь пробы за счет адсорбции авторы производили периодическую промывку колонки с помощью нескольких повторных вводов изоамилового спирта. При определении в воздухе диметиламина, триметиламина и аммиака использовали стеклянные спиральные колонки с инзенским кирпичом и дибутилфтала-том. Искусственные смеси готовили в токсикологических камерах емкостью 100 л [9]. Дальнейшие работы по определению [c.100]
Зайцев с сотрудниками [206] применили полярографический метод для контроля процесса электролиза диметилового эфира себа-циновой кислоты, в частности для определения формальдегида в растворах, полученных после электролиза монометиладипината. Формальдегид определяется этим автором путем полярографирования соединения, образующегося за счет взаимодействия формальдегида с моноэтаноламином. Полярографический метод в данном случае позволил изучить взаимосвязь между процессами электроокисления метанола и электросинтеза диметилсебацината в различных условиях электролиза и выбрать оптимальные условия ведения технологического процесса. Зайцев, Вахрушев и их соавторы [207] предложили косвенный метод полярографического определения бутил-2-диола-1, 4, имеющего широкое применение в качестве исходного сырья для получения поливинилпирролидона, Ы-ме-тилпирролидона, полиуретанов и др. Зтот продукт образуется при [c.120]
Диметиловый эфир диссоциирует в определенных условиях с образованием этана и этанала (С2Н5)20 - СгНб + СН3СНО. В этом случае наблюдаемый порядок реакции равен 1. Покажите на основании предложенного цепного механизма процесса, что указанная реакция действительно имеет первый порядок [c.138]
Изящный метод определения гомологов в двухосновных кислотах основан на применении масс-спектрометра с высоким разрешением. Предположим, например, что нам необходимо проанализировать малое количество янтарной кислоты в адипиновой кислоте. После приготовления диметиловых эфиров в масс-спектре эфира адипиново кислоты можно обнаружить большой пик, отвечающий ионам [СНзОСО(СН2)41" , с массой 115, образованным благодаря отрыву СООСНз от молекулярных ионов. Этот пик налагается на интенсивный пик в спектре янтарной кислоты, отвечающий ионам [СНзОСО(СН2)2СО], образованным при отрыве ОСНд от молекулярных ионов. Другие пики в спектре эфира янтарной кислоты, за исключением малоинтенсивного пика молекулярных ионов, также налагаются на пики ионов эфира адипиновой кислоты. Однако ионы с массой 115 отличаются по составу (на величину С2Н4— [c.389]
Первым обширным исследованием, проведенным с помощью масс-спектрометра, была работа Лейфера и Ури [23], которые изучали пиролиз диметилового эфира и ацетальдегида.Хотя им и не удалось обнаружить радикалы, но они смогли показать, что промежуточным продуктом разложения димети лового эфира является формальдегид, и проследить его концептрацию. Более успешной была попытка Эльтентона [24, 25], которому удалось сконструировать установку, способную обнаружить свободные радикалы при пиролитических реакциях и в пламенах даже нри высоких давлениях (около 160 мм рт. ст.). Он также смог обнаружить присутствие радикалов СНз при пиролизе углеводородов, радикалов СНг из СНгКг, а также СНО и СНз при горении СН в кислороде. Метод определения основан в принципе на том, что энергия электронов, необходимая для ионизации радикалов, меньше энергии электронов, необходимой для образования ионизированных частиц из самих исходных молекул. Это дает возможность определять малые количества радикалов в присутствии больших количеств соединений, собственные спектры которых затмевают спектры радикалов. [c.97]
Определенное внимание в отчете привлек вопрос, связанный с историей данного резервуара. Между прочим упоминался тот факт, что она пострадала в результате аварии, происшедшей за год до этого во Франции, в ходе которой вышли из строя вентили цистерны. Никаких расследований аварии не проводилось. Впоследствии цистерна принадлежала предприятию, выпускающему аммиак, и в надписи на цистерне по-прежнему значилось "Наибольшая масса при заполнении жидким аммиаком - 26,8 т" [Stahl,1949]. Данная информация свидетельствует о том, что цистерна могла использоваться для транспортировки не только диметилового эфира, но и других веществ, каким, например, был безводный аммиак. В настоящее время стало известно, что это вещество способно воздействовать на хрупкостные свойства некоторых сталей [ IA, 1975]. [c.320]
Состав большинства неорганических веществ однозначно характеризует их молекулярное строение Н2304 — это всегда серная кислота ЫазР04 — это всегда фосфат натрия КА1 (504)2 —это всегда алюмокалиевые квасцы и т. д. В органической химии широко распространено явление изомерии— существуют разные вещества, имеющие одинаковый состав молекул. Эмпирические, суммарные формулы становятся поэтому для органических соединений неоднозначными простая формула С2Н6О отвечает как этиловому спирту, так и диметиловому эфиру более сложные эмпирические формулы могут соответствовать десяткам, сотням и даже тысячам различных веществ. С созданием бутлеровской теории химического строения стало ясно, что изомеры отличаются друг от друга порядком химической связи атомов — химическим строением. Определение химического строения, установление структурной формулы стало (и остается до сих пор) главной задачей при исследовании органических веществ. [c.84]
Электрохимическое восстановление диметилового и других эфиров малеиновой кислоты на ртутном капающем электроде в водных и водно-этанольных средах изучено Акимовым с сотр. [213]. На основании проведенных исследований разработана методика количественного полярографического определения этих веществ в различных условиях. Методика применена для определения диэтилгексилового эфира малеиновой кислоты в поверхностно-активных веществах на основе солей диэтилгексилового эфира сульфоянтарной кислоты [0,1—1% эфира с ошибкой определения 1% (отн.)]. [c.139]
Зайцев с сотр. [79, с. 135] применили полярографический метод контроля процесса электролиза диметилового эфира себациновой кислоты (для определения формальдегида). Формальдегид определяли полярографированием продукта его взаимодействия с моноэтаноламином. Полярографический метод в данном случае позволил изучить взаимосвязь между процессами окисления метанола и электросинтеза диметилсе- [c.153]
Деметиленирование сезамина, сопровождающееся метилированием, дало возможность установить определенную связь между обеими группами соединений. Например, D-сезамин был превращен таким путем в оптический антипод эвдесмина, О-диметиловый эфир D-пинорезинола [101. Аналогичным образом L-азаринин был превращен в L-эвдесмин. [c.7]
В качестве пластификаторов для аиетатов целлюлозы чаше всего применяется диметиловый эфир фталевой кислоты (ДМФ) и диэтиловый эфнр фталевой кислоты (ДЭФ) Они мо1ут применяться раздельно или совместно. Кроме того, в состав композиции из АЦ часто входиттрифениловый эфирфталевой кислоты (ТФФ), Чаще всего при разработке рецептур для определенного назначения применяю г смесь пластификаторов >[ а смесь можег создавать [c.98]
КАЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ПРОДУКТОВ ГИДРИРОВАНИЯ ДИМЕТИЛОВОГО ЭФИРА ТЕРЕФТАЛЕВОЙ КИСЛОТЫ [c.81]
Как упоминалось ранее, при гидрировании в качестве побочного продукта получается метиловый эфир толуиловой кислоты, имеющий спектр поглощения, идентичный спектру диметилтерефталата. Поэтому результаты определения содержания в гидрюре не вступившего в реакцию диметилового эфира терефталевой кислоты получаются несколько завышенными. Для нахождения истинного процентного содержания диэфира необходимо определить количество метилового эфира п-толуиловой кислоты в легкой фракции, а затем, исходя из того, что коэффициенты удельного погашения диметилтерефталата и метилового эфира л-толуиловой кислоты практически равны, вычислить процентное содержание диметилового эфира терефталевой кислоты по разности. Определение процентного содержания С метилового эфира л-толуиловой кислоты в легкой фракции [c.83]
Диметиловый эфир винилфосфиновой кислоты. Колесников и др. [161] исследовали полимеризацию этого мономера в области температур 40—70° С. Инициатором служил Азо. Для определения констант кр/ко" скорость инициирования вычислялась из скорости распада Азо (/ = 0,6) по данным Арнетта (стр. 51). Таким образом [c.127]
chem21.info
Диметиловый эфир - это... Что такое Диметиловый эфир?
Димети́ловый эфи́р (C2H6O) (метиловый эфир, метоксиметан, древесный эфир) Н3С-О-СН3 — широко применяемый на практике простой эфир.
Свойства
| 233.128 | 54.61 | 298.172 | 596.21 | 348.147 | 2022.45 |
| 238.126 | 68.49 | 303.160 | 687.37 | 353.146 | 2242.74 |
| 243.157 | 85.57 | 305.160 | 726.26 | 353.158 | 2243.07 |
| 248.152 | 105.59 | 308.158 | 787.07 | 358.145 | 2479.92 |
| 253.152 | 129.42 | 313.156 | 897.59 | 363.148 | 2735.67 |
| 258.160 | 157.53 | 316.154 | 968.55 | 368.158 | 3010.81 |
| 263.160 | 190.44 | 318.158 | 1018.91 | 373.154 | 3305.67 |
| 268.161 | 228.48 | 323.148 | 1152.35 | 378.150 | 3622.60 |
| 273.153 | 272.17 | 328.149 | 1298.23 | 383.143 | 3962.25 |
| 278.145 | 321.87 | 333.157 | 1457.50 | 388.155 | 4331.48 |
| 283.160 | 378.66 | 333.159 | 1457.76 | 393.158 | 4725.02 |
| 288.174 | 443.57 | 338.154 | 1631.01 | 398.157 | 5146.82 |
| 293.161 | 515.53 | 343.147 | 1818.80 | 400.378 | 5355.8 |
J.
Chem. Eng. Data 2004, 49, 32-34Производство
В промышленности производится из природного газа, угля, или биомассы.
Применение
Применение в качестве топлива
Диметиловый эфир — экологически чистое топливо без содержания серы, содержание оксидов азота в выхлопных газах на 90 % меньше, чем у бензина. Цетановое число диметилового дизеля более 55, при том что у классического нефтяного 38-53. Применение диметилового эфира не требует специальных фильтров, но необходима переделка систем питания (установка газобалонного оборудования, корректировка смесеобразования) и зажигания двигателя. Без переделки возможно применение на автомобилях с LPG-двигателями при 30 % содержании в топливе.
Теплота сгорания ДМЭ около 30 МДж/кг, у классических нефтяных топлив — около 42 МДж/кг. Одна из особенностей применения ДМЭ — его более высокая окисляющая способность (благодаря содержанию кислорода), чем у классического топлива.
В июле 2006 года Национальная Комиссия Развития и Реформ (NDRC) (Китай) приняла стандарт использования диметилового эфира в качестве топлива. Китайское правительство будет поддерживать развитие диметилового эфира, как возможную альтернативу дизельному топливу. В ближайшие 5 лет Китай планирует производить 5—10 млн тонн диметилового эфира в год.
Автомобили с двигателями, работающими на диметиловом эфире разрабатывают KAMAZ, Volvo, Nissan и китайская компания Shanghai Automotive.
Опасность
Является слабым наркотиком. Огнеопасен, смесь с воздухом взрывоопасна, температура вспышки −41 °C. ПДК в воздухе рабочей зоны составляет 200 мг/м³.
3dic.academic.ru
Диметиловый эфир - это... Что такое Диметиловый эфир?
Димети́ловый эфи́р (C2H6O) (метиловый эфир, метоксиметан, древесный эфир) Н3С-О-СН3 — широко применяемый на практике простой эфир.
Свойства
| 233.128 | 54.61 | 298.172 | 596.21 | 348.147 | 2022.45 |
| 238.126 | 68.49 | 303.160 | 687.37 | 353.146 | 2242.74 |
| 243.157 | 85.57 | 305.160 | 726.26 | 353.158 | 2243.07 |
| 248.152 | 105.59 | 308.158 | 787.07 | 358.145 | 2479.92 |
| 253.152 | 129.42 | 313.156 | 897.59 | 363.148 | 2735.67 |
| 258.160 | 157.53 | 316.154 | 968.55 | 368.158 | 3010.81 |
| 263.160 | 190.44 | 318.158 | 1018.91 | 373.154 | 3305.67 |
| 268.161 | 228.48 | 323.148 | 1152.35 | 378.150 | 3622.60 |
| 273.153 | 272.17 | 328.149 | 1298.23 | 383.143 | 3962.25 |
| 278.145 | 321.87 | 333.157 | 1457.50 | 388.155 | 4331.48 |
| 283.160 | 378.66 | 333.159 | 1457.76 | 393.158 | 4725.02 |
| 288.174 | 443.57 | 338.154 | 1631.01 | 398.157 | 5146.82 |
| 293.161 | 515.53 | 343.147 | 1818.80 | 400.378 | 5355.8 |
J.
Chem. Eng. Data 2004, 49, 32-34Производство
В промышленности производится из природного газа, угля, или биомассы.
Применение
Применение в качестве топлива
Диметиловый эфир — экологически чистое топливо без содержания серы, содержание оксидов азота в выхлопных газах на 90 % меньше, чем у бензина. Цетановое число диметилового дизеля более 55, при том что у классического нефтяного 38-53. Применение диметилового эфира не требует специальных фильтров, но необходима переделка систем питания (установка газобалонного оборудования, корректировка смесеобразования) и зажигания двигателя. Без переделки возможно применение на автомобилях с LPG-двигателями при 30 % содержании в топливе.
Теплота сгорания ДМЭ около 30 МДж/кг, у классических нефтяных топлив — около 42 МДж/кг. Одна из особенностей применения ДМЭ — его более высокая окисляющая способность (благодаря содержанию кислорода), чем у классического топлива.
В июле 2006 года Национальная Комиссия Развития и Реформ (NDRC) (Китай) приняла стандарт использования диметилового эфира в качестве топлива. Китайское правительство будет поддерживать развитие диметилового эфира, как возможную альтернативу дизельному топливу. В ближайшие 5 лет Китай планирует производить 5—10 млн тонн диметилового эфира в год.
Автомобили с двигателями, работающими на диметиловом эфире разрабатывают KAMAZ, Volvo, Nissan и китайская компания Shanghai Automotive.
Опасность
Является слабым наркотиком. Огнеопасен, смесь с воздухом взрывоопасна, температура вспышки −41 °C. ПДК в воздухе рабочей зоны составляет 200 мг/м³.
muller.academic.ru
Ацетилен — диметиловый эфир - Справочник химика 21
Оксициклогексил-1-ацетилен Циклогексил-метилкетон Диметиловый эфир адипиновой кислоты Диэтиловый эфир янтарной кислоты Нитрил 2-этилкапроновой кислоты [c.194]АЦЕТИЛЕН - ДИМЕТИЛОВЫЙ ЭФИР [c.122]
Температура затвердевания смесей ацетилен — диметиловый эфир [9] [c.122]
В спиртовой среде ацетилен реагирует с окисью углерода и спиртом с образованием соответствующих эфиров янтарной, акриловой и других кислот. Так, в метанольной среде при температуре 95° и давлении 250 ати получается смесь метиловых эфиров упомянутых кислот. После вакуумной разгонки реакционной смеси было получено 10-30 мол,% диметилового эфира янтарной кислоты, 3-2 иож.% метилового эфира " акриловой кислоты и др. При повышении температуры до 120° увеличивается выход ненасыщенных карбоновых кислот и соответственно уменьшается выход янтарной кислоты [193, [c.74]Наиболее известными газовыми топливами являются природные и попутные нефтяные газы, представляющие собой смеси низкомолекулярных углеводородов. Физико-химические свойства этих углеводородов (табл. 6.1) и определяют моторные качества указанных газовых топлив [6.22, 6.26-6.27]. В качестве самостоятельных топлив рассматриваются биогазы и некоторые индивидуальные вещества и соединения диметиловый эфир (см. главу 4), водород, монооксид углерода, аммиак, ацетилен (табл. 6.2) [6.3, 6.4, 6.27]. [c.222]
Водород и предельные углеводороды определяют сожжением над окисью меди остаточный газ представляет собой смесь азота и редких газов. Таким способом нельзя определить галогеноводороды, галогены, нитрозные газы, двуокись серы, аммиак, амины, сероводород, сероокись углерода, цианистый водород, диметиловый эфир, хлористый метил и ацетилен. Эти газы, которые также могут содержаться в газовых смесях, должны быть определены отдельно, после соответствующей обработки смеси. Необходимые для такого исследования качественные реакции и методы количественного определения рассматриваются в соответствующих разделах этой книги. [c.736]
Поликонденсация динатрий-п-диэтинилбензола с диметилдихлорсиланом [42]. Реакцию проводили в среде полярного растворителя (тетрагидрофурана диметилового эфира, диэтиленгликоля, этилового эфира). Предварительно получали ацетиленид взаимодействием тонкораздробленного натрия или амида натрия с бмс-ацетиленом в растворителе. Затем прибавляли элементоорганическое соединение в том же растворителе, поддерживая температуру не выше комнатной. После прибавления всего количества элементоорганического соединения реакционную смесь нагревали непродолжительное время при 60— 100° С, отфильтровывали осадок хлористого натрия и из фильтрата выделяли полимер. [c.461]
Если ацетилен заменить диметиловым эфиром ацетилендикарбоновой кислоты, то электронооттягивающие группы последнего благоприятствуют присоединению по Дильсу — Альдеру к одному из цикло-пентадиенильных остатков и получается оранжево-красный комплекс-(т, пл. 84 °С), которому приписывают строение III (Дюбек, 1960) [c.511]
Ацетиленовые соединения и азиды. Продукт присоединения фенилазида к метиловому эфиру ацетилендикарбоновой кислоты неустановленного состава впервые описан в 1893 г. [2—41. Несколько лет спустя Димрот и Фестер установили, что 1-фенилтриазол получается в результате присоединения фенилазида к ацетилену [51. По-видимому, эта общая реакция образования кольца триазола необратима. В частности, фенилазид, присоединяясь к аддукту, обратимо образующемуся из дивинилфульвена и метилового эфира ацетилендикарбоновой кислоты, дает диметиловый эфир 1-фенилтриазолдикарбоно-вой-4,5 кислоты (I) [61. [c.297]
Аммиак. ... Диметиловый эфир Метнл ацетилен Аллен. ... [c.375]
Диметилтерефталат, этиленгликоль, бисфенол Ацетилен (I), Н О Смешанный полиэфир Присо Ацетальдегид ZnO — трифенилфосфин, модифицирующая добавка — диметиловый эфир 2,5-дигидрокси-терефталевой кислоты в атмосфере N3, 10— 2 торр, 271—-275° G. 2,5 ч [28]. См. также [416] единение Zn— u-молибдатный в паровой фазе, 400 С, 150 1. Производительность ио 1—215 г/л- [419] [c.958]
Ацетилен, метанол, метиловый эфир 2,5-гексадиен-7-ацетокси -карбоновой кислоты, СО Диметиловый эфир 2,5,8-октатриендикар-боновой кислоты Ni( 0)4 в метаноле в присутствии НС1, 1 бар, 42° С, 70 мин [3228] [c.182]
Галогенный мостик в этом комплексе может быть разрушен с помощью аминов, дающих, например, транс-[(СНз)зСС СС(СНз)з, пиперидин, РЮЬ]. Более простые диацетилены, по-видимому, не дают платиновых комплексов этого типа, хотя стабильные соли типа соли Цейзе образуются из такого диоксиацетилена, как (СНз)2С(ОН)С СС(ОН) (СНз)г и его диметилового эфира (см. [15], обзор ранней литературы). Вполне может быть, что в этих соединениях связи платина — ацетилен аналогичны связям в олефиновых комплексах и образуются за счет перекрывания разрыхляющих орбит ацетилена и йр-гибридных орбит платины. Относительно соединений этого типа пока еще имеется недостаточно данных однако рентгенографическое изучение комплекса хлорида меди (I) с бутином-2 показывает, что атом меди лежит на линии, перпендикулярной к ацетиленовой связи и как бы делящей эту связь [c.531]
Диполярное присобдинение относится к той же категории реакций. Дильс и Альдер [50] осуществили взаимодействие пиридина с диметиловым эфиром ацетилен-дикарбоновой кислоты и получили красный аддукт 1 2, структура которого была полностью установлена лишь значительно позже. [c.453]
Вейцман для получения изопрена несколько видоизменил реакцию Фаворского (см, стр. 275), проводя конденсацию ацетилена с ацетоном в присутствии порошкообразного едкого кали в растворителе, содержа-шем группы —О—С—О— или —О—С—С—О. Когда твердый КОН нагревают с диметиловым эфиром диэтиленгликоля (СНз—О—СНг—СН2)гО, шелочь диспергируется до высокоактивного тонко измельченного порошка и с большой жадностью абсорбирует ацетилен. Ни едкий натр, ни едкий литий не могут заменить едкое кали. Ацетилен, абсорбируясь, образует ацетиленид калия, а выделяющаяся вода связывается избытком едкого кали, что препятствует течению обратной реакции. Добавление при —10 °С ацетона вызывает бурную экзотермическую реакцию, в результате которой образуется калиевое производное, гидролизующееся при добавлении воды до З-метилбутин-1-ола-3 [c.277]
Из металлорганических соединений элементов I группы наибольший интерес вызывают соединения лития, в меньшей степени соединения натрия и калия. Все они являются ионны >ш и в заметных количествах в углеводородах не растворяются все эти соединения чрезвычайно реакционноспособны, неустойчивы при хранении на воздухе и легко гидролизуются. Хотя алкил- и частично арилпро-изводные натрия люжно использовать в качестве промежуточных продуктов в момент образования, их редко удается выделить. Наиболее важными являются соединения, образованные кислыми углеводородами, такими, как циклопентадиен, инден, ацетилен и др. Их можно получить при взаимодействии углеводородов с раствором натрия в жидком аммиаке или, более обычным способом, при взаимодействии с натрием, диспергированным в тетрагидрофуране, диметиловых эфирах этиленгликоля и диэтиленгликоля, или в ди-метилформамиде [c.269]
В табл. X—XVII приведены примеры гидратации олефинов, диенов и ацетиленов при помощи реакции гидроборирования, опубликованные в литературе до марта 1962 г. В таблицах применяются такие сокращения диглим — диметиловый эфир диэтиленгликоля триглим — диметиловый эфир триэтиленгликоля. [c.41]
Ацетилены. Радикальное присоединение тиолов к ацетиленам с различными заместителями (например, алкил, арил, карбоксил, а-оксиалкил, -а-галогеналкил, алкокси- и алкилтио-) протекает легко, причем образуются моноаддукты, диаддукты или и те и другие в зависимости от относительных количеств исходных веществ. Обычно первая молекула тиола присоединяется легче, чем вторая. Только моноаддукты получаются из диметилового эфира ацетилендикарбоновой кислоты и этантиола [170], п-метоксифенилацетилена и тиолуксусной кислоты [171], З-метил-З-окси-1-бутинилэтилового эфира и этантиола [1721 и из 4-оксипентина-1 [173] или фенилаце-тилена и тиолуксусной кислоты [171]. Присоединение первой молекулы тиола протекает против правила Марковникова с образованием аномального продукта реакции. Вторая молекула тиола обычно присоединяется с образованием диаддукта с тиогруппами у соседних атомов углерода [170, 174, 175]. Реакции присоединения к фенил ацетилену, однако, приводят к продуктам, в которых обе [c.206]
Циклопептадиен легко реагирует с диметиловым эфиром ацетилен-дикарбоновой кислоты с образованием аддукта, который при омылении [c.26]
Кларк и Холлидей [140] при действии диборана на ацетилен в диметиловом эфире этиленгликоля получили полимер I [c.205]
chem21.info
Диметиловый эфир образование - Справочник химика 21
Механизм с участием перекисей требует взаимодействия двух радикалов на каждую молекулу потребленного кислорода, для чего, по-видимому, необходима более высокая концентрация радикалов, чем действительная концентрация их во многих смесях. В том случае, если бы реакция радикал — радикал происходила часто, можно было бы предполагать образование определенных стабильных продуктов, нанример этана или диметилового эфира в качестве основных конечных продуктов реакции. Однако эти соединения почти полностью отсутствуют в продуктах окисления пропана в рассматриваемой области температур. Но если сделать вполне-вероятное допуш ение, что реакция алкильного радикала с кислородом происходит быстро, а реакция образуюш егося радикала перекиси алкила с углеводородом вследствие очень высокой энергии активации медленно, то концентрация радикалов ЛОз-должна достигать большой величины и реакции их с другими радикалами должны играть важную роль. [c.334] В промышленных процессах не используют давления выше 30—35 МПа из-за увеличения скорости побочных реакций образования метана, диметилового эфира, высших спиртов. Степень превращения СО в процессах низкого давления за проход колеблется в пределах 15—50%, а в процессах высокого давления не превышает 25%. [c.327]Эта сумма одинакова для изомерных соединений, в том числе и соединений, содержащих разные функциональные группы, например этилового спирта и диметилового эфира. Она не зависит и от агрегатного состояния, и кристаллической модификации ве-1 щества. Но в отдельности теплота образования и теплота сгорания в общем случае различны для изомеров и зависят от агрегатного состояния и кристаллической модификации. [c.209]
Решение. Метанол, образующийся в результате реакции (I), вступает в реакцию (И) с образованием диметилового эфира и воды. Обе реакции протекают без изменения количества молей, отсюда [c.274]
В качестве побочных превращений при синтезе метанола наблюдается образование воды, метана, диметилового эфира и высших спиртов [c.250]
Диметилсульфат медленно реагирует с фенолом [368] при температуре 100—120°, выделяя диметиловый эфир, наряду с образованием анизола и продуктов сульфирования. Возможно, что в этом случае протекают указанные ниже реакции [c.65]
Нагревание смеси сухого метилата магния с диметилсульфатом ведет к образованию диметилового эфира согласно уравнению [393] [c.68]
Некоторое количество метанола можно заменить на диметиловый эфир - побочный продукт синтеза метанола. Источником катализатора является иодистый кобальт, который в условиях реакции превращается в гидрокарбонил кобальта и иодистый водород. Реакция протекает при температуре 250°С и давлении 650 атм. Как и следовало ожидать, в этих условиях метанол взаимодействует с уксусной кислотой с образованием метилацетата. Поэтому, чтобы регулировать концентрацию ме-тилацетата, в реакционную смесь вводят воду, В реакторе имеются примерно следующие концентрации упомянутых компонентов 30% метилацетата, 30% уксусной кислоты, 30% воды и 10% метанола. Метилацетат, катализатор и незначительное количество побочных продуктов возвращаются в реактор. Выход уксусной кислоты в расчете на метанол составляет 90%. [c.297]
Аналогично получают простые эфиры и из других спиртов. Метиловый спирт с серной кислотой легко образует диметиловый эфир. Высшие спирты, начиная с бутиловых, образуют простые эфиры с малыми выходами, так как нарастает тенденция к образованию олефинов. [c.460]
Диметиловый эфир при нагревании распадается с образованием метана, оксида углерода (И) и водорода. Составьте уравнение реакции. [c.165]
В качестве примера реакции, проходящей, вероятно, через промежуточную стадию образования радикала с трехвалентным атомом углерода в пара-положении, можно привести окисление 1,3-диметилового эфира пирогаллола (Гофман, 1878) [c.310]
Нафталин не реагирует с натрием в диэтиловом эфире, но если натрий вводить в раствор нафталина в диметиловом эфире (или в диметиловом эфире этиленгликоля), металл растворяется с образованием окрашенного в темно-зеленый цвет раствора (Скотт, 1936). [c.468]
Как указывалось выше, одним из продуктов термокаталитического расщепления метоксисиланов является диметиловый эфир, образование которого объяснено следующим образом [1887] [c.190]
Браун и Гэлловэй [98] нашли в метаноле, полученном под действием обычного катализатора ZnO—СгаОд, 10% диметилового эфира. Образование простого эфира было объяснено последующей дегидратацией метанола на катализаторе, поскольку отношение эфира к спирту уменьшалось с увеличением объемной скорости. [c.85]
Таким методом пользовались Хиншельвуд и Аски [28] для того, чтобы определить закон скорости разложения диметилового эфира СН3ОСН3. Эта реакция — чрезвычайно сложная цепная реакция, включающая образование формальдегида найдено, что основные продукты этой реакции следующие [c.75]
Первым обширным исследованием, проведенным с помощью масс-спектрометра, была работа Лейфера и Ури [23], которые изучали пиролиз диметилового эфира и ацетальдегида.Хотя им и не удалось обнаружить радикалы, но они смогли показать, что промежуточным продуктом разложения димети лового эфира является формальдегид, и проследить его концептрацию. Более успешной была попытка Эльтентона [24, 25], которому удалось сконструировать установку, способную обнаружить свободные радикалы при пиролитических реакциях и в пламенах даже нри высоких давлениях (около 160 мм рт. ст.). Он также смог обнаружить присутствие радикалов СНз при пиролизе углеводородов, радикалов СНг из СНгКг, а также СНО и СНз при горении СН в кислороде. Метод определения основан в принципе на том, что энергия электронов, необходимая для ионизации радикалов, меньше энергии электронов, необходимой для образования ионизированных частиц из самих исходных молекул. Это дает возможность определять малые количества радикалов в присутствии больших количеств соединений, собственные спектры которых затмевают спектры радикалов. [c.97]
Теплота сгорания газообразного диметилового эфира, СН —О—СН3, с образованием диоксида углерода и жидкой воды равна -1461 кДж на 1 моль эфира, а) Вычислите стандартную теплоту образования диметилового эфира и сравните полученный результат со значением, приведенным в приложении 3. б) При помощи таблицы энергий связей вьиислите стандартную теплоту образовании диметилового эфира. Проиллюстрируйте ващи вычисления при помощи энергетической диаграммы типа изображенной на рис. 15-7 укажите на ней все энергетические уровни и энергетические переходы. Согласуется ли ваш ответ с ответом на вопрос (а) [c.42]
В другой работе [48] для синтеза метанола описаны промотированные цинком медные катализаторы Ренея, которые готовят выщелачиванием алюминий-медь-цинковых сплавов. Эти катализаторы имеют высокую активность и селективность, приводят к образованию диметилового эфира, что может оказаться благоприятным, если смесь метанола и диметилового эфира используется в производстве бензина по способу Мобил [49]. [c.232]
Попытки моделирования взрывов парового облака стали осуществляться лишь после того, как существование этого явления бьшо реально осознано. Наиболее известна модель, предложенная в отчете [51геЫочу,1972], в которой взрыв парового облака сравнивается со взрывом эквивалентного количества ТНТ. Несмотря на достаточную обоснованность предложенной модели можно заметить, что она неспособна представить явления, происходящие вблизи центра взрыва ТНТ. Это обусловлено тем, что взрыву парового облака не свойственно бризантное действие, характерное для конденсированного ВВ. В непосредственной близости от места взрыва конденсированного ВВ давление может превышать 1 ГПа [Соок,1966], в то время как максимальная величина избыточного давления взрыва парового облака даже при наличии соответствующих условий не достигает и нескольких единиц МПа. Данное положение может быть проиллюстрировано сравнением двух случаев аварий 21 сентября 1921 г. в Оппау (Германия) и 29 июня 1943 г. в Людвигсхафене (Германия). В первой из них из-за детонации примерно 4 тыс. т смеси нитрата аммония на месте взрыва образовалась воронка глубиной 10 м (см. разд. 11.1). Во втором случае произошел взрыв парового облака, содержащего примерно 18 т диметилового эфира (см. разд. 13.12). Образования воронки не было, так же как и в любой другой аварии, причиной которой являлся взрыв парового облака. Если иногда при взрыве парового облака воронка и образуется, то это обусловлено истечением сжиженного газа, вызывающим размыв почвы в непосредственной близости от места утечки. Не исключено, что взрыв парового облака может вызвать незначительное приминание легкого грунта, что регистрируется приборами, однако такое образование не имеет кромки, характерной для кратера, образованного в результате взрыва обычного ВВ. [c.290]
Количество тех или иных побочных соединений в продукциои-ной смеси зависит от температуры, давления, состава исходной газовой смеси, селективности и состояния катализатора. Наиболее существенными примесями являются метан и диметиловый эфир. По сравиению со всеми побочными процессами (а) — (е) получение метилового спирта идет с максимальным уменьшением объема, поэтому Б соответствии с принципом Ле Шателье повышение давления сдвигает равновесие в сторону образования метилового спирта. Так как процесс экзотермичен, то при повышении температуры равновесие сдвигается влево и равновесная степень превращения синтез-газа в метиловый спирт уменьшается. В то же время при недостаточно высоких температурах скорость процесса чрезвычайно мала. Поэтому в промышленности процесс ведут в узком интервале температур с колебаниями в 20—30°С. Константа равновесия основной реакции [c.165]
Английские ученые Уинфилд и Диксон в 1941—1945 гг. показали возможность получения полиэфиров терефталевой кислоты и гли-колей. Поликонденсация диметилового эфира терефталевой кислоты и этиленгликоля — диаметилтерефталата — приводит к образованию лавсана, имеющего следующую формулу [c.351]
В настоящее время известно большое количество гомогенных мономолекулярных реакций, протекающих в газовой фазе и удовлетворяющих кинетическим уравнениям первого порядка. К ним относятся реакции распада NjOs с образованием NO2, реакция разложения азометана HgNa H., с образованием СаН и N . процесс разложения диметилового эфира с получением СН4, На и СО, гидролиз ряда углеводородов и многие другие. [c.348]
Нагревание пиридиновых солей высокомолекулярных алкилсерных кпслот выше 130° ведет к образованию эмульгаторов [135], которые, возможно, имеют общую формулу (RNGsHj) HSO4. Метилсульфат калия разлагается при температурах 220—280° с образованием диметилового эфира [136] [c.26]
Метилсерная кислота. При нагревании эквимолекулярных количеств метилового спирта и серной кислоты при температуре 100° или ниже получается только метилсерная кислота [143], но в условиях применения избытка спирта и перегонки реакционной смеси метилсерная кислота испытывает дальнейшее превращение в диметиловый эфир. Кремап и Нейман [144] определили скорости образования метилсерной кислоты при температурах 40 и 50° и скорость образования диметилового эфира при 100° путем измерения кислотности реакционных смесей [c.26]
Все эти соединения могут быть получены синтетическим путем, и поэтому их строе11ие не вызывает никаких сомнений. Диметиловый эфир морфола синтезируют по методу, разработашгому Пшорром. Для этого 2-нитро-3,4-диметоксибензальдегид конденсируют с фенилуксусной кислотой, полученную 2-нитро-3,4-диметокси-а-фенилкоричную кислоту (I) восстанавливают до соответствующего аминосоединения, превращают в диазосоединение (И) и обрабатывают медным порошком. При этом происходит замыкание кольца с образованием 3,4-диметоксифенантрен- [c.1111]
Напишите схемы реакций образования а ) диметилового эфира фталевой кислоты б) диэтилового эфира терефталевой кислоты. [c.102]
На самом же деле возможно сосуществование соединений-изомеров, свободные энергии образования которых АО / очень сильно различаются. Так, ДО / диметилового эфира СН3ОСН3 на 54,4 кДж/моль выше, чем у изомерного ему этилового спирта. Равновесная смесь этих веществ практически не должна содержать диметилового эфира. [c.154]
При температуре 800 К. В справочных таблицах имеются стандартные изобарные потенциалы образования метанола, диметилового эфира и воды в виде идеального газа при 800 К AGf.soo (СН3ОН) = = — 88,28 кДж, ДО/, 800 ( aH O) = 19,41 кДж, ДО/, аоо (HjO) = = — 203,55 кДж. [c.138]
Для получения полиэфиров используют диметиловый эфир терефталевой кислоты. Преимущества его в сравнении со свободной терефталевой кислотой те, что он растворим в органических растворителях, в частности в этиленгликоле, и плавится при сравнительно низкой температуре (140—14ГС). Благодаря этому образование полиэфира осуществляется в однородной среде, что обеспечивает более высокую скорость реакции и получение однородного продукта. [c.217]
Как правило, реакция элиминирования сопровождается побочной реакцией нуклеофильного замещения, приводящей к образованию спирта Р4М+ОН - РОН-ЬКзН [179], но это редко вызывает затруднения. Однако если ни один из четырех заместителей атома азота не содержит р-водорода, то единственно возможной реакцией оказывается замещение. При нагревании Me4N+0H- в воде получается метанол, а в отсутствие растворителя образуется не метанол, а диметиловый эфир [180]. [c.50]
На самом же деле возможно сосуществование соединений-изомеров, свободные энергии образования которых G отличаются на очень большие величины. Так, ДО диметилового эфира СН3ОСН3 на 13 ктлЫоль выше, чем у изомерного ему этилового спирта. Равновесная смесь этих веществ практически не должна содержать диметилового эфира, а смеси с другим составом должны быть термодинамически неустойчивы. Тем не менее устойчивые во времени смеси диметилового эфира и этилового спирта могут быть составлены с каким угодно соотношением концентраций. Это объясняется тем, что термодинамическое равновесие реакции К Н не достигается, т. е.-реакции Н К и К Н протекают с неизмеримо малой скоростью. При заметной скорости взаимопревращения термодинамическое равновесие достигается с течением времени, но неустойчивый изомер довольно / олго сосуществует с устойчивым. При больших скоростях реакций изомеризации существование изомеров определяется только термодинамическими критериями. [c.59]
Природные хлорины с 6-лактонным циклом обладает всеми характерными свойствами циклических сложных эфиров. Было изучено взаимодействие лакгона диметилового эфира хлорина рб с аммиаком, гидразином и этаноламином. Оказалось, что при воздействии всех оснований происходит раскрытие лактоиного кольца с образованием спирта по положению 18. [c.38]
Простые эфиры легко дают оксониевые соединения, типа комплексных, с трехфтористым бором, с галоидными солями магния и т. д. подобное соединение образуется и с серным ангидридом. При непосредственном действии серного ангидрида на простой эфир сначала образуется продукт присоединения се-рного ангидрида и затем происходит перегруппировка, в результате которой получается диалкилсульфат. Эта перегруппировка затрудняется с утяжелением радикалов образование диалкилсульфатов проходит с хорошим выходом только для диметилового эфира уже хлорметнловый эфир дает соответствующий сульфат с выходом только 30% для этилового эфира выходы еще меньше, а прн действии серного ангидрида на диизопропиловый эфир образуются смолы, из которых не удается выделить индивидуальных веществ даже при перегонке в глубоком вакууме Весьма возможно, 0 промежуточные продукты присоединения серного ангидрида могли бы быть получены, если проводить реакщгю при низких температурах и больших разбавлениях в инертных растворителях. [c.249]
Исследованием диметилового эфира апоморфина было установлено, что он является третичным основанием, содержащим НСНз-группу, и что в его молекуле имеются два фенольных гидроксила. При двукратном гофманском распаде происходит отщепление трнметиламина во второй стадии с образованием непредельного соединения — вН вО, [c.460]
chem21.info