Реакция с простыми эфирами. Реакция образования простого эфира
Реакция с простыми эфирами
Условно считается что простые эфиры не реагируют с реактивами Гриньяра, а говоря о реакциях реагентов Гриньяра с эфирами как правило имеются в виду их реакции нуклеофильного замещения с $\alpha$-галогензамещенными эфирами и оксиранами (эпоксидами). Но в жестких условиях реактивы Гриньяра могут реагировать и с простыми эфирами в результате чего также происходит нуклеофильное замещение. Кроме того в данном случае также можно рассмотреть процесс образования эфиратов - координированных соединений реактивов Гриньяра с двумя атомами кислорода эфиров, которые образуются в обычных эфирных растворах реагентов Гриньяра. Кроме того особым случаем реакций реактивов Гриньяра с простыми эфирами является олефиновый синтез Бурда.
Реакции с эпоксидами
Реактивы Гриньяра взаимодействуют с большинством циклических эфиров (эпоксидов) с малым размером колеца по типу $S_{N2}$-замищення. Угловое напряжение наблюдающееся в трех- и четырехчленных циклах облегчает раскрытие кольца, тогда как свободные от напряжения пяти- и шестичленные циклические эфиры практически не реагируют с реактивами Гриньяра или реагируют, но при крайне жестких условиях и иногда с деструкцией эфиров.
Рисунок 1.
Рисунок 2.
Реакция с ацеталями обычно идет в очень жестких условиях. В случае смешанных ацеталей преимущественно отщепляется именно та группа, которая является лучшей уходящей группой в нуклеофильном замещении, например, группа $ArO$, а не $AlkO$:
Рисунок 3.
Циклические ацетали, особенно 1,3-диоксоланы (ХVIII) обычно настолько инертны в этой реакции, что их часто используют как защиту соответствующей карбонильной группы.
Рисунок 4.
Взаимодействие реактивов Гриньяра с этилортоформиатом используется для синтеза альдегидов или их ацеталей:
Рисунок 5.
Реакции с галогензамещенными эфирами
В случае галогензамещенных эфиров реакция с реактивами Гриньяра идет иначе:
Рисунок 6.
В данном случае радикал из реактива Грньяра меняется на галоген и образуется эфир с более длинной молекулой.
Принимая во внимание различную реакционную способность атомов галогенов в реакцях замещения, можно с высокой долей вероятности правильно предсказывать строения продуктов реакций реагентов Гриньяра с галогензамещенными эфирами. Так, если в эфире содержится два атома галогена, первый из которых расположен в аллильном (или бензильном) положении, а другой расположен в винильном (или арильном) положении, тозамещение будет происходить избирательно только по аллильному (бензильному) галогену.
Аналогично при наличии двух атомов галогенов, которые находятся по $\alpha$ - и $\beta$ положениям относительно эфирного кислорода, замещение будет проходить только по галогену в $\alpha$ - положении:
Рисунок 7.
Образование эфиратов
Простые эфиры обычно используются в качестве растворителей при получении реактива Гриньяра: диэтиловый эфир при синтезе алкил- и арилмагнийгалогенидов, а тетрагидрофуран - винилмагнийгалогенидов.
Реактивы Гриньяра растворимы в растворителях типа эфиров, так как мономерные диалкилмагниевые соединения координируются с двумя атомами кислорода эфиров и образуют т.н. эфираты:
Рисунок 8. Диалкилмагний координируется с двумя молекулами эфира. Автор24 - интернет-биржа студенческих работ
В этих структурах доступность неподеленной электронной пары кислорода удовлетворяет требования трехцентровой двуэлектроннй связи для дополнения октета у магния.
При концентрировании эфирного раствора реактива Гриньяра можно получить эфираты, которые при дальнейшем нагревании довольно трудно теряли эфир даже при критическом нагревании в вакууме. В большинстве случаев этим эфиратам отвечала эмпирическая формула $RMgXx_2(C_2H_5)_2O$. Для отдельных эфиратов (например, фенилмагнийбромида) был сделан даже рентгеноструктурный анализ, который выявил, что этот диэфират имеет структуру неправильного тетраэдра, в центре которого находится атом магния.
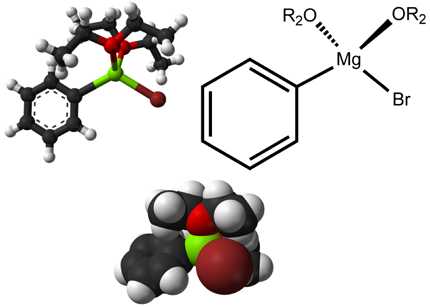
Рисунок 9.
Существенно, что расстояния между атомом магния и атомами кислорода молекул эфира достаточно малы, что свидетельствует о прочности этих ковалентных связей построенных по принципу донорно-акцепторных. А расстояния между атомами магния и галогена в структуре для соседних молекул, наоборот, настолько велики, что можно полностью исключить возможность образования димера. Итак, в твердом состоянии реактив Гриньяра представляет собой мономерный диэфират.
Олефиновый синтез Бурда
Олефиновый синтез Бурда представляет собой органическую реакцию формирования алкенов из простых эфиров, несущих атом галогена сопряженном с атомом кислорода ($\beta$-гало-эфиров) с использованием металла, таких как магний или цинк. Данную реакцию открыл Сесил Е. Бурд в 1930 году и теперь она является классической реакцией идущей с высокими выходами и широкой областью применения.
Рисунок 10.
Данная реакция является реакцией элиминирования с магнием, в которой формируется промежуточный реагента Гриньяра. Алкокси группа является плохой уходящей группой, и поэтому предложен $E1cB$ механизм реакции элиминирования. В оригинальной методике описан органический синтез изоптена в несколько этапов.
Рисунок 11.
И уже в 1931 данная методика распространилась на получение 1,4-диенов с магнием. В первой части реакции аллильный реагент Гриньяра действует в качестве нуклеофила и происходит нуклеофильное алифатическое замещение.
Рисунок 12.
spravochnick.ru
Образование простых эфиров - Справочник химика 21
Как видно из механизма образования простых эфиров из спиртов, неподеленная пара электронов атома кислорода способна взаимодействовать с сильными кислотами, образуя оксониевые соединения [c.166]
Образование простых эфиров из спиртов может происходить в газовой фазе в присутствии оксида алюминия, оксида тория или обезвоженного КА1 (804)2. При проведении реакции необходимо строго соблюдать температурный режим, так как повышение температуры влечет за собой образование алкенов. [c.146]
Образование олефинов из первичных спиртов осложняется реакцией образования простых эфиров [c.345]
Б мягких условиях (270—300 °С, 30 кгс/см, WS2) происходит не только восстановление спиртов, но и образование простых эфиров, являющихся промежуточными продуктами [c.193]
Ион RS , реагируя с хлорпроизводными, дает диалкилсульфид, являющийся главным из побочных продуктов (аналогично образованию простых эфиров ири щелочном гидролизе хлорпроизводных) [c.270]
Образование простых эфиров [c.18]
Основной побочной реакцией при гидролизе алкилсульфатов является образование простых эфиров [c.221]
Дегидратация спиртов до олефинов протекает в ряде случаев, вероятно, через стадию образования простых эфиров. [c.60]
Побочные реакции заключаются в образовании простых эфиров, полимеров и диалкилсульфатов [c.140]
Процесс сопровождается побочными реакциями образования простого эфира, ацетальдегида, олигомеров этилена [c.65]
К категории нуклеофильных реакций относятся такие распространенные процессы органической химии, как гидролиз галоидных алкилов, этерификации и омыление эфиров, амидирование, образование простых эфиров, синтез нитрилов по Кольбе, реакция Манниха и т. п. [c.189]
На наличие гидроксильной группы (спирты). Образование простых эфиров при нагревании. Определяются по запаху. [c.357]
В присутствии спиртов помимо образования простых эфиров фенолов происходит также образование углеводородов (см. Замещение диазогруппы водородом ) [c.190]
Введение в цепь связи —О— при образовании простого эфира [c.443]
Атом водорода гидроксильной группы замещается на углеводородный радикал (образование простых эфиров) [c.269]
В присутствии водоотнимающих катализаторов спирты могут взаимодействовать между собой с образованием простых эфиров [c.320]
Следует обратить внимание на реакцию образования простых эфиров фенолов вода выделяется за счет гидроксигруппы [c.327]
Следует обратить внимание на реакцию образования простых эфиров фенолов вода выделяется за счет гидроксигруппы спирта и водорода фенольного гидроксида. Это свидетельствует о том, что связь С —О в фенолах гораздо прочнее, чем в спиртах, что достигается за счет взаимодействия я-электронов бензольного ядра с неподеленной парой электронов кислорода. Поэтому ОН-группа в фенолах не замещается на другие атомы или группы атомов, как это имело место в спиртах. При взаимодействии фенолов с карбоновыми кислотами образуются сложные эфиры [c.367]
Таьим образом, гидролиз с замещением атома галогена следует проводить с помощью соды, что предотвращает отщепление НС1 и снижэ Т побочное образование простого эфира. Оптимальное соотношение хлорпроизводного и воды выбирают исходя из экономических соображений — сопоставляя селективность с энергетическими затратами на отгонку избытка воды (обычно этот оптимум соответствует получению водных растворов спирта с концентрацией 1—1,5 моль/л). Наконец, для повышения селективности гидролиза целессобразно применять реакторы, близкие к модели идеального вытес ения. [c.175]
Побочные реакции и селективность процесса. При гидратации элефинов наряду с основной реакцией протекают олигомеризация элефина (получение низкомолекулярных полимеров) и образование простого эфира. Все они идут через промежуточную стадию иона карбония, что можно изобразить схемой [c.186]
Внутримолекулярная дегидратация имеет более высокую энергию активации по сравнению с образованием простого эфира. По этой причине, а также из рассмотрения приведенной выше схемы следует, что дегидратацию с образованием ненасыщенной связи надо осуществлять при повышенной температуре и низком парциальном давлении или концентрации спирта. Дегидратацию с образованием простого эфпра проводят при более низкой температуре, более высоких концентрации и парциальном давлении спирта (например под некоторым давлением) и при неполной коиБсрсии спирта в реакторе. [c.187]
Дегидратация с образованием простых эфиров. Ранее уже го- зрилось о побочном образовании простых эфиров при гидролизе слорпроизводных (стр. 174) и гидратации олефинов (стр. 186). [c.198]
Л еркантаны в свою очередь способны присоединяться по двойной вязи олефина, за счет чего гюзиикает система последователь-но-п 1раллельных реакций (сравн. с образованием простых эфиров при гидратации олефинов стр. 186), приводящая к сульфидам [c.271]
В случае ароксидных нуклеофилов реакция промотируется солями меди [73а], в присутствии которых нет необходимости в наличии активирующих групп. Эта реакция служит методом получения диариловых эфиров и носит название синтез эфиров по Ульману [74] ее не следует путать с более важной реакцией сочетания Ульмана (реакция 13-16). Несмотря на присутствие солей меди, порядок реакционной способности типичен для нуклеофильного замещения [75]. Поскольку арилоксимедные (I) реагенты ArO u взаимодействуют с арилгалогенидами с образованием простых эфиров, было высказано предположение, что они являются интермедиатами в синтезе эфиров по Ульману [c.21]
Реакции со спиртами. Алкилсульфонаты реагируют со спиртами с образованием простых эфиров или олефинов в зависимости от природы алкильной группы и спирта [c.360]
Реакции оптически активных сульфонатов. В 1923 г. было сделано наблюдение [212 а], что при алкилировании посредством оптически активных эфиров п-толуолсульфокислоты обычно имеет место вальденовская перегруппировка. Реакции этого типа впоследствии подробно исследовались, так как вопрос о том, в какой из двух реакций происходит перегруппировка, в данном случае легко разрешим, тогда как в классических примерах перегруппировки это не так легко сделать. Эфир -бензилметилкарбинола с п-толуолсульфокислотой реагирует с ацетатом калия в спиртовом растворе с образованием /-уксусного эфира этого спирта, а с алкоголятом натрия — с образованием простого -эфира [c.371]
Простые эфиры целлюлозы получаются действием на целлюлозу галоидалкилов, галоидарилов, алкил- и арилсульфатов, а также алкиленоксидов в щелочной среде. Реакция образования простых эфиров целлюлозы необратима и протекает по следующей схеме [c.308]
Эфиры третичных спиртов могут быть омылены при нагревании со спиртами с образованием простых эфиров (алкоголиз). В этом случае расщепление происходит не по связи ацил—кислород, а по связи алкил—кислород (Коен, Шне11дер) [c.263]
Образование простых эфиров по.пиметиленфенолов. Полнме-1иленфенол1)1 могут вступать в реакцию с иодалкилами или диал-килсульфатами, образуя простые эфиры [c.387]
Однако диазометан в обычных условиях неспособен метилировать спирты с образованием простых эфиров. Эту реакцию можно проводить только в присутствии каталитических количеств кислот Льюиса (например, ВРз), алкоксидов некоторых металлов [например, А1(ОС2Н5)з] или некоторых кислот с комп- [c.466]
Образование простых эфиров. Взаимодействие алкоголятов с га-логеноалкылами можно получать простые эфиры [c.109]
При температуре 140°С с серной кислотой спирты претерпевают межмолску-лярную дегидратацию с образованием простых эфиров (см. выше). [c.343]
Феноляты вступают во взаимодействие е галогснзамсщенными углеводородами с образованием простых эфиров. [c.346]
chem21.info
Кислород образования простых эфиров - Справочник химика 21
Простые эфиры и им подобные вещества при хранении, особенно на свету, способны окисляться кислородом воздуха с образованием чрезвычайно взрывоопасных пероксидов. При перегонке таких растворителей пероксиды концентрируются в перегонной колбе, в результате чего часто происходят взрывы. Перед работой с эфирами следует обязательно проверять, не присутствуют ли в них пероксиды. Для этого 2—3 мл эфира встряхивают в пробирке с равным объемом 2 1)-ного раствора иодида калия и несколькими каплями разбавленной серной или соляной кислоты. Бурое окрашивание (выделяется свободный иод) указывает на присутствие пероксидов. [c.59]
О том, что в данном случае реакция протекает по механизму N2, а не с промежуточным образованием карбокатиона, свидетельствует то, что при расщеплении оптически активного простого эфира (56) образуется оптически активный спирт. Это означает, что связь атома кислорода с асимметрическим атомом углерода в процессе реакции не затрагивается. [c.156]Следует обратить внимание на реакцию образования простых эфиров фенолов вода выделяется за счет гидроксигруппы спирта и водорода фенольного гидроксида. Это свидетельствует о том, что связь С —О в фенолах гораздо прочнее, чем в спиртах, что достигается за счет взаимодействия я-электронов бензольного ядра с неподеленной парой электронов кислорода. Поэтому ОН-группа в фенолах не замещается на другие атомы или группы атомов, как это имело место в спиртах. При взаимодействии фенолов с карбоновыми кислотами образуются сложные эфиры [c.367]
Сульфиды КЗК являются аналогами простых эфиров КОК. Присутствие двух неподеленных электронных пар атома серы в сульфидах, как н атома кислорода в простых эфирах, объясняет образование комплексных продуктов присоединения. Фтористый водород, галоиды, фтористый бор, гидрид бора, сернистый ангидрид, хлорная ртуть, мочевина и многие другие соединения образуют с сульфидами стабильные комплексы. Продукты [c.273]
Внедрение ио связям гетероатом —водород Z—Н., Карбены реагируют со спиртами с образованием простых эфиров. Сначала происходит атака электронной пары п кислорода, а затем — миграция протона [c.478]
Простые эфиры кольчатого строения. Многоатомные спирты также способны к образованию простых эфиров. При этом возможно внутримолекулярное взаимодействие двух гидроксильных групп с образованием веществ кольчатого строения, у которых эфирный кислород входит в состав кольца. Степень легкости образования подобных кислородсодержащих кольчатых группировок и, соответственно, степень их стойкости зависят от напряжений при их замыкании. Правило напряжения, разобранное ранее для кольчатых углеводородов (стр. 59), действительно и в данном случае. [c.175]
Если в реакцию вступает относительно много серной кислоты и мало спирта, то при дальнейшем нагревании этилсульфата образуется непредельное соединение — этилен (стр. 60). Это указывает на то, что в данных условиях регенерация серной кислоты происходит за счет отщепления атома водорода в той же молекуле, но от соседнего атома углерода этилсульфата, ибо только при этих условиях можно ожидать образования непредельного углеводорода, в данном случае этилена. При обратном соотношении, когда имеется мало серной кислоты и относительно много спирта, образуется эфир. Обычно регенерация серной кислоты в этих условиях протекает за счет отщепления атома водорода от новой молекулы спирта, ибо только в таком случае можно ожидать образования простого эфира, для которого характерен кислород- [c.142]
Сопоставляя формулы простого и сложного эфира, легко сделать вывод, что сложные эфиры (содержащие избыток отрицательного кислорода) должны быть менее устойчивыми. Действительно, реакция образования простого эфира практически необратима напротив, реакция образования сложного эфира — процесс обратимый (что показано стрелками) сложные эфиры легко подвергаются гидролизу (омылению) с обратным переходом в спирт и кислоту. Эта особенность сложных эфиров используется в практике для получения и спиртов и кислот. [c.128]
Биполярные апротонные растворители имеющие высокую диэлектрическую постоянную и большой дипольный момент, сильно сольватируют растворенное соединение. Благодаря тому, что их электронная плотность локализована на атомах кислорода (диме-тилсульфоксид, диметилформамид, Л -метил-2-пирролидон, простые эфиры и др.), они являются активными акцепторами протона дри образовании водородной связи, и весьма эффективно сольватируют катионы. Анионы биполярными растворителями сольватируются слабо, особенно если они жесткие, мало поляризуемые. Соли в таких растворителях обычно диссоциируют с образованием сильно сольватированных катионов и слабо сольватированных анионов. [c.162]
В отличие от фурана, в котором неподеленные пары р-электронов атома кислорода участвуют в образовании ароматической системы, тетрагидрофуран обладает всеми свойствами простых эфиров в частности, он способен образовывать эфираты, предоставляя свои пары электронов кислотам Льюиса [c.513]
Из-за смещения неподеленной электронной пары кислорода к л-элект-ронам бензольного кольца атомы углерода получают отрицательный заряд. Вследствие этого происходит смещение электронов связей С—Н в бензольном кольце в сторону водорода, т. е. поляризация и соответственно ослабление связей С—Н. Поэтому водород в бензольном кольце фенола легко (без катализаторов и нагревания) замещается атомами или группами атомов (галогенами, ЫОа", СНз и т. п.). Реакции образования простых и сложных эфиров для фенолов не характерны. [c.261]
Одновалентный атом имеет только одну орбиталь, которая может участвовать в образовании связи, но атомы с валентностью 2 и более должны образовывать связи, используя по крайней мере две орбитали. Так, атом кислорода имеет две наполовину заселенные орбитали, определяющие его валентность, равную двум. Кислород образует простые связи за счет перекрывания этих орбиталей с орбиталями двух других атомов. Согласно принципу максимального перекрывания, ядра этих двух атомов должны образовывать с ядром кислорода угол 90°, так как в образовании связи участвуют р-орбитали кислорода, расположенные взаимно перпендикулярно. Аналогичным образом следовало бы ожидать, что при образовании трех простых связей у атома азота, имеющего три взаимно перпендикулярные р-орбитали, углы между связями должны составлять 90°. Однако в действительности наблюдаемые величины валентных углов отличаются так, в молекуле воды они составляют 104°27, в молекуле аммиака — 106°46 [5], а в спиртах и простых эфирах углы еще больше (табл. 1.5). Этот вопрос будет обсуждаться в разд. 1.11 здесь же важно отметить, что ковалентные соединения действительно имеют определенные углы между связями, и хотя атомы постоянно колеблются, средние положения для каждой молекулы данного соединения остаются неизменными. [c.19]
На воздухе простые эфиры способны окисляться с образованием перекисей, в которых группа —О — О— внедряется по связи С—Н углеродного атома, соседнего с эфирным кислородом, наири-мер [c.168]
Простые эфиры обладают особенной склонностью к автоокислению, причем атака направляется на атом углерода, расположенный в а-положении по отношению к кислороду. Реакции окисления часто идут, однако, дальше образования перекисных [c.300]
В настоящем разделе рассматриваются,область применения реакции различных диазоалканов с арЩёгйдами и кетонами и границы указанной реакции. При этом не делается попыток дать полный обзор реакций (некоторых типов карбонильных соединений, например р-кетоальдегидов (оксиметиленкетонов), эфиров -кетонокислот, р-дикетонов и т. д., поскольку они реагируют с образованием производных, алкилированных по кислороду. Образование простых эфиров енолов представляет собой пример [c.474]
Эфиры третичных спиртов могут быть омылены при нагревании со спиртами с образованием простых эфиров (алкоголиз). В этом случае расщепление происходит не по связи ацил—кислород, а по связи алкил—кислород (Коен, Шне11дер) [c.263]
Синглетные карбены представляют собой производные с дефицитом электронов, которые могут взаимодействовать с основным, атомом кислорода в простых эфирах с образованием океониевых илидов, особенно в тех случаях, когда карбен несет группы, оттягивающие электроны [уравнение (27)]. Постулировано образование илидов оксония как интермедиатов в реакциях взаимодействия эфиров с карбенами [69]. Основным типом реакции синглетного [c.314]
А. Е. Фаворский проводил исследования и с двухатомными спиртами, в частности по дегидратации гликолей. Эти явления он истолковывал как процессы окисления — восстановления и образования оксониевых соединений, в которых кислород четырхвалентен. При изучении дегидратации простейшего двухатомного спирта (этиленгликоля) А. Е. Фаворский развил и уточнил работы зарубежных авторов (Вюрц, 1859 Лоренцо, 1863), в подробностях выяснил ход реакции и предложил простой метод получепия диоксана из гликоля — перегонка гликоля в присутствии небольших количеств серной кислоты [210]. Ход реакции заключался в следующих превращениях (аналогичных процессу образования простых эфиров из алкоголей, как это установил еще в середине XIX в. английский химик Вильямсон) [c.211]
Могут быть рассмотрены два механизма замещения алкилкар-боксилатов нормальная реакция, включающая нуклеофильную атаку по карбонильной группе с разрывом связи ацил—кислород, в результате чего образуется новый алкоксид и измененный сложный эфир [уравнение (35)], и вторая возможность, где подобно нормальной реакции сульфонатов происходит нуклеофильная атака у алкильного атома углерода с разрывом связи алкил—кислород с образованием простого эфира и аниона кислоты [уравнение (36)]. Первая реакция обратима, вторая — необратима. По этому методу получают хорощий выход диметилового эфира [104] уравнение (37) , однако он не применим в общем случае для синтеза смещанных алкильных эфиров, вероятно вследствие эфирного обмена за счет обратимости реакции, что может приводить к смесям продуктов. [c.320]
Апротонные кислоты способны к образованию различных комплексов путем присоединения к атому кислорода в простых эфирах и других соединениях, содержащих карбонильную группу (альдегиды, кетоны, сложные эфиры и др.). Примером может служить образование комплекса этилового эфира с трифторобором [c.265]
АгЗОаОН). Реакция протекает параллельно в двух направлениях алкилирование в ядро с образованием алкилфенолов и алкилирование по атому кислорода с образованием простых эфиров фенола [c.344]
Причем скорость значительно больше, чем для соответствующих спиртов. Большая основность кислорода в простом эфире, чем в спирте, наводит на мысль, что в обоих случаях переходное состояние может включать перенос протона от кислоты с последующим образованием ионной пары XIII [c.309]
Ни в одном из этих случаев гидролиза но механизму Вдь не было подтверждено, что кинетически они действительно представляют собой мономолекулярные реакции нанример, не было показано, что скорости гидролиза или образования простых эфиров нечувствительны к щелочам. Однако это наблюдалось в некоторых других случаях. Хэммонд и Радесилл изучили превращение трифенилметилового эфира бензойной кислоты в смеси этилового спирта и метилэтилкетона в трифенилметилэтиловый эфир и в бензойную кислоту, которое должно включать расщепление связи алкил — кислород [c.945]
К числу обычных функциональных групп, способных образовывать водородные связи с водой, относятся окси-, карбокси-, амино- и амидогруппы, а также слон ноэфирная, карбонильная, эфирная и нитрильная группы. Значительная растворимость простейших алифатических карбонильных соединений легко объяснима тем, что несвязанная пара кислорода полярной группы С == О допускает образование сильной водородной связи с водой. Атом кислорода в простом эфире и атом азота в нитриле также могут давать водородные связи с водой за счет своих свободных пар электронов, а растворимость амидов, слоишых эфиров, кислот и фенолов отчасти объясняется также реакцией с водой. [c.128]
Миграция водорода энергетически более выгодна по сравнению с простым разрывом связи без миграции, так как она приводит к образованию двойной связи с каждой разорванной связью образуется новая. Атом водорода мигрирует из Р-положения к разрываемой связи. Наличие в цепи атома кислорода или азота в а-положении к разрываемой связи увеличивает вероятность данной перегруппировки, очевидно, благодаря наличию у них несвязанных электронов. Так, в спектре пропилбензола интенсивность перегруппировочного пика с массой 92 равна всего 0,3%. При введении кислорода (фе-нилэтиловый эфир) пик соответствующего перегруппировочного иона с массой 94 становится максимальным в спектре. [c.112]
Алкилгалогениды можно алкилировать простыми эфирами или кетонами, что приводит к образованию оксониевых солей в том случае, если присутствуют очень слабый отрицательно заряженный нуклеофил, который может выступать противоионом, и кислота Льюиса, которая может связывать Х [588]. Типичная методика состоит в обработке алкилгалогенида эфиром или кетовом в присутствии AgBp4 или AgSbFa. Ион серебра служит для связывания Х , а ВР4- или SbPe становится противоионом. Согласно другому методу, алкилгалогенид обрабатывают комплексом, образующимся при взаимодействии кислородсодержащего соединения и кислоты Льюиса, например R2O—BFa-f RF- RaO+BF,-, однако наилучшие результаты этот метод дает, если в одной молекуле присутствуют атомы кислорода и галогена так, что образуется циклический оксониевый ион. Простые эфиры и оксониевые ионы также вступают в реакции обмена [c.136]
Наиболее интересной реакцией простых эфиров является их взаимодействие с галоидными алкилами, ведущее к образованию комплексных рксониевых соединений по схеме RQR + Rr = [ОНз]Г. Кислород играет в них роль, аналогичную роли азота при подобной же реакции галоидного алкила с третичным амином NR3 + КГ = = [NR4]r. Различны лишь координационные числа обоих крмплексообразователей -4 для азота и 3 для кислорода. Получаемые комплексные соединения можно рассматривать как продукты замещения водорода на алкильные радикалы в ионах аммония [c.558]
Тенденция к аналогичному разрыву связи алкил — кислород имеет место также в случае эфиров таких вторичных спиртов, как РЬгСНОН, образующих наиболее устойчивые карбониевые ионы. Попытки осуществить переэтерификацию сложных эфиров, образованных такими спиртами, привели не к ожидаемому новому сложному эфиру, а к смеси кислота простой эфир [c.228]
Эти неподвижные фазы плохо растворяют алифатические углеводороды, но обладают некоторой селективностью для отделения к-парафипов от разветвленных и ненасыщенных углеводородов. Селективно задерживаются алкилбензолы. Одновременное присутствие атомов-акцепторов (кислород гидроксила и простых эфиров) и атомов-доноров (водород гидроксила) приводит благодаря образованию водородной связи к тому, что низшие члены ряда полигликолей способны к сильному взаимодействию не только с соединениями, содержащими гидроксильные группы и первичные аминогруппы, но и с соединениями, содержащими карбонильный кислород, вторичные и третичные аминогруппы или гетероциклически связанные азот или кис.пород. Так как водородная связь во всех этих случаях составляет главную часть сил притяжения, то для упомянутых классов соединений не наблюдается заметных различий в селективности. Поэтому не удивительно, что альдегиды, кетоны и простые эфиры выходят в последовательности повышения температур кипения. Так например, полиэтиленгликоль 2000 является наименее селективной неподвижной фазой для кислородных соединений. [c.200]
Соединения, молекулы которых ассоциированы за счет образования водородных связей (например, спирты и карбоновые кислоты) или содержат атомы кислорода или азота, которые могут служить акцепторами атомов водорода, обладающих протонной п JЛBижнo тью (например, некоторые простые эфиры и амины), очень легко растворяются в протонных растворителях (например, в этаноле). Если же в соединении нет ионных и полярных связей и оно не способно образовывать водородные связи (например, углеводороды и некоторые их галогенпроизводные), то такое соединение будет лучше растворимо в малополярных растворителях с низкой диэлектрической постоянной. [c.18]
Многие реакции термического разложения углеводородов, простых эфиров, альдегидов и кетонов протекают, по-видимому, по свободнорадикальному цепному механизму. В 1935 г. Райс и Герцфельд показали, как можно представить цепной механизм этих реакций, который приводил бы к простому суммарному кинетическому уравнению. В реакциях участвуют свободные радикалы, в том числе радикалы СН , С2Н5 и Н. Участие радикалов в ряде таких реакций было доказано с помощью металлических зеркал, посредством катализирования реакции полимеризации олефина, о которой известно, что она протекает по цепному механизму, и путем ингибирования реакций с помощью таких веществ, как окись азота или пропилен. Если каждая молекула ингибитора обрывает цепь, а каждая цепь приводит к образованию большого числа молекул продукта реакции, то очевидно, что даже следы ингибиторов должны оказывать заметное влияние на реакцию. Например, окисление сульфит-иона в растворе кислородом воздуха заметно подавляется добавлением следов спирта. [c.310]
chem21.info
Механизм простых эфиров - Справочник химика 21
Как видно из механизма образования простых эфиров из спиртов, неподеленная пара электронов атома кислорода способна взаимодействовать с сильными кислотами, образуя оксониевые соединения [c.166]
В табл. XII, 1 дана сводка сравнительных данных о кинетике реакций, ускоряемых молекулярным иодом. Механизм этих реакций сходен с механизмом распада диэтилового эфира. Характерным во всех случаях является изменение направления процесса в присутствии катализатора. Если ограничиться рассмотрением данных для распада трех простых эфиров, то бросается в глаза следующая закономерность для некаталитической реакции энергия активации увеличивается с усложнением молекулы, для каталитической — уменьшается. Ускорение, как видно из двух последних столбцов таблицы, обусловлено в основном снижением энергии активации в присутствии катализатора. Предэкспоненты увеличиваются не более чем в 70 раз этот эффект, по-видимому, также усиливается с усложнением молекулы распадающегося вещества. [c.276]О том, что в данном случае реакция протекает по механизму N2, а не с промежуточным образованием карбокатиона, свидетельствует то, что при расщеплении оптически активного простого эфира (56) образуется оптически активный спирт. Это означает, что связь атома кислорода с асимметрическим атомом углерода в процессе реакции не затрагивается. [c.156]
Opi гидролизе содой, в соответствии с ранее рассмотренным механизмом, реакция с карбонатным ионом дает только спирт, а простой эфир может получиться лишь за счет реакции со спиртом или с алкоголятом, образовавшимся из гидроксильного иона — продукта гидролиза соды водой. Тогда дифференциальная селективность будет равна [c.175]
На этом основании можно утверждать, что в данном случае расщепление протонированного простого эфира протекает уже по механизму 5ы1 [c.156]
В заключение можно сказать, что проведение омыления в условиях МФК синтетически выгодно в случае стерически затрудненных эфиров. При этом следует использовать систему твердый гидроксид калия/толуол и краун-эфиры или криптанды в качестве катализаторов. Кроме того, скорость гидролиза простых эфиров карбоновых кислот концентрированным водным раствором гидроксида натрия значительно выше для гидрофильных карбоксилатов. Хорошими катализаторами являются четвертичные аммониевые соли, особенно BU4NHSO4 и некоторые анионные и неионные ПАВ. Это указывает на то, что может осуществляться любой из трех возможных механизмов реакции на поверхности, мицеллярный катализ или истинная МФК-реакция. В зависимости от условий может реализоваться каждый из этих механизмов. Как было показано раньше, при МФК возможна экстракция кислот в форме ионной пары R4N+X----HY [57]. Ранние работы, в которых рассматривалось кислотное МФК-омыление, оказались ошибочными [1202, 1348]. Однако недавно было описано мягкое и селективное расщепление трет-бутиловых эфиров, которое происходит при перемешивании с [c.250]
Аутоокислению подвержены алканы. алкены, спирты, альдегиды и простые эфиры. Механизм образования гидропероксидов представлен ниже [c.151]
Все простые эфиры весьма устойчивы по отношению к ионным реагентам, но легко реагируют с кислородом по радикальному механизму. Практически это означает, что вследствие этою эфиры легко горят, причем даже взрывообразно (особенно легко окисляются С-Н-связи в а-положении к атому кислорода). [c.53]
Показано, что расщепление диэтилового эфира в присутствии литийорганического соединения приводит к образованию этилена и этилата лития, а расщепление ТГФ дает енолят ацетальдегида и этилен. Интенсивное изучение механизма разрыва связей простых эфиров показало, что он меняется в зависимости от природы реагирующих соединений и даже для одного и того же эфира возможна реализация альтернативных механизмов. Так, например, для расщепления диэтилового эфира под действием литийорганического соединения постулированы механизмы, включающие и даже а ф -элиминирование [c.255]
Обычно при получении эфиров не предполагают образования промежуточного дегидробензола, но его можно ожидать в тех случаях, когда наличие электроноакцепторных заместителей в исходном соединении не благоприятствует нуклеофильному механизму. Кроме того, для отрыва протона от бензольного кольца нужны такие сильные основания, что образование промежуточного дегидробензола редко имеет место при синтезе простых эфиров. Приведем два примера [c.358]
Следовательно, механизмы расш епления простых эфиров, содержащих неразветвленные и разветвленные алкильные остатки, различны. Это различие показано также при изучении поведения в условиях жидкофазного процесса не только модельных простых эфиров, но и возможных промежуточных продуктов — углеводородов и спиртов (табл. 34). [c.186]
Карбонилирование спиртов при катализе комплексами металлов имеет преимущество перед кислотным катализом, поскольку в последнем случае образуется много побочных продуктов дегидратации спирта (олефины и простые эфиры), а также изомерных кислот. Реппе впервые осуществил эти реакции при помощи карбонилов никеля и промоторов, которыми служили иод и его соли, галогенпроизводные и др. Активны карбонилы кобальта, железа, палладия н особенно родня, но в присутствии тех же промоторов. Роль последних объясняют промежуточным образованием алкилгалогенидов, которые затем карбонилируются по механизму близкому к оксосинтезу [c.543]
ЭПХГ обладает высокой химической активностью, при его гидролизе идут побочные реакции. Например, ЭПХГ может легко полимеризоваться, чему способствуют повышение температуры и контакт с некоторыми металлами, особенно с железом. В зависимости от применяемого катализатора получаются подвижные жидкости, высоковязкие масла или смолообразные продукты. Поэтому аппаратуру и трубопроводы для ЭПХГ рекомендуют делать из хромоникелевых сталей [167, 168]. Описан ионный механизм полимеризации эпоксидной группы под действием кислотных или щелочных катализаторов с образованием соединений типа полимерных простых эфиров [169]. В случае присутствия кислотного катализатора реакция протекает следующим образом [c.41]
Формилирование ароматических соединений под действием Zn( N)2 и НС1 называется реакцией Гаттермана (обзор см. [269]). В отличие от реакции 11-17 этот метод можно с успехом применять к фенолам и их простым эфирам, а также ко многим гетероциклическим соединениям, но не к ароматическим аминам. В оригинальном варианте этой реакции субстрат обрабатывали H N, НС1 и Zn b однако использование Zn( N)2 и НС1 (H N и Zn l2 генерируются in situ) делает проведение этой реакции более удобным и не снижает выхода продукта. Механизм реакции Гаттермана не исследовался подробно, но известно, что первоначально образуется азотсодержащее соединение, которое обычно не выделяют, а сразу гидролизуют до альдегида. Для промежуточного продукта предполагается структура, приведенная в уравнении реакции выше. Реакцию Гаттермана можно рассматривать как частный случай реакции 11-29. [c.361]
Для замены ингибиторов углекислотной коррозии ИКИПГ-1, КО, АНПО и ряда других был создан новый ингибитор, получивший название СТ. В его состав входят алифатические амины (до 10%), диэтиленгликоль (до 30%) и флотореагент ВЖС (до 60%). Диэтиленгликоль является гомогенизатором тройной смеси, а также снижает температуру застывания. Его защитное действие как простого эфира проявляется в том, что, будучи десорбентом воды, диэтиленгликоль создает благоприятные условия для адсорбции основных компонентов ингибитора на поверхности металла. Механизм действия ингибитора СТ [146] можно упрощенно представить следующей схемой удаление воды с поверхности образование органических радикалов [c.224]
Полагают, что синтез простых эфиров по методу Эрлепмейера протекает именно по этому механизму. [c.154]
Механизм аутоксидации альдегидов уже рассмотрен выше (стр. 234) в основе его лежат цепные механизмы. Простые эе зиры при хранении также постепенно самоокисляются. Хорошо известно, что долго хранящийся диэтиловый эфир содержит различные перекиси, из которых изучена перекись диоксиэтила СНдСНОН—О—О—СНОНСН.,, при нагревании переходящая в очень неустойчивую и взрьшчатАто диперекись диэтилидена [c.237]
Эти результаты можно объяснить, пр дположив, что реакция протекает по механизму 5к2. В протониривинной молекуле простого эфира иодид-ион атакует предпочтите, и.ыо атом углерода с большим положительным зарядом и при взаимодействии с которым возникает меньше пространственных затруднений, т. е. атом углерода метильной группы [c.156]
Эпоксисоединения — оксиран и его гомологи — также можно отнести к классу простых эфиров, однако их реакционная способность значительно выше. Это, по-видимому, объясняется тем, что в эпоксидах, как и в трехчленных циклических углеводородах, имеется значительное угловое напряжение валентные углы деформированы по сравнению с тетраэдрическим. В отличие от простых эфиров сс-эпоксиды способны реагировать не только с иодоводородной кислотой, но и с разбавленными хлороводородной и бромоводородной кислотами с образованием галогенгид-ринов. Эта реакция протекает по механизму, аналогичному взаимодействию галогеноводородов со спиртами. Кроме того, эпо- [c.157]
Несимметричные эпоксиды разветвленного строения, подобно третичным простым эфирам, реагируют по механизму 5, 1, т. е. в протонированном эпоксиде сначала раскрывается цикл с образованием карбокатиона (стадия, определяющая скорость всего процесса), а уже потом происходит в 1аимодействие со спиртом как с нуклеофилом [c.158]
Приведите схемы реакций образования из спиртов в присутствии серной кислоты следующих простых эфиров 1) диэтилового, 2) метплзтилового, 3) дииро-ПИЛ0В0Г0. Рассмотрите механизм реакции 2. [c.53]
Протекание реакций по механизму Вдь2 легко обнаружить, так как это единственный из шести наблюдаемых механизмов, при котором должно происходить обращение конфигурации R. Однако в последнем примере механизм становится очевидным из природы продукта, так как простой эфир не может образоваться иным путем. [c.114]
Механизмы переэтерификации (см. обзор [553]) идентичны механизмам гидролиза сложных эфиров, за исключением того, что вместо НОН действуют ROH, т. е. это механизмы с разрывом связи между ацильной группой и атомом кислорода. Если происходит алкильное расщепление, то образуется кислота и простой эфир [c.130]
Кетоны можно получать также при действии на фенолы или их простые эфиры нитрилов в присутствии РзСЗОаОН [324]. В этом случае реакция идет по другому механизму. [c.372]
Механизм реакции изучен недостаточно. Принято считать, что взаимодействие диазониевых солей с этанолом, приводящее к простым эфирам, происходит по ионному механизму (SnU, тогда как восстановление до АгН осуществляется по свободнорадикальному механизму [304]. Предполагается, что восстановление под действием Н3РО2 также идет по свободнорадикальному механизму [305]. Было показано, что при восстаповлении с помощью NaBh5 в качестве интермедиата образуется арил-диазен ArN = NH [306], получающийся в результате нуклеофильной атаки ионом 1ЗН4 атома азота в -положении. Подобные диазены можно получить в виде довольно устойчивых, частиц (время полупревращения несколько часов) в растворе [c.102]
Таким образом, механизм гидролиза енаминов аналогичен механизму гидролиза виниловых простых эфиров (т. 2, реакция 10-7). [c.328]
Перегруппировка простых эфиров под действием алкильных соединений лития называется перегруппировкой Виттига [не путать с реакцией Виттига (т. 3, реакция 16-47)]. Она аналогична перегруппировке 18-24 [282], однако требует более сильных оснований, например таких, как фениллитий или амид натрия R и R = алкил, арил или винил [303]. Один из атомов водорода можно заменить алкильной или арильной группами, и тогда образуется соль третичного спирта. Миграционная способность изменяется в ряду алил, бензил>этил>метил>фенил [304]. После отрыва протона основанием реакция, вероятно, протекает по механизму с участием радикальных пар [305], аналогичному механизму а из реакции 18-24. В радикальную пару входит кетильный радикал. В пользу этого механизма можно привести, например, такие доводы 1) внутримолекулярный характер перегруппировки в большинстве случаев 2) соответствие миграционной способности устойчивости свободных радикалов. [c.169]
Доказательство того, что основной механизм Криге действует даже и в этих случаях, получено в экспериментах с меченым кислородом Ю. Эти эксперименты основаны на том, что, как указывалось выше, при введении добавок альдегидов могут быть выделены смешанные озониды (например, 18). Как обычный, так и уточненный механизм Криге предсказывают, что если к реакционной смеси прибавить меченный Ю альдегид, то метка окажется на кислороде простого эфира (см. реакцию между 13 и 14), что и наблюдалось [174]. Имеются указания на то, что анты-форма 14 вступает в реакцию сочетания намного легче, чем сын-форма [175]. [c.284]
Простые эфиры — значительно более инертные соединения, чем спирты, где химическая активность обусловлена наличием гидроксильной группы. Эфиры устойчивы к действию щелочных металлов и щелочей, однако в сильнокислой среде за счет протонирования атома кислорода они превращаются в алкилоксо-ниевые катионы. Образовавшиеся катионы могут реагировать со многими нуклеофильными агентами. Механизм раскрытия эфирной связи под действием бромоводорода (или иодоводорода) приведен на следующей схеме (сравни механизм превращения спиртов в алкилгалогениды, разд. 4.1.1) [c.89]
Хотя механизм реакции остается далеко не ясным, можно все же полагать, что он связан с промежуточным расщеплением фуранового цикла пирослизевой кислоты. Во всяком случае, этот факт можно сопоставить с успешным применением рядом авторов (см., напр., 181—184) простых эфиров для алкилирования бензола и фенолов в присутствии А1С1з, [c.23]
Небезынтересным является вопрос о влиянии растворителя на восстановительную силу комплексных гидридов металлов. Для алюмогидрида лития такую зависимость проследить не удается, так как его высокая реакционная способность ограничивает выбор растворителей, сводя его лишь к простым эфирам, в которых он является мощным реагентом различия в восстановительной силе при этом незначительны. Напротив, использование борогидрида натрия, являющегося мягким восстановителем, позволяет заключить, что роль растворителя может быть чрезвычайно большой. Так, восстановление ацетона заканчивается за несколько минут в водном или спиртовом растворе и вовсе не наблюдается при проведении реакции в растворителях эфирного типа - ТГФ, диглиме и триг-лиме, хотя КаВН4 хорошо растворим в них. Следовательно, растворитель важен не только для достижения гомогенности среды. Роль его более сложна и может быть осмыслена лишь с учетом механизма реакции. [c.120]
К рассматриваемому типу реакций можно отнести и раскрытие кольца циклических простых эфиров, особенно легко протекающее с эпоксидами. Реакция сопровождается инверсией конфигурации менее пространственно затрудненного атома углерода и протекает по механизму внзоримолекулярного замещения [c.248]
В этой монографии методы синтеза простых эфиров разделены на шесть типов в соответствии с механизмом протекающих при этом реакций. Иногда реакции, отнесенные к разным типам, протекают по одинаковым механизмам. В некоторых случаях подобная классификация может показаться поверхностной или произвольной с точки зрения понимания истинного механизма процесса. Однако она придает большую связггость обсуждению, сопровождающему каждый раздел. Наиболее полезным направлением развития методов синтеза этого типа является превращение карбонильных соединений в эпокиси под действием диметилсульфонийметилида [разд. В.4]. [c.325]
Галогенпроизводные или сложные эфиры бензилов, аллилов и трет-глкитв склонны ионизироваться по механизму 5 1. При этом они не обязательно превращаются в простые эфиры с хорошим выходом, поскольку конкурирующей реакцией может быть реакция образования олефинов. Если образование олефина невозможно, [c.343]
Сложные эфиры можно получить из а,а-дихлоралкилзамещенных простых эфиров при гидролизе их водой [161]. Для гидролиза а,а-дифторалкилзамещенных простых эфиров необходимо применять более сильные гидролизующие агенты, такие, как 95%-ную серную кислоту [162, 163]. Выходы при этих реакциях гидролиза составляют от 55 до 83%. Механизм этого расщепления точно не установлен [163], но можно предполагать, что этот гидролиз протекает с большей легкостью, чем гидролиз тригалогензамещенных, в результате влияния простой эфирной группы [c.305]
Одиако весь процесс обратим и некоторое количество стирола остается в равновесии со спиртом таким образом, обмен оказывается возможным. Реакция замещенных стиролов со спиртами в присутствии сильных кислот приводит к ойрааованию простых эфиров по механизму, аналогичному описанному для гидраташтн [18]. [c.244]
По одному из двух возможных механизмов может протекать реакция образования простого эфира при рзаимо-действии диалкилсульфата со спиртом [c.149]
В более мягких условиях при нагревании простейших первичных спиртов с 96%-й серной кислотой при 130 -140 - С преимущественно получаются простые эфиры. Механизм этого превращения заключается в алкршировании первичного спирта либо под действием иолуэфира серной кислоты, либо при взаимодействии с катионом алкоксония, кинетически оба этих механизма 5//2-замещения неразличимы [c.882]
chem21.info
Типы простых эфиров и их реакции
Одной из характерных химических реакций моносахаридов является их взаимодействие с алкилирующими агентами, приводящее к образованию соединений типа простых эфиров. Особенно легко реагирует гликозидный гидроксил. При простом нагревании со спиртами в присутствии кислотных катализаторов образуются построенные по эфирному типу гликозиды. Роль спиртового компонента в этой реакции может взять на себя и вторая молекула моносахарида. В результате такой реакции из двух молекул моносахарида с потерей воды образуется молекула дисахарида [c.299]
ТИПЫ ПРОСТЫХ ЭФИРОВ И ИХ РЕАКЦИИ [c.367]
Литийорганические соединения выгодно отличаются от реактивов Гриньяра, часто используемых в синтезе, так же как и от других металлорганических соединений. Они, как правило, более реакционноспособны, и вследствие этого конечные продукты получаются с высокими выходами. Выделелять продукты проще, так как большинство литиевых солей хорошо растворимо в воде. Они менее, чем магнийорганические реактивы, склонны к реакциям восстановления и сопряженного присоединения. Немаловажным фактором является также то, что при синтезе литийорганических соединений меньше трудностей возникает с выбором растворителей. Обладая не очень сильно поляризованными связями, эти соединения хорошо растворяются как в слабополярых (типа простых эфиров), так и в неполярных (типа углеводородов) растворителях, чем выгодно отличаются от более реакционноспособных натрий-органических соединений, которые вследствие солеобразного строения не растворяются в указанных растворителях, и от магнийорганических соединений, которые требуют более полярных растворителей. Возможность применения углеводородных растворителей особенно ценна для промышленной наработки литийорганических соединений (многие из них благодаря этому вполне доступны) и для использования их в синтезе практически важных соединений, в частности лекарственных препаратов. [c.220]
Проведены исследования реологических свойств растворов простых эфиров целлюлозы [63, П8, 207, 223]. Реологические, пленкообразующие и адгезионные свойства имеют важное значение для практического применения простых эфиров целлюлозы. Простые эфиры используют в качестве эмульгаторов, диспергаторов, ста билизаторов в косметической, фармацевтической, пищевой, химической промышленности, в производстве пластмасс, в качестве материалов при изготовлении бумаги и текстильных изделий, в производстве цемента и бетона, в качестве загустителей типографских красок и лаков, для изготовления клеев, в частности для обоев и клеевых красок, в качестве защитных покрытий и пленок [8, 9]. Другие типы простых эфиров, которые хорошо набухают, но не растворяются в воде, применяют при получении гигиенических бумаги и тканей и для добавки к почвам. Эти продукты получают с помощью реакций сшивания цепей при обработке формальдегидом, гидроксиметилкарбамидом, эпихлоргидрином, хелатами металлов и т. д. [96, П5, 229]. [c.395]
Типы простых эфиров и их реакции [c.443]
ТИПЫ ПРОСТЫХ ЭФИРОВ и их РЕАКЦИИ [c.367]
Использование реакции нуклеофильного замещения дало возможность получить новые типы простых эфиров целлюлозы, синтез которых другим методом невозможен. Так, неоднократно предпринимавшиеся попытки синтеза фениловых эфиров целлюлозы удалось успешно осуществить Роговину и Владимировой . Реакция протекает по схеме [c.36]
Реакции спиртовых гидроксилов. Являясь многоатомными спиртами, моносахариды растворяют голубой осадок гидрата окиси меди с красивым синим окрашиванием. Эта реакция аналогична растворению гидрата окиси меди в гликоле и глицерине. Атомы водорода спиртовых групп моносахаридов можно заместить радикалами при этом получаются соединения типа простых эфиров. [c.214]
Оксониевый ион может атаковаться сильными нуклеофилами. Реакция такого типа протекает при нагревании алифатических простых эфиров с иодоводородной кислотой [c.660]
Однако в присутствии избытка оксисоединения реакция протекает далее. В образовавшемся полуацетале гидроксильная группа отличается от спиртовых гидроксилов значительно большей реакционной способностью и поэтому легко вступает в реакцию со второй молекулой спирта, образуя соединение, построенное по типу простых эфиров, называемое ацеталем [c.241]
По типу реакций первого порядка протекают превращения юдних изомеров в другие, например энольной формы ацето-уксусного эфира в кетонную, реакции разложения простых эфиров, реакция радиоактивного распада, реакция распада молекулы йода на атомы и др. [c.203]
Для синтейа простых эфиров методом О-алкилирования целлюлозы могут быть применены алкилсульфаты, алкилгалогениды, эфиры ароматических сульфокислот, реагенты, содержащие в молекуле трех- или четырехчленные напряженные гетероциклы (эпоксисоединения, этиленимин и его производные, этиленсуль-фид, р-пропиолактон и др.), непредельные соединения (акрило-нитрил, акриламид), ониевые соединения. Наиболее широко используются для О-алкилированця алкилгалогениды и алкилсульфаты. Остальные методы синтеза простых эфиров либо представляют чисто научный интерес, либо имеют практическое значение для синтеза таких типов простых эфиров целлюлозы, которые не могут быть получены действием алкилгалогенидов- или алкилсуль-. фатов. Характерной особенностью почти всех методов О-алкилирования целлюлозы, в отличие от способов ее этерификации, является протекание побочных реакций, приводящих к заметному увеличению удельного расхода реагентов. Как правило, расход реагентов на побочные реакции в 3—4 раза превышает расход на оснорцую реакцию О-алкилирования, [c.370]
Реакции нуклеофильного замещения широко применяются в органической химии низкомолекулярных соединений и, в частности, в химии сахаров для синтеза большого числа разнообразных производных. По механизму нуклеофильного замещения протекают, в частности, все реакции О-алкилирования целлюлозы, т- е. получение различных типов простых эфиров целлюлозы. При этом роль нуклеофильного реагента, атакующего различные 0-алкили-рующие реагенты, играют ионизированные гидроксильные группы целлюлозы. Однако синтез производных целлюлозы по реакции нуклеофильного замещения может быть осуществлен и по принципиально иной схеме — взаимодействием различных низкомолекулярных нуклеофильных реагентов с цёллюлозой (редко) или с некоторыми сложными эфирами целлюлозы. Таким путем можно синтезировать новые классы производных целлюлозы, получение которых другими известными методами до настоящего времени не представлялось возможным. [c.430]
Метод введения новых функциональных групп в молекулу целлюлрзы по реакции электрофильного замещения может применяться только для производных целлюлозы, содержащих двойную связь или ароматические ядра, в частности для некоторых типов простых эфиров целлюлозы (бензилцеллюлоза , эфир целлюлозы и 4-Р-оксиэтилсульфониланилина ), а также для эфиров целлюлозы и фурандикарбоновой кислоты . Так, например, реакция меркурирования бензилцеллюлозы протекает по схеме [c.39]
Благодаря легкости протекания реакцией с HJ часто пользуются для количественного определения некоторых групп, например — СНз и — С2Н5, связанных по типу простых эфиров, т. е. для определения так называемых метоксильных групп —О — СНз и этоксильных групп —О — С2Н5. [c.125]
Авторы сохранили общий строй книги, но для облегчения пользования материалом отказались от разделения процессов на реакции, проходящие в присутствии и в отсутствие щелочи, воспользовавщись классификацией по типам реакций. Введены отдельные разделы по хиральным и полимерносвязанным катализаторам, которые отсутствовали в первом издании, а также новые разделы относительно нуклеофильного ароматического замещения и реакций металлоорганических соединений в условиях межфазного катализа. Основную часть книги занимает гл. 3, посвященная практическому использованию межфазного катализа, где достаточно подробно освещены вопросы техники проведения межфазных реакций, а затем последовательно обсуждено применение межфазного катализа в реакциях замещения (синтез галогенидов, включая фториды, синтезы нитрилов, сложных эфиров, тиолов и сульфидов, простых эфиров, Ы- и С-алкилирование, в том числе амбидентных ионов), изомеризации и дейтерообмена, присоединения к кратным С—С-связям, включая неактивированные, присоединения к С = 0-связям, р-элиминирования, гидролиза, генерирования и превращения фосфониевых и сульфониевых илидов, в нуклеофильном ароматическом замещении, в различных реакциях (ион-радикальных, радикальных, электрохимических и др.), в металлоорганической химии, при а-элиминировании (генерировании и присоединении дигалокарбенов и тригалометилид-ных анионов), окислении и восстановлении. В каждом разделе приведены конкретные методики проведения реакций в различных условиях межфазного катализа и таблицы примеров синтеза разнообразных классов соединений. В монографии использовано более 2000 литературных источников. [c.6]
Реакции оптически активных сульфонатов. В 1923 г. было сделано наблюдение [212 а], что при алкилировании посредством оптически активных эфиров п-толуолсульфокислоты обычно имеет место вальденовская перегруппировка. Реакции этого типа впоследствии подробно исследовались, так как вопрос о том, в какой из двух реакций происходит перегруппировка, в данном случае легко разрешим, тогда как в классических примерах перегруппировки это не так легко сделать. Эфир -бензилметилкарбинола с п-толуолсульфокислотой реагирует с ацетатом калия в спиртовом растворе с образованием /-уксусного эфира этого спирта, а с алкоголятом натрия — с образованием простого -эфира [c.371]
Поставщик этого специфического катализатора не известен, тем не менее мы сочли целесообразньпу рассмотреть реакцию указанного типа, так как она представляет собой метод получения ряда простых эфиров (как, например, динеопен-тилового). При проведении процесса с другими катализаторами дегидратации получить такие эфиры не удается, [c.61]
ЭПХГ обладает высокой химической активностью, при его гидролизе идут побочные реакции. Например, ЭПХГ может легко полимеризоваться, чему способствуют повышение температуры и контакт с некоторыми металлами, особенно с железом. В зависимости от применяемого катализатора получаются подвижные жидкости, высоковязкие масла или смолообразные продукты. Поэтому аппаратуру и трубопроводы для ЭПХГ рекомендуют делать из хромоникелевых сталей [167, 168]. Описан ионный механизм полимеризации эпоксидной группы под действием кислотных или щелочных катализаторов с образованием соединений типа полимерных простых эфиров [169]. В случае присутствия кислотного катализатора реакция протекает следующим образом [c.41]
Диазоалканы можно превратить в простые эфиры н результате термического или фотохимического расщепления в присутствии спирта. Это реакции карбенового и карбеноидного типа [498]. Аналогичные интермедиаты образуются и в реакции диазоалка-нов со спиртами в присутствии трет-BuO l, приводящей к аце-талям [499]. [c.122]
Арилирование соединений типа 2СНг2 аналогично реакции 10-96, рассмотренной в т. 2, где дано определение группы 2. Активированные арилгалогениды, как правило, дают хорошие результаты [130]. В присутствии избытка амида натрия в реакцию можно вводить даже неактивированные арилгалогениды [131]. Подобным образом можно арилировать также простые кетоны [132] и сложные эфиры. Реакция с неактивированными галогенидами происходит ио ариновому механизму и представляет собой метод расширения синтезов на основе малонового эфира (или сходных соединений) с использованием ароматических молекул. Основание здесь выполняет две функции оно отрывает протон от молекулы 2СН22 и катализирует реакцию с образованием дегидробензола. Реакция была использована для осуществления процесса замыкания цикла [133] [c.29]
С субстратами, более подверженными атаке нуклеофилов, например полигалогеноолефинами и олефинами типа С = С—Z, лучше проводить реакцию в щелочном растворе, где атакующей частицей является R0- [147]. Реакции с субстратами типа С = С—Z относятся к реакциям присоединения по Михаэлю, и группа 0R всегда присоединяется к атому углерода, более удаленному от группы Z. Поскольку тройные связи более чувствительны к нуклеофильной атаке, чем двойные, то можно ожидать, что основания будут катализировать реакции присоединения к тройным связям особенно эффективно. Так оно и есть на самом деле, и эта реакция применяется для синтеза простых эфиров енолов и ацеталей [148] [c.167]
Олефины, содержащие элетроноакцепторные группы, могут давать циклобутаны по реакции с олефинами, содержащими электронодонорные группы. Примером этого могут служить упоминавщиеся выще реакции енаминов, но в реакцию введены также тетрацианоэтилен и другие подобные молекулы, которые дают замещенные циклобутаны при обработке олефинами типа С = С—А, где A = 0R, SR (простые эфиры енолов или тиоенолов) [703], циклопропильная [704] и некоторые арильные группы [705]. [c.254]
Диапазон условий, в которых устойчивы защрпы спиртовых гидроксилов, охватывает практически всю область, в которой могут проводиться основные реакции, применямые в органическом синтезе (кроме суперкислых сред). В целом для простых эфиров, aцeтaJ eй и кеталей характерна высокая устойчивость по отношению к основаниям и нуклеофилам, а также к окислителям и восстановителям для сложных эфиров — к электрофилам и окислителям и в довольно широком диапазоне к кислотам для силиловых эфиров — к окислителям и восстановителям и электрофилам некоторых типов. Поэтому для обеспечения сохранности спиртовой группы в условиях практически любой реакции, протекающей с участием др -тих имеющихся функций, всегда можно подобрать какую-либо защиту из имеющегося богатого набора вариантов. [c.187]
По той же причине наблюдаются различия в величинах удерживания для определенного спирта при применении диоктилсебацината, динонилфта-лата, дибутилфталата и трикрезилфосфата. Неподвижные фазы типа сложных эфиров обладают средней растворяющей способностью по отношению к алканам, простым и сложным эфирам, кетонам, меркаптанам и тиоэфирам. Благодаря их электроне акцепторным свойствам наблюдается также сильное взаимодействие с донорами электронов, например с олефинами, ароматическими углеводородами и гетероциклическими соединениями, но селективность отделения алкенов от алканов незначительна она немного возрастает в последовательности диоктилсебацинат — динонилфталат — дибутилфталат — трикрезилфосфат (см. табл. 1). Вообще можно установить, что селективность не особенно сильно выражена и для других гомологических рядов вследствие одновременного присутствия арильных и алкильных групп (которые обусловливают растворяющую способность по отношению к углеводородам) и карбоксильных или фосфатных групп (которые способствуют растворению кислородных соединений). Исключение составляет лишь разделение галогенопроизводных углеводородов, протекающее, впрочем, в случае сложных эфиров не хуже, чем на многих других неподвижных фазах, например нитрил-силиконовых маслах (Ротцше, 1963). При температурах выше 120° при исследовании спиртов и аминов следует быть осторожным вследствие возможности химических реакций с неподвижной фазой. [c.202]
chem21.info
Реакции образования простых и сложных эфиров целлюлозы
Реакция образования простых эфиров целлюлозы необратима. Если степень этерификации сложных эфиров можно регулировать изменением состава этерифицирующей омеси (для нитрата целлюлозы) или последующим омылением продукта реакции (ацетат и ацетобутират целлюлозы), то для простых эфиров целлюлозы эти методы регулирования степени замещения не могут быть использованы. Поэтому степень замещения определяется главным образом соотношением алкилирующего агента и целлюлозы, а также степенью активирования целлюлозы набуханием. Следует иметь в виду, что при получении эфиров целлюлозы особенно велика доля побочных реакций, на которые расходуется алкилирую-щий агент. К таким реакциям преимущественно относится омыление алкилгалогенидов, приводящее к образованию соответствующих спиртов и эфиров [c.416]
Эфиры целлюлозы являются производными наиболее широко распространенного природного стереорегулярного полимера — целлюлозы. Каждое элементарное звено макромолекулы целлюлозы содержит три гидроксильные группы, которые могут вступать в реакции этерификации и алкилирования с образованием простых и сложных эфиров целлюлозы. [c.196]
Реакции этерификации и 0-алкилирования, приводящие к образованию сложных и простых эфиров целлюлозы, широко используются для получения пленкообразующих производных целлюлозы. К их числу относятся нитрат, ацетат и ацетобутират целлюлозы, а также этил- и бензилцеллюлоза. [c.411]
Продукты замещения образуются благодаря химической реакции между гидроксильными группами целлюлозы и реагентами, которые связываются с кислородом гидроксильных групп. Водород гидроксильных групп макромолекул целлюлозы замещается ацильными или алкильными группами с образованием сложных и простых эфиров целлюлозы или смешанных сложно-простых эфиров. [c.326]
В зависимости от особенностей строения низкомолекулярного сложного эфира алкоголиз его целлюлозой мол ет привести к образованию либо сложного, либо простого эфира целлюлозы. Проведенные исследования закономерностей реакции алкоголиза целлюлозой сложных эфиров алифатических и ароматических карбоновых кислот позволили сформулировать представления о взаимосвязи между строе-ние.м и реакционной способностью низкомолекулярных эфиров в этой реакции и направлением реакции [19—21]. Согласно полученным данным [21] [c.18]
Основные химические реакции, происходящие при образовании сложных и простых эфиров целлюлозы, и их свойства уже подробно описывались в этой главе, особенно в тех ее разделах, где говорилось о механизме образования производных целлюлозы и о соотношении между молекулярным составом и свойствами продуктов. Здесь мы только вкратце коснемся технологии приготовления некоторых сложных и простых эфиров, имеющих наиболее важное значение. [c.294]
Спиртовые группы каждо го глюкозного остатка целлюлозы могут замещаться функциональными группами с образованием сложных и простых эфиров и т. п. При рассмотрении этих реакций должны учитываться следующие факторы [c.112]
Химич. свойства М. связаны с природой функциональных групп, входящих в состав М. Специфическими химич. реакциями М. являются 1) деструкция полимеров, приводящая к разрыву цепей и снижению мол. веса 2) структурирование (см. Вулканизация), т. е. возникновение химич. связей между различными М., приводящее к возрастанию мол. веса и в пределе к образованию сплошной сетчатой структуры (см. Структурирование полимеров пространственное), 3) реакции присоединения и отщепления пизкомолекулярных веществ без изменения степени полимеризации, приводящие к образованию поли-мераналогов (напр., этерификация целлюлозы с получением простых и сложных эфиров целлюлозы, омыление поливипилацетата с получением поливинилового спирта, внутримолекулярное отщепление воды от полиакриловой кислоты с получением полиангидрида и т. п.). [c.518]
Сообщается , что полимеризация винилхлорида в латексе натурального или синтетического каучука под действием УФ- и видимого света приводит к образованию эластомера, в котором содержание привитого сополимера превышает 50%. Введение фотосенсибилизатора позволяет ускорить реакцию. Синтез привитых сополимеров ряда мономеров (в том числе и винилхлорида) с неполными простыми и сложными эфирами целлюлозы, поливиниловым спиртом и другими полимерами под дегствием УФ-света предложено проводить в присутствии хлорноватистой и бромноватистой кислот или их солей, а также соединений олова Сообщается , что при облу- [c.403]
Эфиры целлюлозы являются производнымв природного стереорегулярного полимера — целлюлозы. Каждое элементарное звено макромолекулы целлюлозы содержит три гидроксильные группы, которые могут вступать в реакции этери-фикацив в алкилирования с образованием простых и сложных эфиров целлюлозы. Сложные и простые эфиры целлюлозы используют для получения пластмасс (этролов, целлулоида), пленок и лаков. [c.390]
Алкоголиз целлюлозой эфиров слабых карбоновых кислот протекает с расщеплением только ацил-кисло-родной связи и образованием сложного эфира целлюлозы. С повышением константы диссоциации кислоты С. 3. получаемого сложного эфира целлюлозы увеличивается и достигает максимума при рКа кислоты 2—2,5. При этом рКд частично изменяется направление атаки ОН-группы, а дальнейшее увеличение константы диссоциации кислоты вызывает резкое изменение направления реакции в сторону образования простых эфиров. Так, метилперфторбутират (константа диссоциации перфтормасляной кислоты 6,8-10" ) подвергается алкоголизу целлюлозой с расщеплением практически только алкил-кислородной связи с образованием простого эфира целлюлозы. Определенное влияние на реакционную способность низкомолекулярных сложных эфиров в реакции переэтерификации [c.19]
Скорость метилирования целлюлозы, так же как и скорость реакции образования других простых и сложных эфиров целлюлозы, в значительной степени зависит от условий предварительной обработки целлюлозного материала. При применени-и в качестве исходного материала не целлюлозы, а ее производных, у которых число водородных связей между макромолекулами невелико, скорость реакции значительно повышается. [c.472]
Взаимодействие целлюлозы с Р-пропиолактоном может протекать по двум направлениям. В одном случае образуется простой эфир целлюлозы, содержащий свободную карбоксильную группу, во втором — сложный эфир целлюлозы, содержащий свободную гидроксильную группу. Обычно имеют место обе реакции [82], но было установлено, что преимущественно образуется сложный эфир целлюлозы [144]. В обоих случаях реакция может протекать и более глубоко с образованием привитого гетероцепного сополимера. Реакцию проводят в горячем органическом растворителе (кипящем ксилоле), а при использовании щелочной целлюлозы — в воде [82]. Карбоксиэтилцеллюлоза с низкой степенью замещения получается при щелочном омылении сложноэфирной связи в этом продукте. [c.307]
Большое практическое применение имеют реакции функциональных групп с получением новых искусственных полимеров — различных сложных и простых эфиров целлюлозы. При образовании сложных и простых эфиров происходит замещение водорода в гидроксилах целлюлозы на другие группы, например — N02, —СООНз, —С2Н5. Процессы получения сложных и простых эфиров целлюлозы представляют основные направления ее химической переработки. [c.121]
Большинство процессов химической переработки целлюлозы основывается на реакциях гидроксильных групп целлюлозных макромолекул. Получающиеся производные целлюлозы могут быть разделены на три основных класса молекулярные соединения, продукты замещения и продукты окисления. Молекулярные соединения являются нестабильными продуктами, образованными за счет водородных связей между гидроксилами целлюлозы и некоторыми сильно полярными реагентами. Продукты замещения образуются путем химической реакции между гидроксилами целлюлозы и реагентами, которые связываются с кислородом гидроксила ковалентной связью. К ним относятся сложные и простые эфиры целлюлозы. Эти продукты имеют наибольшее техническое значение. Продукты окисления целлюлозы обычно деструктированы. Они долгое время не имели широкого практического применения. В настоящее время в промышленных масштабах уже производится целлюлоза, окисленная двуокисью азота. Этот продукт применяется в медицине, в первую очередь, как хорошее кровоостанавливающее средство, а также в текстильной и других отраслях промышлен- ности. Окисленные целлюлозы, кроме того, представляют интерес как волокнистые ионообменники. Ведутся интенсивные исследования с целью введения в целлюлозные макромолекулы новых реакционноспособных функциональных групп, использования их для химических превращений, описанных в классической органической химии, синтеза привитых сополимеров целлюлозы и так называемых сендвич-полимеров целлюлозы с другими полимерными веществами. Исследования в области модификации целлюлозы в ближайшие годы безусловно приведут к широкому использованию препаратов модифицированной целлюлозы в различных отраслях народного хозяйства. [c.322]
Впервые реакция переэтерификации была использована для получения бората целлюлозы [10]. При алкоголизе целлюлозной метил- и н-пропнлборатов был получен борат целлюлозы со степенью замещения 2,88, легко гидролизовавшийся водой. Позднее были проведены систематические исследования синтеза фосфорсодержащих эфиров целлюлозы алко-голизом целлюлозой эфиров кислот трехвалентного фосфора. При переэтерификации были использованы моно- [И], ди- [12] и триметилфосфиты [13], а также эфиры фосфонистой кислоты [14]. Проведенные исследования показали, что степень замещения эфира целлюлозы в этих реакциях может быть повышена при проведении их в среде апротонного растворителя (диметилформамида), а снижение температуры реакции может быть достигнуто при использовании вместо диметилфосфитов фенил-Р-хлорэтил- или Р-фторэтилфосфитов [15, 16]. Значительный интерес представляет реакция алкоголиза ОН-группами целлюлозы эфиров арил- и нафталинсульфокислот, приводящая к образованию не сложных, как в рассмотренных выше случаях, а простых эфиров целлюлозы [17, 18]. Как известно, алкоголиз целлюлозой сложных эфиров серной кислоты (диметилсульфата) лежит в основе одного из широко распространенных методов получения метилцеллюлозы. [c.18]
При действии на эфиры целлюлозы низкомолекулярных нуклеофильных реагентов реакции нуклеофильного за.мещения могут протекать как по межмо-лекулярному механизму с образованием дезоксипро-изводных целлюлозы, простых или сложных ее эфиров, так и по внутримолекулярному механизму. В этом случае действие низкомолекулярного нуклеофильного реагента в полярном растворителе приводит к ионизации ОН-групп элементарного звена с последующей атакой этими группами углеродных [c.24]
Реакции гидроксил I. ттых групп целлюлозы. Целлюлоза является полиатомным спиртом и содержит в каждом остатке глюкозы 3 спиртовых гидроксила. Благодаря этому она может давать ряд реакций, характерных для спиртов, а именно реакции замещения, приводящие к образованию простых и сложных эфиров, ацеталей, алко-голятов и т. п., и реакции окисления, приводящие к образованию альдегидных, кетонных и карбоксильных групп. Общей особенностью этих реакций целлюлозы является то обстоятельство, что в огромной молекуле целлюлозы, имеющей несколько тысяч гидроксильных групп, во всех этих реакциях обычно участвует лишь какая-то часть их. Йоэтому легче всего образуются продукты, соответствующие замещению одной или двух гидроксильных групп, и очень больших усилий требует замещение всех гидроксильных грунн. Нередко это вообще не удается. Причина этих трудностей заключается в том, что для получения полностью замещенного продукта необходимо обеспечить 100%-ный выход в данной реакции, что, как известно, возможно не всегда ввиду наличия побочных реакций, изменяющих природу реакционных групп. Иногда причина зах лючается в различной реакционной способности первичных и вторичных гидроксилов целлюлозы. Достаточно достоверным примером такого рода являются реакции тритилирования и тозилирования. Трифенилхлорметап и п-толуолсульфохлорид оказались веществами, способными реагировать лишь с первичными гидроксильными группами, оставляя свободными [c.443]
Во внутримицеллярной химической реакции цепи затрагиваются при образовании простых и сложных эфиров, например нри образовании ацетилцеллюлозы и нитроцеллюлозы (азотнокислый эфир целлюлозы). Эти реакции происходят так же, как на малых молекулах, и показывают, что функциональные группы в длинных цепях могут быть обнаружены точно так же, как и в малых молекулах. Производные целлюлозы сохраняют ВОЛОКНИСТУЮ структуру и поэтому дают все виды реакций, обусловленные мицеллярной структурой, подобно самой целлюлозе. Их растворимость в подходящих органических растворителях, могущих образовать коллоидный раствор, больше, чем растворимость целлюлозы, так как на месте гидроксилов, между которыми может установиться относительно прочный водородный мостик, находятся теперь эфирные группы, развивающие лишь слабые вандерваальсовы силы. Путем омыления из эфиров может быть получена в результате внутримицеллярной реакции целлюлоза (в случае нитроцеллюлозы после предварительного восстановления N3148). Полученная обратно целлюлоза отличается от природной несколько измененным расстоянием цепей, которые несколько деструктированы [223, IV, стр. 446]. Если исходить из целлюлозы, уже подвергшейся деструкции, то, соблюдая определенные условия опыта, можно добиться того, что в процессе этерифи-кации не будет происходить дальнейшая деструкция в этом случае происходит полимероаналогичное превращение. Дальнейшее об этом см. на стр. 311. [c.310]
Другие превращения полисахаридов. Интересные производные целлюлозы представляют собой эфиры толуолсульфокислоты (то-зилаты), которые могут служить исходным продуктом для многочисленных 2-реакций с образованием сложных и простых эфиров дезоксицеллюлозы. Некоторые подобные реакции приведены ниже [c.66]
chem21.info
Образование - простой эфир - Большая Энциклопедия Нефти и Газа, статья, страница 2
Образование - простой эфир
Cтраница 2
Помимо образования простых эфиров, фенолы и феноляты способны выступать в качестве пуклеофилов во многих других реакциях. [16]
Кроме образования простых эфиров, которого приходится опасаться как побочной реакции, сильные основания часто приводят к элиминированию галогеноводородов, в результате чего образуются олефины или ацетилены ( см. гл. [17]
Кроме образования простых эфиров, которого приходится опасаться как побочной реакции, сильные основания часто приводят к элиминированию галогеноводородов, в результате чего образуются олефины или ацетилены ( разд. [18]
Кроме образования простых эфиров, которого приходится опасаться как побочной реакции, сильные основания часто приводят к элиминированию галогеноводородов, в результате чего образуются олефины или ацетилены ( см. гл. [19]
Невозможность образования простого эфира в результате взаимодействия триметилкарбинола с другим спиртом ( R OH) в условиях реакции показана специальными опытами. [20]
Невозможность образования простого эфира в результате взаимодействия три-метилкарбинола с другим спиртом ( R OH) в условиях реакции показана специальными опытами. [21]
Реакция образования простых эфиров также обратима, и в общем очень инертные простые эфиры можно расщепить в присутствии лишь сильных кислот. [22]
Реакции образования простых эфиров используют в химии моносахаридов для изучения строения и для защиты определенных гидро-ксильных групп, причем для тех и других целей обычно используют различные простые эфиры. [23]
Реакция образования простых эфиров также обратима, и обычно очень ияертяые простые эфвры можно расщепить в присутствии лишь сильных кислот. [24]
Реакция образования простых эфиров [ уравнение ( XI-40) ] катализируется кислотами или ангидридами. Тесты на отвержденные смолы, выпускаемые промышленностью [54], показывают, что простые моноэфирные и ангидридные группы присутствуют в этих продуктах в небольших количествах, тогда как содержание оксигрупп, простых и сложных эфирных групп, образующихся в процессе сшивания, значительно. [25]
Реакция образования простых эфиров фенолов особенно легко протекает со средними эфнрами серной кислоты, например с диметил-сульфатом. [26]
Реакция образования простых эфиров целлюлозы необратима. В отличие от сложных эфиров, степень этерификации которых можно регулировать изменением состава этерифицирующей смеси ( при нитровании целлюлозы) или последующим омылением продукта реакции ( при получении ацетатов или ксантогенатов), для простых эфиров целлюлозы эти методы регулирования степени замещения не могут быть использованы. [28]
Реакция образования простых эфиров целлюлозы необратима. В отличие от сложных эфиров, степень этерификации которых можно регулировать изменением состава этерифицирующей смеси ( при нитровании целлюлозы) или последующим омылением продукта реакции ( при получении ацетатов или ксантогенатов), для простых эфиров целлюлозы эти методы регулирования степени замещения не могут быть использованы. [30]
Страницы: 1 2 3 4
www.ngpedia.ru