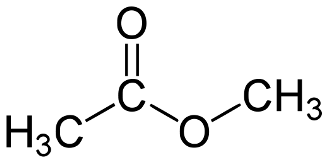
Химические свойства сложных эфиров. Образование сложных эфиров
Образование - сложный эфир - Большая Энциклопедия Нефти и Газа, статья, страница 1
Образование - сложный эфир
Cтраница 1
Образование сложных эфиров может служить реакцией на карбоксильную группу и для выделения к а р б о н о в ы х кислот. Сложные эфиры в общем очень прочны ( см. эту главу, В, I, 1), нерастворимы в воде, кислотах и щелочах и потому в большинстве случаев легко могут быть изолированы и получены в чистом состоянии. Они имеют большое препаративное значение как основные продукты для синтеза многих исходных веществ. [1]
Образование сложных эфиров ( фосфатов) - типичная реак-я в метаболизме углеводов. Например, все стадии гликолиза ревращения глюкозы в пируват) осуществляются с соединении только в фосфатной форме. [2]
Образование сложного эфира идет по схеме, аналогичной схеме получения солей из кнелот и оснований, ио при этом гидроксильная группа отщепляется от кислоты, а водород от спирта. Реакция получения сложного эфира обратима, так как конечный продукт, реагируя с водой, может вновь образовать исходные спирт и кислоту. [3]
Образование сложных эфиров и амидов в реакции ацилирования в значительной степени зависит от нуклеофильности спиртов и аминов. Последние во всех случаях проявляют большую реакционную способность, чем спирты. [4]
Образование сложного эфира у фенолов способствует потере активности, как и у соединений первого типа. [5]
Образование сложных эфиров является характерной реакцией для глицерина, как и вообще для всех спиртов. Сложные эфиры глицерина образуются как с органическими, так и с неорганическими кислотами, с ангидридами и хлорангидридами кислот. Они составляют основную часть всех природных жиров, и свойства их изложены в другом разделе курса. [6]
Образование сложного эфира из двух молекул альдегида является общей реакцией, свойственной многим альдегидам. [7]
Образование сложного эфира из кислоты и спирта каталитически ускоряется водородными ионами. [8]
Образование сложных эфиров у фенолов протекает не так легко, как у спиртов. [9]
Образование сложных эфиров происходит легче всего у первичных спиртов, труднее - у вторичных и очень трудно - у третичных. [10]
Образование сложных эфиров происходит легче всего у первичных спиртов, хуже - у вторичных и очень плохо - у третичных. [11]
Образование сложных эфиров, или ацилиро-вание, при действии кислЪт, их ангидридов или хлорангидридов является общей реакцией, свойственной как спиртам, так и фенолам. В аналитической химии большое значение имеет ацилирование органическими кислотами. Превращение в сложные эфиры, как правило, имеющие четкие температуры плавления и кипения, позволяет характеризовать и спирты, и фенолы. При действии щелочей или кислот сложные эфиры распадаются на составные части. Это расщепл & ние, или гидролиз, используется для количественного определения гидроксильной группы, так как количество выделенной кислоты, эквивалентное содержанию гидроксилъных-групяг-вестных условиях может быть точно определено. [12]
Образование сложных эфиров из галоидалкилов и солей органических кислот, например ацетата натрия или ацетата серебра [33] в ледяной уксусной кислоте ( в вышеприведенном уравнении вместо OR должно стоять тогда OCOR), в значительной мере подобно вышеприведенным реакциям образования простых эфиров или омыления в отношении стереохимического протекания. [13]
Образование сложных эфиров или ацилирование, протекающее под действием кислот, их ангидридов или хлорангидридов, является общей реакцией, свойственной как спиртам, так и фенолам. [14]
Образование сложных эфиров может быть затруднено как особенностями строения карбоновой кислоты ( пространственные трудности), так и побочными реакциями, например присоединением хлористого водорода по двойной связи, могущим иметь место в случае ненасыщенных кислот. [15]
Страницы: 1 2 3
www.ngpedia.ru
СЛОЖНЫЕ ЭФИРЫ | Энциклопедия Кругосвет
Содержание статьиСЛОЖНЫЕ ЭФИРЫ – класс соединений на основе минеральных (неорганических) или органических карбоновых кислот, у которых атом водорода в НО-группе замещен органической группой R. Прилагательное «сложные» в названии эфиров помогает отличить их от соединений, именуемых простыми эфирами.
Если исходная кислота многоосновная, то возможно образование либо полных эфиров – замещены все НО-группы, либо кислых эфиров – частичное замещение. Для одноосновных кислот возможны только полные эфиры (рис.1).

Рис. 1. ПРИМЕРЫ СЛОЖНЫХ ЭФИРОВ на основе неорганической и карбоновой кислоты
Номенклатура сложных эфиров.
Название создается следующим образом: вначале указывается группа R, присоединенная к кислоте, затем – название кислоты с суффиксом «ат» (как и в названиях неорганических солей: карбонат натрия, нитрат хрома). Примеры на рис. 2

Рис. 2. НАЗВАНИЯ СЛОЖНЫХ ЭФИРОВ. Фрагменты молекул и соответствующие им фрагменты названий выделены одинаковым цветом. Сложные эфиры обычно рассматривают как продукты реакции между кислотой и спиртом, например, бутилпропионат можно воспринимать как результат взаимодействия пропионовой кислоты и бутанола.
Если используют тривиальное (см. ТРИВИАЛЬНЫЕ НАЗВАНИЯ ВЕЩЕСТВ) название исходной кислоты, то в название соединения включают слово «эфир», например, С3Н7СООС5Н11 – амиловый эфир масляной кислоты.
Классификация и состав сложных эфиров.
Среди изученных и широко применяемых сложных эфиров большинство представляют соединения, полученные на основе карбоновых кислот. Сложные эфиры на основе минеральных (неорганических) кислот не столь разнообразны, т.к. класс минеральных кислот менее многочисленен, чем карбоновых (многообразие соединений – один из отличительных признаков органической химии).
Когда число атомов С в исходных карбоновой кислоте и спирте не превышает 6–8, соответствующие сложные эфиры представляют собой бесцветные маслянистые жидкости, чаще всего с фруктовым запахом. Они составляют группу фруктовых эфиров. Если в образовании сложного эфира участвует ароматический спирт (содержащий ароматическое ядро), то такие соединения обладают, как правило, не фруктовым, а цветочным запахом. Все соединения этой группы практически нерастворимы в воде, но легко растворимы в большинстве органических растворителей. Интересны эти соединения широким спектром приятных ароматов (табл. 1), некоторые из них вначале были выделены из растений, а позже синтезированы искусственно.
| Табл. 1. НЕКОТОРЫЕ СЛОЖНЫЕ ЭФИРЫ, обладающие фруктовым или цветочным ароматом (фрагменты исходных спиртов в формуле соединения и в названии выделены жирным шрифтом) | ||
| Формула сложного эфира | Название | Аромат |
| СН3СООС4Н9 | Бутилацетат | грушевый |
| С3Н7СООСН3 | Метиловый эфир масляной кислоты | яблочный |
| С3Н7СООС2Н5 | Этиловый эфир масляной кислоты | ананасовый |
| С4Н9СООС2Н5 | Этиловый эфир изовалериановой кислоты | малиновый |
| С4Н9СООС5Н11 | Изоамиловый эфир изовалериановой кислоты | банановый |
| СН3СООСН2С6Н5 | Бензилацетат | жасминовый |
| С6Н5СООСН2С6Н5 | Бензилбензоат | цветочный |
При увеличении размеров органических групп, входящих в состав сложных эфиров, до С15–30 соединения приобретают консистенцию пластичных, легко размягчающихся веществ. Эту группу называют восками, они, как правило, не обладают запахом. Пчелиный воск содержит смесь различных сложных эфиров, один из компонентов воска, который удалось выделить и определить его состав, представляет собой мирициловый эфир пальмитиновой кислоты С15Н31СООС31Н63. Китайский воск (продукт выделения кошенили – насекомых Восточной Азии) содержит цериловый эфир церотиновой кислоты С25Н51СООС26Н53. Кроме того, воски содержат и свободные карбоновые кислоты и спирты, включающие большие органические группы. Воски не смачиваются водой, растворимы в бензине, хлороформе, бензоле.
Третья группа – жиры. В отличие от предыдущих двух групп на основе одноатомных спиртов ROH, все жиры представляют собой сложные эфиры, образованные из трехатомного спирта глицерина НОСН2–СН(ОН)–СН2ОН. Карбоновые кислоты, входящие в состав жиров, как правило, имеют углеводородную цепь с 9–19 атомами углерода. Животные жиры (коровье масло, баранье, свиное сало) – пластичные легкоплавкие вещества. Растительные жиры (оливковое, хлопковое, подсолнечное масло) – вязкие жидкости. Животные жиры, в основном, состоят из смеси глицеридов стеариновой и пальмитиновой кислоты (рис. 3А,Б). Растительные масла содержат глицериды кислот с несколько меньшей длиной углеродной цепи: лауриновой С11Н23СООН и миристиновой С13Н27СООН. (как и стеариновая и пальмитиновая – это насыщенные кислоты). Такие масла могут долго храниться на воздухе, не меняя своей консистенции, и потому называются невысыхающими. В отличие от них, льняное масло содержит глицерид ненасыщенной линолевой кислоты (рис. 3В). При нанесении тонким слоем на поверхность такое масло под действием кислорода воздуха высыхает в ходе полимеризации по двойным связям, при этом образуется эластичная пленка, не растворимая в воде и органических растворителях. На основе льняного масла изготавливают натуральную олифу.

Рис. 3. ГЛИЦЕРИДЫ СТЕАРИНОВОЙ И ПАЛЬМИТИНОВОЙ КИСЛОТЫ (А И Б) – компоненты животного жира. Глицерид линолевой кислоты (В) – компонент льняного масла.
Сложные эфиры минеральных кислот (алкилсульфаты, алкилбораты, содержащие фрагменты низших спиртов С1–8) – маслянистые жидкости, эфиры высших спиртов (начиная с С9) – твердые соединения.
Химические свойства сложных эфиров.
Наиболее характерно для эфиров карбоновых кислот гидролитическое (под действием воды) расщепление сложноэфирной связи, в нейтральной среде оно протекает медленно и заметно ускоряется в присутствии кислот или оснований, т.к. ионы Н+ и НО– катализируют этот процесс (рис. 4А), причем гидроксильные ионы действуют более эффективно. Гидролиз в присутствии щелочей называют омылением. Если взять количество щелочи, достаточное для нейтрализации всей образующейся кислоты, то происходит полное омыление сложного эфира. Такой процесс проводят в промышленном масштабе, при этом получают глицерин и высшие карбоновые кислоты (С15–19) в виде солей щелочных металлов, представляющих собой мыло (рис. 4Б). Содержащиеся в растительных маслах фрагменты ненасыщенных кислот, как и любые ненасыщенные соединения, могут быть прогидрированы, водород присоединяется к двойным связям и образуются соединения, близкие к животным жирам (рис. 4В). Этим способом в промышленности получают твердые жиры на основе подсолнечного, соевого или кукурузного масла. Из продуктов гидрирования растительных масел, смешанных с природными животными жирами и различными пищевыми добавками, изготавливают маргарин.

Основной способ синтеза – взаимодействие карбоновой кислоты и спирта, катализируемое кислотой и сопровождаемое выделением воды. Эта реакция обратна показанной на рис. 3А. Чтобы процесс шел в нужном направлении (синтез сложного эфира), из реакционной смеси дистиллируют (отгоняют) воду. Специальными исследованиями с применением меченых атомов удалось установить, что в процессе синтеза атом О, входящий в состав образующейся воды, отрывается от кислоты (отмечено красной пунктирной рамкой), а не от спирта (нереализующийся вариант выделен синей пунктирной рамкой).
По такой же схеме получают сложные эфиры неорганических кислот, например, нитроглицерин (рис. 5Б). Вместо кислот можно использовать хлорангидриды кислот, метод применим как для карбоновых (рис. 5В), так и для неорганических кислот (рис. 5Г).
Взаимодействие солей карбоновых кислот с галоидалкилами RCl также приводит к сложным эфирам (рис. 5Г), реакция удобна тем, что она необратима – выделяющаяся неорганическая соль сразу удаляется из органической реакционной среды в виде осадка.

Применение сложных эфиров.
Этилформиат НСООС2Н5 и этилацетат Н3СООС2Н5 используются как растворители целлюлозных лаков (на основе нитроцеллюлозы и ацетилцеллюлозы).
Сложные эфиры на основе низших спиртов и кислот (табл. 1) используют в пищевой промышленности при создании фруктовых эссенций, а сложные эфиры на основе ароматических спиртов – в парфюмерной промышленности.
Из восков изготавливают политуры, смазки, пропиточные составы для бумаги (вощеная бумага) и кожи, они входят и в состав косметических кремов и лекарственных мазей.
Жиры вместе с углеводами и белками составляют набор необходимых для питания пищевых продуктов, они входят в состав всех растительных и животных клеток, кроме того, накапливаясь в организме, играют роль энергетического запаса. Из-за низкой теплопроводности жировой слой хорошо предохраняет животных (в особенности, морских – китов или моржей) от переохлаждения.
Животные и растительные жиры представляют собой сырье для получения высших карбоновых кислот, моющих средств и глицерина (рис. 4), используемого в косметической промышленности и как компонент различных смазок.
Нитроглицерин (рис. 4) – известный лекарственный препарат и взрывчатое вещество, основа динамита.
На основе растительных масел изготавливают олифы (рис. 3), составляющие основу масляных красок.
Эфиры серной кислоты (рис. 2) используют в органическом синтезе как алкилирующие (вводящие в соединение алкильную группу) реагенты, а эфиры фосфорной кислоты (рис. 5) – как инсектициды, а также добавки к смазочным маслам.
Михаил Левицкий
www.minilinx.com.krugosvet.ru
Образование - простой сложный эфир
Образование - простой сложный эфир
Cтраница 2
Следовательно, для крахмала возможны реакции, характерные для многоатомных спиртов, в частности, образование простых и сложных эфиров. Однако эфиры крахмала большого практического значения не имеют. [16]
Если подходить к процессам химического реагирования целлюлозы с позиций изменения ее надмолекулярной структуры, то почти любой процесс образования простых и сложных эфиров целлюлозы должен начинаться с рыхления структуры волокна, так как замещение гидроксильных групп на алкильные и арильные радикалы, обладающие большим объемом, должно привести к некоторому раздвиганию смежных участков цепевых молекул целлюлозы, а это должно вызвать разрыв или ослабление межмолекулярных водородных связей у далее стоящих гидроксильных групп. Водородная же связь в целлюлозе, по-видимому, в значительной степени определяет не только взаимное расположение молекулярных цепей в этом полимере, но и физико-химические свойства целлюлозы. [17]
Отличие фенолов от спиртов. Образование простых и сложных эфиров является общим как для фенолов, так и для спиртов. В отличие от спиртов, фенолы обладают довольно резко выраженными кислотными свойствами: образующиеся с едким натром феноляты не разлагаются водой, в отличие оталко-голятов ( стр. Кроме того, спирты при окислении образуют альдегиды или кетоны и далее переходят в кислоты. [18]
Отличие фенолов от спиртов. Образование простых и сложных эфиров является общим как для фенолов, так и для спиртов. В отличие от спиртов, фенолы обладают довольно резко выраженными кислотными свойствами: образующиеся с едким натром феноляты не разлагаются водой, в отличие от алко-голятов ( стр. Кроме того, спирты при окислении образуют альдегиды или кетоны и далее переходят в кислоты. [19]
Из-за смещения неподеленной электронной пары кислорода к л-элект-ронам бензольного кольца атомы углерода получают отрицательный заряд. Реакции образования простых и сложных эфиров для фенолов не характерны. [20]
Некоторые реакционноспособные вещества, например олефины и альдегиды, под действием фтористого водорода полимеризуются. При образовании простых и сложных эфиров фтористый водород выступает как дегидратирующий агент. Кроме того, он катализирует перегруппировки, изомеризацию и рацемизацию. Он способствует также замыканию циклов и катализирует реакции окисления. Все вышесказанное относится к уже опубликованным исследованиям. Не исключено, что в дальнейшем будут открыты также новые реакции, катализируемые фтористым водородом. [21]
Наличие этих гидроксилов можно доказать реакциями образования простых и сложных эфиров. Реакция получения некоторых сложных эфиров имеет огромное практическое значение. [22]
Естественно, что в связи с почти полной нерастворимостью клетчатки наличие свободных гидрок-силов нельзя доказать обычной и хорошо известной нам реакцией растворения гидрата окиси меди. Наличие этих гидроксилов можно доказать реакциями образования простых и сложных эфиров. Реакция получения некоторых сложных эфиров имеет огромное практическое значение. [23]
Химические свойства полисахаридов ГМЦ определяются строением их молекул. Сравнительно подробно изучены: поведение гидроксильных групп при взаимодействии с гидроксидами металлов при образовании простых и сложных эфиров, в ряде реакций замещения, поведение полуацетальных связей в процессе реакций гидролиза, аммонолиза, устойчивость а-гликольных группировок при селективном окислении, ендиольныи распад в присутствии гидроксидов металлов, пиролиз и др. Рассмотрим основные из перечисленных реакций. [24]
Эфиры целлюлозы являются производными наиболее широко распространенного природного стереорегулярного полимера - целлюлозы. Каждое элементарное звено макромолекулы целлюлозы содержит три гидроксильные группы, которые могут вступать в реакции этерификации и алкилирования с образованием простых и сложных эфиров целлюлозы. [25]
Эфиры целлюлозы являются производными природного стереорегулярного полимера - целлюлозы. Каждое элементарное звено макромолекулы целлюлозы содержит три гидроксильные группы, которые могут вступать в реакции этери-фикацин и алкилирования с образованием простых и сложных эфиров целлюлозы. Сложные и простые эфиры целлюлозы используют для получения пластмасс ( этролов, целлулоида), пленок и лаков. [26]
Благодаря наличию в молекулах моносахаридов нескольких гидроксильных групп моносахариды проявляют свойства многоатомных спиртов. Наибольшее значение имеют реакции образования простых и сложных эфиров. Они получаются в результате замещения водорода гидроксильных групп алкильными, ацильными или другими радикалами. [27]
Благодаря наличию в молекулах моносахаридов нескольких гидроксильных групп моносахариды проявляют свойства многоатомных спиртов. Наибольшее значение среди реакций, протекающих за счет гидрок-силов, имеют реакции образования простых и сложных эфиров. Эфиры получаются при взаимодействии моносахаридов со спиртами, кислотами или их производными в результате замещения водорода гидроксильных групп алкильными, ацильными или другими радикалами. [28]
Одним из наиболее надежных методов подхода к стереохимии природных соединений является получение циклических производных. Образование этих производных возможно лишь при наличии строго определенных стереохимических предпосылок, что позволяет делать совершенно определенные заключения о конфигурации молекулы. Этот метод используется настолько широко, что в данном обзоре может быть рассмотрена лишь небольшая часть примеров, относящихся к его применению в области стереохимии. Наиболее широко используются реакции образования циклических простых и сложных эфиров, лактонов, лактамов, ангидридов, циклических четвертичных солей и С-С - мостиков. Кроме того, существуют и другие разнообразные типы циклизации, которые имеют ограниченное значение. [29]
В некоторых реакциях реагентами служат также алифатические углеводороды. Изопа-рафины более реакционноспособны, но даже нормальные парафины с прямой цепью в известных условиях вступают в реакцию. Фтористый водород вызывает полимеризацию таких реакционно-способных соединений, как олефины и альдегиды. Он действует как водуотнимающее средство при образовании простых и сложных эфиров. Фтористый водород катализирует перегруппировки, изомеризацию и рацемизацию. Он способствует замыканию колец и катализирует окисление. Позже могут быть найдены и другие реакции; все вышеуказанные реакции описаны в литературе. [30]
Страницы: 1 2 3
www.ngpedia.ru
Образование сложных эфиров. Некоторые производные углеводов
УГЛЕВОДЫ
Оглавление
Введение
1. Образование сложных эфиров
2. Превращение в циклические ацетали и кетали
3. Удлинение цепи по Килиани-Фишеру
4. Укорочение цепи по Руфу
5. Аскорбиновая кислота
6. Целлофан и вискозный шелк
7. Нитрат целлюлозы
8. Азотсодержащие сахара
Введение
В живой природе широко распространены вещества, многим из которых соответствует формула Сх (Н2 О)у . Они представляют собой, таким образом, как бы гидраты углерода, что и обусловило их название – углеводы. К углеводам относится обычный сахар – сахароза, виноградный сахар – глюкоза, фруктовый сахар – фруктоза и молочный сахар – мальтоза. Этим объясняется еще одно их общепринятое название сахара. Растения синтезируют углеводы из двуокиси углерода и воды в процессе фотосинтеза. При этом солнечная энергия переходит в химическую:
хСО2 + уh3 О + солнечная энергия ¾® Сх (Н2 О)у + хО2
При окислении углеводов в организме энергия высвобождается и используется для жизнедеятельности:
Сх (Н2 О)у + хО2 ¾® хСО2 + уh3 О + энергия
1. Образование сложных эфиров
Углеводы реагируют с уксусным ангидридом в присутствии таких оснований, как пиридин или ацетат натрия с превращением всех гидроксильных групп, включая аномерный гидроксил в сложноэфирные. Если реакция проводится при охлаждении, то она проходит стереоспецифически; a-аномер дает a-ацетат, а b-аномер - b-ацетат:
D-глюкопираноза D-пентацетилглюкоза
D-тетраацетилбромгюкоза
При обработке пентаацетилглюкозы бромистым водородом в уксусной кислоте замещению подвергается ацетоксигруппа только при атоме С-1.
Действием на целлюлозу уксусным ангидридом в уксусной кислоте получают растворимый в ацетоне ацетат целлюлозы:
целлюлоза ацетат целлюлозы
Из ацетилцеллюлозы получают ацетатный шелк и безопасную в обращении кинофотопленку.
Упр. 24. Как получают ацетилцеллюлозу, и какое применение она находит?
Упр. 25. Как получают пентаацетат глюкозы? Подвергается ли он мутаротации?
14.

2. Превращение в циклические ацетали и кетали
При изучении альдегидов и кетонов мы видели, что, реагируя с диолами, они превращаются в циклические ацетали и кетали.

1,2-диол циклический кеталь
Углеводы образуют циклические ацетали и кетали лишь в том случае, когда вицинальные гидроксильные группы находятся в цис-положении по отношению друг к другу. Например, α-D-галактопираноза реагирует с ацетоном следующим образом:


a-D-галактопираноза ацетонид a-D-галактопиранозы
Ацетали ацетона называют ацетонидами.
3. Удлинение цепи по Килиани – Фишеру
Метод удлинения цепи углевода на один атом углерода основан на реакции альдегидов с синильной кислотой. Рассмотрим его на примере D-глицеринового альдегида:








альдоновые кислоты




g-альдонолактоны




D-эритроза D-треоза
Упр. 26. Какие пентозы могут быть получены по Килиани-Фишеру из D-эритрозы.
Упр. 27. Напишите формулы пентоз, котрые могут быть получены по Килиани-Фишеру из D-треозы. Их называют D-ксилоза и D-ликсоза. D-ксилоза окисляется азотной кислотой в оптически не активную альдаровую кислоту, а D-ликсоза – в оптически активную. Каково строение этих пентоз?
16. 17.
4. Укорочение цепи по Руфу
Укорочение цепи по Руфу включает две стадии: окисление альдозы бромной водой до альдоновой кислоты и окислительное декарбоксилирование альдоновой кислоты перекисью водорода и сульфатом железа до альдозы, например:

D-рибоза D-рибоновая к-та D-эритроза
Упр. 28. Напишите реакции укорочения цепи по Руфу D-галактозы и назовите образующуюся пентозу.
18.
5. Аскорбиновая кислота
Промышленный способ получения аскорбиновой кислоты основан на микробиологическом окислении сорбита в L-сорбозу. Защитив четыре гидроксильные группы L-сорбозы кетализацией ее окисляют перманганатом калия и после гидролиза продукта окисления получают 2-оксо-L-гулоновую кислоту. Последняя переводится в лактон, существующий в енольной форме и представляющий собой L-аскорбиновую кислоту. Раствор аскорбиновой кислоты обладает кислой реакцией (pKa = 4,17) и сильными восстановительными свойствами. Суточная потребность взрослого человека в витамине С составляет примерно 30 мг.

D-сорбит L-сорбоза




2-оксогулоновая к-та

аскорбиновая кислота
Упр. 29. Напишите реакции получения аскорбиновой кислоты исходя из глюкозы.
6. Целлофан и вискозный шелк
Многие важные продукты получают из целлюлозы путем ее растворения, а затем осаждением из раствора. Полученная таким образом регенерированная целлюлоза, отличается от исходной природной тем, что она менее кристаллична из-за процессов расщепления (деградации) проходящих при ее растворении и дальнейшем осаждении. Наиболее широко используемым методом регенерации является ксантатный или вискозный процесс.
Исходным сырьем для производства является древесная целлюлоза, содержащая 95-99% высокомолекулярной целлюлозы со степенью полимеризации 800-1100. Ее обрабатывают 20%-ным раствором NaOH (мерсеризация) в течение 10 мин при 50о С. Полученную таким образом щелочную целлюлозу отделяют от лигнина и оставляют на созревание, при котором молекулярный вес целлюлозы уменьшается. Далее щелочную целлюлозу обрабатывают СS2 и получают ксантат целлюлозы:

целлюлоза ксантат целлюлозы (вискоза)
Конечно не все гидроксильные группы целлюлозы прореагируют, но прореагурующего количества достаточно, для ее растворения в водной щелочи. Получаемый раствор называют вискозой. Ее продавливают через фильеры в раствор серной кислоты, где регенерируется целлюлоза:

целлофан или вискозное волокно
Если фильеры представляют собой узкие щели, то получают целлофан, а если тонкие отверстия – вискозное волокно.
Целлофан и вискозный шелк являются лишь измененной формой целлюлозы.
7. Нитрат целлюлозы
При обработке целлюлозы азотной кислотой образуется нитрат целлюлозы:

mirznanii.com
Образование сложных эфиров ароматических кислот
Б. Образование сложных эфиров ароматических кислот [c.205]Нагревание дизельного топлива (ДТ) при 120 С в течение 5 часов в присутствии металлической меди приводит к образованию смеси кислородсодержаш,их соединений. НК-спектр оксидата ДТ является спектром сложной смеси кислородсодержащих ароматических структур, о чем свидетельствуют полосы поглощения С=0-групп (1720 см ) и групп ОН (3400-3500 см 1030-1250 см ), а также полоса при 3380 см обусловленная валентными колебаниями фрагмента 0-Н ассоциированной гидропероксидной группы. Широкая полоса при 800-1450 см указывает также на значительное содержание в оксидате кислородсодержащих структур. В этой области проявляются валентные колебания С=0-группы сложных эфиров ароматических кислот (1300-1250 см 1150-1100 см ), фенолов [c.5]
Окись углерода с жирными или ароматическими спиртами реагирует с образованием сложных эфиров муравьиной кислоты реакция ускоряется в присутствии этилата натрия или муравьинокислого натрия и других катализаторов. Фенолы в этих условиях не реагируют лишь при температуре 130—160° и давлении около 30 ат фенолы в присутствии спирта реагируют по схеме [c.142]Ряд смешанных ангидридов из алифатических кислот разлагается с образованием сложных эфиров по пути А, а смешанные ангидриды ароматических кислот разлагаются по пути либо А, либо Б. При 250 °С происходит также реакция В [74]. Трифторуксусная кислота и фениловый эфир хлормуравьиной кислоты при смешивании образуют. фениловый эфир трифторуксусной кислоты с выходом 75—80% [75]. Рассмотренные реакции декарбоксилирования, по-видимому, протекают через промежуточное циклическое состояние, причем происходит сдвиг электронов в цикле. [c.292]
Предсказание азеотропии в jPj, было выполнено приблизительно для ста бинарных и нескольких десятков многокомпонентных смесей, образованных компонентами, которые относятся к различным классам химических соединений (парафины, олефины, диены, циклопарафины, ароматические соединения, спирты, альдегиды, кетоны, ацетали, простые и сложные эфиры, жирные кислоты, хлорпарафины, пиридины, нитрилы, вода). [c.67]
Окисление ароматических альдегидов пероксидами или перкислотами может приводить либо к карбоновым кислотам, либо к перегруппировке (окисление по Байеру — Виллигеру) с образованием сложного эфира фенола, который часто гидролизуется, [c.730]
Реакции образования и гидролиза сложного эфира карбоновой кислоты были рассмотрены ранее (см. опыты 93—95). Этерификация кислот ароматического ряда протекает с различной скоростью в зависимости от их строения, в частности от числа и положения заместителей в бензольном ядре. Наличие заместителей в орто-положении к карбоксильной группе обычно резко замедляет этерификацию (так называемые пространственные затруднения)-, поэтому салициловая кислота этерифицируется труднее, чем бензойная. [c.254]
По типу альдольного присоединения с альдегидами могут реагировать также карбоновые кислоты и их производные. Синтезом Перкина называют конденсацию ароматического альдегида с ангидридом или сложным эфиром алифатической кислоты. В качестве основных конденсирующих средств применяются щелочные соли карбоновых кислот или пиридин. Так, при нагревании бензойного альдегида с уксусным ангидридом и уксуснокислым натрием образуется коричная кислота. Роль метиленовой компоненты в этой реакции выполняет уксусный ангидрид. Продукт альдольного типа неустойчив и не может быть выделен. Отщепление воды приводит к образованию смешанного ангидрида коричной и уксусной кислот, который быстро гидролизуется при обработке водой [c.288]
Дикетен присоединяется к спиртам с образованием сложных эфиров ацетоуксусной кислоты, к ароматическим аминам — с образованием арил-амидов ацетоуксусной кислоты. Присоединение дикетена к ароматическим гидразинам приводит к получению метиларилпиразолонов. Эти соединения используют как промежуточные продукты в производстве красителей, пигментов и химико-фармацевтических препаратов. Все они получаются из дикетена, тогда как раньше приходилось для этого исходить из этилового эфира ацетоуксусной кислоты, который синтезировали из этилацетата по методу Кляйзена. [c.325]
Нагревание дизельного топлива (ДТ) при 120 С в течение 5 часов в присутствии металлической меди приводит к образованию смеси кислородсодержащих соединений, состоящих из гидропероксидов, фенолов, сложных эфиров, ароматических кислот, ароматических и арилароматических эфиров с преимущественным содержанием гидропероксидов, ароматических карбоновых кислот и смол. [c.18]
Способ получения ацетапей, по Фишеру, в жирно. ад ряду дает хорошие результаты, однако на вышеприведенном основании в случае некоторых аро.адатических альдегидов типа бензальдегида — оставляет желать лучшего. Только при введении в ядро сильно электроотрицательной группы образование ацеталей протекает гладко. Так, о-нитробензальдегид уже при комнатной температуре превращается в ацеталь на 70%, 2, 5-д и х л о р б е н з а л ь-л с г и д — на 83%, 2- н и т р о-З, 6-дихлорбензальдегид — на 70%. Затруднений с образованием ацеталей при орто-замещенных, как при образовании сложных эфиров ароматических карбоновых кислот, установить не удалось. [c.229]
Хотя химия бензоинов АгСН (ОН) СОАг изучается уже в течение нескольких десятилетий, только недавно бензоин и его простые эфиры приобрели промышленное значение. Они сейчас широко используются в качестве фотоинициаторов радикальной полимеризации. Симметричные и несимметричные бензоины легко получаются с помощью бензоиновой конденсации (см. разд. 5.3.8) симметричные бензоины можно синтезировать также из сложных эфиров ароматических кислот путем ацилоиновой конденсации [131] (см. гл. 9.8). Несимметричные бензоины изомеризуются в присутствии кислот и оснований в более устойчивый изомер (в котором карбонильная группа соседствует с ароматическим кольцом, содержащим более электронодонорный заместитель) эта реакция, вероятно, протекает через ендиол (101) [схема (59)]. Некоторые ендиолы, образующиеся при восстановлении бензилов, можно выделить [132] если присутствует 2,6-дизамещенное ароматическое кольцо, то кетонизация стерически затруднена, и ендиол (102) устойчив [132]. Гетероциклические бензоины часто существуют только в форме ендиолов, если возможна ее стабилизация в виде хелата за счет образования водородной связи, как в (103) [132]. В последнем случае известны только (Я)-изомеры, тогда как для сильно затрудненных ендиолов обычно присутствуют как (Е)-, так и (Z)-изомеры. Недавно показано, что дианион ендиола (101) можно генерировать из бензоина и гидроксида натрия в присутствии катализаторов межфазного переноса [133] и использовать в [c.812]
Карбоний ионный механизм. Под влиянием серной кислоты олефины подвергаются различным реакциям гидратации, образованию сложных эфиров, нолиморизации и конденсации с ароматическими углеводородами. Наиболее просто механизм различных реакций можно понять с точки зрения нродстаплений об образовании в качестве промежуточного продукта карбопнй-иопа [1381. Так, нанример, в разбавленных растворах кислот третичные олофины подвергаются гидратации в третичные спирты [78, 196, 204, 205 . С бо. гое концентрированными кислотами образуется сложный эфир сорной кислоты [170]. В разбавленных водных растворах кислот вода является главным нуклеофильным агентом, в то время как в 67%-ной серной кислоте концентрация свободной воды ничтожно мала и бисульфат-ион присутствует в очень большой концентрации (ЬХХУП) [c.435]
Ароматические карбоновые кислоты этерифицируются медленнее, чем алифатические, но реакции можно ускорить введением больших количеств катализатора. В отдельных случаях скорость образования сложных эфиров у ароматических кислот близка к нулю. Зависимость между скоростью реакции и строением кислот изучена достаточно хорошо. Было найдено, что введение заместителей в ароматические кислоты снижает скорость образования сложных эфиров. Наличие заместителя в орто-положении наиболее сильно тормозит реакцию при заместителях в мета- и пара-положении скорость несколько возрастает. На основании экспериментальных исследований было выведено следующее эмпирическое правило метиловые эфиры ароматических кислот не образуются, если в кольце, рядом с карбоксильными группами, стоят заместители Alk, Аг, С1, NO2. NHa, СООН и т. д. Это можно пояснить рядом примеров. Меллитовая кислота (I) совершенно не дает эфира, пиромелли-товая же (II) образует 90% эфира, так как в ней орто-положения свободны [c.468]
Анализ ИК-спек гров окисленных образцов ятелыюго топпива показал наличие сложной с.меси кислородсодержащих ароматических структур, состояитих из гидропероксидов, спиртов, фенолов, ароматических и арилароматическнх. эфиров (ароматических альдегидов и карбоновых кислот), сложных эфиров ароматических карбоновых кислот, которые легко. могут вступать в реакции уплотнения (этерификации, конденсации, полимеризации) с образованием высокомолекулярных соединений, часть которых коагулирует в нерастворимые соединения, вызывая осадко- и смолообразование [6]. [c.117]
Восстановление сложных эфиров титаноцендихлоридом отличается от реакций 10-82 (т. 2), 19-41 и 19-43. Продуктами являются алкан R h4 и спирт R OH [447]. Механизм, по-ви-димому, включает образование алкенового интермедиата. Ароматические кислоты восстанавливаются до метилбензолов при кипячении вначале с трихлоросиланом в ацетонитриле, затем [c.319]
Структура молекулы и температура плавления (между 100— 140 С) говорят об их растворимости в ароматических углеводородах и уайт-спирите [2, 3]. Для модификации канифоли часто исиользуют низкомолекулярные алкилфенольные смолы, которые активно взаимодействуют с маслами. Эти смолы способствуют пре-вращеиию кислот, содержащихся в канифоли, в полиэфир поли-карбоновой кислоты либо через образование хроманового кольца (см. разд. 3.3.5 и 17.1), либо, что более вероятно, через алкилиро-вание, чему благоприятствует кислотность среды и наличие карбоксильной груины. Фенольную смолу добавляют к раснлавленной канифоли ири ПО—140°С в этих условиях смола должна легко растворяться, потому что в противном случае может произойти самоконденсация резола. Затем температуру повьпнают примерно до 250 °С и добавляют в систему глицерин илн иентаэритрит с целью образования сложных эфиров и повышения молекулярной массы смолы. Прн температуре выше 250 °С начинается декар-боксилирование. В некоторых случаях реакцию проводят при относительно высоких температурах с участием новолаков. Кислоты канифоли могут предварительно взаимодействовать с формальдегидом (механизм реакции Принса, см. разд. 2.17), образуя соединения, содержащие гидроксильные группы в таких случаях интервал температур размягчения канифоли поднимается примерно с 45 до 105 °С. Прн температурах выше 125 °С в систему рекомендуют медленно добавлять ангидрид малеиновой кислоты (механизм реакцпи 1,4-присоедииения сопряженных диенов) [c.206]
Используют три основных способа получения фторсодержащих ПАВ. Детально эти процессы описаны в [147]. Один из них заключается в электрохимическом фторировании соответствующих алифатических соединений с требуемой функциональной группой. Он состоит из электрофторирования раствора углеводородного сырья фтористым водородом (реакция Д. Саймонса). Наилучшим образом этот процесс объясняется образованием фторрадикалов. Могут быть использованы лишь соединения, устойчивые в безводном НЕ, такие как алифатические углеводороды, дезактивированные ароматические соединения, простые эфиры, тиоэфиры, сложные эфиры, галоиды кислот, третичные амины и сульфонилгалоиды. Спирты, кетоны и карбоновые кислоты в таких условиях не применяются. [c.66]
Реакцш с диоксидом углерода (реакция Кольбе) Взаимодействие фенолята натрия с диоксидом углерода идет через промежуточное образование сложного эфира с последующей миграцией карбоксильной группы от кислорода в орто-положение ароматического ядра по аналогии с перегруппировкой Фриса Эта реакция лежит в основе промышленного способа получения салициловой кислоты — полупродукта при синтезе аспирина [c.514]
Ароматические кетоны. Окисление диарилкетонов надкксло-тами неизменно приводит к образованию сложных эфиров или продуктов их гидролиза. Хотя значение этой реакции в качества препаративного метода невелико, она дает возможность устанавливать строение полизамещенных бензофенонов и алкиларил-кетонов[48]. Указанный метод является менее жестким и в то жа время более специфичным, чем процессы расщепления, при которых используются сплавление со щелочью [49] или гидролиз кислотами [50], применявшиеся при исследовании природных веществ. [c.88]
Так как конденсация альдегидов с фенолами всегда происходит в орто-положении к фенольной ОН-группе, то при конденсации с глиоксалевой кислотой, возможно, происходит выделение воды за счет фено 1ьной ОН-группы и СООН-группы глиоксалевой кислоты с образованием сложно о эфира фенола. Предположение, что появление интенсивного окрашивания в известной степени связано с образованием сложного эфира фенола, подтверждается тем фактом, что пропионовый, масляный, изомасляный, изовалерьяновый и ароматические альдегиды реагируют с образованием лишь желтого окрашивания. Формальдегид и акролеин дают оранжевое окрашивание. [c.480]
Вейганд и Штеглих [2499] описали способ декарбобензоксилирования при действии кипящей трифторуксусной кислоты. Реакция протекает с выделением двуокиси углерода и с образованием бензилового эфира трифторуксусной кислоты. Последний очень легко бензилирует ароматические аминокислоты эту побочную реакцию можно предотвратить добавлением таких соединений, как фенол, резорцин или анизол, которые легко вступают в реакции замещения. Время реакции варьируется в широких пределах от 2 мин до 2,5 час в зависимости от природы используемой аминокислоты выходы составляют 40—98 /о. Продолжительное действие реагента приводит к расщеплению как простых 0-бензиловых эфиров (например, в случае 0-бен-зилтирозина), так и сложных бензиловых эфиров. По наблюдениям Косла и Ананда [12246], декарбобензоксилирование может протекать даже в более мягких условиях (3 час, 38°). Бензиловые, п-нитробензиловые и метиловые эфиры расщепляются наряду с карбобензоксигруппой при гидролизе смесью трифторуксусной кислоты с соляной кислотой (4 час, 40 ). Карбобензоксигруппа особенно легко отщепляется от соответствующего производного пироглутаминовой кислоты [1975]. [c.60]
Последующие стадии превращения бензоилсалицилата меди определяются природой среды. В протонном растворителе (например, вода или бензойная кислота) бензоилсалицилат меди декарбоксилируется с образованием фенилбензоата, дающего при гидролизе фенол. В апротонных ароматических растворителях (бензол и его гомологи) в основном образуется фенилбензоат и в небольшом количестве — сложные эфиры бензойной кислоты и растворителя. В связи с этим было высказано предположение о возможности другой пространственной конфигурации бензоата меди, способствующей межмо-лекулярному взаимодействию бензоата меди с молекулами растворителя. Так, при окислении бензойной, фталевой и других кислот в присутствии солей переходных металлов в растворе замещенного бензола отмечается образование дифенила и дифенилкарбоновых кислот [94]. [c.232]
Окислительная стабильность смазочных жидкостей, как правило, повышается с введением небольшого количества присадок, обладающих антиокислительными свойствами. Фенотиазин является одним из наиболее эффективных антиокислителей для сложных алкил-диэфиров . Хотя эта присадка повышает окислительную стабильность малостабильных эфиров алифатических двухосновных кислот и фторспиртов, она совсем неэффективна или даже ухудшает свойства эфиров, стабильных к окислению при температурах 177° С и выше , так как при высоких температурах она способствует образованию осадка. Отрицательное влияние на окислительную стабильность фторспиртов оказывает и ряд других антиокислителей, таких как фенольные соединения, амины, соединения, содержащие серу и селен Эфиры ароматических кислот и фторспиртов, даже без антиокислителей, чрезвычайно стабильны к окислению и вполне удовлетворяют требованиям, предъявляемым нормами MIL-L-9236A (ВВС США) (260° С) В этом отношении они гораздо лучше масел, выпускаемых по нормам MIL-L-7808 которые содержат ингибиторы окисления. [c.276]
Свободный 50з превращает мало реакционноспособные олефины и ароматические углеводороды в сложные эфиры серной кислоты и сульфокислоты. При использовании концентрированной серной кислоты протекают и реакции полимеризации. Насыщенные парафиновые и циклопарафиновые углеводороды также взаимодействуют с 50з, что приводит к значительным потерям при очистке. Продукты реакции в основном отделяются от масла вместе с непрореагировавшей кислотой в виде черного, высоковязкого кислого гудрона. Часть этих продуктов остается растворенными в масле. Сульфированные продукты ( нафтасульфокислоты ) не могут быть нейтрализованы гидроксидом кальция, так как эта реакция протекает только при температурах выше 100 °С, а при таких температурах увеличивается коррозионная агрессивность среды и ухудшается качество масла. Кроме того, сульфонаты кальция набухают в масле, что приводит к забивке масляных фильтров. Поэтому нафтасульфокислоты нейтрализуют водным раствором гидроксида натрия и экстрагируют спиртами. Экстракция спиртами предотвращает образование стабильных водных эмульсий щелочными сульфонатами. После спиртовой экстракции масло подвергают обесцвечиванию отбеливающей глиной. Именно этот тип нейтрализации объясняет, почему олеумную очистку иногда называют мокрым, а сернокислотную — сухим способом очистки масел, поскольку в этом способе применяется гидроксид кальция. Применение больших количеств олеума (до 100 % масс, в расчете на масло) позволяет практически полностью удалить олефины и ароматические углеводороды. В результате такой очистки получают белые масла без цвета, запаха и вкуса, которые используют в медицине. [c.61]
Тв рмическое разложение полиэтилентерефталата является сложным процессом, при котором последовательно протекает ряд реакций, что приводит к образованию довольно большого числа газообразных и нелетучих продуктов. Изучение термического разложения ПЭТФ и низкомолекулярных алкильных эфиров ароматических кислот в области температур 282—383 °С [230] и 370—475 °С 1[231] показало, что продукты пиролиза ПЭТФ аналогичны продуктам пиролиза модельных соединений. [c.407]
Авторы установили, что коричная и малеиновая кислоты с жирноароматическими триазенами реагируют нормально с образованием сложных эфиров. Двойная связь не влияет на результат реакции. С выходами 51—83% были получены соответствующие эфиры коричной и малеиновой кислот. При реакции гликолевой кислоты с метилфенилтриазеном обнаружилось, что реакция происходит с участием обеих функциональных групп — карбоксильной и оксигруппы с образованием эфира метоксиуксусной кислоты, который получен с выходом 79% [351]. По-видимому, под влиянием карбоксильной группы повышаются кислые свойства оксигруппы. Жирно-ароматические триазены, как и диазометан, со спиртами в обычных условиях не реагируют. [c.66]
Неокотоны представляют собой растворимые натриевые соли сложных эфиров нерастворимых азокрасителей — производных азотолов. Для получения их в качестве этерифицирующих агентов применяют ароматические, алифатические и гетероциклические сульфокарбоновые кислоты, а также ароматические ди- и трисульфокислоты и аналогичные соединения, у которых после образования сложного эфира остается по крайней мере одна свободная солеобразующая группа. Ацилирование гидроксигруппы нерастворимого азокрасителя осуществляют нагреванием с хлорангидридами этих кислот в присутствии третичных оснований (обычно пиридина) или взаимодействием красителя с многоосновной кислотой в пиридиновом растворе в присутствии хлоридов фосфора. [c.435]
Все исследовавшиеся органические фосфаты образовывали нод действием ядерного излучения большое количество сильных одноосновных кислот. Так, ири воздействии дозы излучения 1,9 10 р 22% исходного трикрезилфосфата превратилось в кисл1>1е продукты. Если учесть ароматическую природу этого соедипения, у него наблюдался очень значительный рост вязкости под действием ядерного излучения (см. табл. 5). Аналогичные результаты были получены по алифатическим сложным эфирам фосфорной кислоты. Даже ири использовании фосфатов в малых концентрациях в качестве противозадирных присадок к маслам, приготовленным на базе сложных эфиров, действие облучения вызывало образование большого количества сильных кислот. Наиример, при действии дозы излучения 1,19 10 р в смеси дп-2-этилгексилсебацината с 5% трикрезилфосфата 60—70% трикрезилфосфата превращалось в сильную кис.7[оту. Это указывает на то, что сложный эфир фосфорной кислоты, введенный в масло, приготовленное на базе дпэфиров, действует как поглотитель радикалов. Образование фосфорных кислот ухудшает свойства базовых масел и придает пос,ледпим коррозийную агрессивность, что исключает применение фосфатов в качестве базовых масел и, возможно, в качестве противозадирных присадок нри создании радиационно-стойких масе.п. [c.238]
Прпс0ед1п1еппе к кратной связи Отщепление с образованием кратной связи Гидролиз сложных эфиров карбоновых кислот Реакции карбонильных соединений и их ана.ю-гов в качестве электрофилов Электрофильное замещение в ароматическом ядре [c.6]
chem21.info
Химические свойства сложных эфиров
Способы получения сложных эфиров
Важнейший способ получения сложных эфиров – реакция этерификации – кислота + спирт.

С помощью метода меченых атомов доказано, что при этерификации от молекулы кислоты отщепляется гидроксил, а от молекулы спирта – водород.
Химические свойства сложных эфиров
1. Реакция этерификации
Основное химическое свойство – гидролиз сложных эфиров – расщепление сложных эфиров под действием воды. Эта реакция обратна реакции этерификации. Реакция протекает как в кислой (катализаторы реакции – протоны Н+), так и в щелочной среде (катализаторы реакции – гидроксид-ионы ОН –).

В присутствии щелочи реакция необратима, т.к. происходит омыление – образование солей карбоновых кислот.
В растворах разбавленных минеральных кислот соли карбоновых кислот вновь превращаются в исходную карбоновую кислоту:
2СН3СООNa + h3SO4 разб.→ 2СН3СООН + Na2SO4
ацатат натрия уксусная кислота
2. Реакция восстановления
При восстановлении сложных эфиров образуется смесь двух спиртов:

3. Взаимодействие с аммиаком
При взаимодействии сложных эфиров с аммиаком образуются амиды:

Применение сложных эфиров
Многие сложные эфиры обладают приятным запахом. Так, амиловый эфир муравьиной кислоты имеет запах вишни, изоамиловый эфир уксусной кислоты – запах груш. Эти эфиры идут на изготовление искусственных эссенций, используемых в производстве фруктовых вод и т.п., а также в парфюмерии.
Этилацетат используется в качестве растворителя, а также при изготовлении лекарственных средств.
biofile.ru
Реакция - образование - сложный эфир
Реакция - образование - сложный эфир
Cтраница 1
Реакция образования сложного эфира носит название реакции этерификации ( от лат. Она является обратимой реакцией: вода разлагает сложные эфиры с образованием исходных веществ - кислоты и спирта. [1]
Реакция образования сложного эфира, называемая также реакцией этерификации ( ecther по-латыни - эфир), протекает медленно. Эта реакция является обратимой, обычно не доходит до конца и является ярким примером единства противоположно направленных процессов. [2]
Реакция образования сложного эфира из кислоты и спирта ( или фенола) называется реакцией этерификации. Она катализируется ионами водорода и поэтому ускоряется в присутствии минеральных кислот. [3]
Реакция образования сложного эфира из кислоты и спирта ( или фенола) называется реакцией э т е р и ф и к а ц и и. Она катализируется ионами водорода и поэтому ускоряется в присутствии минеральных кислот. [4]
Реакция образования сложного эфира из кислоты и спирта ( пли фенола) называется реакцией э т е р и ф и к а ц и и. Она катализируется ионами водорода и поэтому ускоряется в присутствии минеральных кислот. [5]
Реакция образования сложного эфира из кислоты и спирта ( или фенола) называется реакцией э т е р и ф и к а ц и и. Ока катализируется ионами водорода и поэтому ускоряется в присутствии минеральных кислот. [6]
Реакция образования сложного эфира из кислоты и спирта ( или фенола) называется реакцией этерификации. Она катализируется ионами водорода и поэтому ускоряется в присутствии минеральных кислот. [7]
Реакция образования сложных эфиров носит название реакции этерификации. Реакция этерификации обратима: вода в присутствии кислот или щелочей разлагает сложные эфиры с образованием исходных веществ - кислоты и спирта. Такое гидролитическое разложение сложных эфиров называется реакцией гидролиза. Механизм этой реакции разобран в гл. [8]
Реакция образования сложных эфиров носит название реакции этерификации. Реакция этерификации обратима: вода в присутствии кислот или щелочей разлагает сложные эфиры с образованием исходных веществ - кислоты и спирта. Механизм этой реакции разобран в гл. [9]
Реакции образования сложных эфиров протекают при довольно высоких температурах, поэтому эпоксидные кольца могут разрываться. [10]
Реакция образования сложного эфира была разобрана в разделе о спиртах. [11]
Реакция образования сложного эфира из кислоты и спирта ( или фенрла) называется реакцией этерификации. Она катализируется ионами водорода и поэтому ускоряется в присутствии минеральных кислот. [12]
Реакция образования сложного эфира из кислоты и спирта ( или фенола) называется реакцией э т е р и ф и к а ц и и. Она катализируется ионами водорода и поэтому ускоряется в присутствии минеральных кислот. [13]
Реакция образования сложного эфира из кислоты и спирта ( или фенола) называется реакцией этерификации. Она катализируется ионами водорода и поэтому ускоряется в присутствии минеральных кислот. [14]
Реакция образования сложного эфира из кислоты и спирта ( или фенола) называется реакцией этерификации. [15]
Страницы: 1 2 3
www.ngpedia.ru