Метилфениловый эфир структурная формула
Этилфениловый эфир, - Справочник химика 21
Бромэтан Этилфениловый эфир (простой эфир) [c.551]
Этилфениловый эфир Этоксибензол С Н,ОСо.Н, [c.494]
Этилфениловый эфир см. Фенетол [c.570]
ФЕНЕТОЛ (этоксибёнзол, этилфениловый эфир), мол.м. 122,2 бесцв. жидкость с приятным запахом т. пл. -30,7 С, т.кип. 170 С, 62 "С/15 мм рт.ст. 5 1,0114 1,5171 Л% -4419,6 кДж/моль г 6,87 Па с (15 С) у 32,8 мН/м М-4,67 -10 Кл м, е 4,130 (30 °С). Раств. в этаноле, диэтиловом эфире, соляной к-те, плохо раств. в воде (1,21 г в 1 л) легко перегоняется с водяным паром образует азеотроп с водой (т.кип. 97,3 С, 43% Ф. по массе). [c.64]
Этилфениловый эфир (фенетол). [c.94]Фенетол (этилфениловый эфир, этоксибензол) — бесцветная жидкость с приятным запахом, смешивается с этиловым спиртом и диэтиловым эфиром, нерастворим в воде Температура плавления —30,2°С, температура кипения 172 °С, 0,9666, По — 1,5076 УФ спектр Яд1а1.С — 269 им, 8-1500 [c.95]
Этилпропиловый эфир . 92 13. Этилфениловый эфир 94 [c.254]
Фенетол, этоксибензол, этилфениловый эфир [c.10]
Фенетол Этилфениловый эфир Железоалюминиевый сплав, содержание А1 — 50, 60 н 66%, наиболее активен последний сплав [251] [c.733]
Вини лфени ловый эфир Этилфениловый эфир Палладиевая чернь [269]= Рё (1%) на АЬОа в диизопропиловом эфире, 20° С [270] Сплав Р1—Р(1 (1 10) 20—50° С, жидкая фаза [198] Рс1 (чернь) — А [269] [c.1038]
Этилен с фенолом в присутствии 5 объемн. % BFg и 2% НС1 при температуре 150—300° и давлении 50 атм. образует фенетол [169]. Крезол и фенол в присутствии BF3 дают этилтолиловый эфир [97]. Образование при указанных условиях этилфениловых эфиров и отсутствие этилфенолов объясняется высокой устойчивостью этих эфиров. [c.169]
Из анилина получите фенол, йодбензол, фторбензол, нитрил бензойной кислоты, хлорбензол, этилфениловый эфир. [c.109]
При перегруппировке л1-этилфениловых эфиров высших жирных кислот как при низкой температуре в нитробензоле, так к при высокой температуре в отсутствие растворителя образуются только о-оксикетоны [c.260]
ЭТОКСИБЕНЗОЛ ЭТИЛФЕНИЛОВЫЙ ЭФИР [c.576]
Сколько граммов этилфенилового эфира можно получить из 18,8 г фенола при его взаимодействии с необходимым количеством едкого натра и последующей реакции образовавшегося продукта с хлористым этилом [c.118]
Этилфениловый эфир (фене- 172 [c.208]
ФЕНЕТОЛ (этилфениловый эфир) СвН50С2Н5, мол. в. 122,1 — бесцветная жидкость, приятного запаха т. пл.—29,52° т. кпп. 170°/760 мм, 108,4°/100 мм [c.193]
Р-Роданэтил-2-бром-4-этилфениловый эфир 889 [c.410]
chem21.info
Основные положения органической химии — 2. Основные понятия органической химии — ЗФТШ, МФТИ
Брутто-формула химического вещества – формула, дающая информацию о том, какие атомы и в каком количестве присутствуют в молекуле данного соединения:
С12Н22О11 С2Н2О4 С3Н9N
сахароза щавелевая кислота триэтиламин
Чаще брутто-формулы называют молекулярными. Они удобны для проведения расчетов, связанных с молярными массами веществ, однако химики всё же предпочитают при написании брутто-формул вносить минимальную информацию о структуре молекул:
C2H5OH HCOOH C6H5COONa
этанол муравьиная кислота бензоат натрия
Структурная формула описывает порядок соединения атомов в молекуле. Химические связи изображаются чёрточками. Связь между водородом и остальными атомами обычно не указывается. Для изображения циклических структур широко используются общепринятые символы:
| пропанол-2 | метилфениловый эфир | 2-метилцикло-пентанон |
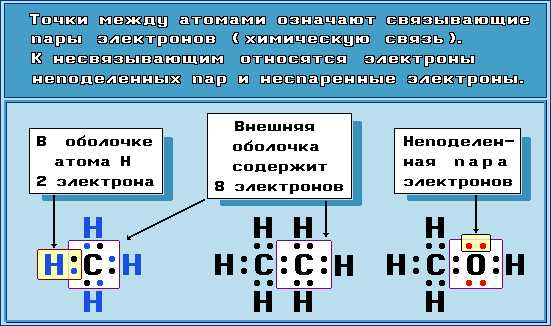
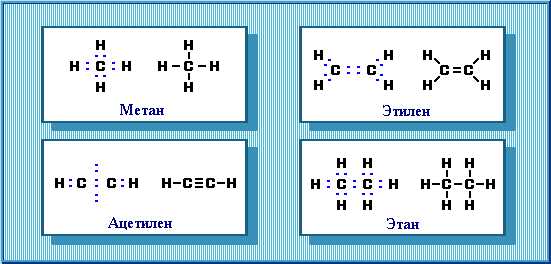
Для изображения электронного строения молекул используются электронные формулы (структуры Льюиса, октетные формулы). При написании электронной формулы должно выполняться правило октета, согласно которому атом, участвуя в образовании химической связи (отдавая или принимая электроны), стремится приобрести электронную конфигурацию инертного газа – октет (восемь) валентных электронов. Исключение составляет атом водорода, для которого устойчивой является конфигурация гелия, т. е. 2 валентных электрона.
Общую пару электронов иногда обозначают чёрточкой, которая и символизирует внутримолекулярную химическую связь.
zftsh.online
2. Основные понятия органической химии — ЗФТШ, МФТИ
Брутто-формула химического вещества – формула, дающая информацию о том, какие атомы и в каком количестве присутствуют в молекуле данного соединения:
С12Н22О11 С2Н2О4 С3Н9N
сахароза щавелевая кислота триэтиламин
Чаще брутто-формулы называют молекулярными. Они удобны для проведения расчетов, связанных с молярными массами веществ, однако химики всё же предпочитают при написании брутто-формул вносить минимальную информацию о структуре молекул:
C2H5OH HCOOH C6H5COONa
этанол муравьиная кислота бензоат натрия
Структурная формула описывает порядок соединения атомов в молекуле. Химические связи изображаются чёрточками. Связь между водородом и остальными атомами обычно не указывается. Для изображения циклических структур широко используются общепринятые символы:
| пропанол-2 | метилфениловый эфир | 2-метилцикло-пентанон |
Для изображения электронного строения молекул используются электронные формулы (структуры Льюиса, октетные формулы). При написании электронной формулы должно выполняться правило октета, согласно которому атом, участвуя в образовании химической связи (отдавая или принимая электроны), стремится приобрести электронную конфигурацию инертного газа – октет (восемь) валентных электронов. Исключение составляет атом водорода, для которого устойчивой является конфигурация гелия, т. е. 2 валентных электрона.
Общую пару электронов иногда обозначают чёрточкой, которая и символизирует внутримолекулярную химическую связь.


zftsh.online