Автомобильная безопасность - Безопасный автомобиль. Метилбутиловый эфир
Лекция МТБЭ
Одним из основных источников загрязнения воздушного бассейна являются продукты сгорания моторных топлив в двигателях внутреннего сгорания автомобилей. Наиболее опасными компонентами выхлопных газов в настоящее время считаются соединения свинца, наличие которых связано с использованием тетраэтилсвинца и тетраметилсвинца для улучшения антидетонационных свойств бензина.
В последние годы во многих промышленно развитых странах с целью оздоровления экологической обстановки приняты законодательства, обязывающие промышленность выпускать улучшенные сорта моторных топлив, содержание соединений свинца в которых существенно снижено или полностью исключено. Кроме того, новые "экологически чистые" сорта бензинов должны содержать в своем составе не менее 2 % масс, кислорода.
Все это предопределило бурное развитие производства и применения высокооктановых кислородсодержащих компонентов – метил-третбутилового (МТБЭ), метил-третамилового (МТАЭ) и этил-третбутилового (ЭТБЭ) эфиров.
Метил-третбутиловый эфир (МТБЭ) представляет собой высокооктановый кислородосодержащий компонент автомобильных бензинов, применяемый для повышения октанового числа при производстве автомобильных бензинов, взамен высокотоксичного тетраэтилсвинца.
Химизм и механизм процесса
Одним из основных способов получения МТБЭ является проведение селективного взаимодействия метанола с содержащимся в С4-фракциях изобутиленом в присутствии кислотных катализаторов. В основе процесса получения МТБЭ лежит реакция:
СН3 СН3
│ │
СН2 = С – СН3 + СН3ОН → СН3 – C – О – СН3
│
СН3
Из имеющегося в нефтехимической промышленности углеводородного сырья пригодными для получения МТБЭ являются С4-фракция пиролиза до и после извлечения дивинила, бутан-бутиленовая фракция каталитического крекинга и изобутан-изобутиленовая фракция дегидрирования изобутана.
Реакция взаимодействия олефинов со спиртами является реакцией электрофильного присоединения по кратным связям, механизм которой описывается карбоний-ионной теорией, согласно которой каталитически активным центром является протон. Первая стадия ‑ взаимодействие протона катализатора с кратной связью олефина:

Образующийся карбониевый ион неустойчив из-за дефицита электронов и он должен быть черезвычайно реакционноспособен к реагентам, которые могут предоставить электронную пару для образования ковалентной связи. Вследствие этого на второй стадии карбониевый ион быстро взаимодействует с нуклеофильным реагентом с образованием продукта реакции.

Присоединение, как и при других реакциях этого типа, происходит по правилу Марковникова.
Кроме того, в процессе образуется небольшое количество побочных продуктов, таких как димеры изобутилена, триметилкарбинол (ТМК), диметиловый эфир. Образование ТМК в основном зависит от содержания воды в исходном сырье, которое не должно превышать 0,1 % масс. Реакции димеризации изобутилена и межмолекулярной дегидратации метанола протекают в незначительной степени при оптимальных температурном режиме и соотношении исходных реагентов.
Реакция синтеза МТБЭ является обратимой и экзотермической и при реагировании одного моля изобутилена с одним молем метанола выделяется 10 ккал/моль тепла. Поэтому низкая температура на выходе из реактора способствует более полному превращению исходных реагентов, а повышение температуры напротив сдвигает равновесие влево и уменьшает степень превращения изобутилена и метанола. Высокая температура в реакционной зоне ускоряет протекание основной, но в большей степени побочных реакций, в том числе межмолекулярной дегидратации метанола.
Используются различные приемы для получения наибольших конверсий:
- снижение температуры в заключительном пространстве реакционной зоны: синтез МТБЭ проводят при температуре не более 77 °С. В нижней части каждого яруса катализатора регистрируется температура: после 1-го слоя не более 77 °С, после 2-го и 3-го слоев не более 70 °С.
- увеличение мольного соотношения спирт/изоолефин: характерно использование избыточного от эквимолярного количества метанола с целью увеличения степени превращения изобутилена и исключения процесса димеризации последнего. Мольное соотношение метанол/изобутилен 1,075:1
Процесс синтеза МТБЭ проводят при повышенном давлении - не более 1,15 МПа, обеспечивающем перевод всех компонентов реакционной массы в жидкое состояние.
Катализатор избранной технологии
Известны два основных направления синтеза МТБЭ из третичных олефинов и первичных спиртов, связанные с применением гомогенных и гетерогенных катализаторов кислотно-основного типа.
В качестве гомогенных катализаторов были предложены минеральные кислоты ‑ серная, фосфорная, соляная, борная, катализаторы Фриделя - Крафтса, органические сульфокислоты.
Общими недостатками большинства перечисленных гомогенных катализаторов являются высокая коррозионная агрессивность среды и связанная с этим необходимость использования оборудования из дорогостоящих материалов, а также низкая селективность процесса и трудности разделения реакционной смеси от катализатора. Перечисленные недостатки в значительной степени могут быть устранены при использовании гетерогенных катализаторов.
Наиболее эффективны для синтеза МТБЭ сульфированные ионообменные смолы. Самыми распространенными являются сульфокатиониты (СФК) со стирол-дивинилбензольной матрицей. Достаточно эффективны и применяются в промышленности формованные катализаторы такие как КУ‑2 ФПП. КУ‑2 ФПП выпускаются в форме цилиндров и колец размерами 5‑20 мм и обладают одновременно свойствами катализатора и массообменной насадки.
Основные трудности, возникающие при использовании СФК в промышленности для получения МТБЭ, связаны с большим гидродинамическим сопротивлением слоя. Кроме того, недостатком существующих СФК является относительно невысокая термостабильность (ФПП – формованные полипропиленом).
Для обеспечения высокой производительности катализатора, с одной стороны, и высокой степени превращения исходных реагентов в состоянии близком к равновесному, с другой, необходимо разработать и строго поддерживать температурный режим работы реактора. На расчет оптимального температурного режима работы реактора определяющее влияние оказывает большое количество выделяемого при синтезе эфира тепла (10 ккал/моль) наряду с кинетическими и термодинамическими закономерностями протекания реакции.
Равновесное состояние любой обратимой реакции, в том числе и синтеза МТБЭ, характеризует наивысшую степень превращения исходных реагентов при различных условиях проведения процесса (содержание изобутилена в исходной С4-фракции; мольное отношение метанол/изобутилен, температура).
Требования к исходному сырью
Образование побочного продукта – ТМК - в основном зависит от содержания воды в исходном сырье, которое не должно превышать 0,1 % масс.
Используемые в качестве исходного сырья бензиновые фракции каталитического крекинга или пиролиза могут содержать в своем составе щелочные или азотные соединения и другие примеси, которые способствуют быстрой дезактивации катализатора.
С целью разрешения данной проблемы в технологической схеме многих процессов предусмотрена очистка углеводородов от нежелательных примесей до подачи их в реакционную зону.
Технологическая схема процесса
Из анализа приведенных в научно-технической и патентной литературе данных видно, что процесс получения МТБЭ должна включать в себя несколько стадий.
1.Проведение синтеза эфира в реакторном блоке в присутствии катализатора при повышенных температуре и давлении.
Разделение реакционной смеси и выделение товарного продукта.
Отмывка отработанных углеводородов от метанола и выделение его безводного раствора.
Наличие азеотропа метанола с углеводородами С4 и МТБЭ, ограничение содержания спирта и других побочных продуктов (триметилкарбинола, димеров, углеводородов С4) в товарном продукте, содержание изобутилена в исходной С4-фракции, требования к качеству отработанных углеводородов и многие другие факторы во многом – предопределяют разработку технологической схемы и технологических параметров проведения процесса получения МТБЭ, в том числе и реакторного блока.
В состав промышленной установки входит реакторный блок, узел ректификации, в котором получают товарный продукт, и блок выделения метанола из отработанной С4-фракции, включающий отмывочную и ректификационную колонны.
Реакторный блок состоит адиабатического реактора. Использование трехзонного реактора позволяет получить качественный МТБЭ при высокой степени превращения исходных реагентов и высокой производительности катализатора без заметного протекания побочных реакций.
Тип реактора
Реактор адиабатического типа, он представляет собой полый цилиндрический аппарат. Адиабатические реакторы работают в таких условиях, когда теплообмен с внешней средой практически исключен. Этого достигают хорошей теплоизоляцией внешней поверхности реактора. При протекании реакции в адиабатических условиях изменяется температура в реакторе и, следовательно, меняется скорость реакции. Скорость экзотермических реакций в адиабатических условиях увеличивается, так как выделяющееся в результате реакции тепло расходуется только на нагрев реакционной смеси. Эндотермические реакции в адиабатических условиях проводить невыгодно ввиду того, что уменьшение скорости реакции приводит к значительному увеличению времени пребывания компонентов в реакторе.
Синтез МТБЭ ведется в реакторах шахтного типа с тремя реакционными зонами, работающими в адиабатическом режиме с промежуточным охлаждением реакционной массы. Отвод выделяемого реакцией синтеза МТБЭ тепла осуществляется в выносных кожухотрубчатых теплообменниках промышленной водой. Внутренняя часть реактора разделена перегородками на три реакционных зоны. Внутри реактора находятся три слоя сульфокатионитного катализатора. Для удерживания зерен катализатора в нижней части каждой зоны устанавливается сетка с разметом ячеек менее 0,2 мм, закрепленная на колосниковой решетке.

Смесь метанола с С4 фракцией (изобутиленсодержащая фракция предварительно отделяется от воды), нагретая до температуры не более 55 ºС, поступает в реактор Р-1.
Тепло экзотермической реакции после каждого яруса катализатора снимается охлаждением реакционной смеси от 77 ºС до 55 ºС в теплообменниках оборотной водой.
На линиях выхода реакционной смеси из каждой секции реактора Р-1, а также на линии входа реакционной шихты в реактор, имеются фильтры Ф-1, Ф-2, Ф-3 для улова возможно уносимого катализатора.
Реакционная смесь из реактора Р-1 поступает в ректификационную колонну Кт-1.
Колонна Кт-1 предназначена для отгонки отработанной С4 фракции из реакционной смеси. Пары фракции С4 с верха колонны Кт-1 конденсируется и сливаются в емкость Е-1.
В шлемовую линию колонны Кт-1, подается пар для отмывки отработанной С4 фракции от не прореагировавшего метанола. В емкости Е-1 происходит отстой и расслоение смеси С4 фракции и метанольной воды. Отработанная С4 фракция подается в колонну Кт-1 в виде флегмы. Избыток отработанной С4 фракции откачивается на склад.
Метанольная вода с низа емкостей Е-1 отводится на сжигание на установку обезвреживания химически загрязненных сточных вод.
Кубовая жидкость колонны Кт-1 (МТБЭ-ректификат) при необходимости дальнейшей очистки МТБЭ поступает в колонну Кт-2.
Кубовый продукт колонны Кт-2, содержащий МТБЭ, димеры изобутилена и ТМК (МТБЭ технический) откачивается на склад.
studfiles.net
Вред и польза топливных присадок

Присадки для автомобильного топлива. Что это вред или польза?
|
НЕРЕКОМЕНДУЕМЫЕ ПРИСАДКИ К ТОПЛИВУ |
Тетраэтилсвинец (ТЭС) Pb(Ch4Ch3)4 — ядовитое металлоорганическое соединение. Применялось в основном как антидетонирующая присадка к моторному топливу, повышающая его октановое число.

Снижает дымность, шумность, повышает мощность. Способен подавить детонацию в двигателе и даже повысить детонационную стойкость керосина (из него иногда и делают бодяжный бензин).

Сильнейший яд для человека: в двигателе переходит в парообразное состояние и через верхние дыхательные пути проникает в организм (способен просачиваться и через неповрежденную кожу). Поражает нервную систему, вызывая отравления, вплоть до инвалидности и смерти.
Нафтали?н С10Н8 — твёрдое кристаллическое вещество с характерным запахом, в воде не растворяется, хорошо растворяется в бензоле, эфире.

Добавление 500 г нафталина на 10 л бензина приводит к увеличению октанового числа бензина на 3—4 единицы — 92-й бензин «превращается» в 95-й.

Сильнейший яд для человека: в двигателе переходит в парообразное состояние и через верхние дыхательные пути проникает в организм (способен просачиваться и через неповрежденную кожу). Поражает нервную систему, вызывая отравления, вплоть до инвалидности и смерти.
Спирт — спирты являются обширным и очень разнообразным классом органических соединений: они широко распространены в природе, имеют важнейшее промышленное значение и обладают исключительными химическими свойствами.

При добавлении 5—20% спирта в бензин октановое число растет на 3—8 единиц (из А-95 делают А-98), при этом улучшается процесс сгорания, возрастают мощность и КПД двигателя.

Оказывает серьезное разъедающее действие на прокладки в двигателе. При передозировке компоненты топлива не смешиваются в цилиндре и октановое число падает: возникает детонация, стук клапанов.
Ацетон (метилбутиловый эфир) — хорошо растворяет многие органические вещества (ацетилцеллюлозу и нитроцеллюлозу, жиры, воск, резину и др.), а также ряд солей (хлорид кальция, иодид калия).

В небольших количествах допустим для повышения октанового числа.

Его часто добавляют прямо на заводах. Если добавить еще «флакончик» в бак, получается многократное превышение допустимых норм — образуются вредные вещества. Также быстро понижается октановое число.
Марганец — 14-й элемент по распространённости на Земле, а после железа — второй тяжёлый металл, содержащийся в земной коре (0,03 % от общего числа атомов земной коры).
 Увеличивает октановое число на 3—6 единиц.
Увеличивает октановое число на 3—6 единиц.

Выводит из строя нейтрализаторы и свечи: падает мощность, из выхлопной трубы идет сизый дым.
Ферроцен — одно из наиболее известных металлоорганических соединений, представитель класса сэндвичевых соединений.
 Повышает октановое число на 4—5 единиц.
Повышает октановое число на 4—5 единиц.

При использовании ферроцена на свечах и в цилиндрах образуется красный нагар: срок службы двигателя сильно снижается.
Бензол, толуол (от исп. Tolu, толуанский бальзам), метилбензол С7H8 — бесцветная жидкость с характерным запахом, простейший алкиларен.

Повышает октановое число на 10%.

Является сильным растворителем, который уничтожает практически все эластичные детали мотора и приводит к активной коррозии.
ВНИМАНИЕ! Некачественный бензин с добавленными присадками, в отличие от заводского, проводит электричество. Возможно самовозгорание автомобиля.
|
УСЛОВНО РЕКОМЕНДУЕМЫЕ ПРИСАДКИ |
Метилтретбутиловый эфир (МТБЭ) (трет-бутилметиловый эфир, 2-метил-2-метоксипропан, МТБЭ) — химическое вещество с химической формулой СН3—O—C(СН3)3, один из важнейших представителей простых эфиров.

Благодаря высокому собственному октановому числу (выше 110 единиц) полезен для двигателя: содержащийся в нем кислород обеспечивает полноту сгорания и тем самым снижает выбросы СО и СН.

Повышенное содержание МТБЭ (больше 15%) ведет к падению мощности и росту выбросов окислов азота (NOx). Кроме того, бензин с повышенной концентрацией МТБЭ агрессивен к уплотнениям топливной системы и ускоряет процесс коррозии.
Монометиланилин (ММА) — формально является производным аммиака, в котором атомы водорода замещены на фенильный и два метильных радикала.

В малой концентрации (до 1,3%) безвреден для мотора, снижает детонацию.

При превышении содержания в двигателе образовывается нагар, что может привести к «зависанию» клапанов. К тому же ММА относится к категории ядов: при вдыхании паров человеку грозит серьезное отравление.
|
МОЮЩИЕ ПРИСАДКИ — БЕЗВРЕДНЫ |

Это тщательно сбалансированный пакет из ингибиторов коррозии, деэмульгатора (поглотителя воды) и моющего компонента, в качестве которого обычно выступают поверхностно-активные вещества (ПАВ). «Разрыхляет» нагар и лаковые отложения, а мельчайшие частички уносятся с потоком топливо-воздушной смеси в цилиндр, где благополучно сгорают.

Передозировка (более 10%) приведет к тому, что двигатель не будет заводиться.
| Источник: wikipedia.org |
| Следующая > |
cardefence.ru
8. Производство метилтретбутилового эфира (мтбэ)
В последнем десятилетии XX и начале XXI века проблемы экономичности транспортных средств и загрязнения воздушного бассейна выхлопными газами как никогда ранее потребовали существенных изменений в технологии производства моторных топлив.
Борьба за улучшение экологии окружающей среды вынудила правительства многих стран мира принять ряд мер в законодательном порядке. В странах ЕС были введены ограничения на использование высокотоксичного тетраэтилсвинца в качестве высокооктановой присадки автомобильных бензинов, а принятые в США дополнения к Закону о чистом воздухе установили новые жёсткие нормативы к качеству топлив, что вызвало аналогичные последствия в странах Западной Европы и во всем мире. Впервые в мировой практике было сформулировано понятие "экологически чистого моторного топлива".
В США модифицированные бензины новых поколений, удовлетворяющие перспективным требованиям предстоящего десятилетия, получили название реформулированных бензинов. Впервые эти требования были выдвинуты в 1990 году в Дополнениях к "Акту по чистому воздуху" ("САА"), подготовленному Агентством по охране окружающей среды США. Выход такого Акта означал конец эпохи этилированных бензинов, и с 1994 года они практически исчезли с рынка США. Использование первого поколения реформулированных бензинов в 1995-2000 гг. позволило сократить на 15% токсичные выхлопы и выхлопы летучих органических компонентов, образующих смог в городах.
Проблема обеспечения высокой детонационной стойкости бензинов остается актуальной на любом этапе развития нефтепереработки. На современном этапе эта проблема стоит не менее остро, чем в период перехода к поколению неэтилированных бензинов. Причиной тому являются новые экологические требования к неэтилированным бензинам новых поколений, ограничивающие использование ряда высокооктановых компонентов: бензола, других ароматических углеводородов, олефинов.
Доводка эксплуатационных и экологических свойств автомобильных бензинов до требований мирового рынка является важнейшей проблемой выживания любого НПЗ России и конкурентоспособности российской нефтепереработки в целом. При этом нужно четко представлять, что выработка просто неэтилированных бензинов еще не означает, что создана технология производства экологически чистых автобензинов мирового уровня. Для достижения в России требований мировых стандартов на экологически чистые автобензины необходимо не только исключить из технологии применение тетраэтилсвинца, но и существенно снизить содержание в товарных бензинах ароматики и в частности бензола, осуществить замену ароматики на изопарафиновые углеводороды. Ввести в состав бензинов высокооктановые кислородосодержащие добавки (МТБЭ, МТАЭ, ИПТБЭ, ДИПЭ и др.), которые, наряду с положительным эффектом по снижению содержания в выхлопных газах окиси углерода и углеводородов, обеспечат прирост октанового индекса автобензинов. Снизить содержание в бензинах олефинов и при всем этом повысить их дорожное октановое число ([ИОЧ + МОЧ] / 2) до уровня минимальных требований общеевропейских норм.
Развивающаяся автомобильная техника и выход России на европейский и другие рынки требуют существенного совершенствования технологии и оборудования, а также основных процессов, входящих в комплексные технологические системы производства и компаундирования автобензинов.
Давно известно, что двигатели внутреннего сгорания прекрасно работают, например, на низших спиртах, а метанол уже применялся как автомобильное топливо. В США давно уже заправляют автомобили смесью бензина и этанола (синтетического или ферментативного) и называется это новое топливо gasohol (газохол) - гибрид от слова gasoline (бензин) и alcohol (спирт). В Италии получают из оксида углерода и водорода смесь спиртов от С1 до С5 и добавляют эту присадку в автомобильные бензины для повышения их октанового числа.
Но самым эффективным средством является метилтретбутиловый эфир (2-метил-2-метоксипропан) (СНЗ)ЗСОСНЗ. Во всем мире его теперь называют МТБЭ. Это соединение как компонент автомобильных бензинов уникально во всех отношениях.
Известно, что практически все низшие кислородсодержащие соединения имеют высокое октановое число - до 100 ОЧИ (октановое число по исследовательскому методу). А вот у МТБЭ октановое число смешения доходит до 135 ОЧИ, в зависимости от углеводородного состава бензина, к которому добавляется МТБЭ.
Метанол СНЗОН и этанол С2Н5ОН прекрасно растворяются в бензине, имеют неплохие октановые числа смешения, но растворимы и в воде. А поскольку в товарных бензинах всегда есть вода, то спирт будет переходить в водную фазу и с ней отслаиваться. В резервуарах при хранении он окажется внизу. Чтобы расслоения не происходило, требуется добавка гомогенизатора, например, изобутилового спирта С4Н9ОН. В результате потребуются дополнительные затраты. С МТБЭ этой проблемы нет, так как он растворим только в бензине и в водную фазу не переходит.
Низшие спирты имеют значительно более низкую, чем бензин, теплоту сгорания. Это значит, что запас топлива в баке автомобиля должен быть увеличен, либо чаще надо тратить время на заправку. МТБЭ имеет равную с бензином топливную характеристику. Мало того, наличие в нем кислорода существенно улучшает процесс сгорания топлива в цилиндрах, повышая экономичность двигателя и снижая содержание в выхлопе продуктов неполного сгорания.
При использовании МТБЭ сокращается расход нефти на производство заданного количества товарного бензина, а также достигается её заметная экономия благодаря смягчению требований к октановой характеристике традиционных углеводородных компонентов бензина.
Технология производства МТБЭ чрезвычайно проста. Его получают в одну стадию, присоединяя метиловый спирт СНЗОН к изобутилену (2-метилпропену) С4Н8. При этом не требуется ни высоких температур, ни высоких давлений. Реакцию осуществляют на специальном катализаторе (чаще всего это ионообменные смолы) с высокой селективностью и почти полной конверсией за проход. Более того, в качестве сырья, чаще всего, используют не чистый изобутилен, а фракцию С4 каталитического крекинга, в которой кроме изобутилена присутствуют и н-бутилены (1- и 2-бутены) С4Н8. Селективность образования МТБЭ такова, что из смеси углеводородов в реакцию вступает только изобутилен. Тем самым синтез МТБЭ одновременно служит и процессом разделения фракции С4. Не прореагировавшие н-бутилены служат наряду с МТБЭ товарной продукцией установки.
Первые опытные партии МТБЭ появились в Италии в 1973 году. Подсчитано, что наиболее экономично добавлять в бензин 5-12% МТБЭ.
studfiles.net
Производство МТБЭ алкилированим метанола изобутиленом
Роль кинетики и катализа в выборе условий процесса
Для обеспечения высокой производительности катализатора, с одной стороны, и высокой степени превращения исходных реагентов в состоянии близком к равновесному, с другой, необходимо разработать и строго поддерживать температурный режим работы реактора. На расчет оптимального температурного режима работы реактора определяющее влияние оказывает большое количество выделяемого при синтезе эфира тепла (10 ккал/моль) наряду с кинетическими и термодинамическими закономерностями протекания реакции.
Равновесное состояние любой обратимой реакции, в том числе и синтеза МТБЭ, характеризует наивысшую степень превращения исходных реагентов при различных условиях проведения процесса (содержание изобутилена в исходной С4-фракции; мольное отношение метанол/изобутилен, температура).
Для определения состава реакционной массы в состоянии близком равновесному, а также содержания исходных реагентов в отработанной С4-фракции и товарном МТБЭ, следует знать значения констант равновесия в интересуемом интервале температур.
Известно, что при одной и той же температуре концентрационная константа равновесия практически не зависит от мольного отношения метанол/изобутилен в интервале от 0,8:1 до 1,1:1. Показано, что  температурную зависимость концентрационной константы равновесия можно выразить уравнением Вант-Гоффа:
температурную зависимость концентрационной константы равновесия можно выразить уравнением Вант-Гоффа:
Kс=K0*exp(-ΔH/RT),
где Кс - концентрационная константа равновесия, л/моль;
К0 - предэкспоненциальный множитель;
ΔН--энтальпия реакции, Дж/моль;
R - универсальная газовая постоянная, равная 8,31441 Дж/моль*град.
Вычислены параметры уравнения и получена следующая зависимость концентрационной константы равновесия от температуры:
Кс=ехр[-12,824 + 5854,36/(t+273)]
Равновесный состав реакционной смеси рассчитывали по известным константам равновесия реакции синтеза МТБЭ:

где С/эф, С/из., С/м. - равновесные концентрации МТБЭ, изобутилена иметанола, соответственно, моль/л.
При известных концентрации изобутилена в исходной С4-фракции имольном отношении метанол/изобутилен, а также высокой селективности превращения исходных реагентов в конечный продукт (что имеет место при синтезе МТБЭ) можно записать константу равновесия в следующем виде:

где С0из и С0м. - концентрация изобутилена и метанола в исходной смеси,соответственно, моль/л;
(С0из-С/из) - равновесная концентрация МТБЭ, моль/л;
(С0м-С0из+С/из) - равновесная концентрация метанола, моль/л
Использование С4-фракции с содержанием изобутилена 18 % масс, позволяет проводить процесс синтеза МТБЭ при мольном избытке метанола. Расчеты равновесного состояния, проведенные для С4-фракций с содержанием 18 % масс, изобутилена, показали, что мольный избыток метанола можно поддерживать равным 1,075:1. Следует отметить, что увеличение мольного избытка метанола ведет к увеличению степени превращения изобутилена, однако, в не очень высокой степени. Для исходной С4-фракции с содержанием изобутилена 18 % масс, увеличение мольного избытка метанола от 1 до 1,075 повышает степень превращения от 92,77 до 95,55 % при 60°С, то есть менее, чем на 3 %. Более сильное влияние на конверсию исходных реагентов оказывает температура. При мольном избытке метанола 1,075 снижение температуры от 90 до 50°С повышает степень превращения от 87,95 до 97,07 % (более, чем на 9 %). Поэтому температуру лучше всего поддерживать ниже 70°С.
studfiles.net
трет-Бутилметиловый эфир — Википедия РУ
Мети́л-трет-бути́ловый эфи́р (трет-бутилметиловый эфир, 2-метил-2-метоксипропан, МТБЭ) — химическое вещество с химической формулой СН3—O—C(СН3)3, один из важнейших представителей простых эфиров.
Физические свойства
- Температура кипения 54—55 °C при 764 мм рт. ст.
- d204 0,7578; n20D 1,37566.
- Растворимость в воде — низкая.
- Азеотропные смеси с водой (52,6 °C) и метанолом (51,3 °C).
Плотность при 20 °С: 0,7405.
Коэффициент преломления при 20 °С: 1,3690.
Удельная теплоёмкость: 2,1 кДж/кг·К.
Теплота парообразования: 332,5 кДж/кг.
Растворим в этаноле, диэтиловом эфире, плохо — в воде (4,6 % при 20 °С).
Образует азеотропные смеси:
- с метанолом (МТБЭ — 85 % мас.), температура кипения — 52 °С;
- с водой (МТБЭ — 96 % мас.), температура кипения — 52,6 °С.
При нагревании выше 460С, а также при нагревании с катализатором разлагается на метанол и изобутилен.
Пероксидных соединений не образует.
Температура вспышки: минус 33 °С.
Температура самовоспламенения: 443 °С.
Концентрационные пределы воспламенения: 1,4—10 %.
Предельно допустимая концентрация в воздухе рабочей зоны: 100 мг/м³.
Предельно допустимая концентрация в атмосфере населенных мест: 0,1 мг/м³.
Хорошо растворяется в бензине в любых соотношениях, практически не растворяется в воде, не ядовит.
Топливные характеристики:
- октановое число по исследовательскому методу — 115—135.
- октановое число по моторному методу — 100—101.
Производство
Получается при взаимодействии метанола с изобутиленом в присутствии кислых катализаторов (например, ионообменных смол). 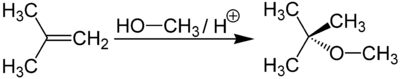
Синтез МТБЭ в присутствии кислотного катализатора осуществляется путём алкилирования метанола изобутиленом по обратимой реакции: iС4Н8 + СН3ОН ↔ СН3ОС(СН3)3
Реакция протекает в жидкой фазе с выделением тепла. Тепловой эффект реакции составляет 41,8 кДж/моль. Равновесие реакции смещается вправо при повышении давления и снижении температуры. Процесс синтеза МТБЭ ведут при температуре от 50 до 100 °С и давлении, необходимом для поддержания реагентов в жидкой фазе. При правильно подобранных режимах побочные реакции можно практически полностью подавить, обеспечив селективность процесса 98 % и выше.
На 2004 год производство в США составляло половину мирового выпуска, на 1999 год произведено более 8,5 млн т. во время использования его в качестве добавки к топливу. Однако (из-за утечек из подземных хранилищ на территории США) МТБЭ был запрещён различными инстанциями, и с конца 2006 года его производство начало сокращаться. Вообще в США в конце 90-х гг. началась мощная кампания за запрет использования МТБЭ в составе автомобильных бензинов. Особо интенсивно эта кампания проводилась в штате Калифорния, в котором запрет на применение МТБЭ предполагалось ввести в 2003 г., однако позднее эта дата была перенесена на январь 2004 г. При этом сохраняется требование о содержании кислорода в автомобильном бензине на уровне 2 %, что привело к росту потребления этанола с 13,9 тыс. т/сутки в 2000 г до 30,8 тыс. т/сутки в 2005 и 2010 гг., соответственно[1].
Во многих штатах загрязнение водоносного горизонта МТБЭ вызывает серьёзные опасения. Большинство поставщиков бензина отказались от его использования в пользу этил-трет-бутилового эфира в связи с налоговыми льготами производителям.
В Евросоюзе на 2003 год произведено около 2,6 млн т, крупнейшее производство размещено в Роттердаме (в 2004 году произведено более 1 млн т. — 90 % производства Голландии), в Бельгии производство составляет около 387 тыс. т. в год. Динамика производства в Европе повторяет ситуацию в США.
В целом мировое производство и применение эфира на 2006 год продолжает расти и имеет значительные перспективы.
Применение
Применяется в качестве добавки к моторным топливам, повышающей октановое число бензинов (антидетонатор). Максимально допустимая законодательно объемная доля МТБЭ в бензинах Европейского союза — 15 %, в Польше — 5 %, в России — 15 %[2].
МТБЭ широко применяется в производстве высокооктановых бензинов, при этом выступает как нетоксичный, но менее теплотворный высокооктановый компонент и как оксигенат (носитель кислорода), способствующий более полному сгоранию топлива и предотвращению коррозии металлов. Мировое потребление МТБЭ находится на уровне 20—22 млн т в год.
Подготовка сырья МТБЭ
Основным сырьём МТБЭ на нефтеперерабатывающих заводах является бутан-бутиленовая фракция (ББФ) после каталитического крекинга, которую необходимо очищать от сернистых соединений. Сернистые соединения в ББФ представлены в основном метил- и этилмеркаптаном, очистка от которых осуществляется их щелочной экстракцией и последующим окислением тиолятов с применением гомогенных или гетерогенных катализаторов в присутствии кислорода воздуха с получением дисульфидного масла.
Происшествия
7 апреля 2018 в общине Мянтюхарью[d] (Финляндия) в результате схода с рельсов из российской железнодорожной цистерны в почву вылилось около 35 тысяч литров метилтретбутилового эфира, в результате был нанесён большой ущерб экологии[3].
Примечания
Литература
- Химический энциклопедический словарь. — М.: Советская энциклопедия, 1983.
- Справочник. Пожаровзрывоопасность веществ и материалов и средства их тушения. — М: Химия, 1990.
- Ахмадуллина А. Г. и др. Гетерогенно-каталитическая демеркаптанизация легкого углеводородного сырья. // Нефтепереработка и нефтехимия, № 2, 1994, с. 39.
Ссылки
http-wikipediya.ru



















