Изомеры гептана: общая характеристика и применение. Гептановый эфир
Гептановая кислота, эфиры - Справочник химика 21
Известно много методов окисления. Однако большое значение этой реакции побудило исследовать применимость межфазных катализаторов в реакции окисления в тех случаях, когда органический субстрат нерастворим в водных средах, а окислитель в свою очередь нерастворим или плохо растворим в органических растворителях. Принципиальная возможность использования межфазных катализаторов для окисления нерастворимых в воде субстратов в апротонном растворителе была показана еще в 1965 г. [388]. В качестве катализатора была использована четвертичная арсониевая соль — метилтрифенил-арсонийхлорид при этом происходил обмен хлор-аниона на анион перманганата из водного раствора перманганата калия и перенос этого аниона в хлороформенный раствор субстрата (октен-1, пропанолы-1 и -2, гептанол-4 и др.), где и проходило окисление. В таких условиях пропанол-2, например, на 100% превращался в ацетон. грет-Бутиловый спирт, толуол, этилацетат, диэтиловый эфир, ацетон или дипропилкетон не окислялись. Позже было установлено, что октен-1 и децен-1 превращаются соответственно в гептановую кислоту (количественный выход) и нонановую кислоту (выход 91%) при окислении нейт- [c.136] На рис. 32 приведены результаты, полученные для четырех фракций полиизобутилена в изооктане (хороший растворитель) и в этиловом эфире -гептановой кислоты (тета-растворитель при 34°) [131]. Следует отметить, что для наиболее высокомолекулярных фракций при неидеальных условиях измерения могут дать ошибку до 25%. [c.63]Гептиловый спирт (гептан-10-ол), С Н О, мм. 116,21, бесцветная жидкость с пряным, жирным, фруктово-цветочным запахом, / ип 176,3 °С, пл 34,6 °С, 1,42351, 0,8240, содержится в сивушном масле. Гептиловый спирт выделяют из сивушного масла, синтезируют его оксосинтезом из а -гексена, каталитическим гидрированием гепта-наля или гидрогенолизом сложных эфиров н-гептановой кислоты [c.28]
Этилирование [37]. Пробы определенного объема (1 мл) этанольного экстракта растительных тканей, полученных по методу, изложенному в разделе Б,1,а,3, высушивают на воздухе в пробирке размером 15 х X о, 15 см и обрабатывают 4-процентным (по объему) раствором концентрированной серной кислоты в абсолютном этаноле (5 мл). Пробирку закрывают стеклянной пробкой и содержимое кипятят с обратным холодильником в течение 1 час при 90°. Затем смесь концентрируют до объема 2 жл и разбавляют дистиллированной водой (4 мл). Для извлечения эфиров реакционную смесь встряхивают с н-гептаном (0,5—1 мл). Часто в процессе экстракции на линии раздела гептанового и водного слоев образуется черный осадок, который затрудняет получение прозрачных проб гептанового раствора. н-Гептановый слой осветляют, переводя всю смесь в закрытую пробкой пробирку размером 100 х 6 мм, и центрифугируют в течение 15 мин при 3000 g. Известный объем верхнего слоя вводят в хроматограф. [c.545]
АЛЛИЛЭНАНТАТ (аллиловый эфир гептановой кислоты), 10h28O2, мол.м. 170,24 СНз(СН2)5СООСН2СН=СН2 бесцветная жидкость с нежным фруктовым запахом 210 С (760 мм рт.ст.), 0,890, 1,429 растворим в этаноле и органических растворителях, нерастворим в воде. [c.32]
Для разбавленных растворов полиизобутилена в изооктане было найдено dnId = = 1,42-10 (г/этиловом эфире и-гептановой кислоты та же величина, измеренная на дифференциальном рефрактометре Феникс при 34° составляет 1,04-10 (г/Эл) . Для определения парциального удельного объема измеряли плотность разбавленных растворов полиизобутилена в этиловом эфире н-гепта-новой кислоты при 34° с помощью калиброванного пикнометра и полумикровесов. Парциальный удельный объем, вычисленный из этих данных по методу отрезков, описанному Люисом и Рендаллом [129], равен 1,106 см 1г. Плотность растворителя при этой температуре составляла 0,8563 г см . Для растворов полиизобутилена в изооктане при 25° необходимая для расчетов величина (1 — V q) равна 0,272. [c.65]
С2Не)з 0 Метиловый эфир 2, 2-диметил-гептановой кислоты 83 38 [c.301]
Сульфоокпсление замещенных парафинов изучено мало. Уксусная, гексановая и гептановая кислоты подвергаются сульфоокисле-нию в присутствии различных катализаторов [1306]. Последние две кпслоты дают хорошие выходы сульфопродуктов прп сульфоокислении уксусной кислоты выход составляет лишь 10—15%. Этот результат показывает, что сульфоокисление в а-положение проходит легче, чем сульфохлорирование, так как уксусная кислота сульфохлорированию не подвергается (см. стр. 124). В патентах сообщается о сульфоокислении хлорированных алканов и цхткло-алканов [92, 142], кислот и нитрилов [93], сложных и простых эфиров [94, 143] и спиртов [94]. [c.127]
Путем крекинга алкилрицинолеата был получен гептаналь, который можно перевести в гептановую кислоту. Глицериновый эфир чистой гентановой кислоты (т. кип. 200° С при 1 мм рт. ст.) является особенно хорошим пластификатором поливинилхлорида. [c.628]
При алкилировании изобутана пропиленом при 30° в присутствии 98 %-ной серной кислоты [29] была получена гептановая фракция с выходом 62—70%, состоявшая приблизительно из 85% 2,3-диметилпентана и 15% 2,4-диметилпентана, триметилпентанов было выделено 12% пропан не обнаружен. Алкилирование пе шло при использовании 97 %-ной серной кислоты при температуре 20°. Вместо алкилатов при 20° получались моноизопропиловый эфир серной кислоты и смешанные полимеры (т. е. олефины и парафины). Алкилирование идет при 20° лишь при применении 101,7%-ной кислоты. Выход алкилата составлял при этом 215% вес., 90% алкилата выкипало выше 150°. [c.322]
Та же кристаллизующаяся на холоду третичная гидроперекись этил-циклогоксана содернгалась (около 50%) в гидроперекисном продукте, выделенном, как описано выше, при помощи концентрированного раствора щелочи в виде гидроперекисной натриевой соли. Для извлечения гидроперекиси эта соль разлагалась на холоду избытком 5 %-ной серной кислоты. Выделившийся верхний слой растворялся в четырехкратном обт.еме н.гептана и вновь обрабатывался на этот раз половинным от требуемого по расчету количеством 30/6-пого раствора едкого натра. После удаления выпавшей соли гептановый фильтрат 13 раз обрабатывался 7%-ным водным раствором едкого натра. Последние 10 вытяжек соединялись и экстрагировались эфиром. Выделенная из эфирных экстрактов описанным выше методом третичная гидроперекись этилциклогексана обладала теми же константами, что и изолированная из остатка после первого получения соли порция ее и объединялась вместе с нею. [c.138]
Пропионовый, масляный, изомасляный, валериановый и н-гептановый альдегиды подвергались полимеризации при высоком давлении с образованием растворимых в органических растворителях полиоксиалкилиденов, имеющих концевые гидроксильные группы [62]. Полимеры изомасляного и -гептанового альдегидов частично кристалличны остальные аморфны. Предполагая присутствие неизбежных примесей карбоновых кислот, считают, что полимеризация протекает по катионному механизму. В присутствии действительно катионных реагентов (фтористый бор, бромистый алюминий, этилалюминийдихлорид) при —78° в этиловом эфире образуются изотактические полимеры пропионового, масляного, изомасляного и изо-валерианового альдегидов [2]. [c.396]
В работе [39] приведены результаты исследования низкомолекулярных алифатических кислот одной из калифорнийских нефтей. В качестве исходного материала авторы использовали первые 180 из 720 четко фракционированных метиловых эфиров кислот (см. рис. 13). Из нескольких фракций эфиров, имевших низкие показатели преломления и практически постоянные температуры кипения, было получено омылением и идентифицировано десять кислот 2- и 3-метилпентановые, гексановая, 2-, 3-, 4- и 5-ме-тилгексановые, гептановая, октановая и нонановая. Идентификацию осуществляли по составу и температурам плавления одного или нескольких производных кислоты в смешанных пробах с соответствующими производными синтетических кислот. В результате работ [31] и [39] были идентифицированы девять алифатических кислот нормального строения (С1-С9) и восемь изомерных 2-, 3-, 4- и 5-метилзамещенных кислот. [c.59]
В работе [48] идентифицированы методом газожидкостной хроматографии алифатические кислоты нормального строения от гептановой до пентакозановой в кислотах, выделенных из дизельного топлива смеси (10 1) ромашкинской и мухановской нефтей. Из исходных кислот, тщательно очищенных от нейтральных соединений и фенолов, была получена смесь алифатических кислот в виде аддуктов с карбамидом. Выделенные из аддуктов кислоты составляли 20% от исходных кислот. После дополнительной очистки кислоты перегоняли в вакууме и превращали в метиловые эфиры. Четыре полученные фракции и смесь эфиров подвергали хроматографированию в колонках с силоксановым эластомером Е-301 и апьезоном М. [c.61]
chem21.info
Свойства спиртов - химические свойства, превращения. Эфиры и сложные эфиры.
Про то, что такое спирты, я уже писал чуть раньше. Теперь подробнее об их свойствах. В первую очередь спирты в некотором отношении родственны воде, т.к. так же, как и вода, содержат OH- группу. Поэтому спирты реагируют с щелочными металлами с выделением водорода и образованием соединения, называющимся алкоголятом. Для метилового спирта оно будет называться метилатом, для этилового - этилатом, и так далее.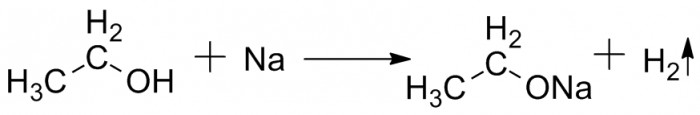 Реакции металлов со спиртами (на примере этанола) Реакция идёт обычно более спокойно, чем с водой (собственно, так и рекомендуют уничтожать остатки натрия или калия – заливая их спиртом), и алкоголяты являются более сильными основаниями, чем гидроксиды. Поэтому при добавлении воды (или при её наличии в спирте изначально) произойдёт реакция обмена с образованием соответствующего гидроксида и исходного спирта. В некоторых случаях эта реакция используется для осушения спиртов. Алкоголяты щелочных металлов используются в органической химии как катализаторы или сильные основания (рекордсмен - трет-бутилат калия). Изопропилат алюминия является восстановителем. Под действием кислоты и/или водоотнимающих реагентов две молекулы спирта могут соединиться с выделением молекулы воды. Получится вещество, имеющее кислородный "мостик". Такие вещества называются эфирами. Например, из этилового спирта получается диэтиловый эфир (это тот, который называют просто "эфиром"). Эфиры испаряются легче, чем соответствующие спирты, и очень хорошо горят - поэтому диэтиловый эфир используется в смесях для запуска двигателей на морозе, а метил-трет-бутиловый эфир используется как присадка к бензину, повышающая его октановое число.
Реакции металлов со спиртами (на примере этанола) Реакция идёт обычно более спокойно, чем с водой (собственно, так и рекомендуют уничтожать остатки натрия или калия – заливая их спиртом), и алкоголяты являются более сильными основаниями, чем гидроксиды. Поэтому при добавлении воды (или при её наличии в спирте изначально) произойдёт реакция обмена с образованием соответствующего гидроксида и исходного спирта. В некоторых случаях эта реакция используется для осушения спиртов. Алкоголяты щелочных металлов используются в органической химии как катализаторы или сильные основания (рекордсмен - трет-бутилат калия). Изопропилат алюминия является восстановителем. Под действием кислоты и/или водоотнимающих реагентов две молекулы спирта могут соединиться с выделением молекулы воды. Получится вещество, имеющее кислородный "мостик". Такие вещества называются эфирами. Например, из этилового спирта получается диэтиловый эфир (это тот, который называют просто "эфиром"). Эфиры испаряются легче, чем соответствующие спирты, и очень хорошо горят - поэтому диэтиловый эфир используется в смесях для запуска двигателей на морозе, а метил-трет-бутиловый эфир используется как присадка к бензину, повышающая его октановое число. 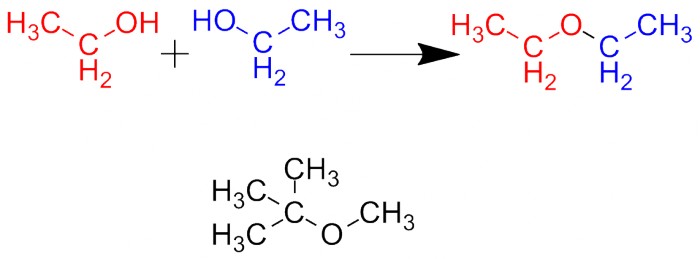 Реакция получения простых эфиров. Формула диэтилового и метил-трет-бутилового эфира. Карбоновые кислоты тоже имеют ОН-группу, и аналогичная реакция может пройти между кислотой и спиртом. При этом образуется соединение, называющееся сложным эфиром. Изображённое на рисунке вещество называется этиловым эфиром уксусной кислоты. Все другие сложные эфиры именуются аналогично, но иногда такие называния сокращают, используя названия фрагмента кислоты: например, этилацетат.
Реакция получения простых эфиров. Формула диэтилового и метил-трет-бутилового эфира. Карбоновые кислоты тоже имеют ОН-группу, и аналогичная реакция может пройти между кислотой и спиртом. При этом образуется соединение, называющееся сложным эфиром. Изображённое на рисунке вещество называется этиловым эфиром уксусной кислоты. Все другие сложные эфиры именуются аналогично, но иногда такие называния сокращают, используя названия фрагмента кислоты: например, этилацетат. 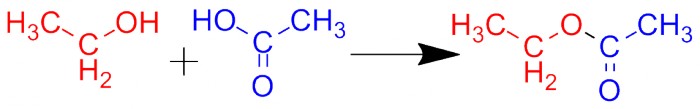 Реакция получения сложных эфиров на примере этилового эфира уксусной кислоты. Сложные эфиры в небольших концентрациях пахнут приятно - запах напоминает запах фруктов. Это и неудивительно, поскольку это и есть те самые вещества, которыми и пахнут фрукты. Например, этиловый эфир масляной кислоты пахнет ананасами, амиловый эфир уксусной кислоты пахнет бананами, а этиловый эфир гептановой кислоты пахнет виноградом. Считается, что этилацетат тоже пахнет фруктами, но большинство людей скажет, что его запах - это запах лака для ногтей. Всё это нетрудно проверить - реакция получения сложных эфиров описана в любом лабораторном практикуме и легко воспроизводится даже людьми, не имеющими большого опыта в синтезе.Жиры являются сложными эфирами глицерина и т.н. "жирных" (содержащих 12-20 атомов углерода) карбоновых кислот. В жёстких условиях (например, нагревание с концентрированной серной кислотой) спирты могут дегидратироваться с отщеплением молекулы воды и образованием ненасыщенного (содержащего двойную связь) соединения. Этанол дегидратируется в этилен, изопропанол - в пропилен. Третичные спирты дегидратируются проще всего - под действием каталитических количеств любой сильной кислоты.
Реакция получения сложных эфиров на примере этилового эфира уксусной кислоты. Сложные эфиры в небольших концентрациях пахнут приятно - запах напоминает запах фруктов. Это и неудивительно, поскольку это и есть те самые вещества, которыми и пахнут фрукты. Например, этиловый эфир масляной кислоты пахнет ананасами, амиловый эфир уксусной кислоты пахнет бананами, а этиловый эфир гептановой кислоты пахнет виноградом. Считается, что этилацетат тоже пахнет фруктами, но большинство людей скажет, что его запах - это запах лака для ногтей. Всё это нетрудно проверить - реакция получения сложных эфиров описана в любом лабораторном практикуме и легко воспроизводится даже людьми, не имеющими большого опыта в синтезе.Жиры являются сложными эфирами глицерина и т.н. "жирных" (содержащих 12-20 атомов углерода) карбоновых кислот. В жёстких условиях (например, нагревание с концентрированной серной кислотой) спирты могут дегидратироваться с отщеплением молекулы воды и образованием ненасыщенного (содержащего двойную связь) соединения. Этанол дегидратируется в этилен, изопропанол - в пропилен. Третичные спирты дегидратируются проще всего - под действием каталитических количеств любой сильной кислоты. 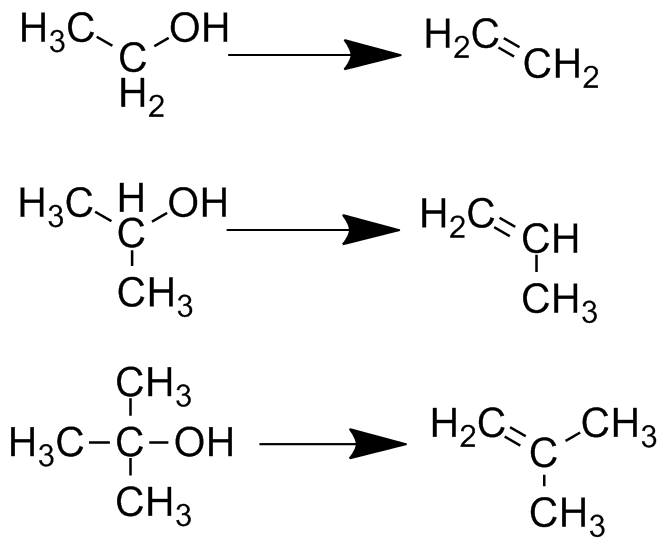 Реакция дегидратации спиртов Под действием, например, бромоводорода ОН-группа может отщепиться и на её место встанет атом брома. Реакция обратима (так же, как и реакция этерификации) и представляет собой способ получения алкилбромидов. Поскольку все вышеописанные реакции (образование простого эфира, дегидратация и замена гидроксильной группы на галоген) проходят в сходных условиях, все они являются конкурирующими и ответственны за образование побочных продуктов.
Реакция дегидратации спиртов Под действием, например, бромоводорода ОН-группа может отщепиться и на её место встанет атом брома. Реакция обратима (так же, как и реакция этерификации) и представляет собой способ получения алкилбромидов. Поскольку все вышеописанные реакции (образование простого эфира, дегидратация и замена гидроксильной группы на галоген) проходят в сходных условиях, все они являются конкурирующими и ответственны за образование побочных продуктов. 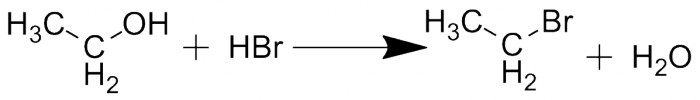 Получение алкилбромидов из соответствующих спиртов Спирты также способны окисляться. В случае с первичными спиртами продуктом будет альдегид и соответствующая карбоновая кислота. Вторичные спирты не могут образовывать кислоты (вернее, могут, но в жёстких условиях и с разрывом C-C связи), поэтому реакция останавливается на веществе, которое называется кетоном. Простейший пример - это ацетон (диметилкетон), получающийся окислением изопропанола. Третичные спирты окисляться не способны. Окислителем может являться, например, перманганат калия (марганцовка), дихромат калия или триоксид хрома, двуокись марганца, а также кислород воздуха. Также окисление спиртов способны производить аэробные бактерии, получающие при этом энергию. В организме этанол превращается ферментами печени сначала в ацетальдегид (который токсичен), а затем в уксусную кислоту (нетоксичную в разумных количествах).
Получение алкилбромидов из соответствующих спиртов Спирты также способны окисляться. В случае с первичными спиртами продуктом будет альдегид и соответствующая карбоновая кислота. Вторичные спирты не могут образовывать кислоты (вернее, могут, но в жёстких условиях и с разрывом C-C связи), поэтому реакция останавливается на веществе, которое называется кетоном. Простейший пример - это ацетон (диметилкетон), получающийся окислением изопропанола. Третичные спирты окисляться не способны. Окислителем может являться, например, перманганат калия (марганцовка), дихромат калия или триоксид хрома, двуокись марганца, а также кислород воздуха. Также окисление спиртов способны производить аэробные бактерии, получающие при этом энергию. В организме этанол превращается ферментами печени сначала в ацетальдегид (который токсичен), а затем в уксусную кислоту (нетоксичную в разумных количествах). 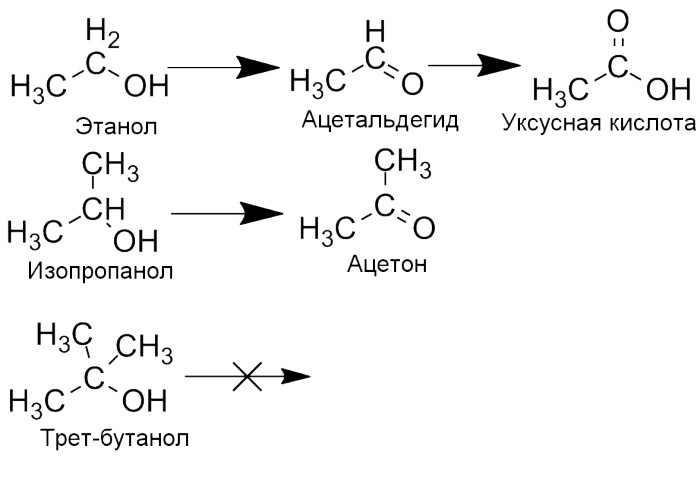 Реакция окисления спиртов Применения изопропилата натрия: https://www.alfa.com/ru/catalog/089446/ Восстановление изопропилатом алюминия называется восстановлением по Меервейну-Понндорфу-Верли (Meerwein–Ponndorf–Verley reduction). Пример можно найти, например, в книге «Лабораторные работы в органическом практикуме» Агрономова, с.131 и 133. Методику получения сложных эфиров можно найти в том же Агрономове (стр. 78)
Реакция окисления спиртов Применения изопропилата натрия: https://www.alfa.com/ru/catalog/089446/ Восстановление изопропилатом алюминия называется восстановлением по Меервейну-Понндорфу-Верли (Meerwein–Ponndorf–Verley reduction). Пример можно найти, например, в книге «Лабораторные работы в органическом практикуме» Агрономова, с.131 и 133. Методику получения сложных эфиров можно найти в том же Агрономове (стр. 78) chemiday.com
Гептан
Парафины нефтяные и синтетические. Синтетический растворитель типа уайт-спирита.[ ...]
Определению не мешают: гексан, гептан, бензол, толуол, ксилол, спирты, кислоты, эфиры, хлороформ.[ ...]
Экстракционное концентрирование к-гептаном применяют для определения С12—С36 углеводородов. Последующее выпаривание гептанового экстракта в токе азота для увеличения чувствительности определения (от 25 мл до 3 мл) вызывало ощутимые потери углеводородов С 12 С24 [63]. Описано выделение и идентификация высокомолекулярных углеводородов из морских вод, источником которых являются микро- и макропланктон. Концентрирование и фракционирование включают экстракцию хлороформом, выделение неомыляемой фракции путем химических обработок, предварительное ее разделение методом тонкослойной хроматографии. Идентификация индивидуальных углеводородов различных рядов в выделенных фракциях осуществляется методами газовой хроматографии и масс-спектрометрии [65].[ ...]
В таких растворителях, как изооктан, гексан, гептан, пентан с величиной Log Р > 3.0, наблюдалась высокая конверсия субстрата, в то время как в хлороформе, бензоле и толуоле конверсия гептанола-2 снижалась, а в растворителях с величиной Log Р [ ...]
Предельные углеводороды (бутан, пентан, гексан, гептан, октан) среди органических соединений наиболее инертны. При попадании в организм человека оказывают наркотическое действие, вызывают потерю координации движения и расслабление организма. С ростом числа атомов углерода в предельных углеводородах отрицательное действие на организм человека усиливается.[ ...]
Определение в крови и тканях. Экстрагирование С. гептаном и спектрофотометрическое определение его в ультрафиолетовой области спектра при длине волны 245 ммк (Русин и Филов).[ ...]
Из сточной воды а—метилс-тирол экстрагируется п-гептаном экстракт высушивается от влапГ хлористым кальцием и вкалывается на хроматограф. Для количественной оценки хро- » матограмм был выведен поправочный коэффициент для а — ме-тилстирол по искусственным смесям.[ ...]
Сточные воды коксохимических предприятий Бензол, н-гептан, толуол, пиридин, пропилбензол, псевдокумол, ксилол, нафталин, а-метилнафта-лин, хинолин, антрацен, фенол и др.[ ...]
Реактивы и материалы.[ ...]
Отбор проб с концентрированием в поглотительную жидкость (гептан + этанол 5:1) для образования этилового эфира перметриновой кислоты.[ ...]
Определению не мешают ксилолы и этилбензол, а мешают гексан, гептан и ацетон.[ ...]
Готовят в гептане с содержанием от 0,5 до 20 мкг/мл (см. с. 32).[ ...]
Физические свойства. Тяжелые жидкости. Тетрахлорпентан, тетрахлор-гептан практически не растворимы в воде; растворимы в спирте и эфире.[ ...]
Стандартный раствор № I с концентрацией 1 мг/мл готовят взвешиванием в гептане в мерной колбе, вместимостью 50 мл.[ ...]
Отбор проб производится в жидкостные поглотители с концентрированием в гептан.[ ...]
В сосновых скипидарах найдено два парафиновых углеводорода. Нормальный гептан (C7Hi6), естественная составная часть бензина, составляет 95% скипидаров из P. jeffreyi и P. sabiniana. Он найден также в P. coulteri и P. torreyana. Все эти сосны растут на западе Соединенных Штатов. Нормальный ундекан (СцНг4), керосиноподобное парафиновое вещество, встречается в скипидаре из P. coulteri в количестве до 10% и возможно — в небольших количествах в трех других соснах: Р. excelsa, Р. montícola и Р. torreyana. Парафиновый углеводород, о присутствии которого в P. lamber-tiana сообщил Шоргер [159], также является вероятно л-ундеканом.[ ...]
Спурлин [ 1801 фракционировал нитроцеллюлозу, осаждая ее из раствора ацетона гептаном. В результате повторного фракционирования осажденного материала было выделено 66 различных фракций. У некоторых фракций удельная вязкость была в три раза больше, чем у исходного материала, а у других составляла lj3 исходной вязкости. Пленки, приготовленные из различных фракций и их смесей, испытывались па сопротивление излому. Имеется определенный предел вязкости, ниже которого пленки не выдерживали испытания на излом. Пленки, приготовленные из отдельных фракций, обладали большим сопротивлением излому, чем те, которые были приготовлены из смесей фракций с той же вязкостью.[ ...]
Октановое число численно равно процентному содержанию изооктана в эталонной смеси с н.гептаном, которая по детонационной стойкости в условиях стандартного одноцилиндрового двигателя эквивалентна испытуемому образцу.[ ...]
Гептановые растворы НП (образцы, отобранные без применения растворителей, растворяют в гептане; концентрация раствора должна быть около 10 мг/мл), высушивают безводным сернокислым натрием, переносят в перегонный аппарат. В горловину насадки вставляют трубку с оттянутым в капилляр концом, касающимся дна колбы, подсоединяют трубку через редуктор к баллону с азотом, гелием, аргоном или углекислым газом. Вместо баллона допускается пользоваться резиновой камерой по ТУ 38—10—6179, наполненной одним из указанных газов. Между редуктором (или камерой) и трубкой устанавливают кран, U-образную трубку с активным углем и склянку Тищенко с нелетучей жидкостью, например с глицерином. Под куб подставляют баню с глицерином или силиконовой жидкостью; температуру в бане, нагреваемой электроплиткой, рекомендуется поддерживать посредством электрореле и контактного термометра. Отгонку гептана ведут в токе газа со скоростью около 5 мл/мин при температуре бани 120вС. Кубовый остаток упаривают в фарфоровой чашке на водяной бане при 80—90 С в течение 10 мин. В итоге этой процедуры получают термообработанный НП.[ ...]
Шеррер и Рауз 1184] фракционировали растворы нитрата целлюлозы в этилацетате, производя осаждение гептаном.[ ...]
Стандартный раствор додецилбензена № 1 с концентрацией 1000 мкг/мл готовят растворением 100 мг додецилбензена в гептане в мерной колбе вместимостью 100 мл.[ ...]
Стандартный раствор N° 2 готовят в мерной колбе, объемом 100 мл, с притертой пробкой разбавлением 10 мл раствора № 1 гептаном до метки.[ ...]
Жидкая фаза ПМФС (неполярная жидкость) на кирпиче 60—80 меш. хорошо разделяла смесь легких углеводородов (гек-сан, гептан), а также ароматических (бензол, толуол) при оптимуме температуры + 50° С.[ ...]
Большую часть легкой фракции составляют метановые углеводороды с числом углеродных атомов С5-Сп (пентан, гексан, гептан, октан, ионан, декан, ундекан). Нормальные (неразветвленные) алканы составляют в этой фракции 50-70% [150, 228]. Эти углеводороды легко проникают в клетки организмов через мембраны, дезорганизуют цитоплазматические органоиды.[ ...]
Меры предупреждения. Изъятие Б. из рецептуры растворителей. Замена его алициклическими и другими углеводородами (гептан, циклогексан, уайт-спирит) или ароматическими углеводородами (толуол, ксилол, изопропилбен-зол): применение их не так опасно (тяжелые и смертельные отравления описывались редко), тем более, что они менее летучи. Контроль за рецептурой растворителей и разбавителей. Распоряжением Совета Министров СССР № 2168-р от 3 августа 1962 г. запрещено применение Б. в производстве эфироцеллюлозных лаков, эмалей и растворителей к ним с заменой его толуолом. См. также «Временные санитарные правила при работе с мастиками, красками, лаками, клеями и эмалями, для которых в качестве растворителя или разбавителя, применяется бензол», утвержд. ГСИ СССР 14 января 1957 г. за № 234—57, и «Извлечения из правил промышленной санитарии и техники безопасности при отпарке цистерн» [168].[ ...]
При полимеризации пропилена в качестве растворителей обычно применяют насыщенные углеводороды, например гек-сан, гептан, бензин и др. Растворители в процессе служат одновременно осадителями для образовавшегося полипропилена.[ ...]
| Растворимость асфальтенов в растворителях с различной плотностью энергии когезии при 25 °С. Растворители |  |
Стандартный раствор додецилбензена № 2 с концентрацией 250 мкг/мл готовят разбавлением 50 мл стандартного раствора № 1 гептаном до объема 250 мл в мерной колбе.[ ...]
Препарат расслаивается, поэтому перед употреблением его тщательно перемешивают; при работе опрыскиватель должен быть снабжен мешалкой.[ ...]
При приготовлении стандартных растворов исследуемых веществ в качестве растворителя могут быть использованы гептан и пентан. Пробу воздуха в испаритель прибора можно также вводить с использованием градуированной дозы, прилагаемой к хроматографу.[ ...]
Алканы - эмпирическая формула СпН2п+2. Агрегатное состояние С14 газы (метан, этан, пропан, бутан), С 515 - жидкости (пентан, гексан, гептан, октан и т. д.), свыше С15- твердые вещества. Слабо растворимы в воде и физиологических растворах, отличаются большой стойкостью и малой химической активностью.[ ...]
Исходный раствор сероуглерода для градуировки (с = 8,0 мг/см3). 800 мг сероуглерода вносят в колбу вместимостью 100 см , доводят до метки гептаном и тщательно перемешивают. Срок хранения раствора - не более 10 дней.[ ...]
Рабочий раствор нитробензола с содержанием 0,001 мг/см . 25 мм3 исходного раствора нитробензола вносят в мерную колбу вместимостью 25 см3, доводят объем до метки смесью 0,1 % пропанола-2 в гептане и тщательно перемешивают. Срок хранения - 4 дня.[ ...]
Качественное горение топлива в карбюраторном двигателе сопровождается невысоким числом детонаций. Критерием качества топлива является октановое число. Оно соответствует процентному содержанию изооктана (октановое число 100) в модельной смеси с нормальным гептаном (октановое число 0), которая показывает такое же число детонаций, что и исследуемый образец. Мощные двигатели работают с высокими степенями сжатия, а последние возможно достичь только при использовании высокооктанового бензина.[ ...]
Процесс очистки может осуществляться при больших нагрузках на катализаторы по водяному пару и органическим веществам: предельно допустимая нагрузка по водяному пару составляет 84 г/см3«ч (объемная скорость по пару 104000 ч- , глубина окисления 90,2-92,4 ) (опыт 3,4), по гептану - 720 мг/см3 (опыт 7).[ ...]
За рубежом для очистки сточных вод прачечных запатентован целый ряд приемов с применением жидких ионообменных реагентов. В частности, в США выдан патент 1 на применение ■четвертичных аммониевых оснований, не смешивающихся с водой, но растворяющихся в органических растворителях — изо-октане, керосине, бензине, гексане, октане, гептане и т. п. После ■обработки сточных вод растворитель, содержащий четвертичные аммониевые основания, отделяют от водной фазы и регенерируют или используют в качестве топлива. Для регенерации растворителя могут быть использованы растворы перхлоратов. Отношение объемов сточных вод и растворителя может колебаться от 1 : 1 до 500 000 : 1. Экстракция ПАВ может происходить при pH = 1-г 11 и температурах в интервале от точки замерзания до точки кипения растворителя.[ ...]
Из колбы, содержащей упаренный раствор пробы, отбирают микрошприцом 2 мкл раствора и вводят в испаритель хроматографа. Массу додецилбензена в пробе, взятой для хроматографирования, находят по градуировочному графику. При высокой концентрации додецилбензена (выходящей за пределы градуировочного графика) упаренный раствор количественно разбавляют гептаном (при этом степень разбавления рекомендуется определять исходя из масс, а не из объемов упаренного раствора и добавляемого гептана - для повышения точности анализа).[ ...]
В 1991 г. специалистами ОАО «Магистральные нефтепроводы Центральной Сибири» и сотрудниками Томского политехнического института (ТПИ) вводилась полимерная присадка «Виол» на конечном участке нефтепровода Александровское—Анжеро-Судженск с диаметром трубы 1220 мм и длиной 69 км [59]. Присадка «Виол» была получена по рецептуре ТПИ в Томском нефтехимическом комбинате и представляет собой 10%-й раствор в гептане сополимера альфа-алефинов.[ ...]
Реперные НП от возможных источников перед термообработкой дополнительно подвергают искусственному выветриванию. Процедура заключается в следующем. 1 —3 г НП помещают на поверхность природной, либо искусственной морской воды (30 г поваренной соли на 1 л дистиллированной воды), налитой доверху в эксикатор, включают направленные на образец источник УФ-излучения (ОРК-21), вентилятор и проводят выветривание в течение 4 ч. По окончании процедуры НП переносят с помощью чистого поролонового тампона, зажатого в пинцете, в склянку (колбу), растворяют в гептане и высушивают безводным сульфатом натрия.[ ...]
ru-ecology.info
Изомеры гептана: общая характеристика и применение
Алканы (парафины, предельные углеводороды) – биосоединения, состоящие только из атомов С и Н, в которых все атомы связаны простыми сигма-связями. Простейшим предельным углеводородом является метан. Каждый последующий углеводород этого ряда отличается от предыдущего на группу СН2. В указанном ряду соединений соседние члены отличаются друг от друга на гомологическую разность (СН2), подобные ряды называются гомологическими. Для таких рядов характерны близкие химические свойства и закономерно изменяющиеся физические свойства.
Основной источник синтеза алакнов – нефть. Следует отметить, что ее биохимический состав зависит от месторождения. Непредельные углеводороды являются ценным источником для получения формальдегида, метанола, хлороформа, пластических масс, синтетических смол, эфиров, ацетона, глицерина, пропилена, полипропилена, синтетического бутандиенового каучука, ацетатной кислоты и т.д. В промышленности алканы получают из сланцев бурого и каменного угля. В обычных условиях алканы – химически инертные вещества. При комнатной температуре они не взаимодействуют ни с концентрированной сульфатной кислотой, ни со щелочными металлами, ни с едкими щелочами. Парафины легко вступают в реакции замещения, которые протекают по радикальному механизму. В термических условиях они могут окисляться и претерпевать разложение.
Изомеры гептана могут быть получены как обычными способами синтеза алканов, так и путем выделения из синтетического бензина либо нефти. н-Гептан – бесцветная жидкость со слабым специфическим запахом, он хорошо растворим в органических растворителях (этанол, хлороформ, диэтиловый эфир). Изомеры гептана, в частности триптан (2,2,3-триметилбутан – СН3-С(СН3)2-СН(СН3)-СН3) имеют и практическое использование. Указанное соединение используют в качестве добавки к моторному топливу. Изомеры гептана содержатся в бензиновых фракциях нефти и газовых конденсатах. н-Гептан – первичный эталон при определении детонационных свойств карбюраторного топлива. В процессе реформинга н-Гексан превращается в изомеры гептана, далее дегидроциклизируется в ароматическое соединение – толуол.
В органической химии широко распространено явление изомерии. Различают два основных типа изомерии – структурная и стереоизомерия. Каждый тип можно разделить на виды: изомерия углеводородной цепи, размещение двойных связей и функциональных групп в карбоновом радикале, метамерия, изомерия расположения заместителей в бензельном ядре. Особое место среди стереоизомерии занимает оптическая изомерия. Данный вид связан со способностью некоторых групп органических веществ в растворах проявлять оптическую активность. Вещества, которые способны проявлять оптическую активность, называются оптически активными веществами. Изомерия органических соединений определяется с помощью специального прибора – поляриметра. Прибор оснащен двумя призмами Николя, анализатором, поляриметрической трубой.
Оптически активные вещества, как правило, существуют в виде двух оптических изомеров. Их называют оптическими антиподами, или энантиомерами. Смесь, в состав которой входят эквимолекулярные количества энантиомеров, оптически неактивная, называется рацематом или рацемическим соединением. Рацематы обозначаются знаком ±. Простейшим оптически активным веществом является лактатная кислота, в молекуле которой присутствует один асимметрический атом углерода, валентности которого связаны с четырьмя разными заместителями – водородом, гидроксильной, метильной и карбоксильной группами.
Каждое органическое соединение, в молекуле которого есть асимметрический атом углерода, существует в виде пространственных форм (моделей) с одинаковым количеством одних и тех же атомов и атомных групп, размещенных вокруг асимметрического углерода так, что при совмещении их (форм, моделей) в пространстве невозможно достичь их полного совпадения. Указанные модели похожи как правая и левая рука человека или как предмет и его зеркальное отображение. Поэтому их называют хиральными изомерами, а изомерию - оптической, или зеркальной.
fb.ru
Гептановая кислота - Справочник химика 21
Рассчитать удельную адсорбцию гептановой кислоты и построить изотерму адсорбции по зависимости a — f( ) для ее водных растворов при Г = 293 К. [c.25]Гептановая кислота СНз(СН,),СООН [c.550]
Нз 9Н3 1. 1,3,5-Триметил-2-пентановая кислота Т 2. 4-Метил-З-гептановая кислота [c.110]
Энантовая кислота, гептановая кислота [c.292]
Известно много методов окисления. Однако большое значение этой реакции побудило исследовать применимость межфазных катализаторов в реакции окисления в тех случаях, когда органический субстрат нерастворим в водных средах, а окислитель в свою очередь нерастворим или плохо растворим в органических растворителях. Принципиальная возможность использования межфазных катализаторов для окисления нерастворимых в воде субстратов в апротонном растворителе была показана еще в 1965 г. [388]. В качестве катализатора была использована четвертичная арсониевая соль — метилтрифенил-арсонийхлорид при этом происходил обмен хлор-аниона на анион перманганата из водного раствора перманганата калия и перенос этого аниона в хлороформенный раствор субстрата (октен-1, пропанолы-1 и -2, гептанол-4 и др.), где и проходило окисление. В таких условиях пропанол-2, например, на 100% превращался в ацетон. грет-Бутиловый спирт, толуол, этилацетат, диэтиловый эфир, ацетон или дипропилкетон не окислялись. Позже было установлено, что октен-1 и децен-1 превращаются соответственно в гептановую кислоту (количественный выход) и нонановую кислоту (выход 91%) при окислении нейт- [c.136]
На основании выводов о составе и строении вещества X напишите его формулу, а также продуктов реакций А, Б, В, Г, Д и гептановой кислоты. [c.22]
Гептановая кислота см. Энантовая кислота Гептанол-1 см. Гептпловый спирт [c.127]
Назвать соединение по систематической номенклатуре Н0-С=0 РНз 1. 2,5-Диметил-З-гептановая кислота [c.109]
ГЕПТАНОВАЯ КИСЛОТА (гептиловая к-та, энантовая к-та) СНз(СН2)5СООН, tn. от --7,0 до 10,5 °С, iaa r -7,5 °С, i 223 °С 0,9184, 1,4230 ц 5,046 10 = Па-с (15 °С) К (1,42—1,46)-10- плохо раств. в воде (0,244 г в 100 г), раств. в СП., эф. Содержится в эфирном масле аира входит во фракции Сз—Сэ и С —Сэ синт. жирных к-т образуется при окисл. пальмитолеиновой к-ты. [c.127]
Свободная гептановая кислота. Растворяют 0,5 г испытуемого вещества (точная навеска) в 10 мл этанола ( — 750 г/л) ИР, предварительно нейтрализованного по раствору бромтимолового синего в этаноле ИР, и сразу же титруют раствором гидроксида натрия (0,01 моль/л) ТР, используя в качестве индикатора раствор бромтимолового синего в этаноле ИР для получения среднего значения индикатора (зеленый цвет) требуется не более 0,6 мл раствора гидроксида натрия (0,С1 моль/л) ТР. [c.355]
Для инфракрасных спектров карбоновых кислот характерна широкая полоса поглощения при 3300-2500 см , обусловленная валентными колебаниями связи О-Н, которая часто представляет собой несколько перекрывающихся полос (см., например, спектр гептановой кислоты на рис. 3.15). [c.71]
В результате этих превращений цепь молекулы удлиняется на один атом углерода. Образование гептановой кислоты (семь атомов С) указывает, что молекула исходного вещества содержит шесть атомов С. [c.84]
Раств-сть гидрохлорид х.р. Н О, МеОН, свободное основание м. р. Н О о.п.р. EtOH н.р. орг. раств-ли. Семейство включает 7 декапептидов, различающихся по аминокислотному составу, все содержат 5 или 6 остатков Dab ацильная группа-6 Me-O t или 6-Ме-гептановая кислота ингибирует рост микроорганизмов (при 2 мкг/мл рост Е. со1[) грамотрицательные в целом более чувствительны, чем грамположительные. Полимиксины связываются с клеточной [c.249]
ЛД50 5 г/кг (крысы, перорально), > 5 г/кг (кролики, при нанесении на кожу) в организме превращается в гептановую кислоту 35 °С, 1 45 °С, Гр спл 206 °С, КПВ 1,07-5,2%, ТПВ 40-66 °С. [c.21]
АЛЛИЛЭНАНТАТ (аллиловый эфир гептановой кислоты), 10h28O2, мол.м. 170,24 СНз(СН2)5СООСН2СН=СН2 бесцветная жидкость с нежным фруктовым запахом 210 С (760 мм рт.ст.), 0,890, 1,429 растворим в этаноле и органических растворителях, нерастворим в воде. [c.32]
Кислые, нейтральные или щелочные растворы перманганата, могут быть использованы для окисления как ароматических, так и алифатических альдегидов. Несмотря на то, что как в кислых, так и в щелочных средах промотируется расщепление енолизующихся алифатических альдегидов, кислоты могут быть получены с хорошими выходами. Например, при окислении гептаналя смесью перманганата калия и концентрированной серной кислоты с выходом 76% получается гептановая кислота [120]. [c.351]
Органическая химия. Т.2 (1970) -- [ c.524 , c.594 ]Органический синтез в двухфазных системах (1982) -- [ c.136 , c.141 ]
Органическая химия (1974) -- [ c.934 ]
Органическая химия (1979) -- [ c.0 ]
Реагенты для органического синтеза Т.7 (1978) -- [ c.41 ]
Реагенты для органического синтеза Том 7 (1974) -- [ c.41 ]
Количественный органический анализ по функциональным группам (1983) -- [ c.133 ]
Органическая химия Том2 (2004) -- [ c.211 ]
Большой энциклопедический словарь Химия изд.2 (1998) -- [ c.127 ]
Основания глобального анализа (1983) -- [ c.0 ]
Органическая химия Углубленный курс Том 2 (1966) -- [ c.511 ]
Органикум Часть2 (1992) -- [ c.2 , c.31 , c.104 , c.114 , c.135 ]
Химия органических лекарственных препаратов (1949) -- [ c.230 , c.237 ]
Поверхностно-активные вещества _1979 (1979) -- [ c.75 , c.221 , c.222 , c.224 , c.236 ]
Синтезы на основе окиси углерода (1971) -- [ c.105 ]
Начала органической химии Кн 1 Издание 2 (1975) -- [ c.0 ]
Биохимия Издание 2 (1962) -- [ c.309 ]
chem21.info
Гептановая кислота, как растворитель Гептановая кислота
На рис. 32 приведены результаты, полученные для четырех фракций полиизобутилена в изооктане (хороший растворитель) и в этиловом эфире -гептановой кислоты (тета-растворитель при 34°) [131]. Следует отметить, что для наиболее высокомолекулярных фракций при неидеальных условиях измерения могут дать ошибку до 25%. [c.63]Известно много методов окисления. Однако большое значение этой реакции побудило исследовать применимость межфазных катализаторов в реакции окисления в тех случаях, когда органический субстрат нерастворим в водных средах, а окислитель в свою очередь нерастворим или плохо растворим в органических растворителях. Принципиальная возможность использования межфазных катализаторов для окисления нерастворимых в воде субстратов в апротонном растворителе была показана еще в 1965 г. [388]. В качестве катализатора была использована четвертичная арсониевая соль — метилтрифенил-арсонийхлорид при этом происходил обмен хлор-аниона на анион перманганата из водного раствора перманганата калия и перенос этого аниона в хлороформенный раствор субстрата (октен-1, пропанолы-1 и -2, гептанол-4 и др.), где и проходило окисление. В таких условиях пропанол-2, например, на 100% превращался в ацетон. грет-Бутиловый спирт, толуол, этилацетат, диэтиловый эфир, ацетон или дипропилкетон не окислялись. Позже было установлено, что октен-1 и децен-1 превращаются соответственно в гептановую кислоту (количественный выход) и нонановую кислоту (выход 91%) при окислении нейт- [c.136]
АЛЛИЛЭНАНТАТ (аллиловый эфир гептановой кислоты), 10h28O2, мол.м. 170,24 СНз(СН2)5СООСН2СН=СН2 бесцветная жидкость с нежным фруктовым запахом 210 С (760 мм рт.ст.), 0,890, 1,429 растворим в этаноле и органических растворителях, нерастворим в воде. [c.32]
Для разбавленных растворов полиизобутилена в изооктане было найдено dnId = = 1,42-10 (г/этиловом эфире и-гептановой кислоты та же величина, измеренная на дифференциальном рефрактометре Феникс при 34° составляет 1,04-10 (г/Эл) . Для определения парциального удельного объема измеряли плотность разбавленных растворов полиизобутилена в этиловом эфире н-гепта-новой кислоты при 34° с помощью калиброванного пикнометра и полумикровесов. Парциальный удельный объем, вычисленный из этих данных по методу отрезков, описанному Люисом и Рендаллом [129], равен 1,106 см 1г. Плотность растворителя при этой температуре составляла 0,8563 г см . Для растворов полиизобутилена в изооктане при 25° необходимая для расчетов величина (1 — V q) равна 0,272. [c.65]
Соли окисной и закисной меди в инертных растворителях. Восстановление окисной медной соли гептановой кислоты до закисной соли протекает гомогенно в различных неполярных растворителях. В среде гептановой кислоты в активации водорода участвуют как окисная, так и закисная соль, причем закисная соль более активна [28]. Поэтому реакция является автокатали-тической (рис. 4) и кинетическое уравнение имеет вид [c.349]
Добавление гептаноата натрия к раствору приводит к образованию более сложных комплексов двух- и одновалентной меди, вероятно Маг(СиНр4) и Ыа2(СиНрз) эти вещества также являются неактивными. По-видимому, гептановая кислота в данной системе действует как инертный растворитель, так как по существу аналогичные результаты, за исключением небольших количественных отличий, были получены с применением октадекана и дифенила в качестве растворителей. [c.350]
Несмотря на высокую основность иона гептаноата, энергия активации для реакции СиНрг в растворе гептановой кислоты (30 ккал/моль) значительно выше, чем энергия активации как для Си +, так и для СиАсг в водном растворе (26 и 24 ккал/моль соответственно). Правдоподобное объяснение этого заключается в том, что при образовании переходного состояния происходит разрыв связи металл — лиганд, который в неполярном растворителе требует большей энергии активации. [c.350]
Экстракционные бензины [61—65]. Бензины в достаточно широких масщтабах используются для процессов экстракции. Сюда относится экстрагирование остаточного масла из жмыхов касторовых и соевых бобов, семени хлопчатника, зерен пшеницы. Растворителем, используемым в качестве экстрагента, в вышеописанных случаях служит гексано-гептановая фракция с пределами кипения 65—120° С. Там где извлекаемые из жмыхов масла являются съедобными или предназначены для целей очистки, необходимо иметь стабильный экстрагент, полностью лишенный остаточного запаха или привкуса. Для получения такого экстрагента вполне пригодны прямогонные продукты из нейтральных (не содержащих нафтеновых кислот) парафинистых нефтей. [c.564]
Пропионовый, масляный, изомасляный, валериановый и н-гептановый альдегиды подвергались полимеризации при высоком давлении с образованием растворимых в органических растворителях полиоксиалкилиденов, имеющих концевые гидроксильные группы [62]. Полимеры изомасляного и -гептанового альдегидов частично кристалличны остальные аморфны. Предполагая присутствие неизбежных примесей карбоновых кислот, считают, что полимеризация протекает по катионному механизму. В присутствии действительно катионных реагентов (фтористый бор, бромистый алюминий, этилалюминийдихлорид) при —78° в этиловом эфире образуются изотактические полимеры пропионового, масляного, изомасляного и изо-валерианового альдегидов [2]. [c.396]
chem21.info
Гептан - это... Что такое Гептан?
| н-Гептан | |
 | |
 | |
| Систематическое наименование | н-Гептан |
| Сокращения | н-C7 |
| Химическая формула | C7h26 |
| Эмпирическая формула | С7h26 |
| Отн. молек. масса | 100,125200512 а. е. м. |
| Молярная масса | 100,21 г/моль |
| Плотность | 0,6795 г/см³ |
| Динамическая вязкость (ст. усл.) | 0,000386 Па·с(при 20 °C) |
| Температура плавления | −90,61 °C |
| Температура кипения | 98,42 °C |
| Температура кипения | 371.2-371.8 K, 208-210 °F |
| Температура вспышки | -4 °C |
| Температура самовоспламенения | 223,0 °C |
| Пределы взрываемости | 1,05–6,7 % |
| Молярная теплоёмкость (ст. усл.) | 224,64 Дж/(моль·К) |
| Энтальпия образования (ст. усл.) | −225,2 — -223,6 кДж/моль |
| Давление пара | 5,33 кПа при 20 °C |
| Дипольный момент | 0 Д |
| Рег. номер CAS | 142-82-5 |
| Рег. номер PubChem | 8900 |
| SMILES | CCCCCCC |
| Регистрационный номер EC | 205-563-8 |
| RTECS | MI7700000 |
| ЛД50 | 103 г/м3 в воздухе, экспоз. 4 ч, крысы мг/кг |
Гептан (от др.-греч. ἑπτά — семь) СН3(СН2)5СН3 — органическое соединение класса алканов. Гептан и его изомеры — бесцветные жидкости, хорошо растворимые в большинстве органических растворителей, нерастворимые в воде. Обладают всеми химическими свойствами алканов.
Физические свойства
Бесцветная подвижная жидкость с резким запахом.
Химические свойства
Аналогичны химическим свойствам других высших алканов.
Получение
Может быть выделен из бензина прямой перегонки путем адсорбционного выделения на цеолитах из соответствующей фракции
Использование
Гептан имеет несколько изомеров; н-гептан применяют при определении детонационной стойкости карбюраторных топлив; его октановое число по определению равно 0.
Изомеры и энантиомеры
Гептан имеет девять изомеров, или одиннадцать, если учитывать оптические изомеры.
| название | формула | температура кипения |
| Гептан (н-гептан) | h4C–Ch3–Ch3–Ch3–Ch3–Ch3–Ch4 | 98.43 °C |
| 2-Метилгексан | h4C–CH(Ch4)–Ch3–Ch3–Ch3–Ch4 | 90.05 °C |
| 3-Метилгексан | h4C–Ch3–C*H(Ch4)–Ch3–Ch3–Ch4 | 91.85 °C |
| 2,2-Диметилпентан | (h4C)3–C–Ch3–Ch3–Ch4 | 79.20 °C |
| 2,3-Диметилпентан | (h4C)2–CH–C*H(Ch4)–Ch3–Ch4 | 89.78 °C |
| 2,4-Диметилпентан | (h4C)2–CH–Ch3–CH–(Ch4)2 | 80.50 °C |
| 3,3-Диметилпентан | h4C–Ch3–C(Ch4)2–Ch3–Ch4 | 86.06 °C |
| 3-Этилпентан | h4C–Ch3–CH(Ch3Ch4)–Ch3–Ch4 | 93.48 °C |
| 2,2,3-Триметилбутан | (h4C)3-C–CH(Ch4)–Ch4 | 80.88 °C |
(C* обозначает хиральный центр, то есть существование асимметрического центра, относительно которого различают «правые» и «левые» оптические изомеры)
dic.academic.ru