Содержание
1 1 2
СН3 — О —СН — СН3
│
СН3
Название: метокси
— 1 -метилэтан
По радикальной
номенклатуре: Метилизопропиловый эфир.
Сложные эфиры
можно рассматривать как продукт замещения
гидроксильного водорода в спиртах на
кислотный радикал органических кислот.
Общая формула:
R-
С = О
│
О — R1
Например:
О
ll
СН3 — С — О
— СН3
О — С3Н7
│
С2Н5 — С = О
Брутто-формула
простых эфиров СnН2nО2.
По номенклатуре
ИЮПАК сложные эфиры называют, прибавляя
в качестве приставки название спиртового
радикала к названию кислоты, в которой
окончание –оваязаменяется на-оат
Формула | Остаток | Остаток | Окончание, | Общее |
О Ll СН3 | — метил | О ll СН3 Этан | оат | метилэтаноат |
О Ll Н— С — О — СН3 | — метил | О ll Н— С — О — Метан(овая) | оат | метилметаноат |
О — С4Н9 │ С2Н5 | — бутил | О │ С2Н5 Пропан(овая) | оат | бутилпропаноат |
В литературе широко
используется другое название сложных
эфиров:
метилэтаноат –
метиловый эфир этановой кислоты,
бутилпропаноат – бутиловый эфир
пропановой кислоты.
Составление
структурной формулы по названию.
Пример
6.3.Написать структурную формулу
для соединений:
А.
2,3 — диметил- 4-этилгексанол -2
Б.
2,7 – диметил — 4 – изопропилнонандиол
– 2,6
В.
2 – метил – 4,5 – диэтилгептанон – 3
Г.
3,4,5 – триметил – 2 – пропилгексаналь
Д.
3 – этил – 3 – изопропилпентановая
кислота
Написать
брутто-формулу этого соединения.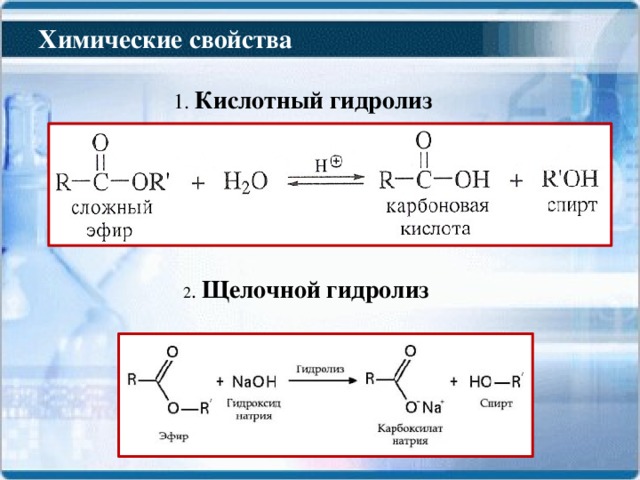
6.3.А
1.Записывается
главная цепь, т.е. углеродный скелет
спирта стоящего в конце формулы. К
углероду, указанному цифрой в конце
названия, присоединяется гидроксильная
группа, затем номеруются все углеродные
атомы, начиная с конца молекулы, к
которому ближе расположена гидроксильная
группа:
1
2 3 4 5 6
С
– С – С — С – С – С
│
ОН
2. В соответствии
с цифрами, указанными в формуле,
расставляются все заместители.
СН3 СН3
1
2│
3│
4 5 6
С
– С — С — С – С — С
│
│
ОНС2Н5
3.
Соблюдая условия четырехвалентности
углеродных атомов, заполняют оставшиеся
свободные валентности атомов углерода
в углеродном скелете атомами водорода:
СН3
СН3
1
2 │
3│
4
5 6
СН3– С — СН — СН – СН2– СН3
│ │
ОНС2Н5
Количество
углеродных атомов в данном соединении
10. Брутто-формула этого соединения
Брутто-формула этого соединения
С10Н22
Выполняя
последовательно п.п. 1-3 предыдущей задачи
составляются структурные формулы для
соединений Б и В
Б. 1. С – С -С — С – С – С — С — С — С │ │ ОН | В. 1. С — С — С — С — С Ll О |
2 СН3 -СН 1 С – С — С — С – С │ │ │ │ СН3 | 2. С2Н5 7 6 С — С — С — С — С │ ll С2Н5О СН3 |
3. 1 СН3–СН — СН2– С –СН2–СН– СН— СН2— СН3 │ СН3 2,7 брутто-формула: | 3. 7 6 СН3— СН2— СН — СН — С — СН — СН3 │ ll С2Н5О СН3 2 брутто-формула: |
Выполняя
последовательно п.п. 1-3 предыдущей задачи
составляются структурные формулы для
соединений Г и Д
Г. 1. 1│ О │ С3Н7 СН3 | Д. 1. 5 С — С — С — С — С ll О |
2 Н 1│ О │ │ С3Н7 | 2. СН3 — СН 5 С — С — С — С — С │ С2Н5 |
3. Н 1│ О │ │ С3Н7 3,4,5 брутто-формула: | 3. СН3 — 5 СН3– СН2— С — СН2— С — ОН │ ll С2Н5 3 – этил – 3 – брутто-формула: |
Пример
6. 4.Написать структурную формулу
4.Написать структурную формулу
для соединений:
А.
изопропилбутиловый эфир
Б.
бутилэтаноат
Написать
брутто-формулу этого соединения.
6.4.А
Название
простых эфиров обычно состоит из двух
названий углеводородных радикалов,
которые связаны кислородным мостиком.
В данном примере:
Изопрпил
│бутил + овый + эфир
СН3
— СН — О — СН2— СН2—
СН2— СН3
│
СН3
Изопропилбутиловый
эфир
Брутто=формула С7Н16О
6.4.Б
Название
сложных эфиров состоит из названия
спирта, преобразованное в соответствующий
радикал, и названия кислоты при замене
окончания «-овая» на окончание «оат».
Остатки названия спирта и кислоты
связаны кислородным мостиком.
В
данном примере:
Бутил
│этан+оат
СН3— СН3 — СН2 — СН2— О
— С — СН3
ll
О
Бутилэтаноат
Брутто=формула С6Н12О2
Изомерия
кислородсодержащих углеводородов.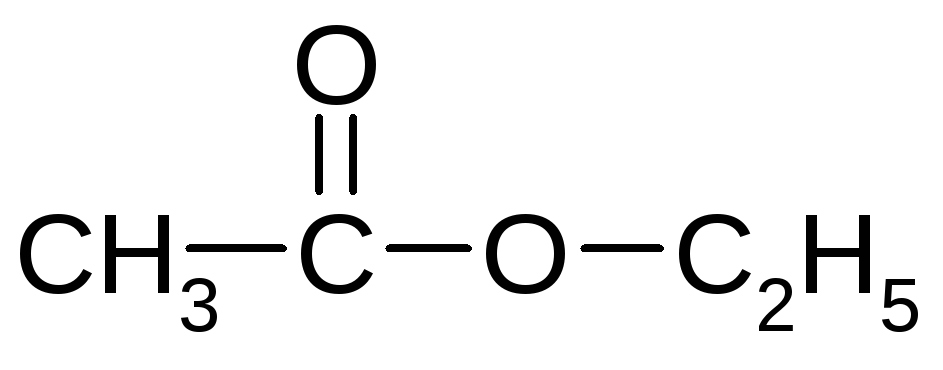
Вывод структурных формул изомеров.
В
таблице приведены виды изомерии,
характерные для кислородсодержащих
углеводородов
Виды | Гомологические |
Углеродного | Спирты, |
Положения | Спирты. |
Межклассовая | спирты альдегиды кислоты |
Пример 6.5.Составить и назвать по два изомера
соединения С4Н10, принадлежащие
различным видам изомерии.
Структурная | Название |
1. | бутанол -1 |
2. │ ОН | Бутанол — 2 |
3. СН3— │ СН3 | 2 |
4. │ СН3— СН │ СН3 | 2, |
5. СН3— | Метилпропиловый |
| Этилэтиловый Диэтиловый |
Пример 6.6.Составить и назвать по два изомера
соединения С5 Н10 О,
принадлежащие различным видам
изомерии.
Структурная | Название |
│ Н | Пентаналь |
│ │ СН3Н | 3 |
3. │ │ СН3Н | 2-метилбутаналь |
4. ll О | Пентанон |
5. ll О | Пентанон |
6. ll О | 3- |
Пример 6. 7.Составить и назвать по два изомера
7.Составить и назвать по два изомера
соединения С5 Н10 О2,
принадлежащие различным видам
изомерии.
Структурная | Название |
│ ОН | Пентановая |
│ │ СН3 ОН | 2 |
СН3 │ СН3— С – С = О │ │ СН3 ОН | 2. |
│ О — СН2 — СН3 | Этилпропаноат |
5. ll О | Пропилэтаноат |
ll О | бутилметаноат |
Сложные эфиры — презентация онлайн
1.
 Сложные эфиры
Сложные эфиры
Составитель: И.Н. Пиялкина,
учитель химии МБОУ СОШ № 37
города Белово
Определение
• Производные карбоновых кислот, в
которых атом водорода
карбоксильной группы замещен на
углеводородный радикал, называют
сложными эфирами
Номенклатура
В общей формуле сложных
эфиров можно R и R’ –
углеводородные радикалы (для
эфиров муравьиной кислоты R –
атом
водорода).
Широко
используют несколько типов
названий
сложных
эфиров.
Самые длинные происходят от
названия
соответствующий
кислоты
с
указанием
углеводородного
заместителя,
например,
бутиловый
эфир
уксусной
кислоты,
изопропиловый эфир масляной
кислоты. В русском языке
приняты названия, состоящие из
двух слов: уксуснобутиловый
эфир, масляноизопропиловый
Номенклатура
Если используют тривиальное название исходной
кислоты, то в название соединения включают слово
«эфир»
O
O
Ch4
H
C
O
Ch4
метиловый эфир
уксусной кислоты
C
O
C3H7
пропиловый эфир
муравьиной кислоты
Номенклатура
Названия сложных эфиров производят от названия,
углеводородного радикала и названия соли кислоты,
например, муравьиная – формиат, уксусная – ацетат,
пропионовая – пропионат, масляная – бутаноат и т. д.
д.
O
O
Ch4
C
H
O
метилацетат
Ch4
C
O
C3H7
пропилформиат
Изомерия
Сложные эфиры являются межклассовыми изомерами
карбоновых кислот для насыщенных R и R’ имеют общую
формулу Cnh3nO2.
Изомерия
Им свойственна структурная изомерия. Структурная изомерия может
быть связанна с длиной углеродной цепи (приведенные ниже эфиры
изомерны) в заместителях и строением углеродного скелета
O
Ch4 – Ch3 – C – O – Ch3 – Ch3 – Ch3 – Ch4
O
Ch4 – Ch3 – Ch3 – C – O – CH – Ch4
Ch4
НАЗОВИТЕ !
Физические свойства
Сложные эфиры с относительно небольшой молекулярной
массой
представляют
собой
легковоспламеняющиеся
жидкости с невысокими температурами кипения, имеют
различные запахи. Они практически нерастворимы в воде и
имеют более низкие температуры кипения, чем изомерные им
карбоновые кислоты. Это связанно с тем, что в молекулах
сложных эфиров отсутствуют межмолекулярные водородные
связи.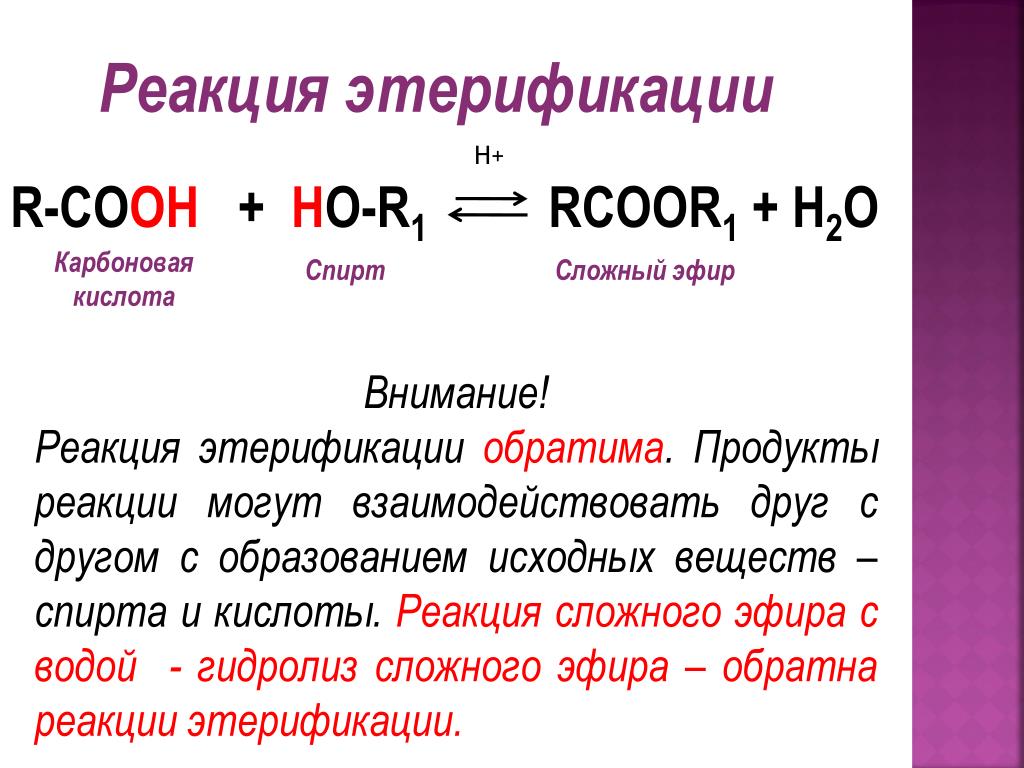
цветы
воск
фрукты
Классификация и состав сложных эфиров
Когда число атомов С в исходных карбоновой кислоте и спирте
не превышает 6–8, соответствующие сложные эфиры
представляют собой бесцветные маслянистые жидкости, чаще
всего с фруктовым запахом. Они составляют группу фруктовых
эфиров. Если в образовании сложного эфира участвует
ароматический спирт (содержащий ароматическое ядро), то
такие соединения обладают, как правило, не фруктовым, а
цветочным запахом. Все соединения этой группы практически
нерастворимы в воде, но легко растворимы в большинстве
органических растворителей. Интересны эти соединения
широким спектром приятных ароматов (см. табл. 1), некоторые
из них вначале были выделены из растений, а позже
синтезированы искусственно.
Классификация и состав сложных эфиров
При увеличении размеров органических групп, входящих в
состав сложных эфиров, до С15–30 соединения
приобретают
консистенцию
пластичных,
легко
размягчающихся веществ. Эту группу называют восками,
Эту группу называют восками,
они, как правило, не обладают запахом.
Пчелиный воск
Ch4(Ch3)14–CO–OCh3(Ch3)29Ch4
Искусственный
воск
Воска
Воска — сложные эфиры одиночных жирных кислот и одноатомных спиртов с
длинной углеводородной цепочкой.
Пчелиный воск содержит смесь различных сложных эфиров, один из
компонентов воска, который удалось выделить и определить его состав,
представляет
собой
мирициловый
эфир
пальмитиновой
кислоты
C15h41COOC31H63. Китайский воск (продукт выделения кошенили – насекомых
Восточной
Азии)
содержит
цериловый
эфир
церотиновой
кислоты
C25H51COOC26H53. Кроме того, воски содержат и свободные карбоновые
кислоты и спирты, включающие большие органические группы. Воски не
смачиваются водой, растворимы в бензине, хлороформе, бензоле.
Молекула воска
Классификация и состав сложных эфиров
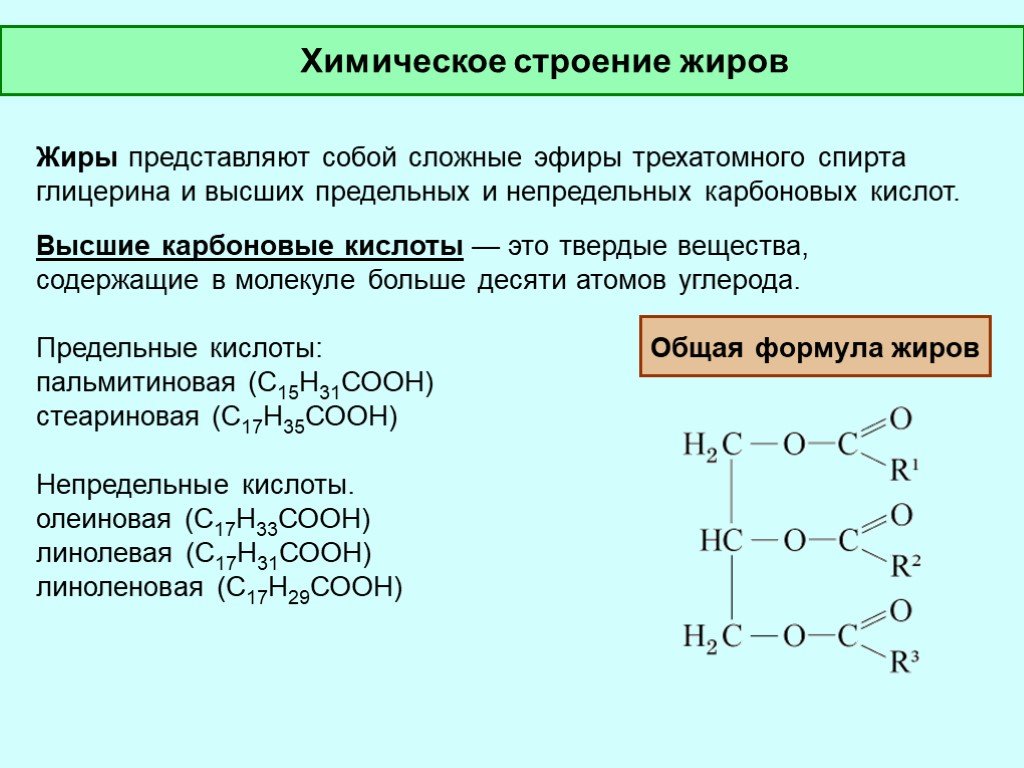
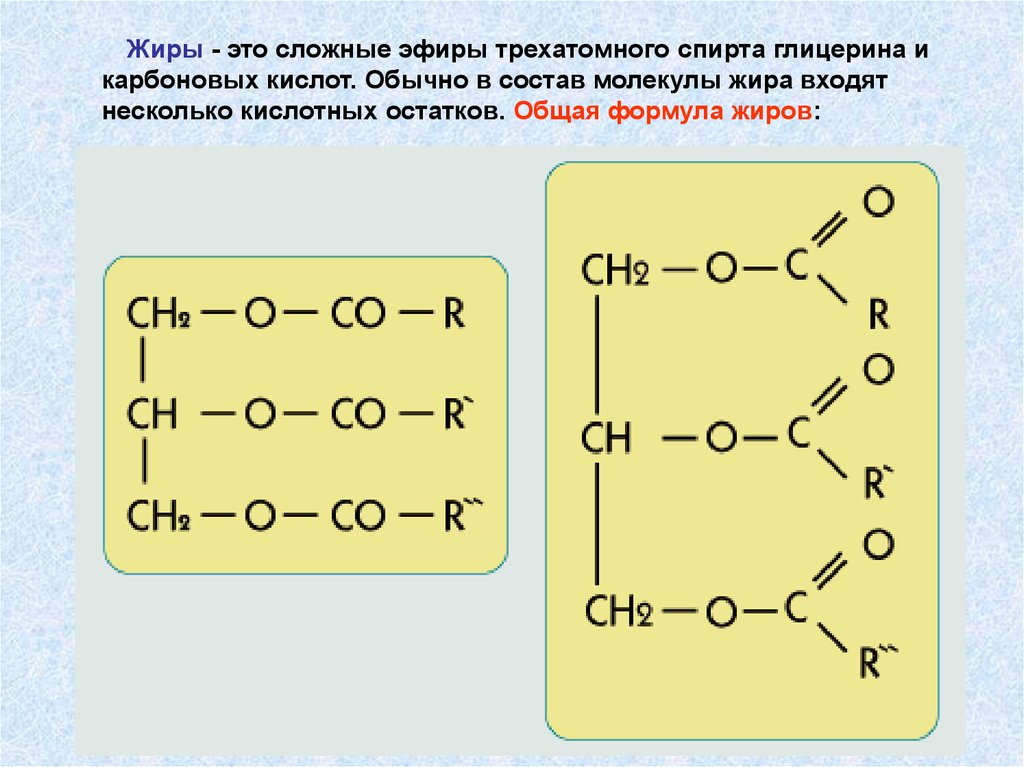
Третья группа – жиры. В отличие от предыдущих двух групп
на основе одноатомных спиртов ROH, все жиры
представляют собой сложные эфиры, образованные из
трехатомного спирта глицерина НОСН2–СН(ОН)–СН2ОН.
Карбоновые кислоты, входящие в состав жиров, как правило,
имеют углеводородную цепь с 9–19 атомами углерода.
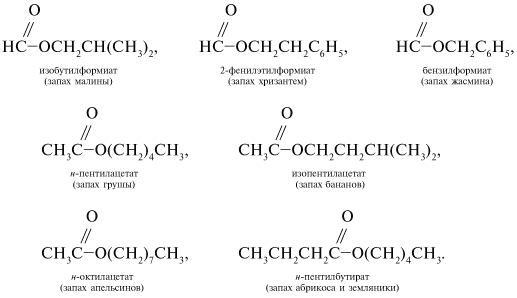
13. Таблица 1
НЕКОТОРЫЕ СЛОЖНЫЕ ЭФИРЫ, обладающие фруктовым или цветочным ароматом
(фрагменты исходных спиртов в формуле соединения и в названии выделены
жирным шрифтом)
Формула сложного эфира
Название
Аромат
СН3СООС4Н9
Бутилацетат
грушевый
С3Н7СООСН3
Метиловый эфир масляной
кислоты
яблочный
С3Н7СООС2Н5
Этиловый эфир масляной
кислоты
ананасовый
С4Н9СООС2Н5
Этиловый эфир
изовалериановой кислоты
малиновый
С4Н9СООС5Н11
Изоамиловый эфир
изовалериановой кислоты
банановый
СН3СООСН2С6Н5
Бензилацетат
жасминовый
С6Н5СООСН2С6Н5
Бензилбензоат
цветочный
амилформиат
метилбутират
октилацетат
изоамилформиат
изобутилформиат
этилбутират
амилацетат
изоамилацетат
бутилбутират
15. «Одежда украшает внешность, а духи отражают внутренний мир.
 ..» Жак Польж, парфюмер фирмы Шанель
..» Жак Польж, парфюмер фирмы Шанель
«Одежда украшает внешность,
а духи отражают внутренний мир…»
Жак Польж, парфюмер фирмы Шанель
Виды запахов:
o
ГОРЬКИЕ: герань, лимон, мандарин, пион, сирень,
флердоранж (цветок апельсина).
o
ТОНКИЕ: акация, гелиотроп, ирис, левкой, магнолия, мимоза,
настурция, пион, роза.
СЛАДКОВАТЫЕ: акация, мандарин, тубероза, ваниль.
o ЗЕЛЕНЫЕ: гвоздика, фиалка (листья), нарцисс, гальбанум (смола),
o
мирра.
o
ТЕПЛЫЕ: акация, душистый горошек, персик, сандал, тубероза,
жимолость, животные запахи.
o
ГУСТЫЕ, ТЯЖЕЛЫЕ: гвоздика, ладан, лилия, пачули,
тубероза, ладан.
o
ПРЯНЫЕ: жасмин, пачули, цикламен, корица, гвоздика, ветивер
(корни), ладан.
ЗАПАХ КОЖИ, ТАБАКА получают из бессмертника.
o ЖИВОТНЫЕ запахи: Серая амбра-железа кашалота выделяет
o
секрет, который дает живой, теплый
Способы получения
Сложные эфиры могут быть получены при
взаимодействии карбоновых кислот со спиртами
(реакция этерификации)
Катализаторами являются минеральные
кислоты.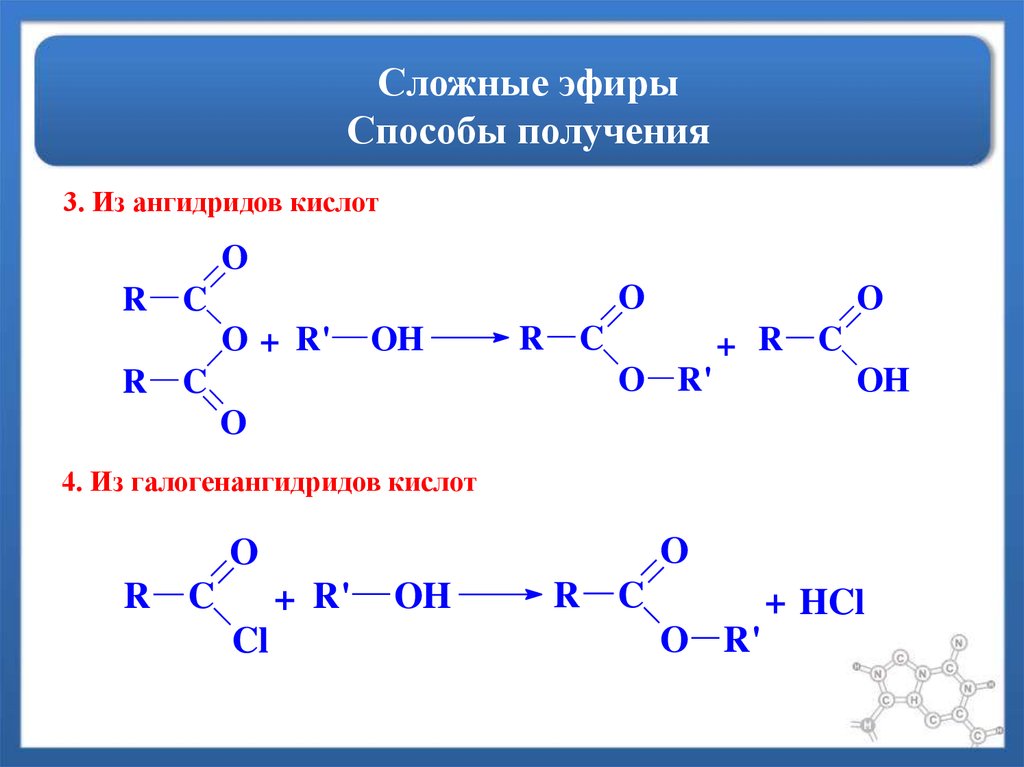
Способы получения
Алкилирование солей карбоновых кислот
Способы получения
Взаимодействие ангидрида со спиртом
(Ch4CO)2O + 2C2H5OH = 2СН3COOC2H5 + h3O
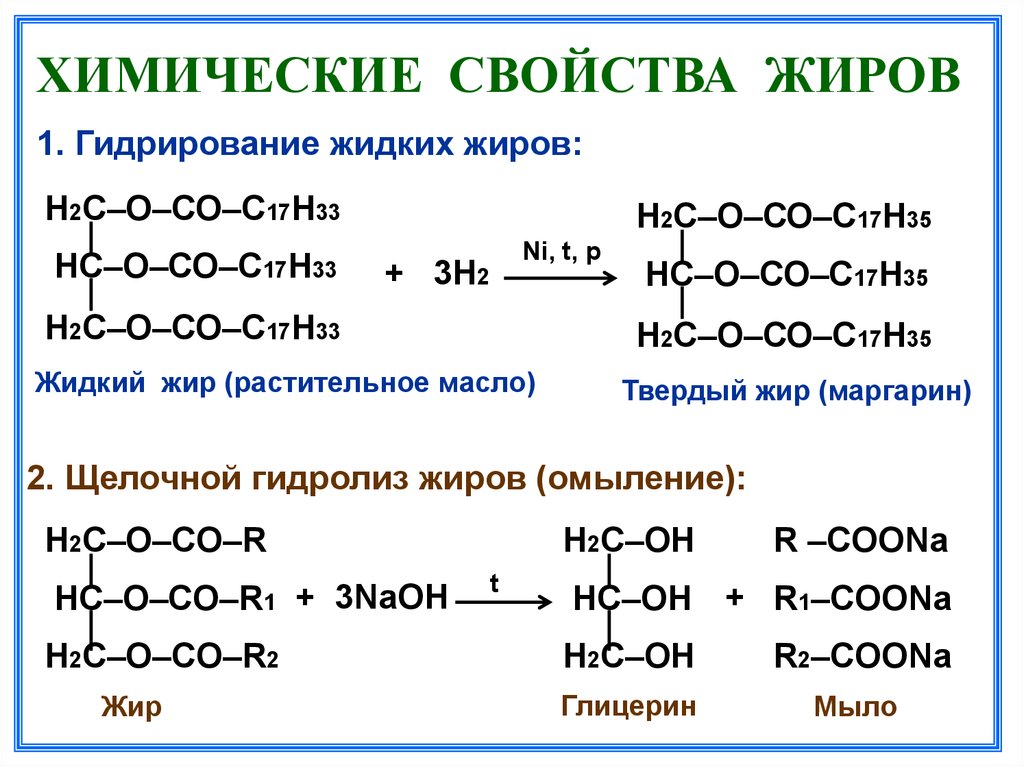
Химические свойства
Реакция горения
2Ch4 – COOCh4 + 7O2
6CO2 + 6h3O
Химические свойства
Процесс — расщепление сложного эфира при действии
воды с образованием карбоновой кислоты и спирта называют гидролизом сложного эфира.
Гидролиз в присутствии щелочи протекает необратимо
(т.к. образующийся отрицательно заряженный
карбоксилат-анион RCOO– не вступает в реакцию с
нуклеофильным реагентом — спиртом).
Эта реакция называется омылением сложного эфира.
Химические свойства
Кислотный гидролиз сложных
обратимым процессом:
эфиров
является
Химическое равновесие, устанавливающееся при равенстве скоростей
прямой (этерификация) и обратной (гидролиз) реакций, может быть
смещено в сторону образования эфира присутствием водоотнимающих
средств и нагреванием.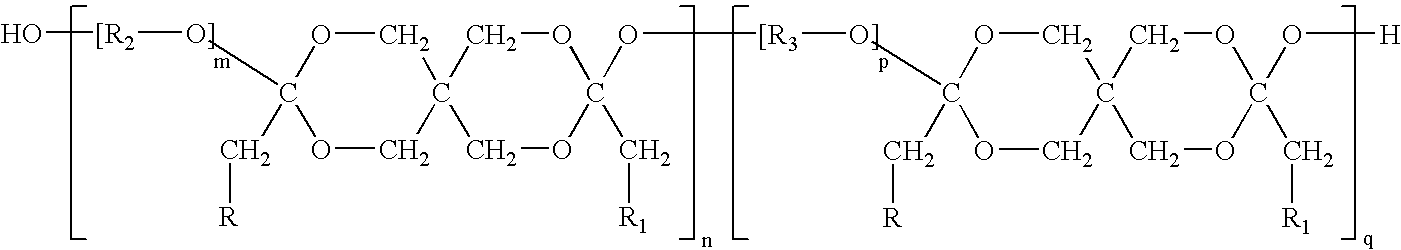
Увеличение концентрации реагентов смещает химическое равновесие в сторону
продуктов реакции как в газовой, так и в жидкой среде.
Удаление продуктов из среды реакции так же смещает равновесие в сторону продуктов
реакции.
Увеличение концентрации продуктов смещает химическое равновесие в сторону
обратной реакции.
Применение
лаки
синтетические и
искусственные волокна
производство напитков и
кондитерских изделий
лекарственные средства
парфюмерия и косметика
Применение
Полиметилметакрилат – органическое стекло (плексиглас) –
получается при полимеризации метилового эфира
метакриловой кислоты (метилметакрилата) и представляет
собой бесцветную прозрачную массу:
Применение
• Полиэтилентерефталат – ПЭТ, ПЭТФ (PET, валокс, ULTRADUR,
CELANEX, RYNITE) — это линейный термопластичный
полиэфир, который имеет широкое коммерческое
применение в виде синтетического волокна лавсан), а
также в виде пленок и изделий, изготавливаемых из ПЭТматериала экструзией и литьем под давлением.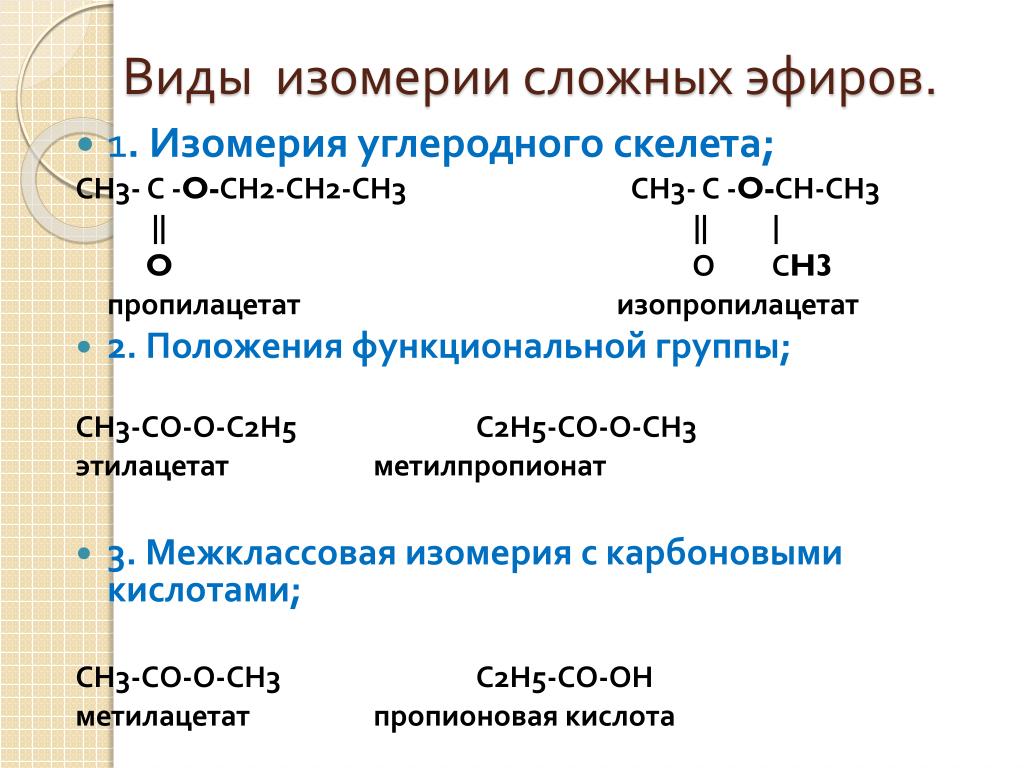
Реакция поликонденсации между терефталевой кислотой и
этиленгликолем
Домашнее задание
Параграф 21, №1-3, 8, 12
СПАСИБО ЗА
ВНИМАНИЕ!
Спирты и эфиры | Химия по специальностям
Результаты обучения
- Описывать строение и свойства спиртов
- Описать строение и свойства эфиров
- Назовите и нарисуйте структуры для спиртов и эфиров
Спирты
Включение атома кислорода в углерод- и водородсодержащие молекулы приводит к новым функциональным группам и новым семействам соединений. Когда атом кислорода присоединен одинарными связями, молекула представляет собой либо спирт, либо эфир.
Спирты – это производные углеводородов, в которых атом водорода заменен группой –ОН. Хотя все спирты имеют одну или несколько гидроксильных (-OH) функциональных групп, они не ведут себя как основания, такие как NaOH и KOH. NaOH и KOH являются ионными соединениями, которые содержат ионы OH – . Спирты представляют собой ковалентные молекулы; группа –ОН в молекуле спирта связана с атомом углерода ковалентной связью.
Спирты представляют собой ковалентные молекулы; группа –ОН в молекуле спирта связана с атомом углерода ковалентной связью.
Этанол, CH 3 CH 2 OH, также называемый этиловым спиртом, является особенно важным спиртом для человека. Этанол — это спирт, вырабатываемый некоторыми видами дрожжей, который содержится в вине, пиве и дистиллированных напитках. Его долгое время готовили люди, используя метаболические усилия дрожжей для ферментации различных сахаров:
Большие количества этанола синтезируются реакцией присоединения воды к этилену с использованием кислоты в качестве катализатора:
Могут быть получены спирты, содержащие две или более гидроксильных групп. Примеры включают 1,2-этандиол (этиленгликоль, используемый в антифризах) и 1,2,3-пропантриол (глицерин, используемый в качестве растворителя для косметики и лекарств):
Наименование спиртов
Название спирта происходит от углеводород, из которого он был получен. Финал – е в названии углеводорода заменяется на -ол , а атом углерода, с которым связана группа –ОН, обозначается цифрой, стоящей перед названием.
Вы можете просмотреть расшифровку «Именование спиртов с использованием правил номенклатуры ИЮПАК» здесь (откроется в новом окне).
Пример 1. Именование спиртов
Рассмотрим следующий пример. Как это должно называться?
Показать решение
Проверьте свои знания
Назовите следующую молекулу:
Показать решение
Эфиры
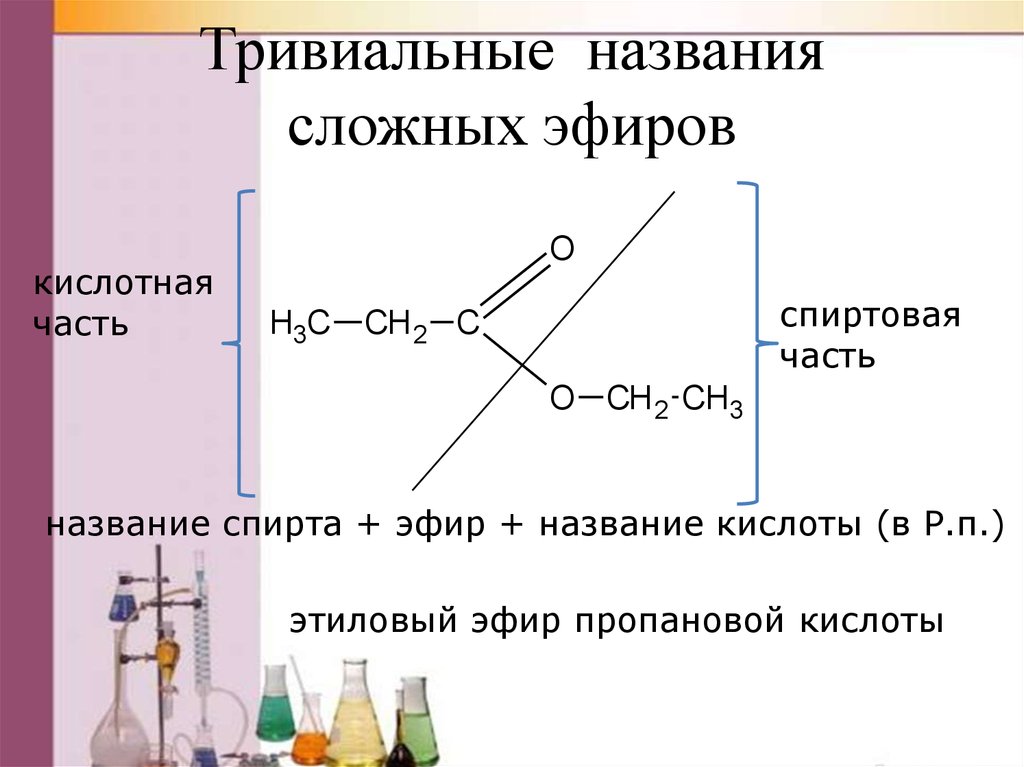
Эфиры представляют собой соединения, содержащие функциональную группу –O–. У простых эфиров нет обозначенного суффикса, как у других типов молекул, которые мы назвали до сих пор. В системе IUPAC атом кислорода и меньшая углеродная ветвь называются алкокси-заместителем, а остальная часть молекулы — основной цепью, как в алканах.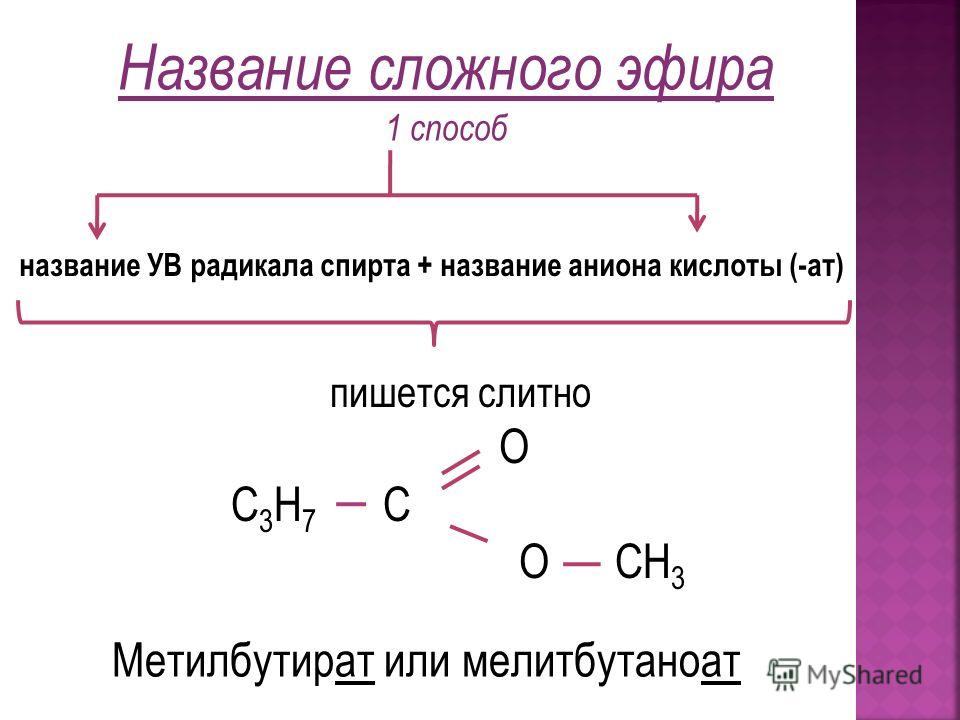 Как показано в следующем соединении, красные символы представляют меньшую алкильную группу и атом кислорода, который можно назвать «метокси». Более крупная углеродная ветвь будет этаном, что сделает молекулу метоксиэтаном. Многие эфиры называются общими именами вместо системных имен IUPAC. Для общих названий две ветви, связанные с атомом кислорода, называются отдельно, а за ними следует -эфир. Общее название соединения, показанного в Примере 2 – этилметиловый эфир:
Как показано в следующем соединении, красные символы представляют меньшую алкильную группу и атом кислорода, который можно назвать «метокси». Более крупная углеродная ветвь будет этаном, что сделает молекулу метоксиэтаном. Многие эфиры называются общими именами вместо системных имен IUPAC. Для общих названий две ветви, связанные с атомом кислорода, называются отдельно, а за ними следует -эфир. Общее название соединения, показанного в Примере 2 – этилметиловый эфир:
Пример 2. Именование эфиров
Укажите IUPAC и общепринятое название эфира, показанного здесь:
Показать решение
Проверьте свои знания
Укажите IUPAC и общее название показанного эфира:
Показать решение
Эфиры могут быть получены из спиртов отщеплением молекулы воды от двух молекул спирта. Например, при обработке этанола ограниченным количеством серной кислоты и нагревании до 140 °С образуются диэтиловый эфир и вода:
В общей формуле простых эфиров R— O —R углеводородные группы (R) могут быть одинаковыми или разными. Диэтиловый эфир, наиболее широко используемое соединение этого класса, представляет собой бесцветную летучую жидкость, которая легко воспламеняется. Впервые он был использован в 1846 году в качестве анестетика, но в настоящее время его место в значительной степени заняли более совершенные анестетики. Диэтиловый эфир и другие простые эфиры в настоящее время используются главным образом в качестве растворителей камедей, жиров, восков и смол. Третичный -Бутилметиловый эфир, C 4 H 9 OCH 3 (сокращенно МТБЭ — части названий, выделенные курсивом, не учитываются при ранжировании групп в алфавитном порядке — поэтому в обычном названии бутил стоит перед метилом), используется в качестве присадки к бензину. МТБЭ принадлежит к группе химических веществ, известных как оксигенаты, из-за их способности повышать содержание кислорода в бензине.
Диэтиловый эфир, наиболее широко используемое соединение этого класса, представляет собой бесцветную летучую жидкость, которая легко воспламеняется. Впервые он был использован в 1846 году в качестве анестетика, но в настоящее время его место в значительной степени заняли более совершенные анестетики. Диэтиловый эфир и другие простые эфиры в настоящее время используются главным образом в качестве растворителей камедей, жиров, восков и смол. Третичный -Бутилметиловый эфир, C 4 H 9 OCH 3 (сокращенно МТБЭ — части названий, выделенные курсивом, не учитываются при ранжировании групп в алфавитном порядке — поэтому в обычном названии бутил стоит перед метилом), используется в качестве присадки к бензину. МТБЭ принадлежит к группе химических веществ, известных как оксигенаты, из-за их способности повышать содержание кислорода в бензине.
Хотите попрактиковаться в именовании эфиров? Этот краткий видеообзор подытоживает номенклатуру эфиров.
Вы можете просмотреть стенограмму «Именование эфира и введение | Органическая химия | Академия Хана» здесь (открывается в новом окне).
Углеводы и диабет
Углеводы представляют собой большие биомолекулы, состоящие из углерода, водорода и кислорода. Пищевые формы углеводов — это продукты, богатые этими типами молекул, такие как макароны, хлеб и конфеты. Название «углевод» происходит от формулы молекул, которые можно описать общей формулой C m (H 2 O) n , что показывает, что они в некотором смысле являются «углеродом и водой» или «гидраты углерода». Во многих случаях m и n имеют одинаковое значение, но могут быть разными. Меньшие углеводы обычно называют «сахарами». Биохимический термин для этой группы молекул — «сахарид» от греческого слова «сахар» (рис. 1). В зависимости от количества сахарных единиц, соединенных вместе, их можно классифицировать как моносахариды (одна сахарная единица), дисахариды (две сахарные единицы), олигосахариды (несколько сахаров) или полисахариды (полимерная версия сахаров — полимеры были описаны в раздел о вторичной переработке пластика ранее в этой главе). Научные названия сахаров можно узнать по суффиксу 9.0035 –оза в конце названия (например, фруктовый сахар представляет собой моносахарид, называемый фруктозой, а молочный сахар представляет собой дисахарид, называемый лактозой, состоящий из двух моносахаридов, глюкозы и галактозы, соединенных вместе). Сахара содержат некоторые функциональные группы, которые мы обсуждали: обратите внимание на спиртовые группы, присутствующие в структурах, и на то, как моносахаридные звенья связаны с образованием дисахарида путем образования эфира.
1). В зависимости от количества сахарных единиц, соединенных вместе, их можно классифицировать как моносахариды (одна сахарная единица), дисахариды (две сахарные единицы), олигосахариды (несколько сахаров) или полисахариды (полимерная версия сахаров — полимеры были описаны в раздел о вторичной переработке пластика ранее в этой главе). Научные названия сахаров можно узнать по суффиксу 9.0035 –оза в конце названия (например, фруктовый сахар представляет собой моносахарид, называемый фруктозой, а молочный сахар представляет собой дисахарид, называемый лактозой, состоящий из двух моносахаридов, глюкозы и галактозы, соединенных вместе). Сахара содержат некоторые функциональные группы, которые мы обсуждали: обратите внимание на спиртовые группы, присутствующие в структурах, и на то, как моносахаридные звенья связаны с образованием дисахарида путем образования эфира.
Рисунок 2. На рисунках показаны молекулярные структуры фруктозы, пятиуглеродного моносахарида, и лактозы, дисахарида, состоящего из двух изомерных шестиуглеродных сахаров.
Организмы используют углеводы для различных функций. Углеводы могут накапливать энергию, например полисахариды гликоген у животных или крахмал у растений. Они также обеспечивают структурную поддержку, такую как полисахаридная целлюлоза в растениях и модифицированный полисахаридный хитин в грибах и животных. Сахара рибоза и дезоксирибоза являются компонентами остова РНК и ДНК соответственно. Другие сахара играют ключевую роль в функционировании иммунной системы, в межклеточном распознавании и во многих других биологических функциях.
Диабет — это группа метаболических заболеваний, при которых у человека наблюдается высокая концентрация сахара в крови (Рисунок 2). Диабет может быть вызван недостаточной выработкой инсулина поджелудочной железой или клетками организма, которые не реагируют должным образом на вырабатываемый инсулин. У здорового человека инсулин вырабатывается, когда он необходим, и функционирует для транспортировки глюкозы из крови в клетки, где она может использоваться для получения энергии. Долгосрочные осложнения диабета могут включать потерю зрения, болезни сердца и почечную недостаточность.
Долгосрочные осложнения диабета могут включать потерю зрения, болезни сердца и почечную недостаточность.
В 2013 г. было подсчитано, что примерно 3,3% населения мира (~380 миллионов человек) страдали диабетом, что ежегодно приводило к более чем миллиону смертей. Профилактика включает в себя здоровое питание, много физических упражнений и поддержание нормальной массы тела. Лечение включает в себя все эти методы образа жизни и может потребовать инъекций инсулина.
Рисунок 2. Сахарный диабет — заболевание, характеризующееся высокой концентрацией глюкозы в крови. Лечение диабета включает в себя изменение образа жизни, контроль уровня сахара в крови, а иногда и инъекции инсулина. (кредит: «Blausen Medical Communications»/Wikimedia Commons)
Основные понятия и резюме
Многие органические соединения, не являющиеся углеводородами, можно рассматривать как производные углеводородов. Углеводородное производное может быть образовано путем замены одного или нескольких атомов водорода углеводорода функциональной группой, которая содержит по меньшей мере один атом элемента, отличного от углерода или водорода. Свойства производных углеводородов во многом определяются функциональной группой. Группа –ОН является функциональной группой спирта. Группа –R–O–R– является функциональной группой эфира.
Свойства производных углеводородов во многом определяются функциональной группой. Группа –ОН является функциональной группой спирта. Группа –R–O–R– является функциональной группой эфира.
Попробуйте
- Почему соединения гексан, гексанол и гексен имеют такие похожие названия?
- Напишите сокращенные формулы и укажите названия IUPAC для следующих соединений:
- спирт этиловый (в напитках)
- Спирт метиловый (используется как растворитель, например, в шеллаке)
- этиленгликоль (антифриз)
- изопропиловый спирт, CH 3 CH(OH)CH 3 , используемый в медицинском спирте)
- глицерин
- Дайте полное название IUPAC для каждого из следующих соединений:
- Дайте полное название IUPAC и общепринятое название для каждого из следующих соединений:
- Напишите конденсированные структуры обоих изомеров по формуле C 2 H 6 O.
 Обозначьте функциональную группу каждого изомера.
Обозначьте функциональную группу каждого изомера. - Напишите сокращенные структуры всех изомеров с помощью формулы C 2 Н 6 О 2 . Обозначьте функциональную группу (или группы) каждого изомера.
- Нарисуйте сокращенные формулы для каждого из следующих соединений:
- дипропиловый эфир
- 2,2-диметил-3-гексанол
- 2-этоксибутан
- МТБЭ, метил трет -бутиловый эфир, CH 3 OC(CH 3 ) 3 , используется в качестве источника кислорода в насыщенных кислородом бензинах. МТБЭ получают путем взаимодействия 2-метилпропена с метанолом.
- Используя структуры Льюиса, напишите химическое уравнение реакции.
- Какой объем метанола плотностью 0,7915 г/мл требуется для производства ровно 1000 кг МТБЭ при условии выхода 100%?
- Напишите два полных сбалансированных уравнения для каждой из следующих реакций, одно с использованием сокращенных формул, а другое с использованием структур Льюиса.

- пропанол превращается в дипропиловый эфир
- обрабатывают водой в разбавленной кислоте.
Пропен
- Напишите два полных сбалансированных уравнения для каждой из следующих реакций, одно с использованием сокращенных формул, а другое с использованием структур Льюиса.
- 2-бутен обрабатывают водой в разбавленной кислоте
- обезвоживается с получением этилена
Этанол
.
Показать выбранные решения
Глоссарий
спирт: органическое соединение с гидроксильной группой (–ОН), связанной с атомом углерода
эфир: органическое соединение с атомом кислорода, связанным с двумя атомами углерода
Разница между сложным эфиром и простым эфиром
Сложный эфир и эфир представляют собой два различных функциональных класса органических соединений. Это производные, полученные в процессе, известном как этерификация/этерификация. Основное различие между ними заключается в их молекулярной структуре.
Основное различие между ними заключается в их молекулярной структуре.
Концепция сложного эфира
Сложный эфир представляет собой химическое соединение, полученное из кислоты. имеет приятный запах; вещества с низким молекулярным весом обычно используются в качестве ароматизаторов и содержатся в эфирных маслах и феромонах. Фосфоэфиры образуют основу молекул ДНК.
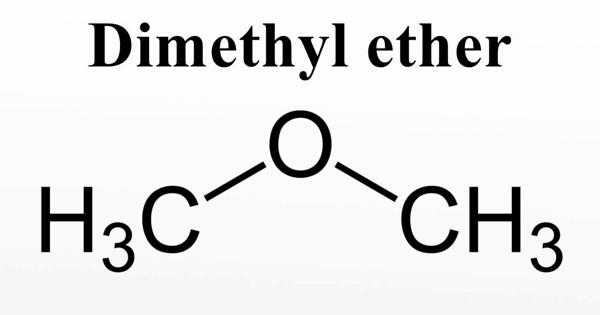
Понятие простого эфира
Простые эфиры имеют общую формулу R–O–R′, где R и R′ представляют собой алкильные или арильные группы. Типичным примером первой группы является растворитель и анестетик диэтиловый эфир, обычно называемый просто «эфир» (CH 3 –CH 2 –O–CH 2 –CH 3 ).
Обзор различий между сложным эфиром и простым эфиром:
Основное различие между сложным эфиром и простым эфиром заключается в том, что сложному эфиру необходимы два атома углерода и кислорода для завершения его структуры, полученной из карбоновых кислот, и иметь карбонильную группу, в то время как; Эфир и эфир оба являются функциональными группами и используются для классификации органических химических соединений. Эфир представляет собой органическую молекулу, имеющую два атома углерода, связанных с одним атомом кислорода, например, диметиловый эфир, в то время как сложный эфир представляет собой поэтому они отличаются друг от друга из-за своей структуры.
Эфир представляет собой органическую молекулу, имеющую два атома углерода, связанных с одним атомом кислорода, например, диметиловый эфир, в то время как сложный эфир представляет собой поэтому они отличаются друг от друга из-за своей структуры.
Что такое эфир?
Эфир представляет собой легковоспламеняющееся органическое соединение, в котором кислород соединяет алкильные и арильные группы с обеих сторон. Они имеют общую химическую формулу R–O–R′. Соединения эфира используются в промышленности, красителях, парфюмерии, масле и воске.
Структура эфира
В эфире 1 атом О образует связи с двумя атомами С, завершая свою структуру.
Этилацетат или этилэтанолат
(Изображение будет загружено в ближайшее время)
Метилбутаноат
(Изображение будет загружено в ближайшее время)
Пропилметаноат
(Изображение будет загружено в ближайшее время)
Пропилэтаноат
Этилпропаноат
Что такое этерификация?
Этерификация или алкилирование – это процесс, используемый для синтеза эфира путем дегидратации спирта.
(Изображение будет загружено в ближайшее время)
Что такое Эстер?
Сложный эфир представляет собой химическое соединение, образованное комбинацией органической или неорганической кислоты. Он должен иметь гидроксил (-OH), который заменен алкильной (-O-) группой. Сложные эфиры обладают приятным сладким ароматом, поэтому они используются в синтетических ароматизаторах, парфюмерии, средствах для снятия лака с ногтей, чернилах, фармацевтической промышленности и биодизельном топливе.
Структура сложного эфира
В структуре сложного эфира 2 атома О образуют связи с 2 атомами С.
Например,
(Изображение будет загружено в ближайшее время)
Этиловый эфир креатина
Общая химическая формула карбоксильного эфира: RCOOR’, где R и R’ — углеводороды. R’ представляет собой алкильную группу, тогда как R может представлять собой другую алкильную группу, или водород, или арильную группу.
(Изображение будет загружено в ближайшее время)
Эфиры карбоновых кислот
Что такое этерификация?
Процесс образования сложного эфира в результате реакции карбоновой кислоты со спиртом называется этерификацией.
Необходимо учитывать следующие ключевые различия между эфирными и эфирными группами.
Ester vs Ether: Key Differences On Various Parameters
Verticals | Ether | Ester |
Linkage | Простые эфиры представляют собой химические соединения, содержащие одинарную связь кислорода между двумя простыми углеводородными цепями. | Сложные эфиры представляют собой химические соединения, которые имеют двойную связь между кислородом и соседним углеродом. |
Tensile Strength | Ether is flexible | Ester has high tensile & tear strength |
Sliding abrasion | UV & wear-resistant | Greater |
Temperature resistance | They are less susceptible to industrial heat | They can withstand high-temperature longer |
Boiling Point | Меньше, чем спирт | Ниже, чем кислота и спирт |
Производное | alcohol | carboxylic acids |
Process of formation | Etherification | Esterification |
Functional group | –O- | –COO |
Связь между кислородом и углеродом | Одинарный | Двойной |
Structure | They may have a symmetrical structure | They do not have a symmetrical structure |
Polarization | Ethers have both polar or nonpolar bonds | Esters have polar bonds |
Растворимость в воде | Хорошие растворители | Могут до некоторой степени растворяться в воде |
Решенные примеры
Пример 1
Приведите химические реакции для бутилацетата.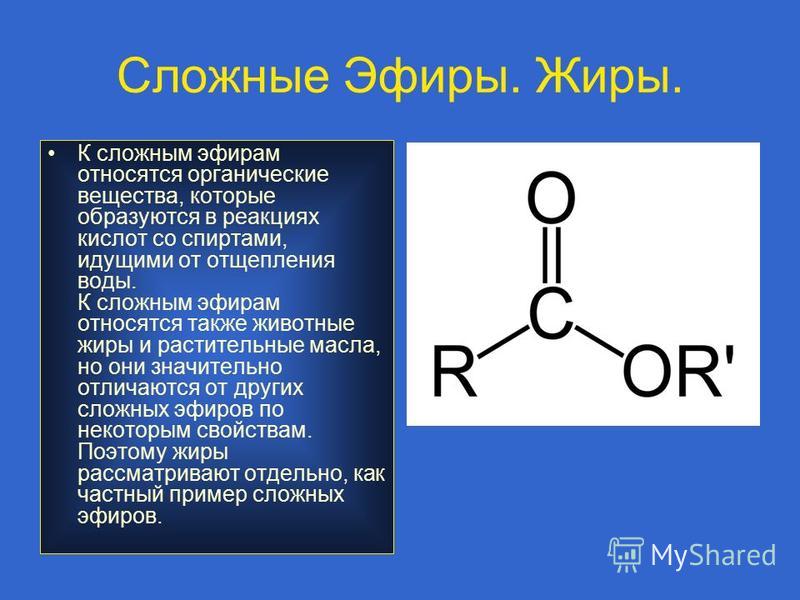
Бутилацетат представляет собой сложный эфир, образованный реакцией этерификации уксусной кислоты и 1-бутанола. Реакция протекает в присутствии минерального катализатора (H + ). При этом выделяется одна молекула воды.
(Изображение будет загружено в ближайшее время)
Это обратимая реакция.
Пример 2
Что такое Т-бутилметиловый эфир?
Метил-трет-бутиловый эфир или метил-трет-бутиловый эфир (МТБЭ) является компонентом бензина. Он используется в качестве оксигенатора для повышения октанового числа и вытеснения тетраэтилсвинца. Однако он производится во всем мире из-за растущего спроса на азиатских рынках. Использование МТБЭ вызывает споры в США.
МТБЭ также используется в медицинских процедурах на желчном пузыре для растворения камней в желчном пузыре.
МТБЭ искусственно синтезируется путем химической реакции метанола и изобутилена.
Знаете ли вы?
В старину эфир применяли в качестве анестетика в хирургии.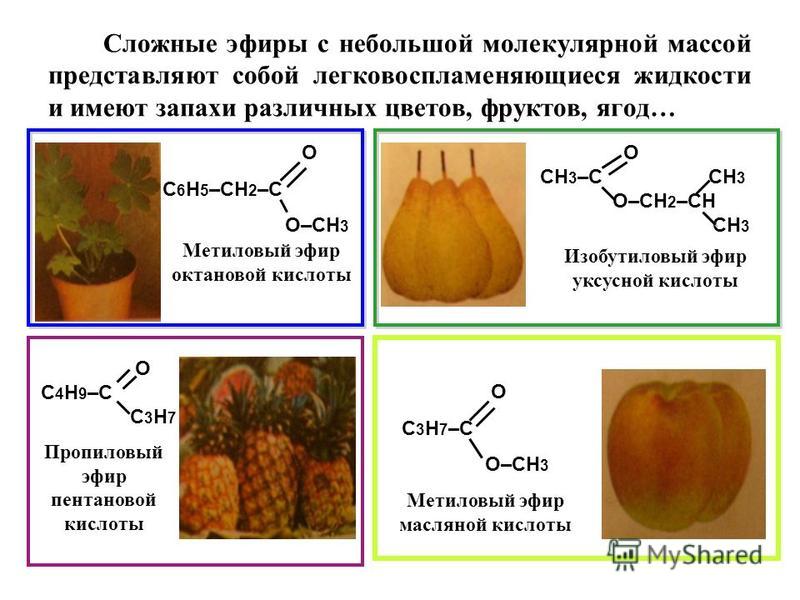





 СН3
СН3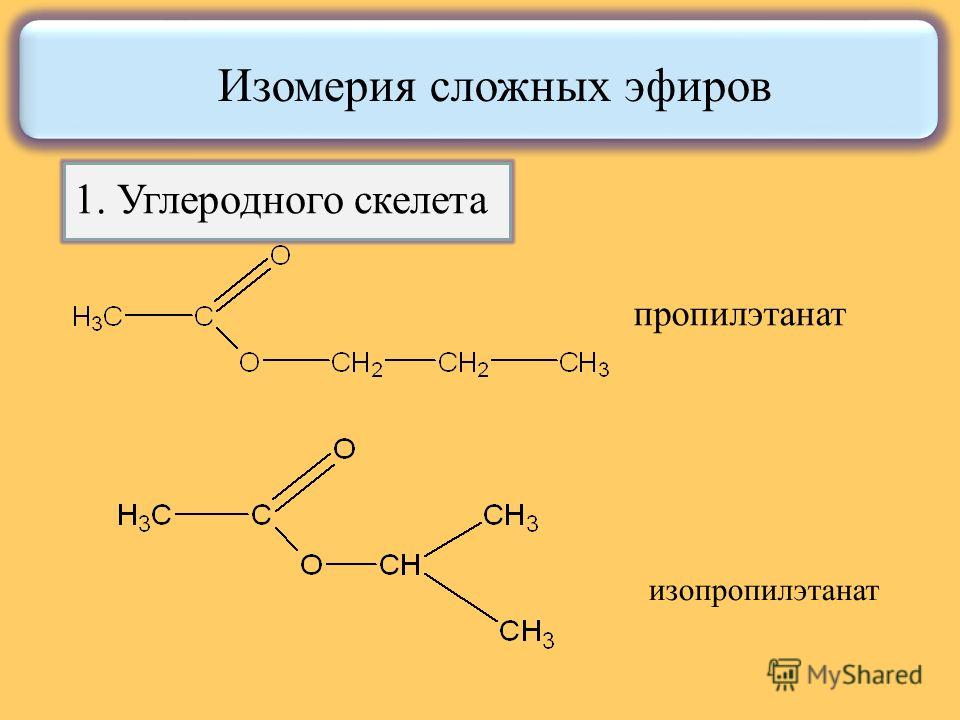
 2
2 Обозначьте функциональную группу каждого изомера.
Обозначьте функциональную группу каждого изомера.