Опыт 13. Получение простого диэтилового эфира. Диэтиловый эфир получение
формула. Диэтиловый эфир: физические и химические свойства :: SYL.ru
Сотни лет назад известному ученому того времени Луллию, которого после смерти стали называть алхимиком, удалось открыть незаменимый в настоящее время диэтиловый эфир. Формула, свойства, температура кипения, способы получения вещества будут подробно описаны в данной статье.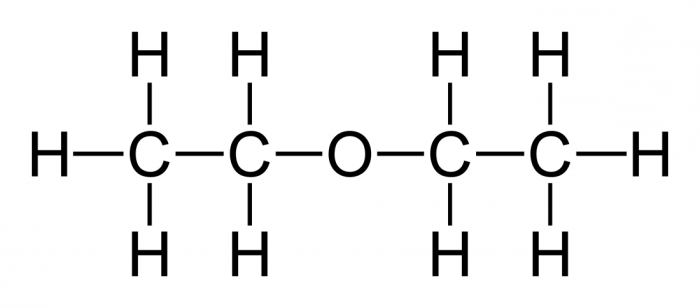
История
В 13 веке известный испанский ученый Раймонд Луллий открыл диэтиловый эфир. Свойства его были описаны в 1540 году не менее известным научным деятелем Парацельсом. В 1846-м эфир впервые попробовали использовать в качестве наркоза. Операция, проведенная американским врачом Д. Уорреном с применением паров этого вещества, прошла успешно. Изобретателями наркоза считают стоматолога У. Мортона и его наставника – врача и химика Ч. Джексона.
Способы получения эфира в 16 столетии описал Валериус Кордус – известный ботаник и фармацевт родом из Касселя. С начала 18 века спиртово-эфирная смесь использовалась в качестве успокаивающего средства – это было предложение Фридриха Гофмана. Петербуржский аптекарь Томас Ловиц в 1796 году получил чистый диэтиловый эфир, формула которого, кстати, имеет два варианта (об этом немного позже). А вот принцип действия упомянутого вещества на организм человека обнародовал английский физик М. Фарадей, после чего в 1818 году была опубликована даже научная статья, посвященная этой теме.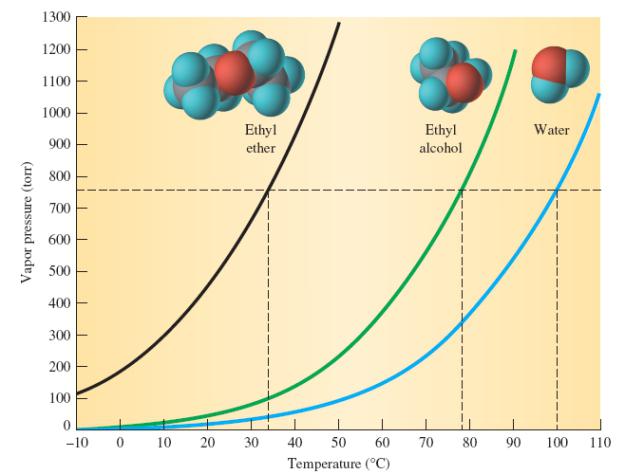
Характеристика
Что же называют простым эфиром? Это органическое соединение, молекулы которого состоят из двух углеводородных радикалов и атома кислорода. Наиболее важен простой, диэтиловый эфир, формула которого имеет следующий вид:
(С2Н5)2О или С4Н10О.
Он представляет собой бесцветную, прозрачную, очень подвижную летучую жидкость, имеющую своеобразный запах и жгучий вкус.
Под воздействием света, воздуха, тепла и влаги эфир способен разлагаться, образовывая при этом токсичные альдегиды, пероксиды и кетоны, которые раздражают дыхательные пути.
При температуре воды в 20 градусов растворяется на 6,5%. Хорошо смешивается с жирными и эфирными маслами, бензолом и спиртом, независимо от соотношения.
Сам эфир, впрочем, как и его пары, легко воспламеняется. В определенной пропорции с кислородом или же воздухом пары диэтилового эфира, используемые для наркоза, взрывоопасны.
Химические свойства
Для диэтилового эфира характерны все химические свойства простых эфиров. Итак, разберемся с этим вопросом подробнее. Это довольно инертное вещество. Основное отличие от сложных эфиров – отсутствие гидролиза, правда, есть и исключения. На холоде не взаимодействует с хлоридом фосфора, металлическим натрием и многими разбавленными минеральными кислотами. Несмотря на это, концентрированные кислоты (серная и йодоводородная) даже при низких температурах разлагают эти эфиры, а нагретый металлический натрий их расщепляет.
Эфир с неподеленными парами электронов взаимодействует с протоном сильной кислоты, в результате чего образуется неустойчивое оксониевое соединение:
- Ацидолиз. Серная и йодоводородная кислоты, а также FeCl3 в ангидриде уксусной кислоты способны расщеплять простые эфиры. Химическая реакция выглядит так: Ch4—Ch3—O—Ch3—Ch4 + HJ → Ch4—Ch3—OH + J—Ch3—Ch4.
- Реакция металлирования, получившая название реакции Шорыгина. Нагретый металлический натрий расщепляет диэтиловый эфир: C2H5–O–C2H5 + 2Na → C2H5ONa + C2H5Na
- Относительная химическая инертность не препятствует эфирам при хранении на воздухе образовывать перекиси, что зачастую приводит к взрывам в конце перегонки.
Диэтиловый эфир: физические свойства
Своеобразный запах, низкая температура кипения простых эфиров – свидетельство слабого межмолекулярного воздействия, а это говорит о низкой полярности и отсутствии предпосылок к образованию водородных связей. В отличие от спиртов эфирам присущи более сильные электронодонорные свойства, что подтверждается значением потенциалов ионизации. Усиление этих особенностей связано с положительным индуктивным эффектом группы атомов, получающихся из алканов при удалении атома водорода.
Температура кипения диэтилового эфира – 35,6 градуса по Цельсию (это гораздо ниже, чем у изомерных спиртов), а замерзания – 117 оС. Простые эфиры почти не смешиваются с водой. Объяснение этому довольно простое: они не способны образовывать водородные связи, поскольку их молекулы не имеют полярных связей. Плохо растворяется в воде и диэтиловый эфир, плотность которого по отношению к оксиду водорода составляет 0,714. Одной из особенностей рассматриваемого вещества является склонность к электризации. Вероятность возникновения разрядов статического электричества особо высока при переливании или сливе химсостава, в результате чего может произойти воспламенение. Пары эфира образуют с воздухом, который в 2,5 раза легче, взрывчатые смеси. Нижний предел взрываемости – 1,7%, а верхний – 49%. Работая с эфиром, не следует забывать, что его пары имеют свойство распространяться на большие расстояния без потерь способности к горению. Так что основная мера предосторожности – отсутствие вблизи открытого огня и прочих источников воспламенения.
Простой эфир – малоактивное соединение, в разы менее реакционноспособное по сравнению со спиртами. Замечательно растворяет большую часть органических веществ, благодаря чему используется в качестве растворителя. Исключением не является и диэтиловый эфир. Физические свойства, равно как и химические, позволяют применять его в медицине и на производстве.
Получение диэтилового эфира
Простые эфиры в природе не встречаются - их получают синтетическим путем. Под воздействием кислотных катализаторов на этиловый спирт при повышенной температуре получается диэтиловый эфир (формула указана выше). Проще всего получить это вещество посредством перегонки смеси, состоящей из серной кислоты и спирта. Для этого ее необходимо разогреть до 140-150 градусов по Цельсию. Нам понадобится этиловый спирт и серная кислота (в равных пропорциях), пипетки, пробирки и газоотводные трубки.
Итак, после того как оборудование и реактивы подготовлены, можно приступать к проведению опыта. В пробирку (она обязательно должна быть сухой) необходимо налить 2-3 мл смеси спирта и кислоты и медленно нагреть. Как только начнется кипение, горелка убирается, а в горячую смесь при помощи пипетки по стенке пробирки добавляется от 5 до 10 капель этилового спирта. Протекающая реакция выглядит следующим образом:
- СН3—СН2—ОН (этилсерная кислота) + h3S04 СН3—СН2—OSO3H + Н2О;
- Ch4—СН2—OSO3H + СН3—СН3—О;
- СН3—СН2—О—СН2—СН3(диэтиловый эфир)+ Н2SO4.
Об образовании диэтилового эфира свидетельствует появившийся запах.
Использование в медицине
В качестве лекарственного средства общеанестезирующего действия медики используют диэтиловый эфир. Свойства этого вещества не позволяют применять его при операциях, где задействуются электроинструменты, поскольку оно легко воспламеняется, а при соединении с воздухом может взорваться. Диэтиловый эфир широко распространен в хирургии, где используется для ингаляционного наркоза. В стоматологии им обрабатывают зубные корневые каналы и кариозные места, подготавливая, таким образом, полость рта к пломбированию.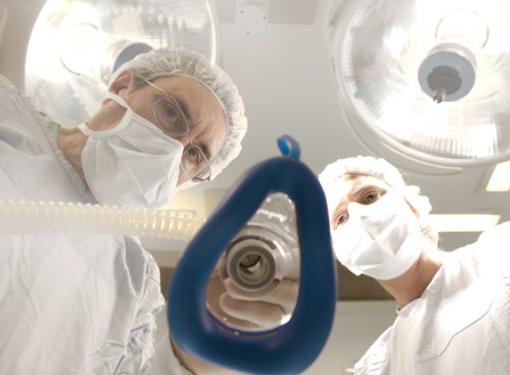
Диэтиловый эфир как топливо
Вещество обладает высоким цетановым числом (85-96), благодаря чему его можно использовать как стартовую жидкость для бензиновых и дизельных двигателей. Благодаря высокой изменчивости и низким температурам вспышки диэтиловый эфир применяют в качестве составляющей топливной смеси для образцовых дизельных двигателей. Получается, что данное вещество подобно этанолу.
Правильное хранение
Диэтиловый эфир рекомендуется хранить в бутылочках темного цвета (тщательно закупоренных) в прохладном месте, поскольку на свету, в тепле и под воздействием влаги он разлагается, в результате чего выделяются токсические вещества.
www.syl.ru
Опыт 13. Получение простого диэтилового эфира
Реактивы и оборудование: смесь этилового спирта и концентрированной серной кислоты в объемном соотношении 1:1, этиловый спирт; пипетки, прямые газоотводные трубки с оттянутыми концами, пробирки.
В сухую пробирку наливают 2—3 мл смеси этилового спирта и концентрированной серной кислоты (1:1) и осторожно нагревают до начинающегося кипения. Затем горелку убирают и к горячей смеси по стенке пробирки добавляют пипеткой 5—10 капель этилового спирта.
СН3СН2ОН + h3SO4 СН3СН2OSO3H + Н2О
этилсерная кислота
t
СН3СН2OSO3H + СН3СН2ОН СН3СН2ОСН2СН3 + h3SО4
диэтиловый эфир
Образование диэтилового эфира обнаруживают по запаху. Потом пробирку закрывают пробкой с прямой газоотводной трубкой с оттянутым концом, осторожно ее нагревают и поджигают выделяющийся эфир.
Напишите механизмы реакций образования этилсерной кислоты и диэтилового эфира (SN2).
3.2. Фенолы Осторожно! Фенолы вызывают ожоги кожи Опыт 14. Образование и разложение фенолятов
Реактивы и оборудование: фенол, 10%-ный раствор гидроксида натрия, 10%-ный раствор серной кислоты, пробирки.
К 2 мл смеси фенола с водой прибавляют по каплям при перемешивании 10%-ный раствор гидроксида натрия до полного растворения фенола:
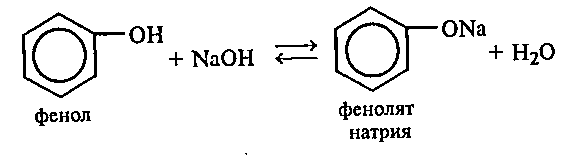
К полученному раствору фенолята натрия по каплям приливают 10%-ный раствор серной кислоты. Наблюдают помутнение раствора в результате разложения фенолята натрия серной кислотой и выделения малорастворимого в воде фенола:
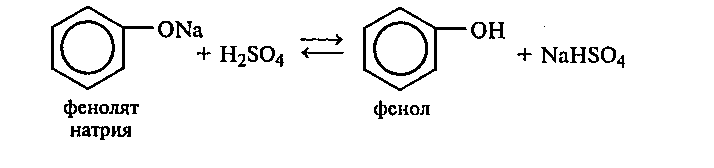
Объясните происходящее. Сравните свойства фенолов с алифатическими спиртами в данной реакции.
Опыт 15. Взаимодействие фенола с бромной водой
Реактивы и оборудование: 5%-ный раствор фенола, бромная вода; пробирки.
В пробирку наливают 1 мл 5%-ного раствора фенола и по каплям приливают бромную воду. Наблюдают образование белого осадка. При добавлении избытка бромной воды осадок становится желтым.
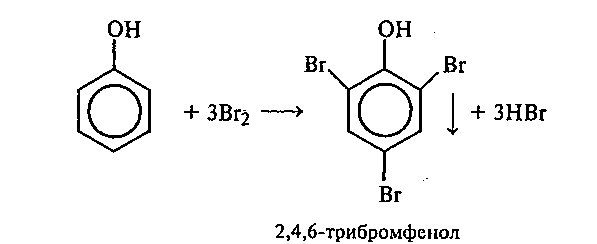
Рассмотрите механизм реакции бромирования фенола (SE). Почему реакция бромирования фенола идет в более мягких условиях по сравнению с толуолом и бензолом? Какой продукт образуется при действии избытка бромной воды на трибромфенол?
Опыт 16. Окисление фенола
Реактивы и оборудование: 5%-ный раствор фенола, 5%-ный раствор карбоната натрия, 1%-ный раствор перманганата калия; пипетки, пробирки.
В пробирке смешивают 1 мл 5%-ного раствора фенола и 1 мл 5%-ного раствора карбоната натрия. По каплям при перемешивании приливают 1%-ный раствор перманганата калия. Наблюдают обесцвечивание раствора и выпадение бурого осадка оксида марганца (IV).
Объясните наблюдаемое изменение окраски. Напишите реакцию окисления фенола.
Опыт 17. Взаимодействие фенолов с хлоридом железа (III)
Реактивы и оборудование: 1%-ный раствор фенола, 1%-ный раствор пирокатехина, 1%-ный раствор резорцина, 1%-ный раствор гидрохинона, 1%-ный раствор пирогаллола, 2%-ный раствор хлорида железа (III), 2М раствор гидроксида натрия; пипетки, фильтровальная бумага.
Реакция с хлоридом железа (III) является качественной на енольные и фенольные гидроксильные группы.
В четыре пробирки наливают по 1 мл 1%-ных растворов: в первую — фенола, во вторую — пирокатехина, в третью — резорцина, в четвертую — гидрохинона. В каждую пробирку добавляют по 3—4 капли 2%-ного раствора хлорида железа (III). В пробирке с фенолом появляется сине-фиолетовая окраска, с пирокатехином — зеленая, с резорцином — фиолетовая, с гидрохиноном — зеленая, очень быстро переходящая в желтую (гидрохинон окисляется в хинон).
Следует помнить, что растворы фенолов должны быть приготовлены не ранее, чем за 1-2 дня до проведения реакции, так как фенолы легко окисляются и их растворы темнеют.
studfiles.net
Диэтиловый эфир получение из спирта
Название серный сохранилось от первоначального способа получения диэтилового эфира взаимодействием спирта с серной кислотой, [c.312]Это не просто формальная схема. Простые эфиры действительно можно получить указанным способом. Хорошо изученной реакцией этого типа является получение диэтилового эфира (в обиходе называемого эфиром). При смешивании концентрированной серной кислоты с этиловым спиртом идет реакция с образованием сложного эфира (т. е. спирт этерифицируется серной кислотой) [c.167]
Получение нативных лигнинов. Термин нативный используют не в буквальном переводе как синоним термина природный , а для обозначения препаратов лигнина, получаемых обработкой древесины (после экстрагирования диэтиловым эфиром или спирто-толуольной смесью) нейтральными органическими растворителями при комнатной температуре без применения кислотных катализаторов. Чаще всего получают нативный лигнин Браунса извлечением 95%-м этанолом при температуре около 20°С. Этот препарат назвали нативным лигнином, поскольку при выделе- [c.369]Некоторый интерес представляет гидролиз диэтилового эфира, так как при получении синтетического каучука по методу Лебедева образующиеся побочные продукты содержат значительное количество диэтилового эфира. Последний рационально вновь превращать в спирт для получения из него дивинила. Эту операцию удобно вести в паровой фазе с водяным паром над Л1 О..-катализатором при 300—350° или с серной кислотой. [c.529]
Простейшим примером этой группы реакций служит получение простых эфиров из индивидуальных спиртов. Образован .диэтилового эфира из этилового спирта является наиболее давно известной реакцией. [c.460]
Разложение этилсерной кислоты в вакууме [1371 ведет к получению диэтилсульфата с небольшим выходом, но при атмосферном давлении реакция протекает обычным путем с образованием этилена [138]. Обратная реакция указана ниже (стр. 38). При перегонке смеси, содержащей бариевую соль этилсерной кислоты, в качестве одного из главных продуктов реакции прлу-чается диэтилсулъфат [139]. Калиевые соли этил-, изобутил- и изо-амилсерных кислот при нагревании выше 250° превращаются в олефины и соответствующие спирты [140]. Этилсульфат ка-лпя, кроме того, дает небольшое количество диэтилового эфира. Аммониевые соли этил-, к-иропил- и изобутилсерных кислот не перегруппировываются в соли аминов [133, 141], вместо них образуются олефины. н-Октилсульфат бария [6] при 100° дает октилен. Нагревание алкилсерной кислоты приблизительно до 300° в присутствии соли, которая может перевести свободную серную кислоту в инертное соединение, способствует образованию олефина [142]. [c.26]
Диэтиловый эфир получен нагреванием диметилового эфира нафталевой кислоты с этиловым спиртом в присутствии небольшого количества этилата натрия [3231. Вислиценус и Понндорф синтезировали этот эфир с почти количественным выходом многочасовым нагреванием серебряной соли нафталевой кислоты с иодистым этилом при 100 "С кристаллизуется из спирта в листочках. Т. пл. 59—60 °С, т. кип. 238—239 "С при 19 мм рт. ст. [451[. Ди-н-бутиловый эфир, т. пл. 52—53 °С [1821. [c.148]
Впервые диэтиловый эфир получен в 1540 г. нагреванием этилового спирта с серной кислотой, откуда произошло его неправильное название серный эфир . [c.208]
Был предложен [324] метод получения безводного этанола путем азеотропной ректификации, с использованием в качестве разделяющего агента диэтилового эфира, дающего с водой азеотропную смесь с минимумом температуры кипения. Для того чтобы повысить содержание воды в азеотропе, процесс проводится под давлением 6—11 ати. Конденсат азеотропа эфир— вода расслаивается. Эфирный слой возвращается в колонну, а отбирается только водный слой, из которого затем отгоняется содержащийся в нем эфир. Абсолютный этиловый спирт получается в процессе азеотропной ректификации в виде кубовой жидкости. [c.283]
При получении этанола прямой гидратацией этилена из 1000 кг газа получают 1460 кг спирта, 31 кг диэтилового эфира. 30 кг смол и 15 кг ацетальдегида. Какова селективность катализатора по спирту [c.128]
Диэтиловый (этиловый) эфир. Имеет очень большое практическое значение его обычно называют просто эфиром. Получается главным образом дегидратацией этилового спирта при действии концентрированной серной кислоты (стр. 109). Этим методом диэтиловый эфир был получен впервые еще в 1540 г. В. Кордусом долгое время диэтиловый эфир неправильно называли серным эфиром, так как предполагали, что он должен содержать серу. В настоящее время диэтиловый эфир получают так же, пропуская пары этилового спирта над окисью алюминия А120д, нагретой до 240—260 С. [c.129]
Полученные закономерности были проверены на растворах нитрата кобальта в различных органических растворителях (изопропиловом спирте, метиловом спирте, метилизобутилкетоне и диэтиловом эфире). Полученные результаты показали, что выявленная закономерность для чистых растворителей при определении 2п, Си и Mg сохраняется и при определении данных примесей в органическом растворе соли. [c.200]
В 1959 г. Коп и Додж [74] вычислили равновесные концентрации этанола, получаемого гидратацией этилена, с учетом образования диэтилового эфира. Полученные ими результаты приведены в табл. 15. Как видно из данных этой таблицы, учет образования эфира вносит существенные изменения в состав жидкой и паровой фаз. Авторы сообщили, что в отдельных опытах, проведенных с катализатором — серной кислотой — при 221° С и давлении 273 атм, им удалось получить выходы этилового спирта и диэтилового эфира, близкие к равновесным. [c.44]
Полученную кашицу переносят в колбу, снабженную мешалкой с водяным или ртутным затвором, заливают 100 мл 20%-ной НС1 (ч.), вытесняют из колбы воздух водородом и нагревают до 70—90 °С при перемешивании до прекращения растворения остатков непрореагировавшего алюминия. После охлаждения реакционной смеси осадок промывают водой декантацией до исчезновения кислой реакции промывных вод, затем отсасывают на воронке Бюхнера и промывают этиловым спиртом и диэтиловым эфиром. Полученную смесь сушат сначала на воздухе, а в конце — слабо нагревая в струе водорода. [c.231]
Определение неомыляемых сводится к омылению жира и извлечению не-омыляемой части петролейным или диэтиловым эфиром. Полученные после омыления спиртовые растворы разбавляются водой перед экстракцией петролейным эфиром так, чтобы концентрация спирта составляла 50%. В большинстве случаев извлечение петролейным эфиром, имеющим низкую температуру кипения, обходится без образования эмульсии. Затруднения возникают только в тех случаях, когда исследуемый жир содержит много холестерина, как, например, рыбий жир. [c.361]
Ректификацию осуществляют в одной колонне. При этом получают этиловый спирт-ректификат с содержанием ацетальдегида не выше 2% и до 1% диэтилового эфира. Если спирт идет на получение бутадиена, ацетальдегид е мешает процессу. Такой спирт пригоден для получения и ацетальдегида, и уксусной кислоты. [c.155]
При повышении концентрации кислоты и температуры несколько увеличивается скорость абсорбции, но одновременно значительно усиливается полимеризация этилена и возрастает выход диэтилового эфира. На получение 1 т 100%-ного этилового спирта расходуется 700—718 кг этилена. [c.224]
Диэтиловый эфир (СгНб) называется также серным, или этиловым, эфиром. Получение его из этилового спирта и серной кислоты уже рассматривалось выше. Он представляет собой подвижную, очень горючую и легколетучую жидкость (т. кип. +34,6°). Смеси паров эфира с воздухом взрывчаты. Этиловый эфир немного растворим в воде в 100 вес. ч. воды при 16° растворяются 7,5 вес. ч. эфира с другой стороны, эфир растворяет небольшое количество воды (1 — 1,57о при комнатной температуре). [c.152]
При действии на амиловый спирт перманганата калия образуется раствор валериановой кислоты в спирте. Какое количество кислоты можно извлечь из 100 мл полученного раствора, содержащего 3,7 г кислоты, экстракцией 30 мл диэтилового эфира Коэффициент распределения валериановой кислоты в указанной системе равен 0,043, [c.183]
В полученном препарате могут быть примеси диэтилового эфира и этилового спирта, которые легко обнаружить с помощью газовой хроматографии. Бромистый этил освобождают от примесей промыванием в делительной воронке концентрированной серной кислотой. [c.109]
СЕРНЫЙ ЭФИР — устаревшее название диэтилового эфира, возникшее в связи с его главным способом получения (действием серной кислоты на этиловый спирт). [c.225]
Процесс превращения этилового спирта в диэтиловый эфир является примером реакции алкилирования. Превращение это можно осуществить также и в газовой фазе, пропуская пары спирта при температуре 200—300 °С над водоотнимающими катализаторами (оксиды алюминия, титана, тория, ванадия). Из высших спиртов (особенно вторичных и третичных) выход эфиров по описанному способу меньше, чем при получении диэтилового эфира, а фенолы этим путем совсем не образуют простых эфиров. [c.167]
Этанол (метилкарбинол, этиловый спирт) — бесцветная подвижная жидкость с жгучим вкусом и характерным запахом. Температура кипения этанола 78,4°С, температура плавления -114,15°С, плотность 0,794 т/м . Этанол смешивается во всех отношениях в водой, спиртами, глицерином, диэтиловым эфиром и другими органическими растворителями. С некоторыми из них (водой, бензолом, этилацетатом, хлороформом) он образует азеотропные смеси различного состава. Азеотропная смесь с водой, содержащая 95,6% об. этанола, кипит при постоянной температуре 78,1°С. Поэтому, для получения безводного ( абсолютного ) этанола в промышленности используют специальные методы его обезвоживания, например, абсолютирование бензолом. Этанол образует алкоголяты с солями кальция и магния, например СаС12 4С2Н50Н и МяСЬ бСгНбОН. [c.270]
Ректификация осуществляется в одной колонне получается апирт-ректификат с содержанием не выше 2% ацетальдегида и до 1 % диэтилового эфира. Если спирт идет на получение дивинила, то ацетальдегид не мешает процессу. Спирт пригоден также и для получения уксусного альдегида и уксусной кислоты. [c.214]
Вскрытие серной кислотой. По сернокислотному методу [9] отвальный кек подвергается действию 98%-ной НзЗО (Т Ж = I 1) в течение 4 ч при 220° С, что обеспечивает практически полный переход скандия в воднорастворимое состояние. При водном выщелачивании сульфатизированной массы в раствор вместе со скандием (0,2—0,3 г/л) переходит большая часть железа (15—25 г л) и марганца (15—20 г л), цирконий, титан, торий, редкоземельные элементы, алюминий, ниобий, тантал и другие примеси. Для отделения от железа и марганца, которые являются основными примесями, используется способность скандия к образованию комплексных карбонатов с содой Ыа53с(СОз)4, и с карбонатом аммония — ЫН48с(СОз)2, растворимых в избытке соответствующего карбоната. Осуществляют эту операцию следующим образом. Сернокислотные растворы после нейтрализации аммиаком до pH 2 и кипячения в течение 30—40 мин отстаивают, декантацией отделяют осадок, который отмывают горячей водой. Объединенные основной и промывной растворы при перемешивании вливают в 20%-ный раствор соды или карбоната аммония равного объема. После 2-часового отстаивания раствор, в котором содержится скандий, отделяют от осадка, где остается основная часть Ре, Мп и Са. Осадок подвергают 3-кратной репульпации 10%-ным раствором соды. Из объединенных основного и промывного растворов после подкисления соляной кислотой (pH гидроокись скандия осаждают прибавлением концентрированного раствора аммиака. Прокаливанием при 850° С гидроокись переводят в окись, содержащую 40—70% ЗсгОд. Схема процесса представлена на рис. 54. Основные примеси в полученном концентрате — Т1, 2х, А, Ве, ТЬ и РЗЭ. От Т1, 2г, ТЬ и РЗЭ отделяют экстракционными методами с применением в качестве экстрагентов диэтилового эфира, изоамилового спирта, бутилацетата, ацетофенона. Для отделения от А1 и Ве можно осаждать скандий в виде оксалата. Извлечение скандия в окись чистотой 99,99% составляет 80—88% [9]. [c.262]
Полученные хлорангидриды, за иск.11ючением хлорангидрида -ацет-окси-р-хлорпропилфосфиновой кислоты (VI R = СНд), были затем превращены в соответствующие диэтиловые эфиры действием спирта в присутствии или отсутствие основания. Их формулы приведены ниже [c.239]
Температура кипения чистого бромистого этила 38 °С. Полученный бромистый этил может содержать нримеси диэтилового эфира и спирта. Для освобождения от спирта и эфира бромистый этил можно промыть серной кислотой. Необходимость в такой операции можно определить хроматографически. [c.32]
По принятому в технике методу получения эфиров, главным образом диэтилового эфира, в качестве исходных веществ применяют снирт и серную кислоту. В результате многих тщательных исследовании, особенно Виллиа.мсона, наиболее существенные стадии этого процесса вполне выяснены. Сначала спирт взаимодействует с серной кислотой, образуя алкилсериую кислоту и воду. Затем алкилсерная кислота при нагревании реагирует со второй молекулой спирта, — образуется эфир к регенерируется серная кислота [c.149]
Исходным продуктом для получения чистых транс- и цис-/изомеров пиперилена служила амилен-пипериленовая фракция, являющаяся побочным продуктом в синтезе бутадиена-1,3 из этилового спирта. Фракция представляет собой в основном смесь продуктов из цис- и транс-пиперилена, амиленов, диэтилового эфира, альдегидов, циклопентадиена и изопрена. Большую часть в ней составляют пиперилен (около 85%), амилены и диэтиловый эфир. Диэтиловый эфир -сравнительно легко удаляется из исходного (Продукта многократной промывкой его водой. От альдегидов продукт. может быть освобождай путем осмоления их при повышенной температуре над твердой щелочью (при кипячении) и обра- боткой раствором соляношслого шдрокоилам1ина. Из оставшейся смеси углеводородов выделение пиперилена и разде- [c.83]
При дегидратации этанола образуются этилен и диэтиловый эфир. Количество брома (М 160), которое прореагировало с этиленом, составляет 16 г (0,1 моля), что эквимолекулярно количеству этилена (0,1 моля, 22,4 л) и еоответственно этиловому спирту (0,1 моля, 4,6г), из которого получен этилен. Количество спирта, из которого образовался диэтиловый эфир, находим по разности 23 г — 4,6 г=18,4 г, что составляет 0,4 моля. Согласно уравнению (2), из 0,4 моля этилового спирта образуется 0,2 моля (14,8 г) диэтилового эфира С4Н10О, так как выход по условию задачи количественный. Следовательно, из спирта было получено 2,24 л этилена и 14,8 г диэтилового эфира. [c.203]
Несравненно чаще встречается в практике этиловый эфир—(С2Н5)20, получаемый обычно действием этилового спирта на серную кислоту (водоотнимающее средство) при повышенной температуре. В связи с таким способом получения этиловый эфир иногда неправиль( о называют серным . Этиловый (точнее, диэтиловый) эфир представляет собой бесцветную летучую жидкость (т. пл. —116, т. кип. +35 °С). Пары его легко воспламеняются на воздухе, а при вдыхании вызывают состояние опьянения и затем наркоза. В воде этиловый эфир заметно растворим (V 2 доп. 20). [c.559]
Среди низкомолекулярных алифатических спиртов, получаемых гидратацией, ведущее место принадлежит этиловому спирту. Наиболее крупный потребитель этанола — промышленность синтетического каучука. Кроме того, он идет на получение уксусного альдегида, уксусной кислоты, диэтилового эфира, этилацетата. В СССР синтетический этиловый спирт получают преимущественно прямой гидратацией этилена, применяя в качестве катализатора фосфорную кислоту на силикагеле. Примерный план аналитического контроля одного из таких цехов представлен в приложении I. Независимо от метода гидратации этилена, на синтетический этиловый спирт по ГОСТ П547—65 предъявляются единые требования (табл. 33). [c.151]
chem21.info