Большая Энциклопедия Нефти и Газа. Уксусноэтиловый эфир формула
Этилацетат в косметике (Ethyl acetate, E1504)
Этилацетат в косметике Ethyl acetate, E1504 - растворитель и смягчитель.
Свойства этилацетата, применяемые в косметике:
Растворяющее. Этилацетат легко вступает в реакции с органическими веществами и эффективно растворяет жиры, воски, масла, смолы, растворяется в спирте, эфире и немного хуже - воде. Поэтому этилацетат включают в состав косметики, предназначенной для очистки или обезжиривания – например, средствах для ухода за волосами, ногтями.
Ароматическое. Этилацетат обладает легким и приятным фруктовым ароматом, что позволяет использовать его в качестве эффективного растворителя растительных смол и эфирных масел при создании парфюмов, не опасаясь того, что духи будут дурно пахнуть.
Смягчающее. Этилацетат за счет содержания ионов уксусной кислоты обладает смягчающими свойствами, поэтому его включение в косметические средства позволяет смягчить кожу.
В какой косметике встречается этилацетат?
- лак для ногтей
- жидкость для снятия лака
- парфюмы
- шампунь
- краска для волос
- крем после бритья
- смягчающий крем для рук
Косметику с этилацетатом хранят подальше от источников тепла и солнечных лучнй.
Применение косметики с этилацетатом нежелательно:
- при склонности к аллергии
- при бронхиальной астме
- в случае повышенной чувствительности кожи
Этилацетат в медицине
В медицине этилацетат нашел широкое применение благодаря экстрагирующим способностям. Этилацетат используется в производстве препаратов противовоспалительного и обезболивающего ряда, лекарств от аллергии и кишечных расстройств. Этилацетат применяют при производстве кофе без кофеина и чая без теина.
Что такое этилацетат?
Этилацетат – это химическое вещество из класса эфиров, произведенное на основе уксусной кислоты. Промышленный интерес к этилацетату вызван редкими свойствами этого вещества: этилацетат легко получать из доступных недорогих ингредиентов, он прекрасно растворяет целлюлозу и многие органические вещества, практически нетоксичен для человека и обладает приятным запахом. При непосредственной работе с этилацетатом, безусловно, необходимы меры предосторожности, поскольку вдыхание его паров может вызвать раздражение слизистой оболочки дыхательных путей и глаз, а при контакте с кожей этилацетат может вызвать дерматит. Однако сегодня нет доказательных данных о том, что в составе других продуктов этилацетат способен нанести вред здоровью человека.
Сегодня этилацетат используют в разных отраслях промышленности: в составе чистящих, ароматических, смягчающих и растворяющих средств при производстве искусственной кожи, печатной продукции, лаков и эмалей, лекарственных препаратов, моющих средств, кинопленки, ликеров, прохладительных напитков, фруктовых эссенций, искусственного шелка, духов и косметики. Особенно часто находят применение обезжиривающие свойства этилацетата при изготовлении шампуня и средств для ухода за ногтевой пластиной, а в составе лака для ногтей этилацетат отвечает за формирование пленочки на ногте и за скорость высыхания покрытия.
Откуда берется этилацетат?
Традиционно в промышленных масштабах этилацетат получают в результате химической реакции этерификации – перегонки уксусной кислоты с большим количеством этилового спирта-сырца и добавления некоторого количества серной кислоты. Годовой объем производства этилацетата в мире превышает 500 тыс. тонн, поскольку методы его получения очень дешевы, а в результате выходит нетоксичная летучая бесцветная жидкость, обладающая отличными свойствами растворителя и при этом имеющая приятный фруктовый аромат.
cosmetic.ua
Уксусноэтиловый эфир - Большая Энциклопедия Нефти и Газа, статья, страница 3
Уксусноэтиловый эфир
Cтраница 3
Уксусноэтиловый эфир должен содержать 2 - 3 % спирта и не содержать влаги. Если спирта в эфире имеется очень мало, то реакция идет медленно. Эфир, содержащий много спирта, реагирует бурно с натрием, но дает низкие выходы ацетоуксусного эфира. [32]
Уксусноэтиловый эфир отгоняют на водяной бане, оставшуюся жидкость перегоняют на масляной бане в вакууме. Небольшую фракцию, кипящую ниже 128 С ( 6 мм рт. ст.), отбрасывают. [33]
Уксусноэтиловый эфир предварительно должен быть промыт раствором бикарбоната натрия ( для связывания уксусной кислоты), затем насыщенным раствором хлористого кальция ( для связывания этилового спирта), высушен прокаленным сернокислым натрием и перегнан. [34]
Уксусноэтиловый эфир, не содержащий вовсе этилового спирта, не взаимодействует с натрием. Следовательно, конденсирующим средством является не металлический натрий, а алкоголят натрия, образующийся при действии натрия на спирт, обычно имеющийся в эфире в качестве примеси. [35]
Уксусноэтиловый эфир должен содержать 2 - 3 % спирта к не содержать влаги. Если спирта в эфире имеется очень мало, то реакция идет медленно. Эфир, содержащий много спирта, реагирует бурно с натрием, но дает низкие выходы ацетоуксусного эфира. [37]
Уксусноэтиловый эфир отгоняют на водяной бане, оставшуюся жидкость перегоняют на масляной бане в вакууме. Небольшую фракцию, кипящую ниже 128 С ( 6 мм рт. ст.), отбрасывают. [38]
Уксусноэтиловый эфир получают по реакции Ти-щенко из уксусного альдегида в присутствии алкоголя-тов алюминия. [39]
Уксусноэтиловый эфир, СН3 - СООС2Нб, приятно пахнущая жидкость, кипит при 78; находит применение в медицине. [40]
Уксусноэтиловый эфир, СНз-COOCaHs, приятно пахнущая жидкость, кипит при 78; находит применение в медицине. [41]
Уксусноэтиловый эфир СН3 - С - 0 - С2Н5 - жидкость с приятным запахом, кипящая при 78 С, применяется в медицине. [42]
Уксусноэтиловый эфир, или этилацетат, применяется в качестве растворителя. [43]
Уксусноэтиловый эфир при термическом разложении ( 650 - 780 и 150 мм) образует кетен и этилен с выходом 90 и 80 / 0 соответственно [ швейцар, пат. [44]
Уксусноэтиловый эфир должен содержать 2 - 3 % спирта, но не влаги. Если спирта в эфире очень мало, то реакция идет медленно; если спирта имеется большое количество, то реакция идет бурно и выход ацетоуксусного эфира уменьшается. [45]
Страницы: 1 2 3 4
www.ngpedia.ru
Уксусноэтиловый эфир - Википедия
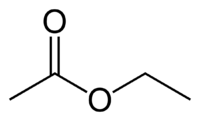
| Этилацетат | |
 | |
 | |
| C4H8O2 | |
| 88,11 г/моль | |
| 0,902 г/см³ | |
| 25,13±0,01 мН/м[1], 23,39±0,01 мН/м[1], 20,49±0,01 мН/м[1], 17,58±0,01 мН/м[1] и 14,68±0,01 мН/м[1] | |
| 0,578±0,001 мПа·с[2], 0,423±0,001 мПа·с[2], 0,325±0,001 мПа·с[2] и 0,259±0,001 мПа·с[2] | |
| 10,01±0,01 эВ[3] | |
| -84 °C | |
| 77 °C | |
| 24±1 °F[3] и -4±1 °C[4] | |
| 2±1 об.%[3] и 2±0,1 об.%[4] | |
| 73±1 мм рт. ст.[3], 10±1 кПа[5], 12,6±0,1 кПа[6] и 100±1 кПа[5] | |
| 1,3720 | |
| 1,78±0,09 Д[7] | |
| 141-78-6 | |
| 8857 | |
| 205-500-4 | |
| E1504 | |
| AH5425000 | |
| 27750 | |
| 8525 | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
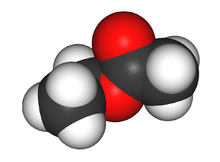 3D модель молекулы этилацетата
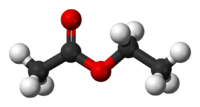
3D модель молекулы этилацетата Этилацетат (этиловый эфир уксусной кислоты) СН3-СОО-Ch3-Ch4 — бесцветная летучая жидкость с резким запахом.
Получение[ | ]
Этилацетат образуется при прямом взаимодействии этанола с уксусной кислотой:
Ch4COOH+C2H5OH→Ch4COOC2H5+h3O{\displaystyle {\mathsf {CH_{3}COOH+C_{2}H_{5}OH\rightarrow CH_{3}COOC_{2}H_{5}+H_{2}O}}}Лабораторный метод получения этилацетата заключается в ацетилировании этилового спирта хлористым ацетилом или уксусным ангидридом:
Ch4COCl+C2H5OH→Ch4COOC2H5+HCl{\displaystyle {\mathsf {CH_{3}COCl+C_{2}H_{5}OH\rightarrow CH_{3}COOC_{2}H_{5}+HCl}}}К промышленным способам синтеза этилацетата относятся:
- Перегонка смеси этилового спирта, уксусной и серной кислот.
- Обработке этилового спирта кетеном.
- По реакции Тищенко из ацетальдегида при 0-5 °C в присутствии каталитических количеств алкоголята алюминия:
Физические свойства[ | ]
Бесцветная подвижная жидкость с резким запахом эфира. Молярная масса 88,11 г/моль, температура плавления −83,6 °C, температура кипения 77,1 °C, плотность 0,9001 г/см³, n204 1,3724. Растворяется в воде 12 % (по массе), в этаноле, диэтиловым эфире, бензоле, хлороформе; образует двойные азеотропные смеси с водой (т. кип. 70,4 °C, содержание воды 8,2 % по массе), этанолом (71,8; 30,8), метанолом (62,25; 44,0), изопропанолом (75,3; 21,0), CCl4 (74,7; 57), циклогексаном (72,8; 54,0) и тройную азеотропную смесь Э.: вода: этанол (т. кип. 70,3 °C, содержание соотв. 83,2, 7,8 и 9 % по массе). [8]
Применение[ | ]
Этилацетат широко используется как растворитель, из-за низкой стоимости и малой токсичности, а также приемлемого запаха. В частности, как растворитель нитратов целлюлозы, ацетилцеллюлозы, жиров, восков, для чистки печатных плат, в смеси со спиртом — растворитель в производстве искусственной кожи. Годовое мировое производство в 1986 году составляло 450—500 тысяч тонн. Мировое производство этилацетата на 2014 год составляет около 3,5 млн. тонн в год.
Один из самых популярных ядов, применяемых в энтомологических морилках для умерщвления насекомых. Насекомые после умерщвления в его парах гораздо мягче и податливее в препарировании, чем после умерщвления в парах хлороформа.
Применяется как компонент фруктовых эссенций. Зарегистрирован в качестве пищевой добавки E1504.
Лабораторное применение[ | ]
Этилацетат часто используется для экстракции, а также для колоночной и тонкослойной хроматографии. Редко в качестве растворителя для проведения реакций из-за склонности к гидролизу и переэтерефикации.
Используется для получения ацетоуксусного эфира[9]:
2Ch4COOC2H5→Ch4COCh3COOC2H5{\displaystyle {\mathsf {2CH_{3}COOC_{2}H_{5}\rightarrow CH_{3}COCH_{2}COOC_{2}H_{5}}}}Очистка и сушка[ | ]
Продажный этилацетат обычно содержит воду, спирт и уксусную кислоту. Для удаления этих примесей его промывают равным объёмом 5%-го карбоната натрия, сушат хлоридом кальция и перегоняют. При более высоких требованиях к содержанию воды несколько раз (порциями) добавляют фосфорный ангидрид, фильтруют и перегоняют, защищая от влаги. С помощью молекулярного сита 4А содержание воды в этилацетате можно снизить до 0,003 %.
Безопасность[ | ]
ЛД50 для крыс составляет 11,6 г/кг, показывая низкую токсичность. Пары этилацетата раздражают слизистые оболочки глаз и дыхательных путей, при действии на кожу вызывают дерматиты и экземы. ПДК в воздухе рабочей зоны 200 мг/м³. ПДК в атмосферном воздухе населенных мест 0,1 мг/м³[10].
Температура вспышки — 2 °C, температура самовоспламенения — 400 °C, концентрационные пределы взрыва паров в воздухе 2,1-16,8 % (по объему).
Безопасность при транспортировке. В соответствии с ДОПОГ (ADR) класс опасности 3, код по реестру ООН 1173.
Примечания[ | ]
- ↑ 1 2 3 4 5 6 7 8 9 10 CRC Handbook of Chemistry and Physics / W. M. Haynes — 95 — Boca Raton: CRC Press, 2014. — P. 6–183. — ISBN 978-1-4822-0868-9
- ↑ 1 2 3 4 5 6 7 8 CRC Handbook of Chemistry and Physics / W. M. Haynes — 95 — Boca Raton: CRC Press, 2014. — P. 6–232. — ISBN 978-1-4822-0868-9
- ↑ 1 2 3 4 5 6 7 8 http://www.cdc.gov/niosh/npg/npgd0260.html
- ↑ 1 2 3 4 CRC Handbook of Chemistry and Physics / W. M. Haynes — 95 — Boca Raton: CRC Press, 2014. — P. 16–22. — ISBN 978-1-4822-0868-9
- ↑ 1 2 3 4 CRC Handbook of Chemistry and Physics / W. M. Haynes — 95 — Boca Raton: CRC Press, 2014. — P. 6–99. — ISBN 978-1-4822-0868-9
- ↑ 1 2 CRC Handbook of Chemistry and Physics / W. M. Haynes — 95 — Boca Raton: CRC Press, 2014. — P. 15–17. — ISBN 978-1-4822-0868-9
- ↑ 1 2 CRC Handbook of Chemistry and Physics / W. M. Haynes — 95 — Boca Raton: CRC Press, 2014. — P. 9–56. — ISBN 978-1-4822-0868-9
- ↑ Химическая энциклопедия, Москва 1998, стр. 494
- ↑ Органикум. Том 2. Москва, Мир, 1992, стр. 180
- ↑ Предельно допустимые концентрации (ПДК) загрязняющих веществ в атмосферном воздухе населенных мест
encyclopaedia.bid
Ацетали, сложные эфиры, липиды в винограде и вине
Представители всех этих соединений содержатся в винограде, потом, в биотехнологических процессах брожения, переходят в вино, многие из них образуются в процессе изготовления вин. Ацетали − это простые диэфиры гидратов альдегидов. Сложные эфиры характеризуются как производные кислот, в которых атом водорода в карбоксиле замещен радикалом:

В связи с тем, что одним из способов получения сложных эфиров является отделение молекулы воды от молекулы кислоты и спирта, их следует рассматривать как ангидриды кислоты и спирта (например, уксусно-этиловый эфир или этилацетат).
Ацетали образуются в результате химической реакции альдегидов со спиртами.
Например, образование диацетила происходит следующим образом:

В коньяках и винах основным фактором, влияющим на концентрацию ацеталей, является содержание спирта. Например, в вине с объемной долей спирта 10 % только 3 % ацетальдегида может быть связано в ацетали, а при спиртуозности вина 20 % об. – 6,3 %. Легче всего ацетали образуют алифатические альдегиды. В значительных количествах ацетали образуются в коньячных спиртах и коньяках с высокой концентрацией спирта.
Основное количество ацеталей в винах приходится на этилацеталь. В хересах его содержание достигает 300 мг/дм3 и это является одним из показателей хорошего Хереса. В обычном вине до 20 мг/дм3 этилацеталя. В концентрациях 10 – 100 мг/дм3 он придает вину приятные тона плодового аромата. В готовом хересе соотношение альдегидов и ацеталей должно быть 1:1.
Сложные эфиры относятся к наиболее важным производным карбоновых кислот. Механизм образования их из кислот и спиртов был выяснен сравнительно недавно с применением изотопов. Образуются сложные эфиры и биологическим путем во время брожения под действием ферментов дрожжей. По данным Риберо-Гайона в результате химической этерификации образуются, в основном, кислые сложные эфиры, а вследствие биологической этерификации – нейтральные сложные эфиры.
Основным сложным эфиром является Уксусноэтиловый эфир (этилацетат), образуемый при взаимодействии уксусной кислоты и этилового спирта:

уксусная этанол этилацетат
кислота
При брожении виноградного сусла сложные эфиры образуются под воздействием ферментных систем дрожжей. В вине эфиров содержится во много раз больше, чем в винограде. Основной сложный эфир этилацетат возрастает с 2 - 5 до 200 мг/дм3. Каждый из остальных сложных эфиров жирных кислот возрастает с 0,1 – 0,5 до 1 – 10 г/дм3. В значительных количествах в вине образуются этиловые эфиры оксикислот (диэтиллактат, диэтилсукцинат, диэтилмалат), которых нет в винограде: до 100 – 500 мг/дм3.
В винограде американских сортов и в гибридах на их основе обнаружен Метиловый эфир антраниловой кислоты. Это соединение обладает сильным специфическим «лисьим» запахом, который называют гибридным тоном винограда и вина.
Этиловые эфиры жирных кислот С3-С20 (представители сложных эфиров) является составной частью энантового эфира, имеют приятный фруктовый запах и принимают участие в формировании фонового аромата молодых виноматериалов. Этиловые эфиры жирных кислот образуются при спиртовом брожении, на их синтез влияют условия брожения (температура и др.), раса дрожжей и продолжительность выдержки виноматериалов на осадке дрожжей. При брожении они синтезируются в концентрациях выше равновесных, а при хранении и выдержке виноматериалов их содержание уменьшается. Массовая концентрация в вине составляет 0,012...0,20 г/дм3.
Этиловые эфиры органических кислот (представители сложных эфиров) при брожении синтезируются в концентрациях ниже равновесных, а при хранении и выдержке виноматериалов их содержание увеличивается. Они относятся к нелетучим веществам, принимающим участие в формировании качественных показателей вина. Массовая концентрация в вине не превышает 1 г/дм3.
В основном, сложные эфиры простейших и средних представителей кислот и спиртов являются летучими жидкостями, они легче воды. Большинство из них имеет приятный фруктовый запах, а неприятные по запаху кислоты (масляная и валерьяновая) в процессе этерификации образуют вещества с приятным ароматом.
В воде растворяются только те сложные эфиры, которые имеют наименьшее число атомов углерода в молекуле, но большинство из них плохо растворяется в воде. Они хорошо растворяются в этиловом спирте и диэтиловом эфире.
В сравнении с температурами кипения и плавления органических кислот, соответствующие температуры сложных эфиров более низкие. Но из-за высокой летучести сложные эфиры более стойкие к нагреванию, чем свободные кислоты, и могут легко перегоняться в тех условиях, при которых кислоты распадаются.
Омыление эфиров щелочью более эффективно и происходит в тысячи раз быстрее, чем кислотой. Особенно легко омыляются низкомолекулярные эфиры жирных кислот, и этот биохимический процесс может протекать при комнатной температуре. Наоборот, гидролиз высокомолекулярных эфиров происходит эффективно только при высокой температуре. Такое свойство используется для качественного разделения смеси высоко - и низкомолекулярных сложных эфиров.
При нагревании в кислой среде сложные эфиры способны к переэтерификации (в присутствии большого количества другого спирта). Они способны достаточно легко образовывать с аммиаком и его производными амиды (реакция амонолиза). В этом случае амонолиз может происходить при комнатной температуре под действием раствора аммиака на сложный эфир.
С гидроксиламином сложные эфиры при взаимодействии образуют гидроксаматы. Такая реакция используется для количественного определения сложных эфиров (в присутствии железа гидроксаматы дают характерный темно-синий цвет).
В винограде сложных эфиров, в основном эфиров жирных кислот и алифатических спиртов, немного, их количество составляет от 5 до 30 мг/дм3. В винах сложных эфиров содержится на много больше, чем в винограде. Их количество зависит от условий брожения, вида и расы дрожжей. Содержание этиловых эфиров жирных кислот с парным числом атомов углерода в молекуле при брожении увеличивается до 200 мг/дм3 и больше, а также небольшое количество кислых эфиров винной, янтарной и яблочной кислот. Этиловые эфиры высокомолекулярных жирных кислот (от С3 до С20) являются основной составной частью энантового эфира, в составе которого преобладают эфиры жирных кислот с парным числом атомов углерода.
Энантовый эфир имеет сильный, приятный фруктовый аромат и значительно влияет на формирование букета вин.
При выдержке вина накапливаются, главным образом, кислые эфиры винной, яблочной и янтарной кислот: в молодых до 50 мг/дм3, в выдержанных больше 10 лет – до 300 мг/дм3. При хранении вина вместе с этерификацией происходит омыление, а также реакция переэтерификации.
Количество сложных эфиров значительно увеличивается в процессе биотехнологии вин типа херес. Например, при выдержке вина под пленкой хересных дрожжей происходит интенсивное образование средних эфиров жирных (от С2 к С10), а также двухосновных кислот, придающих вину специфический приятный аромат.
Добавить комментарий
vinograd-vino.ru
Этилацетат
ЭТИЛАЦЕТАТ ТЕХНИЧЕСКИЙ
Основные сведения: Этилацетат - бесцветная летучая жидкость с приятным фруктовым запахом. Растворяется в воде 12 %(по массе), в этаноле, диэтиловом эфире, бензоле, хлороформе.
Синонимы: этиловый эфир уксусной кислоты.
Эмпирическая формула: С4Н8О2
Технические условия: ГОСТ 8981-78
|
ПОКАЗАТЕЛЬ |
ЗНАЧЕНИЕ |
|||
| Марка А | Марка Б | |||
| Высший сорт | Первый сорт | |||
|
Внешний вид |
Прозрачная жидкость без механических примесей |
|||
|
Цветность по платиново-кобальтовой шкале,ед. Хазена, не более |
5 |
10 |
10 |
|
|
Плотность при 20 0С, г/см3 |
0,898-0,900 |
0,897-0,900 |
0,890-0,900 |
|
|
Массовая доля этилацетата, % |
не менее 99,0 |
не менее 98,0 |
91,0±1 |
|
|
Массовая доля кислот в пересчете на уксусную кислоту, %, не более |
0,004 |
0,008 |
0,010 |
|
|
Массовая доля нелетучего остатка, %, не более |
0,001 |
0,003 |
0,007 |
|
|
Температурные пределы перегонки при давлении 101,3 кПа (760 мм рт.ст.): 95% (по объему) продукта должно отгоняться в пределах температур, 0С |
75-78 |
74-79 |
70-80 |
|
|
Массовая доля воды, %, не более |
0,1 |
0,2 |
1,0 |
|
|
Массовая доля альдегидов в пересчете на уксусный альдегид, %, не более |
0,05 |
не нормируется |
- |
|
|
Относительная летучесть (по этиловому эфиру) |
2-3 |
2-3 |
2-3 |
|
Получение: Получают перегонкой смеси этилового спирта, уксусной и серной кислот.
Применение: Этилацетат широко используется как растворитель в производстве лакокрасочных материалов, клеевых композиций, как растворитель эфиров целлюлозы, ацетилцеллюлозы, жиров, восков, в смеси со спиртом как растворитель в производстве искусственной кожи, как экстрагирующий агент для различных органических веществ из водных растворов, как желатинизирующее средство при изготовлении взрывчатых веществ.
Опасность: Этилацетат технический по степени воздействия на организм человека относится к числу малоопасных веществ. Легковоспламеняющаяся жидкость, образует в смеси с воздухом взрывоопасную смесь.
Упаковка: Этилацетат технический наливают в стальные оцинкованные бочки, алюминиевые бочки, железнодорожные, автомобильные цистерны.
Транспортировка: Транспортировку осуществляют в бочках железнодорожным или автомобильным транспортом в крытых транспортных средствах, железнодорожных цистернах, автоцистернах с соблюдением правил перевозок опасных грузов, действующих на транспорте данного вида.
Хранение: Этилацетат технический хранят в складских помещениях или в специально оборудованных металлических емкостях с соблюдением правил хранения огнеопасных веществ.Гарантийный срок хранения – шесть месяцев со дня изготовления.
himexi.com.ua























