Урок химии по теме "Сложные эфиры". Сложные эфиры строение
Урок химии по теме "Сложные эфиры"

Разделы: Химия
Цель урока:
- Изучить строение, получение и свойства сложных эфиров.
- Познакомить с применением сложных эфиров, раскрыть их значение в жизни общества.
- Способствовать развитию умений и навыков учащихся составлять химические уравнения, интереса к химической науке, познавательных интересов учащихся, расширению кругозора.
- Воспитывать эстетическое восприятие природы, эстетические вкусы.
Тип урока: Урок усвоения знаний на основе имеющихся.
Методы: Эвристический, применение элементов компьютерных технологий, показательный.
Оборудование: презентация «Сложные эфиры», фрукты, фруктовые воды, эфирные масла.
Ход урока
I. Организационный момент. Целеполагание.
(Вступительное слово учителя. Обоснование значения темы и цели урока. )
Мотивация: Попробуйте с завязанными глазами определить фрукты и цветы.
( К доске приглашаются двое учащихся, завязывают глаза). Определяют по запаху апельсин, яблоко, розы, лилии.
Чем можно объяснить благоухание цветов, трав и деревьев, фруктов?
Предполагаемый ответ: возможно, присутствуют какие - то вещества, которые характеризуют запах этих фруктов и цветов.
Вы абсолютно правы, есть такие вещества. Это сложные эфиры. Мы с вами рассмотрим строение сложных эфиров, узнаем, где в природе мы встречаемся со сложными эфирами, какими свойствами они обладают и где применяют сложные эфиры. ( слайд №1) Но прежде чем приступить к изучению новой темы, давайте вспомним что мы изучали на предыдущих уроках?
II. Актуализация знаний. (Слад №2)
- Какой состав имеют спирты? (R-ОН)
- Какую функциональную группу содержат спирты? (-ОН)
- Каков состав карбоновых кислот? (R-СООН)
- Каким общим свойствам обладают спирты и карбоновые кислоты? (взаимодействуют друг с другом с образованием сложных эфиров)
III. Организация деятельности по изучению нового материала.
Изложение с применением компьютерной презентации (Приложение 1) и наглядного материала.
- Строение сложных эфиров. (слайд №3)
- Получение сложных эфиров. (слайд №4)
- Номенклатура и изомерия сложных эфиров. (слайд №5,6)
- Нахождение в природе: (слайд №7) Все сложные эфиры органических кислот обладают приятным запахом. Эти душистые вещества содержатся в растениях в виде маленьких капелек в особых клетках. Они встречаются не только в цветах, но и в листьях, плодах и даже древесине. Лавровый лист который мы используем, как специи, его запах обусловлен наличием эфира (лауриловый эфир лауриновой кислоты (СН3-(СН2)10СООН; СН3(СН2)10СН2ОН). Пчелиный воск это тоже сложный эфир ( эфир пальмитиновой кислоты и мирицилового спирта С15Н31СООС31Н63 ) – сложный эфир высших карбоновых кислот и высших одноатомных спиртов.
- Свойства сложных эфиров: - Физические свойства. (слайд №8) - Химические свойства (слайд №9, 10)– для сложных эфиров характерна реакция гидролиза – взаимодействие с водой.
- Применение: (слайд №11, 12 )Химику очень трудно прогнозировать запах вещества по виду структурной формулы. Иногда небольшое вмешательство в состав вещества весьма сильно влияет на его запах. В зависимости от числа групп СН2 оттенок запаха меняется так: при пяти группах мы ощущаем запах горького миндаля, а при шести – мяты, при 8-9 – запах камфоры, при 9 – 12 – кедровой смолы, при 14 – 15 – запах мускуса.
Давайте вместе с вами назовем области применения сложных эфиров.
- Ароматизаторы изделий пищевой промышленности. В виде фруктовых эссенций для изготовления карамели, газированных напитков. Например: этиловый эфир муравьиной кислоты имеет запах рома, этиловый эфир масляной кислоты - запах ананаса.
- Парфюмерной промышленности. Много веков назад древние арабы уже знали способы получения душистых веществ из растений. Их добывали, в основном, из лепестков роз и лаванды. Душистые благовония, наряду с драгоценными камнями, в странах Востока служили символом богатства. Ведь для того, чтобы получить 1 кг розового масла, необходимо собрать и обработать около 5 тонн розовых лепестков. В настоящее время химикам не только удалось разгадать секрет запаха, но и синтезировать душистые вещества, причём, с новыми оттенками запаха. Так же как из цветов можно составить букет, так и из нескольких ароматических веществ создаются « букеты» запахов, которые называются духами. Для получения духов иногда используется до 50 различных душистых веществ.
- Медицинские препараты, например аспирин.
- Волокно лавсан.
- Растворители красок и лаков.
- Ароматерапия.
Современная ароматерапия – это профилактический, оздоровительный натуральный способ поддержания хорошей формы, терапия, позволяющая снять ежедневные стрессы, не допустить развитие недугов и придать повседневной жизни красоту ароматов.
IV. Закрепление и обобщение изученного.
Китайский философ Конфуций как-то сказал: « Хорошо обладать природным дарованьем, но, упражнения друзья, дают нам больше чем природное дарованье». (Слайд №13)
Самостоятельная работа. (составить уравнение реакции этерификации и гидролиза)
Двое учащихся к доске с индивидуальным заданием, остальные работают на местах. (Приложение 2)
V. Подведение итогов урока.
Что нового и интересного вы узнали сегодня на уроке? Чему научились?
VI. Рефлексия
ароматерапия, музыка.
Поделиться страницей:xn--i1abbnckbmcl9fb.xn--p1ai
Cложные эфиры - Информация
Содержание стр.
Введение -3-
1. Строение -4-
2. Номенклатура и изомерия -6-
3. Физические свойства и нахождение в природе -7-
4. Химические свойства -8-
5. Получение -9-
6. Применение -10-
6.1 Применение сложных эфиров неорганических кислот -10-
6.2 Применение сложных эфиров органических кислот -12-
Заключение -14-
Использованные источники информации -15-
Приложение -16-
Введение
Среди функциональных производных кислот особое место занимают сложные эфиры производные кислот, у которых кислотный водород заменён на алкильные (или вообще углеводородные) радикалы.
Сложные эфиры делятся в зависимости от того, производной какой кислоты они являются (неорганической или карбоновой).
Среди сложных эфиров особое место занимают природные эфиры жиры и масла, которые образованы трехатомным спиртом глицерином и высшими жирными кислотами, содержащими четное число углеродных атомов. Жиры входят в состав растительных и животных организмов и служат одним из источников энергии живых организмов, которая выделяется при окислении жиров.
Цель моей работы заключается в подробном ознакомлении с таким классом органических соединений, как сложные эфиры и углублённом рассмотрении области применения отдельных представителей этого класса.
1. Строение
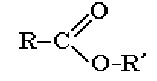
Общая формула сложных эфиров карбоновых кислот:
где R и R углеводородные радикалы (в сложных эфиpax муравьиной кислоты R атом водорода).
Общая формула жиров:
где R, R", R" углеродные радикалы.
Жиры бывают “простыми” и “смешанными”. В состав простых жиров входят остатки одинаковых кислот (т. е. R = R" = R"), в состав смешанных различных.
В жирах наиболее часто встречаются следующие жирные кислоты:
Алкановые кислоты
1. Масляная кислота СН3 (Ch3)2 СООН
2. Капроновая кислота СН3 (Ch3)4 СООН
3. Пальмитиновая кислота СН3 (Ch3)14 СООН
4. Стеариновая кислота СН3 (Ch3)16 СООН
Алкеновые кислоты
5. Олеиновая кислота С17Н33СООН
СН3(СН2)7СН === СН(СН2)7СООН
Алкадиеновые кислоты
6. Линолевая кислота С17Н31СООН
СН3(СН2)4СН = СНСН2СН = СНСООН
Алкатриеновые кислоты
7. Линоленовая кислота С17Н29СООН
СН3СН2СН = CHCh3CH == CHCh3CH = СН(СН2)4СООН
2. Номенклатура и изомерия
Названия сложных эфиров производят от названия углеводородного радикала и названия кислоты, в котором вместо окончания -овая используют суффикс -ат, например:
Для сложных эфиров характерны следующие виды изомерии:
1. Изомерия углеродной цепи начинается по кислотному остатку с бутановой кислоты, по спиртовому остатку с пропилового спирта, например, этилбутирату изомерны этилизобутират, пропилацетат и изопропилацетат.
2. Изомерия положения сложноэфирной группировки СОО. Этот вид изомерии начинается со сложных эфиров, в молекулах которых содержится не менее 4 атомов углерода, например этилацетат и метилпропионат.
3. Межклассовая изомерия, например, метилацетату изомерна пропановая кислота.
Для сложных эфиров, содержащих непредельную кислоту или непредельный спирт, возможны еще два вида изомерии: изомерия положения кратной связи и цис-, транс-изомерия.
3. Физические свойства и нахождение в природе
Сложные эфиры низших карбоновых кислот и спиртов представляют собой летучие, нерастворимые в воде жидкости. Многие из них имеют приятный запах. Так, например, бутилбутират имеет запах ананаса, изоамилацетат груши и т. д.
Сложные эфиры высших жирных кислот и спиртов воскообразные вещества, не имеют запаха, в воде не растворимы.
Приятный аромат цветов, плодов, ягод в значительной степени обусловлен присутствием в них тех или иных сложных эфиров.
Жиры широко распространены в природе. Наряду с углеводородами и белками они входят в состав всех растительных и животных организмов и составляют одну из основных частей нашей пищи.
По агрегатному состоянию при комнатной температуре жиры делятся на жидкие и твердые. Твердые жиры, как правило, образованы предельными кислотами, жидкие жиры (их часто называют маслами) непредельными. Жиры растворимы в органических растворителях и нерастворимы в воде.
www.studsell.com
Разработка поурочного планирования по теме "Сложные эфиры" 10 КЛАСС
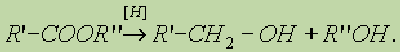
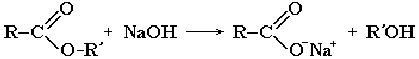
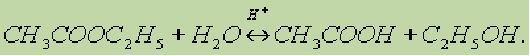
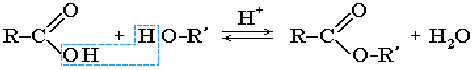
 Урок № 38
Урок № 38
Дата: 30.01.2014г.
Тема: Сложные эфиры. Получение, содержание в природе, применение на основе их свойств.
Цель урока: дать уч-ся представление о строении молекул, номенклатуре, нахождении в природе, физических и химических свойствах, получении и применении сложных эфиров.
Задачи урока:
Дать уч-ся представление о строении молекул сложных эфиров.
Научить уч-ся составлять формулы сложных эфиров и давать им названия.
Дать уч-ся представление о реакции этерификации как реакции получения сложных эфиров, научить уч-ся составлять реакции этерификации.
Научить уч-ся составлять уравнения реакций, отражающих химические свойства сложных эфиров.
Дать уч-ся представление о способах применения сложных эфиров, основанных на их свойствах.
Тип урока: лекция + элементы самостоятельной работы.
Оборудование: уксусная кислота, этиловый спирт, конц серная кислота, спиртовка, спички, пробиркодержатель, пробирки, презентация по теме, СД «Кирилл и Мефодий. Химия 10-11 класс», учебник О.С. Габриелян изд. «Дрофа» 2010 г., раздаточный материал.
Ход урока: I. Организация класса.
II. Анализ контрольной работы по теме «Альдегиды и карбоновые кислоты».
III. Новый материал.
1. Актуализация внимания учащихся.
В беседе с учащимися вспомнить:
1) общие формулы, особенности номенклатуры (как по системе СИ, так и тривиальной) ранее изученных кислородсодержащих органических соединений (предельных одноатомных спиртов, альдегидов, предельных одноосновных карбоновых кислот). Учащиеся приводят примеры формул и названия веществ.
2) особенности физических и химических свойств данных классов соединений.
3) обратить внимание учащихся на то, что при изучении химических свойств предельных одноосновных карбоновых кислот мы рассматривали реакцию взаимодействия кислот со спиртами с образованием сложных эфиров, подчеркнув, что с таким классом органических веществ, как сложные эфиры мы уже встречались. Предложить учащимся написать на доске уравнения реакций, отражающих данное свойство кислот.
Строение молекул сложных эфиров.
Дать учащимся представление о строении молекул и общей формуле сложных эфиров. Работа по учебнику стр. 92 и презентации (слайд 1).
Учащиеся записывают определение и общую формулу в тетрадь:
СЛОЖНЫЕ ЭФИРЫ – это соединения, содержащие карбоксильную группу, связанную с двумя алкильными радикалами.
Общая формула сложных эфиров такая же, как у карбоновых кислот: Cnh3nO2
3.Нахождение сложных эфиров в природе (слайд 2), стр. 93 учебника:
фрукты, ягоды, цветы, духи, парфюмерия, растительные и животные жиры, воски.
4. Физические свойства: жидкости, легко воспламеняются, имеют низкие температуры кипения, летучие, легче воды, в воде не растворимы, легко воспламеняются, в большинстве обладают приятными запахами. (слайд 3)
5. Номенклатура сложных эфиров.
Названия сложных эфиров определяются названиями кислоты и спирта, из которых они образуются (слайд 4,5). Учащиеся записывают формулы и названия сложных эфиров, используя записи на доске и презентацию.
Формула эфира
Полное название
Другие названия.
СН3-С-О - СН3
║
О
метиловый эфир уксусной кислоты
метилацетат
уксусно-метиловый эфир
Н-С –О - С2Н5
║
О
этиловый эфир муравьиной кислоты
этилформиат
муравьино-этиловый эфир
С2Н5 -С–О - С3Н7
║
О
пропиловый эфир пропановой (пропионовой) кислоты
пропилпропаноат (пропионат)
6. Виды изомерии сложных эфиров (слайды 6,7)
1) Изомерия углеродной цепи начинается по кислотному остатку с бутановой кислоты, по спиртовому остатку — с пропилового спирта, например, этилбутирату изомерны этилизобутират, пропилацетат и изопропилацетат.
2) Изомерия положения сложноэфирной группировки —СО—О—. Этот вид изомерии начинается со сложных эфиров, в молекулах которых содержится не менее 4 атомов углерода, например этилацетат и метилпропионат.
3) Межклассовая изомерия с карбоновыми кислотами. Например, пропановая кислота и метилацетат являются изомерами по отношению друг к другу, так как имеют одинаковый состав С3Н7О2
7. Получение сложных эфиров (слайд 8):
1)Cложные эфиры могут быть получены при взаимодействии карбоновых кислот со спиртами (реакция этерификации). Катализаторами являются минеральные кислоты.
2) Сложные эфиры фенолов нельзя получить с помощью этерификации, для их получения используют реакцию фенолята с галогенангидридом кислоты:
С6Н5-О-Na+ + C2H5–C=O NaCl + C6H5–O-C=O
| |
Cl C2H5
фениловый эфир пропановой кислоты
(фенилпропаноат)
8. Химические свойства сложных эфиров (слайды 9,10):
1). Гидролиз сложных эфиров.
Реакция этерификации обратима. Обратный процесс – расщепление сложного эфира при действии воды с образованием карбоновой кислоты и спирта – называют гидролизом сложного эфира.
Кислотный гидролиз обратим:
Щелочной гидролиз протекает необратимо:
Эта реакция называется омылением сложного эфира.
2. Реакция восстановления. Восстановление сложных эфиров водородом приводит к образованию двух спиртов:
Дополнительно: сложные эфиры высших карбоновых кислот и спиртов с длинными углеводородными радикалами называются восками:
С15Н31 – СООС30Н61 - воск, сложный эфир мерицилового спирта и пальмитиновой кислоты.
IV. Закрепление:
1. Составить формулы:
1) бутиловый эфир пропионовой кислоты;
2) этиловый эфир масляной кислоты;
3) пропиловый эфир муравьиной кислоты;
4) метиловый эфир валериановой кислоты.
2. Работа по заданиям раздаточного материала:
Дать названия сложных эфиров, используя систематическую и тривиальную номенклатуру:
O O O
║ ║ ║
Ch4 – C – O – Ch4 2) C2H5 – C – O – C2H5 3) H – C – O - C2H5
4) H C O О C3H7 5) C4H9 – C О O C2H5 6) C3H7 – C O ОCh4
Выбрать и закончить уравнения реакций, отражающих получение сложных эфиров, указать условия реакций, назвать продукты реакций, указать тип данной реакции:
C3H7 – C O О C2H5 + h3O = 2) H – C О OH + C3H7OH =
3) C3H7 – C ОOH + C4H9OH = 4)C2H5 – C O ОC4H9 + h3O =
Закончить уравнения реакций гидролиза сложных эфиров, указать условия реакций, назвать вещества:
H – C – O О C2H5 + h3O = 2) C2H5 – C ОOH + C4H9OH =
3) C2H5 – C О OH + C3H7OH = 4) Ch4 – C – O О C3H7 + h3O =
Составить уравнение реакции получения:
Метилформиата; 2) пропилацетата; 3) этилового эфира масляной кислоты; 4) метилового эфира валериановой кислоты.
Составить уравнения реакций, при помощи которых можно осуществить следующие превращения:
Ch5 C2h3 ? Ch4COOH Ch4 – C O ОC2H5
C2H6 C2H5Cl C2H5OH Ch4 – C О OH Ch4 – C O О C5h21 C5h21OH CO2
V. Домашнее задание: пар. 13, стр. 92-94, стр. 100 вопр. 1,2,3, упр. в тетради (по раздаточному листу № 3,4).
infourok.ru
Эфиры сложные структура - Справочник химика 21
Карбоновые кислоты в процессе обмена веществ часто объединяются. Реакция осуществляется через стадию образования сложных эфиров с коферментом А, представляющим собой тиол сложной структуры (разд. 19.3). [c.166]Длины связей 122 и 136 пм указывают на то, что в кислотах и сложных эфирах вклад структуры А составляет примерно 80% и структуры Б примерно 20%. Для иона карбоновой кислоты структуры А и эквивалентны [c.237]
О-содержащие соединения представлены кислотами сложной структуры, имеются сложные эфиры, строение которых пока не выяснено. [c.688]Обычно сложную структуру целевого вещества разделяют на фрагменты и затем на относительно простые кирпичики , из которых и начинают проектировать схему синтеза, идя в обратном направлении — от простого к сложному ( ретросинтетический анализ ). В будущем для этой цели реально использовать ЭВМ. Нельзя обойти обширную химию элементоорганических соеди-. нений. Например, известно уже более десятка тысяч только органических соединений бора, многие из которых эффективно исполь- зуются в органическом синтезе как реагенты, как промежуточные вещества при построении органических молекул различной сложности. Некоторые борорганические соединения выпускаются химической промышленностью как продукты (эфиры борной кислоты). [c.29]
Ясно, что положение каждого из этих равновесий зависит не только от кислоты, но также и от основания, которое с ней реагирует. Другими словами, константа диссоциации данной кислоты зависит от природы растворителя. Из этого следует, что кислотность слабых кислот не может быть выявлена иначе, как в достаточно основных растворителях, и, наоборот, выявление основности слабых оснований требует применения достаточно кислых растворителей. Так, для изучения зависимости основности от структуры для таких веществ, как кетоны, простые эфиры, сложные эфиры и карбоновые кислоты, в качестве растворителя берут обычно серную кислоту [c.52]
Для получения пленки из ультрамида 6А можно применять так называемый способ осаждения в ванне . В качестве осаждающих жидкостей для коагуляции растворов сополимерных полиамидов применимы спирты, сложные эфиры и кетоны, из которых технически легкодоступными являются эфиры циклической структуры—тетрагидрофуран и диоксан, способные коагулировать полиамиды чрезвычайно быстро. Приготовленные таким образом пленки-в сравнении с пленками, полученными методом литья, обладают лучшей прозрачностью. В качестве осаждающих жидкостей были предложены алифатические соединения с присоединенной непосредственно к атому углерода ОН-группой (например, 5—15%-ные растворы муравьиной или 40—55%-ные растворы уксусной кислоты или этиловый спирт) . Впрочем, полиамидную пленку в технике до настоящего времени по этому способу не получают. [c.224]
Сопоставив данные таблицы, можно сделать вывод о связи структуры молекул растворителя с его экстракционными свойствами. В целом значения К много выше у полиэфиров и кетонов, чем у простых эфиров, сложные эфиры занимают промежуточное положение. В гомологическом ряду данного класса К быстро уменьшается с ростом молекулярного веса. В работе [190] было отмечено, что Ig/ прямо пропорционален отношению числа атомов кислорода к числу атомов углерода в молекуле экстрагента. [c.97]
Циклические поливиниловые простые эфиры имеют более сложную структуру полосы поглощения группы С—О, чем линейные полиэфиры. Их спектры характеризуются двумя или более достаточно широкими полосами высокой интенсивности в области от 1250 до 910 см . Наблюдается слабая полоса карбонильной группы сложного эфира, она, как и полоса около 1250 см , указывает на присутствие поливинилацетата. [c.207]
Значение темплатного эффекта для синтеза макроциклических соединений трудно переоценить Темплатным путем синтезируется значительное количество краун-эфиров и большинство полназамакро-циклов Темплатные реакции позволяют в одну стадию и с высоким выходом синтезировать соединения сложной структуры, пол чение многих из которых другим путем практически невозможно Таким образом, применение различных ионов металлов позволяет синтезировать макроциклы, различающиеся как по виду, так п по количеств донорных атомов, входящих в состав макрокольца [c.31]
Коэнзим А имеет сложную структуру, включающую последовательно связанные остатки гетероцикла аденина, фосфорного эфира пентозы — рибозы, остаток пирофосфорной кислоты, связанный далее с остатком пантотеновой кислоты, ацилирующей в свою очередь тиоэтаноламин. Структура коэнзима А рассматривается в книге И. Пока обозначим его символом КоА—8Н. Пировиноградная кислота при действии кислорода и участии соответствующих ферментов декарбоксилируется, окисляется и ацетилирует по сере коэнзим А [c.466]
К нейтральным кислородсодержащим соединениям нефти относят также сложные и простые эфиры. Большинство сложных эфиров содержатся в высококипящих фракциях или нефтяных остатках. Многие из них являются ароматическими соединениями, иногда представленными внутренними эфирами — лактонами. Имеются сведения, что в калифорнийской нефти лайдены эфиры насыщенной структуры типа [c.278]
Первый пример полного синтеза стероидов был описан в 1939 г. Бахманном, осуществившим вместе с сотрудниками линейную синтетическую цепочку, при которой последовательно проводилось построение одного за другим колец А, В, С и О. Примером подобного синтеза может служить и синтез холестерина по Вудворду [3.7.3]. В последнее время ( ыли разработаны конвергентные сходящиеся) синтетические цепочки при этом сначала получают два фрагмента целевой молекулы по раздельно осуществляемым схемам, а затем, по возможности на одной из последних стадий, соединяют эти фрагменты в более сложную структуру. Такой путь синтеза позволяет уменьшить потери промежуточно синтезируемых соединений, на получение которых ступень за ступенью затрачивается много времени и средств. Поэтому конвергентные пути синтеза со сходящимися цепочками особенно привлекательны для промышленного производства стероидов. Ниже приводится пример построения стероидного скелета с помощью линейного синтеза из метилового эфира 5-оксогептен-6-овой-1 кислоты и 2-метилциклопентандиона-1,3 [3.7.4] (см. схему на с. 696). [c.695]
Для проведения ГХ-анализа одинаково важны как химическая, так и термическая устойчивость рассмотренных выше производных. Химическая устойчивость прежде всего определяет условия обработки, хранения и дозировки образцов. Как уже упоминалось, в результате слишком длительного анализа одного и того же образца могут образовываться несколько продуктов и, следовательно, получаться неоднозначные данные. Если ТФА-производные эфиров простых моноаминомонокарбоновых кислот — устойчивые вещества, которые могут храниться неограниченное время, то этого нельзя сказать о производных аминокислот сложной структуры, содержащих несколько ацильных групп. Большинство таких соединений крайне чувствительны к гидролизу и частично разлагаются в присутствии следов воды [53]. У оксиаминокислот Сер и Тре это может привести к полной потере защитных групп, так как кислота, образующаяся при гидролизе О-ТФА-группы, по типу кислотноосновного катализа может способствовать N—О-ацильной миграции и таким образом вызвать полную потерю Ы-ТФА-групп [126]. Рекомендуется эти соединения хранить и даже вносить в прибор в присутствии избытка трифторуксусного ангидрида, к которому могут добавляться другие растворители. [c.318]
И трижды защищенного производного этого же тетраола — ортоэфира 78 как реагента для наращивания цепей. Трансформацией 77 в бромид 77а с последующим стандартным алкилированием этим бромидом алкоголята 78а бьш получен защищенный дендример первого поколения 79. После удаления за-щитньгх групп этот дендример был подвергнут аналогичной последовательности реакций и т. д., что вело к дендримерам второго (81) и третьего (82) поколений. Таким образом, чрезвычайно простая химия (старый добрый метод синтеза простых эфиров по Вильямсону) оказалась очень эффективной для построения достаточно сложных структур. Но дальнейшее продвижение по этому пути оказалось практически невозможным из-за стерических препятствий. Анализ молекулярных моделей дендримера третьего поколения, 82, показал, что эти шарообразные молекулы (около 22—24 A в диаметре) имеют весьма плотную упаковку ветвей. Поэтому нереалистично бьшо бы рассчитывать на необходимую полноту конверсии 108 поверхностных гидроксильных групп в соответствующий полибромид, не говоря уже о достижении полноты последующей конденсации с реагентом 78а, который и сам предъявляет достаточно жесткие пространственные требования к реакционному партнеру. [c.410]
При поликонденсации эпихлоргидрина с бис-фенолами или с резорцином получаются эпоксидйые смолы . Эти смолы имеют сложную структуру и получаются по реакции между кислородом эфира и атомом хлора эпихлоргидрина, с одной стороны, и атомами водорода гидроксильной группы бис-фенола (основное сырье бензол и ацетон), с другой стороны [c.423]
Аминокислоты и пептиды. Метод масс-спектрометрии можно с успехом применять для установления структуры аминокислот и пептидов. На первый взгляд это кажется удивительным, так как хорошо известно, что такие соединения нелетучи однако после превращения их в этиловые эфиры (сложные) и нолиимипоспирты (эти реакции можно легко провести в микромасштабе) получаются достаточно летучие соединения [11, 15]. [c.343]
Химическая стабильность эфирной связи в простых эфирах позволяет использовать при структурных исследованиях различные методы деградации без затрагивания эфирной связи аналогичным образом, существует широкий круг синтетических методик, позволяющих превращать простые эфиры в гораздо более сложные структуры. Например, устойчивость эфирных групп к расщеплению и миграции в ходе гидролиза, восстановления и превращения в удобные для анализа производные служит важным фактором, превращающим метилирование в один из самых надежных методов определения структуры полисахаридов [164]. В то же время такая устойчивость к расщеплению ограничивает возможности использования эфирных групп для защиты гидроксильных функций в ходе синтетических последовательностей лишь некоторыми специальными случаями [165]. Один из таких случаев наблюдается при достаточной устойчивости конечного продукта в относительно жестких условиях удаления защищающих групп. К немногим эфирным группам, которые могут широко использоваться для защиты вследствие легкости их удаления, следует отнести бензильную, другие арилметильные и силильную (см. часть 13). [c.332]
Предшественники (зимогены) — пепсиноген, трипсиноген и химо-трипсиноген получены в чистом виде. Активация заключается в удалении небольшого пептидного фрагмента и катализируется либо активной формой самого фермента, либо энтерокиназой, другим ферментом, имеющимся в пищеварительном тракте. При превращении трипсиноге-на в трипсин с N-конца белка отщепляются гексапептид вал— (асп)4 — лиз и N-концевой аминокислотой становится изолейцин (Нейрат , 1955). Активация других зимогенов более сложна. Ранние работы Бергмаина (1937) на простейших модельных пептидах показали, что ферменты избирательно расщепляют определенно пептидные связи. Пепсин, трипсин и химотрипсин известны как эндопептидазы, так как они расщепляют пептидные связи, расположенные внутри молекулы. Пепсин расщепляет амидные связи, образованные аминогруппами фенилаланина или тирозина химотрипсин расщепляет связи, образованные карбоксильными группами этих ароматических аминокислот. Трипсин расщепляет амидные связи, образованные карбоксильными группами основных аминокислот (лиз, арг). Эти протеолитические ферменты расщепляют также эфиры аналогичной структуры. Во всех случаях затрагиваются только пептиды, образованные -аминокислотами. Предположение Михаэлиса (1913), что реакции, катализируемые ферментами, проходят через стадию образования промежуточного фермент-субстратного комплекса, были подтверждены всеми последующими работами. С большой очевидностью показано, что каталитическая активность определяется небольшим участком фермента, так называемым его активным центром. [c.697]
Иногда применяют эфиры более сложной структуры, например дихлорэтилди-гликолевый эфир и аналогичные ему соединения. Можно пользоваться и ацеталями, в алкильной группе которых имеются галогены или остатки кислот (в том числе ЗОзИ) нх получают из СНгО, ацетальдегида или нз кетонов (ацетон) и тиоальдегидов и тиокетонов [c.573]
При этерификации кислоты ХХХУП метиловым спиртом в присутствии т олуолсульфокислоты образуется ее метиловый эфир XXXIX. Для получения эфиров более сложной структуры часто используют реакцию переэтерификации. Например, при нагреваний эфира XXXIX с пентаэритритом в присутствии метилата натрия [c.300]
Таким образом, исследованные фракции, как и описанные, выше кислородсодержащие фракции нетролейного экстракта (Н-2, -3 и-4), следует рассматривать как сложные эфиры алициклической структуры с боковыми алифатическими цепями, кетоиньши и свободными гидроксильньши группами. Вероятно наличие двойной связи С=Си простых эфирных группировок—О—, связывающих отдельные звенья молекулы или входящих в состав гетер6- циклических ядер. Все эти соединения могут быть отнесены к производным терпенового ряда, различающихся между собой как степенью конденсированности молекул, так и числом отдельных функциональных групп. [c.295]
Реакции гидролиза и конденсации являются, пожалуй, наиболее важными реакциями как в органической и неорганической, так и в биологической химии. Разнообразен круг используемых для этих реакщй гомогенных катализаторе , от простейшего - протона - до металлоферментов весьма сложной структуры. Для иллюстрации рассмотрим гидролиз органических эфиров или амидов, катализируемый кислотами. [c.131]
chem21.info
Сложные эфиры, их строение. Жиры
Понятие о химическом строении белков. Как мы неоднократно имели случай убедиться, наиболее устойчивыми к воздействию химических реактивов в органических молекулах являются углерод-углеродные связи. Нагревание вещества с водными растворами кислот или щелочей обычно не нарушает этих связей гидролиз, как правило, приводит к расщеплению связей у кислорода или азота. Таковы реакции гидролитического расщепления сложных эфиров (например, жиров) и амидов. Белковые вещества при гидролизе распадаются в конечном итоге до а-аминокислот. Если в состав белка входят только различные а-аминокислоты, то мы имеем дело с так называемыми собственно белками, или протеинами Но существуют и сложные белки, или протеиды, в состав которых входят остатки соединений, принадлежащих к иным классам органических и неорганических соединений. [c.393] Состав, строение. Классификация. Жиры — это смесь сложных эфиров глицерина и высших жирных кислот (ВЖК). В образовании сложных эфиров, входящих в состав жиров, могут принимать участие различные высшие жирные кислоты, но из спиртов — только один — глицерин. Поэтому эти эфиры называют глицеридами [c.169]Жиры синтезируются во всех организмах, и в зависимости от источника их получения различают растительные жиры, которые часто называют маслами, и животные жиры. Растительные и животные жиры различаются по ряду свойств, связанных с особенностями их строения. Жиры —это смеси сложных эфиров (глицеридов), глицерина и высокомолекулярных жирных кислот. Они имеют следующую общую формулу [c.305]
Основным сырьем для их получения долгое время служили природные жиры — сложные эфиры глицерина и различных жирных кислот, омылением которых обычно и получали мыла карбоновых кислот. Необходимость огромного расхода ценного пищевого сырья потребовала развития производства синтетических жирных (кислот (СЖК). В настоящее время СЖК нормального строения, содержащие 10—20 атомов углерода в молекуле, получают рядом методов (см. ниже) и широко используют в производстве ПАВ. [c.77]
Жиры — сложные эфиры трехатомного спирта глицерина и высших карбоновых кислот нормального строения, содержащих от 8 до 24 углеродных атомов. Жиры несут энергетическую функцию в организме. [c.295]
Сложные эфиры. Строение, химические свойства. Реакция этерификации. Жиры, их роль в природе, химическая переработка жиров (гидролиз, гидрирование). [c.505]
Различные типы жирных кислот, образующих мыла, находятся в природе в виде сложных эфиров глицерина (жиры и масла) и в виде сложных эфиров высших алифатических спиртов (воски). Жирные кислоты, входящие в состав этих естественных продуктов, представляют собой насыщенные и ненасыщенные кислоты нормального и разветвленного строения, а также оксикислоты, как, например, рицинолевая кислота касторового масла или кислоты, находящиеся в шерстяном жире. [c.29]
Жиры и масла растительного и животного происхождения [129, 160, 161] представляют собою смеси сложных эфиров глицерина и жирных кислот (триглицериды) строения [c.405]
Нормальные жирные кислоты с длинной цепью получают из сырья нефтяного происхождения, а именно из твердого парафина окислением воздухом (гл. 4, стр. 74). Такие кислоты можно использовать для производства высших жирных спиртов нормального строения при этом либо каталитически гидрируют сложные эфиры, либо соли тяжелых металлов этих кислот подвергают действию водорода при высоких температуре и давлении [19]. Этерификацией синтетических высших кислот с глицерином, полученным из пропилена (гл. 10, стр. 179), можно изготовить жир полностью искусственного происхождения. В Германии, исходя из синтетических Си—С12-кислот, производили этим способом синтетическое масло. Последнее в некоторых отношениях имеет преимущество перед натуральным маслом, например синтетическое масло рекомендуют в пищу диабетикам [20]. [c.341]
Реакция этерификации. Понятие о сложных эфирах. Высшие жирные кислоты. Жиры, их строение. [c.217]
Сложные эфиры, их строение. Жиры [c.236]
По химическому строению жиры представляют собой сложные эфиры глицерина и высших предельных и непредельных карбоновых кислот. Их называют также триглицеридами. [c.419]
Жиры представляют собой сложные эфиры глицерина и гомологов уксусной кислоты, начиная с масляной и до стеариновой (и выше). В природных жирах содержатся кислоты только с четным числом углеродных атомов. Кроме того, в жирах (больше в жидких, чем в твердых) находятся непредельные жирные кислоты с тем же числом углеродных атомов, в цепи которых имеются от одной до трех двойных связей (стр. 329). Строение предельных жиров следуюш ее [c.174]
Методом гидролиза определено строение многих растительных и животных жиров и восков. Так, например, установлено, что воскообразный жир нз хвостовых желез птиц содержит октадециловый С1аНд70Н спирт, а жиры из шерсти состоят из сложного эфира холестерина со стеариновой кислотой (холестериновые жиры). [c.534]
Жиры — это смеси сложных эфиров, образованных трехатомным спиртом — глицерином и высшими жирными кислотами. Строение жиров было выяснено в 1811 г. французским химиком Шеврелем. [c.246]
Шееле, нагревая жиры со щелочами, получил сладкое масло , названное впоследствии глицерином. В 1823 г. Шеврель установил, что жиры при гидролизе дают, кроме глицерина, ряд органических кислот. Он изучил строение важнейших кислот, входящих в состав жиров, и дал им названия (стеариновая, пальмитиновая, олеиновая и др.). Шев,рель выяснил также, что жиры являются сложными эфирами глицерина и соответствующих кислот. Вскоре Бертло произвел синтез жиров. Синтез глицеридов в лаборатории, произведенный Бертло, так же как и синтез углеводов, произведенный А. М. Бутлеровым (стр. 70), явились большими научными достижениями. [c.91]
По химическому строению жиры — смеси сложных эфиров (глицеридов), глицерина и высокомолекулярных жирных кислот. Они построены по такой общей схеме [c.31]
Многие высшие жирные карбоновые кислоты, преимущественно нормального строения и с четным числом атомов углерода, в виде сложных эфиров глицерина входят в состав животных и растительных жиров, из которых их получают каталитическим гидролизом. Значительные количества высших жирных карбоновых кислот получают в производственных условиях каталитическим окислением [c.166]
Различные жиры и масла отличаются друг от друга по типу, числу и распределению жирных кислот, входящих в молекулы глицеридов. В большей части случаев, особенно в маслах растительного происхождения, жирные кислоты распределяются между молекулами глицеридов относительно равномерно. Кроме глицеридов в жирах и маслах, по крайней мере неочищенных, содержатся небольшие количества свободных жирных кислот, образующихся при частичном гидролизе триглицеридов, фосфа-тидов (триглицеридов, в которых одна из жирных кислот замещена сложным эфиром фосфорной кислоты, например летицин или кефалин), а также стерины, витамины, углеводы, кароти-ноидные пигменты, белки, токоферолы и другие вещества неустановленного строения. [c.641]
Жиры — сложные эфиры глицерина и высших карбоновых кислот (триглицериды). Неизменной составной частью животных и растительных жиров является глицерин. Карбоновые кислоты могут быть различны, но всегда нормального строения и преимущественно с четным числом атомов углерода. Большая часть животных и растительных жиров содержит кислоты с 16 и 18 атомами углерода. [c.172]
Многие высшие жирные карбоновые кислоты, преимущественно нормального строения и с четным числом атомов углерода, в виде сложных эфиров глицерина входят в состав животных и растительных жиров, из которых их получают каталитическим гидролизом. Значительные количества высших жирных карбоновых кислот получают в производственных условиях каталитическим окислением жидких или твердых алканов нефти при этом образуется смесь карбоновых кислот [c.169]
В этом разделе изучаются номенклатура, строение и свойства большой группы производных углевс1Доро-дов, содержащих кислородсодержащие функциональные группы. Простейшими представителями этой группы являются спирты, поэтому они открывают настс ящий раздел. Далее в нем последовательно рассматриваются фенолы, содержащие такую же функциональную группу, как и спирты, альдегиды, карбоновые кислоты, сложные эфиры, в частности, жиры-триглицериды, углеводы [c.526]
Структурным изомером эруковой кислоты является цетолеиновая кислота (т. пл. 33,0—33,7° С), строения h4( Hj)s H= H( Hj), СООН. Цетолеиновая кислота содержится в виде сложных эфиров в жирах морских млекопитающих и рыб. [c.475]
Нейтральные жиры (триглицериды) состоят из трех молекул жирных йслот, химически связанных с одной молекулой глицерина 1в виде сложного эфира. Свойства жиров определяются свойствами жирных 1кислот, вхо дящих в их состав. Молекула жира (глицерида) имеет следующее строение [c.7]
Общие сведения о г л и ц е р и и е. Ви. ють до совсем недав" пего времени потребность в глицерине почти целиком удовлетворяли путем омыления природных 5киров, которые, как известно, являются сложными эфирами глицерина с высшими алифатическими одноосновными кислотами нормального строения, имеющими четное число атомов углерода. Содержание глицерина в жирах составляет в среднем всего лишь около 10,5%, за исключением кокосового и пальмового масел, в которых в результате относительно большего удельного веса низкомолекулярных кислот глицерина содержится около 14%. Следовательно, нри ежегодном потреблении 50 ООО m глицерина необходимо подвергать омылению и дальнейшей переработке приблизительно 600 000 т жиров. [c.373]
Эруковая кислота С21Н41СООН (темп, плавл. 34°) содержится в виде сложного эфира глицерина в некоторых жирах, например в масле репы, белой и черной горчицы, семян винограда и других. В присутствии следов азотистой кислоты она переходит в плавящуюся при 60° твердую брассидиновую кислоту. Расщепление обеих кислот при окислении с образованием пеларгоновой кислоты gHir OOH и брассиловой кислоты НООС—(СНз) —СООН показывает, что обе кислоты имеют одинаковое строение СНз(СН2)7СН=СН(СН2)цСООН, т. е. являются стереоизомерами. [c.407]
Натуральные ВЖК-преим. одноосновные к-ты нормального строения с четным числом атомов углерода в молекуле м. 6. насыщенными и ненасыщенными (с двойными связями, реже с тройными). Кроме карбоксильной группы, они могут содержать др. функц. группы, напр. ОН. Содержатся в животных жирах и растит, маслах в виде сложных эфиров глицерина (т. наз. глицеридов), а также в прир. восках в виде эфиров высших жирных спиртов. Наиб. распространены к-ты с 10-22 атомами углерода в молекуле (см. табл. 1). [c.443]
Эпоксиды являются реакционноспособными соединениями и могут служить ценными полупродуктами (см. разд. 25.1.6.4, 25.1.9.2) [49]. Информацию об их строении можно получить методом масс-спектрометрии или расщеплением до альдегидов метаиодной кислотой. Из эпоксидов могут быть регенерированы алкены (схема 46). Частично эпоксидированные жиры или сложные эфиры получают в промышленном масштабе их применяют в качестве пластификаторов. [c.50]
Зависимость скорости гидролиза жиров и вообще сложных эфиров от природы исходных продуктов стала объектом изучения с конца прошлого столетия. Ловенгерц [112] показал, что при кислотном гидролизе влияние строения спиртового радикала эфира сравнительно невелико, тогда как зависимость скоростей гидролиза от химического строения кислоты огромна этилфор-миат, например, гидролизуется примерно в 20 раз быстрее этил-ацетата. В принципе такая же зависимость обнаружена и при щелочном гидролизе [106]. Но в этом случае и строение спиртового радикала играет значительную роль метилацетат, например, гидролизуется в два раза быстрее, чем изобутилацетат. [c.281]
Состав жиров и их строение были установлены более 100 лет назад благодаря работам французских химиков Шевреля и Берт-ло. В начале прошлого столетия Шеврель установил, что жиры и масла при длительном нагревании с водой и шелочью разлагаются, выделяя карбоновые кислоты и глицерин. Несколько позднее (1854 г.) Бертло удалось синтезировать жиры из глицерина и карбоновых кислот. Таким образом было показано, что жиры являются сложными эфирами карбоновых кислот и трехатомного спирта глицерина. В дальнейшем было установлено, что в состав природных жиров, кроме глицерина, входят карбоновые кислоты главным образом с прямой неразветвленной углеродной цепью, состоящей из четного числа (8—20) углеродных атомов. [c.149]
Жироподобные вещества. В свое время некоторые органические вещества, напоминающие по своей растворимости жиры, были выделены в осо бую группу жироподобных веществ, или липоидов. Впоследствии оказалосЬ что большинство этих веществ напоминает жиры не только по растворимости, но и имеет с ними некоторые общие черты строения. Большинство липоидов представляет собой так же, как и жиры,. сложные эфиры. К числу таких веществ относятся фосфатиды, стериды, цериды и другие. Остановимся корот ко на некоторых из них с целью предварительного ознакомления с их строением. Многие из фосфатидов и стеридов играют важную роль в жизнедеятельности организмов и потому будут подробно рассмотрены в курсе биологической химии. [c.144]
По химическому строению фосфатиды, как и жиры, представ-ллют собой сложные эфиры глицерина. Однако в отличие от жиров одна из трех спиртовых групп глицерина связана в фосфатидах не с жирной, а с фосфорной кислотой, которая в свою очередь связана эфирной связью с аминоалкоголями холином (в лецитинах) и коламином (в кефалинах) или с аминокислотой серином (в фосфатидилсерипах). Остальные два гидроксила глицерина этерифицированы жирными кислотами — пальмитиновой, стеариновой, олеиновой, линолевой и др. [c.120]
Холинфосфатиды, или лецитины (греч. 1ек11Ноз — желток), представляют собой, так же как и жиры, сложные эфиры глицерина. Химическое строение лецитинов было впервые изучено К- Дьяконовым в 1867 г. В отличие от жиров одна из трех спиртовых групп глицерина связана в лецитинах не с жирной, а с фосфорной кислотой. Другая особенность лецитинов состоит в том, что фосфорная кислота в них связана эфирной связью с азотистым основанием — холииом. Следовательно, в молекуле лецитина соединены глицерин, высшие жирные кислоты, фосфорная кислота и холин. [c.97]
chem21.info





















