Содержание
1. Какие побочные продукты образуются при получении п-толуолсульфокислоты и как можно уменьшить их образование?
№4А
Синтез
уксусноэтилового эфира
Цель работы:
На примере синтеза уксусноэтилового
эфира познакомиться с реакциями
нуклеофильного замещения у алифатического
ненасыщенного атома углерода, в частности,
с реакциями этерификации.
Основная реакция:
Реактивы:
уксусная кислота (ледяная)-10 мл., этиловый
спирт-11,25 мл., серная кислота(1.84)-1,25 мл.,
карбонат натрия, хлорид кальция-4 г.
Оборудование:
Колба Вюрца на 100 мл., нисходящий водяной
холодильник, капельная воронка, песчаная
баня, делительная воронка, термометр
на 1500С,
коническая колба на 100 мл., цилиндры на
50 и 10 мл.
Ход работы:
Колбу Вюрца на
100 мл. закрепляют в лапке штатива и
закрепляют в лапке штатива и
помещают в песчаную баню. Вносят в колбу
2.5 мл. этилового спирта и осторожно при
помешивании добавляют 2.5 мл. концентрированной
серной кислоты, закрывают её пробкой,
в которую вставлен термометр и капельная
воронка. После этого колбу соединяют
снисходящим водяным холодильником.
Холодильник снабжают аллонжем, конец
которого опускают в приёмник. Затем
колбу нагревают на песчаной бане. По
достижении температуры 110-1200С
начинают постепенно приливать из
капельной воронки смеси (20 мл. этилового
спирта и 20 мл. ледяной уксусной кислоты)
с такой скоростью, скакой отгоняется
образующийся этилацетат.
Требования
при выполнении синтеза:
1. Перед началом
работы поместите в колбу Вюрца «кипелки»
для равномерного кипения.
2. В процессе
отгонки, которая длиться 2 часа,
поддерживать температуру бани 1400С
( при более высокой температуре усиливается
образование побочного продукта-
диэтилового эфира).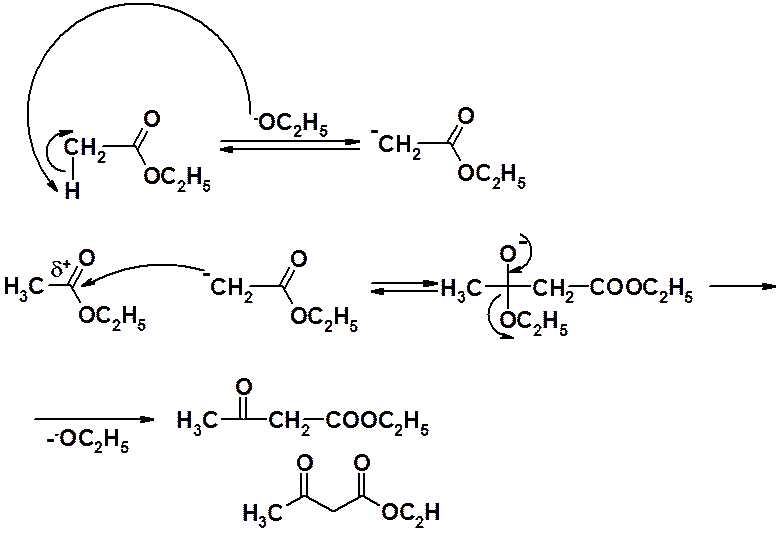
По окончании
реакции полученный дистиллят, содержащий
примеси уксусной кислоты, нейтрализуют
концентрированным раствором карбоната
натрия. Его добавляют постепенно, при
перемешивании жидкости стеклянной
палочкой ( происходит вспенивание
вследствие выделения углекислого газа).
Раствор карбоната натрия добавляют до
тех пор, пока синяя лакмусовая бумажка,
опущенная в верхний эфирный слой, не
перестанет краснеть.
Уксусноэтиловый
эфир отделяют при помощи делительной
воронки от нижнего водяного слоя и
встряхивают с насыщенным раствором
хлорида кальция. Отделив эфир, его сушат
хлоридом кальция и перегоняют на водяной
бане.
Хлорид кальция
используют для удаления примеси этилового
спирта: с первичными спиртами он образует
кристаллические соединения. В данном
случае получается соединение состава,
не растворимое в уксусноэтиловом эфире,
но растворимое в воде.
Уксусноэтиловый
эфир(этилацетат)—
бесцветная жидкость, смешивается с
этанолом,эфиром, хлороформом, бензолом
ограничено растворяется в воде.
Молекулярная масса 88.10., температура
плавления-83,6, температура кипения
77,150С.
Этилацетат
образует с этанолом и водой следующие
азеотропные смеси:
А) 91,8% этилацетата
и 8,2% воды, кипит при 70,40С
Б) 83,2% этилацетата
и 9% этанола и 7,8% воды, кипит при 70,30С
В) 69,2% этилацетата
и 30% этанола, кипит при 71,80С
Контрольные
вопросы.
1. Какова роль
серной кислоты в синтезе этилацетата?
2. Реакция
этерификации обратима. В случае получения
этилацетата каким образом удаётся
сместить равновесие вправо?
3. К каким побочным
продуктам может привести повышение
температуры реакции?
Литература:
1. Практикум по
Практикум по
органическому синтезу. — М., Просвещение,
1974
2. Конспект лекции
по органической химии и органическому
синтезу.
3. Васильева В.В.,
Зонис С.А. Органическая химия. — М.,
Просвещение,1972.
№ 5Б Синтез
антрахинона
Цель работы:
На примере синтеза антрахинона из
антрацена познакомиться с реакциями
окисления органических соединении, в
частности, с реакциями окисления
ароматических углеводородов по ядру.
Основная реакция:
Реактивы:
антранцен-0,625 г., оксид хрома-2,5 г., ледяная
уксусная кислота-15 мл., гидроксид натрия-2
н.
Оборудование:
круглодонная
колба на 300 мл., двурогий форшторсс,
обратный холодильник, капельная воронка
на 100 мл., химический стакан на 500 мл.,
цилиндры на 10 мл. и на 100 мл. , фарфоровая
, фарфоровая
ступка, водяная баня, прибор для
отсасывания.
Ход работы:
В круглодонную
колбу ёмкостью 300 мл. снабженную двурогим
форштоссом с обратным холодильником и
капельной воронкой, помещают 0,625 г. тонко
растертого в порошок антроанцена (
осторожно, вызывает раздражение слизистых
оболочек) и 15 мл. уксусной кислоты.
Полученную смесь нагревают до кипения
для полного растворения антранцена.
Затем в течение часа при постоянном
кипячении из капельной воронки прибавляют
раствор 2,5 г. оксида хрома в 2,5 мл. воды
и 10 мл. ледяной уксусной кислоты
(окрашивание реакционной смеси в зеленый
цвет указывает на окончание реакции).
После охлаждения реакционную смесь
переносят в стакан, разбавляют 70 мл.
воды. Выдерживают один час, затем
отсасывают выпавшие кристаллы антрахинона,
промывают их водой, затем разбавленным
раствором щелочи для нейтрализации
уксусной кислоты. Полученный влажный
антрахинон сушат на воздухе. Выход около
0,5 г.
Требования при
выполнении синтеза:
1. Перед началом
работы поместите в колбу «кипелки» для
равномерного кипения.
2. Перед началом
работы смажьте все шлифы небольшим
количеством смазки.
3. Хромовую смесь
готовьте в
стакане
и наливайте в капельную воронку ПОД
ТЯГОЙ.
4. Посуду,
загрязненную уксусной кислотой мойте
и дегазируйте под тягой.
Качественная
реакция. Восстановление антрахинона.
В пробирку помещают
несколько кристалликов антрахинона и
2-3 мл разбавленного раствора гидроксида
натрия. Нагревают смесь до кипения.
Затем вносят немного цинковой пыли,
нагревают еще 1-2 мин. И охлаждают. По
окончании реакции восстановления
(прекращение выделения пузырьков
водорода) появляется ярко-красное
окрашивание аниона антрагидрохинона.
При встряхивании раствор обесцвечивается.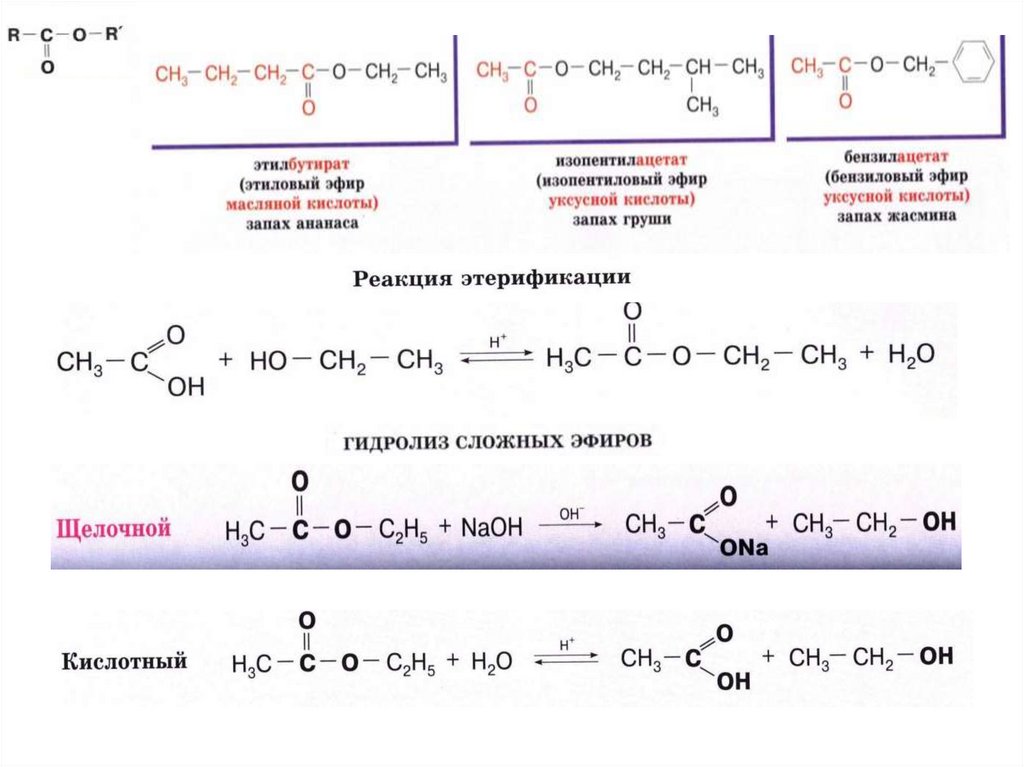
Антрахинон
(9,10-дигидро-9,10дикетоантранцен)-кристаллическое
вещество в виде светложёлтых ромбов,
нерастворим в воде, трудно растворим в
спирте, эфире, хорошо растворим в серной
кислоте, анилине, нитробензоле и горячем
толуоле. Молекулярная масса 208,2.,
температура кипения 379-3810С,
температура плавления 2860С.
Контрольные
вопросы:
1. Расставить
степени окисления над атомами, у которого
они изменились в процессе реакции.
2. Почему в
антранцене действию окисления легче
всего подвергается атомы углерода?
3. Какова роль
уксусной кислоты в реакции окисления
антранцена в антрахинон?
4. По каким
изменениям реакционной смеси можно
судить о конце реакции?
Синтез натриевой
соли толуолсульфокислоты.
Цель работы:
На примере синтеза п- толуолсульфокислоты
познакомиться с реакциями электрофильного
замещения ароматических углеводородов,
в частности, с реакциями сульфирования
бензола.
Основная реакция:
Реактивы:
толуол-16 мл., серная кислота-9.5 мл.,
углекислый натрий-8 г., насыщенный раствор
хлористого натрия-20 мл.
Оборудование:
длинногорлая круглодонная колба на 100
мл., химические стаканы на 100 мл., обратный
холодильник (водяной), прибор для
отсасывания, плитка с закрытой спиралью,
асбестовая сетка.
Ход работы:
В круглодонную
колбу помещают несколько кипелок, 16 мл.
толуола и осторожно вносят 9.5 мл. конц.
серной кислоты. Колбу снабжают обратным
холодильником и слабо кипятят в течение
одного часа на плитке с асбестовой
сеткой, время от времени встряхивая
колбу. При правильном нагревании толуол
кипит равномерно. Чрезмерное нагревание
выводит толуол из зоны реакции и
способствует образованию дисульфопроизводных.
Непрерывное встряхивание ускоряет
реакцию и способствует хорошему выходу.
Реакция считается законченной, когда
слой толуола почти исчезнет, из
холодильника, изредка стекают капли
конденсанта. Затем теплую реакционную
смесь выливают в стакан с 70 мл. воды
(если смесь начинает кристаллизоваться,
то ее необходимо подогреть и колбу
ополаскивать из промывалки. Кислый
раствор осторожно нейтрализуют 8 г.
углекислого натрия, добавляют его
небольшими порциями. Добавляют в раствор
20 г. хлористого натрия и нагревают смесь
до кипения (если хлористый натрий не
растворяется, добавляют еще немного
воды). Раствор охлаждают водой со льдом.
Выпавшие кристаллы
натриевой соли толуолсульфокислоты
отсасывают на воронке Бюхнера, со
стеклянным фильтром. Промывают 20 мл.
насыщенного раствора хлористого натрия
и отжимают между листами фильтровальной
бумаги и оставляют сушиться на воздухе.
Выход натриевой
соли толуолсульфокислоты с примесью
хлористого натрия-8 г.
Требования при
выполнении синтеза:
1. Перед началом
Перед началом
работы поместите в колбу «кипелки» для
равномерного кипения.
2. Перед началом
работы смажьте все шлифы небольшим
количеством смазки.
Контрольные
вопросы:
2. Когда можно считать реакцию сульфирования законченной?
3. С какой целью после окончания реакции разбавленной водой реакционной смеси добавляют углекислый натрий?
№3 Синтез
бромистого этила.
Цель работы:
На примере синтеза бромистого этила
познакомиться с реакциями нуклеофильного
замещения у насыщенного атома углерода.
Основная реакция:
KBr +
H2SO4→
KHSO4
+ HBr
C2H5OH+
HBr→ C2H5Br
+ H2O
C2H5OH+
H2SO4→
C2H5O-SO2-OH
+ H2O
Побочные
реакции:
2HBr
+
H2SO4
→
Br2+
H2O
+SO2
C2H5O-SO2-OH
+ C2H5OH→
C2H5OC2H5+
H2SO4
Реактивы:
этиловый спирт 95%-16 мл.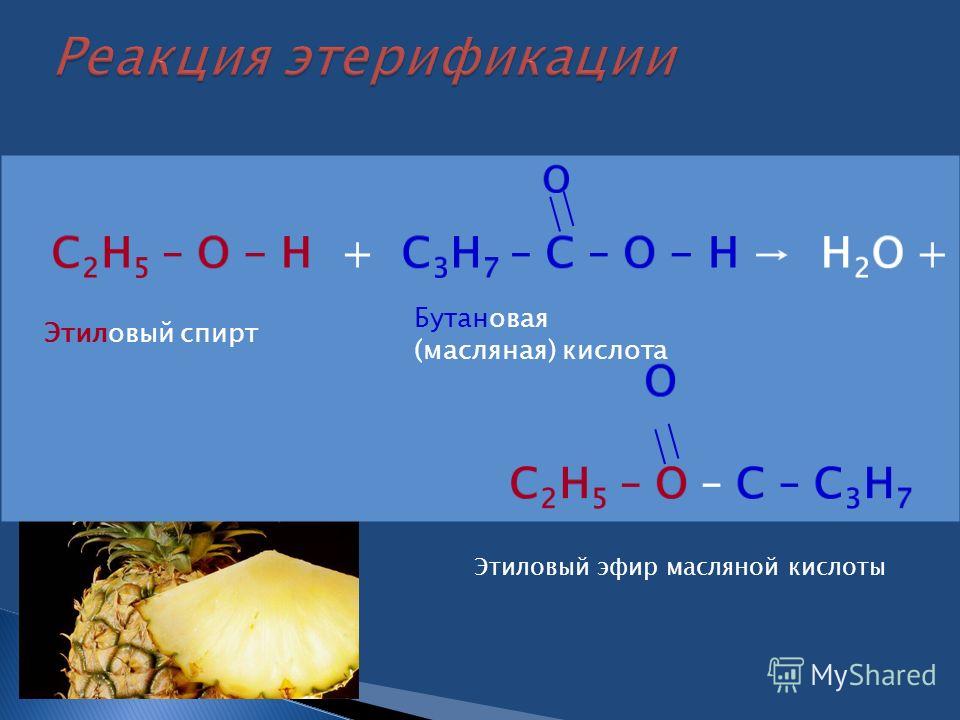 , бромистый калий-15
, бромистый калий-15
г., серная кислота-16мл, вода-10 мл
Оборудование:
колба круглодонная на 100 мл., приемник,
воронка делительная на 100 мл., воронка
капельная на 100 мл., воронка простая,
холодильник Либиха, дефлегматор, насадка
к дефлегматору, аллонж, песчаная баня,
кристаллизатор, цилиндры на 10 мл. и на
50 мл., железный шпатель, термометр.
Ход работы:
В песчаную баню
помещают круглодонную колбу ёмкостью
100 мл. соединяют её с дефлегмотором и
длинным холодильником, к которому
присоединяют аллонж. Конец аллонжа
опускают на 1-1.5 см в смесь воды со льдом,
налитую в колбу- приемник, которую
погружают в ледяную баню. Так как
бромистый этил летуч, то для уменьшения
потерь погон собирают в приёмник с водой
и ьдом.
В реакционную
колбу ёмкостью 100 мл. заливают 16 мл.
этилового спирта и 10 мл. холодной воды
При постоянном
перемешивании реакционной смеси и
охлаждении колбы проточной водой к
смеси осторожно добавляют 16 мл. серной
серной
кислоты. Затем в охлажденную смесь
добавляют 30 г. тонко измельченного
бромистого калия. При появлении паров
брома приостановите добавление соли.
Собирают прибор
(по схеме).
Нагрейте песчаную
баню до 130-1500С,
через некоторое время начнется отгонка
бромэтана (tкип=38-400С),
представляющего собой тяжелые, маслянистые
капли, опускающиеся на дно приемника.
Оптимальная скорость отгонки 1 капля в
сек.
Как правило,
через 1-1,5 часа перегонка бромэтана
заканчивается. Приемник снимите и
оставьте под тягой, уберите песчаную
баню, установку в течение часа не
разбирайте, реактор должен охладиться
до комнатной температуры, после чего
остаток реакционной смеси сливается в
емкость для слива органических веществ.
Содержимое
приемника перенести в делительную
воронку и нижний слой слить в сухую
колбу на 30 мл.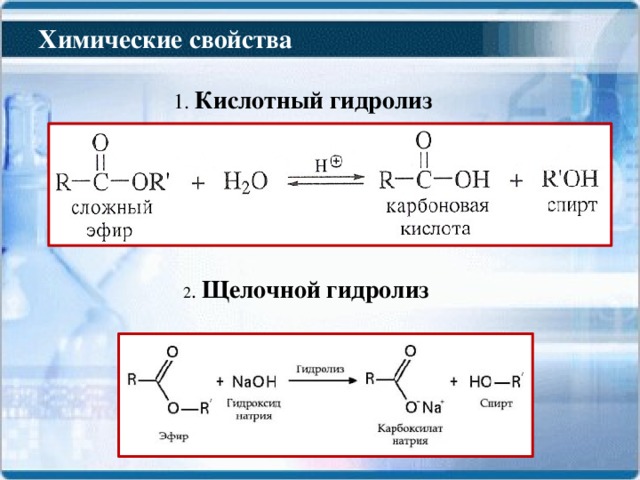 В бромэтане содержатся
В бромэтане содержатся
примеси воды, этанола, диэтилового эфира
и их удаляют конц. Серной кислотой,
добавляя ее осторожно по каплям до тех
пор, пока она не соберется в виде
отдельного слоя над бромэтаном. Если
будет разогрев колбы, охладите ее в бане
с холодной водой. Используя сухую
делительную воронку, нижний слой
отделите, и перенесите в сухую колбу
для последующей перегонки бромистого
этила на водяной бане.
Соберите фракцию
с tкип=38-390С,
измерьте объем бромэтана.
Требования
при выполнении синтеза:
1. Перед началом
работы поместите в колбу «кипелки» для
равномерного кипения.
2. Перед началом
работы смажьте все шлифы небольшим
количеством смазки.
3. Бромэтан из-под
тяги не выносить,
т.к. пары этого вещества вызывают сильную
головную боль.
Бромистый этил(
бромэтан)-бесцветная
жидкость с запахом эфира, в 100 г. воды
воды
при 200С
растворяется 0.914 г., хорошо растворяется
в спирте, эфире, обладает свойствами
типичными для галогенопроизводных
предельных углеводородов. На свету
желтеет, температура кипения 38.30С,
ρ=1.4586.
Контрольные
вопросы:
Практическая работа № 6. Получение этилового эфира уксусной кислоты. ГДЗ Химия 10-11 класс Цветков. – Рамблер/класс
Практическая работа № 6. Получение этилового эфира уксусной кислоты. ГДЗ Химия 10-11 класс Цветков. – Рамблер/класс
Интересные вопросы
Школа
Подскажите, как бороться с грубым отношением одноклассников к моему ребенку?
Новости
Поделитесь, сколько вы потратили на подготовку ребенка к учебному году?
Школа
Объясните, это правда, что родители теперь будут информироваться о снижении успеваемости в школе?
Школа
Когда в 2018 году намечено проведение основного периода ЕГЭ?
Новости
Будет ли как-то улучшаться система проверки и организации итоговых сочинений?
Вузы
Подскажите, почему закрыли прием в Московский институт телевидения и радиовещания «Останкино»?
Есть подсказки к этой лабе?
Составьте уравнение реакции образования сложного эфира из уксусной кислоты и этилового спирта.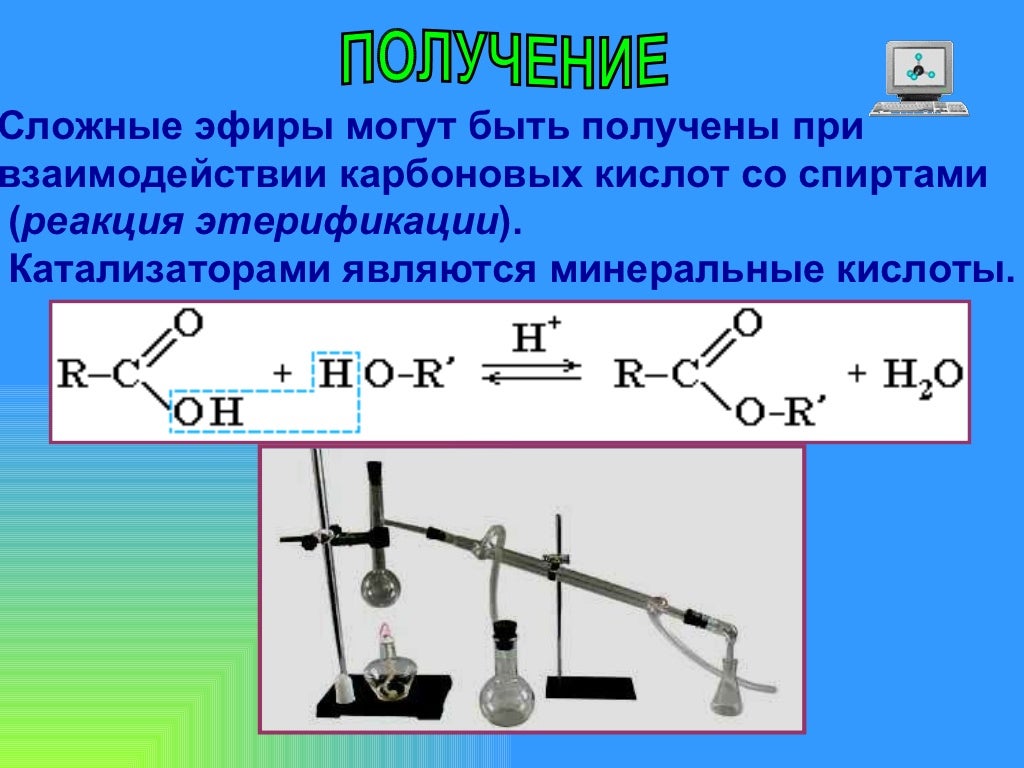
Для работы воспользуйтесь прибором, изображенным на рисунке 64, несколько видоизменив его, как указано ниже.
Налейте в колбу 10-12 мл выданной вам смеси этилового спирта, уксусной кислоты и серной кислоты. Присоедините к колбе водяной или воздушный холодильник, нижний конец которого опустите в приемник, помещенный в смесь воды со льдом. Нагревайте смесь в колбе на водяной бане или через сетку (осторожно!). Когда соберется достаточное количество эфира и перегонка замедлится, опыт прекратите.
Чтобы освободить эфир от примеси спирта и кислоты, добавьте воды и смесь взболтайте. Затем разделите ее при помощи делительной воронки.
ответы
Собрали прибор, как это показано на рисунке 64 учебника. В
пробирку налили этанол, добавили уксусной кислоты и серной ки-
слоты. Полученную смесь нагрели. Наблюдаем конденсацию паров
эфира в приемнике. Отделили эфир при помощи делительной во-
ронки.
ваш ответ
Можно ввести 4000 cимволов
отправить
дежурный
Нажимая кнопку «отправить», вы принимаете условия пользовательского соглашения
похожие темы
Юмор
Олимпиады
ЕГЭ
9 класс
похожие вопросы 5
Глава 11. Вопрос 5 ГДЗ Химия 10-11 класс Цветков. Какую роль играют водородные связи в построении белковой молекулы?
Вопрос 5 ГДЗ Химия 10-11 класс Цветков. Какую роль играют водородные связи в построении белковой молекулы?
Какую роль играют водородные связи в построении белковой
молекулы? Какие еще вам известны примеры зависимости свойств ве-
(Подробнее…)
ГДЗХимия10 класс11 классЦветков Л. А.
Почему сейчас школьники такие агрессивные ?
Читали новость про 10 классника который растрелял ? как вы к этому относитесь
Новости10 классБезопасность
Здравствуйте.
(Подробнее…)
Химия
Какой был проходной балл в вузы в 2017 году?
Какой был средний балл ЕГЭ поступивших в российские вузы на бюджет в этом году? (Подробнее…)
Поступление11 классЕГЭНовости
11. Выпишите слово, в котором на месте пропуска пишется буква Е. Русский язык ЕГЭ-2017 Цыбулько И. П. ГДЗ. Вариант 12.
11.
Выпишите слово, в котором на месте пропуска пишется буква Е.
произнос., шь (Подробнее…)
ГДЗЕГЭРусский языкЦыбулько И.П.
Синтез этилацетата из глюкозы Kluyveromyces marxianus, Cyberlindnera jadinii и Wickerhamomyces anomalus в зависимости от режима индукции
1.
Чан, В.-К.
,
Су, М.-К.
, Биофильтрация этилацетата и амилацетата с использованием биофильтра из композитных шариков. Биоресурс. Технол.
2008, 99, 8016–8021. [PubMed] [Google Scholar]
2.
Альварес-Орнос, Ф. Дж.
,
Волкерт, Д.
,
Хейндерикс, П. М.
,
Ван Лангенхове, Х.
, Производительность композитного мембранного биореактора для удаления этилацетата из отработанного воздуха. Биоресурс. Технол.
2011, 102, 8893–8898. [PubMed] [Google Scholar]
3.
Посада, Дж. А.
,
Патель, А. Д.
,
Роуз, А.
,
Блок, К.
и др., Потенциал биоэтанола в качестве химического строительного блока для биоперерабатывающих заводов: предварительная оценка устойчивости 12 продуктов на основе биоэтанола. Биоресурс. Технол.
2013, 135, 490–499. [PubMed] [Google Scholar]
4.
Нильсен, М.
,
Юнг, Х.
,
Каммер, А.
,
Беллер, М.
, На пути к экологичному процессу крупномасштабного синтеза этилацетата: эффективное безакцепторное дегидрирование этанола. Ангью. хим. Междунар. Эд.
2012, 51, 5711–5713
[PubMed] [Академия Google]
5.
Лезер, К.
,
Урит, Т.
,
Блей, Т.
, Перспективы биотехнологического производства этилацетата дрожжами. заявл. микробиол. Биотехнолог.
2014, 98, 5397–5415. [PubMed] [Google Scholar]
6.
Страхоф, А.Дж.Дж.
,
Бамбули, А.
, Потенциал перехода товарных химикатов на биооснову в соответствии с максимальным выходом и ценами на нефтехимию. Биотопливо Биопрод. биореф.
2017, 11, 798–810. [Google Scholar]
7.
Падилья, Б.
,
Гил, Дж. В.
,
Мансанарес, П.
, Проблемы нетрадиционных дрожжей Wickerhamomyces anomalus в виноделии. Ферментация
2018, 4(68), 1–14. [Google Scholar]
8.
Равасио, Д.
,
Карлин, С.
,
Бэкхут, Т.
Греневальд, М.
и др., Придание вкуса напиткам с помощью нетрадиционных дрожжей. Ферментация
2018, 4(15), 1–16. [Google Scholar]
[Google Scholar]
9.
Парк, YC
,
Шаффер, C.E.H.
,
Беннетт, Г. Н.
, Микробное образование сложных эфиров. заявл. микробиол. Биотехнолог.
2009, 85, 13–25. [PubMed] [Google Scholar]
10.
Круис, А.Дж.
,
Левиссон, М.
,
Марс, А.Э.
,
ван дер Плёг, М.
и др., Производство этилацетата неуловимой алкогольацетилтрансферазой дрожжей. Метаб. англ.
2017, 41, 92–101. [PubMed] [Google Scholar]
11.
Круис, А.Дж.
,
Боненкамп, A.C.
,
Патиниос, К.
ван Нуланд, Ю.М.
и др., Микробное производство сложных эфиров с короткой и средней цепью: ферменты, пути и приложения. Биотехнолог. Доп.
2019, 37:107407, 1–19. [PubMed] [Google Scholar]
12.
Кусано, М.
,
Сакаи, Ю.
,
Като, Н.
,
Ёсимото, Х.
и др., Активность алкогольдегидрогеназы в отношении полуацетального дегидрирования в Saccharomyces cerevisiae
. Бионауч. Биотехнолог. Биохим.
1998, 62, 1956–1961. [PubMed] [Google Scholar]
13.
Кусано, М.
,
Сакаи, Ю.
,
Като, Н.
,
Ёсимото, Х.
,
Тамай, Ю.
, Новая активность полуацетальдегидрогеназы, участвующая в синтезе этилацетата в Candida utilis
. Дж. Биоци. биоинж.
Дж. Биоци. биоинж.
1999, 87, 690–692. [PubMed] [Google Scholar]
14.
Лёбс, А.-К.
,
Энгель, Р.
,
Шварц, С.
,
Флорес, А.
,
Уилдон, И.
, генетические нарушения с помощью CRISPR-Cas9 для понимания биосинтеза этанола и этилацетата у Kluyveromyces marxianus
. Биотехнолог. Биотопливо
2017, 10:164, 1–14. [Бесплатная статья PMC] [PubMed] [Google Scholar]
15.
Лёбс, А.-К.
,
Шварц, С.
,
Торвалл, С.
,
Уилдон, И.
, Высокомультиплексное подавление респираторных функций CRISPRi усиливает митохондриальный локализованный биосинтез этилацетата в Kluyveromyces marxianus
. АКС Синтез. биол.
2018, 7, 2647–2655. [PubMed] [Google Scholar]
16.
Томас, К.С.
,
Доусон, P.S.S.
, Взаимосвязь между ограниченным по железу ростом и ограничением энергии при поэтапном культивировании Candida utilis
. Можно. Дж. Микробиол.
1978, 24, 440-447. [PubMed] [Google Scholar]
17.
Армстронг, Д. У.
,
Мартин, С.М.
,
Ямадзаки, Х.
, Производство этилацетата из разбавленных растворов этанола с помощью Candida utilis
. Биотехнолог. биоинж.
Биотехнолог. биоинж.
1984, 26, 1038–1041. [PubMed] [Google Scholar]
18.
Уиллеттс, А.
, Образование сложного эфира из этанола с помощью Candida pseudotropicalis
. Антони ван Левенгук
1989, 56, 175–180. [PubMed] [Академия Google]
19.
Калель-Мхири, Х.
,
Энгассер, Дж. М.
,
Микло, А.
, Непрерывное производство этилацетата с помощью Kluyveromyces fragilis на пермеате сыворотки. заявл. микробиол. Биотехнолог.
1993, 40, 201–205. [Google Scholar]
20.
Калель-Мхири, Х.
,
Микло, А.
, Механизм синтеза этилацетата Kluyveromyces fragilis
. ФЭМС микробиол. лат.
1993, 111, 207–212. [Google Scholar]
21.
Лезер, К.
,
Урит, Т.
,
Нель, Ф.
,
Блей, Т.
, Скрининг штаммов Kluyveromyces для производства этилацетата: разработка и оценка системы культивирования. англ. Жизнь наук.
2011, 11, 369–381. [Google Scholar]
22.
Урит, Т.
,
Лезер, К.
,
Вундерлих, М.
,
Блей, Т.
, Образование этилацетата Kluyveromyces marxianus на сыворотке: исследования удаления сложных эфиров. Биопроцесс Биосист. англ.
Биопроцесс Биосист. англ.
2011, 34, 547–559. [PubMed] [Google Scholar]
23.
Лезер, К.
,
Урит, Т.
,
Ферстер, С.
,
Штукерт, А.
,
Блей, Т.
, Образование этилацетата Kluyveromyces marxianus на сыворотке при аэробном периодическом и хемостатном культивировании при ограничении по железу. заявл. микробиол. Биотехнолог.
2012, 96, 685–696. [PubMed] [Google Scholar]
24.
Урит, Т.
,
Штукерт, А.
,
Блей, Т.
,
Лезер, К.
, Образование этилацетата Kluyveromyces marxianus на сыворотке при периодическом аэробном культивировании при ограничении специфических микроэлементов. заявл. микробиол. Биотехнолог.
2012, 96, 1313–1323. [PubMed] [Google Scholar]
25.
Лезер, К.
,
Урит, Т.
,
Штукерт, А.
,
Блей, Т.
, Образование этилацетата из сыворотки с помощью Kluyveromyces marxianus в экспериментальном масштабе. Дж. Биотехнология.
2013, 163, 17–23. [PubMed] [Академия Google]
26.
Урит, Т.
,
Манти, Р.
,
Блей, Т.
,
Лезер, К.
, Образование этилацетата Kluyveromyces marxianus на сыворотке: влияние аэрации и ингибирования роста дрожжей этилацетатом. англ. Жизнь наук.
англ. Жизнь наук.
2013, 13, 247–260. [Google Scholar]
27.
Урит, Т.
,
Ли, М.
,
Блей, Т.
,
Лезер, К.
, Рост Kluyveromyces marxianus и образование этилацетата в зависимости от температуры. заявл. микробиол. Биотехнолог.
2013, 97, 10359–10371. [PubMed] [Академия Google]
28.
Круис, А.Дж.
,
Марс, А.Э.
,
Кенген, S.W.M.
,
Борст, Дж. В.
и др., Алкоголь-ацетилтрансфераза Eat1 находится в митохондриях дрожжей. заявл. Окружающая среда. микробиол.
2018, 84, e01640-18. [Бесплатная статья PMC] [PubMed] [Google Scholar]
29.
Рохас, В.
,
Гил, Дж. В.
,
Пиньяга, Ф.
,
Мансанарес, П.
, Исследования производства ацетатных эфиров винными дрожжами, не относящимися к сахаромицетам. Междунар. Дж. Пищевая микробиология.
2001, 70, 283–289. [PubMed] [Google Scholar]
30.
Лезер, К.
,
Урит, Т.
,
Кейл, П.
,
Блей, Т.
, Исследования механизма синтеза этилацетата в Kluyveromyces marxianus DSM 5422. Заявл. микробиол. Биотехнолог.
2015, 99, 1131–1144. [PubMed] [Google Scholar]
31.
Круис, А.Дж.
,
Боненкамп, A.C.
,
Нэп, Б.
,
Нильсен, Дж.
и др., From Eat to trEat: Разработка митохондриального фермента Eat1 для усиленного производства этилацетата в Escherichia coli
. Биотехнолог. Биотопливо
2020, 13, 76. [Бесплатная статья PMC] [PubMed] [Google Scholar]
32.
Боненкамп, A.C.
,
Круис, А.Дж.
,
Марс, А.Э.
,
Вийффелс, Р. Х.
и др., Многоуровневая оптимизация производства анаэробного этилацетата в инженерных Кишечная палочка
. Биотехнолог. Биотопливо
2020, 13, 65. [Бесплатная статья PMC] [PubMed] [Google Scholar]
33.
Лезер, К.
,
Купш, С.
,
Вальтер, Т.
,
Гофман, А.
, Новый подход к балансировке микробного синтеза этилацетата и других летучих метаболитов при культивировании в аэробных биореакторах. англ. Life Sci, 2021, 21, 137–153. [Google Scholar]
34.
Плата, С.
,
Миллан, С.
,
Маурисио, Дж. К.
,
Ортега, Дж. М.
, Образование этилацетата и изоамилацетата различными видами винных дрожжей. Пищевой микробиол. 2003, 20, 217–224. [Академия Google]
35.
Виана, Ф.
,
Гил, Дж. В.
,
Женовес, С.
,
Валес, С.
,
Мансанарес, П.
, Рациональный выбор винных дрожжей, отличных от Saccharomyces, для смешанных заквасок на основе образования эфиров и энологических признаков. Пищевой микробиол. 2008, 25, 778–785. [PubMed] [Google Scholar]
36.
Ву, Дж.
,
Эллистон, А.
,
Ле Галл, Г.
,
Колкухун, И. Дж.
и др., Разнообразие дрожжей в связи с производством топлива и химикатов. науч. Респ.
2017, 7:14259, 1–11. [Бесплатная статья PMC] [PubMed] [Google Scholar]
37.
Хорш, Р.
,
Лезер, К.
,
Блей, Т.
, Двухступенчатый каскад CSTR для изучения действия ингибирующих и токсических веществ в биопроцессах. англ. Жизнь наук. 2008, 8, 650-657. [Google Scholar]
38.
Круяц, Ф.
,
Хартель, П.
,
Хельбиг, К.
,
Хауфе, Н.
и др., Производство водорода Rhodobacter sphaeroides DSM 158 при интенсивном облучении. Биоресурс. Технол.
2015, 175, 82–90. [PubMed] [Google Scholar]
39.
Лезер, К.
,
Хаас, С.
,
Лю, В.
,
Грал, С.
,
Блей, Т.
, Поглощение железа на Kluyveromyces marxianus DSM 5422, культивированные на среде на основе молочной сыворотки.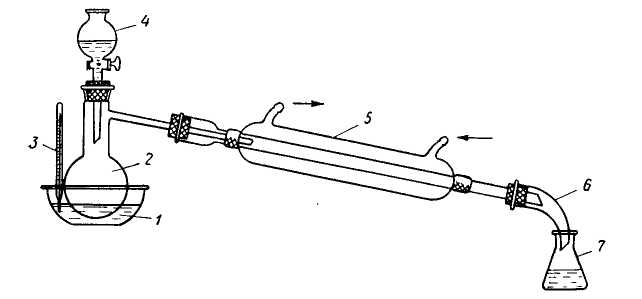 англ. Жизнь наук.
англ. Жизнь наук.
2018, 18, 459–474. [Бесплатная статья PMC] [PubMed] [Google Scholar]
40.
Кастрилло, Дж. И.
,
Калитерна, Дж.
,
Weusthuis, R.A.
,
ван Дейкен, Дж. П.
,
Пронк, Дж. Т.
, Культивирование дрожжей с высокой плотностью клеток на дисахаридах в периодических культурах с ограниченным содержанием кислорода. Биотехнолог. биоинж.
1996, 49, 621–628. [PubMed] [Google Scholar]
41.
Беллавер, Л.Х.
,
де Карвалью, Н.М.Б.
,
Абрахао-Нето, Дж.
,
Гомперт, А.К.
, Образование этанола и активность ферментов вокруг глюкозо-6-фосфата в Kluyveromyces marxianus CBS 6556, подвергшиеся воздействию избытка глюкозы или лактозы. FEMS Yeast Res. 2004, 4, 691–698. [PubMed] [Google Scholar]
42.
Уордроп, Ф. Р.
,
Лити, Г.
,
Кардинал, Г.
,
Уокер, Г. М.
, Физиологические реакции Крэбтри-положительных и Крэбтри-отрицательных дрожжей на повышение уровня глюкозы в хемостате. Анна. микробиол.
2004, 54, 103–114. [Google Scholar]
43.
Фонсека, Г.Г.
,
де Карвалью, Н.М.Б.
,
Гомберт, А.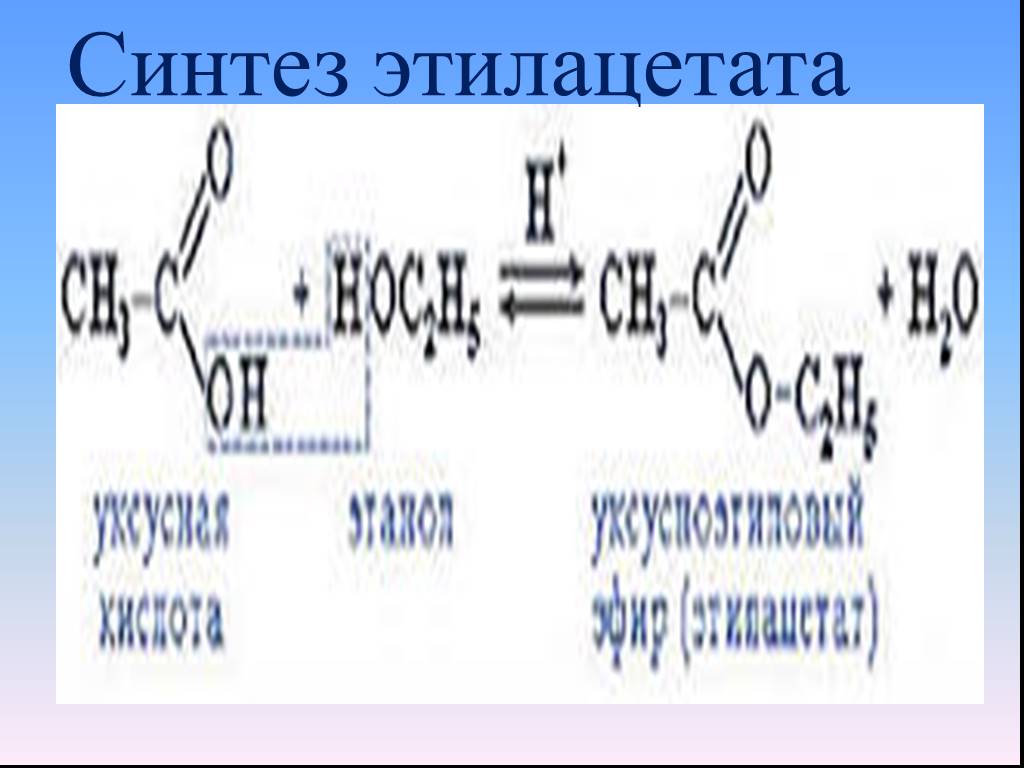 К.
К.
, Рост дрожжей Kluyveromyces marxianus CBS 6556 о различных комбинациях сахаров как единственном источнике углерода и энергии. заявл. микробиол. Биотехнолог.
2013, 97, 5055–5067. [PubMed] [Google Scholar]
44.
Weusthuis, R.A.
,
Виссер, В.
,
Пронк, Дж. Т.
,
Шефферс, В. А.
,
ван Дейкен, Дж. П.
, Влияние ограничения кислорода на метаболизм сахара у дрожжей: исследование эффекта Клюйвера в непрерывном культивировании. микробиол.
1994, 140, 703–715. [PubMed] [Google Scholar]
45.
Фредлунд, Э.
,
Бланк, Л. М.
,
Шнюрер, Дж.
,
Зауэр, У.
,
Пассот, В.
, Кислород- и глюкозозависимая регуляция центрального углеродного обмена в Пихия аномальная
. заявл. Окружающая среда. микробиол.
2004, 70, 5905–5911. [Бесплатная статья PMC] [PubMed] [Google Scholar]
46.
Уокер, Г. М.
,
Pichia anomala : клеточная физиология и биотехнология по сравнению с другими дрожжами. Антони ван Левенгук
2011, 99, 25–34. [PubMed] [Google Scholar]
47.
Армстронг, Д. У.
У.
,
Ямадзаки, Х.
, Влияние железа и ЭДТА на накопление этилацетата в Candida utilis
. Биотехнолог. лат.
1984, 6, 819–824. [Академия Google]
48.
ван Дейкен, Дж. Р.
,
Weusthuis, R.A.
,
Пронк, Дж. Т.
, Кинетика роста и потребления сахара дрожжами. Антони ван Левенгук
1993, 63, 343–352. [PubMed] [Google Scholar]
49.
Армстронг, Д. У.
,
Мартин, С.М.
,
Ямадзаки, Х.
, Производство ацетальдегида из этанола с помощью Candida utilis
. Биотехнолог. лат.
1984, 6, 183–188. [Google Академия]
50.
Грей, В. Д.
, Первоначальные исследования метаболизма Hansenula anomala (Hansen) Sydow. Являюсь. Дж. Бот.
1949, 36, 475–480. [Google Scholar]
51.
Бол, Дж.
,
Кнол, В.
,
тен Брик, Б.
, Оптимизация производства этилацетата из этанола по Hansenula anomala
. Монографии Дечема
1987, 105, 235–236. [Google Scholar]
52.
Корзо, Г.
,
Рева, С.
,
Кристен, П.
, Влияние кислорода на производство этилацетата из непрерывного потока этанола с помощью Candida utilis в погруженных культурах. Развивать. Пищевая наука.
Развивать. Пищевая наука.
1995, 37Б, 1141–1154. [Академия Google]
53.
Лезер, К.
,
Шредер, А.
,
Депонте, С.
,
Блей, Т.
, Уравновешивание образования этанола в биореакторах непрерывного действия с отгонкой этанола. англ. Жизнь наук.
2005, 5, 325–332. [Google Scholar]
54.
Табачник, Дж.
,
Джослин, Массачусетс
, Образование сложных эфиров дрожжами. I. Производство этилацетата поверхностными культурами Hansenula anomala .
. Дж. Бактериол.
1953, 65, 1–9. [Бесплатная статья PMC] [PubMed] [Google Scholar]
55.
Кристен, П.
,
Доменек, Ф.
,
Пака, Дж.
,
Рева, С.
, Оценка Штаммы Candida utilis для производства биомассы, уксусной кислоты и этилового спирта из этанола. Биоресурс. Технол.
1999, 68, 193–195. [Google Scholar]
Этилацетат — wikidoc
Template:Chembox new
Главный редактор: C. Майкл Гибсон, MS, MD [1]
Этилацетат (систематически этилэтаноат, обычно сокращенно EA ) представляет собой органическое соединение с формулой CH 3 CH 2 OC(O)CH 3 . Эта бесцветная жидкость имеет характерный, не неприятный запах (похожий на грушевые капли), как некоторые клеи или жидкости для снятия лака, в которых она используется. Поскольку сложный эфир, полученный из этанола и уксусной кислоты, обычно обозначаемый аббревиатурой EtOAc, производится в больших масштабах для использования в качестве растворителя.
Эта бесцветная жидкость имеет характерный, не неприятный запах (похожий на грушевые капли), как некоторые клеи или жидкости для снятия лака, в которых она используется. Поскольку сложный эфир, полученный из этанола и уксусной кислоты, обычно обозначаемый аббревиатурой EtOAc, производится в больших масштабах для использования в качестве растворителя.
Содержание
- 1 Свойства
- 2 Подготовка
- 3 Промышленное производство
- 4 варианта использования
- 4.1 Растворитель
- 4.2 Присутствие в винах
- 4.3 Другое использование
- 5 реакций
- 6 Каталожные номера
- 7 Внешние ссылки
Свойства
Этилацетат представляет собой умеренно полярный растворитель, преимуществом которого является летучесть, относительно нетоксичность и негигроскопичность. Он является слабым акцептором водородной связи и не является донором из-за отсутствия кислотного протона (прямо связанного с электроотрицательным атомом, таким как фтор, кислород или азот). Этилацетат может растворять до 3% воды и имеет растворимость 8% в воде при комнатной температуре. При повышенной температуре его растворимость в воде выше. Он нестабилен в присутствии сильных водных оснований и кислот.
Этилацетат может растворять до 3% воды и имеет растворимость 8% в воде при комнатной температуре. При повышенной температуре его растворимость в воде выше. Он нестабилен в присутствии сильных водных оснований и кислот.
Подготовка
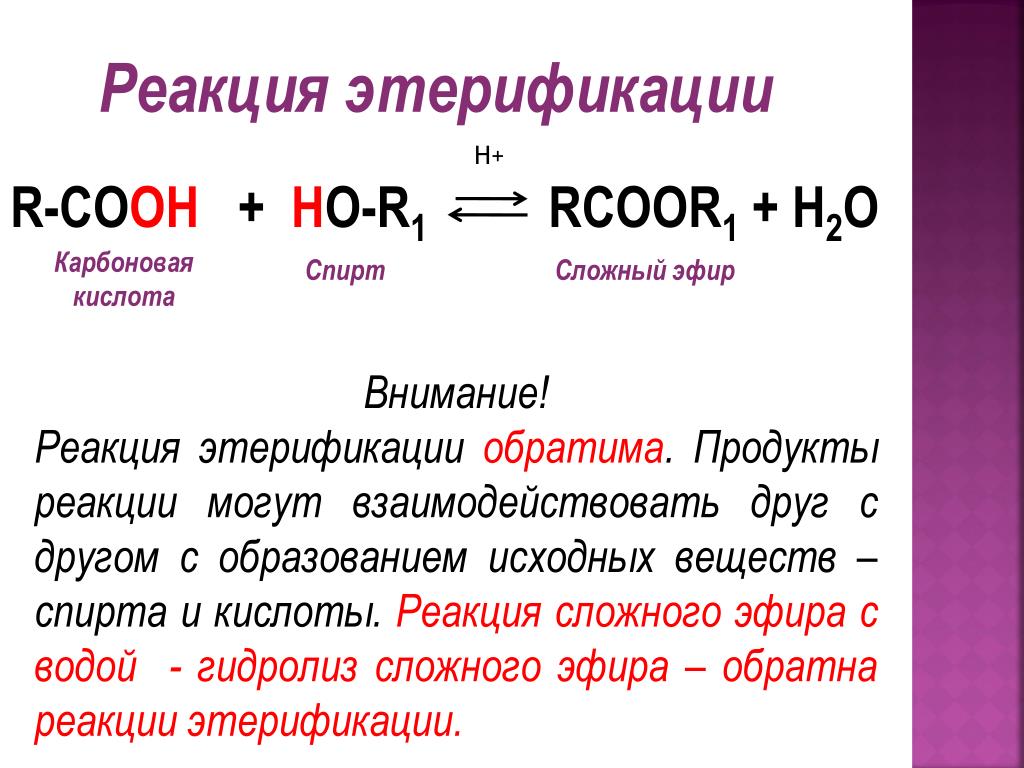
Этилацетат синтезируют с помощью реакции этерификации Фишера из уксусной кислоты и этанола, обычно в присутствии кислотного катализатора, такого как серная кислота.
- CH 3 Ch 2 OH + CH 3 COOH → CH 3 COOCH 2 CH 3 + H 2 CH 3 + H 2 CH 3 + H 2 CH 3 + H 2 CH 3 + H 2 CH 3 + H 2 CH . получают каталитическим дегидрированием этанола. По соображениям стоимости этот метод в основном применяется для преобразования избыточного сырья в виде этанола, в отличие от заранее определенного производства в промышленных масштабах.
 Кроме того, он обычно считается менее практичным и менее рентабельным.
Кроме того, он обычно считается менее практичным и менее рентабельным.Катализаторы для дегидрирования включают медь, работающую при повышенной температуре, но ниже 250 °C. Площадь поверхности меди может быть увеличена за счет ее осаждения на цинк, что способствует росту снежинок, фрактальных структур. Эту площадь поверхности можно снова увеличить путем осаждения на цеолит, обычно ZSM-5. Также было обнаружено, что следы редкоземельных металлов или щелочей, таких как натрий и калий, полезны для процесса. Побочные продукты гидрирования включают диэтиловый эфир (считается, что он возникает в первую очередь из-за участков алюминия в катализаторе), ацетальдегид, альдольные продукты ацетальдегида, высшие сложные эфиры и кетоны. Ацетальдегид и МЭК усложняют конверсию и очистку, поскольку этанол образует азеотроп с водой, а также этилацетат с этанолом и водой и МЭК с этанолом и ацетатом. Чтобы получить продукт высокой чистоты, эти азеотропы должны быть «разбиты», и этого можно добиться, используя перегонку при переменном давлении.

Состав дистиллята, удаляемого из продуктов конверсии, смещен в сторону ацетата при атмосферном давлении и этанола при повышенном давлении. Сначала сырой продукт подают в колонну высокого давления, где удаляется основная часть загрязняющего этанола. Затем путем подачи обедненного этанолом дистиллята в колонну низкого давления ацетат можно удалить из оставшегося азеотропа этанола.
МЭК образуется в процессе конверсии 2-бутанола. Последний не образует азеотропа с ацетатом, поэтому МЭК можно удалить гидрированием загрязненного продукта над никелем и дальнейшей перегонкой для удаления 2-бутанола. Это обеспечивает одновременную выгоду от удаления загрязнителя ацетилальдегида путем его возвращения в этанольную форму и легко достигается, поскольку водород является побочным продуктом начального процесса дегидрирования.
Возможно также разложение азеотропов с использованием мембранной перегонки, молекулярных сит, азеотропа или абсорбирующей среды.
Дистиллированный этанол и регидрированные загрязняющие вещества затем могут быть переработаны в сырье.

Применение
Растворитель
Этилацетат в основном используется в качестве растворителя. Например, он обычно используется для растворения пигментов лаков для ногтей и отвечает за растворяющее действие некоторых жидкостей для снятия лака (также используются ацетон и ацетонитрил). В промышленности он используется для удаления кофеина из кофейных зерен и чайных листьев. [ необходима ссылка ] Он также используется в красках в качестве активатора или отвердителя. [ , необходима ссылка ]
В лаборатории смесь этилацетата и гексана является наиболее распространенной системой растворителей, используемой в качестве растворителя для хроматографии. Он также используется в качестве растворителя для экстракции. Его редко используют в качестве реакционной смеси, поскольку он склонен к гидролизу.
Как и большинство простых эфиров, этилацетат имеет фруктовый запах. Этилацетат присутствует в кондитерских изделиях, парфюмерии и фруктах.
 В парфюмерии он быстро испаряется, оставляя на коже лишь аромат духов.
В парфюмерии он быстро испаряется, оставляя на коже лишь аромат духов.Присутствие в винах
Этилацетат присутствует в винах. Его можно считать загрязнителем при слишком высоких концентрациях, что обычно происходит, когда вино подвергается воздействию воздуха в течение длительного периода времени. Когда он присутствует в вине в слишком высокой концентрации, он считается неприятным привкусом.
Другое применение
В области энтомологии этилацетат является эффективным ядом для сбора и изучения насекомых. В сосуде для уничтожения, наполненном этилацетатом, пары быстро убивают собранное (обычно взрослое) насекомое, не разрушая его. Поскольку он не гигроскопичен, этилацетат также сохраняет насекомое достаточно мягким, чтобы его можно было правильно закрепить, подходящим для коллекции.
Реакции
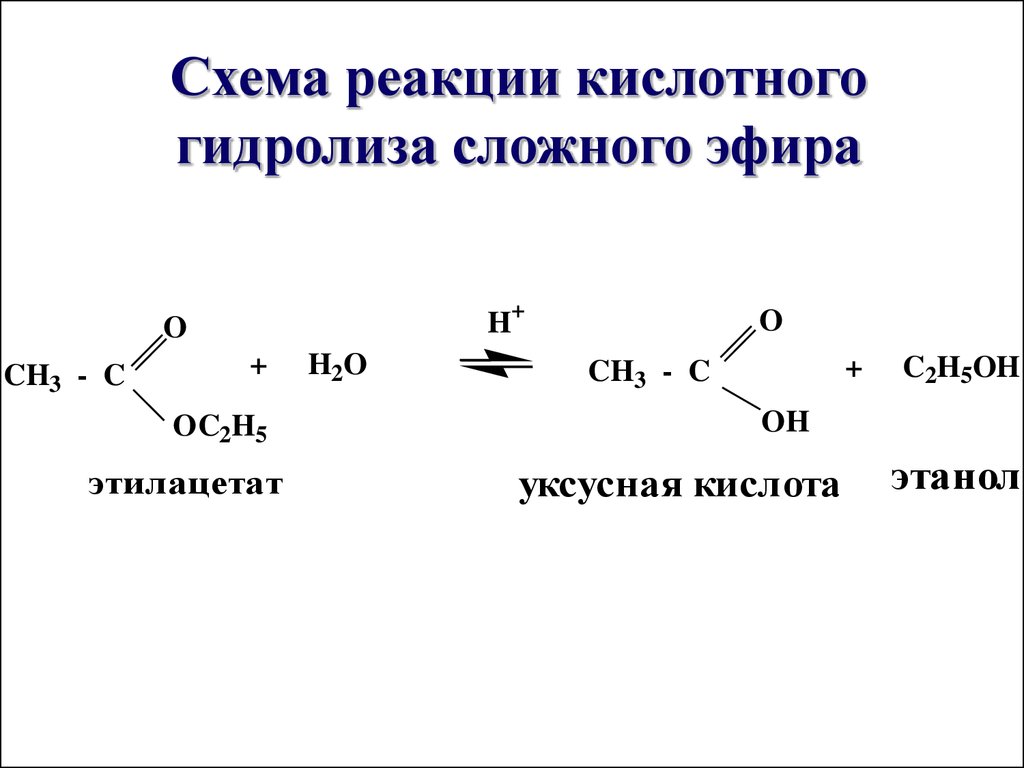
Этилацетат можно гидролизовать в кислой или щелочной среде для восстановления уксусной кислоты и этанола. Использование кислотного катализатора, такого как серная кислота, дает низкие выходы из-за того, что он является равновесным — реакция, обратная этерификации Фишера.


 Кроме того, он обычно считается менее практичным и менее рентабельным.
Кроме того, он обычно считается менее практичным и менее рентабельным.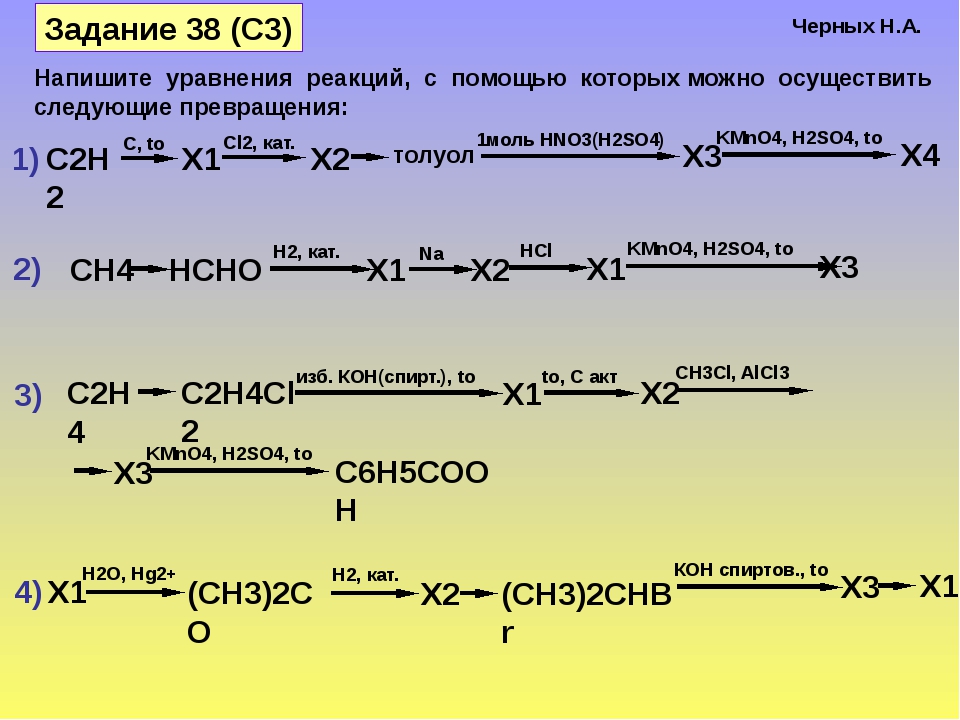

 В парфюмерии он быстро испаряется, оставляя на коже лишь аромат духов.
В парфюмерии он быстро испаряется, оставляя на коже лишь аромат духов.