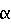Химические свойства сложных эфиров. Реакции сложных эфиров
| Обратная связь ПОЗНАВАТЕЛЬНОЕ Сила воли ведет к действию, а позитивные действия формируют позитивное отношение Как определить диапазон голоса - ваш вокал Как цель узнает о ваших желаниях прежде, чем вы начнете действовать. Как компании прогнозируют привычки и манипулируют ими Целительная привычка Как самому избавиться от обидчивости Противоречивые взгляды на качества, присущие мужчинам Тренинг уверенности в себе Вкуснейший "Салат из свеклы с чесноком" Натюрморт и его изобразительные возможности Применение, как принимать мумие? Мумие для волос, лица, при переломах, при кровотечении и т.д. Как научиться брать на себя ответственность Зачем нужны границы в отношениях с детьми? Световозвращающие элементы на детской одежде Как победить свой возраст? Восемь уникальных способов, которые помогут достичь долголетия Как слышать голос Бога Классификация ожирения по ИМТ (ВОЗ) Глава 3. Завет мужчины с женщиной Оси и плоскости тела человека - Тело человека состоит из определенных топографических частей и участков, в которых расположены органы, мышцы, сосуды, нервы и т.д. Отёска стен и прирубка косяков - Когда на доме не достаёт окон и дверей, красивое высокое крыльцо ещё только в воображении, приходится подниматься с улицы в дом по трапу. Дифференциальные уравнения второго порядка (модель рынка с прогнозируемыми ценами) - В простых моделях рынка спрос и предложение обычно полагают зависящими только от текущей цены на товар. | Сложные эфиры термически нестабильны: при нагревании до 200 – 250оС они разлагаются на гораздо более стабильные карбоновые кислоты и алкены, например: Если у первого атома углерода спиртовой части сложного эфира имеется разветвление, то получаются два разных алкена, причём каждый из них может получаться в виде двух цис- и транс - изомеров: Сложные эфиры могут гидролизоваться в кислой, нейтральной и щелочной средах. В реакция обратима и скорость её зависит от концентрации добавленной сильной кислоты. Кинетические кривые, то есть кривые в координатах время – концентрация представляют собой нисходящую экспоненту для сложного эфира и одинаковые восходящие экспоненты для спирта и карбоновой кислоты. Ниже представлен график для реакции гидролиза в общем виде:
Если кислоту не добавлять, то наблюдается автокаталитический процесс: гидролиз сначала идёт очень медленно, но при этом образуется карбоновая кислота – катализатор и процесс ускоряется, а через некоторое время скорость его опять падает и концентрация сложного эфира доходит до равновесной. Эта равновесная концентрация при прочих равных условиях ничем не отличается от той равновесной концентрации, которая получается при катализе сильными кислотами. Однако время для достижения полупревращения (t1/2) значительно больше: Под действием щелочей сложные эфиры так же «гидролизуются», но здесь щёлочь не катализатор, а реагент: Сложные эфиры вступают в реакцию переэтерификации как со спиртами, так и с кислотами: Для того чтобы сдвинуть равновесие в сторону образования целевого сложного эфира спирт - исходный реагент берут в большом избытке. При переэтерификации кислотой берут в большом избытке её.
Сложные эфиры вступают в реакцию с аммиаком и аминами. Равновесие в этих реакциях очень сильно сдвинуто в сторону образования амидов и алкиламидов кислот: избыток аммиака или амина не нужен (!!!)
Сложные эфиры могут быть окислены сильными окислителями в кислой среде. По-видимому, сначала проходит гидролиз и фактически окисляется только образовавшийся при этом спирт. Например: Сложные эфиры могут быть восстановлены до спиртов металлическим натрием в среде какого-либо спирта. Реакция была предложена в 1903 году и подробно изучена в 1906 году французскими химиками Буво и Бланом и носит их имя. Например: В две стадии сложные эфиры могут быть восстановлены до спиртов с помощью комплексных гидридов металлов. На первой стадии в случае использования тетрагидридобората натрия получаются эфир борной кислоты и алкоголят натрия, на второй они гидролизуются до спиртов:
В случае применения тетрагидридоалюмината лития на первой стадии получаются алкоголяты алюминия и лития, а на второй они так же гидролизуются до спиртов:
Содержание
|
megapredmet.ru
Реакции сложных эфиров терпеновых — Мегаобучалка
Спиртов
Сложные эфиры терпеновых спиртов входят в состав многих эфирных масел и нередко оказываются главными компонентами масел.
Наиболее распространены эфиры уксусной кислоты. В эфирных маслах шалфея, лаванды, бергамота основным и наиболее ценным компонентом является (-)-линалилацетат. В пальмарозовом масле, в цитронелловом, кориандровом маслах присутствует геранилацетат. Нерилацетат найден в неролиевом масле; ацетат α-терпинеола в значительных количествах (30 – 35 %) содержится в кардамоновом масле, в состав которого входят также ацетаты линалоола и нерола. Борнилацетат – главный компонент масла сибирской пихты. Аромат мятного масла вместе с ментолом и ментоном формирует также ментилацетат.
Реже, и в основном в качестве минорных компонентов, встречаются сложные эфиры других карбоновых кислот – муравьиной, пропионовой, масляной, валериановой. Тем не менее, в гераниевом масле доля формиатов терпеновых спиртов достигает 15 %, бутиратов – 2 %.
Основными реакциями сложных эфиров являются реакции гидролиза и отщепления кислоты (элиминирования).
Гидролиз сложных эфиров может осуществляться в кислой и щелочной средах. Гидролиз в кислой среде является реакцией, обратной этерификации. Он протекает по тому же механизму и подчиняется тем же кинетическим и термодинамическим закономерностям, что и реакция этерификации.
Гидролиз в щелочной среде (омыление) является необратимым процессом:
Реакция начинается с присоединения нуклеофила – иона ОН- по карбонильной группе сложного эфира и протекает по схеме:
Процесс завершается передачей протона от кислоты к алкоголят-аниону, поскольку кислотные свойства спиртов выражены значительно слабее, чем у карбоновых кислот, и протон в молекуле спирта оказывается связанным более прочно, чем в молекуле кислоты:
Приведенный механизм был подтвержден рядом экспериментальных исследований, в том числе с использованием радиоактивных изотопов.
На скорость омыления большое влияние оказывает растворитель. Реакция протекает легко и количественно в среде этанола. Омыление спиртовым раствором щелочи используют в аналитических целях для определения сложных эфиров. Наиболее быстро омыляются эфиры первичных спиртов. Обычно в этом случае для завершения реакции требуется кипячение пробы в спиртовом растворе щелочи в течение не более одного часа.
Значительно труднее реагируют эфиры третичных спиртов, а также кислот с разветвлением цепи при α-углеродном атоме. Это связано с пространственными затруднениями при атаке карбонильной группы сложного эфира ионом гидроксила. В ряде случаев для определения трудноомыляемых эфиров используют растворы щелочи в более высококипящих спиртах – изопропиловом, бензиловом, диэтиленгликоле. Повышение температуры омыления способствует более быстрому завершению реакции.
Реакция элиминирования (отщепление кислоты от сложных эфиров) приводит к образованию алкена. Данная реакция похожа на дегидратацию спиртов и характеризуется аналогичными закономерностями. Наиболее легко подвергаются элиминированию сложные эфиры третичных спиртов и спиртов аллильной структуры. Сложные эфиры первичных спиртов к элиминированию устойчивы.
Скорость реакции возрастает с повышением температуры. Катализаторами процесса являются кислоты, в том числе кислота, образующаяся в результате реакции. Это приводит к тому, что скорость реакции возрастает с увеличением глубины превращения, т. е. реакция элиминирования относится к автокаталитическим химическим процессам.
В производстве душистых веществ реакция элиминирования является нежелательным превращением. Ее негативные последствия проявляются, например, при получении эфирных масел лаванды и шалфея мускатного, в которых наиболее ценным компонентом выступает линалилацетат. Отщепление уксусной кислоты от линалилацетата в процессе паровой отгонки масла может приводить к существенным потерям этого ценного душистого вещества и повышению в эфирном масле доли углеводородов, не обладающих парфюмерными достоинствами, что снижает качество масла.
megaobuchalka.ru
II. Реакции образования простых и сложных эфиров
1. Спирты взаимодействуют с минеральными и органическими кислотами с образованием соответствующих сложных эфиров и воды:

Эти реакции обратимы, и в присутствии водоотнимающих веществ равновесие сдвинуто вправо, в сторону образования сложных эфиров (механизм нуклеофильный).
81. Напишите уравнения реакций этерификации уксусной кислоты следующими спиртами: а) изопропилкарбинол; б) 2-метилбутанол-1; в) трет-бутилкарбинол; г) пентанол-2; д) втор-бутилкарбинол; е) З-метилбутанол-1; ж) изобутилкарбинол; з) пентанол-3.
2. При действии на спирты водоотнимающих веществ происходит межмолекулярное или внутримолекулярное отщепление воды.
Водоотнимающими веществами являются:
h3SО4 (конц), Н3Р04 (конц), CuS04, KHSO4, ZnCl2 и др.
При межмолекулярной дегидратации получаются простые эфиры. Например, при действии на этиловый спирт концентрированной серной кислоты при температуре ниже 170°С образуется диэтиловый или серный эфир:

Внутримолекулярное отщепление воды от спиртов происходит при более высокой температуре (при действии h3S04 (конц.) выше 170°С) и дает алкены (см. способы получения алкенов).
82. Напишите уравнения межмолекулярного отщепления воды от следующих спиртов: а) изопропиловый; б) изобутиловый; в) пропиловый; г) втор-бутиловый; д) пентанол-2; е) 3-метил-бутанол-1; ж) 2-метилбутанол-1; з) бутанол-1.
3. Образование простых эфиров происходит и при нагревании алкоголятов с моногалогеналканами:
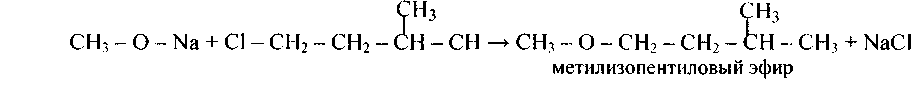
83. Напишите уравнения следующих реакций, назовите продукты: а) этилат натрия + бромистый этил; б) 2-йодбутан + метилат натрия; в) изопропилат калия + хлорметан; г) 1-хлорпропан + этилат натрия; д) 1 -хлор-2-метилпропан + этилат калия; е) изопропилат калия + бромистый изобутил; з) этилат натрия + бромистый 1-метилбутил.
Похожие статьи:
poznayka.org
Сложные эфиры типы реакций - Справочник химика 21
Карбанионы различных структурных типов, стабилизованные присутствием серы, реагируют со сложными эфирами. Эти реакции в ряде случаев можно использовать в синтетических целях примеры представлены на схемах (262) —(265) (соответственно по работам [224—227]). [c.353]Ката- лиза- тор Среда Сложный эфир Тип реакция н п а 4) h Константа скорости, л/(моль-мни) т RI t. Ш S о. S j иЧ Л я к [c.75]
ПОЛУЧЕНИЕ СЛОЖНЫХ ЭФИРОВ ПО РЕАКЦИИ ТИПА ВИЛЬЯМСОНА [c.54]Анионообменные смолы (типа амберлита) каталитически активируют реакции конденсации альдегидов со сложными эфирами (типа ацетоуксусного, цианоуксусного, малонового). Эти реакции про-30 [c.483]
Кроме рассмотренного метода получения ненасыщенных сложных эфиров, к реакции Клайзена относятся следующие типы реакций конденсации [c.596]
Гомогенных каталитических реакций в растворах, ускоряем мых ионами гидроксила и водорода, довольно много. К реакциям этого типа относятся этерификации кислот и спиртов, инверсия сахаров, галоидирование соединений, содержащих карбонильную группу, омыление сложных эфиров и др. [c.286]
Бендер (1958) изучал гидролиз меченых сложных эфиров типа R OOR в обычной воде и немеченых сложных эфиров в Нг 0 и нашел, что в каждом случае кислород при гидролизе обменивается в приблизительно равной степени это доказывает, что реакция протекает через промежуточное образование соединений, имеющих две равнозначные гидроксильные группы. [c.435]
Бекмановские перегруппировки, катализируемые пятихлористым фосфором, протекают, вероятно, через образование сложных эфиров типа КаС = К—ОРС . Оказалось возможным доказать, что в реакции не играют никакой роли К-хлор-имины, соответствующие формуле K2 =N 1, так как подобные соединения, полученные другим путем, не перегруппировываются в амиды (И. Штиглиц, 1910 г.). Хлор, связанный с азотом подобным образом, не диссоциирует. [c.702]
Карбоновые кислоты декарбоксилируются [211] под действием тетраацетата свинца, давая разнообразные продукты, включая сложные эфиры типа ROA (образующиеся при замещении СООН на ацетокси-группу), алканы RH (см. т. 2, реакцию 12-39) И, если субстрат содержит 3-атом водорода, алкены, получающиеся в результате элиминирования Н и СООН, а также ряд других продуктов, являющихся результатом перегруппировок, внутримолекулярных циклизаций [212] и взаимодействия с молекулами растворителя. Если R — третичная группа, основным продуктом обычно является алкен, который часто образуется с хорошим выходом. Высокие выходы алкенов достигаются также в случае первичных или вторичных групп R, но для этой цели вместо тетраацетата свинца используют систему u(0A )2 — РЬ(0Ас)4 [213]. В отсутствие ацетата меди неразветвленные кислоты дают в основном алканы (хотя выходы, как правило, низки), а кислоты, имеющие разветвление в а-положении, могут давать сложные эфиры или алкены. Сложные эфиры с хорошими выходами получены из некоторых разветвленных кислот, из р,у-ненасыщенных кислот, а также из кислот, где R = бензильная группа. у-Кетокислоты с хорошими выходами приводят к а,р-ненасыщенным кетонам [214]. В окислительном декарбоксилировании использовались и другие окислители, включая соединения Со(П1), Ag(II), Mn(III) и Се (IV) [215]. [c.289]
Кроме реакций Перкина и Кневенагеля—Дёбнера широкое применение для синтеза -фенилакриловых кислот имеет реакция Клайзена , заключающаяся в конденсации ароматических альдегидов со сложными эфирами типа R Hj OOR в присутствии натрия или алкоголята натрия. Продуктом реакции является эфир непредельной кислоты, из которого путем гидролиза получают свободную кислоту [c.596]
Наличие больших количеств спирта в исходном сложном эфире вредно, так как реакция Клайзена обратима -кетоэфир под действием спирта и алкоголята натрия распадается на две молекулы сложного эфира. Обратимость реакции Клайзена обусловливает понижение выходов, особенно при конденсации эфиров высших жирных кислот типа R H GOOH [c.597]
Опубликован обзор [ПО], посвященнйй этому методу синтеза, являющемуся основным методом получения ацилоинов с одинаковыми алкильными труппами. Применяют такие растворители, как эфир, бензол, ксилол или избыток сложного эфира, и реакцию проводят при температуре кипения растворителя. Превосходные результаты при синтезе ацилоинов стероидного типа дает применение натрия в жидком аммиаке и эфира [111]. Время, требующееся для завершения реакции, весьма различно для разных случаев очень существенным является удаление аммиака до подкисления соли ацилоина [112]. Ацилоины с кольцами больших размеров лучше всего получать реакцией конденсации при помощи натрия. Очевидно, на поверхности натрия сложноэфирные группы близко подходят друг к другу, что способствует образованию кольца, а не межмолекулярной конденсации [113]. [c.238]
Другой нередко наблюдаемой побочной реакцией при гидрогенизации сложных эфиров типа КСОгСгНб, когда процесс вследствие низкого давления водорода или других факторов протекает медленно, является образование заметных количеств сложных [c.8]
Альдегиды конденсируются с сложными эфирами типа R- Hj- 00 aH5( p. Б, П1, 1,а)с образованием эфиров а,/3-н е н а с ы щ е н н ы X кислот (реакция Клайзена) [c.422]
Пептидный синтез. Зервас и сотр. [11 получили фенациловые 5,(1)Пры аминокислот при обработке карбобензоксиаминокислот Б. в присхтствии триэтиламина в этилацетате. Фенацильная сложноэфирная группа устойчива к кислотам, но расщепляется при каталитическом гидрировании или при обработке тиофенолятом натрия в неводной среде в мягких условиях. Австралийские химики [2], изучавшие д-бромфенациловые эфиры, пришли к выводу, что сложные эфиры типа фенациловых, как правило, непригодны для защиты карбоксильной группы в случае медленных реакций конденсации. [c.45]
Анионы сложных эфиров типа этилацетоацетата и диэтилмалоната могут быть проалкилированы алкилгалогенидами. Эти реакции имеют важное значение для синтеза карбоновых кислот и кетонов и в основных чертах сходны с рассмотренным выше алкилированием кетонов по Халлеру — Бауэру (стр. 429). Сложный эфир превращается при действии сильного основания в енолят-анион [уравнение (16-19)], и последний далее алкилиру-ется по 8к2-реакции алкилгалогенидом [уравнение (16-20)]. Обычно преобладает С-алкилирование. [c.488]
Многие важные в синтетическом отношении реакции, при которых образуются связи С—С, происходят с участием сложных эфиров и осуществляются при действии реагентов основного характера. Это оказывается возможным вследствие того, что а-водородные атомы сложного эфира типа КСНаСО СаНэ обладают слабыми кислотными свойствами, и сильное основание, например этилат натрия, может создавать в равновесной смеси значительную концентрацию [c.577]
С названными конденсирующими средствами могут быть введены в реакцию и сложные эфиры типа Ra H— OOR, так как ход [c.357]
Все эти реакции протекают с образованием промежуточных продуктов типа сложных эфирив. Так, реакция с хлористым тионилом идет в две стадии [c.72]
Реакции с металлоорганическими соединениями. Эти реакции могут быть двух типов реакции сложных эфиров и реакции солей кислородсодержащих кислот. При получении металлалкилов или металларилов действием алкилирующих агентов, в качестве которых используются реактивы Гриньяра или алкильные производные щелочных металлов, иногда удобнее пользоваться не галогенидами металлов, а алкоксильными производными металлов с низшими алифатическими радикалами, так как последние вследствие растворимости в углеводородах или эфире алкилируются почти так же хорошо, как и галогениды металлов. Эфиры борной кислоты, например триэтокси-бор (С2Н50)зВ, несколько легче получить и очистить, чем галогениды бора они также удобнее в обращении. Это же можно сказать относительно эфиров некоторых других элементов, таких, как кремний или германий. Могут также встретиться случаи, когда при получении смешанных алкилпроизводных метал- [c.74]
Сложные эфиры типа геранил- и линалилацетатов при реакции дегидратации разлагаются почти количественно, образуя углеводороды и уксусную кислоту эфиры спиртов, цитронеллола, фенилэтилового спирта, не имеющие двойной связи в а-, р-положении к карбонильной группе, не изменяются. По количеству выделившейся уксусной кислоты судят о присутствии сложных эфиров, линалоола, гераниола. [c.200]
Титрованием выделяющейся при этой реакции кислоты можно определить сложный эфир типа КСН = СНСН20С0Р в присутствии других сложных эфиров. Таким путем было проведено определение геранилацетата в кориандровом масле. [c.279]
Реакции окисления циклопентенонов имеют как теоретический, так и практический интерес и потому исследовались неоднократно. Они широко применяются для установления строения циклопентенонов, ими пользуются также для введения в молекулу циклопентенона гидроксильных групп (например, при синтезах редуктонов или сложных эфиров типа пиретринов) или с целью перехода от циклопентенонов к циклопентендионам и циклопентандионам. Последние имеют большое значение как исходные вещества во многих синтезах в разных областях органической химии и, в частности, при синтезах [c.162]
Приведенная выше равновесная реакция (4) не является постоянной частью мехапизма конденсации. Однако эта реакция происходит в том случае (как в приведенном примере), когда продукт конденсации содержит водород, способный к ионизации тогда реакция (4) входит в общее термодинамическое равновесие, определяющее степень конденсации. Так, ацетоуксусный эфир, образующийся в результате описанных последовательных процессов, в значительной степени превращается в анион по уравнению (4), что способствует смещению вправо равновесных реакций (1) — (3). Равновесная реакция типа (4) не способствует протеканию прямой реакции в случае конденсации этилового эфира изомасляной кислоты с другой молекулой того же эфира с образованием этилового эфира изобутироизомасляной кислоты. Образование молекулы спирта в правой части уравнения реакции (1) замедляет протекание равновесных реакций (1) — (3) в прямом направлении. Это, безусловно, является одной из причин лучших выходов ацетоуксусного эфира при применении металлического натрия, а не этилата натрия, или, иными словами, в присутствии небольших количеств этилового спирта. Существуют некоторые независимые доказательства реальности равновесной реакции (1). Кеньон и Янг [99] показали, что оптически активные сложные эфиры типа И К"СНС00С2Нд рацемизируются в присутствии этилата натрия. Браун и Эберли [100] установили, что сложные эфиры, содержащие водород в а-положении, претерпевают водородный обмен с тяжелым спиртом СаНдОВ, содержащим этилат натрия, и что скорость такого обмена характеризует реакционную способность а-водородных атомов этих эфиров в конденсациях Кляйзена. [c.972]
Тот или иной тип распада молекулы сложного эфира при реакциях с аминами или оксисоединениями зависит в основном от силы кислоты, образовавшей сложный эфир эфиры слабых (органических) кислот действуют ацилируюш,е, а эфиры сильных минеральных кислот (серной и галогеноводородных)—алкилирующ,е. [c.189]
Единственное исследование, посвященное катализу трифторуксусной кислотой, было проведено Шварцем и сотр. [79]. Были поставлены опыты двух типов. Когда стирол приливали к трифторуксусной кислоте, то почти мгновенно получался полимер с довольно высоким молекулярным весом (степень полимеризации 163 при 0°, Есп = —3 ккал1моль) степень полимеризации не зависела от величины капель стирола, вводимого в трифторуксус-ную кислоту. Когда трифторуксусную кислоту приливали к стиролу, то образовывалась смесь полимера и олигомерных сложных эфиров. Было показано, что полимер образуется на поверхности капель трифторуксусной кислоты. Для предотвращения этого основные опыты этой серии были поставлены так, что к стиролу добавляли раствор трифторуксусной кислоты в этилбензоле при этом были получены только олигомерные сложные эфиры. В реакциях обоих типов небольшие количества воды не оказывали никакого действия. Это несоответствие с результатами Матизона и Брауна остается необъясненным. [c.232]
Авторы сохранили общий строй книги, но для облегчения пользования материалом отказались от разделения процессов на реакции, проходящие в присутствии и в отсутствие щелочи, воспользовавщись классификацией по типам реакций. Введены отдельные разделы по хиральным и полимерносвязанным катализаторам, которые отсутствовали в первом издании, а также новые разделы относительно нуклеофильного ароматического замещения и реакций металлоорганических соединений в условиях межфазного катализа. Основную часть книги занимает гл. 3, посвященная практическому использованию межфазного катализа, где достаточно подробно освещены вопросы техники проведения межфазных реакций, а затем последовательно обсуждено применение межфазного катализа в реакциях замещения (синтез галогенидов, включая фториды, синтезы нитрилов, сложных эфиров, тиолов и сульфидов, простых эфиров, Ы- и С-алкилирование, в том числе амбидентных ионов), изомеризации и дейтерообмена, присоединения к кратным С—С-связям, включая неактивированные, присоединения к С = 0-связям, р-элиминирования, гидролиза, генерирования и превращения фосфониевых и сульфониевых илидов, в нуклеофильном ароматическом замещении, в различных реакциях (ион-радикальных, радикальных, электрохимических и др.), в металлоорганической химии, при а-элиминировании (генерировании и присоединении дигалокарбенов и тригалометилид-ных анионов), окислении и восстановлении. В каждом разделе приведены конкретные методики проведения реакций в различных условиях межфазного катализа и таблицы примеров синтеза разнообразных классов соединений. В монографии использовано более 2000 литературных источников. [c.6]
Такой тип реакции присоединения по Михаэлю с последующим замыканием циклопропанового кольца наблюдается в реакциях между ненасыщенными нитрилами, кетонами, альдегидами, сложными эфирами, фосфонатами и фосфониевыми солями с а-хлорнитроалканами, галогенмалоновыми эфирами, а-хлор-нитрилами и а-хлорэфирами [1094, 1095, 1096, 1214, 1215, 1427]. Как правило, всегда необходимо использовать концентрированный гидроксид натрия и ониевую соль, однако по крайней мере в некоторых случаях медленная реакция возможна и в отсутствие катализатора. [c.225]
chem21.info
Цветные реакции сложных эфиров - Справочник химика 21
Аспирин—ацетилсалициловая кислота—не дает цветной реакции с хлорным железом, так как фенольный гидроксил в его молекуле ацетилирован. Гидролиз аспирина, являющегося сложным эфиром не салициловой (ср. опыт 191), а уксусной кислоты, протекает очень легко даже без добавления кислот или щелочей [c.258]Будучи не только кислотами, но одновременно и фенолами, фенолокислоты за счет своего фенольного гидроксила могут образовывать со спиртами простые эфиры, с кислотами — эфиры сложные. Подобно фенолам фенолокислоты дают цветную реакцию с хлорным железом. Они способны вступать в реакции нитрования, сульфирования и галоидирования с замещением атомов водорода в бензольном ядре. [c.164]
Аспирин как сложный эфир легко гидролизуется при кипячении в воде с образованием исходных продуктов — салициловой и уксусной кислот. Гидролизат аспирина, представляющий собой смесь салициловой и уксусной кислот, дает цветную реакцию с хлорным железом благодаря тому, что фенольный гидроксил салициловой кислоты освобожден (опыт 91). [c.91]Примечание. Эту цветную реакцию дают также сложные эфиры других карбоновых кислот. [c.83]
Обычно можно обнаруживать лишь те классы растворителей, которые характеризуются определенными функциональными группами. Иногда удается определить некоторые группы веществ в пределах того или другого класса соединений, реже — первые члены гомологических рядов, например сложные эфиры, кетоны, спирты — как классы, метилкетоны — как частную группу, метиловый спирт — как первый член гомологического ряда. Хлороформ и четыреххлористый углерод обнаруживают в смеси при помощи цветных реакций. Многие другие растворители тоже можно идентифицировать при помощи реакций на функциональные группы, но только после их выделения из смеси или увеличения их концентрации. [c.933]
Цветные реакции. Реакция с хлоридом железа (III). Большая часть фенолов и многие другие соединения, содержащие фенольный гидроксил, дают с хлоридом железа (П1) (1% раствор) интенсивную окраску. Реакция свойственна только самим фенолам ни простые, ни сложные эфиры фенолов ее не дают, не удается она и в щелочных растворах фенолов. Рекомендуется применять разбавленные нейтральные или, в крайнем случае, слабокислые водные растворы фенолов. Реакция свойственна не только одноатомным, но и многоатомным фенолам. Часто интенсивность окраски повышается с увеличением числа гидроксильных групп в молекуле фенола. [c.75]
Образование гидроксамовых кислот. При обработке гидроксиламином сложные эфиры расщепляются на гидроксамовые кислоты и соответствующие спирты. Гидроксамовые кислоты обнаруживают цветной реакцией с хлоридом железа (П1) (см. IX.a). [c.192]
Реакция сложных эфиров с гидроксиламином при образования соответственной гидроксамовой кислоты пригодна для классификации как сложных эфиров, так и нитрилов нитрилы отличаются от сложных эфиров тем, что дают окращивание только в растворе пропиленгликоля. В том и другом случае цветная реакция получается не сразу, когда испытуемое вещество поступает в реакционную смесь, а только после прибавления РеС1з. [c.269]
Фенольны.й гидроксил в этих кислотах может быть ацили-рован, алк 1лирован и обычно эти соединения дают цветную реакцию ари действии хлорного железа Кислотный характер фенолкарбоновых кислот проявляется в ряде нормальных реакций карбоксильной группы, например в образовании солей и сложных эфиров. Действие треххлористого или пятихлористого фосфора на фенолкарбоновые кислоты ке ограничивается образованием хлорангидридов галоидные соединения фосфора реагируют с фенольным гидроксилом с образованием сложных эфиров фосфорной или фосфористой кислоты. При более энергичном действии пятихлористого фосфора фенольный гидроксил может быть замещен хлором, хотя эта реакция не протекает гладко [c.284]
Первое сообщение о гидроксамовых кислотах принадлежит Лос-сену (1869 г.) [7], который установил, что они могут перегруппировываться в изоцианаты (общеизвестная перегруппировка Лоссена). Однако широкое использование гидроксамовых кислот для аналитических целей относится не ранее чем к 1934 г., когда Файгль с сотр. [8] сообщил о капельной пробе на сложные эфиры и ангидриды, основанной на указанной выше цветной реакции. С того времени этой реакцией стали широко пользоваться для [c.141]
Джекверт и Спекер [40] использовали цветную реакцию перхлората меди с хлоридом лития для создания быстрого и простого метода определения воды в таких органических растворителях, как кетоны, сложные и простые эфиры. При выполнении анализов [c.364]
Под названием реакция Комаровского известны цветные реакции высших спиртов с ароматическими альдегидами в присутствии концентрированной Н2504. Эту реакцию дают спирты с чис-эода в молекуле больше трех, а также аллиловый, сложные эфиры этих спиртов [272], некоторые [c.191]
Лучшие наполнители для Э.-п. к.— слабощелочные или нейтральные печные сажи в светлых и цветных резинах м. б. использованы практически все минеральные наполнители (за исключением имеющих кислую реакцию). Пластификаторами служат гл. обр. насыщенные соединения — парафины, сложные эфиры. В смесях на основе тройных этилен-пропиленовых каучуков применяют вулканизующиеся пластификаторы — низкомолекулярные полибутадиены с высоким содержанием винильных звеньев и без функциональных концевых групп (см. Жидкие каучуки). [c.511]
Механизм цветной реакции ацетилхинализарина с борной кисло-т о й 1. Согласно литературным данным [10, 22, 23], борная кислота в концентрированной серной кислоте, превраш аясь в метаборную кислоту, образует с а-оксиантрахипопами, в том числе и с хинализарином, сложные эфиры, в которых атом бора связывается с молекулой реагента через кислородный атом а-оксигруппы главной валентностью и координационно — с карбонильным кислородом. Образовавшийся сложный эфир , который правильнее рассматривать как внутрикомплексное соединение, обладает более глубокой окраской. Сопоставление кривых поглощения сернокислых растворов внутрикомплексных соединений бора с хинализарином и ацетилхпнализарином показывает их полную идентичность (рис. 1). Это дает основание считать строение внутрикомплексных соединений в обоих случаях одинаковым. [c.225]
Смешивают 0,5 г измельченной пробы с трехкратным количеством прокаленного песка, смесь помещают в сухой стакан, который накрывают стекловолокном или стеклянной ватой. Стакан осторожно нагревают (при деполимеризации полимера выделяется мономер, пары которого конденсируются на стекловолокне). После деполимеризации пробы стекловолокно помещают в чистый стакан, приливают 1 мл свежеприготовленного раствора гидроксиламина, смесь перемешивают и выливают в 100 мл дистиллированной воды, затем осторожно подкисляют 5%-ной соляной кислотой и прибавляют несколько капель 1% раствора РеС1з. В присутствии полиметилметакрилата появляется красно-фиолетовая окраска, а полиакрилатов — оранжево-коричневая. Эту цветную реакцию дают также сложные эфиры других карбоновых кислот. [c.218]
Жиры и масла, представляющие собой сложные эфиры глицерина и высокомолекулярных жирных кислот или жирных кислот среднего молекулярного веса, можно обнаружить по реакции на глицерин, описанной на стр. 529. Зта реакция основана на дегидратации глицерина до акролеина, который можно идентифицировать по цветной реакции с раствором нитропруссида натрия, содержащим пиперидин. Различные воски ссстоят преимущественно из эфиров высших одноосновных карбоновых кислот и высших едноатомных спиртов. Их можно обнаружить пробой на сложные эфиры, описанной на стр. 319. Для этого их переводят в гидроксамовые кислоты, которые образуют окрашенные внутренние комплексные соли железа (III), Зтой реакцией можно обнаружить [c.677]
Другими хромогенными субстратами являются различные сложные эфиры п- или о-нитрофенола - 5 и фенилбензоат . Образующийся фенол определяют цветной реакцией Фолина и Циокалтё, а 2-карбонафтоксихолин — по окраске азокрасителя, получающегося после гидролитического расщепления и сочетания с диазотированным о-дианизидином. [c.171]
Холестерин, один из наиболее распространенных стероидов, в чистом виде представляет собой бесцветное кристаллическое вещество (ромбические пластинки) с температурой плавления 150° С. В холестерине имеется вторичная спиртовая группа у третьего атома и двойная связь у пятого атома углерода (см. формулу на стр, 267). Химические свойства холестерина определяются этими функциональными группами. Например, холестерин образует сложные эфиры с жирными кислотами, находящимися в тканях, присоединяет водород, осаждается из растворов дигитонином. Йодное число холестерина составляет 65,8. Для определения холестерина в качественном и количественном анализах применяется несколько цветных реакций. Например, по методу Салковского раствор холестерина в хлороформе встряхивают с серной кислотой, при этом хлороформный слой окрашивается в красный цвет, а кислый слой приобретает зеленую флуоресцирующую окраску. [c.273]
Танниды представляют собой сложные многоатоы 1ые фенолы, размер юлекул и степень гидроксилирования которых придает им способность удовлетворительно растворяться в воде. Они осаждают желатину и алкалоиды пз раствора, являются вяжущими, дают цветные реакции с солями железа, образуют осадки с ионами многих металлов и довольно нестойки в присутствии влаги и света. Образование осадка с желатиной является ценной качественной реакцией на танниды, и отрицательная реакция показывает, что таннид отсутствует или присутствует в очень незначительных количествах. Танниды легко окисляются в щелочных растворах [9]. Танниды обычно растворимы в спиртах, ацетоне, диоксане и этилацетате, если раствор содержит, по крайней мере, небольшое количество воды. В больншистве случаев они нерастворимы в эфире, бензоле и подобных растворителях. В большинстве своем танниды являются аморфными веществами, хотя описано несколько кристаллических таннидов [41. [c.520]
Поскольку реакция этерификации является обратимым процессом, то, если возможно, процесс ведут с удалением вьщеляющейся при реакции воды в виде азеотропа с используемым спиртом, бензолом или толуолом. Для ускорения этерификации стремятся повысить температуру в реакторе. Но в этом случае сильно увеличивается скорость образования побочных продуктов — простых эфиров, алкенов, алкенолов. Поэтому часто приходится выбирать между повышением температуры и длительностью равновесного процесса этерификации. Сложные эфиры для очистки перегоняют при атмосферном давлении в присутствии щёлочи (для улавливания непрореагировавшей кислоты) или обрабатывают активным углём при нагревании для адсорбции цветных примесей. [c.154]
Сложные эфиры, органические кислоты, амиды и ангидриды кислот можно легко перевести в гидроксамовые кислоты, реагирующие с хлоридом окисного железа в слабокислой среде с образованием красного или фиолетового окрашивания. Эта цветная реакция, по Файглю [7], вызывается наличием кислотной группы —СОЫНОН во всех гидроксамовых кислотах. Ион железа, вероятно, образует с веществами, содержащими эту группу, растворимые внут-рикомплексные соли. [c.106]
Реакция Либермана — Бурхарда. Несколько миллиграммов стерина растворяют в 2—3 мл хлороформа и добавляют (иногда при охлаждении) 10 капель уксусного ангидрида и 2—3 капли серной кислоты. В присутствии холестерина появляется розовокрасная окраска, переходяшая затем (через промежуточную синюю) в зеленую. Эргостерин дает сразу же синюю окраску, переходящую в зеленую стигмастерин — через несколько минут синюю, переходяшую в зеленую ситостерин — через несколько минут фиолетовую окраску, переходяшую в синюю. Имеются данное о механизме этой цветной реакции стеринов, тритерпенов и их сложных эфиров [1]. [c.434]
chem21.info
Реакция - сложный эфир - Большая Энциклопедия Нефти и Газа, статья, страница 3
Реакция - сложный эфир
Cтраница 3
Кроме решения чисто синтетической задачи получения третичных спиртов ( и, через них, непредельных углеводородов) реакция сложных эфиров с реактивами Гриньяра служит для ряда других целей. [31]
При попытке этим способом этерифицировать высокомолекулярные сульфохлориды всегда получаются стойкие эмульсии, так как небольшое количество выделяющегося при реакции сложного эфира алкил-сульфокислоты эмульгируется капиллярно-активной солью сульфо-кислоты, которая образуется в преобладающих количествах. [32]
Поскольку величина р для кислотного гидролиза эфиров бензойной кислоты мала, Тафт [36] предположил, что полярные эффекты в этой реакции сложных эфиров ничтожны. [33]
Все эти реакции имеют много общего; принципы, лежащие в их основе, будут пояснены главным образом на примере реакций сложных эфиров, поскольку такого рода превращения изучены наиболее полно. Катализируемый кислотой гидролиз сложных эфиров является реакцией, обратной катализируемой кислотой этерификации, которая была рассмотрена выше ( стр. В противоположность этому происходящий под действием щелочи гидролиз ( омыление) практически необратим. Начальная стадия последнего заключается в атаке гидроксил-иона на электронодефи-цитный углерод карбонильной группы; в результате образуется промежуточный анион XI, который может либо отщепить ОН и превратиться в исходный эфир, либо отщепить СН30 и перейти в кислоту. [34]
Все эти реакции имеют много общего; принципы, лежащие в их основе, будут пояснены главным образом на примере реакций сложных эфиров, поскольку такого рода превращения изучены наиболее полно. [35]
Все эти реакции имеют много общего; принципы, лежащие в их основе, будут пояснены главным образом на примере реакций сложных эфиров, поскольку такого рода превращения изучены наиболее полно. Катализируемый кислотой гидролиз сложных эфиров является реакцией, обратной катализируемой кислотой этерификации, которая была рассмотрена выше ( стр. В противоположность этому происходящий под действием щелочи гидролиз ( омыление) практически необратим. Начальная стадия последнего заключается в атаке гидроксил-иона на электронодефи-цитный углерод карбонильной группы; в результате образуется промежуточный анион XI, который может либо отщепить ОН и превратиться в исходный эфир, либо отщепить СН30 и перейти в кислоту. [36]
RL, RM и Rs при асимметрическом атоме углерода, связанном с гидро-ксилом, и, следовательно, в соответствии с данными, полученными для реакции сложных эфиров а-кетокислот ( разд. [37]
Водородные атомы при а-углеродах нитрилов являются почти такими же кислыми, как и водородные атомы в - положении к карбонильной группе; в соответствии с этим сложные эфиры цианук-сусной кислоты вступают во многие реакции, сходные с реакциями сложных эфиров малоновой и ацетоуксусной кислот ( 1, разд. [38]
Важнейшим химическим свойством сложных эфиров является разложение их водой на кислоту и спирт. Эта реакция сложного эфира с водой называется гидролизом или омылением. [39]
Аналогично при взаимодействии с альдегидами получаются вторичные спирты. При введении в реакцию сложных эфиров обычно образуются кетоны, а в некоторых случаях сложные эфиры взаимодействуют последовательно с двумя молекулами магнийорганического соединения; при этом в конечном счете получается третичный спирт. [40]
Эти реакции могут быть двух типов: реакции сложных эфиров и реакции солей кислородсодержащих кислот. При получении металлал-килов или металларилов действием алкилирующих агентов, в качестве которых используются реактивы Гриньяра или ал-кильные производные щелочных металлов, иногда удобнее пользоваться не галогенидами металлов, а алкоксильными производными металлов с низшими алифатическими радикалами, так как последние вследствие растворимости в углеводородах или эфире алкилируются почти так же хорошо, как и гало-гениды металлов. [41]
Бэнтон с соавторами ( Bunion, Hughes, Ingold, Meigh, 1950) провели кинетическое исследование аналогичного случая-катализируемого кислотами гидролиза метилэтил-мзо-гексилкарбинолаце-тата; авторы показали, что эта реакция сопровождается рацемизацией с некоторым преобладанием обращения конфигурации. Таким образом, здесь наблюдается аналогия между реакциями сложных эфиров с расщеплением по связи алкил-кислород и реакциями галоидных алкилов, в которых также наблюдались подобные эффекты. [42]
Таким образом, соединения, получающиеся при взаимодействии спирта с хлористым, бромистым или йодистым водородом, являются сложными эфирами этих кислот. В действительности реакции моногалоидных соединений очень сходны с реакциями сложных эфиров неорганических кислородсодержащих кислот. [43]
Реакции гидролиза и омыления амидов происходят аналогично рассмотренным выше реакциям сложных эфиров. [44]
Простые эфиры фенолов расщепляются щелочами, причем легкость этого расщепления увеличивается с ростом кислотности фенола, из которого был получен исходный эфир. Действительно, многие реакции простых эфиров фенолов, обладающих ярко выраженными кислыми свойствами, протекают так же, как реакции сложных эфиров. Динитроанизол превращается в 2 4-динитрофенол уже при простом кипячении в течение часа с 1 эквив спиртового раствора едкого кали. [45]
Страницы: 1 2 3 4
www.ngpedia.ru
Сложные эфиры реакции - Справочник химика 21
Реакция альдегидов и аммиака с альдегидами, кетонами или сложными эфирами (реакция Манниха) [c.415]Реакция обратима, и в зависимости от исходных веществ, условий ее проведения и стехиометрических соотношений реагентов устанавливается определенное состояние равновесия. Полученную смесь эфиров и спиртов обычно разделяют перегонкой. Фактором, катализирующим обмен, может явиться минеральная кислота примером применения такой добавки может служить превращение жиров в метиловые эфиры жирных кислот , а также получение бутилового эфира олеиновой кислоты Эту реакцию катализируют также ионы ОН . При добавлении небольшого количества едкого натра к спиртовому раствору сложного эфира реакция алкоголиза значительно ускоряется. Подобным же образом действуют алкоголяты, образующиеся в спиртовом растворе сложного эфира при введении в него небольших количеств металлического натрия . Путем алкоголиза можно получить такие эфиры, получение которых другими методами затруднительно ввиду малой стойкости кислоты, например изобутиловый эфир ацетоуксусной кислоты . [c.357]
Сложные эфиры. Реакции этерификации и омыления [c.329]Реакция альдегидов или кетонов с цинком и а-галогенозамещенными сложными эфирами (реакция Реформатскою) [c.424]
Сложные эфиры. Реакция этерификации. Гидролиз сложных эфиров. Жиры. [c.370]
Образование сложных эфиров (реакция этерификации). Сложные эфиры можно рассматривать как продукты замещения водородного атома в гидроксильной группе на остаток кислоты — ацил [c.109]
Образование сложных эфиров (реакция этерификации) [c.92]
С карбоновыми кислотами спирты образуют сложные эфиры. Реакция обратима. Равновесие прямой реакции может быть сдвинуто в сторону образования эфира добавлением какой-либо кислоты (кислотный катализ). [c.343]
В присутствии сильных минеральных кислот (H SOJ карбоновые кислоты со спиртами (первичными, вторичными) образуют сложные эфиры - реакция этерификации [c.107]
С кислотами спирты образуют сложные эфиры (реакция этерифи-кации) [c.261]
Окисление первичных и вторичных спиртов можно также осуществить косвенным путем через их сложные эфиры (реакция 19-20). В некоторых случаях нет необходимости выделять сложный эфир и спирт можно окислять в альдегид или кетон в одну стадию. Алкоголят-ионы также дают альдегиды и кетоны с высоким выходом при фотоокислении под действием О2 [86] (окислителем здесь служит синглетный кислород, см. т. 3, реакции 14-8 и 15-38). [c.272]
В этих случаях необходимо удалять кислоты из смеси. Удаления можно достичь, переведя кислоты в сложные эфиры реакцией их с диазометаном или другим удобным способом, который бы не приводил к изменению концентрации других компонентов. [c.48]
Ацилирование сложных эфиров сложными эфирами (реакции Кляйзена и Дикмана) [c.425]
Карбоновые кислоты взаимодействуют со спиртами с образованием сложных эфиров (реакция этерификации). Реакция катализируется кислотами. При взаимодействии спирта с карбоновой кислотой отщепляется водород от спирта и гидроксигруппа от кислоты [c.342]
Спирты можно непосредственно превращать в диастереомерные сложные эфиры реакцией с оптически активными кислотами. Довольно часто для образования диастереомер- [c.103]
Гидролиз сложных эфиров — реакция, обратная реакции этерификации. Продуктами гидролиза сложных к зи-ров являются кислота и спирт [c.684]
Ацетилен взаимодействует с 2 молями ароматического соединения, давая 1,1-диарилэтаны, а другие алкины, если и реагируют, то плохо. Спирты более реакционноспособны, чем алкилгалогениды, хотя при катализе реакции кислотами Льюиса требуется большее количество катализатора, так как он расходуется на комплексообразование с группой ОН. Для катализа реакций с участием спиртов часто применяют протонные кислоты, особенно серную. При использовании в качестве реагентов сложных эфиров реакция осложняется конкуренцией между алкилированием и ацилированием (реакция 11-15). И хотя в этой конкуренции обычно преобладает алкилирование и вообще ею можно управлять правильным подбором катализатора, сложные эфиры карбоновых кислот редко используются в реакциях Фриделя — Крафтса. Среди других алкилирующих агентов — тиолы, сульфаты, сульфонаты, алкилнитросоединения [199] и даже алканы и циклоалканы в условиях, когда их можно превратить в карбокатионы. Здесь следует отметить и этиленоксид, с помощью которого можно ввести в кольцо группу СН2СН2ОН, и циклопропан. Для реагентов всех типов реакционная способность соответствует следующему ряду аллильный и бензиль-ный тип>третичный>вторичный> первичный. [c.349]
Гидролиз сложных эфиров—реакция обратимая [c.541]
Карбоновые кислоты или сложные эфиры реакция Буво—Блана) [c.229]
ИЗ СЛОЖНЫХ ЭФИРОВ (РЕАКЦИИ КЛЯЙЗЕНА И ДИКМАНА) [c.162]
ИЗ сложных ЭФИРОВ и ДРУГИХ СОЕДИНЕНИЙ, СОДЕРЖАЩИХ АКТИВНЫЙ ВОДОРОД, ПРИ КОНДЕНСАЦИИ СО СЛОЖНЫМИ ЭФИРАМИ (РЕАКЦИЯ КЛЯЙЗЕНА) [c.321]
ИЗ СЛОЖНЫХ ЭФИРОВ и НЕНАСЫЩЕННЫХ СЛОЖНЫХ ЭФИРОВ (РЕАКЦИЯ МИХАЭЛЯ) [c.330]
В первом случае (а) образуются одноосновные карбоновые кислоты, во втором (б)—изомерные им алкилформиаты, т. е. сложные эфиры. Реакция (а) по теории промежуточного образования кислот является основной в синтезе синтола (стр. 708). [c.733]
Новым процессом снижения ненасыщенности молекул является лимеризация, пригодная как для получения смазочных масел, так и Д.ЧЯ производства присадок к маслам. Известна реакция полимеризации, ведущая к получению двухосновных кислот, образующихся из ненасыщенных жирных моно- или поликислот или из их сложных эфиров. Реакция идет под давлением, при нагреве в присутствии источников радикалов, катализатора (глинистый минерал) и воды. Фракционирование полученных продуктов на MOHO-, ди- и тримеры осуществляют путем молекулярной перегонки. [c.244]
При работе с оксидом алюминия следует помнить о его каталитических свойствах. Так, в процессе хроматографирования могут протекать гидролиз ангидридов, хлорангидридов, сложных эфиров реакции конденсации альдегидов, кетонов отщепление галоге-новодородов и другие химические превращения неустойчивых соединений. [c.58]
Г. сложных эфиров — реакция, широко применяющаяся в промышленности для получения спиртов щелочной гидролиз жиров — для получения глицерина и солей высших алифатических кислот (мыла). Гидролиз винилацетата и поливинилацетата — промышленные способы синтеза соответственно ацетальдегида и П0ЛИВИ1ШЛ0В0Г0 спирта. Кроме большого промышленного значения для ОСНОВНОГО и тонкого органического синтеза, Г. с. э. играет важную роль в процессах жизнедеятельности организмов, в природе, а также в лабораторной практике. [c.74]
Лактоны являются циклическими сложными эфирами и вступают в обычные для сложных эфиров реакции. Присутствие -лактонногэ кольца можно установить по характерной полосе поглощения карбонильной группы в инфракрасном спектре при 5,62—6,63 мк, так как у нециклических эфиров эта полоса расположена в области 5,74—5,82 мк. а у б-лактонов — при 5,73—5,74 мк. [c.75]
СНзСООН, Ha l OOH, H I2 OOH, I3 OOH константы ионизации изменяются в такой последовательности 1,754 10 1,38 -10- 5,6-10-2 2,2-10 2. Гидроксил карбоксильной группы можно. заместить другими группами. Так, при взаимодействии со спиртами образуются сложные эфиры (реакция этери-фикации) [c.121]
Еще одним доказательством в пользу этого механизма служит тот факт, что небольшое, но детектируемое количество продукта обмена Ю (см. разд. 10.9) было обнаружено в катализируемом кислотой гидролизе бензамида [461]. (Обмен 0 наблюдался и в катализируемом основанием процессе [462], что согласуется с механизмом Вдс2.) Однако на основании определенных кинетических результатов сделано предположение [463], что катализируемый кислотами гидролиз амидов, по крайней мере в некоторых случаях, частично или полностью происходит через образующийся в небольшом количестве N-пpoтoниpoвaн-ный амид [464]. Кинетические исследования показали, что иа лимитирующей стадии в реакции участвуют три молекулы воды [465]. Следовательно, как и в случае механизма Адс2 для гидролиза сложных эфиров (реакция 10-11), в процессе принимают участие дополнительные молекулы воды, например, следующим образом [c.118]
Реакция ацилгалогенидов со спиртами — наилучший общий метод получения сложных эфиров. Реакция находит широкое применение и может быть проведена для субстратов, содержащих различные функциональные группы. Для связывания образующегося НХ часто добавляют основание. В методе Шот-тена — Баумана используется водный раствор щелочи, но часто применяется пиридин. Как R, так и R могут быть первичными, вторичными или третичными алкилами или арилами. По этой же методике можно приготовить сложные эфиры енолов, хотя при этом возникает конкуренция с С-алкилированием. В сложных случаях, особенно для стерически затрудненных кислот или третичных R, вместо спирта можно брать алкоголят-ион (см., например, [515]). Таллиевые соли фенолов дают очень высокие выходы эфиров фенолов [516]. Для стерически затрудненных фенолов применялся межфазный катализ [517]. [c.125]
Побочно протекают реакции гомоконденсации кетонов (т. 3, реакция 16-40) и сложных эфиров (реакция 10-111), а также конденсация кетона со сложным эфиром, когда замещение идет в а-положение сложного эфира (т. 3, реакция 16-41). Механизм здесь такой же, как и в реакции 10-111 [1350]. [c.236]
Арилирование соединений типа 2СНг2 аналогично реакции 10-96, рассмотренной в т. 2, где дано определение группы 2. Активированные арилгалогениды, как правило, дают хорошие результаты [130]. В присутствии избытка амида натрия в реакцию можно вводить даже неактивированные арилгалогениды [131]. Подобным образом можно арилировать также простые кетоны [132] и сложные эфиры. Реакция с неактивированными галогенидами происходит ио ариновому механизму и представляет собой метод расширения синтезов на основе малонового эфира (или сходных соединений) с использованием ароматических молекул. Основание здесь выполняет две функции оно отрывает протон от молекулы 2СН22 и катализирует реакцию с образованием дегидробензола. Реакция была использована для осуществления процесса замыкания цикла [133] [c.29]
Конденсация альдегидов или кетонов с а-галогенозамещенными сложными эфирами (реакция Дарзаиа) [c.425]
Реакция между нитрилами, цинком и а-галогенозамещенными сложными эфирами (реакция Блэза) [c.426]
Для ацилирования фенолов чаще всего используют хлорангидриды и ангидриды кислот, обычно в щелочном растворе. Так как гидроксид-анионы катализируют гидролиз сложных эфиров, реакцию ведут на холоду, постепенно до.бавляя ацилирующий агент (реакция Шоттен— Баумана) [c.264]
ИЗ СЛОЖНЫХ ЭФИРОВ (РЕАКЦИЯ БУВО —БЛАИА) ИЛИ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ СО ЩЕЛОЧНЫМИ МЕТАЛЛАМИ И СПИРТАМИ [c.229]
chem21.info