Содержание
Сложные эфиры. Жиры. Мыла. (10 класс)
Похожие презентации:
Сложные эфиры. Жиры
Физические, химические свойства предельных и непредельных карбоновых кислот, получение
Газовая хроматография
Хроматографические методы анализа
Искусственные алмазы
Титриметрические методы анализа
Биохимия гормонов
Антисептики и дезинфицирующие средства. (Лекция 6)
Клиническая фармакология антибактериальных препаратов
Биохимия соединительной ткани
1. Сложные эфиры. Жиры. Мыла.
R–COOR’
Сложные эфиры.
Жиры. Мыла.
Урок 21
10 класс (базовый)
П.13
2. Общая формула сложных эфиров
где R – радикалы
3. Сложными эфирами
— называют производные
карбоновых кислот, в которых
атом водорода карбоксильной
группы замещен на
углеводородный радикал.
• Их состав соответствует общей
формуле
R–COOR’
4. Реакция этерификации
реакции между спиртами и кислотами,
в результате которых образуются сложные
эфиры и выделяется вода (от лат. ether –
ether –
эфир). Катализаторами являются минеральные
кислоты.
5. Гидролиз
• Данная реакция обратима. Обратный
процесс – расщепление сложного эфира
при действии воды с образованием
карбоновой кислоты и спирта – называют
гидролизом сложного эфира.
6. Специфический аромат ягод, плодов и фруктов
• Сложные эфиры широко
распространены в
природе.
Специфический аромат
ягод, плодов и фруктов в
значительной степени
обусловлен
представителями этого
Эфиры низших карбоновых кислот
класса органических
и низших одноатомных спиртов
имеют приятный запах цветов,
соединений.
ягод и фруктов.
7. Воски
• Сложные эфиры
жирных кислот и
спиртов с длинными
углеводородными
радикалами называют
восками.
Например, пчелиный
воск содержит сложный
эфир пальмитиновой
кислоты
и мирицилового
спирта
Ch4(Ch3)14–CO–OCh3(Ch3)29Ch4.
8. Сложные эфиры. Физические свойства
• Сложные эфиры –
жидкости, обладающие
приятными фруктовыми
запахами.
• Их плотность меньше
плотности воды, они
практически не
растворяются в воде.
• Хорошо
растворимы в спиртах.
9. Сложные эфиры имеют большое практическое значение
1. Их применяют в промышленности в
качестве растворителей и промежуточных
продуктов при синтезе различных
органических соединений.
2. Сложные эфиры с приятным запахом
используют в парфюмерии и пищевой
промышленности.
3. Сложные эфиры часто служат исходными
веществами в производстве многих
фармацевтических препаратов.
Ch3-O-CO-R1 — сложные эфиры
трёхатомного
I
спирта глицерина и
CH-О-CO-R2
высших одноатомных
I
Ch3-O-CO-R3, карбоновых кислот.
где R1, R2 и R3 — радикалы (иногда различных)
жирных кислот.
11. Общее название таких соединений — триглицериды
12. Из истории:
• Впервые
химический
состав жиров
определил в
начале прошлого
века французский
химик Мишель
Эжен Шеврель
13.
 Из истории:
Из истории:
• То, что в состав жиров
и масел входит
глицерин, впервые
выяснил в 1779 г
знаменитый шведский
химик
Карл Вильгельм
Шееле.
14. Состав жиров
• В состав жиров могут входить остатки
предельных и непредельных кислот,
содержащих четное число атомов
углерода и неразветвленный углеродный
скелет.
• Природные жиры, как правило, являются
смешанными сложными эфирами, т.е. их
молекулы образованны различными
карбоновыми кислотами.
15. Физические свойства жиров:
• Жиры не растворимы в воде, но хорошо растворяются в
органических растворителях – бензоле, гексане.(эта
способность используется для чистки одежды от
жировых пятен )
• Плотность их меньше 1г/см3
• Если при комнатной температуре они имеют твердое
агрегатное состояние, то их называют жирами, а если
жидкое, то – маслами.
• У жиров низкие температуры кипения.
• С увеличением длины УВ-радикала температура
плавления жира увеличивается.
16. Классификация жиров
17. Жиры= высшие предельные карбоновые кислоты + глицерин
• Жиры, образованные
предельными
кислотами (масляной,
пальмитиновой,
стеариновой и др.),
имеют, как правило,
твердую
консистенцию.
• Это жиры животного
происхождения.
• Говяжий, свиной,
бараний и др.
Классификация жиров:
Животные жиры чаще всего твердые
или полужидкие вещества:
сливочное
масло,
животное
сало, рыбий
жир и др.
19. Жиры= высшие непредельные карбоновые кислоты + глицерин
• Если в составе жира
содержатся остатки
непредельных кислот
(олеиновой и линолевой),
они представляют собой
вязкие жидкости – масла.
• Это: льняное, конопляное,
подсолнечное, оливковое,
соевое, кукурузное и др.
20. Классификация жиров:
Растительные жиры называют маслами.
Это обычно жидкие вещества:
подсолнечное, оливковое, льняное, касторовое
масла и др.
Реакция гидрирования
Жидкие жиры превращают в
твердые путем реакции
гидрогенизации
(гидрирования).
При этом водород
присоединяется по двойной
связи, содержащейся в
углеводородном радикале
молекул масел.
22. Химические свойства жиров
Гидрирование жиров :
Ch4
Ch4
Ch4
23. Химические свойства жиров
• Гидролиз ( омыление с водой и щелочами –
едким натром или едким кали).
Продукт гидрогенизации масел — твердый жир
(искусственное сало, саломас). Маргарин –
пищевой жир, состоит из смеси
гидрогенизированных масел (подсолнечного,
кукурузного, хлопкого и др.),животных жиров,
молока и вкусовых
добавок (соли,
сахара, витаминов
и др.).
Жирам как сложным эфирам
свойственна обратимая реакция
гидролиза, катализируемая
минеральными кислотами. При
участии щелочей гидролиз
жиров происходит необратимо.
Продуктами в этом случае
являются мыла — соли высших
карбоновых кислот и щелочных
металлов.
• Натриевые соли —
твердые мыла,
калиевые — жидкие.
• Реакция щелочного
гидролиза жиров, и
вообще всех сложных
эфиров, называется
также омылением.
27. Жиры получают:
• Сепаратированием. Является наиболее
эффективным методом очистки жиров.
• Вытапливанием.
• Гидрированием. Гидрирование проводится в
специальных автоклавах. Используется этот
процесс для получения маргарина.
• Экстрагированием или прессованием.
Сущность процессов прессования заключается
в отжимании масла из измельченных семян.
28. Применение жиров
В медицине
Применение
в пищу
Производство
мыла
Жиры
Производство
свечей
Корм для
животных
В
Производство Производство
краски
парфюмерии
глицерина
29. Значение жиров:
Жиры имеют большое значение в
жизни человека: они выполняют очень
важные функции в организме, такие
как энергетическая, защитная,
строительная.
30. Вывод:
1. Жиры — это сложные эфиры трехатомного спирта
глицерина и жирных кислот.
2. Жиры подразделяются на животные и
растительные.
3. Жиры получают вытапливанием,
сепарированием, гидрированием,
прессованием или экстрагированием.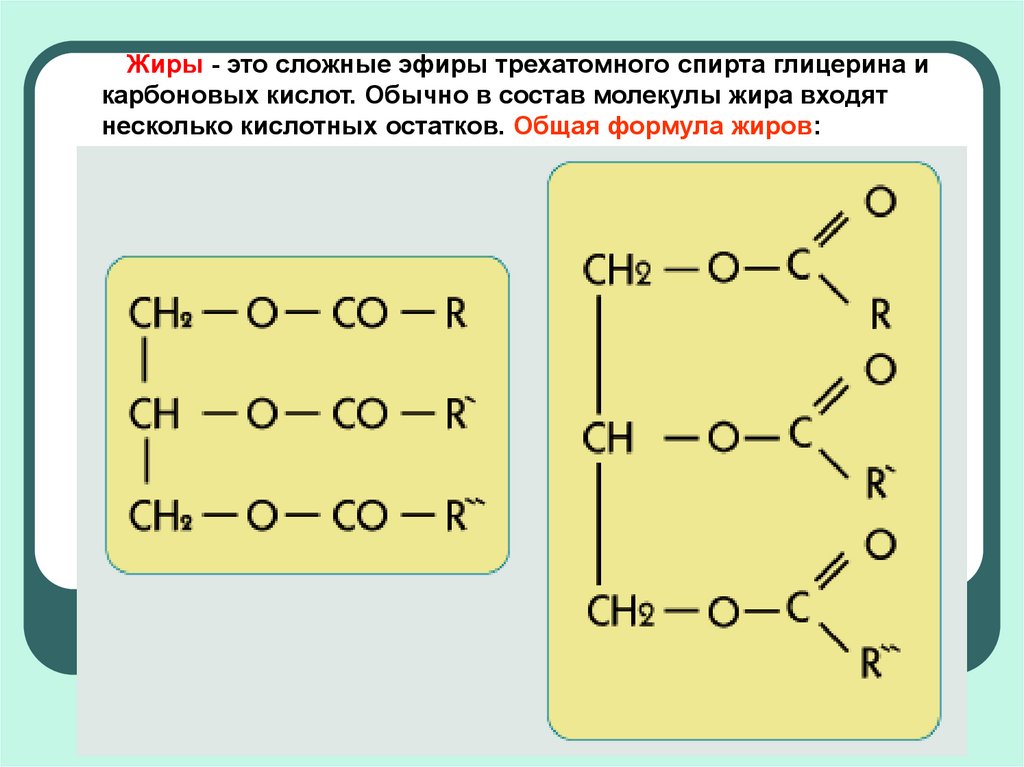
4. Жиры в организме человека выполняют
энергетическую, защитную, строительную
функции.
5. Применение жиров разнообразно.
31. Задание №1
• Составить формулы и дать названия
эфирам, образованным
1 вариант:
бутановой кислотой и
метиловым спиртом;
2 вариант:
метановой кислотой и пропиловым
спиртом;
32. Ответ задание №1
1 вариант:
О
//
СН3 – СН2 – СН2 – СООН + СН3–ОН → СН3 – СН2 – СН2 – С
+ Н 2О
бутановая кислота
метанол
метиловый эфир \
бутановой кислоты О — СН3
2 вариант:
О
О
//
//
Н – С + СН3– СН2 — СН2 — ОН → Н – С
+ Н 2О
\
пропанол
\
ОН
О — СН 2 — СН2 — СН3
метановая
пропиловый эфир метановой
кислота
кислоты
Задание №2
Закончите реакцию, назовите полученные вещества
1 вариант:
С5Н11СООН + С4Н9ОН →
2 вариант:
С7Н13СООН + С2Н5ОН →
34. Ответ задание №2
1 вариант:
С5Н11СООН + С4Н9ОН → С5Н11СООС4Н9 + Н2О
2 вариант:
С7Н13СООН + С2Н5ОН → С7Н13СООС2Н5+ Н2О
35.
 Задание №3 Какая из приведенных структур соответствует молекуле жира?
Задание №3 Какая из приведенных структур соответствует молекуле жира?
Ответ: Б
А
В
Б
36. Задание №4 Какой из приведённых жиров жидкий?
37. Домашнее задание
• Выучить П.13
• Упражнения 1-10 (устно)
• Задача №11,12 стр.100
38. Источники
• images.yandex.ru/
• school.xvatit.com/
• Рисунки — Мультимедийный обучающий
комплекс «1С: Образовательная
коллекция. Органическая химия 10-11
классы
• Автор: Калитина Тамара Михайловна
• Место работы: МБОУ СОШ №2 с.Александров-Гай
Саратовской области
• Должность: учитель химии
• Дополнительные сведения: сайт
http://kalitina.okis.ru/
• Мини-сайт
http://www.nsportal.ru/kalitina-tamara-mikhailovna
English
Русский
Правила
Сложные эфиры
–
это
соединения, содержащие карбоксильную
группу, связанную с двумя алкильными
радикалами.
Общая
формула сложных эфиров такая же, как у
карбоновых кислот:
CnH2nO2
Получение сложных эфиров.

1)Cложные
эфиры могут быть получены при
взаимодействии
карбоновых кислот со спиртами (реакция
этерификации).
Катализаторами
являются минеральные кислоты.
2)
Сложные
эфиры фенолов нельзя получить с помощью
этерификации,
для их получения используют реакцию
фенолята
с галогенангидридом кислоты:
С6Н5-О—Na+
+
C2H5–C=O
NaCl
+
C6H5–O—C=O
\
\
Cl
C2H5
фениловый
эфир пропановой
кислоты
(фенилпропаноат)
НОМЕНКЛАТУРА
СЛОЖНЫХ ЭФИРОВ.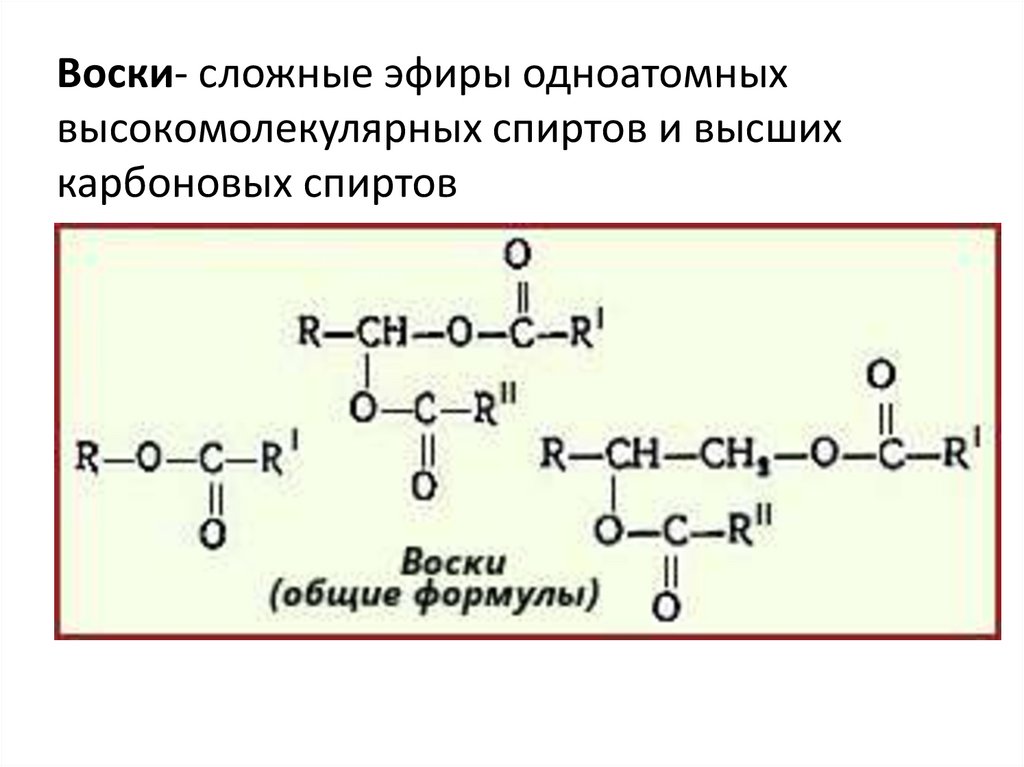
Названия
сложных эфиров определяются названиями
кислоты
и спирта,
из которых они образуются.
Формула | Полное | Другие |
СН3-С-ОСН3 ║ О | метиловый | метилацетат уксусно-метиловый |
Н-С ║ О | этиловый | этилформиат муравьино-этиловый |
С2Н5 ║ О | пропиловый | пропилпропаноат |
Виды
изомерии сложных эфиров.
1.
Изомерия
углеродной
цепи
начинается по кислотному остатку с
бутановой кислоты, по спиртовому остатку
— с пропилового спирта, например,
этилбутирату изомерны этилизобутират,
пропилацетат и изопропилацетат.
2.
Изомерия
положения
сложноэфирной группировки
—СО—О—.
Этот вид изомерии начинается
со
сложных эфиров, в молекулах которых
содержится не менее 4 атомов углерода,
например этилацетат и метилпропионат.
3.
Межклассовая
изомерия
с карбоновыми кислотами.
СВОЙСТВА
СЛОЖНЫХ ЭФИРОВ.
1. Гидролиз сложных эфиров.
Реакция
этерификации обратима. Обратный процесс
– расщепление сложного эфира при
действии воды с образованием карбоновой
кислоты и спирта – называют гидролизом
сложного эфира.
Кислотный
гидролиз обратим:
Щелочной
гидролиз
протекает необратимо:
Эта
реакция называется омылением
сложного эфира.
2.
Реакция
восстановления.
Восстановление сложных эфиров водородом
приводит к образованию двух спиртов:
Видео с вопросами: Определение общей формулы сложных эфиров
Стенограмма видео
R используется в органической химии для
обозначают углеводородную цепь. Что из перечисленного является
общая формула сложных эфиров? (A) прочерк ROR, (B) RCOOH, (C) ROOR
тире, (D) тире RCOOR или (E) ROH.
Вопрос касается сложных эфиров. Сложные эфиры представляют собой обширную группу органических
соединения, содержащие атом углерода, связанный двойной связью с атомом кислорода, и
одинарной связью с другим атомом кислорода. Когда атом связан с этим кислородом
атом не атом водорода, а атом углерода, то мы называем эту функциональную группу
сложноэфирная группа. По обе стороны от этой сложноэфирной группы
у нас есть R и группа тире R.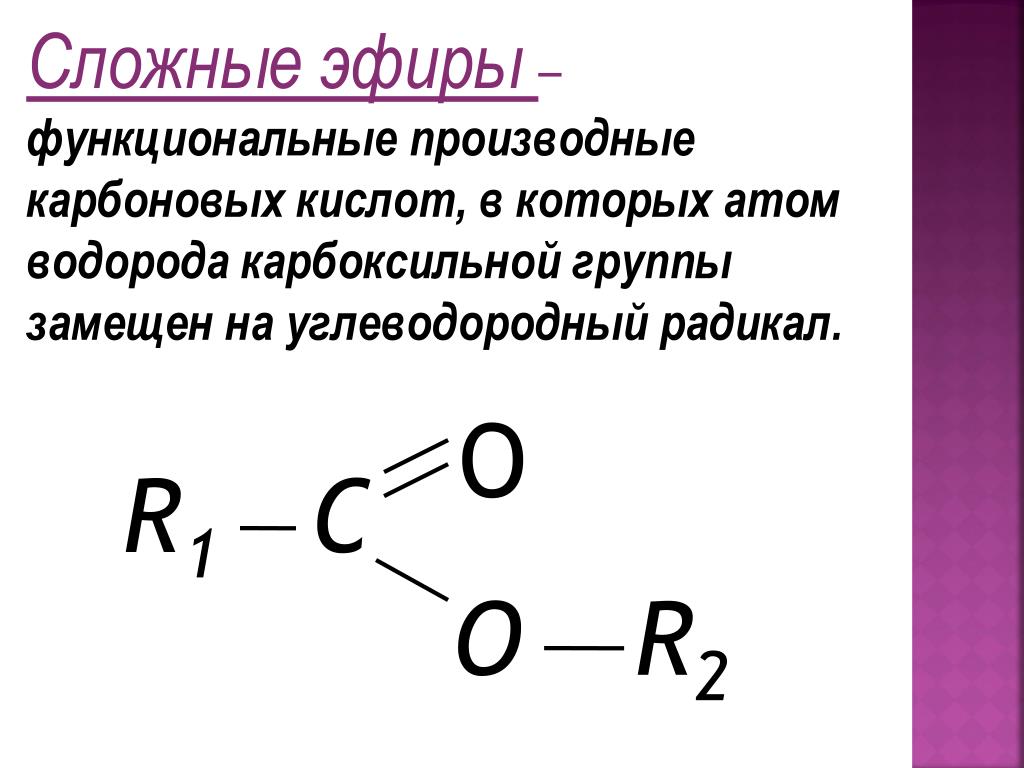 R и R тире обычно используются для
R и R тире обычно используются для
обозначают прямые алкильные цепи, такие как Ch4, метильная группа, или Ch3Ch4, этильная группа
группа или разветвленные алкильные цепи, такие как изопропильная группа, или даже арильные группы,
которые представляют собой группы, содержащие кольца ароматических углеводородов, такие как бензил
группа. Rdash не может быть атомом водорода, т.к.
это сделало бы молекулу карбоновой кислотой, но R может быть атомом водорода.
До сих пор мы обсуждали
что нам сказали в вопросе, что R используется для обозначения углеводородной цепи, или
атом водорода здесь. Сложные эфиры можно получить, реагируя с
карбоновой кислоты со спиртом в присутствии дегидратирующего агента. Эта часть сложного эфира происходит от
карбоновой кислоты, а эту часть из спирта. Одинарная связь углерод-кислород
называется сложноэфирной связью.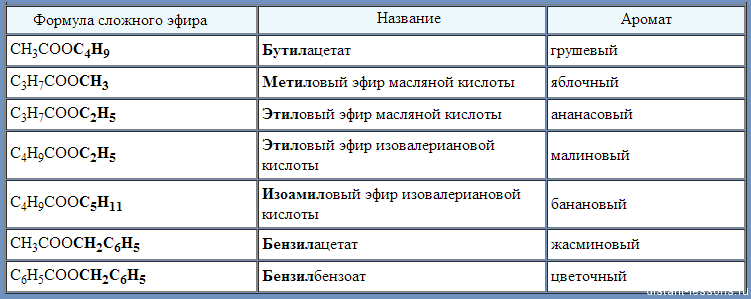 Вода является побочным продуктом этого
Вода является побочным продуктом этого
реакция. Мы можем написать общую формулу
такой сложный эфир или такой, который показывает более правильные валентные углы, или мы можем
сконденсируйте его еще больше. Чтобы начать конденсацию, мы удаляем все
одиночные облигации. Эта частично сокращенная формула
по-прежнему показывает нам, что эта группа R связана с этим атомом углерода. Мы знаем это, потому что они следующие
друг к другу в сокращенной формуле.
Точно так же этот атом углерода
и этот атом кислорода связан, и этот атом кислорода с тире-группой R. Но как мы относимся к
двойная связь углерод-кислород? Мы хотим сжать эту часть
молекула еще дальше. Что мы делаем, так это удаляем двойной
связь и запишите атом кислорода между атомом углерода и другим атомом кислорода,
что дает нам эту формулу. Помните, что существует двойная связь
между этими атомами и простой связью между этими двумя атомами, хотя мы не можем
см. это из этой сжатой формулы. Мы должны признать, что эти
это из этой сжатой формулы. Мы должны признать, что эти
части молекул одинаковы. Итак, какова общая формула
сложные эфиры? Ответ: (D) RCOOR тире.
Общая формула сложного эфира (где R представляет собой алкильную группу): A) R — OHB) R — COOHC) R — COORD) R
Ответ
Verified
231.3k+ views
Подсказка: Встречающиеся в природе химические вещества, которые образуются при сочетании кислоты и спирта, известны как сложные эфиры. Эфиры имеют органическую природу.
Полный ответ:
Функциональная группа спирта – ОН. Таким образом, R — OH — это общая формула спирта.
Таким образом, вариант (А) неверен.
Функциональная группа кислоты – СООН. Таким образом, R — COOH является общей формулой кислоты.
Таким образом, вариант (Б) неверен.
Сложные эфиры образуются при соединении кислоты и спирта. Таким образом, общая формула сложного эфира R — COOR.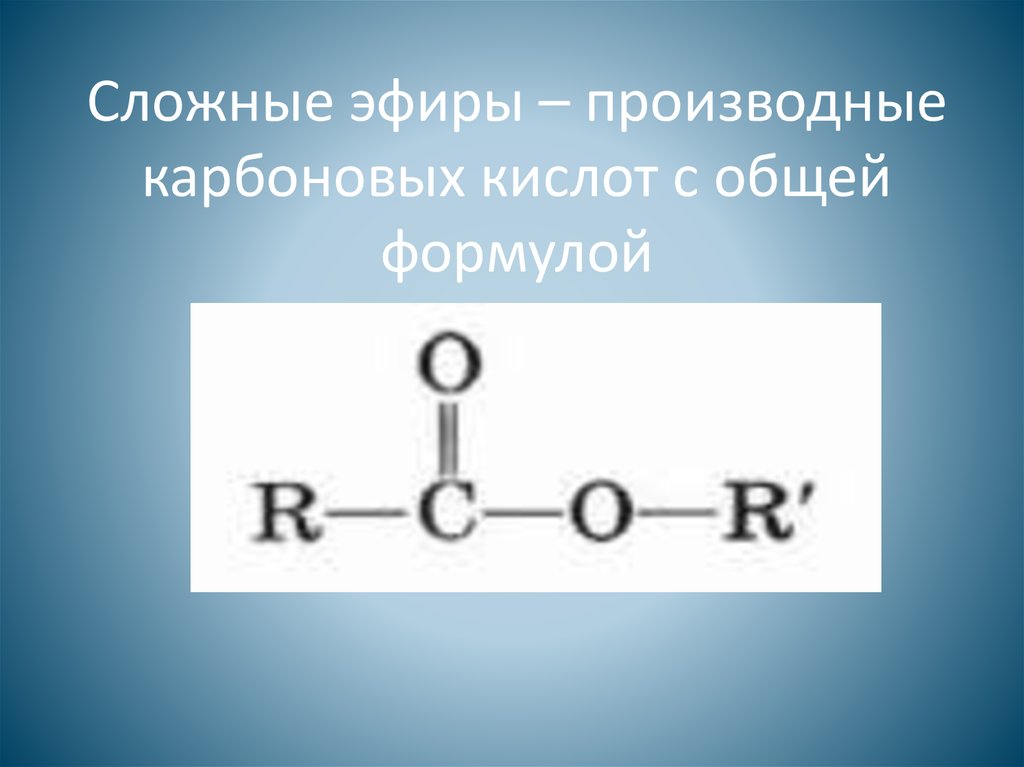
Таким образом, вариант (С) правильный.
Добавление атома водорода к алкильной группе дает исходный алкан. Таким образом, общая формула R-H относится к алкану.
Таким образом, вариант (D) неверен.
Таким образом, правильный вариант (C)R — COOR.
Дополнительная информация: Общая реакция образования сложного эфира при соединении кислоты и спирта выглядит следующим образом:
${\text{R — OH + R — COOH}} \to {\text{ R — COOR + }}{{\text{H}}_2}{\text{O}}$
В ходе реакции удаляется молекула воды.
Реакция пропанола и метановой кислоты дает сложный эфир, называемый пропилметаноатом. Реакция выглядит следующим образом:
${\text{C}}{{\text{H}}_{\text{3}}}{\text{ — C}}{{\text{H}}_{ \text{2}}}{\text{ — C}}{{\text{H}}_{\text{2}}}{\text{ — OH + H — COOH}} \to {\text{ C}}{{\text{H}}_{\text{3}}}{\text{- C}}{{\text{H}}_{\text{2}}}{\text{- C}}{{\text{H}}_{\text{2}}}{\text{ — COOH + }}{{\text{H}}_2}{\text{O}}$
Примечание: При названии сложных эфиров сначала назовите спиртовую группу, затем назовите кислотную группу с окончанием –oate.
In ${\text{C}}{{\text{H}}_{\text{3}}}{\text{ — C}}{{\text{H}}_{\text{2} }}{\text{ — C}}{{\text{H}}_{\text{2}}}{\text{ — COOH}}$, спиртовая группа — пропил, а кислотная группа — метан. В кислотной группе замените –е на –оат. Таким образом, название эфира — пропилметаноат.
Другим примером сложного эфира является этилпропаноат ${\text{C}}{{\text{H}}_{\text{3}}}{\text{ — C}}{{\text{H}}_ {\text{2}}}{\text{ — COO — C}}{{\text{H}}_2}{\text{ — C}}{{\text{H}}_3}$. Этилпропаноат образуется в результате реакции этанола $\left( {{\text{C}}{{\text{H}}_{\text{3}}}{\text{C}}{{\text{ H}}_{\text{2}}}{\text{ — OH}}} \right)$ с пропановой кислотой $\left( {{\text{C}}{{\text{H}}_{ \text{3}}}{\text{C}}{{\text{H}}_{\text{2}}}{\text{ — COOH}}} \right)$.
Недавно обновленные страницы
В Индии по случаю бракосочетания фейерверк 12 класса химии JEE_Main
Щелочноземельные металлы Ba Sr Ca и Mg могут быть организованы 12 класса химии JEE_Main
Что из следующего имеет самый высокий электродный потенциал Химический класс 12 JEE_Main
Что из следующего является истинным пероксидом A rmSrmOrm2 Химический класс 12 JEE_Main
Какой элемент обладает наибольшим атомным радиусом Химический класс 11 JEE_Main
Фосфин получают из следующей руды А Кальций 12 класса по химии JEE_Main
В Индии по случаю бракосочетания фейерверков 12 класса по химии JEE_Main
Щелочноземельные металлы Ba Sr Ca и Mg могут быть отнесены к 12 классу по химии JEE_Main
Что из перечисленного ниже имеет самый высокий электродный потенциал Химический класс 12 JEE_Main
Что из следующего является истинным пероксидом A rmSrmOrm2 Химический класс 12 JEE_Main
Какой элемент обладает наибольшим атомным радиусом Химический класс 11 JEE_Main
Фосфин получается из следующей руды A -Calcium Class 12 Chemistry Jee_main
Трендовые сомнения
Студенты также читают
Гидролиз эфиров
.
