Содержание
Эфирный аромат высоких технологий — Литературная газета
ФУНКЦИОНИРУЕТ ПРИ ФИНАНСОВОЙ ПОДДЕРЖКЕ МИНИСТЕРСТВА ЦИФРОВОГО РАЗВИТИЯ, СВЯЗИ И МАССОВЫХ КОММУНИКАЦИЙ РОССИЙСКОЙ ФЕДЕРАЦИИ.
Реклама. |
ЛГ online
Вспоминая Святогора
09.11.2022
В ЦДЛ прошел вечер памяти поэта и общественного деятеля, постоянного автора «ЛГ» Сергея СОКОЛКИНА.«Жизнь такова, какова она есть, и больше – никакова!»
04.11.2022
Замечательный поэт Владимир КОСТРОВ глазами Владимира СПЕКТОРА.Великолепие Папанова
31.10.2022
К 100-летию выдающегося актера, педагога и режиссера.
Эссе Александра БАЛТИНА.
ЛГ плюс
Звезда не падает дважды
05.11.2022
Поэзию Веры БАГРЕЦОВОЙ с полным правом можно отнести к «тихой лирике».Кеды с белыми шнурками
30.10.2022
Стихам Ольги ШИЛОВОЙ порой присуща почти детская непосредственность.Готовься к погрому, Европа!
25.10.2022
В стихах Руслана КОШКИНА реальность тесно переплетается с историей.
Спецформат
Праздник русской литературы в Янтарном краю
11.11.2022
Завершился двухнедельный литфестиваль «Дни литературы в Калининградской области».Песни, принятые народом
08.11.2022
К 110-летию со дня рождения Льва Ошанина. Материал Владимира КОРНИЛОВА.
Материал Владимира КОРНИЛОВА.Самый человечный… инструмент
06.11.2022
Мария ЗАЛЕССКАЯ – о вручении премии «Органист года»
ОПРОСНИК
Постоянно
Иногда
Никогда
Позиция
Литературный ковчег
07.11.2022
Израильский писатель утверждает, что эмигранты не изменили ни русской культуре, ни языку.Сим-салабим
02.11.2022
Хорошие стихи не каждый умеет писать, а спьяну мы все большие поэты, полагает Нат ВЕСЕНИН.О чем не сказал Путин?
28.10.2022
Виталий ШМАЛЕНЮК полагает, что выступлению президента не хватило самого главного.
Спецпроекты ЛГ / На переднем крае науки и техники
Теги: нефтехимия , карбоновая кислота , эфиры
Оценить:
(Нет голосов)
12+
Новости
- 11.11.2022
«Это моя Земля. Поморье»
Сборник легенд выпущен к 85-летию Архангельской области.
- 11.11.2022
«Сладостный стиль Аксенова»
В Большом зале ЦДЛ состоится вечер памяти писателя.
- 10.11.2022
Мастерская АСПИ
11 ноября открывается пятая Межрегиональная творческая мастерская для начинающих писателей.
- 10.11.2022
Представят работы известного фотографа
В СПб состоится открытие фотовыставки «Мгновение наследия 2022».

- 09.11.2022
«Честь имею»
В Москве состоялась церемония вручения премии, посвященной теме военного образования и военного дела.
Все новости
Книга недели
Николай Долгополов. Легендарные разведчики 3. – М.: Молодая гвардия, 2020. – 352 с. – 7000 экз.
Колумнисты ЛГ
События и мнения
Трамплин для Трампа?
Настал день исполнения российских надежд:8 ноября, промежуточные выборы в США.
Литература
«Индульгенция» на теме
Говорят, для детей надо писать так же хорошо, как для взрослых, только лучше.
События и мнения
Подсказки истории
Минувшая неделя отмечена двумя системными событиями: активным подключением прези…
Литература
Будем мужественны
Рано или поздно придётся махнуть на себя рукой. Не в том смысле, что лежать под …
События и мнения
Осеннее обострение
Многое из происходящего в последние недели на Украине и вокруг неё было ожидаемо.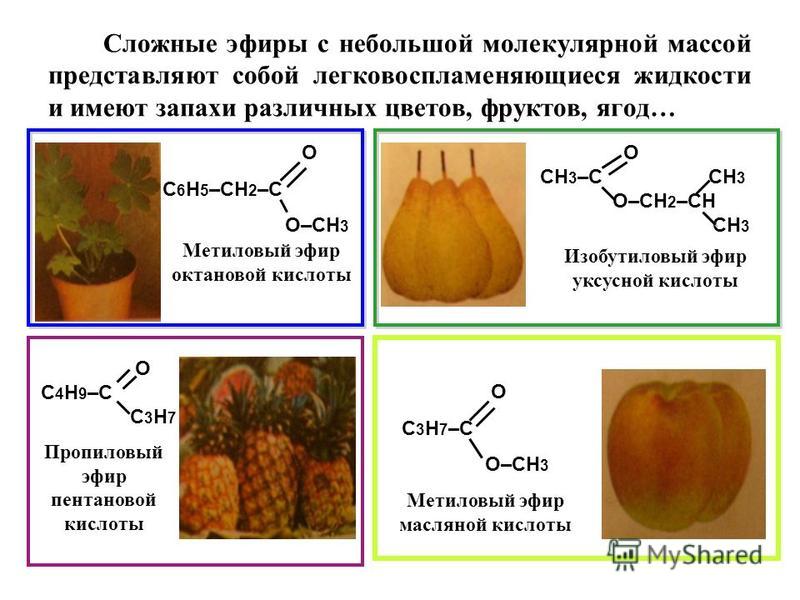 ..
..
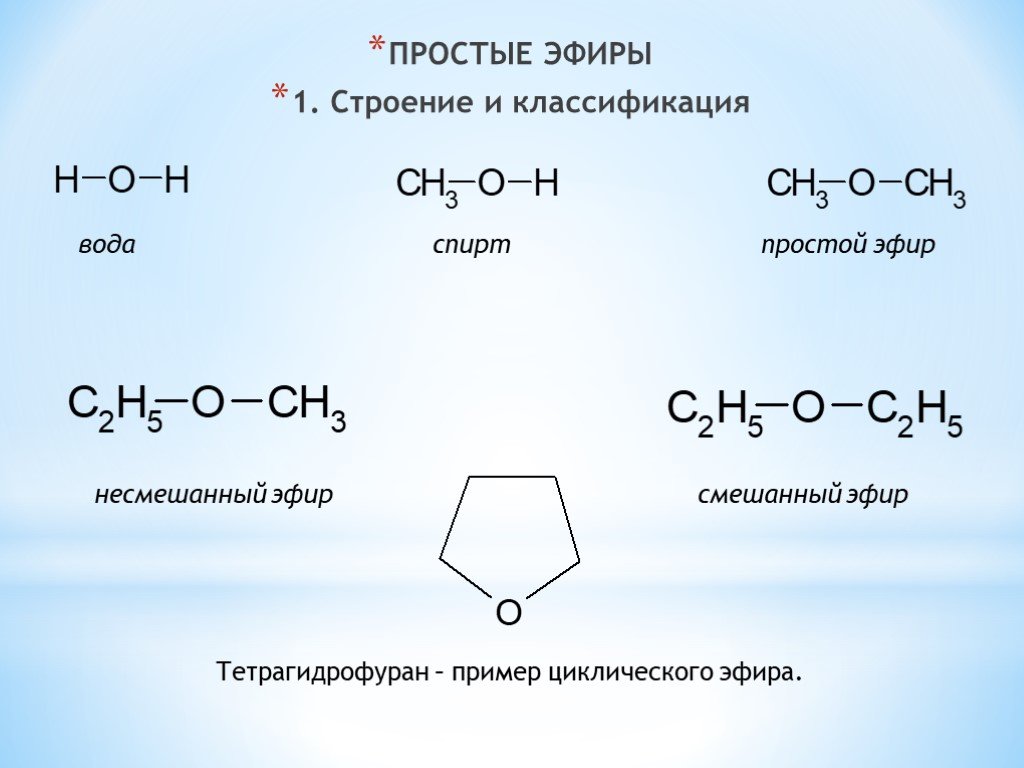
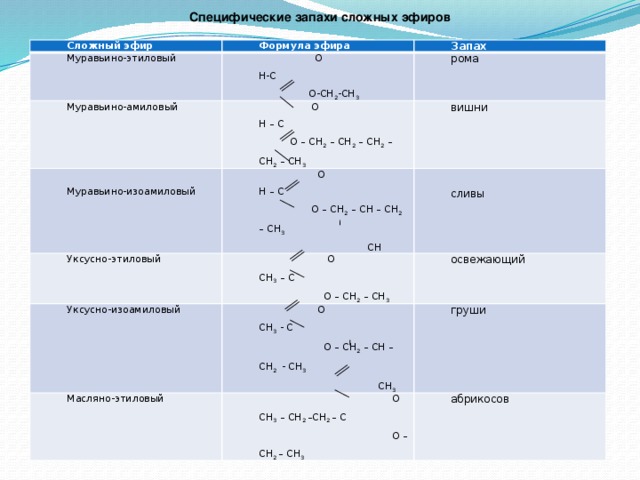
Сложные эфиры
–
это
соединения, содержащие карбоксильную
группу, связанную с двумя алкильными
радикалами.
Общая
формула сложных эфиров такая же, как у
карбоновых кислот: CnH2nO2
НОМЕНКЛАТУРА
СЛОЖНЫХ ЭФИРОВ.
Названия
сложных эфиров определяются названиями
кислоты и спирта,
из которых они образуются.
Формула | Полное | Другие |
СН3-С-ОСН3 ║ О | метиловый | метилацетат уксуснометиловый |
Н-С ║ О | этиловый | этилформиат |
С2Н5 ║ О | пропиловый | пропилпропаноат |
ПОЛУЧЕНИЕ
СЛОЖНЫХ ЭФИРОВ.
1)Cложные эфиры могут
быть получены при
взаимодействии
карбоновых кислот со спиртами (реакция
этерификации).
Катализаторами
являются минеральные кислоты.
2) Сложные
эфиры фенолов
нельзя получить с помощью этерификации,
для их получения используют реакцию
фенолята
с галогенангидридом кислоты:
С6Н5-О—Na+
+
C2H5–C=O
NaCl
+
C6H5–O—C=O
\
\
Cl
C2H5
фениловый
эфир пропановой
кислоты (фенилпропаноат)
Виды
изомерии сложных эфиров.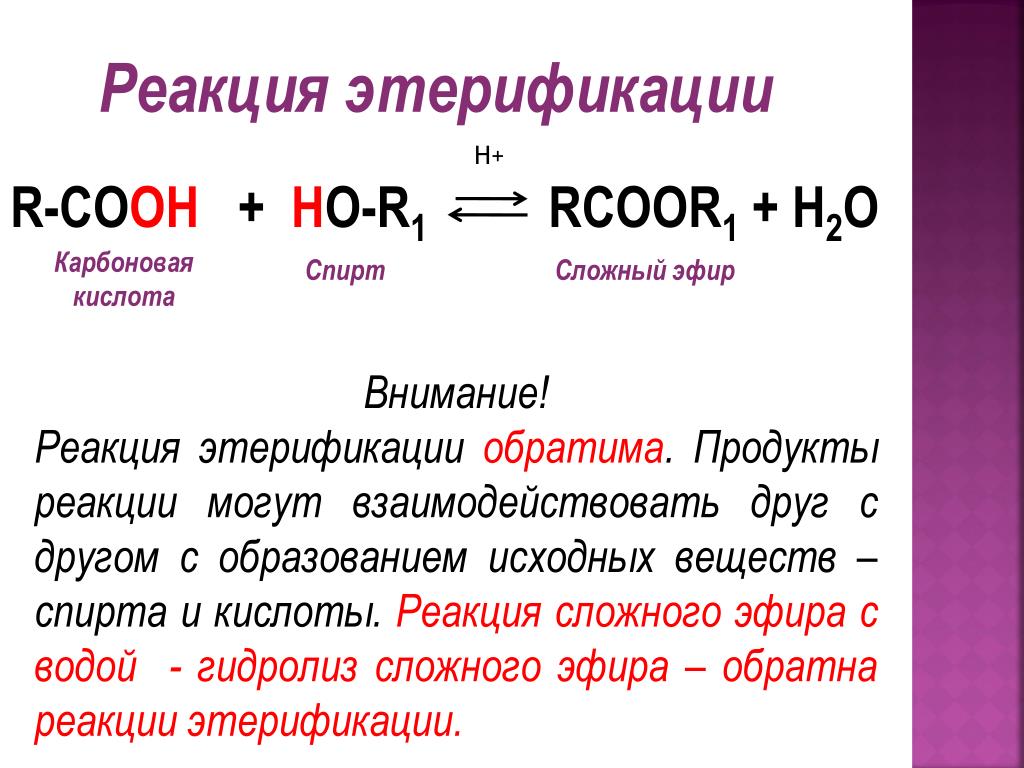
1.
Изомерия
углеродной
цепи начинается
по кислотному остатку с бутановой
кислоты, по спиртовому остатку — с
пропилового спирта, например, этилбутаноату
изомерны этилизобутаноат, пропилацетат
и изопропилацетат.
2.
Изомерия положения
сложноэфирной группировки
—СО—О—.
Этот вид изомерии начинается
со сложных
эфиров, в молекулах которых содержится
не менее 4 атомов углерода, например
этилацетат и метилпропионат.
3.
Межклассовая
изомерия
с карбоновыми кислотами.
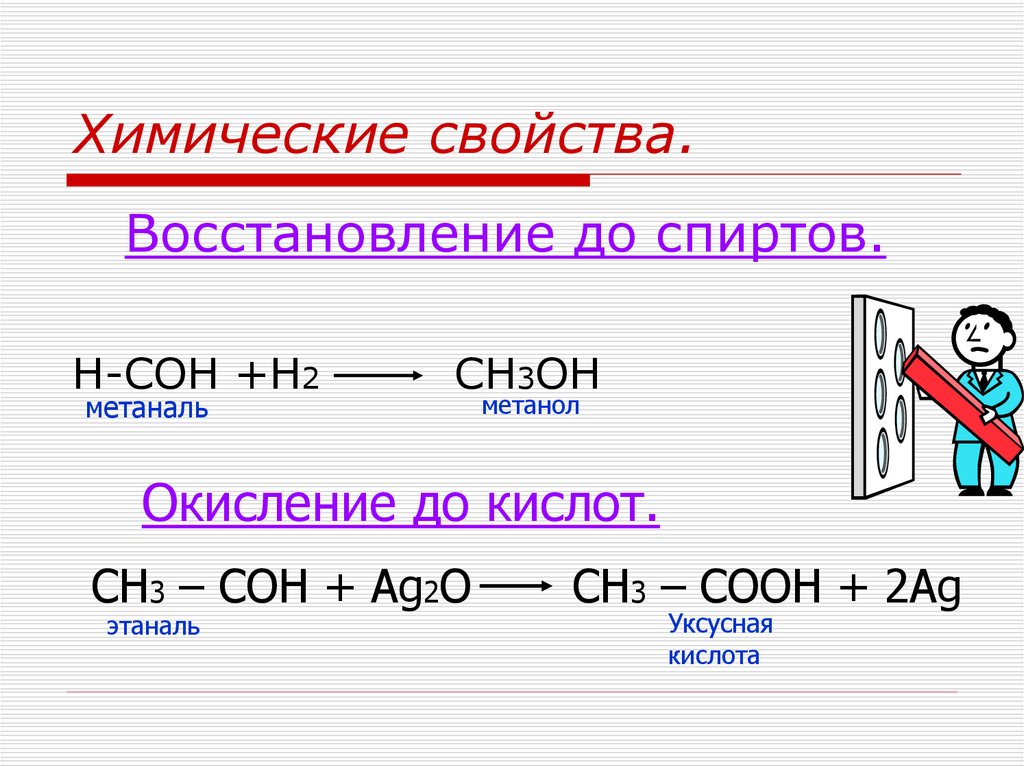
СВОЙСТВА
СЛОЖНЫХ ЭФИРОВ.
Реакция
этерификации обратима. Обратный процесс
– расщепление сложного эфира при
действии воды с образованием карбоновой
кислоты и спирта – называют гидролизом
сложного эфира.
Кислотный
гидролиз обратим:
Щелочной
гидролиз
протекает необратимо:
Эта
реакция называется омылением
сложного эфира.
2.
Реакция
восстановления.
Восстановление сложных эфиров водородом
приводит к образованию двух спиртов:
Спирты и эфиры | Химия: Atoms First
Цели обучения
К концу этого раздела вы сможете:
- Описывать структуру и свойства спиртов
- Описать строение и свойства эфиров
- Назовите и нарисуйте структуры для спиртов и эфиров
Спирты
Включение атома кислорода в углерод- и водородсодержащие молекулы приводит к новым функциональным группам и новым семействам соединений. Когда атом кислорода присоединен одинарными связями, молекула представляет собой либо спирт, либо эфир.
Спирты являются производными углеводородов, в которых атом водорода заменен группой –ОН. Хотя все спирты имеют одну или несколько гидроксильных (-OH) функциональных групп, они не ведут себя как основания, такие как NaOH и KOH. NaOH и KOH являются ионными соединениями, которые содержат ионы OH – . Спирты представляют собой ковалентные молекулы; группа –ОН в молекуле спирта связана с атомом углерода ковалентной связью.
Спирты представляют собой ковалентные молекулы; группа –ОН в молекуле спирта связана с атомом углерода ковалентной связью.
Этанол, CH 3 CH 2 OH, также называемый этиловым спиртом, является особенно важным спиртом для человека. Этанол — это спирт, вырабатываемый некоторыми видами дрожжей, который содержится в вине, пиве и дистиллированных напитках. Его долгое время готовили люди, используя метаболические усилия дрожжей для ферментации различных сахаров:
Большие количества этанола синтезируются реакцией присоединения воды к этилену с использованием кислоты в качестве катализатора:
Могут быть получены спирты, содержащие две или более гидроксильных групп. Примеры включают 1,2-этандиол (этиленгликоль, используемый в антифризах) и 1,2,3-пропантриол (глицерин, используемый в качестве растворителя для косметики и лекарств):
Наименование спиртов
Название спирта происходит от углеводород, из которого он был получен. Финал – е в названии углеводорода заменяется на -ол , а атом углерода, с которым связана группа –ОН, обозначается цифрой, стоящей перед названием.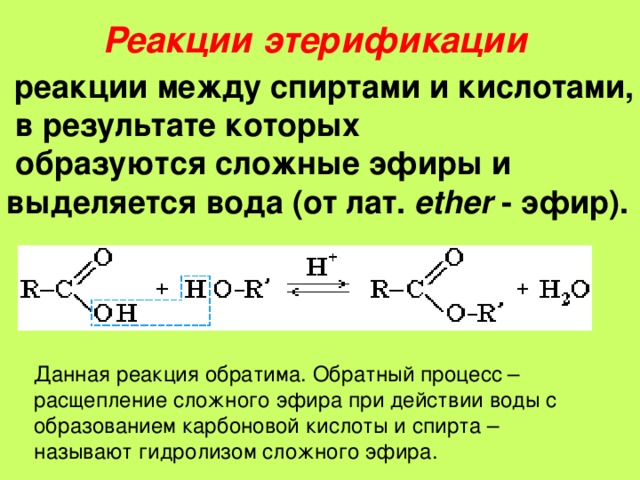
Пример 1. Именование спиртов
Рассмотрим следующий пример. Как это должно называться?
Показать ответ
Проверьте свои знания
Назовите следующую молекулу:
Показать ответ
Эфиры
Эфиры представляют собой соединения, содержащие функциональную группу –O–. У простых эфиров нет обозначенного суффикса, как у других типов молекул, которые мы назвали до сих пор. В системе IUPAC атом кислорода и меньшая углеродная ветвь называются алкокси-заместителем, а остальная часть молекулы — основной цепью, как в алканах. Как показано в следующем соединении, красные символы представляют меньшую алкильную группу и атом кислорода, который можно назвать «метокси». Более крупная углеродная ветвь будет этаном, что сделает молекулу метоксиэтаном. Многие эфиры называются общими именами вместо системных имен IUPAC. Для общих названий две ветви, связанные с атомом кислорода, называются отдельно, а за ними следует -эфир. Общее название соединения, показанного в Примере 2 – этилметиловый эфир:
Общее название соединения, показанного в Примере 2 – этилметиловый эфир:
Пример 2. Именование эфиров
Укажите IUPAC и общее название эфира, показанного здесь:
Показать ответ
Проверьте свои знания
Укажите IUPAC и общее название для показанного эфира:
Показать ответ
Эфиры могут быть получены из спиртов отщеплением молекулы воды от двух молекул спирта. Например, при обработке этанола ограниченным количеством серной кислоты и нагревании до 140 °С образуются диэтиловый эфир и вода:
В общей формуле простых эфиров R— O —R углеводородные группы (R) могут быть одинаковыми или разными. Диэтиловый эфир, наиболее широко используемое соединение этого класса, представляет собой бесцветную летучую жидкость, которая легко воспламеняется. Впервые он был использован в 1846 году в качестве анестетика, но в настоящее время его место в значительной степени заняли более совершенные анестетики. Диэтиловый эфир и другие простые эфиры в настоящее время используются главным образом в качестве растворителей камедей, жиров, восков и смол. Третичный -Бутилметиловый эфир, C 4 H 9 OCH 3 (сокращенно МТБЭ — части названий, выделенные курсивом, не учитываются при ранжировании групп в алфавитном порядке — поэтому бутил стоит перед метилом в обычном названии), используется в качестве присадки к бензину. МТБЭ принадлежит к группе химических веществ, известных как оксигенаты, из-за их способности повышать содержание кислорода в бензине.
Диэтиловый эфир и другие простые эфиры в настоящее время используются главным образом в качестве растворителей камедей, жиров, восков и смол. Третичный -Бутилметиловый эфир, C 4 H 9 OCH 3 (сокращенно МТБЭ — части названий, выделенные курсивом, не учитываются при ранжировании групп в алфавитном порядке — поэтому бутил стоит перед метилом в обычном названии), используется в качестве присадки к бензину. МТБЭ принадлежит к группе химических веществ, известных как оксигенаты, из-за их способности повышать содержание кислорода в бензине.
Хотите попрактиковаться в именовании эфиров? Этот краткий видеообзор подытоживает номенклатуру эфиров.
Углеводы и диабет
Углеводы — это большие биомолекулы, состоящие из углерода, водорода и кислорода. Пищевые формы углеводов — это продукты, богатые этими типами молекул, такие как макароны, хлеб и конфеты. Название «углевод» происходит от формулы молекул, которые можно описать общей формулой C m (H 2 O) n , что показывает, что они в некотором смысле являются «углеродом и водой» или «гидраты углерода». Во многих случаях m и n имеют одинаковое значение, но могут быть и разными. Меньшие углеводы обычно называют «сахарами». Биохимический термин для этой группы молекул — «сахарид» от греческого слова «сахар» (рис. 1). В зависимости от количества сахарных единиц, соединенных вместе, их можно классифицировать как моносахариды (одна сахарная единица), дисахариды (две сахарные единицы), олигосахариды (несколько сахаров) или полисахариды (полимерная версия сахаров — полимеры были описаны в раздел о вторичной переработке пластика ранее в этой главе). Научные названия сахаров можно узнать по суффиксу 9.0037 – ose в конце названия (например, фруктовый сахар представляет собой моносахарид, называемый «фруктозой», а молочный сахар — это дисахарид, называемый лактозой, состоящий из двух моносахаридов, глюкозы и галактозы, соединенных вместе).
Название «углевод» происходит от формулы молекул, которые можно описать общей формулой C m (H 2 O) n , что показывает, что они в некотором смысле являются «углеродом и водой» или «гидраты углерода». Во многих случаях m и n имеют одинаковое значение, но могут быть и разными. Меньшие углеводы обычно называют «сахарами». Биохимический термин для этой группы молекул — «сахарид» от греческого слова «сахар» (рис. 1). В зависимости от количества сахарных единиц, соединенных вместе, их можно классифицировать как моносахариды (одна сахарная единица), дисахариды (две сахарные единицы), олигосахариды (несколько сахаров) или полисахариды (полимерная версия сахаров — полимеры были описаны в раздел о вторичной переработке пластика ранее в этой главе). Научные названия сахаров можно узнать по суффиксу 9.0037 – ose в конце названия (например, фруктовый сахар представляет собой моносахарид, называемый «фруктозой», а молочный сахар — это дисахарид, называемый лактозой, состоящий из двух моносахаридов, глюкозы и галактозы, соединенных вместе). Сахара содержат некоторые функциональные группы, которые мы обсуждали: обратите внимание на спиртовые группы, присутствующие в структурах, и на то, как моносахаридные звенья связаны с образованием дисахарида путем образования эфира.
Сахара содержат некоторые функциональные группы, которые мы обсуждали: обратите внимание на спиртовые группы, присутствующие в структурах, и на то, как моносахаридные звенья связаны с образованием дисахарида путем образования эфира.
Рисунок 2. На иллюстрациях показаны молекулярные структуры фруктозы, пятиуглеродного моносахарида, и лактозы, дисахарида, состоящего из двух изомерных шестиуглеродных сахаров.
Организмы используют углеводы для различных функций. Углеводы могут накапливать энергию, например полисахариды гликоген у животных или крахмал у растений. Они также обеспечивают структурную поддержку, такую как полисахарид целлюлозы в растениях и модифицированный полисахарид хитин в грибах и животных. Сахара рибоза и дезоксирибоза являются компонентами остова РНК и ДНК соответственно. Другие сахара играют ключевую роль в функционировании иммунной системы, в межклеточном распознавании и во многих других биологических функциях.
Диабет — это группа метаболических заболеваний, при которых у человека наблюдается высокая концентрация сахара в крови (Рисунок 2).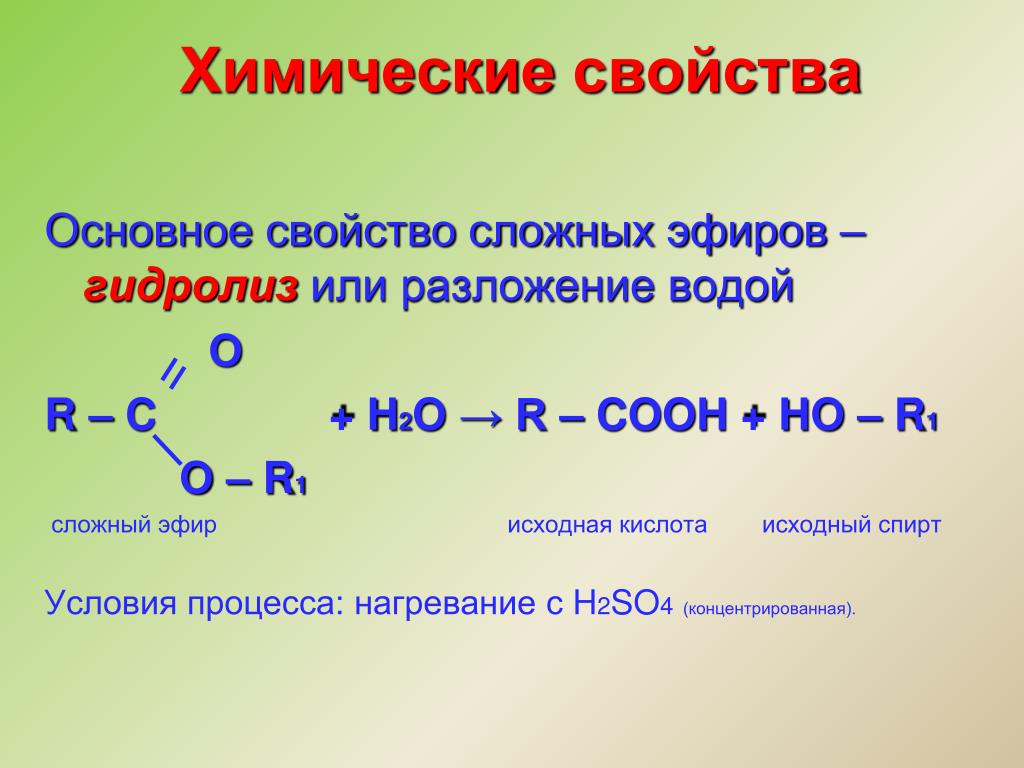 Диабет может быть вызван недостаточной выработкой инсулина поджелудочной железой или клетками организма, которые не реагируют должным образом на вырабатываемый инсулин. У здорового человека инсулин вырабатывается, когда он необходим, и функционирует для транспортировки глюкозы из крови в клетки, где она может использоваться для получения энергии. Долгосрочные осложнения диабета могут включать потерю зрения, болезни сердца и почечную недостаточность.
Диабет может быть вызван недостаточной выработкой инсулина поджелудочной железой или клетками организма, которые не реагируют должным образом на вырабатываемый инсулин. У здорового человека инсулин вырабатывается, когда он необходим, и функционирует для транспортировки глюкозы из крови в клетки, где она может использоваться для получения энергии. Долгосрочные осложнения диабета могут включать потерю зрения, болезни сердца и почечную недостаточность.
В 2013 г. было подсчитано, что приблизительно 3,3% населения мира (~380 миллионов человек) страдали диабетом, что ежегодно приводило к более чем миллиону смертей. Профилактика включает в себя здоровое питание, много физических упражнений и поддержание нормальной массы тела. Лечение включает в себя все эти методы образа жизни и может потребовать инъекций инсулина.
Рисунок 2. Сахарный диабет — это заболевание, характеризующееся высокими концентрациями глюкозы в крови. Лечение диабета включает в себя изменение образа жизни, контроль уровня сахара в крови, а иногда и инъекции инсулина.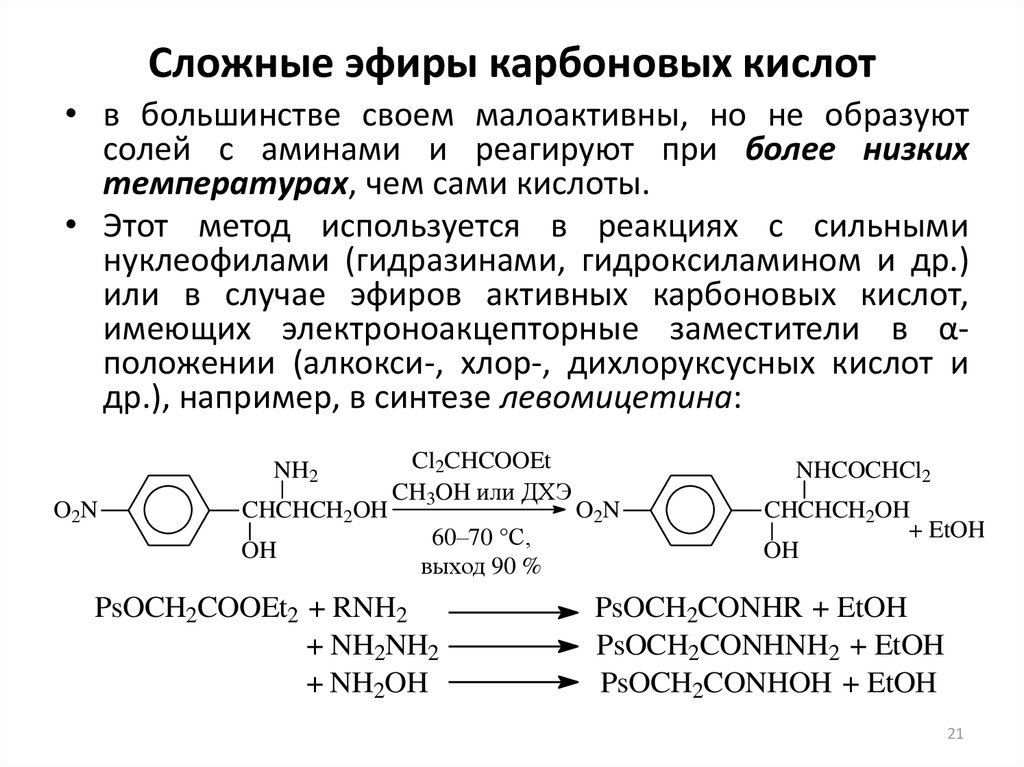 (кредит: «Blausen Medical Communications»/Википедия)
(кредит: «Blausen Medical Communications»/Википедия)
Основные понятия и резюме
Многие органические соединения, не являющиеся углеводородами, можно рассматривать как производные углеводородов. Углеводородное производное может быть образовано заменой одного или нескольких атомов водорода углеводорода функциональной группой, которая содержит по меньшей мере один атом элемента, отличного от углерода или водорода. Свойства производных углеводородов во многом определяются функциональной группой. Группа –ОН является функциональной группой спирта. Группа –R–O–R– является функциональной группой эфира.
Упражнения
- Почему соединения гексана, гексанола и гексена имеют такие похожие названия?
- Напишите сокращенные формулы и укажите названия IUPAC для следующих соединений:
- спирт этиловый (в напитках)
- спирт метиловый (используется как растворитель, например, в шеллаке)
- этиленгликоль (антифриз)
- изопропиловый спирт, CH 3 CH(OH)CH 3 , используемый в медицинском спирте)
- глицерин
- Дайте полное название IUPAC для каждого из следующих соединений:
- Дайте полное название IUPAC и общепринятое название для каждого из следующих соединений:
- Напишите конденсированные структуры обоих изомеров по формуле C 2 H 6 O.
 Обозначьте функциональную группу каждого изомера.
Обозначьте функциональную группу каждого изомера. - Напишите сокращенные структуры всех изомеров с помощью формулы C 2 Н 6 О 2 . Обозначьте функциональную группу (или группы) каждого изомера.
- Нарисуйте сокращенные формулы для каждого из следующих соединений:
- дипропиловый эфир
- 2,2-диметил-3-гексанол
- 2-этоксибутан
- МТБЭ, метил трет -бутиловый эфир, CH 3 OC(CH 3 ) 3 , используется в качестве источника кислорода в насыщенных кислородом бензинах. МТБЭ получают путем взаимодействия 2-метилпропена с метанолом.
- Используя структуры Льюиса, напишите химическое уравнение реакции.
- Какой объем метанола плотностью 0,7915 г/мл требуется для производства ровно 1000 кг МТБЭ при условии выхода 100%?
- Напишите два полных сбалансированных уравнения для каждой из следующих реакций, одно с использованием сокращенных формул, а другое с использованием структур Льюиса.

- пропанол превращается в дипропиловый эфир
- обрабатывают водой в разбавленной кислоте.
Пропен
- Напишите два полных сбалансированных уравнения для каждой из следующих реакций, одно с использованием сокращенных формул, а другое с использованием структур Льюиса.
- 2-бутен обрабатывают водой в разбавленной кислоте
- обезвоживается с получением этилена
Этанол
.
Показать выбранные ответы
Глоссарий
спирт: органическое соединение с гидроксильной группой (–ОН), связанной с атомом углерода
эфир: органическое соединение с атомом кислорода, связанным с двумя атомами углерода
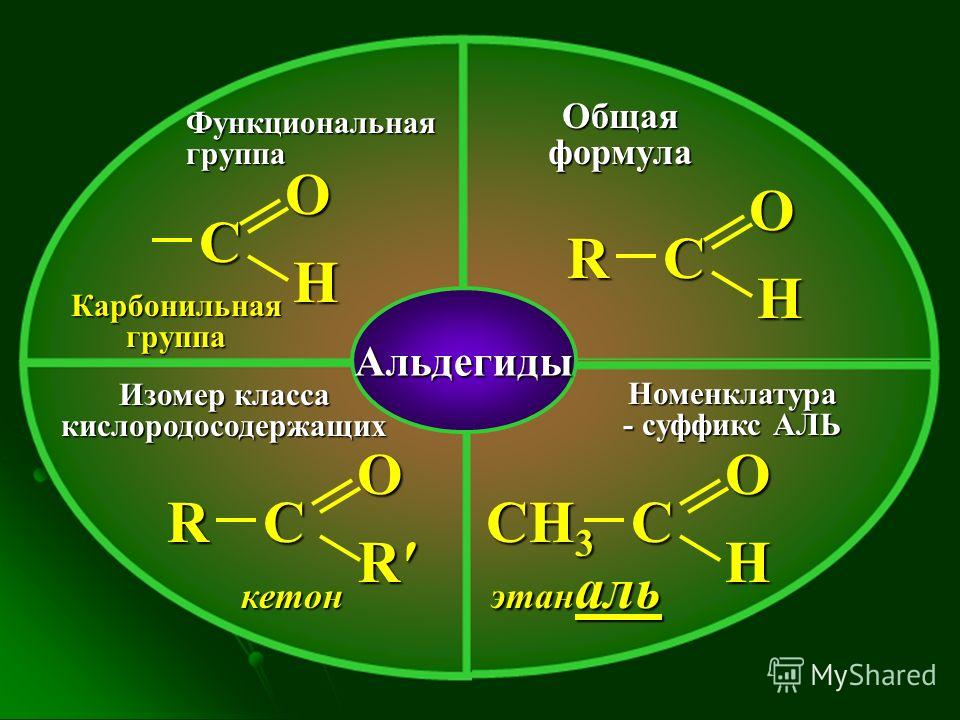
Тип, номенклатура, формула, реакция, свойства, применение
Простые эфиры представляют собой производные углеводородов, в которых атом водорода заменен алкоксигруппой (COR) или арилокси (-OAr) группой. В этой статье мы изучим химию эфиров, типы фенолов, номенклатуру эфиров ИЮПАК, методы получения, физические и химические свойства с реакциями, формулами, примерами и использованием.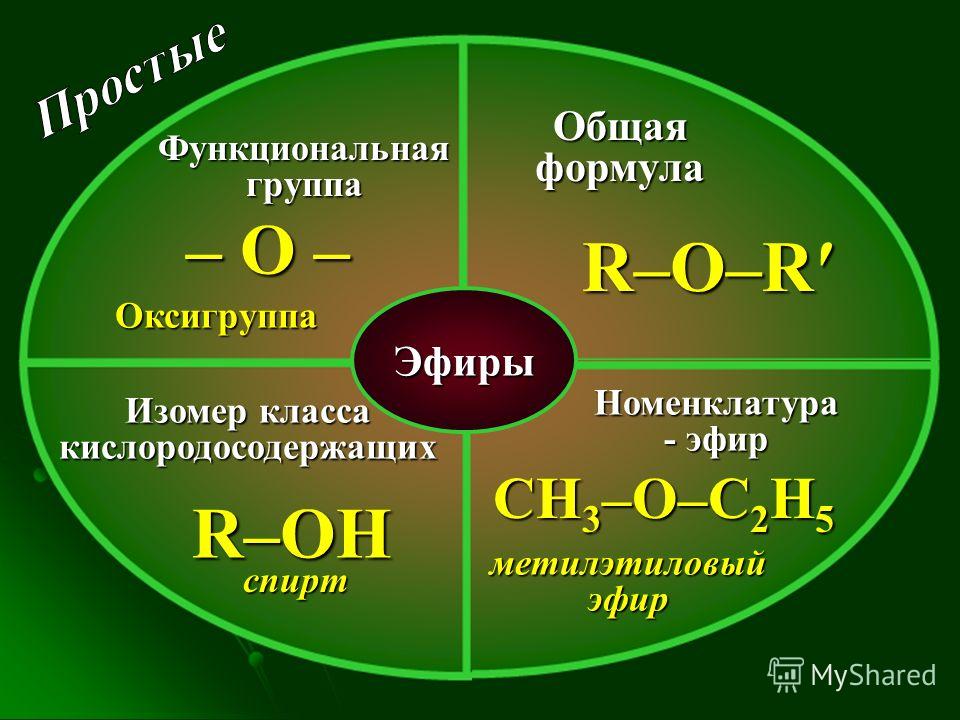
Что такое эфиры?
В органической химии простыми эфирами называются производные углеводородов, в которых атом водорода заменен алкоксигруппой (-OR) или арилоксигруппой (-Ar).
Простые эфиры получают из спиртов межмолекулярной дегидратацией и из алкилгалогенидов синтезом Вильямсона. Температуры кипения простых эфиров несколько выше, чем у алканов, но значительно ниже, чем у спиртов сопоставимых масс. Подобно спиртам, простые эфиры могут образовывать водородные связи с молекулами воды.
Следовательно, эфиры смешиваются с водой. Эфиры расщепляются сильными кислотами HI или HBr, но HCl эфиры не расщепляет.
Это связано с тем, что HI или HBr достаточно кислые, чтобы протонировать эфиры, в то время как иодид- и бромид-ионы являются хорошими нуклеофилами для замещения. Алкилариловые эфиры расщепляются по более слабым связям OR с образованием фенолов и алкилиодидов.
Алкилариловые эфиры подвергаются электрофильному замещению, алкоксигруппа направляет электрофил в орто- и пара-положения.
Простые эфиры также можно рассматривать как соединения, образованные заменой атома водорода
гидроксильной группы спирта или фенола на алкильную или арильную группу. Эфиры представляют собой органические производные воды, имеющие две алкильные или арильные группы, связанные с атомами кислорода. Эфиры также можно рассматривать как алкилоксиды или арилоксиды, \(R_2O\) или \(Ar_2O\)
Функциональной группой простых эфиров является эфирная связь.
Общая формула алифатических эфиров \(C_nH_{2n+2}O\), такая же, как и у одноатомных спиртов.
Таким образом, алифатические эфиры изомерны с одноатомными спиртами. например \(C_2H_5-OH\) и \(CH_3-O-CH_3\) являются изомерами функциональных групп.
Прочитайте об аминах здесь
Классификация эфиров
Эфиры подразделяются на две группы:
Простые или симметричные эфиры
Простые эфиры, в которых и алкильные, и арильные группы, присоединенные к атому кислорода, одинаковы, называются простыми эфирами.
Пример:
- \(CH_3-O-CH_3\) диметиловый эфир
- \(C_6H_5-O-C_6H_5\) дифениловый эфир
Смешанные или несимметричные 4 алкиловые эфиры3 900, 900 или арильные группы, присоединенные к атому кислорода, различны, называются смешанными эфирами.
Пример:
- \(CH_3-O-C_2H_5\) этилметиловый эфир
- \(C_2H_5-O-C_6H_5\) этилфениловый эфир
Номенклатура эфиров
Номенклатура спиртов составляется двумя способами: диариловые эфиры». Общее название смешанных эфиров
получают путем ввода названий алкильных или арильных групп в виде отдельных слов в алфавитном порядке, за которыми следует слово «эфир».
Система ИЮПАК
Согласно системе ИЮПАК, простые эфиры считаются производными углеводородов в
, в котором атом водорода заменен группой -OR или -OAr. В смешанных эфирах алкильная группа, содержащая более крупную углеродную цепь, считается исходным алканом.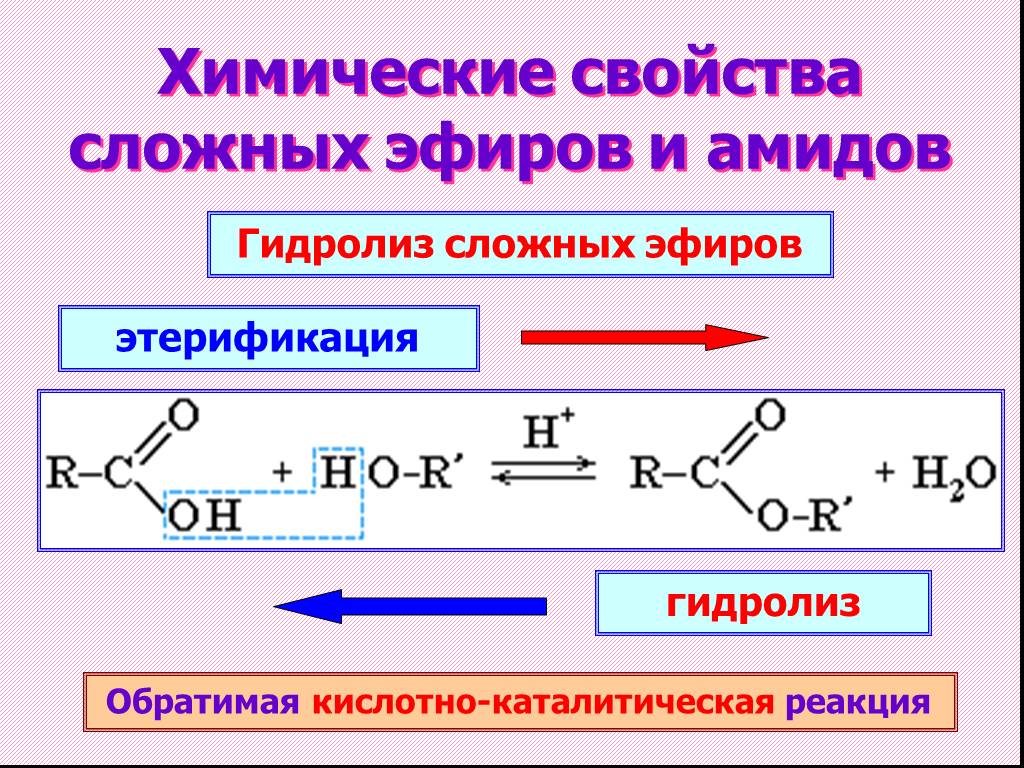
Структура функциональной группы
Как и спирты, простые эфиры имеют почти ту же тетраэдрическую геометрию, что и вода. Атом кислорода находится в sp3-гибридизации из-за отталкивающего взаимодействия между двумя более объемными алкильными группами, валентный угол C-O-C немного больше, чем тетраэдрический угол.
Метамерия
Простые эфиры, имеющие одинаковую молекулярную формулу, но разные алкильные группы, присоединенные по обе стороны от атома кислорода, называются метамерами друг друга. Это явление называется метамерией. Метамеры представляют собой либо изомеры цепи, либо изомеры положения с одной и той же функциональной группой и имеют разные алкильные группы, присоединенные к гетероатому; в данном случае это кислород.
Пример:
Следующие метамеры могут быть представлены формулой \(C_4H_{10}O\)
Изомерия
Простые эфиры проявляют следующие типы изомерии:
Цепная изомерия
Простые эфиры имеют одну и ту же алкильную группу по обе стороны от атома кислорода, но различное расположение углеродной цепи внутри алкильной группы называют цепными изомерами.
Функциональная изомерия
Простой эфир и одноатомный спирт, содержащие одинаковое число атомов углерода, являются функциональными изомерами.
Пример:
Диметиловый эфир и этиловый спирт являются функциональными изомерами.
Узнайте о числах окисления здесь.
Методы получения
Эфиры могут быть получены следующими способами:
Из спиртов (межмолекулярная дегидратация)
При перегонке избытка этилового спирта с концентрированной серной кислотой при 413К получается диэтиловый эфир.
Процедура эксперимента следующая.
Первые равные объемы этилового спирта и конц. серную кислоту помещают в перегонную колбу. Этиловый спирт реагирует с конц. серной кислоты с получением сернокислого этилового спирта.
Затем в колбу для перегонки добавляют избыток этилового спирта. Этилгидросульфат реагирует с добавленным этиловым спиртом с образованием диэтилового эфира.
Полученный эфир перегоняется. Серная кислота, регенерированная на второй стадии, повторно используется на первой стадии. Таким образом, небольшое количество серной кислоты превращает большое количество этилового спирта в диэтиловый эфир, и процесс становится непрерывным. Поэтому он называется непрерывным процессом этерификации.
Серная кислота, регенерированная на второй стадии, повторно используется на первой стадии. Таким образом, небольшое количество серной кислоты превращает большое количество этилового спирта в диэтиловый эфир, и процесс становится непрерывным. Поэтому он называется непрерывным процессом этерификации.
Ограничения
- При кислотной дегидратации спиртов конкурируют две реакции. Одна реакция представляет собой отщепление с образованием алкенов и другое замещение с образованием простых эфиров. При повышении температуры температура становится более благоприятной для элиминации (453К и выше). Замена предпочтительна при 413 К и ниже.
- Метод подходит только для получения эфиров из первичных спиртов. Однако дегидратация вторичных и третичных спиртов из алкенов вместо простых эфиров по мере устранения конкурирует с замещением.
- Этим методом удобно получать простые эфиры. Бимолекулярная дегидратация спиртов не подходит для получения смешанных эфиров.
 Если используется смесь двух разных спиртов, получается смесь трех разных эфиров, которую трудно разделить.
Если используется смесь двух разных спиртов, получается смесь трех разных эфиров, которую трудно разделить.
\(R-OH+R’-OH{\overset{conc.H_2SO_4}{\longrightarrow}}R-O-R+R-O-R’+R-O-R’\)
Из алкилгалогенидов (Williamson Синтез)
Этим методом можно получать как простые, так и смешанные эфиры. При нагревании алкилгалогенида со спиртовым алкоксидом натрия или калия он дает соответствующие эфиры.
При нагревании йодистого метила со спиртовым метоксидом натрия получается диметиловый эфир.
Этим методом фенолы также превращаются в простые эфиры.
Ограничения
Для получения несимметричных эфиров необходим правильный выбор реагентов. Поскольку первичные алкилгалогениды более восприимчивы к реакции SN2, лучший выход несимметричного эфира получается, когда алкилгалогенид является первичным, а алкоксид — третичным.
Пример: трет-бутилэтиловый эфир получают нагреванием бромистого этила с трет-бутоксидом натрия.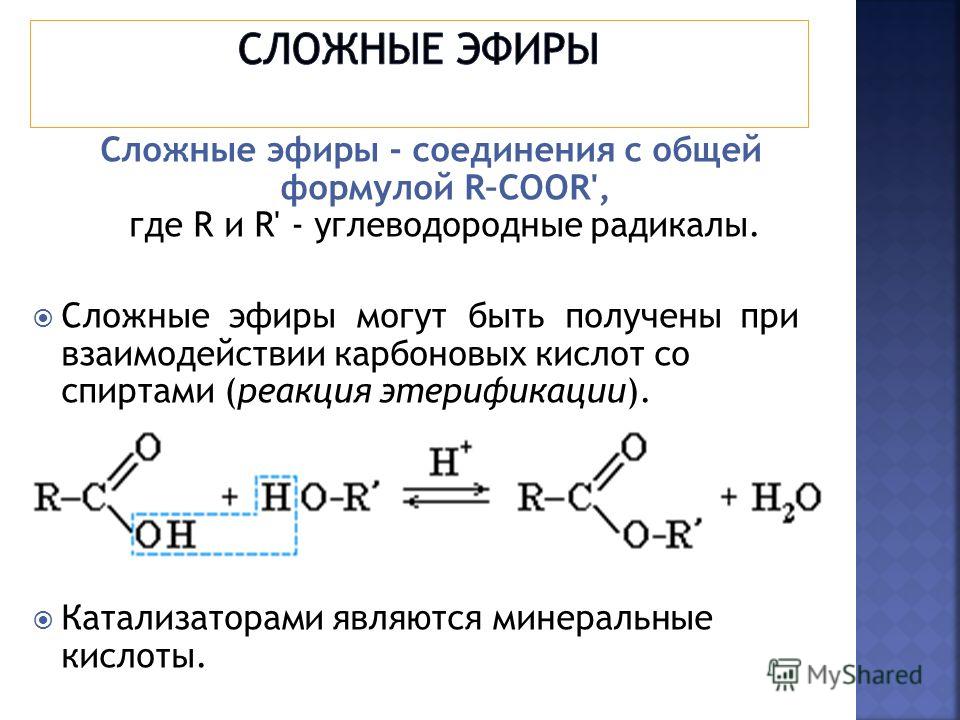
Однако, когда алкилгалогенид является вторичным или третичным, нуклеофильная атака на атом \(\альфа-углерод\) стерически затруднена (эффект краудинга). Кроме того, алкоксиды являются более сильными основаниями, и атаковать \(\бета-водород\) легче, следовательно, преобладает \(\бета-элиминирование\).
Пример: При нагревании трет-бутилбромида с этоксидом натрия получается изобутилен.
Из спиртов и диазометана
При нагревании спирта с диазометаном в присутствии катализатора борфтористоводородной кислоты образуется эфир.
\(R-OH+CH_2N_2\longrightarrow}R-O-CH_3+N_2\uparrow\)
Этим методом удобно получать метиловые эфиры, так как побочный азотный газ выделяется в воздух. В этой реакции в спирт вводится метильная группа; поэтому это называется метилированием спирта
Метиловый спирт реагирует с диазометаном в присутствии катализатора фторборной кислоты с образованием диметилового эфира.
Ограничение
- Этим методом получают только метиловые эфиры.

Физические свойства эфиров
Валентный угол C-O-C в эфире не равен 180°, дипольные моменты двух связей C-O не компенсируют друг друга, следовательно, эфиры имеют небольшой суммарный дипольный момент. Температуры кипения простых эфиров несколько выше, чем у алканов, но значительно ниже, чем у спиртов сопоставимых масс. Это связано с тем, что диполь-дипольные силы притяжения в эфирах вносят незначительный вклад, а в спиртах присутствует водородная связь.
Как и спирты, простые эфиры могут образовывать водородную связь с молекулами воды. Следовательно, эфиры смешиваются с водой. Например, и диэтиловый эфир, и н-бутиловый спирт смешиваются примерно в одинаковой степени, примерно 8 г на 100 г воды.
Химические свойства простых эфиров
Простые эфиры являются относительно инертными соединениями, поскольку связь C-O-C достаточно стабильна. В обычных условиях на них не действуют разбавленные кислоты, основания и большинство окислителей и восстановителей.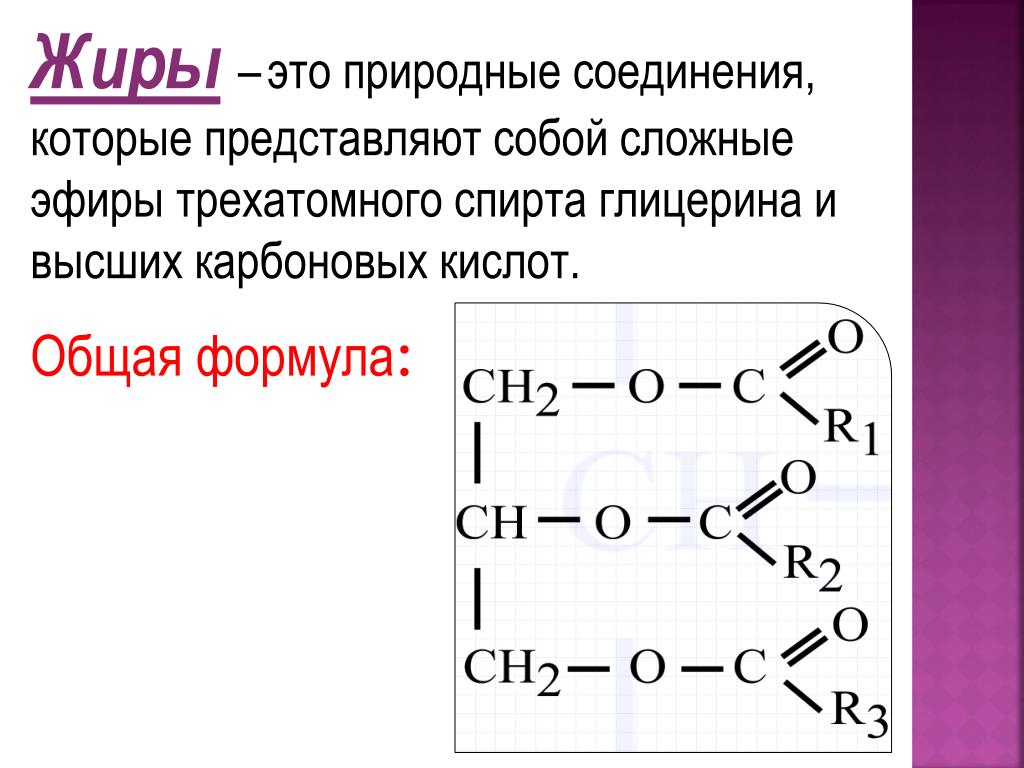
Действие галогеноводородов
В этих реакциях разрываются связи С-О.
Эфиры расщепляются сильными кислотами HI или HBr, но HCl не расщепляет эфиры. Это связано с тем, что HI или HBO достаточно кислые, чтобы протонировать эфиры, в то время как иодид- и бромид-ионы являются хорошими нуклеофилами для замещения.
Эфиры нагревают с избытком концентрированного галогеноводорода с получением алкилгалогенидов. Порядок реакционной способности галогеноводородов: HI > HBr > HCl.
- На холоду простой эфир дает одну молекулу алкилгалогенида и одну молекулу спирта, а при нагревании дает две молекулы алкилгалогенида.
- На холоду смешанный эфир обычно дает низший алкилйодид и высший спирт, а при нагревании дает два разных алкилгалогенида.
- Однако, если одна из алкильных групп является третичной, то образуются третичный алкилгалогенид и низший спирт.
Алкилариловые эфиры расщепляются по более слабым связям OR с образованием фенолов и алкилиодидов.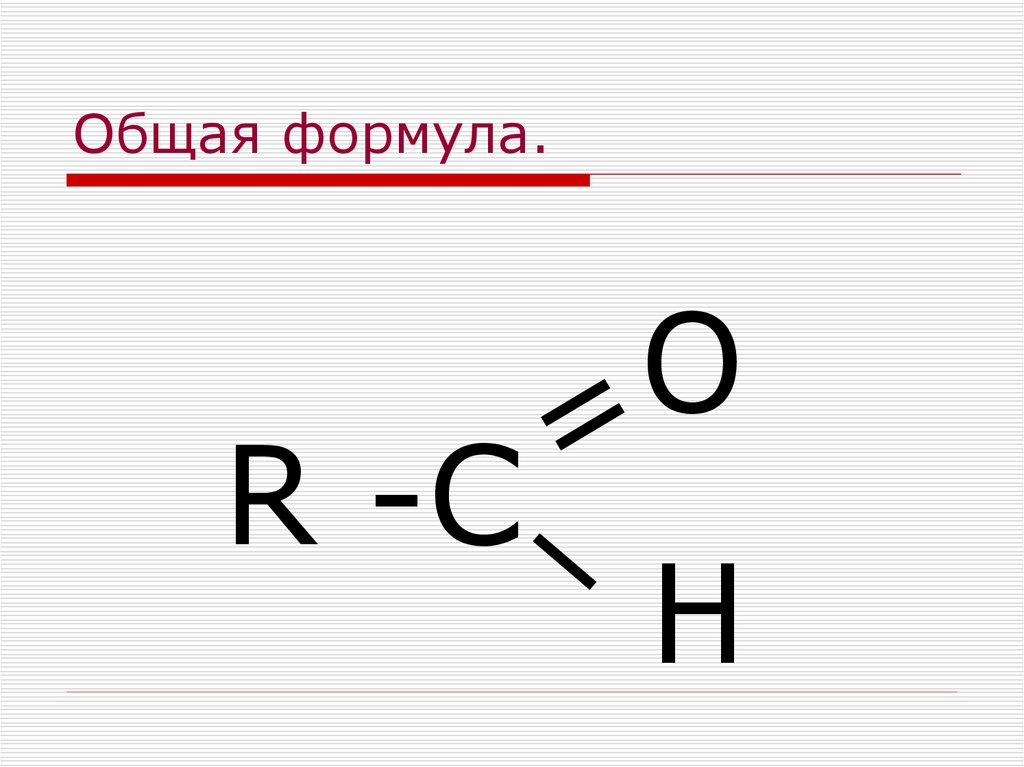 Связь Ar-O прочнее, поскольку атом углерода фенильной группы находится в состоянии sp2-гибридизации и имеет характер частичной двойной связи. Фенол больше не реагирует с HI, так как группа -ОН присоединена к sp-гибридизированному атому углерода и не может быть замещена нуклеофилом.
Связь Ar-O прочнее, поскольку атом углерода фенильной группы находится в состоянии sp2-гибридизации и имеет характер частичной двойной связи. Фенол больше не реагирует с HI, так как группа -ОН присоединена к sp-гибридизированному атому углерода и не может быть замещена нуклеофилом.
Гидролиз/действие разбавленной серной кислоты (образование спиртов)
Простые эфиры при нагревании с разбавленной серной кислотой под давлением дают спирт.
Смешанные эфиры в аналогичных условиях дают смесь двух разных спиртов.
Электрофильное замещение
Алкоксигруппа (-OR) в ароматических эфирах является орто-, пара-направленной и активирует ароматическое кольцо в сторону электрофильного замещения.
Галогенирование
Анизол подвергается бромированию бромом в уксусной кислоте даже в отсутствие FeBr_3 в качестве катализатора. Это связано с активацией бензольного кольца метоксигруппой.
Friedel – Crafts Reaction
Алкильные и ацильные группы вводят в орто- и пара-положениях анизола при реакции с алкилгалогенидом и ацилхлоридом соответственно в присутствии безводного хлорида алюминия (кислоты Льюиса) в качестве катализатора.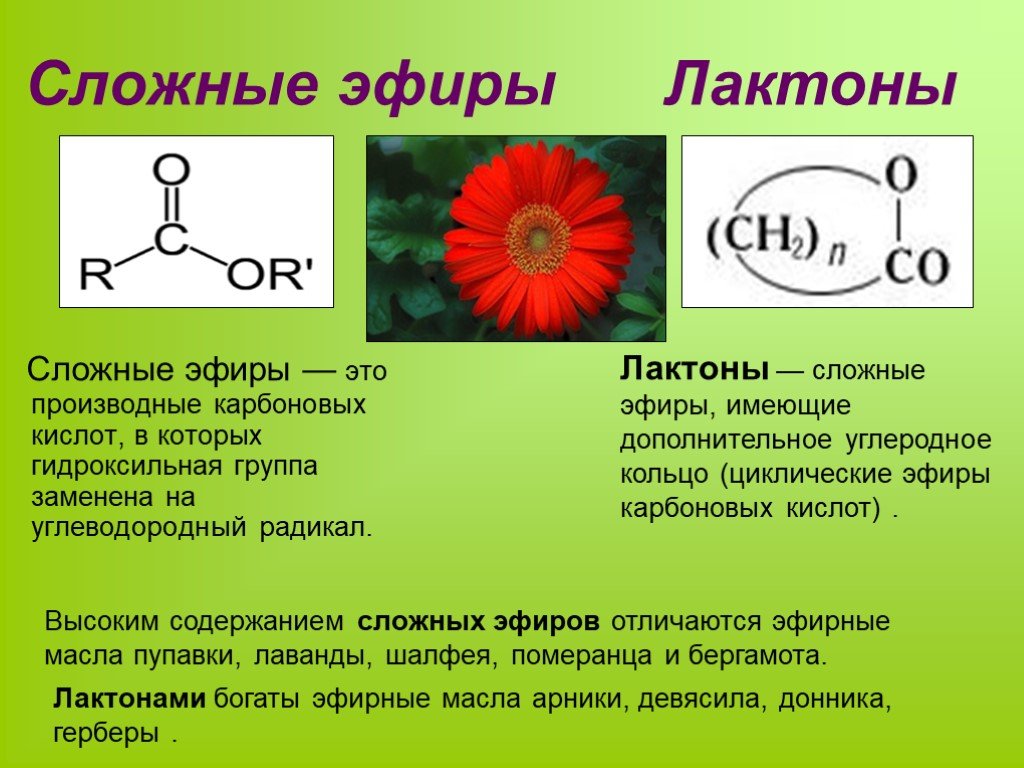
Нитрование
Анизол реагирует с нитрующей смесью с образованием смеси орто- и пара-нитропроизводных.
Использование эфиров
Эфиры используются как:
- Эфиры химически инертны и поэтому часто используются в качестве растворителей во многих химических реакциях.
- Наиболее распространенный член семейства эфиров, диэтиловый эфир, использовался в течение многих лет в качестве хирургического анестетика и в настоящее время заменен
- более безопасными негорючими альтернативами. Анизол, приятно пахнущий ароматический эфир, используется в парфюмерии.
Диэтиловый эфир используется как
- Диэтиловый эфир используется как промышленный растворитель для масел, жиров, камеди, смолы и т. д.
- Он используется в качестве растворителя в реакции реактива Гриньяра.
- Используется в качестве хладагента.
- Смесь диэтилового эфира и этилового спирта, известная как Натали, используется в качестве топлива (заменитель бензина).

- Диэтиловый эфир был намного более безопасным анестетиком, чем хлороформ, поскольку он менее токсичен, чем хлороформ. Эфир лучше растворяется в жирных кислотах по сравнению с водой и, следовательно, быстро воздействует на центральную нервную систему. Поскольку он летучий, его легко администрировать. С 1842 года он использовался в качестве хирургического анестетика более ста лет, а также вызывает рвоту после прихода в сознание. Он легко воспламеняется. Несколько других соединений заменили эфир в качестве анестетика. В настоящее время используются такие соединения, как закись азота и галотан, поскольку они легче переносятся.
Краун-эфиры
Чарльз Дж. Педерсон открыл макроциклические полиэфиры, которые представляют собой органические соединения с молекулами, содержащими большие кольца из атомов углерода и кислорода, называемые краун-эфирами. Краун-эфиры называются n-краун-m, где n — общее число атомов углерода и кислорода, а m — число атомов кислорода в кольце. Первым синтезированным краун-эфиром было соединение 18-краун-6-эфир, структура которого ( 0 = атом кислорода и • = \(-CH_2-\) группа.) показана на рисунке. 9+)\). Стабильность этих комплексов зависит от размера иона относительно имеющейся полости в кольце конкретного краун-эфира.
Первым синтезированным краун-эфиром было соединение 18-краун-6-эфир, структура которого ( 0 = атом кислорода и • = \(-CH_2-\) группа.) показана на рисунке. 9+)\). Стабильность этих комплексов зависит от размера иона относительно имеющейся полости в кольце конкретного краун-эфира.
Использование краун-эфиров
Краун-эфиры можно использовать для повышения растворимости ионных солей в неполярных растворителях. Они также действуют как катализаторы в некоторых реакциях с участием органических солей, образуя комплексы с положительным катионом металла и тем самым увеличивая его отделение от органического аниона. Некоторые из применений краун-эфиров зависят от селективности по отношению к анионам определенного размера. Таким образом, их можно использовать для извлечения определенных ионов из смесей и обогащения смесей изотопов. Их интересные свойства находят большое количество инновационных применений. Эта работа была удостоена Нобелевской премии по химии. Краун-эфиры также используются для удаления радиоактивных элементов из радиоактивных отходов. Специализированные производные 18 – краун 6 используются для извлечения цезия и стронция.
Специализированные производные 18 – краун 6 используются для извлечения цезия и стронция.
Итак, все дело в эфирах. Попрактикуйтесь в том же в нашем бесплатном приложении Testbook. Скачать сейчас!
Часто задаваемые вопросы об эфирах
В.1 Что является примером эфира?
Ans.1 Общая формула алифатических эфиров \(C_nH_{2n+2}O\), такая же, как и у одноатомных спиртов. Пример: диметиловый эфир, этилметиловый эфир, диэтиловый эфир.
Q.2 Каковы свойства эфиров?
Ans.2 Валентный угол C-O-C в эфире не равен 180°, дипольные моменты двух связей C-O не компенсируют друг друга, следовательно, эфиры имеют небольшой суммарный дипольный момент. Температуры кипения простых эфиров несколько выше, чем у алканов, но значительно ниже, чем у спиртов сопоставимых масс. Это связано с тем, что диполь-дипольные силы притяжения в эфирах вносят незначительный вклад, а в спиртах присутствует водородная связь.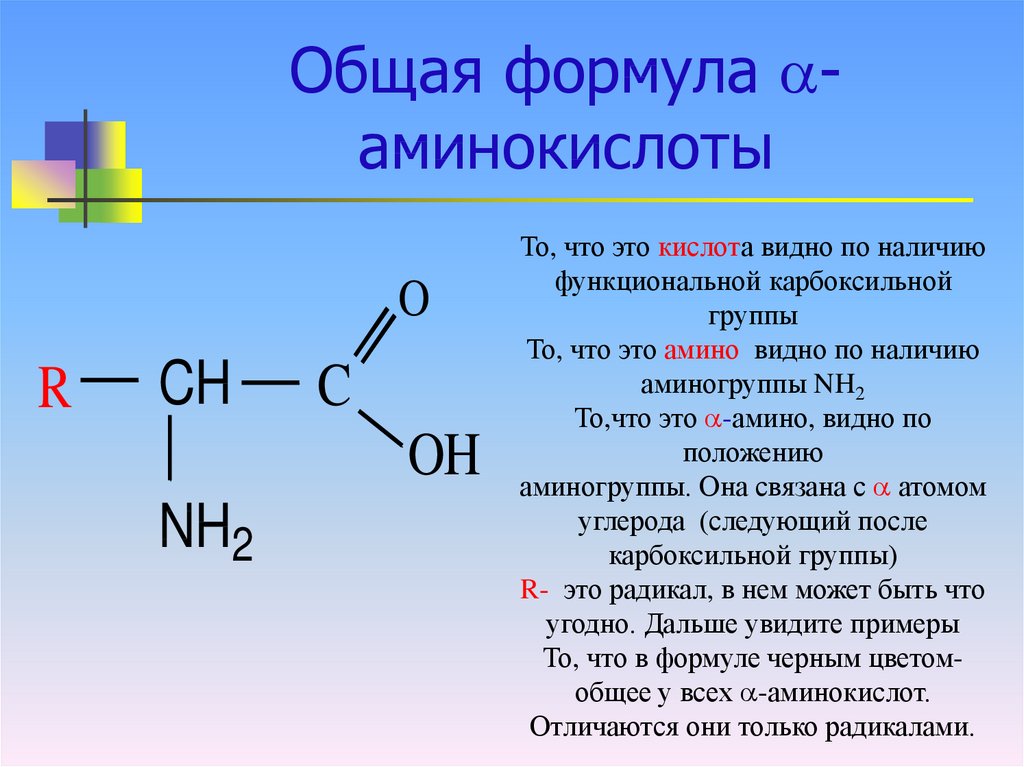 Как и спирты, простые эфиры могут образовывать водородную связь с молекулами воды. Следовательно, эфиры смешиваются с водой.
Как и спирты, простые эфиры могут образовывать водородную связь с молекулами воды. Следовательно, эфиры смешиваются с водой.
Q.3 Что такое эфиры и как они классифицируются?
Ans.3 Простые эфиры представляют собой производные углеводородов, в которых атом водорода заменен алкокси (-OR) или арилокси (- Ar) группой. Эфиры делятся на две группы:
В.4 Является ли эфир кислотой?
Ans.4 Эфиры не являются кислотными и обычно не реагируют с основаниями. Простые или симметричные эфиры: простые эфиры, в которых алкильные или арильные группы, присоединенные к атому кислорода, одинаковы, называются простыми. эфиры. Пример: диметиловый эфир, дифениловый эфир Смешанные или несимметричные эфиры: Эфиры, в которых две алкильные или арильные группы, присоединенные к атому кислорода, различны, называются смешанными эфирами. Пример: этилметиловый эфир, этилфениловый эфир
В.5 Где можно найти эфиры?
Ans.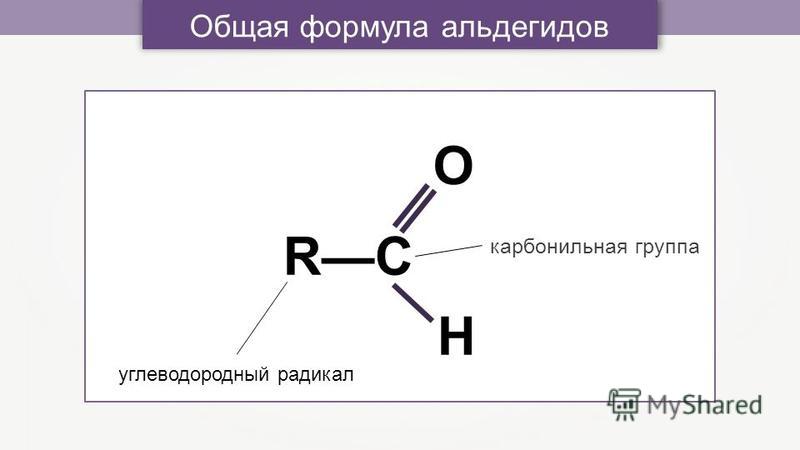


 Материал Владимира КОРНИЛОВА.
Материал Владимира КОРНИЛОВА.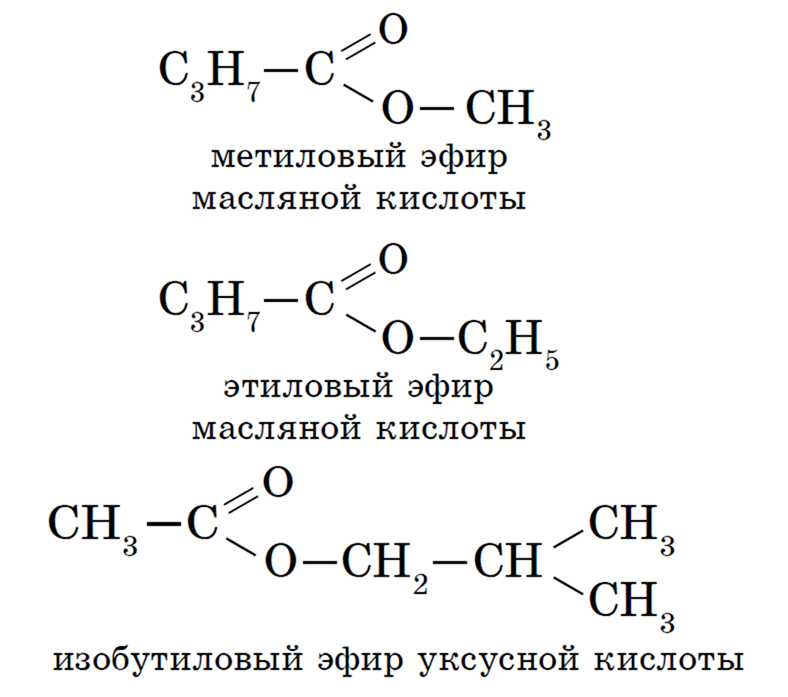
 Обозначьте функциональную группу каждого изомера.
Обозначьте функциональную группу каждого изомера.
 Если используется смесь двух разных спиртов, получается смесь трех разных эфиров, которую трудно разделить.
Если используется смесь двух разных спиртов, получается смесь трех разных эфиров, которую трудно разделить.