Содержание
Метиловый эфир | это… Что такое Метиловый эфир?
ТолкованиеПеревод
- Метиловый эфир
Диметиловый эфир Общие свойства Молекулярная формула C2H6O
H3С-О-СН3Молярная масса 46,07 г/моль Внешний вид беcцветный газ Номер CAS [115-10-6] Свойства Плотность и
агрегатное состояние2,091 кг/м³, газ (SATP)
668 кг/м³, жидкостьРастворимость в воде 328 г/100 мл (20°C) Органические растворители метанол, этанол, толуол Температура плавления −138,5°C (134,6 K) Температура кипения −24,9°C (248,3 K) Критическая точка 127,0°C (400,2 K),
5370 кПа,
0,272 г/см³Строение Форма молекулы ? Дипольный момент 1,3 D (газ) Опасность Температура
вспышки−41°C ПДК в воздухе рабочей зоны 1910 мг/м³ Родственные соединения Родственные эфиры Диэтиловый эфир Димети́ловый эфи́р (C2H6O) (метиловый эфир, метоксиметан, древесный эфир) Н3С-О-СН3 — широко применяемый на практике простой эфир.

Содержание
- 1 Свойства
- 2 Производство
- 3 Применение
- 3.1 Применение в качестве топлива
- 4 Опасность
Свойства
- Бесцветный газ с характерным запахом, химически инертный
- Температура плавления — (−138,5)°C
- Температура кипения — (−24,9)°C
- Плотность при нормальных условиях — 2,1098 кг/м³ (в 1,63 раза тяжелее воздуха)
- Плотность в жидкой фазе — 0,668 г/см³
- Критическая температура — +127,0 °C
- Критическое давление — 53 атм
- Критическая плотность — 0,272 г/см³
- Растворимость в воде — 3700 мл/100 мл при 18 °C
- Растворим в метиловом и этиловом спирте, толуоле
Экспериментальное давление паров диметилового эфира T, K Pexp, кПа T, K Pexp, кПа T, K Pexp, кПа 233.  128
12854.61 298.172 596.21 348.147 2022.45 238.126 68.49 303.160 687.37 353.146 2242.74 243.157 85.57 305.160 726.26 353.158 2243.07 248.152 105.59 308.158 787.07 358.145 2479.92 253.152 129.42 313.156 897.59 363.148 2735.67 258.160 157.53 316.154 968.55 368.158 3010.81 263.160 190.44 318.158 1018.91 373.154 3305.67 268.161 228.48 323.148 1152.35 378.150 3622.60 273.153 272.17 328.149 1298.23 383.143 3962.25 278.145 321.87 333.  157
1571457.50 388.155 4331.48 283.160 378.66 333.159 1457.76 393.158 4725.02 288.174 443.57 338.154 1631.01 398.157 5146.82 293.161 515.53 343.147 1818.80 400.378 5355.8 J. Chem. Eng. Data 2004, 49, 32-34
Производство
В промышленности производится из природного газа, угля, или биомассы.
Применение
- Используется для метилирования ароматических аминов
- Используется для получения диметилсульфата
- Пропеллент для аэрозольных баллонов
- Растворитель и экстрагент
- Хладагент
- Топливо для газовой сварки и резки
- Многоцелевое топливо
- Используется как косметическое средство для удаления бородавок.
Применение в качестве топлива
Диметиловый эфир — экологически чистое топливо без содержания серы, содержание оксидов азота в выхлопных газах на 90% меньше, чем у бензина.
 Цетановое число диметилового дизеля более 55, при том что у классического нефтяного 38-53. Применение диметилового эфира не требует специальных фильтров, но необходима переделка систем питания (установка газобалонного оборудования, корректировка смесеобразования) и зажигания двигателя. Без переделки возможно применение на автомобилях с LPG-двигателями при 30% содержании в топливе.
Цетановое число диметилового дизеля более 55, при том что у классического нефтяного 38-53. Применение диметилового эфира не требует специальных фильтров, но необходима переделка систем питания (установка газобалонного оборудования, корректировка смесеобразования) и зажигания двигателя. Без переделки возможно применение на автомобилях с LPG-двигателями при 30% содержании в топливе.Теплота сгорания ДМЭ около 30 МДж/кг, у классических нефтяных топлив — около 42 МДж/кг. Одна из особенностей применения ДМЭ — его более высокая окисляющая способность (благодаря содержанию кислорода), чем у классического топлива.
В июле 2006 года Национальная Комиссия Развития и Реформ (NDRC) (Китай) приняла стандарт использования диметилового эфира в качестве топлива. Китайское правительство будет поддерживать развитие диметилового эфира, как возможную альтернативу дизельному топливу. В ближайшие 5 лет Китай планирует производить 5-10 млн. тонн диметилового эфира в год.
Автомобили с двигателями, работающими на диметиловом эфире разрабатывают KAMAZ, Volvo,
Опасность
Является слабым наркотиком.
 Огнеопасен, смесь с воздухом взрывоопасна, температура вспышки −41 °C.
Огнеопасен, смесь с воздухом взрывоопасна, температура вспышки −41 °C.
Wikimedia Foundation.
2010.
Поможем решить контрольную работу
- Метилоранж
- Метиловый спирт
Полезное
Метиловый эфир | это… Что такое Метиловый эфир?
ТолкованиеПеревод
- Метиловый эфир
Диметиловый эфир Общие свойства Молекулярная формула C2H6O
H3С-О-СН3Молярная масса 46,07 г/моль Внешний вид беcцветный газ Номер CAS [115-10-6] Свойства Плотность и
агрегатное состояние2,091 кг/м³, газ (SATP)
668 кг/м³, жидкостьРастворимость в воде 328 г/100 мл (20°C) Органические растворители метанол, этанол, толуол Температура плавления −138,5°C (134,6 K) Температура кипения −24,9°C (248,3 K) Критическая точка 127,0°C (400,2 K),
5370 кПа,
0,272 г/см³Строение Форма молекулы ? Дипольный момент 1,3 D (газ) Опасность Температура
вспышки−41°C ПДК в воздухе рабочей зоны 1910 мг/м³ Родственные соединения Родственные эфиры Диэтиловый эфир Димети́ловый эфи́р (C2H6O) (метиловый эфир, метоксиметан, древесный эфир) Н3С-О-СН3 — широко применяемый на практике простой эфир.

Содержание
- 1 Свойства
- 2 Производство
- 3 Применение
- 3.1 Применение в качестве топлива
- 4 Опасность
Свойства
- Бесцветный газ с характерным запахом, химически инертный
- Температура плавления — (−138,5)°C
- Температура кипения — (−24,9)°C
- Плотность при нормальных условиях — 2,1098 кг/м³ (в 1,63 раза тяжелее воздуха)
- Плотность в жидкой фазе — 0,668 г/см³
- Критическая температура — +127,0 °C
- Критическое давление — 53 атм
- Критическая плотность — 0,272 г/см³
- Растворимость в воде — 3700 мл/100 мл при 18 °C
- Растворим в метиловом и этиловом спирте, толуоле
Экспериментальное давление паров диметилового эфира T, K Pexp, кПа T, K Pexp, кПа T, K Pexp, кПа 233.  128
12854.61 298.172 596.21 348.147 2022.45 238.126 68.49 303.160 687.37 353.146 2242.74 243.157 85.57 305.160 726.26 353.158 2243.07 248.152 105.59 308.158 787.07 358.145 2479.92 253.152 129.42 313.156 897.59 363.148 2735.67 258.160 157.53 316.154 968.55 368.158 3010.81 263.160 190.44 318.158 1018.91 373.154 3305.67 268.161 228.48 323.148 1152.35 378.150 3622.60 273.153 272.17 328.149 1298.23 383.143 3962.25 278.145 321.87 333.  157
1571457.50 388.155 4331.48 283.160 378.66 333.159 1457.76 393.158 4725.02 288.174 443.57 338.154 1631.01 398.157 5146.82 293.161 515.53 343.147 1818.80 400.378 5355.8 J. Chem. Eng. Data 2004, 49, 32-34
Производство
В промышленности производится из природного газа, угля, или биомассы.
Применение
- Используется для метилирования ароматических аминов
- Используется для получения диметилсульфата
- Пропеллент для аэрозольных баллонов
- Растворитель и экстрагент
- Хладагент
- Топливо для газовой сварки и резки
- Многоцелевое топливо
- Используется как косметическое средство для удаления бородавок.
Применение в качестве топлива
Диметиловый эфир — экологически чистое топливо без содержания серы, содержание оксидов азота в выхлопных газах на 90% меньше, чем у бензина.
 Цетановое число диметилового дизеля более 55, при том что у классического нефтяного 38-53. Применение диметилового эфира не требует специальных фильтров, но необходима переделка систем питания (установка газобалонного оборудования, корректировка смесеобразования) и зажигания двигателя. Без переделки возможно применение на автомобилях с LPG-двигателями при 30% содержании в топливе.
Цетановое число диметилового дизеля более 55, при том что у классического нефтяного 38-53. Применение диметилового эфира не требует специальных фильтров, но необходима переделка систем питания (установка газобалонного оборудования, корректировка смесеобразования) и зажигания двигателя. Без переделки возможно применение на автомобилях с LPG-двигателями при 30% содержании в топливе.Теплота сгорания ДМЭ около 30 МДж/кг, у классических нефтяных топлив — около 42 МДж/кг. Одна из особенностей применения ДМЭ — его более высокая окисляющая способность (благодаря содержанию кислорода), чем у классического топлива.
В июле 2006 года Национальная Комиссия Развития и Реформ (NDRC) (Китай) приняла стандарт использования диметилового эфира в качестве топлива. Китайское правительство будет поддерживать развитие диметилового эфира, как возможную альтернативу дизельному топливу. В ближайшие 5 лет Китай планирует производить 5-10 млн. тонн диметилового эфира в год.
Автомобили с двигателями, работающими на диметиловом эфире разрабатывают KAMAZ, Volvo,
Опасность
Является слабым наркотиком.
 Огнеопасен, смесь с воздухом взрывоопасна, температура вспышки −41 °C.
Огнеопасен, смесь с воздухом взрывоопасна, температура вспышки −41 °C.
Wikimedia Foundation.
2010.
Нужно сделать НИР?
- Метилоранж
- Метиловый спирт
Полезное
Метиловый эфир жирных кислот, метилсоят Поставщик, дистрибьютор
Метиловые эфиры жирных кислот (МЭЖК) представляют собой продукты, которые получают путем катализируемой щелочью реакции между жирами или жирными кислотами и метанолом. Основным компонентом биодизеля являются метиловые эфиры жирных кислот, которые обычно получают из растительных масел путем переэтерификации.
В растворителях они известны как «зеленые растворители», поскольку метиловые эфиры жирных кислот являются биоразлагаемыми, образуют малолетучие органические соединения (ЛОС) и нетоксичны для человека. Они могут заменить растворители, которые считаются менее экологически безопасными или представляют опасность для окружающей среды.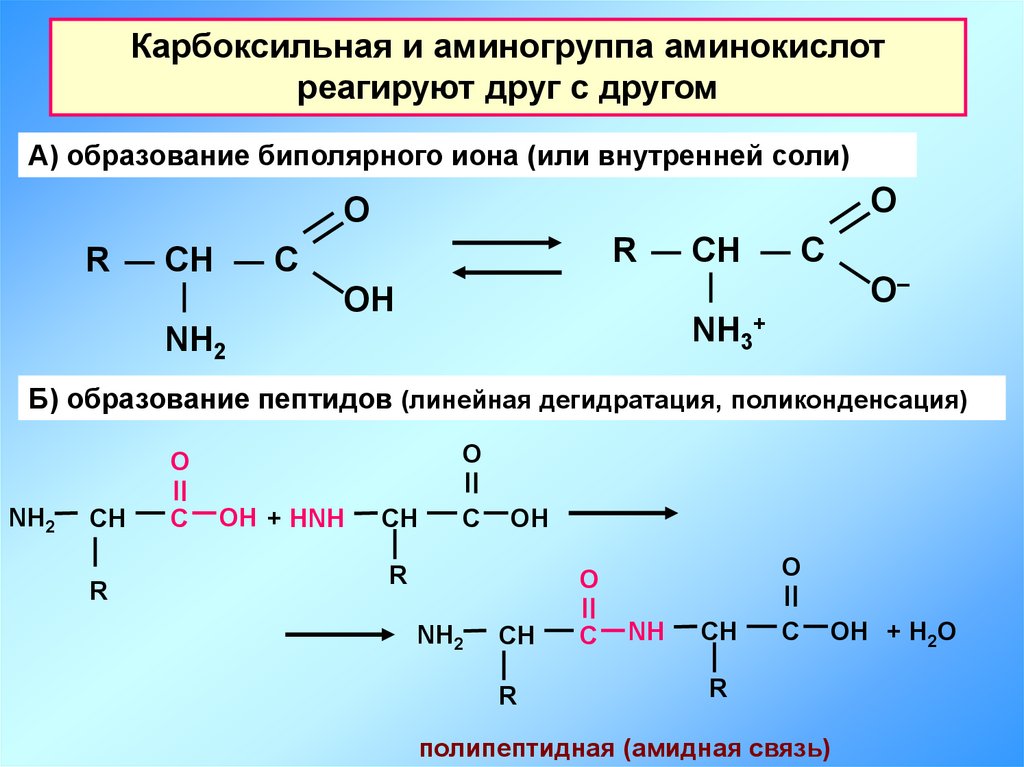
Характеристики метилового эфира жирной кислоты включают высокие температуры кипения, хорошую смазывающую способность и отличную растворимость в органических растворителях. Метиловые эфиры жирных кислот, такие как метилсоат, метилканолат, метиллаурат и метилкаприлат, среди прочего, являются универсальными продуктами, охватывающими широкий спектр продуктов, включая смазочные материалы, жидкости для металлообработки, эмульгаторы, растворители, топливо, сельское хозяйство, поверхностно-активные вещества, полимеры, покрытия. , чистящие средства и продукты питания.
Univar: надежный поставщик метиловых эфиров
Univar является дистрибьютором широкого спектра метиловых эфиров жирных кислот растительного происхождения, в том числе эфиров на основе сои (метилсоат) и пальмового масла, а также их различных фракций. Продукты доступны под собственной торговой маркой, технического сорта и без ГМО.
В дополнение к метиловым эфирам жирных кислот мы можем поставлять специальные эфиры на основе глицерина, полиэтиленгликоля, сорбитана и пентаэритрита.
Univar предлагает сеть из более чем 120 собственных предприятий в Соединенных Штатах с цистернами, железнодорожными вагонами, инфраструктурой для смешивания и упаковки, а также возможностями для поставок метиловых эфиров в:
- Наливной вагон
- Автоцистерна для массовых грузов
- Сумки (IBC)
- Барабаны
- Ведра
Наши возможности включают:
- Эффективный частный автопарк с выделенными водителями, обслуживающими местные регионы
- Партнерство с поставщиками мирового класса, предлагающими различные производственные площадки и производственные процессы
- Опытный торговый персонал с обширными знаниями о продуктах и рынках
- Индивидуальные рецептуры и специальные услуги по смешиванию, доступные через технические службы
Посмотрите нашу продукцию на основе метилового эфира ниже или свяжитесь с нами, чтобы получить ценовое предложение.
Метиловые эфиры жирных кислот предлагают зеленый химический раствор
Результаты 1 — 16 из 16
Код продукта CA
Номер CAS
ПДС
Паспорт безопасности данных
Метиловые эфиры
Портал органической химии
Реакции
>> Защита групп
>> Стабильность
T. W. Green, P. G. M. Wuts,
W. Green, P. G. M. Wuts,
Защитные группы в органическом синтезе ,
Wiley-Interscience, Нью-Йорк, 1999 , 372-381, 383-387,
728-731.
Стабильность
| Н 2 О: | pH < 1, 100°C | pH = 1, RT | pH = 4, RT | pH = 9, RT | pH = 12, RT | pH > 12, 100°C |
| Основания: | ЛДА | NET 3 , Py | т-БуОК | Другие: | ДКК | SOCl 2 |
| Нуклеофилы: | РЛи | RMgX | RCuLi | Эноляты | НХ 3 , РНХ 2 | NaOCH 3 |
| Электрофилы: | RCOC1 | РЧО | Ч 3 I | Другие: | :CCl 2 | Bu 3 SnH |
| Переходник: | H 2 / Ni | H 2 / Rh | Zn/HCl | Na/NH 3 | LiAlH 4 | NaBH 4 |
| Окисление: | КМnО 4 | ОсО 4 | CrO 3 / Py | RCOOOH | I 2 , Br 2 , Cl 2 | MnO 2 / CH 2 Cl 2 |
Защита
Удобный и эффективный сонохимический метод метилэтерификации
карбоновых кислот катализируется нанесенным на полимер трифенилфосфином в
присутствие 2,4,6-трихлор-1,3,5-триазина и Na 2 СО 3 .
Метиловые эфиры различных карбоновых кислот, содержащие реакционноспособные гидроксильные группы в качестве
а также кислото- или щелочелабильные функциональные группы могут быть быстро получены в течение
короткое время от хорошего до отличного выхода при высокой чистоте без колонки
хроматография.
С. Джайта, В. Фаходи, М. Паттараварапан,
Synlett , 2015 , 26 , 2006-2008.
Sc(OTf) 3 катализирует прямую переэтерификацию сложных эфиров карбоновых кислот.
в кипящих спиртах. Получены метиловый, этиловый, изопропиловый и аллиловый эфиры.
из различных субстратов с высоким урожаем. Применение микроволнового излучения
привело к значительному сокращению времени реакции.
Н. Ремме, К. Кошек, К. Шнайдер, Synlett , 2007 ,
491-493.
Катализируемое медью О-метилирование карбоновых кислот с использованием диметилсульфоксида.
(ДМСО) в качестве источника метила обладает широким спектром субстратов и превосходным
функциональная групповая толерантность. Механистические исследования показывают, что метильный радикал
Механистические исследования показывают, что метильный радикал
получают из диметилсульфоксида.
Дж. Цзя, К. Цзян, А. Чжао, Б. Сюй, К. Лю, В.-П. Луо, К.-К. Го, 9 лет0276
Синтез , 2016 , 48 , 421-428.
Высокоэффективный синтез метиловых эфиров из бензиловых спиртов, альдегидов,
или кислоты посредством катализируемого медью расщепления С-С от трет--бутилгидропероксида
легко доступен и практичен и предлагает альтернативу традиционным
путь.
Y. Zhu, H. Yan, L. Lu, D. Liu, G. Rong, J. Mao, J. Org. хим. , 2013 ,
78 , 9898-9905.
Диметилкарбонат является нетоксичным и зеленым метилирующим реагентом. Базовый катализ
перенос метила от диметилкарбоната к карбоновым кислотам обеспечивает высокую
селективность к этерификации и мягкие условия реакции, которые позволяют
сохранение стереохимии в эпимеризуемых стереоцентрах. изотопная маркировка
исследования предполагают механизм прямого переноса метила от диметилкарбоната к
субстрат.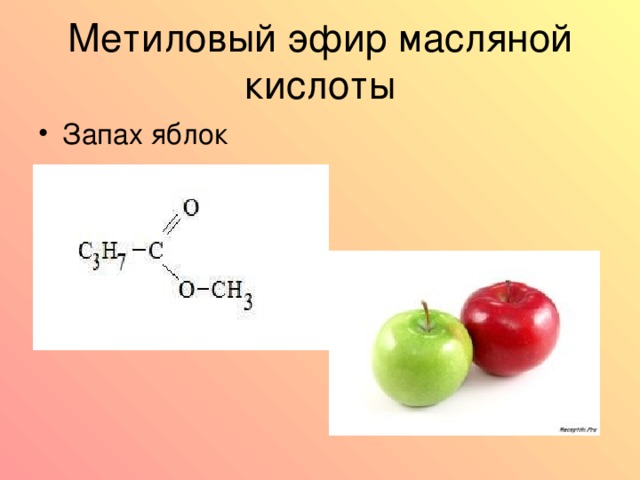
Ю. Джи, Дж. Суини, Дж. Зоглио, Д. Дж. Горин, Ж. Орг. хим. , 2013 ,
78 , 11606-11611.
Cu-катализируемое недекарбоксилативное метилирование карбоновых кислот с
метилборная кислота действует на воздухе как единственный окислитель и предлагает стратегию
замена токсичных, электрофильных алкилирующих реагентов. Исследование изотопной маркировки
поддерживает окислительный механизм кросс-сочетания, по аналогии с тем, который предложен для
Арилирование Чан-Лама.
К. Э. Якобсон, Н. Мартинес-Муоз, Д. Дж. Горин, Ж. Орг. хим. ,
2015 ,
80 , 7305-7310.
Прочие синтезы метиловых эфиров
Легкодоступная каталитическая система, состоящая из комбинации палладия и древесного угля.
с нитратом висмута (III) и металлическим теллуром обеспечивает эффективную аэробную
окислительная метиловая этерификация первичных спиртов имеет широкий спектр
области применения, и эффективен как с активированными, так и с неактивированными спиртами, содержащими
разнообразные функциональные группы.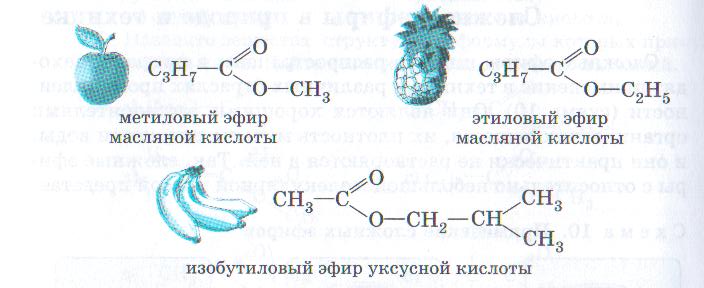 Добавки Bi и Te значительно увеличивают
Добавки Bi и Te значительно увеличивают
скорость реакции, селективность и общий выход продукта.
А. Б. Пауэлл, С. С. Шталь, Org. лат. , 2013 ,
15 , 5072-5075.
Снятие защиты
N,N -диариламмония пиросульфат эффективно катализирует гидролиз
эфиры в условиях отсутствия органических растворителей. Этот метод обратного мицеллярного типа
успешно применяется для гидролиза различных сложных эфиров без
разложение чувствительных к основаниям фрагментов без потери оптической чистоты
для α-гетерозамещенных карбоновых кислот.
Ю. Кошикари, А. Сакакура, К. Исихара, Org. лат. , 2012 ,
14 , 3194-3197.
Алюминиевый порошок и йод в безводном ацетонитриле опосредуют однореакторную реакцию.
снятие защиты с алкилкарбоксилатов в негидролитических условиях. Расщепление
лактоны дают соответствующие ω-иодоалкилкарбоновые кислоты. Этот способ
обеспечивает селективное расщепление сложных эфиров алкилкарбоновых кислот в присутствии
ариловые эфиры.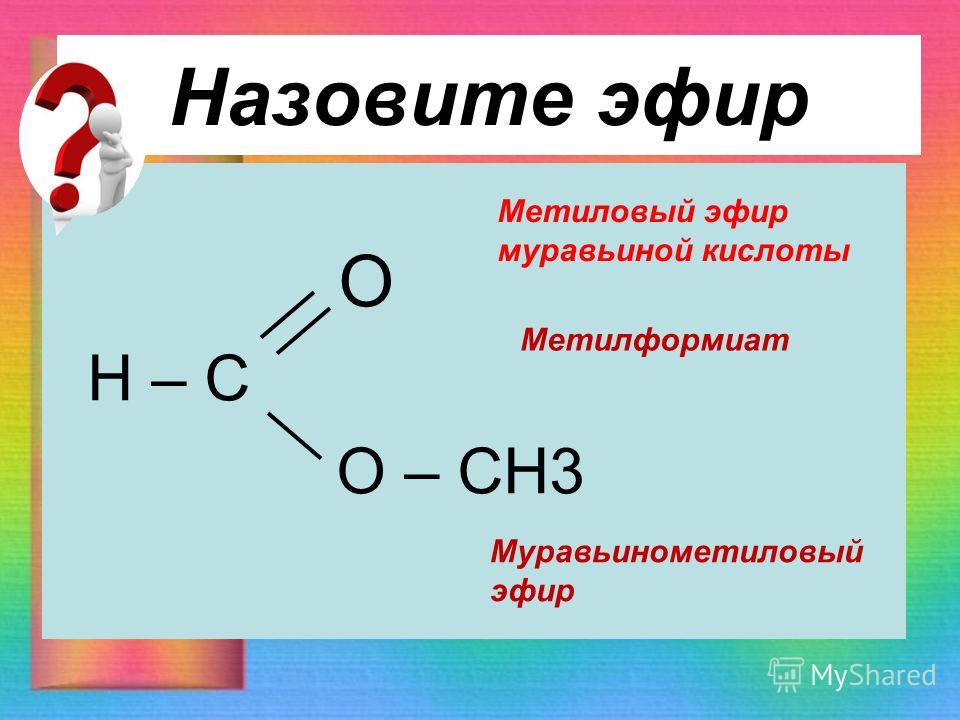


 128
128 157
157 Цетановое число диметилового дизеля более 55, при том что у классического нефтяного 38-53. Применение диметилового эфира не требует специальных фильтров, но необходима переделка систем питания (установка газобалонного оборудования, корректировка смесеобразования) и зажигания двигателя. Без переделки возможно применение на автомобилях с LPG-двигателями при 30% содержании в топливе.
Цетановое число диметилового дизеля более 55, при том что у классического нефтяного 38-53. Применение диметилового эфира не требует специальных фильтров, но необходима переделка систем питания (установка газобалонного оборудования, корректировка смесеобразования) и зажигания двигателя. Без переделки возможно применение на автомобилях с LPG-двигателями при 30% содержании в топливе. Огнеопасен, смесь с воздухом взрывоопасна, температура вспышки −41 °C.
Огнеопасен, смесь с воздухом взрывоопасна, температура вспышки −41 °C.
 128
128 157
157 Цетановое число диметилового дизеля более 55, при том что у классического нефтяного 38-53. Применение диметилового эфира не требует специальных фильтров, но необходима переделка систем питания (установка газобалонного оборудования, корректировка смесеобразования) и зажигания двигателя. Без переделки возможно применение на автомобилях с LPG-двигателями при 30% содержании в топливе.
Цетановое число диметилового дизеля более 55, при том что у классического нефтяного 38-53. Применение диметилового эфира не требует специальных фильтров, но необходима переделка систем питания (установка газобалонного оборудования, корректировка смесеобразования) и зажигания двигателя. Без переделки возможно применение на автомобилях с LPG-двигателями при 30% содержании в топливе. Огнеопасен, смесь с воздухом взрывоопасна, температура вспышки −41 °C.
Огнеопасен, смесь с воздухом взрывоопасна, температура вспышки −41 °C.