Большая Энциклопедия Нефти и Газа. Этиловый эфир глиоксиловой кислоты
Глиоксиловая кислота этиловый эфир - Справочник химика 21
Нитрозирование эфиров 4 приводит к С-нитрозосоединениям 5, которые выделяются в виде вязких голубых масел (Хп,ах 620 нм, 115). В избытке кислоты соединение 5 легко растворяется с образованием голубого раствора, переходящего в желтый через 2-3 ч, очевидно, за счет димеризации в производное 6. Дальнейшая нейтрализация приводит к расщеплению димера 6 с одновременным отщеплением алифатического радикала и образованию во всех случаях одного и того же продукта - оксима этилового эфира 3,3-диметил-3,4-дигидроизохинолин-1-ил-глиоксиловой кислоты 7 [1]. Методом ГЖХ показано, что алифатический радикал отщепляется в виде соответствующего спирта. [c.494]
Метиловый и этиловый эфиры глиоксиловой кислоты [2]. Расщеплением метиловых и этиловых эфиров -винной кислоты в сухом эфире под действием И. к. можно получить соответствующие эфнры глиоксиловой кислоты с выходом 80—85% и [c.241]Расщепление гликолей может происходить также при использовании висмутата натрия. Этот реагент расщепляет диэтиловый эфир винной кислоты, давая этиловый эфир глиоксиловой кислоты [28] [c.205]
Напишите структурные формулы следующих соединений а) ацетоуксусная кислота б) пропионилуксусная кислота в) 2-оксо-3,3-диметилбутановая кислота г) 4-оксо--3-метилбутановая кислота д) 4-оксо-2-метилпентановая кислота е) 3-оксопентандиовая кислота ж) этиловый эфир глиоксиловой кислоты. [c.99]
Разнообразные асимметрические синтезы данного типа многократно использовались для получения оптически активных аминокислот. Высокого оптического выхода удалось добиться при проведении таких синтезов с помощью диастереомерных металлкарбонилиминных комплексов [137]. Реакция (—)-а-фенилэтиламина с этиловым эфиром глиоксиловой кислоты и Ре2(С0)э дает два диастереомерных комплекса ЬУИ [c.146]
Получение полуацеталя этилового эфира глиоксиловой кислоты из диэтилового эфира виииой кислоты действием тетраацетата свинца К раствору 1 моля диэтилового эфира винной кислоты при энергичном перемеш.ивании и охлажде-ЛИИ ледяной водой в течение 1 ч прибавляют 1 МОЛь тетраацетата свинца. Перемешивают 12 ч при комнатной температуре, фильтруют. Медленно, пользуясь 50-сантиметровой колонкой Вигре, в вакууме отгоняют /з бензола (отгонку прекращают, когда проба дистиллята станет давать с концентрированным аммиаком четкое красное окрашивание это признак того, что начал перегоняться продукт реакции). После добавления 800 мл абсолютного спирта оставляют на ночь, фильтруют, твердый остаток промывают небольшим количеством спирта, основную массу спирта отгоняют через ту же колонну в вакууме. Затем колонку снимают и остаток быстро перегоняют в вакууме на воздушной бане до "Тех пор, пока поступление дистиллята полностью прекратится. Весь собранный дистиллят ректифицируют на колонке. Т. кип. 57—59°С (при 22 мм рт. ст.) выход 65%. [c.34]
СКСОгСаИб Этиловый эфир-2,4-диметил-З-ацетил-пиррил-5-глиоксиловой кислоты 84 48 [c.314]
Получение н-бутилового эфира глиоксиловой кислоты в литературе не описано. Анализ для СЛюОа вычислено С 55,37, Н 7,75 найдено С 54,95, Н 7,83. Этиловый эфир ] лиоксиловой кислоты был получен с хорошим выходом окислспием этилового эфира винной кислоты красной окисью свинца или висмутатом натрия В этих работах описано выделение этилового эфира глиоксиловой кислоты в виде карбонильных производных. [c.19]
При конденсации двух альдегидов—этилового эфира глиоксиловой кислоты (XLV) и -треозы (XLVI) — под влиянием щелочного раствора цианистого калия происходит бензоиновая (ацилоиновая) конденсация, по-видимому, через промежуточное получение двух возможных смешанных бензоинов (XLVII) с образованием -аскорбиновой кислоты (I) [1061 [c.31]
Хорнер [517] предполагал, что ему удалось получить оксиндолил-З-уксусную кислоту (IV) при гидролизе этилового эфира оксиндолил-З-уксусной кислоты (III), полученного восстановлением этилового эфира оксиндолил-3-глиоксиловой кислоты (II) амальгамой цинка в уксусной кислоте. [c.121]
Синтез этилового эфира оксиндолил-З-глиоксиловой кислоты (И), осуществленный Хорнером [517] путем конденсации оксиндола с 1 молекулой щавелевого эфира, был упомянут выше. Вислиценус и Бабек [480] получили это вещество тем же способом. [c.126]
Указанный метод применялся для получения изатин-4-карбоновой кислоты из 2-нитро-6-карбоксифенилглиоксиловой кислоты [646] и 5,6-диметокси-изатина из этилового эфира 6-аминовератроилмуравьиной кислоты [647]. В последнем примере необходимый эфир глиоксиловой кислоты был синтезирован конденсацией этилформиата с этиловым эфиром 6-аминовератровой КИС.ПОТЫ. [c.153]
Оксихиноксалины. Хотя а-оксихиноксалины обычно рассматривают как кетогидрохиноксалины (стр. 392), они могут существовать в енольной форме как настоящие хиноксалины и для целей классификации их удобно считать членами последней системы. 2-Оксихиноксалины легко получаются конденсацией а-кетонокислот или их эфиров с ароматическими о-диаминами в условиях, подобных условиям классического синтеза хиноксалина [4, 5, 37, 48 ]. Родоначальное соединение — 2-оксихиноксалин — синтезируют этим методом с 57%-ным выходом из этилового эфира глиоксиловой кислоты [44]. [c.379]
Полученные карбонильные производные тиофенового ряда были испытаны на активность против кишечной палочки и золотистого стафилококка. Как было установлено, все соединения проявляют низкую антимикробную активность, однако отмечено возрастание активности от 1000 мкг/мл до 62.5 мкг/мл при переходе от этилового эфира тиенил-2-глиоксиловой кислоты 17 к этиловому эфиру 4,5-ди-фенилтиенил-2-глиоксиловой кислоты 18 [И]. [c.474]
Хлористый этилок-салил, триметиловый эфир оксигидрохи-нона Этиловый эфир 2,4,5-триметоксифенил-глиоксиловой кислоты, НС1 Al lg в безводном сероуглероде, 100° С, 5 ч [2340] [c.332]
Этиловый эфир щавелевой кислоты восстановлен до этилового эфира этилиолуацеталя глиоксиловой кислоты (см. табл. 81, стр. 394). Католитом служил раствор серной кислоты в этиловом спирте в качестве анодов использовали ртуть и амальгамированный свинец. Водные растворы не способствуют образованию эфира глиоксиловой кислоты. [c.337]
Получение метилгидразона этилового эфира глиоксиловой кислоты С2Н50С0СН= = NNH Hs [I17]. К раствору иодистого метилмагния, приготовленному из 5 г магния и 35 г иодистого метила, при охлаждении прилито по каплям 10 г диазоуксусного эфира, разбавленного двойным объемом сухого эфира. Происходила очень бурная реакция (важно хорошее охлаждение ) После непродолжительного перемешивания смесь вылита в охлаж-денный льдом раствор 50 г хлористого аммония, смешанного с 10 мл 22%-ного аммиака. Эфирный слой отделен, а водный раствор подвергнут многократной экстракции. Собранные вместе эфирные вытяжки высушены хлористым кальцием. После отгонки эфира получены кристаллы, пропитанные маслом с запахом ацетамида. Растиранием с холодным спиртом или эфиром можно освободить кристаллы от пропитывающего их масла. Выход 3—4 г (30%), т. пл. 91—92° С (из спирта, бензола или горячей воды). [c.403]
Несколько лучшие результаты получаются в том случае, если в реакцию конденсации с этиловым эфиром глиоксиловой кислоты вводятся не альдозы, а получаемые нз них ацетилированные нитрилы альдоновых кислот [16]. Исходным веществом для получения аскорбиновой кислоты по этому способу является Ь-ксилоза, которую через оксим (IX) переводят в нитрил 2,3,4,5-тетраацетил-Ь-ксилоновой кислоты (X). Последний в условиях дезацетилиро-вания метилатом натрия по Земплену превращается в Ь-треозу (XI), которая в момент образования конденсируется с этиловым [c.153]
Эфиры а,р-неиредельных карбоновых кислот могут быть также получены из эфира глиоксиловой кислоты или его винилогов примером может служить получение этилового эфира р-ионилиден-уксусной кислоты (142) [240]. [c.349]
Мезоксалевая кислота НООС—СО—СООН известна лишь в виде соединения с водой, которому, подобно аналогичному гидрату глиоксиловой кислоты, приписывается строение диоксисоединения НООС—С(ОН)а—СООН. Этиловый эфир ее известен и в безводном состоянии — в виде зеленоватожелтого масла, легко, однако, дающего бесцветный гидрат С2Н5ООС—С(ОН)а—СООСаНз. [c.529]
Из калиевой соЛи или этилового эфира этилполуацеталя глиоксиловой кислоты и калиевой соли динитрометана образуется дикалиевая соль 3,3-динитро-2-оксипропионовой кислоты или калиевая соль этилового эфира этой кислоты [194]. [c.70]
Метилгидразон этилового эфира глиоксиловой кислоты И2, 403. Аланилглицин В5, 425. [c.59]
chem21.info
Кислота глиоксиловая, эфир - Справочник химика 21
Диэтилацеталь этилового эфира глиоксиловой кислоты) [c.86]
Напишите структурные формулы соединений а) метилового эфира глиоксиловой кислоты б) нитрила пировиноградной кислоты в) метилового эфира ацетоуксусной кислоты г) амида Y-кетовалериановой кислоты д) оксима р-кетомасляной кислоты [c.103]Нитрозирование эфиров 4 приводит к С-нитрозосоединениям 5, которые выделяются в виде вязких голубых масел (Хп,ах 620 нм, 115). В избытке кислоты соединение 5 легко растворяется с образованием голубого раствора, переходящего в желтый через 2-3 ч, очевидно, за счет димеризации в производное 6. Дальнейшая нейтрализация приводит к расщеплению димера 6 с одновременным отщеплением алифатического радикала и образованию во всех случаях одного и того же продукта - оксима этилового эфира 3,3-диметил-3,4-дигидроизохинолин-1-ил-глиоксиловой кислоты 7 [1]. Методом ГЖХ показано, что алифатический радикал отщепляется в виде соответствующего спирта. [c.494]
Из данных рентгеноструктурного и спектрального анализов известно также, что карбонильные группы в алифатических а-дикарбонильных соединениях находятся в энергетически выгодном транс-положении. Поэтому окончательно молекула эфира глиоксиловой кислоты выглядит следующим образом [c.425]
Здесь эфир глиоксиловой кислоты изображен тремя способами в обычной проекции (IVa), в проекции Фишера (IVb) и в проекции Ньюмана (IV ). Первые два способа не требуют пояснений, при проекции Ньюмана наблюдатель смотрит на молекулу вдоль одной связи тетраэдра, в данном случае, вдоль связи О— С. Теперь рассмотрим, с какой стороны магнийметилиодид будет атаковать молекулу глиоксилового эфира. Поскольку атака направляется на углеродный атом карбонильной группы перпендикулярно к связи С—О (что было точно доказано ранее на простых примерах), то могут быть лишь две возможности атака со стороны радикалы R и со стороны радикала Несомненно, более вероятна атака со стороны радикала меньшего объема, т. е со Стороны R - [c.425]
Реакционную массу разлагают водой и сероуглеродный слой последовательно промывают разбаиленными раствора.ми кислоты и соды и упаривают. Полученный эфир омыляют щелочью, раствор подкисляют соляной кислотой (не серной ) и арил-глиоксиловую кислоту извлекают эфиром. При промывании сероуглеродного раствора раствором соды происходит частичное омыление, и позтол1у некоторое количество арилглиоксиловой кислоты можно извлечь эфиром из подкисленных соляной кислотой содовых промывных растворов. [c.460]
Разнообразные асимметрические синтезы данного типа многократно использовались для получения оптически активных аминокислот. Высокого оптического выхода удалось добиться при проведении таких синтезов с помощью диастереомерных металлкарбонилиминных комплексов [137]. Реакция (—)-а-фенилэтиламина с этиловым эфиром глиоксиловой кислоты и Ре2(С0)э дает два диастереомерных комплекса ЬУИ [c.146]
Химические свойства этих кислот обычны. Обе дают по две серии сложных эфиров и солей. Электрофильное присоединение к двойной связи проходит нормально, только очень медленно. При озонолизе образуется глиоксиловая кислота ОНС—СО2Н. Нуклеофильное присоединение к двойной связи также возможно, поскольку алкен сопряжен с двумя карбонильными группами. Нагревание любого изомера с водным раствором гидроксида натрия приводит к образованию рацемической яблочной кислоты реакции с алкоксидами или аминами дают соответствующие замещенные янтарные кислоты. [c.258]
Получение полуацеталя этилового эфира глиоксиловой кислоты из диэтилового эфира виииой кислоты действием тетраацетата свинца К раствору 1 моля диэтилового эфира винной кислоты при энергичном перемеш.ивании и охлажде-ЛИИ ледяной водой в течение 1 ч прибавляют 1 МОЛь тетраацетата свинца. Перемешивают 12 ч при комнатной температуре, фильтруют. Медленно, пользуясь 50-сантиметровой колонкой Вигре, в вакууме отгоняют /з бензола (отгонку прекращают, когда проба дистиллята станет давать с концентрированным аммиаком четкое красное окрашивание это признак того, что начал перегоняться продукт реакции). После добавления 800 мл абсолютного спирта оставляют на ночь, фильтруют, твердый остаток промывают небольшим количеством спирта, основную массу спирта отгоняют через ту же колонну в вакууме. Затем колонку снимают и остаток быстро перегоняют в вакууме на воздушной бане до "Тех пор, пока поступление дистиллята полностью прекратится. Весь собранный дистиллят ректифицируют на колонке. Т. кип. 57—59°С (при 22 мм рт. ст.) выход 65%. [c.34]
Эфиры а.р-нелределыгых карбоновых кислот могут быть также получен). из фира глиоксиловой кислоты или его винилогов примером может служить получение этилоного эфира р-ионилиден-уксусной кислоты (142) [240]. [c.349]
СКСОгСаИб Этиловый эфир-2,4-диметил-З-ацетил-пиррил-5-глиоксиловой кислоты 84 48 [c.314]
Получение н-бутилового эфира глиоксиловой кислоты в литературе не описано. Анализ для СЛюОа вычислено С 55,37, Н 7,75 найдено С 54,95, Н 7,83. Этиловый эфир ] лиоксиловой кислоты был получен с хорошим выходом окислспием этилового эфира винной кислоты красной окисью свинца или висмутатом натрия В этих работах описано выделение этилового эфира глиоксиловой кислоты в виде карбонильных производных. [c.19]
Эти рассуждения, как легко видеть, одинаково справедливы для любой цепи атомов, соединенных простыми связями, и могут быть приняты 1при ра осмотрении конфигурации эфиров глиоксиловой кислоты, если рассматривать атом кислорода как углерод, у которого вместо атомов водорода имеются две пары электронов, т. е. в пространственном смысле — ничего. [c.425]
При конденсации двух альдегидов—этилового эфира глиоксиловой кислоты (XLV) и -треозы (XLVI) — под влиянием щелочного раствора цианистого калия происходит бензоиновая (ацилоиновая) конденсация, по-видимому, через промежуточное получение двух возможных смешанных бензоинов (XLVII) с образованием -аскорбиновой кислоты (I) [1061 [c.31]
chem21.info
Оксокислоты (альдегидо- и кетокислоты)
Общая формула:
Карбоновые кислоты, углеводородный радикал которых содержит карбонильную группу, называются оксокислотами. По взаимному расположению карбоксильной и карбонильной групп различают -, β-, γ- и т.д. оксокислоты.
Номенклатура IUPAC тривиальное название
формилметановая глиоксиловая
(глиоксалевая)
кислота
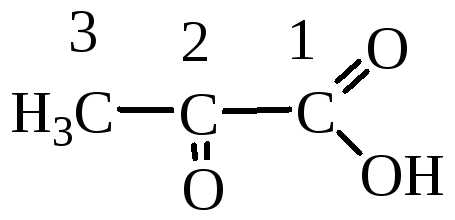 2-оксопропановая пировиноградная
2-оксопропановая пировиноградная
-кетопропионовая кислота
3-оксобутановая ацетоуксусная
β-оксомасляная кислота
Методы получения
1.Глиоксиловая кислота
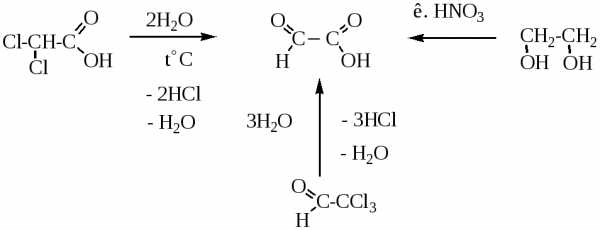
2.Пировиноградная кислота
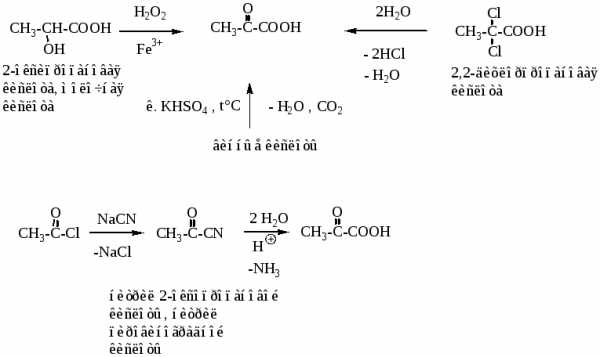
3.Ацетоуксусная кислота
Для синтеза этилового эфира ацетоуксусной кислоты или ацетоуксусного эфира (тривиальное название) используют реакцию сложноэфирной конденсации по Кляйзену (аналог альдольной конденсации), далее после гидролиза сложного эфира получают кислоту.
Реакционная способность
Оксокислоты более сильные кислоты, чем карбоновые (влияние акцепторной карбонильной группы), реакции идут по двум функциональным группам.
-Оксокислоты
Реакции по карбонильной и карбоксильной группам
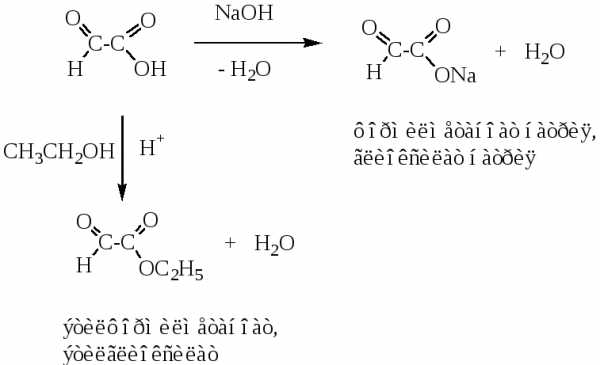
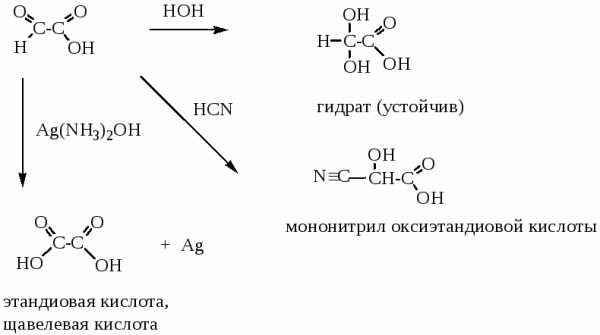
Специфические свойства
-, β-Оксокислоты легко декарбоксилируются при нагревании и под действием сильных кислот. -Оксокислоты легко окисляются.
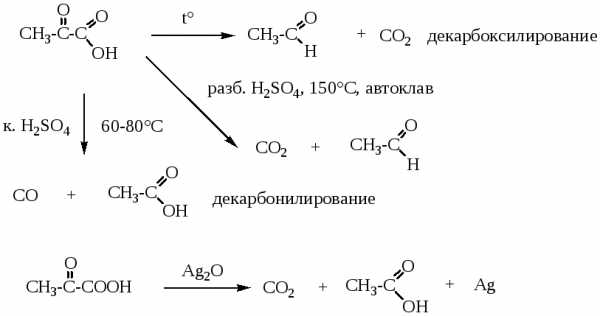
β-Оксокислоты
1. СН-кислотность ацетоуксусного эфира (кето-енольная таутомерия).
По правилу Эльтекова-Эрленмейера енольные формы альдегидов и кетонов неустойчивы и их содержание незначительно (2,510-4 %). Но при введении акцептора к -СН2-группе ее СН-кислотность значительно возрастает, что приводит к значительному увеличению соединения енольной формы.
Ацетоуксусный эфир является достаточно сильной СН-кислотой, подвижность протона в -положении приводит к образованию енола. Стабильность енольной формы обусловлено образованием водородной связи между протоном гидроксильной группы и и атолмом кислорода карбонильной.
Другие примеры кето-енольной таутомерии:
Образование водородной связи обуславливает компланарность фрагмента (С=СН-С=О), что является следствием эффекта сопряжения. Качественной реакцией на енольную форму является реакция с FeCl3, при этом наблюдается сине-фиолетовое окрашивание за счет образования комплексов Fe+3 с участием енольной формы молекул.
Проявлением СН-кислотности ацетоуксусного эфира являются реакции со щелочными металлами, алкоголятами, амидами металлов, с реактивами Гриньяра.
studfiles.net
Глиоксиловая кислота - Справочник химика 21
Глиоксиловая кислота может быть получена окислением гликоля, гликолевой кислоты или спирта азотной кислотой ее получают также кипячением хлораля нли дихлоруксусной кислоты с водой. Эти синтезы доказывают ее строение [c.327]
Щавелевая кислота с/0 — н- Глиоксиловая кислота, гликолевая кислота [c.433]Напишите структурные формулы следующих соединений а) ацетоуксусная кислота б) пропионилуксусная кислота в) 2-оксо-3,3-диметилбутановая кислота г) 4-оксо--3-метилбутановая кислота д) 4-оксо-2-метилпентановая кислота е) 3-оксопентандиовая кислота ж) этиловый эфир глиоксиловой кислоты. [c.99]
Процесс заключается в окислении охлажденного водного раствора амина со взвешенной в нем восстановленной медью кислородом, который заметно адсорбируется. Этиламин частично превращается при этом в ацетальдегид, метиламин—в формальдегид, а гликоколь— в глиоксиловую кислоту [c.206]
Приведите схемы реакций, характеризующие свойства глиоксиловой кислоты. [c.88]
Глиоксиловая кислота этаноловая кислота) [c.305]
Строение аллантоина доказывается его получением из глиоксиловой кислоты и мочевины [c.620]
Щавелевая кислота применяется как протрава при ситцепечатании, для изготовления красителей, крахмального декстрина, чернил, в качестве отбеливающего средства (для соломы), как осадитель редкоземельных элементов и т. д. Посредством электролитического восстановления из щавелевой кислоты получают гликолевую и глиоксиловую кислоты. Оксалаты алюминия и сурьмы также применяются в кращении. [c.340]
Мезоксалевая кислота плавится при 121° как а-кетокислота, она восстанавливает аммиачный раствор соли серебра и распадается при кипячении с водой на двуокись углерода и глиоксиловую кислоту [c.409]
Заслуживает внимания существование гидратной формы, устойчивость которой, очевидно, следует приписать влиянию связанных с карбонилом отрицательных карбоксильных групп (ср. хлораль, глиоксиловая кислота). [c.409]
Напишите структурные формулы соединений а) метилового эфира глиоксиловой кислоты б) нитрила пировиноградной кислоты в) метилового эфира ацетоуксусной кислоты г) амида Y-кетовалериановой кислоты д) оксима р-кетомасляной кислоты [c.103]
Сохраняются тривиальные названия глиоксиловая кислота ОНС—СООН, пировиноградная кислота СНз-СО-СООН. [c.32]
Глиоксиловая кислота может быть получена [c.87]
Глиоксиловая кислота при обычных условиях—сиропообразная жидкость. При кипячении со щелочью она превращается в соли гликолевой и щавелевой кислоты [c.305]
При добавлении к раствору белка глиоксиловой кислоты 0=СНС00Н в присутствии концентрированной h3SO4 происходит интенсивное окрашивание реакционной среды в синефиолетовый цвет, а в присутствии ледяной кислоты СН3СООН - в вишневый. [c.355]
Глиоксиловая кислота обладает свойствами и карбоновой кислоты и альдегида восстановление ею аммиачного раствора нитрата серебра и образование гидразонов обусловлены наличием альдегидной группы. При кипячении со щелочью глиоксиловая кислота превращается в гликолевую и щавелевую кислоты [c.327]
Поскольку она прочно удерживает 1 мол. воды, ее можно рассматривать как гидрат альдегида, соответствующий формуле-(Н0)2СН—(200Н, Безводную глиоксиловую кислоту можно получить, испаряя ее водные растворы в вакууме над Н2804 или Р2О5 это бесцветный, гигроскопичный сироп. [c.327]
Вместо глиоксаля можно применять также другие а-днкарбониль-ные соединения (Гинсберг), например а-альдегидокетомы (I), а-дикетоны (II), глиоксиловую кислоту (III), а-кетокарбоновые кислоты (IV) [c.573]
Изомерные аминокислоты А, В и С имеют молекулярный вес 117 и дают при нагревании три соединения А, В и С. Анализ соединения А показал, что оно является диизопропилдикетопиперазином. Образование В сопровождается выделением газа при озонировании В образуются пропионовый альдегид и глиоксиловая кислота. С представляет собой уметилпирролидон. Установите структуры А, В и С и объясните образование А, В и С. [c.185]
Разнообразные асимметрические синтезы данного типа многократно использовались для получения оптически активных аминокислот. Высокого оптического выхода удалось добиться при проведении таких синтезов с помощью диастереомерных металлкарбонилиминных комплексов [137]. Реакция (—)-а-фенилэтиламина с этиловым эфиром глиоксиловой кислоты и Ре2(С0)э дает два диастереомерных комплекса ЬУИ [c.146]
Химические свойства этих кислот обычны. Обе дают по две серии сложных эфиров и солей. Электрофильное присоединение к двойной связи проходит нормально, только очень медленно. При озонолизе образуется глиоксиловая кислота ОНС—СО2Н. Нуклеофильное присоединение к двойной связи также возможно, поскольку алкен сопряжен с двумя карбонильными группами. Нагревание любого изомера с водным раствором гидроксида натрия приводит к образованию рацемической яблочной кислоты реакции с алкоксидами или аминами дают соответствующие замещенные янтарные кислоты. [c.258]
Глиоксиловая кислота И—СО—СООН-НгО содержится в незрелых фруктах по мере их созревания она постепенно исчезает. Так как молекула глиоксиловой кислоты прочно связана с молекулой воды, то эту кислоту рассматривают как гидрат альдегида. Строение глиоксиловой кислоты доказывается ее получением при кипячении дихлоруйусной кислоты с водой [c.305]
Получение полуацеталя этилового эфира глиоксиловой кислоты из диэтилового эфира виииой кислоты действием тетраацетата свинца К раствору 1 моля диэтилового эфира винной кислоты при энергичном перемеш.ивании и охлажде-ЛИИ ледяной водой в течение 1 ч прибавляют 1 МОЛь тетраацетата свинца. Перемешивают 12 ч при комнатной температуре, фильтруют. Медленно, пользуясь 50-сантиметровой колонкой Вигре, в вакууме отгоняют /з бензола (отгонку прекращают, когда проба дистиллята станет давать с концентрированным аммиаком четкое красное окрашивание это признак того, что начал перегоняться продукт реакции). После добавления 800 мл абсолютного спирта оставляют на ночь, фильтруют, твердый остаток промывают небольшим количеством спирта, основную массу спирта отгоняют через ту же колонну в вакууме. Затем колонку снимают и остаток быстро перегоняют в вакууме на воздушной бане до "Тех пор, пока поступление дистиллята полностью прекратится. Весь собранный дистиллят ректифицируют на колонке. Т. кип. 57—59°С (при 22 мм рт. ст.) выход 65%. [c.34]
Альдегидофталевая кислота (40—41% из нафталина, который окисляют в глиоксиловую кислоту, а затем декарбоксилируют нагреванием с соляной кислотой и бисульфитом натрия, получая в результате указанный альдегид) [19]. [c.90]
ГЛИОКСИЛОВАЯ КИСЛОТА (глиоксалевая к-та) НС(0)С00Н. Существует в виде гидрата (НО)зСНСООН, прочно удерживающего воду, Гпл 98 °С раств. в воде, плохо— в СП., не раств. в эф. и углеводородах для 50%- [c.138]
Основы неорганической химии для студентов нехимических специальностей (1989) -- [ c.81 , c.258 ]Курс органической химии (1965) -- [ c.284 , c.305 , c.620 ]
Химический энциклопедический словарь (1983) -- [ c.138 ]
Начала органической химии Книга первая (1969) -- [ c.336 , c.409 , c.497 ]
Общая органическая химия Т.10 (1986) -- [ c.28 , c.615 ]
Органическая химия (1979) -- [ c.430 , c.449 ]
Справочник биохимии (1991) -- [ c.42 ]
Гетероциклические соединения Т.1 (1953) -- [ c.286 ]
Гетероциклические соединения, Том 1 (1953) -- [ c.286 ]
Биоорганическая химия (1991) -- [ c.263 ]
Органическая химия Часть 2 (1994) -- [ c.201 ]
Органическая химия (1990) -- [ c.603 , c.639 ]
Органическая химия Том2 (2004) -- [ c.298 , c.301 ]
Органическая химия (2001) -- [ c.419 ]
Органическая химия (1998) -- [ c.319 ]
Большой энциклопедический словарь Химия изд.2 (1998) -- [ c.138 ]
Химия справочное руководство (1975) -- [ c.299 ]
Химия углеводородов нефти и их производных том 1,2 (0) -- [ c.557 ]
Органическая химия (1964) -- [ c.275 , c.320 ]
Жидкостная колоночная хроматография том 3 (1978) -- [ c.2 , c.119 , c.171 , c.182 ]
Руководство по малому практикуму по органической химии (1964) -- [ c.259 ]
Реакции органических соединений (1966) -- [ c.253 ]
Основания глобального анализа (1983) -- [ c.0 ]
Аминокислотный состав белков и пищевых продуктов (1949) -- [ c.0 ]
Курс органической химии (1967) -- [ c.284 , c.305 , c.620 ]
Биологическая химия Издание 3 (1960) -- [ c.379 ]
Биологическая химия Издание 4 (1965) -- [ c.402 ]
Основы биологической химии (1970) -- [ c.474 , c.475 ]
Электродные процессы в органической химии (1961) -- [ c.72 , c.80 , c.118 , c.130 ]
Основы синтеза промежуточных продуктов и красителей (1950) -- [ c.712 ]
Органическая химия Издание 2 (1980) -- [ c.319 ]
Лекционные опыты и демонстрационные материалы по органической химии (1956) -- [ c.257 ]
Органическая химия (1972) -- [ c.353 ]
Электрохимия органических соединений (1968) -- [ c.227 , c.548 , c.554 ]
Органическая химия Издание 3 (1963) -- [ c.249 ]
Органическая химия (1956) -- [ c.243 ]
Основы синтеза промежуточных продуктов и красителей (1950) -- [ c.712 ]
Химия и технология пестицидов (1974) -- [ c.255 ]
Органическая химия (1972) -- [ c.353 ]
Органическая химия Издание 2 (1976) -- [ c.359 , c.360 ]
Органическая химия Издание 3 (1980) -- [ c.328 ]
Анализ органических соединений Издание 2 (1953) -- [ c.241 , c.259 , c.282 , c.303 ]
Органическая химия (1964) -- [ c.275 , c.320 ]
Полярографический анализ (1959) -- [ c.415 ]
Пестициды и окружающая среда (1977) -- [ c.58 ]
Начала органической химии Кн 1 Издание 2 (1975) -- [ c.315 , c.385 , c.467 ]
Курс физической органический химии (1972) -- [ c.356 ]
Хроматография на бумаге (1962) -- [ c.245 , c.250 ]
Основы синтеза промежуточных продуктов и красителей Издание 4 (1955) -- [ c.689 ]
Нейрохимия (1996) -- [ c.57 ]
Основы биохимии (1999) -- [ c.233 , c.234 , c.395 , c.414 ]
Органический анализ (1981) -- [ c.177 , c.186 , c.187 , c.190 ]
chem21.info
Глиоксиловой кислоты этиловый - Справочник химика 21
Нитрозирование эфиров 4 приводит к С-нитрозосоединениям 5, которые выделяются в виде вязких голубых масел (Хп,ах 620 нм, 115). В избытке кислоты соединение 5 легко растворяется с образованием голубого раствора, переходящего в желтый через 2-3 ч, очевидно, за счет димеризации в производное 6. Дальнейшая нейтрализация приводит к расщеплению димера 6 с одновременным отщеплением алифатического радикала и образованию во всех случаях одного и того же продукта - оксима этилового эфира 3,3-диметил-3,4-дигидроизохинолин-1-ил-глиоксиловой кислоты 7 [1]. Методом ГЖХ показано, что алифатический радикал отщепляется в виде соответствующего спирта. [c.494]
Метиловый и этиловый эфиры глиоксиловой кислоты [2]. Расщеплением метиловых и этиловых эфиров -винной кислоты в сухом эфире под действием И. к. можно получить соответствующие эфнры глиоксиловой кислоты с выходом 80—85% и [c.241]Метиловый и этиловый эфиры глиоксиловой кислоты [2].Рас- [c.241]
Расщепление гликолей может происходить также при использовании висмутата натрия. Этот реагент расщепляет диэтиловый эфир винной кислоты, давая этиловый эфир глиоксиловой кислоты [28] [c.205]
Глиоксиловая кислота часто содержится в недозрелых фруктах. Она получается окислением азотной кислотой этилового спирта, этиленгликоля или гликолевой кислоты. Кроме того, она может быть получена электрохимическим восстановлением щавелевой кислоты, а также действием воды на дихлоруксусную или дибромуксусную кислоты. [c.603]
Напишите структурные формулы следующих соединений а) ацетоуксусная кислота б) пропионилуксусная кислота в) 2-оксо-3,3-диметилбутановая кислота г) 4-оксо--3-метилбутановая кислота д) 4-оксо-2-метилпентановая кислота е) 3-оксопентандиовая кислота ж) этиловый эфир глиоксиловой кислоты. [c.99]
Разнообразные асимметрические синтезы данного типа многократно использовались для получения оптически активных аминокислот. Высокого оптического выхода удалось добиться при проведении таких синтезов с помощью диастереомерных металлкарбонилиминных комплексов [137]. Реакция (—)-а-фенилэтиламина с этиловым эфиром глиоксиловой кислоты и Ре2(С0)э дает два диастереомерных комплекса ЬУИ [c.146]
Получение полуацеталя этилового эфира глиоксиловой кислоты из диэтилового эфира виииой кислоты действием тетраацетата свинца К раствору 1 моля диэтилового эфира винной кислоты при энергичном перемеш.ивании и охлажде-ЛИИ ледяной водой в течение 1 ч прибавляют 1 МОЛь тетраацетата свинца. Перемешивают 12 ч при комнатной температуре, фильтруют. Медленно, пользуясь 50-сантиметровой колонкой Вигре, в вакууме отгоняют /з бензола (отгонку прекращают, когда проба дистиллята станет давать с концентрированным аммиаком четкое красное окрашивание это признак того, что начал перегоняться продукт реакции). После добавления 800 мл абсолютного спирта оставляют на ночь, фильтруют, твердый остаток промывают небольшим количеством спирта, основную массу спирта отгоняют через ту же колонну в вакууме. Затем колонку снимают и остаток быстро перегоняют в вакууме на воздушной бане до "Тех пор, пока поступление дистиллята полностью прекратится. Весь собранный дистиллят ректифицируют на колонке. Т. кип. 57—59°С (при 22 мм рт. ст.) выход 65%. [c.34]
СКСОгСаИб Этиловый эфир-2,4-диметил-З-ацетил-пиррил-5-глиоксиловой кислоты 84 48 [c.314]
Получение н-бутилового эфира глиоксиловой кислоты в литературе не описано. Анализ для СЛюОа вычислено С 55,37, Н 7,75 найдено С 54,95, Н 7,83. Этиловый эфир ] лиоксиловой кислоты был получен с хорошим выходом окислспием этилового эфира винной кислоты красной окисью свинца или висмутатом натрия В этих работах описано выделение этилового эфира глиоксиловой кислоты в виде карбонильных производных. [c.19]
При конденсации двух альдегидов—этилового эфира глиоксиловой кислоты (XLV) и -треозы (XLVI) — под влиянием щелочного раствора цианистого калия происходит бензоиновая (ацилоиновая) конденсация, по-видимому, через промежуточное получение двух возможных смешанных бензоинов (XLVII) с образованием -аскорбиновой кислоты (I) [1061 [c.31]
Хорнер [517] предполагал, что ему удалось получить оксиндолил-З-уксусную кислоту (IV) при гидролизе этилового эфира оксиндолил-З-уксусной кислоты (III), полученного восстановлением этилового эфира оксиндолил-3-глиоксиловой кислоты (II) амальгамой цинка в уксусной кислоте. [c.121]
Синтез этилового эфира оксиндолил-З-глиоксиловой кислоты (И), осуществленный Хорнером [517] путем конденсации оксиндола с 1 молекулой щавелевого эфира, был упомянут выше. Вислиценус и Бабек [480] получили это вещество тем же способом. [c.126]
Указанный метод применялся для получения изатин-4-карбоновой кислоты из 2-нитро-6-карбоксифенилглиоксиловой кислоты [646] и 5,6-диметокси-изатина из этилового эфира 6-аминовератроилмуравьиной кислоты [647]. В последнем примере необходимый эфир глиоксиловой кислоты был синтезирован конденсацией этилформиата с этиловым эфиром 6-аминовератровой КИС.ПОТЫ. [c.153]
Оксихиноксалины. Хотя а-оксихиноксалины обычно рассматривают как кетогидрохиноксалины (стр. 392), они могут существовать в енольной форме как настоящие хиноксалины и для целей классификации их удобно считать членами последней системы. 2-Оксихиноксалины легко получаются конденсацией а-кетонокислот или их эфиров с ароматическими о-диаминами в условиях, подобных условиям классического синтеза хиноксалина [4, 5, 37, 48 ]. Родоначальное соединение — 2-оксихиноксалин — синтезируют этим методом с 57%-ным выходом из этилового эфира глиоксиловой кислоты [44]. [c.379]
Полученные карбонильные производные тиофенового ряда были испытаны на активность против кишечной палочки и золотистого стафилококка. Как было установлено, все соединения проявляют низкую антимикробную активность, однако отмечено возрастание активности от 1000 мкг/мл до 62.5 мкг/мл при переходе от этилового эфира тиенил-2-глиоксиловой кислоты 17 к этиловому эфиру 4,5-ди-фенилтиенил-2-глиоксиловой кислоты 18 [И]. [c.474]
Хлористый этилок-салил, триметиловый эфир оксигидрохи-нона Этиловый эфир 2,4,5-триметоксифенил-глиоксиловой кислоты, НС1 Al lg в безводном сероуглероде, 100° С, 5 ч [2340] [c.332]
Этиловый эфир щавелевой кислоты восстановлен до этилового эфира этилиолуацеталя глиоксиловой кислоты (см. табл. 81, стр. 394). Католитом служил раствор серной кислоты в этиловом спирте в качестве анодов использовали ртуть и амальгамированный свинец. Водные растворы не способствуют образованию эфира глиоксиловой кислоты. [c.337]
Получение метилгидразона этилового эфира глиоксиловой кислоты С2Н50С0СН= = NNH Hs [I17]. К раствору иодистого метилмагния, приготовленному из 5 г магния и 35 г иодистого метила, при охлаждении прилито по каплям 10 г диазоуксусного эфира, разбавленного двойным объемом сухого эфира. Происходила очень бурная реакция (важно хорошее охлаждение ) После непродолжительного перемешивания смесь вылита в охлаж-денный льдом раствор 50 г хлористого аммония, смешанного с 10 мл 22%-ного аммиака. Эфирный слой отделен, а водный раствор подвергнут многократной экстракции. Собранные вместе эфирные вытяжки высушены хлористым кальцием. После отгонки эфира получены кристаллы, пропитанные маслом с запахом ацетамида. Растиранием с холодным спиртом или эфиром можно освободить кристаллы от пропитывающего их масла. Выход 3—4 г (30%), т. пл. 91—92° С (из спирта, бензола или горячей воды). [c.403]
Несколько лучшие результаты получаются в том случае, если в реакцию конденсации с этиловым эфиром глиоксиловой кислоты вводятся не альдозы, а получаемые нз них ацетилированные нитрилы альдоновых кислот [16]. Исходным веществом для получения аскорбиновой кислоты по этому способу является Ь-ксилоза, которую через оксим (IX) переводят в нитрил 2,3,4,5-тетраацетил-Ь-ксилоновой кислоты (X). Последний в условиях дезацетилиро-вания метилатом натрия по Земплену превращается в Ь-треозу (XI), которая в момент образования конденсируется с этиловым [c.153]
Эфиры а,р-неиредельных карбоновых кислот могут быть также получены из эфира глиоксиловой кислоты или его винилогов примером может служить получение этилового эфира р-ионилиден-уксусной кислоты (142) [240]. [c.349]
Мезоксалевая кислота НООС—СО—СООН известна лишь в виде соединения с водой, которому, подобно аналогичному гидрату глиоксиловой кислоты, приписывается строение диоксисоединения НООС—С(ОН)а—СООН. Этиловый эфир ее известен и в безводном состоянии — в виде зеленоватожелтого масла, легко, однако, дающего бесцветный гидрат С2Н5ООС—С(ОН)а—СООСаНз. [c.529]
Из калиевой соЛи или этилового эфира этилполуацеталя глиоксиловой кислоты и калиевой соли динитрометана образуется дикалиевая соль 3,3-динитро-2-оксипропионовой кислоты или калиевая соль этилового эфира этой кислоты [194]. [c.70]
chem21.info
Глиоксиловая кислота I также - Справочник химика 21
Щавелевая кислота применяется как протрава при ситцепечатании, для изготовления красителей, крахмального декстрина, чернил, в качестве отбеливающего средства (для соломы), как осадитель редкоземельных элементов и т. д. Посредством электролитического восстановления из щавелевой кислоты получают гликолевую и глиоксиловую кислоты. Оксалаты алюминия и сурьмы также применяются в кращении. [c.340]
Из данных рентгеноструктурного и спектрального анализов известно также, что карбонильные группы в алифатических а-дикарбонильных соединениях находятся в энергетически выгодном транс-положении. Поэтому окончательно молекула эфира глиоксиловой кислоты выглядит следующим образом [c.425]При обработке щелочами, а также водой при повышенных температурах глиоксиловая кислота претерпевает окислительно-восстановительное превращение, характерное для альдегидов, не содержащих атомов водорода у а-углеродного атома (см. разд. 4.2.4) и приводящее к образованию смеси гликолевой и щавелевой кислот [c.467]
Необходимый оксим нитрила глиоксиловой кислоты может быть синтезирован также по реакции фенилацетонитрила с алкил-нитритом [c.220]
Глиоксиловая кислота —реакционноспособное вещество. Как карбоксильная, так и карбонильная группы вступают в нормальные реакции последняя образует бисульфитное соединение, циангидрин, оксим, фенилгидразон и т.д. Глиоксиловая кислота восстанавливает аммиачный раствор серебра. С едкими щелочами на холоду, а также и с водой при нагревании она превращается по схеме реакции Канницаро в гликолевую и щавелевую кислоты [c.51]
Расщепление гликолей может происходить также при использовании висмутата натрия. Этот реагент расщепляет диэтиловый эфир винной кислоты, давая этиловый эфир глиоксиловой кислоты [28] [c.205]
Глиоксиловая кислота часто содержится в недозрелых фруктах. Она получается окислением азотной кислотой этилового спирта, этиленгликоля или гликолевой кислоты. Кроме того, она может быть получена электрохимическим восстановлением щавелевой кислоты, а также действием воды на дихлоруксусную или дибромуксусную кислоты. [c.603]
Янтарная кислота, далее, может принимать участие в реакциях цикла трикарбоновых кислот и через фумаровую кислоту образовывать яблочную, а затем щавелевоуксусную кислоты. Глиоксиловая кислота вступает в соединение со второй молекулой ацетилкофермента А, и в результате этого также образуется яблочная кислота. Эта реакция катализируется ферментом, который был назван м а л а тси н тет а з о й [c.323]
Биологические предшественники гликокола в животном организме мало изучены он синтезируется различными путями. Было показано образование гликокола из треонина и серина, а также переаминированием, из глиоксиловой кислоты. [c.345]
Фонде с соавт. [131] исследовал по НИП электродные дроцессы восстановления глиоксиловой и пирови-ноградной кислот, которые в водных растворах гидратируются и диссоциируют как в негидратнрованной форме, так и в гидратированной форме. Гидратированные формы не восстанавливаются на РКЭ, а не-гидратированные кислоты восстанавливаются легче их анионов. В областях pH, на несколько единиц больше показателей констант диссоциации этих кислот, на НИП их растворов наблюдаются две волны. Первые волны в обоих случаях являются кинетическими. Вторая волна глиоксиловой кислоты также является кинетической, а пцровиноградной — диффузионной. [c.65]
Вместо глиоксаля можно применять также другие а-днкарбониль-ные соединения (Гинсберг), например а-альдегидокетомы (I), а-дикетоны (II), глиоксиловую кислоту (III), а-кетокарбоновые кислоты (IV) [c.573]
Химические свойства этих кислот обычны. Обе дают по две серии сложных эфиров и солей. Электрофильное присоединение к двойной связи проходит нормально, только очень медленно. При озонолизе образуется глиоксиловая кислота ОНС—СО2Н. Нуклеофильное присоединение к двойной связи также возможно, поскольку алкен сопряжен с двумя карбонильными группами. Нагревание любого изомера с водным раствором гидроксида натрия приводит к образованию рацемической яблочной кислоты реакции с алкоксидами или аминами дают соответствующие замещенные янтарные кислоты. [c.258]
Эфиры а.р-нелределыгых карбоновых кислот могут быть также получен). из фира глиоксиловой кислоты или его винилогов примером может служить получение этилоного эфира р-ионилиден-уксусной кислоты (142) [240]. [c.349]
См. также Глиоксилат. Глиоксияовая кислота Глиоксиловая кислота 1/35, 195, 504, [c.584]
ДеГйдов такие кислоты, как щавелевая (она восстанавливаете до глиоксиловой кислоты) и молочная [3]. Однако фталевая кислота, которую также можно рассматривать как аюивирован-ную кислоту, в нейтральном или слабо кислом электролите на свинцовом катоде до альдегида не восстанавливается, а превращается во фталид, возможно, из-за того, что промежуточная гидратированная альдегидокислота находится в равновесии с гидр-оксифталидом [15], который после протонирования и отщепления молекулы воды легко восстанавливается (уравнение 113). [c.373]
Ксантоптерин синтезирован из 2,4,5-триамино-6-оксипиримидина и мо-нохлоруксусной кислоты [48], дихлоруксусной кислоты [42] или полуацеталя глиоксиловой кислоты [49], а также из 2-амино-4-хлор-6-оксипири-мидина, хлористого фенилдиазония и эфира аминоуксусной кислоты [50]. [c.463]
Важное значение реагентов, добавляемых при проведении разложения этих перекисей, иллюстрируется также на примере разложения перекиси винилнденхлорида. В отсутствие воды из нее образуются формальдегид и фосген, а в присутствии — хлористый водород и глиоксиловая кислота оба направления хорошо подтверждают строение перекиси [c.352]
Как установлено Рилеем с сотрудниками, двуокись селена является специфичным окислителем для групп — СНгСО — и — СОСО —. Однако ароматические углеводороды с иепре-дeл JHЫMи группами нли подвижным водородом также могут окисляться SeOa например, стильбен при 235° дает бензил, так же как и толан. Антрацен окисляется до антрахинона (с выходом около 76%), фенантрен, так же как и флуорен, окисляемся очень мало (выход 3%). Ацетоуксусный эфир, несмотря на наличие группы — СНгСО —, не окисляется в глиоксиловую кислоту, а реагирует по схеме [c.60]
Попытки получить лактон LU, аналог аскорбиновой кислоты, дей ствием на метиловый эфир 3,4,6-триметилкетоглюконовой кислоты ЬП1 метилата натрия не привели к желаемому результату от исходного эфира отщеплялась молекула метилового спирта и образовывался З-окси-4-метокси-6-метоксиметил-а-пирон LIV [68]. Такая структура полученного соединения подтверждается образованием глиоксиловой кислоты при озонировании, а также измерением спектров абсорбции. [c.286]
Она образуется также при электролитическом восстановлении щавелевой кислоты в сернокислом растворе с ртутным катодом (выход 87 %). Эфир глиоксиловой кислоты получается окислением этилтартрата тетра-ацетатом свинца (Криге, 1933 см. том I) [c.50]
Опытами с донорами меченого аммиака было установлено, что аммиак является предшественником N1, N3 и N9, но не N7. При гидролизе мочевой кислоты, полученной при помощи меченого -рли-цина, был выделен глицин, несущий изотоп азота . таким образом, N7 образуется из аминогруппы глицина. То, что С4 и С5 образуются соответственно из карбоксильной и метиленовой групп глицина, было установлено параллельными опытами с меченым в кал дом из этих положений глицином. Полученная при этом мочевая кислота была окислена до аллантоина, который гидролизовали до глиоксиловой кислоты, выделенной в виде семикарбазона НООС—СН = Ы—ЫН—СО—МНг. При окислении этого производного перманганатом двуокись углерода, образующаяся из карбоксильной группы. глиоксиловой кислоты, выделяется быстро (7 Л1ин), а образующаяся из альдегидной группы — медленно (несколько часов), и таким путем можно различить эти два положения. Полученные результаты показали, что углерод 4 происходит из карбоксильной группы глицина, а углерод 5 из его метиленовой группы. Так было объяснено происхождение всех атомов бицикли-ческой системы мочевой кислоты. Осуществлен также энзиматический синтез мочевой кислоты из указанных предшественников. [c.629]
Важнейшие уреиды этого типа гидантоиновая кислота и ги-дантоин, содержащие остатки гликолевой кислоты, а также аллантоин, содержащий остатки двух молекул мочевины и являющийся производным глиоксиловой кислоты [c.848]
Наиболее подробно изученным представителем этого класса соединений является 2,3-дигидроксибутандиовая (винная) кислота (6). Эта кислота может присутствовать в виде любого из двух оптически активных энантиомеров (36) или (37), рацемата или в виде оптически неактивной лезо-формы (38). Рацемат получают при окислении фумаровой, сорбиновой или пипериновой кислоты перманганатом калия. Восстановление глиоксиловой кислоты цинком в уксусной кислоте или гидролиз цианогидрина, полученного из глиоксаля, приводят к рацемической смеси, из которой оптически активные кислоты можно выделить в индивидуальном виде с помощью стандартных методик схема (54) . Мезовинную кислоту (38) получают при нагревании малеиновой кислоты или фенола с перманганатом калия или из малеиновой кислоты с помощью хлората щатрия и тетраоксида осмия в воде. Реакция влажного оксида серебра с дибромянтарной кислотой также дает мезовинную кислоту схема (55) . [c.175]
В [85] изучена возможность образования муравьиной кислоты в колебательной реакции Белоусова—Жаботинского. Эксперименты показали, что ни глиоксиловая, ни мезоксалевая кислота не является предшественницей муравьиной кислоты, если присутствует бромат в кислой среде. Представляется вероятным, что муравьиная кислота не возникает через промежуточные продукты реакции Белоусова—Жаботинского с малоновой кислотой. Было найдено, что глиоксиловая кислота производит гетерогенные колебания как субстрат реакции Белоусова—Жаботинского и мезоксалевая кислота также проявляет немонотонное кинетическое поведение. [c.256]
Относительно гладко окисляется перманганатом до карбоксила конечная метпльная группа жирноароматических метил-кетонов. Хотя эфиры получающихся при этом арилглиоксиловых кислот могут быть получены также путем синтеза углеродного скелета (см. ниже, стр. 433), можно иллюстрировать способ хотя бы на одном примере. Клаус и Нейкранц [363] подробно исследовали условия реакции. Они дают следующую пропись получения фенил-глиоксиловой кислоты [363] [c.156]
У Вейганда озиибочно указано — соль глиоксиловой кислоты неверна также литературная ссылка. См. Н. Debus, Ann. 102. 26 (1857). (В. В.) [c.544]
ВОДИТ к" образованию глиоксиловой кислоты без потери щавелевоуксусной. В то же время ацетат среды может также включаться в цикл на этапе, обозначенном ацетилкофермент А (2) . В этом случае он взаимодействует с глиоксиловой кислотой, образовавшейся при расщеплении изоцитрата, образуя в результате яблочную и щавелевоуксусную кислоты. Суммарный результат реакций, показанных на фиг. 11, заключается в превращении двух молекул ацетата в молекулу щавелевоуксусной кислоты и пополнении таким образом ее дефицита, возникающего из-за утечки а-кетоглутаровой кислоты, которая расходуется в реакциях биосинтеза. Из фиг. 11 видно, что ацетат, включающийся в процесс на этапе 1, дает начало цитрату, а на этапе 2 — малату. Как показал Корнберг, если процент изотопа, включившегося в цитрат и малат, откладывать против времени, то на графике получатся кривые с отрицательным наклоном, подобные кривой А на фиг. 10 в то же время кривая для глутаминовой кислоты будет похожа на кривую С. Более того, если Pseudomonas культивировать в среде, содержащей радиоактивный ацетат, то в яблочной кислоте радиоактивность будет обнаружена раньше, чем в янтарной. Это находится в соответствии с циклом, показанным на фиг. 11, но не укладывается в рамки цикла трикарбоновых кислот. Изоцитрат-лиаза была обнаружена [c.40]
Образуется также о-иодфенилгидразон глиоксиловой кислоты с выходом 8%. [c.70]
Для обнаружения и количественного определения некоторых а-кетокислот могут быть использованы ферментативные и микробиологические методы. Многие а-кетокислоты восстанавливаются при действии лактатдегидрогеназы, причем по меньшей мере шесть из них (р-меркаптопировиноградная кислота, а-кето-масляная кислота, а-кето-р-оксимасляная кислота, 3-окснпиро-виноградная кислота, пировиноградная кислота и глиоксиловая кислота) восстанавливаются примерно с одинаковой скоростью. Дрожжевая декарбоксилаза а-кетокислот также отличается широким диапазоном субстратной специфичности (см, табл. 9). [c.104]
В опытах на крысах было показано, что внутривенно введенный N -аммоний может выводиться как таковой [71] однако в физиологических условиях аммиак крови, по-видимому, не имеет существенного значения как источник аммиака мочи. Главную роль в образовании аммиака играют а) дезамидирование глутамина и б) действие ферментной системы, состоящей из глутамат-трансаминазы и глутаматдегидрогеназы. Следует учитывать также возможность участия в этом процессе глицин-оксидазы, поскольку в моче обнаружена глиоксиловая кислота [62]. Однако значение глициноксидазы в обмене веществ взято под сомнение [72] возможно, что глиоксиловая кислота мочи представляет продукт других превращений. [c.175]
chem21.info
Глиоксиловая кислота - Большая Энциклопедия Нефти и Газа, статья, страница 3
Глиоксиловая кислота
Cтраница 3
Глиоксиловая кислота встречается в природе в недозрелых фруктах. [31]
Глиоксиловая кислота ОНС-СООН содержится в незрелых фруктах; по мере их созревания она постепенно исчезает. [32]
Если глиоксиловая кислота имеет состав С2Н203, а не С2Н404, то вполне вероятно, что ей подходит эта формула. При этом особенно ясно выступает связь между глиоксалом, глиоксиловой кислотой и щавелевой кислотой. [33]
Соли глиоксиловой кислоты, за исключением аммиакальной, все удерживают воду и представляют С. [34]
При окислении глиоксиловая кислота легко превращается в углекислый газ и воду; очевидно, реакция протекает через стадию образования щавелевой кислоты, которая под действием окислителей дает те же продукты реакции ( см. разд. [35]
В присутствии глиоксиловой кислоты после получасового нагревания до 40 появляется синяя окраска. [36]
Бариевую соль глиоксиловой кислоты вносят в разбавленную соляную кислоту и добавляют несколько миллилитров раствора, приготовленного из 4 0 г димедона в 30 мл 30-процентного спирта. [37]
Но в глиоксиловой кислоте тоже имеется соседняя электроотрицательная группа СООН, хотя, может быть и не столь сильная. Поэтому и здесь два гидроксила могут удерживаться при одном атоме углерода. [38]
А с глиоксиловой кислотой, в результате которой были получены образцы малата. [39]
С фенилгидразином, глиоксиловая кислота дает два изомерных гидразона. [40]
Заметим, что глиоксиловая кислота СНО - СООН является устойчивым продуктом реакции треонин - периодах; любая упомянутая функциональная группа из-за наличия соседней карбоксильной группы проявляет небольшую реакционноспособность с периодатом. [41]
Другие пути образования глиоксиловой кислоты ( не из глицина) еще не вполне ясны. [42]
Наиболее замечательным свойством глиоксиловой кислоты является ее способность в кристаллическом виде прочно удерживать частицу воды. [43]
Получение н-бутилового эфира глиоксиловой кислоты в литературе не описано. В этих работах описано выделение этилового эфира глиоксиловой кислоты в виде карбонильных производных. [44]
В последнее время глиоксиловую кислоту получают в технике восстановлением щавелевой кислоты на ртутных или свинцовых катодах. [45]
Страницы: 1 2 3 4
www.ngpedia.ru

















