Содержание
Борная кислота
Главная
/
Кислоты
/
Борная кислота — Н3ВО3
%D
%d.%M.%y
%h~:~%m
Бо́рная кислота́ (ортоборная кислота) — слабая кислота, имеющая химическую формулу H3BO3.
структура плоского слоя в ортоборной кислоте
Бесцветное кристаллическое вещество в виде чешуек без запаха, имеет слоистую триклинную решетку, в которой молекулы кислоты соединены водородными связями в плоские слои, слои соединены между собой межмолекулярными связями (d= 0,318 нм).
Метаборная кислота (HBO2) также представляет собой бесцветные кристаллы. Она существует в трех модификациях — наиболее устойчивой γ-НВО2 с кубической решеткой, β-НВО2 с моноклинной решеткой и α-НВО2 с ромбической решеткой.
При нагревании ортоборная кислота теряет воду и сначала переходит в метаборную кислоту, затем в тетраборную H2B4O7. При дальнейшем нагревании обезвоживается до борного ангидрида.
При дальнейшем нагревании обезвоживается до борного ангидрида.
Водные растворы борной кислоты являются смесью полиборных кислот общей формулы Н3m-2nВmО3m-n.
Свойства
Борная кислота проявляет очень слабые кислотные свойства. Она сравнительно мало растворима в воде. Ее кислотные свойства обусловлены не отщеплением протона Н+, а присоединением гидроксильного аниона:
- Ka = 5.8·10−10 моль/л; pKa = 9.24.
Она легко вытесняется из растворов своих солей большинством других кислот. Соли ее, называемые боратами, производятся обычно от различных полиборных кислот, чаще всего — тетраборной Н2В4О7, которая является значительно более сильной кислотой, чем ортоборная. Очень слабые признаки амфотерности B(OH)3 проявляет, образуя малоустойчивый гидросульфат бора В(HSO4)3.
При нейтрализации ортоборной кислоты щелочами в водных растворах не образуются ортобораты, содержащие ион (ВО3)3−, поскольку ортобораты гидролизуются практически полностью, вследствие слишком малой константы образования [В(ОН)4]−. В растворе образуются тетрабораты, метабораты или соли других полиборных кислот:
В растворе образуются тетрабораты, метабораты или соли других полиборных кислот:
- Избытком щелочи они могут быть переведены в метабораты:
Мета- и тетрабораты гидролизуются, но в меньшей степени (реакции, обратные приведенным).
В подкисленных водных растворах боратов устанавливаются следующие равновесия:
Наиболее распространенной солью борной кислоты является декагидрат тетрабората натрия Na2B4O7·10H2O (техническое название — бура).
При нагревании борная кислота растворяет оксиды металлов, образуя соли.
Со спиртами в присутствии концентрированной серной кислоты образует эфиры:
Образование борнометилового эфира В(ОСН3)3 является качественной реакцией на Н3ВО3 и соли борных кислот, при поджигании борнометиловый эфир горит красивым ярко-зеленым пламенем.
Нахождение в природе
В природе свободная борная кислота встречается в виде минерала сассолина, в горячих источниках и минеральных водах.
Применение
- В ядерных реакторах в качестве поглотителя нейтронов, растворённого в теплоносителе.
- Борное удобрение
- В лабораториях применяют для приготовления буферных растворов
- В медицине — как самостоятельное дезинфицирующее средство, а также в виде 2% раствора — для промывки кожи после попадания щелочей
- Также на основе борной кислоты производятся различные комбинированные препараты (группа АТХ D08AD), например, паста Теймурова.
- В фотографии — в составе мелкозернистых проявителей и кислых фиксажей для создания слабой кислотной среды.
- В пищевой промышленности — зарегистрирована как пищевая добавка E284 (на территории России эта добавка не входит в список разрешённых к применению[1]).
- В игре Новус борной кислотой натирают игровой стол для лучшего скольжения фишек.

- В ювелирном деле — как основа флюсов для пайки золотосодержащих сплавов.
- В промышленности — связующее при кислой футеровке печей.
Борные эфиры — Госстандарт
В вашем браузере отключена поддержка JavaScript. Для просмотра этой страницы нужно включить JavaScript. Чтобы узнать, как это сделать, нажмите здесь.
>
Спирты>
Метиловый спирт>
Этиловый спирт>
Пропиловый спирт>
Бутаноловый спирт>
Пентиловый спирт>
Бензиловый спирт>
Этиленгликоль>
Глицерин
>
Простые эфиры>
Диметиловый эфир>
Диэтиловый эфир>
Диизопропиловый эфир>
Анизол>
Оксиран>
Тетрагидрофуран>
Диоксан>
Полиэтиленгликоль
>
Сложные эфиры>
Фосфорные эфиры>
Нитратные эфиры>
Нитритные эфиры>
Сульфатные эфиры>
Сульфитные эфиры>
Угольные эфиры>
Борные эфиры>
Эфиры муравьиной кислоты>
Эфиры уксусной кислоты>
Эфиры масляной кислоты
>
Альдегиды>
Метаналь>
Этаналь>
Пропаналь>
Бутаналь
>
Кетоны>
Ацетон>
Метилэтилкетон>
Диэтилкетон>
Ацетофенон>
Бензофенон>
Циклогексанон>
Диацетил>
Ацетилацетон
>
Карбоновые кислоты>
Муравьиная кислота>
Уксусная кислота>
Пропионовая кислота>
Масляная кислота>
Валериановая кислота>
Капроновая кислота
>
Липиды>
Углеводы
- (CH3O)3B — триметилборат
- (C6H5O)3B — трифенилборат
трифениловый эфир борной кислоты
Тип вещества: органическое
Брутто-формула (система Хилла): C18h25BO3
Формула в виде текста: B(OC6H5)3
Молекулярная масса (в а.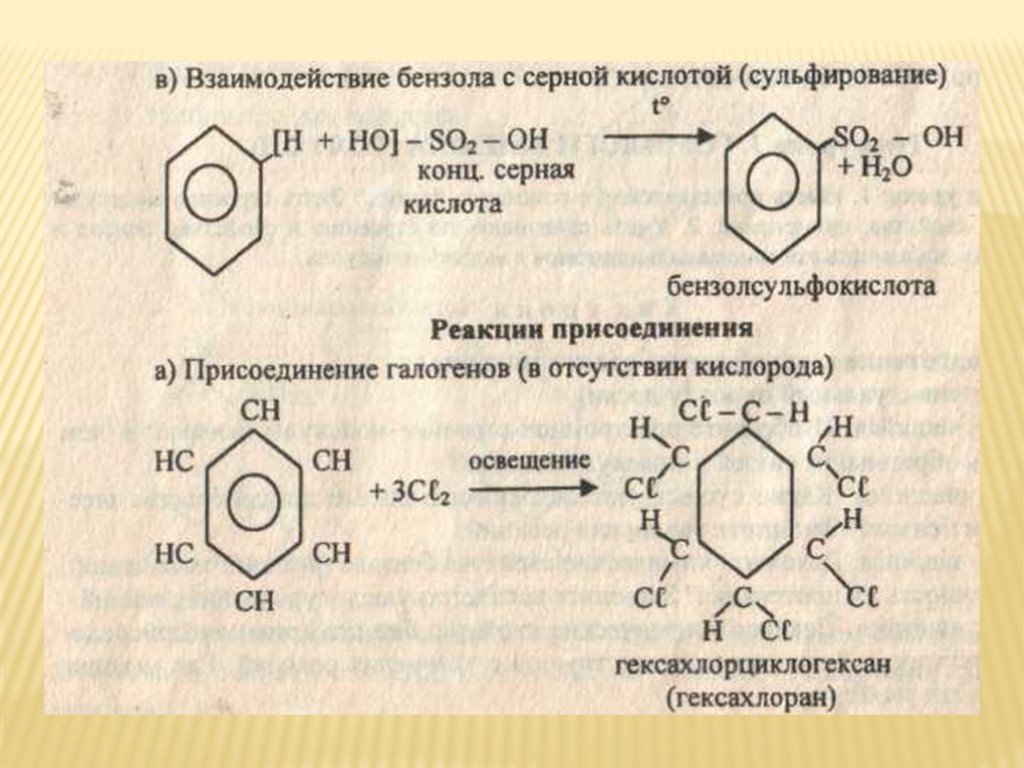 е.м.): 290,121
е.м.): 290,121
Температура плавления (в °C): 89
Давление паров (в мм.рт.ст.): 0,05 (155°C)
Стандартная энтальпия образования ΔH (298 К, кДж/моль): -669 (т)
Триметилборат, эфир борной кислоты
Тип вещества: органическое
Внешний вид: бесцветн. жидкость
Брутто-формула (система Хилла): C3H9BO3
Формула в виде текста: B(OCh4)3
Молекулярная масса (в а.е.м.): 103,91
Температура плавления (в °C): -29,2
Температура кипения (в °C) 68,7
Температурные константы смесей (содержание в весовых процентах):
54,6 °C (температура кипения азеотропа, давление 1 атм) борной кислоты триметиловый эфир 75,5% метанол 24,5%
Растворимость (в г/100 г растворителя или характеристика):
- вода: реагирует
- гексан: смешивается
- диэтиловый эфир: смешивается
- изопропиламин: смешивается
- метанол: смешивается
- тетрагидрофуран: смешивается
- этанол: смешивается
Плотность: 0,9547 (20°C, относительно воды при 4°C, состояние вещества — жидкость)
Применение: Растворитель, дегидратирующий агент, фунгицид для цитрусовых.
Система комментирования SigComments
Не нашли что искали? Вы можете оставить заявку, в форме обратной связи.
Портал Gosstanart.info не осуществляет коммерческой деятельности, не сотрудничает с рекламодателями, производителями товаров и компаниями предоставляющими услуги. Просьба, не обращаться с коммерческими предложениями! Вся информация, представленная на портале, результат независимых исследований и является свободно распространяемой информацией.
Главная Новости портала Черный список Архив Обратная связь
Боратные эфиры — Alfa Aesar
Боратные эфиры представляют собой алкильные или арилорганические соединения типа B(OR)3 и являются предшественниками производных борной кислоты. Триметилборат используется в качестве предшественника сложных эфиров бороновой кислоты для соединений Suzuki. Используется как растворитель или катализатор для производства смол, восков, красок, лаков. Он также используется в качестве метилирующего агента и источника бора в органической реакции для производства биоцидов, антипиренов для текстиля, в сварочных флюсах, антиоксидантов, ингибиторов коррозии, усилителей клейкости для эластомеров и каучуков, сшивающих агентов для полимеров, дегидратирующих агентов. и пластиковые стабилизаторы. Прямое амидирование карбоновых кислот и переамидирование первичных амидов можно осуществить с помощью сложных эфиров борной кислоты.
и пластиковые стабилизаторы. Прямое амидирование карбоновых кислот и переамидирование первичных амидов можно осуществить с помощью сложных эфиров борной кислоты.
Эфиры бората проявляют такие свойства, как противоизносные, антифрикционные и антиокислительные свойства, и поэтому используются в смазочных системах. Боратные эфиры моноэфиров гликоля используются в качестве жидких осушителей для осушки газов, в качестве стабилизаторов и в качестве неводных гидравлических жидкостей. Бораты обладают электронно-дефицитными ор-орбитами в боре, и поэтому они используются в качестве катализатора в трибовосстановлении соединений олова на трущихся поверхностях (см.: Hu, J.; Hu, Y.; Du, Z.; Liu, C. Синергетические противоизносные свойства между бораты и органические соединения олова в смазочных материалах Нефть и уголь 2007, 49 (2), 80-85).
B22060
Триацетоксиборгидрид натрия, 95%
А18728
Триэтилборат, 97%
А17592
Триизопропилборат, 98+%
B20215
Триметилборат, 99%
ПРЕДУПРЕЖДЕНИЕ. Репродуктивный вред — https://www.p65warnings.ca.gov/
Репродуктивный вред — https://www.p65warnings.ca.gov/
22975
Триметилборат, 99,9995+% (мет.прим.)
ПРЕДУПРЕЖДЕНИЕ. Репродуктивный вред — https://www.p65warnings.ca.gov/
43765
Триметилборат, 99,99% (мет.прим.)
ПРЕДУПРЕЖДЕНИЕ. Репродуктивный вред — https://www.p65warnings.ca.gov/
B21933
Триметиленборат, 98%
А19322
Три-н-бутилборат, 98%
22974
Три-н-пропилборат, 98%
L06277
Трис(триметилсилил)борат, 98%
Боратные эфиры: простые катализаторы устойчивого синтеза сложных амидов
1. Pattabiraman V.R., Bode J.W.,
Pattabiraman V.R., Bode J.W.,
Переосмысление синтеза амидной связи. Природа
480,
471–479 (2011). [PubMed] [Google Scholar]
2. Дунец Дж. Р., Магано Дж., Вайзенбургер Г. А.,
Широкомасштабное применение реагентов амидного сочетания для синтеза фармацевтических препаратов. Орг. Процесс Рез. Дев.
20,
140–177 (2016). [Академия Google]
3. Констебль Д. Дж. К., Данн П. Дж., Хейлер Дж. Д., Хамфри Г. Р., Лизер Дж. Л. младший, Линдерман Р. Дж., Лоренц К., Мэнли Дж., Перлман Б. А., Уэллс А., Закс А..
Чжан Т. Ю.,
Основные направления исследований в области «зеленой» химии — точка зрения производителей фармацевтической продукции. Зеленый хим.
9,
411–420 (2007). [Google Scholar]
4. Чан В.-К., Хо С.-М., Вонг М.-К., Че С.-М.,
Окислительный амидный синтез и лигирование N-концевой α-аминогруппы пептидов в водной среде. Варенье. хим. соц.
128,
14796–14797 (2006). [PubMed] [Google Scholar]
5. Гунанатан С., Бен-Дэвид Ю., Мильштейн Д.,
Прямой синтез амидов из спиртов и аминов с выделением H 2 . Наука
Наука
317,
790–792 (2007). [PubMed] [Google Scholar]
6. Вора Х.У., Ровис Т.,
Нуклеофильный карбен и релейный катализ HOAt в соединении амидной связи: реакция образования ортогональной пептидной связи. Варенье. хим. соц.
129,
13796–13797 (2007 г.). [Бесплатная статья PMC] [PubMed] [Google Scholar]
7. Valeur E., Bradley M.,
Образование амидной связи: за пределами мифа о связывающих реагентах. хим. соц. преп.
38,
606–631 (2009 г.)). [PubMed] [Google Scholar]
8. Krause T., Baader S., Erb B., Gooßen L. J.,
Атом-экономный каталитический синтез амидов из аминов и карбоновых кислот, активированных in situ ацетиленами. Нац. коммун.
7,
11732 (2016). [Бесплатная статья PMC] [PubMed] [Google Scholar]
9. Gooßen L. J., Ohlmann D. M., Lange P. P.,
Еще раз о термическом амидировании карбоновых кислот. Синтез
2009 г.,
160–164 (2009). [Google Scholar]
10. Аллен К. Л., Чхатвал А. Р., Уильямс Дж. М. Дж.,
Прямое образование амидов из неактивированных карбоновых кислот и аминов. хим. коммун.
хим. коммун.
48,
666–668 (2012). [PubMed] [Академия Google]
11. Ланиган Р. М., Шеппард Т. Д.,
Последние разработки в области синтеза амидов: прямое амидирование карбоновых кислот и реакции трансамидирования. Евро. Дж. Орг. хим.
2013,
7453–7465 (2013). [Google Scholar]
12. Исихара К., Охара С., Ямамото Х.,
3,4,5-Трифторбензолбороновая кислота как чрезвычайно активный катализатор амидирования. Дж. Орг. хим.
61,
4196–4197 (1996). [PubMed] [Google Scholar]
13. Маки Т., Исихара К..
Ямамото Х.,
4,5,6,7-Тетрахлорбензо[ d ][1,3,2]диоксаборол-2-ол в качестве эффективного катализатора амидной конденсации стерически сложных карбоновых кислот. Орг. лат.
8,
1431–1434 (2006 г.). [PubMed] [Google Scholar]
14. Лундберг Х., Тиннис Ф., Адольфссон Х.,
Прямое амидное сочетание неактивированных карбоновых кислот и аминов, катализируемое хлоридом циркония (IV). хим. Евро. Дж.
18,
3822–3826 (2012). [PubMed] [Google Scholar]
15. Нода Х., Фурутачи М., Асада Ю. , Шибасаки М., Кумагаи Н.,
, Шибасаки М., Кумагаи Н.,
Уникальные физико-химические и каталитические свойства, обусловленные B 3 NO 2 Кольцевая система. Нац. хим.
9,
571–577 (2017). [PubMed] [Google Scholar]
16. Лундберг Х., Адольфссон Х.,
Катализируемое гафнием прямое образование амида при комнатной температуре. Катал.
5,
3271–3277 (2015). [Google Scholar]
17. Фатеми С., Гернигон Н., Холл Д. Г.,
Процедура прямого амидирования, катализируемого MIBA, с более низким коэффициентом E в масштабе нескольких граммов и ее применение для связывания альфа- и бета-аминокислот. Зеленый хим.
17,
4016–4028 (2015). [Академия Google]
18. Мохи Эль Дайн Т., Эрб В., Берхаут Ю., Руден Дж., Бланше Дж.,
Каталитический химический синтез амида при комнатной температуре: еще один шаг к синтезу пептидов. Дж. Орг. хим.
80,
4532–4544 (2015). [PubMed] [Google Scholar]
19. Арнольд К., Дэвис Б., Эро Д., Уайтинг А.,
Асимметричный прямой синтез амида путем кинетического разделения аминов: реакция, катализируемая хиральной бифункциональной аминобороновой кислотой, между рацемическим амином и ахиральной карбоновой кислотой. Ангью. хим. Междунар. Эд.
Ангью. хим. Междунар. Эд.
47,
2673–2676 (2008 г.). [PubMed] [Академия Google]
20. Аль-Зуби Р. М., Марион О., Холл Д. Г.,
Прямые и безотходные амидирования и циклоприсоединения путем органокаталитической активации карбоновых кислот при комнатной температуре. Ангью. хим. Междунар. Эд.
47,
2876–2879 (2008 г.). [PubMed] [Google Scholar]
21. Арнольд К., Дэвис Б., Джайлз Р. Л., Грожан К., Смит Г. Э., Уайтинг А.,
Катализировать или не катализировать? Изучение прямого образования амидной связи из аминов и карбоновых кислот в термических и катализируемых условиях. Доп. Синтез. Катал.
348,
813–820 (2006). [Академия Google]
22. Арнольд К., Бацанов А.С., Дэвис Б., Уайтинг А.,
Синтез, оценка и применение новых бифункциональных катализаторов N , N -диизопропилбензиламинбороновой кислоты для прямого образования амидов между карбоновыми кислотами и аминами. Зеленый хим.
10,
124–134 (2008). [Google Scholar]
23. Гернигон Н., Аль-Зуби Р. М., Холл Д. Г.,
Г.,
Прямое амидирование карбоновых кислот, катализируемое -орто--йодоарилбороновыми кислотами: оптимизация катализатора, объем и предварительное механистическое исследование, подтверждающее особый эффект ускорения галогена. Дж. Орг. хим.
77,
8386–8400 (2012). [PubMed] [Академия Google]
24. Исихара К., Лу Ю.,
Совместный катализ бороновой кислоты и ДМАПО для дегидратационной конденсации карбоновых кислот и аминов. хим. науч.
7,
1276–1280 (2016). [Бесплатная статья PMC] [PubMed] [Google Scholar]
25. Mylavarapu R.K., Kondaiah GCM, Kolla N., Veeramalla R., Koilkonda P., Bhattacharya A., Bandichhor R.,
Катализируемое борной кислотой амидирование в синтезе активных фармацевтических ингредиентов. Орг. Процесс Рез. Дев.
11,
1065–1068 (2007). [Академия Google]
26. Прат Д., Уэллс А., Хейлер Дж., Снеддон Х., МакЭлрой К.Р., Абу-Шехада С., Данн П.Дж.,
CHEM21 руководство по выбору классических и менее классических растворителей. Зеленый хим.
18,
288–296 (2016). [Google Scholar]
27. P. J. Dunn, K. K. Hii, M. J. Krische, M. T. Williams, in Sustainable Catalysis: Challenges and Practices for the Pharmaceutical and Fine Chemical Industries (Wiley, 2013), стр. 89–120. [Google Scholar]
P. J. Dunn, K. K. Hii, M. J. Krische, M. T. Williams, in Sustainable Catalysis: Challenges and Practices for the Pharmaceutical and Fine Chemical Industries (Wiley, 2013), стр. 89–120. [Google Scholar]
28. Старков П., Шеппард Т. Д.,
Боратные эфиры как удобные реагенты для прямого амидирования карбоновых кислот и переамидирования первичных амидов. Орг. биомол. хим.
9,
1320–1323 (2011). [PubMed] [Google Scholar]
29. Ланиган Р. М., Старков П., Шеппард Т. Д.,
Прямой синтез амидов из карбоновых кислот и аминов с использованием B(OCH 2 CF 3 ) 3 . Дж. Орг. хим.
78,
4512–4523 (2013). [Бесплатная статья PMC] [PubMed] [Google Scholar]
30. Cooper T.W.J., Campbell I.B., Macdonald S.J.F.,
Факторы, определяющие выбор органических реакций химиками-медиками и использование этих реакций в массивах (небольших целевых библиотеках). Ангью. хим. Междунар. Эд.
49,
8082–8091 (2010). [PubMed] [Google Scholar]
31. Кэри Дж. С. , Лаффан Д., Томсон К., Уильямс М. Т.,
, Лаффан Д., Томсон К., Уильямс М. Т.,
Анализ реакций, используемых для получения молекул-кандидатов в лекарства. Орг. биомол. хим.
4,
2337–2347 (2006 г.). [PubMed] [Google Scholar]
32. Ланиган Р. М., Каралука В., Сабатини М. Т., Старков П., Бэдленд М., Боултон Л., Шеппард Т. Д.,
Прямое амидирование незащищенных аминокислот с помощью B(OCH 2 CF 3 ) 3 . хим. коммун.
52,
8846–8849(2016). [PubMed] [Google Scholar]
33. Симоенс С.,
Лакосамид в качестве дополнительной терапии парциальных эпилептических припадков: обзор клинической и экономической литературы. Курс. Мед. Рез. мнение
27,
1329–1338 (2011). [PubMed] [Google Scholar]
34. Кинг А. М., Саломе К., Динсмор Дж., Саломе-Грожан Э., Де Рик М., Камински Р., Валаде А., Кон Х.,
Производные первичных аминокислот: соединения с противосудорожной и нейропатической активностью по защите от боли. Дж. Мед. хим.
54,
4815–4830 (2011). [PubMed] [Академия Google]
35. Ривз Дж. Т., Виско М. Д., Марсини М. А., Гринберг Н., Бузакка С. А., Матсон А. Э., Сенанаяке С. Х.,
Д., Марсини М. А., Гринберг Н., Бузакка С. А., Матсон А. Э., Сенанаяке С. Х.,
Общий метод образования имина с использованием B(OCH 2 CF 3 ) 3 . Орг. лат.
17,
2442–2445 (2015). [PubMed] [Google Scholar]
36. Чжао Х., Хуан З., Чен В.,
Полный синтез трикладинов А и В и определение их абсолютной конфигурации. Дж. Орг. хим.
79,
11290–11294 (2014). [PubMed] [Google Scholar]
37. Fennie M.W., Roth J.M.,
Сравнение реакций образования амидов с использованием показателей зеленой химии в студенческой органической лаборатории. Дж. Хим. Образовательный
93,
1788–1793 (2016). [Google Scholar]
38. Мохи Эль Дайн Т., Роуден Дж., Бланше Дж.,
Синтез пептидов, катализируемый бориновой кислотой. хим. коммун.
51,
16084–16087 (2015). [PubMed] [Google Scholar]
39. Бурес Дж.,
Анализ нормализации переменного времени: общее графическое объяснение порядков реакции из профилей концентрации. Ангью. хим. Междунар. Эд.
55,
16084–16087 (2016). [PubMed] [Google Scholar]
40. Бурес Дж.,
Бурес Дж.,
Простой графический метод определения порядка в катализаторе. Ангью. хим. Междунар. Эд.
55,
2028–2031 (2016). [Бесплатная статья PMC] [PubMed] [Google Scholar]
41. Лундберг Х., Тиннис Ф., Чжан Дж., Алгарра А.Г., Химо Ф., Адольфссон Х.,
Выяснение механизма прямого амидирования, катализируемого цирконием. Варенье. хим. соц.
139,
2286–2295 (2017). [PubMed] [Google Scholar]
42. Пелтер А., Левитт Т. Э., Нельсони П.,
Некоторые реакции образования амидов с участием борных реагентов. Тетраэдр
26,
1539–1544 (1970). [Google Scholar]
43. Коллум Д. Б., Чен С.-К., Ганем Б.,
Новый синтез амидов и макроциклических лактамов. Дж. Орг. хим.
43,
4393–4394 (1978). [Google Scholar]
44. Бурес Дж.,
Каков порядок реакции?
Верхний. Катал.
60,
631–633 (2017). [Google Scholar]
45. Колдуэлл Н., Джеймисон К., Симпсон И., Уотсон А. Дж. Б.,
Каталитическое амидирование неактивированных производных сложных эфиров с участием трифторэтанола. хим. коммун.
51,
9495–9498 (2015). [PubMed] [Google Scholar]
[PubMed] [Google Scholar]
46. McPherson C.G., Caldwell N., Jamieson C., Simpson I., Watson A.J.B.,
Амидирование неактивированных производных сложных эфиров опосредуется трифторэтанолом. Орг. биомол. хим.
15,
3507–3518 (2017). [PubMed] [Академия Google]
47. Марфей П.,
Определение D-аминокислот. II. Использование бифункционального реагента 1,5-дифтор-2,4-динитробензола. Карлсберг Рез. коммун.
49,
591–596 (1984). [Google Scholar]
48. Хименес-Гонсалес К., Пондер К.С., Брокстерман К.Б., Мэнли Дж.Б.,
Использование правильного зеленого критерия: почему массовая интенсивность процесса используется в фармацевтической промышленности для обеспечения более устойчивых процессов. Орг. Процесс Рез. Дев.
15,
912–917 (2011). [Google Scholar]
49. Шарма Н., Секар Г.,
Стабильный и многоразовый палладиевый катализатор на бинафтильном носителе для аминокарбонилирования арилиодидов. Доп. Синтез. Катал.
358,
314–320 (2016). [Академия Google]
50. Салехи П., Мотлах А. Р.,
Р.,
Перхлорат железа, нанесенный на силикагель: новый и эффективный реагент для однореакторного синтеза амидов из бензиловых спиртов. Синтез. коммун.
30,
671–675 (2000). [Google Scholar]
51. Каралука В., Ланиган Р. М., Мюррей П. М., Бэдленд М., Шеппард Т. Д.,
B(OCH 2 CF 3 ) 3 — опосредованное прямое амидирование фармацевтически значимых строительных блоков в циклопентилметиловом эфире. Орг. биомол. хим.
13,
10888–10894 (2015). [PubMed] [Академия Google]
52. Судта П., Кирк Н., Безос А., Гурлика А., Митчелл Р., Вебер Т., Уиллис А. К., Прабпай С., Конгсари П., Пэриш К. Р., Суксамран С., Келсо М. Дж.,
Синтез, структурная характеристика и предварительная оценка неиндолин-2-оновых ингибиторов ангиогенеза, связанных с сунитинибом (Сутент®). Ауст. Дж. Хим.
66,
864–873 (2013). [Google Scholar]
53. Агвада В. К.,
Потенциальные активные агенты центральной нервной системы. 2. Синтез N -бензилфенилацетамидов. Дж. Хим. англ. Данные
Данные
27,
481–483 (1982). [Google Scholar]
54. Моримото Х., Фудзивара Р., Симидзу Ю., Морисаки К., Ошима Т.,
Трифлат лантана (III) катализирует прямое амидирование сложных эфиров. Орг. лат.
16,
2018–2021 (2014). [PubMed] [Google Scholar]
55. Аспин С. Дж., Тайлемо С., Сир П., Шаретт А. Б.,
9-Силафлуоренилдихлориды как химически лигирующие связующие агенты и их применение в синтезе пептидов. Ангью. хим. Междунар. Эд.
55,
13833–13837 (2016). [PubMed] [Google Scholar]
56. Мамиллапалли Н. К., Секар Г.,
Хемоселективное восстановительное дезоксигенирование и восстановление α-кетоамидов с использованием палладиевого катализатора. Доп. Синтез. Катал.
357,
3273–3283 (2015). [Академия Google]
57. Уотсон А.Дж.А., Максвелл А.С., Уильямс Дж.М.Дж.,
Катализируемое рутением окисление спиртов в амиды. Орг. лат.
11,
2667–2670 (2009 г.). [PubMed] [Google Scholar]
58. Сароде П. Б., Бахекар С. П., Чандак Х. С.,
DABCO/AcOH совместно ускоряли катализируемое медью (I) циклоприсоединение азидов и алкинов к воде при комнатной температуре. Синлетт
Синлетт
27,
2681–2684 (2016). [Google Scholar]
59. Ясуда С., Кумагаи Н., Шибасаки М.,
Прямое асимметричное α-аллилирование кетонов аллиловыми спиртами через кооперативную функцию Pd/енамин. Гетероциклы
86,
745–757 (2012). [Академия Google]
60. Селкяля С. А., Коскинен А. М. П.,
Получение бицикло[4.3.0]нонанов органокаталитической внутримолекулярной реакцией Дильса–Альдера. Евро. Дж. Орг. хим.
2005 г.,
1620–1624 (2005 г.). [Google Scholar]
61. Mintz M.J., Walling C.,
т — Бутилгипохлорит. Орг. Синтез.
49,
9 (1969). [Google Scholar]
62. Чоу В.-К., Тан К.-В., Чен С.-Ф., Ку Х.,
Однореакторные чистые реакции сложных эфиров карбоновых кислот и алкилендиаминов для эффективного получения N -ацилалкилендиаминов. Дж. Орг. хим.
63,
10015–10017 (1998). [Google Scholar]
63. Шефера И., Опац Т.,
Пирролы и индолизины из депротонированных α-(алкилиденамино)нитрилов. Синтез
2011 г.,
1691–1704 (2011). [Google Scholar]
64. Bermudez J.

