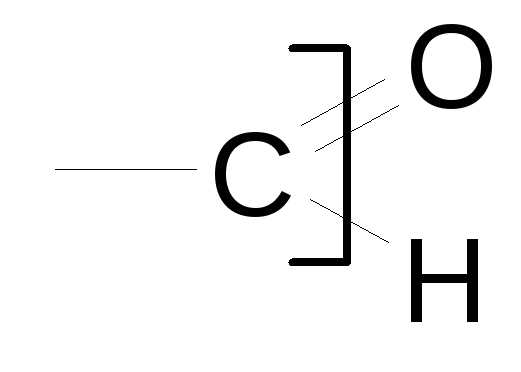
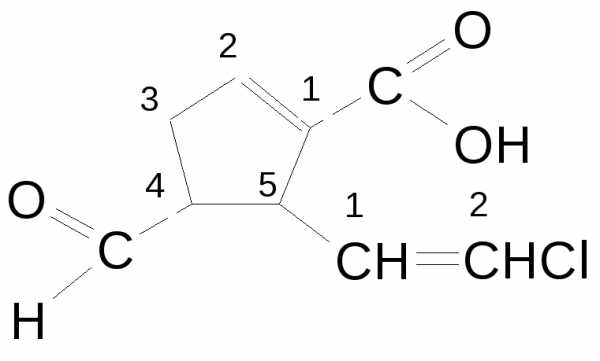
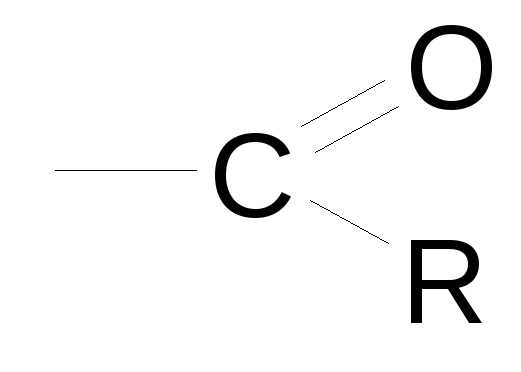
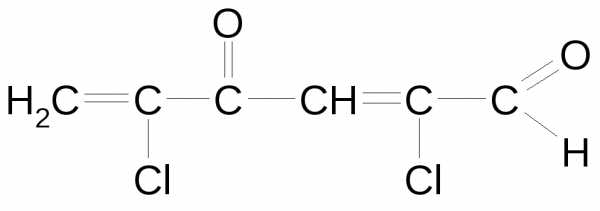
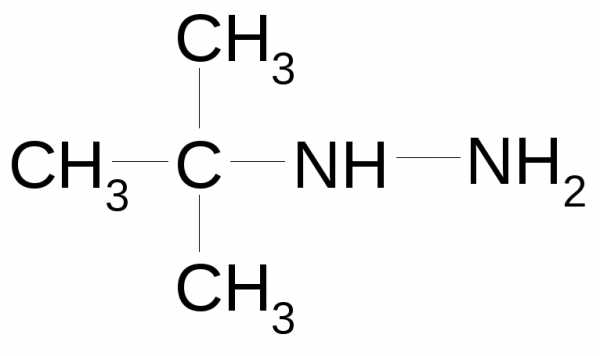
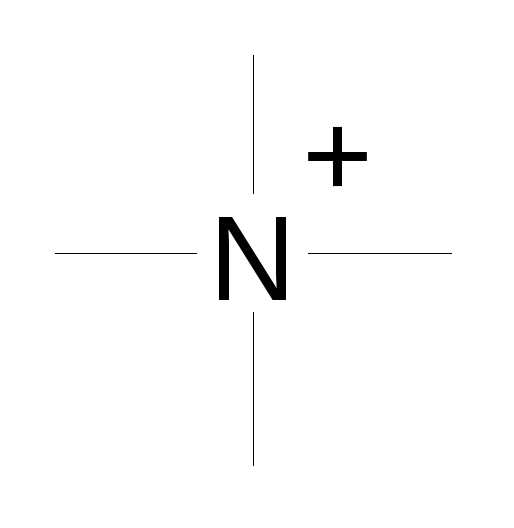Названия ненасыщенных и ароматических углеводородов. Дивиниловый эфир название июпак
Тривиальные названия органических веществ | Дистанционные уроки
09-Фев-2015 | Нет комментариев | Лолита Окольнова
Тривиальная номенклатура используется, в основном, в химии, биологии и в объединении этих двух дисциплин — медицине. Она появились задолго до введения общей системы IUAC (ИЮПАК), которая стала международным общепринятым и общепонятным вариантом.
Автор статьи — Саид Лутфуллин
Исторически тривиальные названия применялись для обозначения веществ, используемых в практической деятельности, и их названия отражали внешний вид или особое свойство, реальное или вымышленное.
Типичный пример – алмаз. По-гречески damasma – покорение, укрощение, damao – сокрушаю; соответственно, adamas – несокрушимый (интересно, что и по-арабски «аль-мас» – твердейший, самый твердый). Многие тривиальные названия введены алхимиками. Они могут иметь разный смысл в различных промышленных областях или регионах.
Надо понимать, что тривиальные названия любых веществ, не только органических, не отображают состав или химические свойства вещества.
Используют их не только профессионалы этих областей, но и мы — в быту
например, бытовое название сахар используется для обозначения дисахарида сахарозы, имеющего систематическое наименование α-D-глюкопиранозил-β-D-фруктофуранозид.
Здесь будут приведены названия веществ, встречающиеся в школьном курсе химии
Тривиальные названия органических веществ
| Тривиальное название | Структурная формула | Систематическое название |
| Ацетилен | CH ≡ CH | Этин |
| Анилин | Фениламин | |
| Бензиловый спирт | ||
| | Ch3 = CH — C ≡ CH | Бутен-1-ин-3 |
| Дивинил | h3C = CH — CH = Ch3 | Бутадиен-1,3 |
| Изобутан | 2-метилпропан | |
| Изопрен | 2-метилбутадиен-1,3 | |
| Крезол | Метилфенол | |
| Ксилол | Диметилбензол | |
| Кумол | Изопропилбензол | |
| Пирогаллол | 1,2,3-тригидроксибензол | |
| Пирокатехин | 1,2-дигидроксибензол | |
| Пропилен | Ch3 = CH- Ch4 | Пропен |
| Стирол | Винилбензол | |
| Толуол | Метилбензол | |
| Хлоропрен | 2-хлорбутадиен-1,3 | |
| Этилен | Сh3 = Ch3 | Этен |
| Глицерин | Пентантриол | |
| Глицерат меди | ||
| Нитроглицерин | ||
| Этиленгликоль | Этандиол | |
| Тротил* | * | 2,4,6 – тринитротолуол* |
| Название кислоты | Структурная формула | Систематическое название | Названия солей и эфиров |
| Муравьиная кислота | HCOOH | Метановая кислота* | Формиат |
| Уксусная кислота | Ch4COOH | Этановая кислота* | Ацетат |
| Пропионовая кислота | C2H5-COOH | Пропановая кислота* | Пропионат |
| Масляная кислота | C3H7-COOH | Бутановая кислота* | Бутират |
| Валериановая кислота | C4H9-COOH | Пентановая кислота* | Валерат |
| | C5h21-COOH | Гексановая кислота* | |
| Щавелевая кислота | HOOC-COOH | Этандиовая кислота* | Оксалат |
| Бензойная кислота | C6H5-COOH | Фенилуксусная кислота* | Бензоат |
| Акриловая кислота | h3C = CH-COOH | Пропеновая кислота* | Акрилат |
| Линолевая кислота | C17h41COOH | Линолеат | |
| Олеиновая кислота | C17h43COOH | Олеат | |
| Пальмитиновая кислота | C15h41COOH | Пальмитат | |
| Пикриновая кислота | | Пикрат* | |
| Стеариновая кислота | C17h45COOH | Стеарат | |
| Фталевая кислота | Фталат | ||
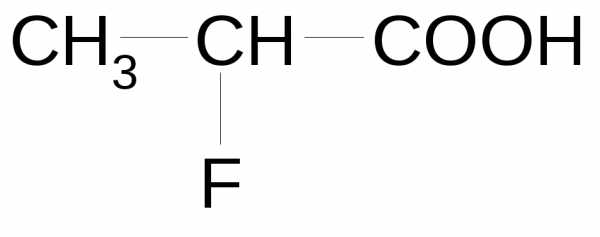
| Молочная кислота | 2-гидроксипропановая | Лактат | |
| Глицин | h3N-Ch3-COOH | Аминоуксусная кислота | Аминоацетат* |
| Аланин | 2-аминопропионовая кислота | Аминопропионат* |
| Название альдегида | Структурная формула | Систематическое название |
Формальдегид | HCOH | Метаналь |
| Ацетальдегид | Ch4COH | Этаналь |
| Название радикала | Структурная форма радикала |
| Изопропил | |
| Бензил | |
| Винил | h3C = CH — |
Еще больше тривиальных названий среди лекарственных средств. В справочниках можно встретить до десятка и более различных синонимов для одного и того же препарата, что связано в основном с фирменными названиями, принятыми в разных странах (например, отечественный пирацетам и импортный ноотропил, венгерский седуксен и польский реланиум и т.п.).
Еще на эту тему:
Обсуждение: "Тривиальные названия органических веществ"
(Правила комментирования)distant-lessons.ru
Номенклатура органических соединений
С развитием химической науки и появлением большого числа новых химических соединений все более возрастала необходимость в разработке и принятии понятной ученым всего мира системы их наименования, т.е. номенклатуры. Далее приведем обзор oсновных номенклатур органических соединений.
Тривиальная номенклатура
В истоках развития oрганической химии новым сoединениям приписывали тривиальные названия, т.е. названия сложившиеся исторически и нередко связанные со способом их получения, внешним видом и даже вкусом и т.п. Такая номенклатура органических соединений называется тривиальной. В таблице ниже приведены некоторые из соединений, сохранивших свои названия и в нынешние дни.
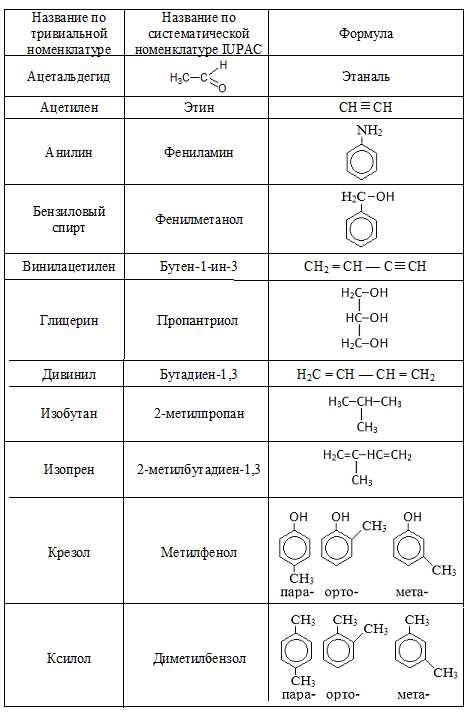
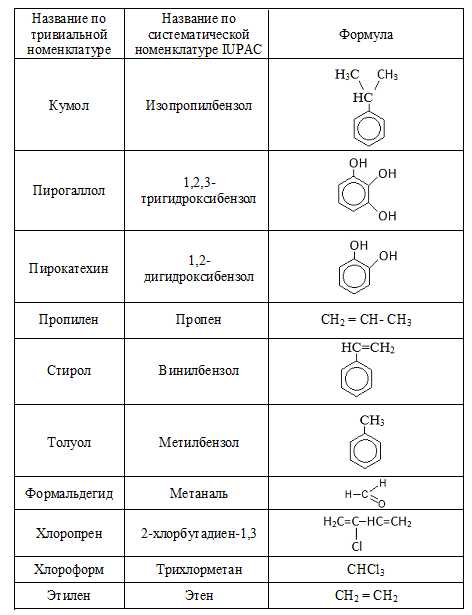
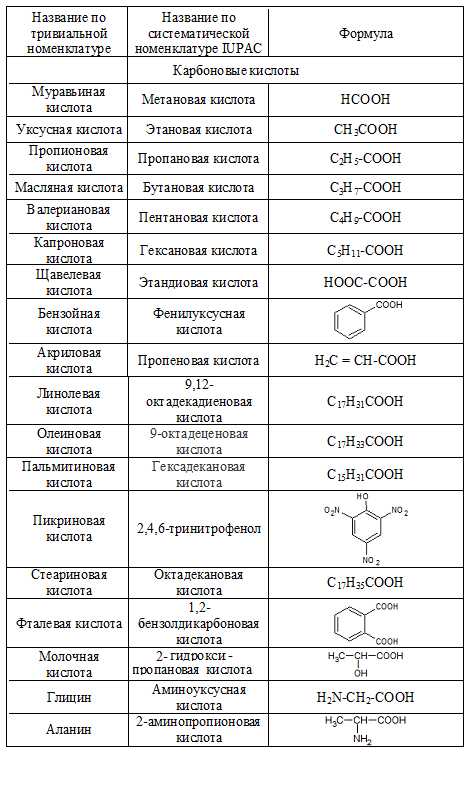 Рациональная номенклатура
Рациональная номенклатура
С расширением списка органических соединений, возникла необходимость связывать их название со строением. Базой рациональной номенклатуры органических соединений является наименование простейшего органического соединения. Например:
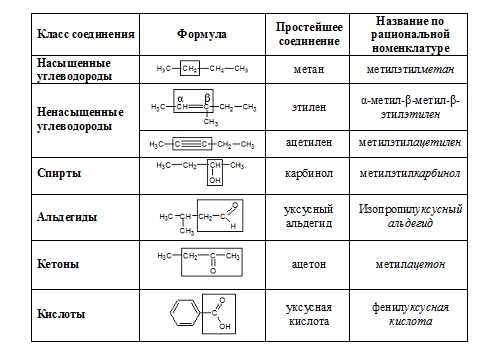
Однако, более сложным органическим соединениям невозможно приписать названия подобным способом. В этом случае следует называть соединения согласно правилам систематической номенклатуры ИЮПАК.
Систематическая номенклатура ИЮПАК
ИЮПАК (IUPAC) — Международный союз теоретической и прикладной химии (International Union of Pure and Applied Chemistry).
В данном случае, называя соединения, следует учитывать местоположение атомов углерода в молекуле и структурных элементов. Наиболее часто применяемой является заместительная номенклатура органических соединений, т.е. выделяется базовая основа молекулы, в которой атомы водорода замещены на какие-либо структурные звенья или атомы.
Прежде чем приступить к построению названий соединений, советуем выучить наименования числовых приставок, корней и суффиксов используемых в номенклатуре ИЮПАК.
А также названия функциональных групп: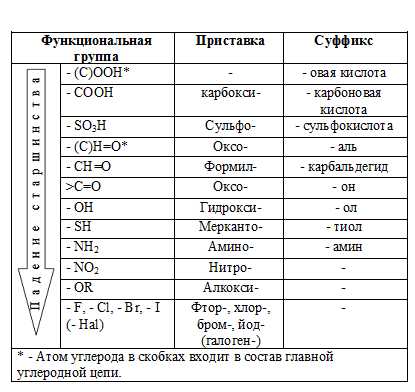
Для обозначения числа кратных связей и функциональных групп пользуются числительными:
Далее приведены наименования радикалов:
Предельные углеводородные радикалы:
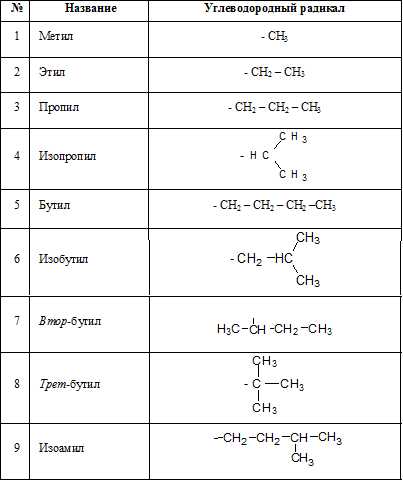
Непредельные углеводородные радикалы:
Ароматические углеводородные радикалы:
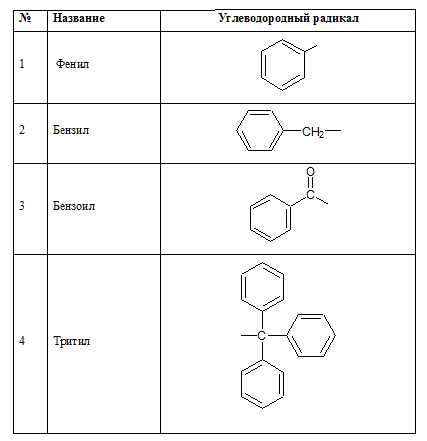
Кислородсодержащие радикалы:
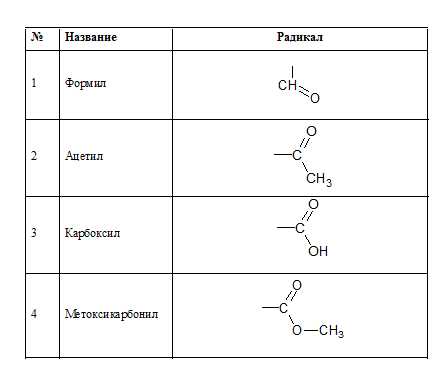
Правила построения названия органического соединения по номенклатуре ИЮПАК:
- Выбрать главную цепь молекулы
Определить все присутствующие функциональные группы и их старшинство
Определить наличие кратных связей
- Пронумеровать главную цепь, причем нумерацию следует начинать с наиболее близкому к старшей группе конца цепи. При существовании нескольких таких возможностей, нумеруют цепь так, чтобы минимальный номер получили или кратная связь, или другой заместитель, присутствующий в молекуле.
Карбоциклические соединения нумеруют начиная со связанного со старшей характеристической группой атома углерода. При наличии двух и более заместителей цепь стараются пронумеровать так, чтобы заместителям принадлежали минимальные номера.
- Составить название соединения:
— Определить основу названия соединения, составляющего корень слова, который обозначает предельный углеводород с тем же количеством атомов, что и главная цепь.
— После основы названия следует суффикс, показывающий степень насыщенности и количество кратных связей. Например, — тетраен, — диен. При отсутствии кратных связей используют суффикс – ск.
— Далее арабскими цифрами показывают местоположение кратных связей. Например, гексин – 2.
— Затем, также в суффикс добавляется наименование самой старшей функциональной группы.
— После следует перечисление заместителей в алфавитном порядке с указанием их местоположения арабской цифрой. Например, — 5-изобутил, — 3-фтор. При наличии нескольких одинаковых заместителей указывают их количество и положение, например, 2,5 – дибром-, 1,4,8-тримети-.
Следует учесть, что цифры отделяются от слов дефисом, а между собой – запятыми.
В качестве примера дадим название следующему соединению:
1. Выбираем главную цепь, в состав которой обязательно входит старшая группа – СООН.
Определяем другие функциональные группы: — ОН, — Сl, — SH, — Nh3.
Кратных связей нет.
2. Нумеруем главную цепь, начиная со старшей группы.
3. Число атомов в главной цепи – 12. Основа названия – метиловый эфир додекановой кислоты.
Далее обозначаем и называем все функциональные группы в алфавитном порядке:
10-амино-6-гидрокси -7-хлоро-9-сульфанил-метиловыйэфир додекановой кислоты.
Или
10-амино-6-гидрокси-7-хлоро-9-сульфанил-метилдодеканоат
Номенклатура оптических изомеров
- В некоторых классах соединений, таких как альдегиды, окси- и аминокислоты для обозначения взаимного расположения заместителей используют D,L – номенклатуру. Буквой D обозначают конфигурацию правовращающего изомера, L – левовращающего.
В основе D,L-номенклатуры органических соединений лежат проекции Фишера:
- чтобы определить конфигурации изомеров α-аминокислот и α- оксикислот вычленяют «оксикислотный ключ», т.е. верхние части их проекционных формул. Если гидроксильная (амино-) группа расположена справа, то это D-изомер, слева L-изомер.
Например, представленная ниже винная кислота имеет D — конфигурацию по оксикислотному ключу:
- чтобы определить конфигурации изомеров сахаров вычленяют «глицериновый ключ», т.е. сравнивают нижние части (нижний асимметрический атом углерода) проекционной формулы сахара с нижней частью проекционной формулы глицеринового альдегида.
Обозначение конфигурации сахара и направление вращения аналогично конфигурации глицеринового альдегида, т.е. D – конфигурации соответствует расположение гидроксильной группы расположена справа, L – конфигурации – слева.
Так, например, ниже представлена D-глюкоза.
2) R -, S-номенклатура (номенклатура Кана, Ингольда и Прелога)
В данном случае заместители при асимметрическом атоме углерода располагаются по старшинству. Оптических изомеры имеют обозначения R и S, а рацемат — RS.
Для описания конфигурации соединения в соответствии с R,S-номенклатурой поступают следующим образом:
- Определяют все заместители у асимметричного атома углерода.
- Определяют старшинство заместителей, т.е. сравнивают их атомные массы. Правила определения ряда старшинства те же, что и при использовании E/Z-номенклатуры геометрических изомеров.
- Ориентируют в пространстве заместители так, чтобы младший заместитель (обычно водород) находился в наиболее отдаленном от наблюдателя углу.
- Определяют конфигурацию по расположению остальных заместителей. Если движение от старшего к среднему и далее к младшему заместителю (т.е. в порядке уменьшения старшинства) осуществляется по часовой стрелке, то это R конфигурация, против часовой стрелки — S-конфигурация.
В таблице ниже приведен перечень заместителей, расположенных в порядке возрастания их старшинства:
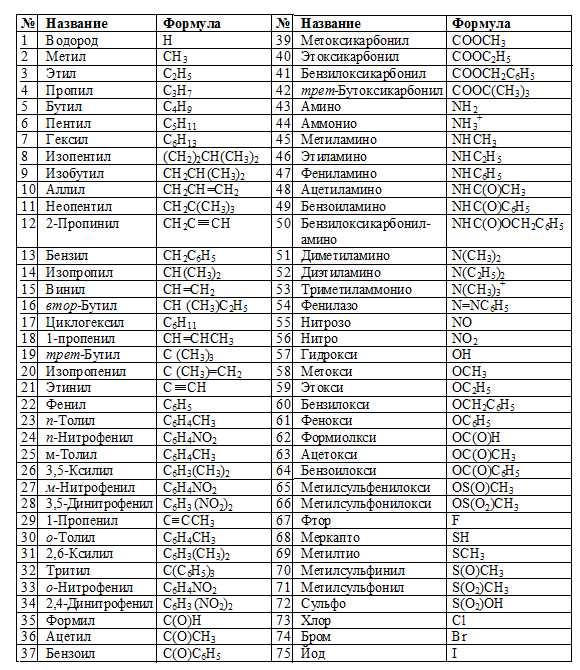
zadachi-po-khimii.ru
Тривиальные названия неорганических и органических веществ




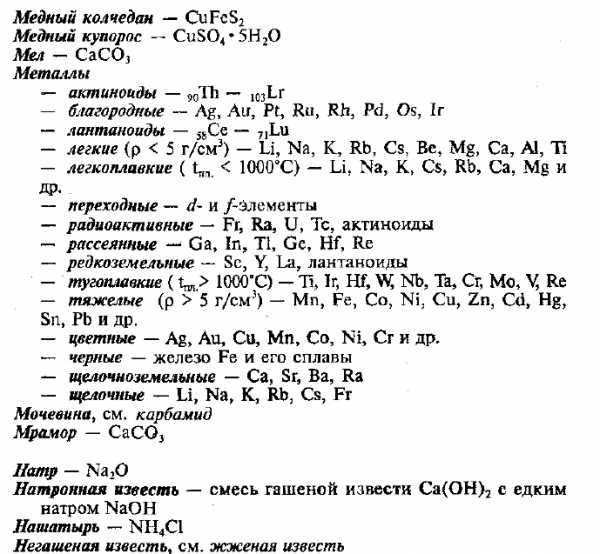



| Тривиальное название | Структурная формула | Систематическое название |
| Ацетилен | CH ≡ CH | Этин |
| Анилин | Фениламин | |
| Бензиловый спирт | ||
| Винилацетилен | Ch3 = CH — C ≡ CH | Бутен-1-ин-3 |
| Дивинил | h3C = CH — CH = Ch3 | Бутадиен-1,3 |
| Изобутан | 2-метилпропан | |
| Изопрен | 2-метилбутадиен-1,3 | |
| Крезол | Метилфенол | |
| Ксилол | Диметилбензол | |
| Кумол | Изопропилбензол | |
| Пирогаллол | 1,2,3-тригидроксибензол | |
| Пирокатехин | 1,2-дигидроксибензол | |
| Пропилен | Ch3 = CH- Ch4 | Пропен |
| Стирол | Винилбензол | |
| Толуол | Метилбензол | |
| Хлоропрен | 2-хлорбутадиен-1,3 | |
| Этилен | Сh3 = Ch3 | Этен |
| Глицерин | Пропантриол-1,2,3 | |
| Глицерат меди | ||
| Нитроглицерин | ||
| Этиленгликоль | Этандиол | |
| Тротил* | 2,4,6 – тринитротолуол |
| Название кислоты | Структурная формула | Систематическое название | Названия солей и эфиров |
| Муравьиная кислота | HCOOH | Метановая кислота | Формиат |
| Уксусная кислота | Ch4COOH | Этановая кислота | Ацетат |
| Пропионовая кислота | C2H5-COOH | Пропановая кислота | Пропионат |
| Масляная кислота | C3H7-COOH | Бутановая кислота | Бутират |
| Валериановая кислота | C4H9-COOH | Пентановая кислота | Валерат |
| Капроновая кислота | C5h21-COOH | Гексановая кислота | |
| Щавелевая кислота | HOOC-COOH | Этандиовая кислота | Оксалат |
| Бензойная кислота | C6H5-COOH | Фенилуксусная кислота | Бензоат |
| Акриловая кислота | h3C = CH-COOH | Пропеновая кислота | Акрилат |
| Линолевая кислота | C17h41COOH | Линолеат | |
| Олеиновая кислота | C17h43COOH | Олеат | |
| Пальмитиновая кислота | C15h41COOH | Пальмитат | |
| Пикриновая кислота | 2,4,6-тринитрофенол | Пикрат | |
| Стеариновая кислота | C17h45COOH | Стеарат | |
| Фталевая кислота | Фталат | ||
| Молочная кислота | 2-гидроксипропановая | Лактат | |
| Глицин | h3N-Ch3-COOH | Аминоуксусная кислота | Аминоацетат |
| Аланин | 2-аминопропионовая кислота | Аминопропионат |
| Название альдегида | Структурная формула | Систематическое название |
| Формальдегид | HCOH | Метаналь |
| Ацетальдегид | Ch4COH | Этаналь |
| Название радикала | Структурная форма радикала |
| Изопропил | |
| Бензил | |
| Винил | h3C = CH — |
Александр Коньков, автор и основатель первого в СНГ проекта по видео-подготовке к ЦТ и ЕГЭ по химии «Your System Education»
www.yoursystemeducation.com
4.1. Спирты
Спиртами называются органические соединения, молекулы которых содержат одну или несколько гидроксильных групп (–ОН), соединенных с углеводородными радикалами.
Классификация спиртов
I. В зависимости от числа гидроксильных групп:
| Одноатомные спирты | Многоатомные спирты |
| СН3– ОН | СН2– СН – СН2 ОН ОН ОН |
| метанол (метиловый спирт) | пропантриол-1,2,3 (глицерин) |
II. По насыщенности углеводородного радикала:
| Предельные спирты | Непредельные спирты |
| СН3– СН2 – СН2– ОН пропанол-1 | СН2= СН – ОН виниловый спирт (этенол) |
| Атомы углерода связаны только одинарными связями | Имеются кратные связи между атомами углерода |
III. По характеру углеводородного радикала, связанного с ОН- группой:
| Первичные спирты | Вторичные спирты | Третичные спирты |
| СН3– СН2 –СН2– ОН пропанол-1 (пропиловый спирт) | СН3– СН–СН3 ОН пропанол-2 (изопропиловый спирт) | СН3 СН3– СН–СН3 ОН 2-метилпропанол-2 (третбутиловый спирт) |
4.1.1. Предельные одноатомные спирты
Общая формула предельных одноатомных спиртов Сnh3n+1OH.
Номенклатура
Используются два возможных названия класса спиртов:“спирты” (от лат. “ спиритус” – дух) и “алкоголи” (арабск.).
По международной номенклатуре название спиртов образуется от названия соответствующего углеводорода с добавлением суффикса ол:
СН3ОН метанол
С2Н5ОН этанол
Главная цепь углеродных атомов нумеруется с того конца, к которому ближе гидроксильная группа:
5СН3–4СН –3СН2–2СН – ОН
СН31СН34-метилпентанол-2
Для некоторых спиртов применяются тривиальные названия:
| Спирт | Номенклатура ИЮПАК | Тривиальное название |
| СН3ОН | метанол | метиловый спирт |
| С2Н5ОН | этанол | этиловый спирт |
| СН3– СН2– СН2– ОН | пропанол-1 | н-пропиловый спирт |
| СН3– СН – СН3 ОН | пропанол-2 | изопропиловый спирт |
| СН3– СН2– СН2– СН2– ОН | бутанол-1 | н-бутиловый спирт |
| СН3– СН – СН2– СН3 ОН | бутанол-2 | втор-бутиловый спирт |
| СН3– СН – СН2– ОН СН3 | 2-метилпропанол-1 | изобутиловый спирт |
| СН3 СН3– СН – СН3 ОН | 2-метилпропанол-2 | трет-бутиловый спирт |
Изомерия спиртов
Строение спиртов зависит от строения радикала и положения функциональной группы, т.е. в гомологическом ряду спиртов может быть два вида изомерии: изомерия углеродного скелета и изомерия положения функциональной группы.
Кроме этого, третьим видом изомерии спиртов является межклассовая изомерия с простыми эфирами.
Так, для пентанолов (амиловых спиртов) С5Н11ОН изомерами являются:
1. Изомерия скелета
СН3– СН2– СН2– СН2– СН2– ОН пентанол-1
СН3– СН – СН2– СН2–ОН 3-метилбутанол-1
СН3
СН3– СН2– СН – СН2–ОН 2-метилбутанол-1
СН3
СН3
СН3– СН – СН2– ОН 2,2-диметилпропанол-1
СН3
Приведенные выше изомеры амилового спирта носят тривиальное название “сивушные масла”.
2. Изомерия положения гидроксильной группы
СН3– СН2– СН2– СН2– СН2– ОН пентанол-1
СН3– СН – СН2– СН2–СН2пентанол-2
ОН
СН3– СН2– СН – СН2–СН2пентанол-3
ОН
3. Межклассовая изомерия
С2Н5– О – С3Н7этилпропиловый эфир
Число изомеров в ряду спиртов быстро растет: спирт с 5 атомами углерода имеет 8 изомеров, с 6 атомами углерода – 17, с 7 атомами углерода – 39, а с 10 атомами углерода – 507.
Способы получения спиртов
1. Получение метанола из синтез-газа
4000С,ZnO,Cr2O3
СО + 2Н2СН3ОН
2. Гидролиз галогенуглеводородов (в водных растворах щелочей):
СН3– СН – СН3+ КOНводный СН3– СН – СН3+ КCl
ClОН
2-хлорпропан пропанол-2
3. Гидратация алкенов. Реакция идет по правилу В.В. Марковникова.
Катализатор – Н2SO4 разбавленная.
СН2= СН2+ НОНСН3– СН2- ОН
этилен этанол
СН2= СН – СН3+ НОНСН2– СН – СН3
пропен пропанол-2
Н ОН
4. Восстановление карбонильных соединений (альдегидов и кетонов):
При восстановлении альдегидов получаются первичные спирты:
СН3– СН2– С = О + Н2СН3– СН2– СН2– ОН
пропанол-1
Н
пропаналь
При восстановлении кетонов получаются вторичные спирты:
Ch4–C–Ch4+ Н2СН3– СН – СН3
II пропанон
О (ацетон) ОН пропанол-2
5. Получение этанола брожением сахаристых веществ:
ферменты ферменты
С12Н22О11+ Н2О2С6Н12О64С2Н5ОН + 4СО2
сахароза глюкоза этанол
ферменты ферменты
(С6Н10О5)n+ Н2ОnС6Н12О6 С2Н5ОН + СО2
целлюлоза глюкоза этанол
Спирт, полученный брожением целлюлозы, называется гидролизным спиртом и применяется только для технических целей, т.к. содержит большое количество вредных примесей – метанола, уксусного альдегида, сивушных масел.
6. Гидролиз сложных эфиров
Н+или ОН–
СН3– С – О– СН2– СН2–СН3+ Н2ОСН3 – С – ОН + ОН – СН2– СН2–СН3
ll ll
О О
пропиловый эфир уксусной кислоты уксусная пропанол-1
(пропилэтаноат) кислота
7. Восстановление сложных эфиров
4[Н]
СН3– С – О– СН2– СН2–СН3СН3 – Сh3– ОН + ОН – СН2– СН2–СН3
ll этанол пропанол-1
О
пропиловый эфир уксусной кислоты
(пропилэтаноат)
Физические свойства спиртов
Таблица 4.2.
Показатели пожарной опасности спиртов
| Спирты | , кг/м3 | tкипения | tсамовоспл. | tвспышки | ТПР | |
| СН3ОН | н-метанол | 731 | 64,7 | 464 | 8 | 7 – 39 |
| С2Н5ОН | н-этанол | 793 | 78,4 | 404 | 13 | 11 – 41 |
| С3Н7ОН | н-пропанол | 804 | 97,8 | 370 | 23 | 20 – 53 |
| С4Н9ОН | н-бутанол | 809 | 117,4 | 345 | 34 | 31 – 60 |
| С5Н11ОН | н-пентанол | 814 | 138 | 300 | 40 | 38 - 80 |
Предельные спирты, содержащие С1 – С12 представляют собой жидкости, С13 – С20 – маслообразные (мазеобразные вещества), > С21 – твердые вещества.
Низшие спирты С1 – С3 имеют специфический алкогольный запах, С4 – С5 – сладкий удушливый запах, > С6 – запаха не имеют.
В воде хорошо растворяются метиловый, этиловый и пропиловый спирты. С увеличением молекулярной массы растворимость спиртов в воде падает.
Существенно более высокая температура кипения спиртов по сравнению с углеводородами, содержащими такое же число атомов углерода (например, tкипения (СН4) = – 1610С, а tкипения (СН3ОН) = 64,70С) связана со способностью спиртов образовывать водородные связи, а следовательно, и способностью молекул к ассоциации.
Н – О Н – О Н – О R– радикал спирта
\ \ \
RRR
При растворении спирта в воде также возникают водородные связи между молекулами спирта и воды. В результате этого процесса происходит выделение энергии и уменьшение объема. Так, при смешении 52 мл этанола и 48 мл воды общий объем образующегося раствора будет не 100 мл, а лишь 96,3 мл.
Пожарную опасность представляют как чистые спирты (особенно низшие), пары которых могут образовывать взрывоопасные смеси, так и водные растворы спиртов. Водные растворы этанола в воде с концентрацией спирта более 25 % и более являются легковоспламеняющимися жидкостями.
Химические свойства спиртов
Химические свойства определяются реакционной способностью гидроксильной группы и строением радикала, связанного с гидроксильной группой.
1. Реакции гидроксильного водорода R – О – Н
За счет электроотрицательности атома кислорода в молекулах спиртов имеет место частичное распределение зарядов:
– +
R– О – Н
Водород обладает определенной подвижностью и способен вступать в реакции замещения.
Взаимодействие со щелочными металлами – образование алкоголя
тов:
2СН3– СН – СН3+ 2Na2СН3– СН – СН3+ Н2
ОН ОNa
пропанол-2 изопропилат натрия
(натриевая соль пропанола-2)
Соли спиртов – алкоголяты – представляют собой твердые вещества. При их образовании спирты выступают как очень слабые кислоты.
Алкоголяты легко подвергаются гидролизу:
С2Н5ОNa+ НОНС2Н5ОН +NaОН
этилат натрия
Взаимодействие с карбоновыми кислотами – реакция этерификации - образование сложных эфиров:
Н2SO4 конц.
СН3– СН – ОН + НО – С – СН3СН3– СН – О – С – СН3+ Н2О
ll ll изопропилацетат
СН3О СН3О (изопропиловый эфир
уксусная кислота уксусной кислоты)
1.3. Взаимодействие с неорганическими кислотами:
СН3– СН – ОН + НО –SO2OHСН3– СН – О –SO2OH+h3O
серная кислота изопропилсерная кислота
Ch4Ch4 (изопропиловый эфир серной ксилоты)
1.4. Межмолекулярная дегидратация – образование простых эфиров:
Н2SO4конц.,t< 1400C
СН3– СН – ОН + НО – СН – СН3СН3– СН – О – СН – СН3+ Н2О
СН3 СН3 СН3 СН3
диизопропиловый эфир
2. Реакции гидроксильной группы R – ОН
2.1. Взаимодействие с галогеноводородами:
Н2SO4 конц.
СН3– СН – СН3+HClСН3– СН – СН3+h3O
OHCl2-хлорпропан
2.2. Взаимодействие с галогенпроизводными фосфора:
СН3– СН – СН3+ РCl5СН3– СН – СН3+ РОCl3+ НCl
OHCl2-хлорпропан
2.3. Внутримолекулярная дегидратация – получение алкенов:
Н2SO4конц.,t> 1400C
СН3– СН – СН2 СН3– СН = СН2+ Н2О
пропен
ОН Н
При дегидратации несимметричной молекулы отщепление водорода идет преимущественно от наименее гидрогенизированного атома углерода – правило А.М. Зайцева.
3. Реакции окисления.
3.1. Полное окисление – горение:
С3Н7ОН + 4,5О23СО2+ 4Н2О
Частичное (неполное) окисление.
Окислители – КMnO4, K2Cr2O7 + h3SO4, катализаторы Cu, Pt.
При окислении первичных спиртов образуются альдегиды:
ОH
СН3– СН2– СН2 – ОН+ [O][СН3– С – ОН]СН3– СН2– С = О+ Н2О
пропанол-1
HН
пропаналь
Реакция окисления метанола при попадании этого спирта в организм – пример так называемого “ летального синтеза”. Сам метиловый спирт – относительно безвредное вещество, но в организме в результате окисления он превращается в чрезвычайно ядовитые вещества – метаналь (формальдегид) и муравьиную кислоту. В результате попадание в организм уже 10 г метанола приводит к потере зрения, а 30 г – к смерти.
Реакция спирта с оксидом меди (II) может использоваться как качественная реакция на спирты.
СН3– СН2– СН2 – ОН+CuOСН3– СН2– С = О+Cu+ Н2О
пропанол-1 черн. красн.
в-во H
пропаналь
В результате частичного окисления вторичных спиртов образуются кетоны:
OH
СН3– СН – СН3 + [O][СН3– С – СН3]СН3– С – СН3 + Н2О
ll
ОН OHО
пропанол-2 пропанон
(ацетон)
Третичные спирты при таких условиях не окисляются, а при окислении в более жестких условиях происходит расщепление молекулы, и при этом образуется смесь карбоновых кислот.
Применение спиртов
Спирты используют в качестве органических растворителей.
Метанол получают в большом объеме и используют для приготовления красителей, незамерзающих смесей, как источник для производства различных полимерных материалов (получение формальдегида). Следует помнить, что метанол сильно токсичен.
Этиловый спирт – первое органическое вещество, которое было выделено в чистом виде в IX веке в Египте.
В настоящее время этанол – многотоннажный продукт химической промышленности. Он применяется для получения синтетического каучука, органических красителей, изготовления фармацевтических препаратов. Кроме этого, этиловый спирт используется как экологически чистое горючее. Этанол употребляется при изготовлении алкогольных напитков.
Этанол – наркотик, возбуждающе действующий на организм; его длительное и неумеренное употребление приводит к алкоголизму.
Бутиловые и амиловые спирты используются в промышленности как растворители и для синтеза сложных эфиров. Все они обладают значительной токсичностью.
Спирты, содержащие в радикале более 10 атомов углерода, относятся к высшим алифатическим спиртам. В свободном виде в природе они не встречаются, а встречаются в виде сложных эфиров в восках, кашалотовом и шерстяном жирах. Высшие жирные спирты применяются для изготовления поверхностно-активных веществ.
studfiles.net
Систематическая международная номенклатура (ИЮПАК) | Химия онлайн
Систематическая номенклатура является научной и отражает состав, химическое и пространственное строение соединения.
В правилах ИЮПАК используется несколько типов номенклатур,наиболее универсальная и распространенная из них – заместительная. Для веществ несложного строения часто применяется радикально-функциональный способ.
В заместительной номенклатуре основой названия служит один углеводородный фрагмент, а другие рассматриваются как заместители водорода (см. ниже).
В радикально-функциональной номенклатуре в основе названия лежит название функциональной группы, определяющей химический класс соединения, к которому присоединяют наименование органического радикала, например:
С2Н5ОН – этиловый спирт
С2Н5Cl – этилхлорид
СН3-О-С2Н5 – метилэтиловый эфир
СН3-СО-СН=СН2 — метилвинилкетон
Правила составления названий по систематической международной номенклатуре ИЮПАК
В основе правил номенклатуры ИЮПАК лежат принципы заместительной номенклатуры.
1. Основу названия соединения составляет корень слова, обозначающий предельный углеводород с тем же числом атомов, что и главная цепь (мет- , эт- , проп- , бут- , пент- , гекс- и т.д.).
2. К корню добавляют суффикс, характеризующий степень насыщенности:
-ан (предельный, нет кратных связей);
-ен (при наличии двойной связи);
-ин (при наличии тройной связи).
Если кратных связей несколько, то в суффиксе указывается число таких связей ( -диен, триен и т.д.), а после суффикса обязательно указывается цифрами положение кратной связи, например:
СН3 –СН2 –СН=СН2 бутен-1
СН3 –СН=СН–СН3 бутен-2
СН2 =СН–СН=СН2 бутадиен-1,3
3. Далее в суффикс выносится название самой старшей характеристической группы в молекуле с указанием ее положения цифрой.
4. Прочие заместители обозначаются с помощью приставок в алфавитном порядке. Положение заместителей указывается цифрой перед приставкой, например: 3-метил, 2-хлор. Если в молекуле имеется несколько одинаковых заместителей, то перед названием этой группы словом указывается их количество (например, диметил- , трихлор- и т.д.).
5. Все цифры в названиях молекул отделяются от слов дефисом, а друг от друга запятыми.
6. Проводят нумерацию главной углеродной цепи так, чтобы старшая характеристическая группа имела наименьший порядковый номер.
Как назвать соединение?
Называем заместители в главной цепи
Нумеруем главную цепь
Строим название соединения
Примеры
1.Выбрать самую длинную цепь (корень слова – пент). Далее следует суффикс –ен, указывающий на наличие кратной связи.
2. Порядок нумерации определяет старшая группа (-ОН) – наименьший номер.
3.Полное название соединения заканчивается суффиксом, обозначающим старшую группу (суффикс –ол указывает на налчие гидроксильной группы). Положение двойной связи и гидроксильной группы указывается цифрами.
Соединение называется пентен-4-ол-2.
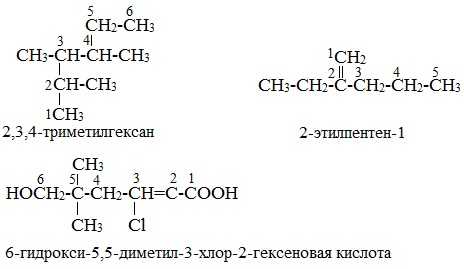
Названия характеристических групп (перечислены в порядке убывания старшинства)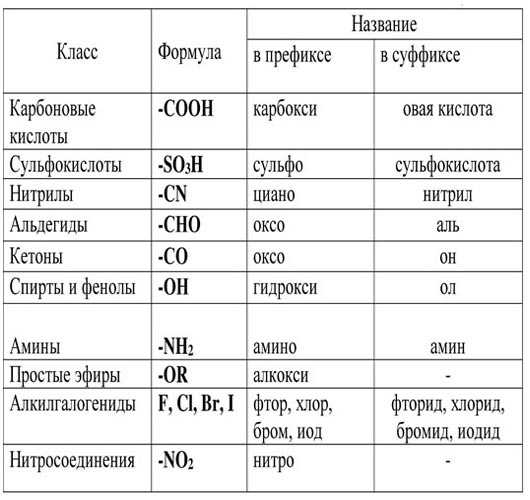
Номенклатура органических соединений
himija-online.ru
Номенклатура и изомерия спиртов — Мегаобучалка
Кислородсодержащие органические соединения
· Спирты,
· Простые эфиры,
· Альдегиды,
· Кетоны,
· Карбоновые кислоты, их ангидриды и галогенангидриды
· Сложные эфиры,
· Фенолы и их простые эфиры.
Спирты
К спиртам относятся соединения, содержащие функциональную группу -OH, связанную с алифатическим радикалом.
Например, Ch3=CH-Ch3-OH, HC≡C-Ch3-OH, Ch4-OH.
аллиловый спирт пропаргиловый спирт метанол
В радикал, соединенный с группой –OH, может входить так же остаток ароматического углеводорода, если он отделён, по крайней мере, одной метиленовой группой.
| бензиловый спирт |
Классификация спиртов
I. По типу атомов углерода, контактирующих с функциональной группой –OH различают первичные , вторичные и третичные спирты.
| Вторичный спирт |
| Первичный спирт |
| Третичный спирт |
Исключение: Ch4-OH (метанол) –он тоже первичный спирт.
II. По количеству гидроксильных групп различают одноатомные, трёхатомные, многоатомные, полиатомные спирты, например:
| (1,2 – этандиол) |
| (1, 2, 3 - пропантриол) глицерин |
| (пентаэритрит) |
| трёхатомный |
| четырёхатомный |
| (поливиниловый спирт) |
Номенклатура и изомерия спиртов
По номенклатуре ИЮПАК в структурной формуле спирта находится самая длинная цепь из атомов углерода, обязательно включающая атом углерода, связанный с гидроксильной группой. Эта цепь нумеруется с той стороны, к которой ближе гидроксил. Сначала называются алкильные радикалы с указанием их места положения в цепи, затем название алкана соответствующего длине выбранной цепи, после чего добавляется окончание спиртов – «ол».
По рациональной номенклатуре атом углерода и связанный с ним гидроксил получают название «карбинол».Сначала называются алкильные радикалы, соединённые с упомянутым выше атомом углерода, а затем слитно слово «карбинол». Ниже в таблице приведены названия спиртов с брутто-формулой С5Н12О по этим видам номенклатур, а также тривиальные (то есть исторически сложившиеся) их названия.
Контрольное задание: написать структурные формулы спиртов C6h24O и дать им названия по номенклатуре ИЮПАК и по рациональной номенклатуре.
megaobuchalka.ru
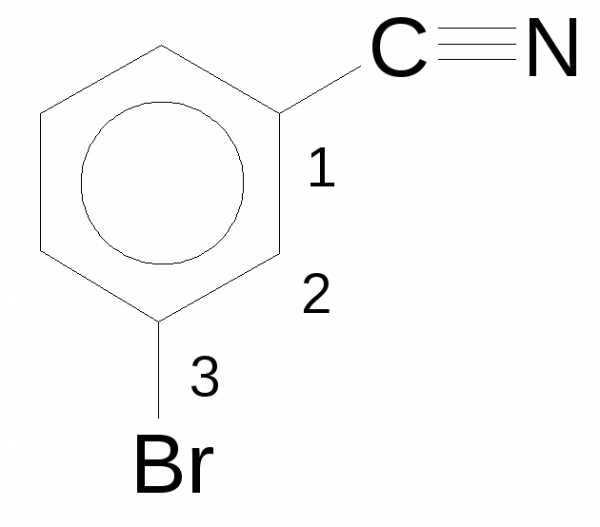
Названия ненасыщенных и ароматических углеводородов
В главную цепь обязательно входит двойная связь с наименьшим порядковым номером. Окончание названия суффикс «ен» (алкены).
Название ненасыщенного углеводородного заместителя строится также, как и насыщенного, нумерацию проводят от свободнойвалентности:
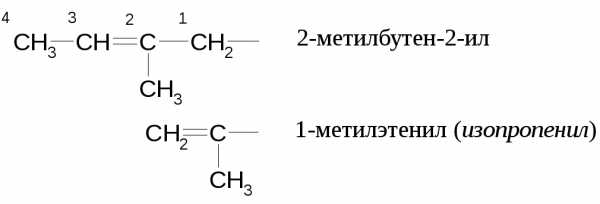
Соединения с одной тройной связью, алкины:
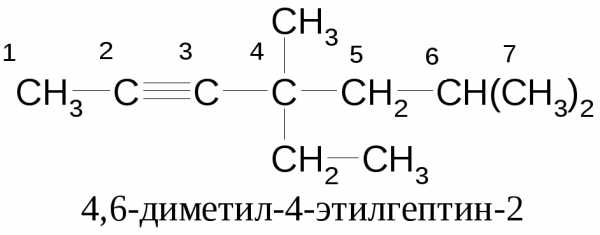
Положению тройной связи - наименьший номер.
Пример названия углеводородного заместителя с тройнойсвязью:
Названия ненасыщенных карбоциклическихуглеводородов
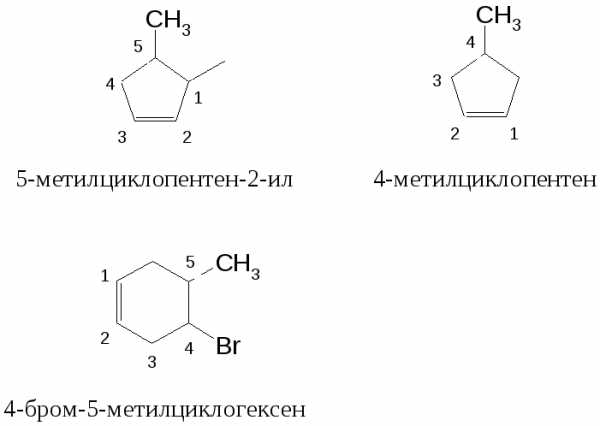
Названия осуществляют по принципам номенклатуры алкенов с применением умножительной приставки «ди-».
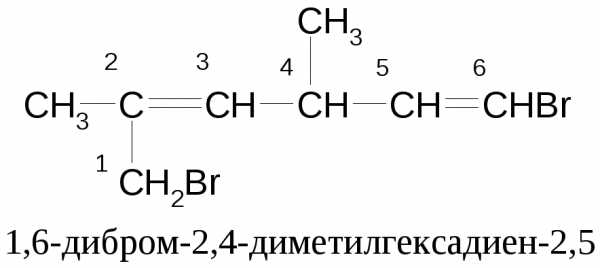
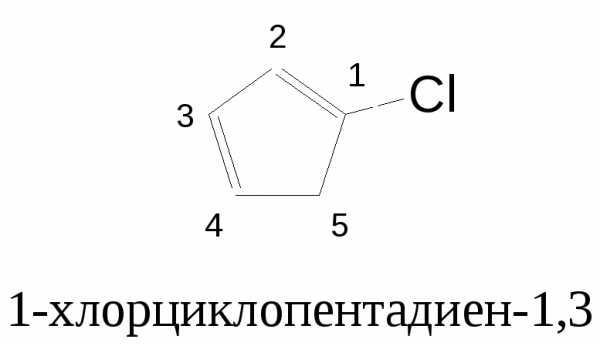
Соединения с двойными и тройнымисвязями (енины)
Двойная связь в номенклатуре ИЮПАК старше тройной, поэтому двойная связь имеет меньший порядковый номер.
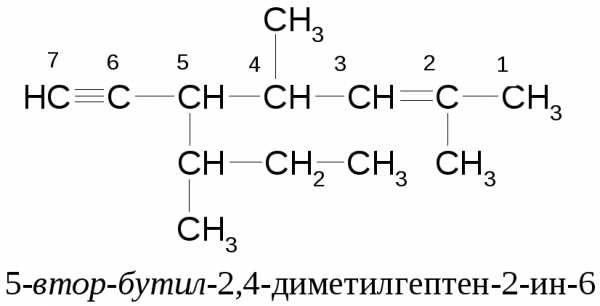
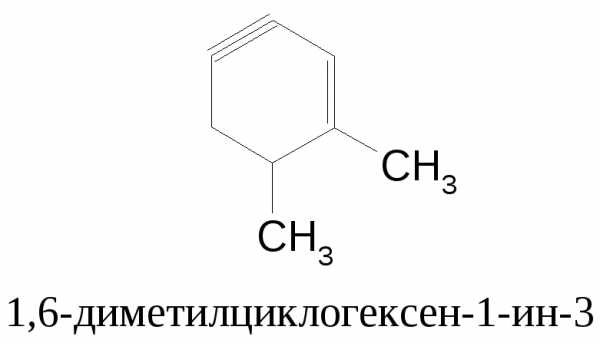
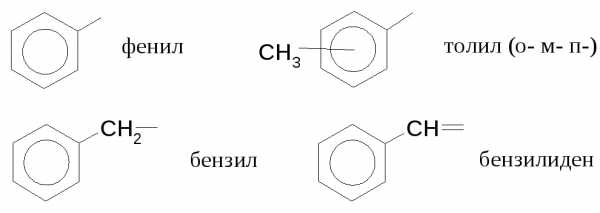
В номенклатуре ИЮПАК бензол и его производные имеют оканчания ен. Однако, в России сохраняются несистематические названия:
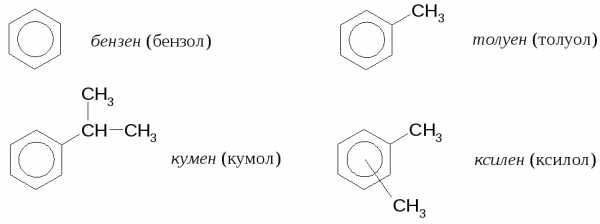
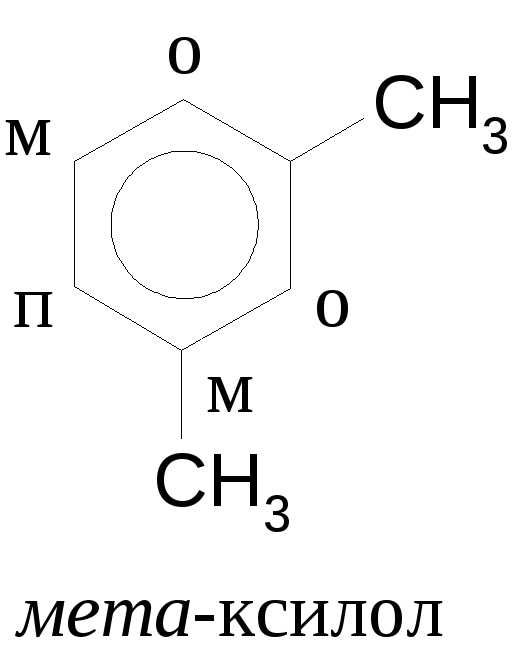
Название ароматических углеводородов, содержащих боковые цепи, строится аналогично названию карбоциклических углеводородов.
Примечание: за основу названия (корень) можно брать известные несистемные названия.
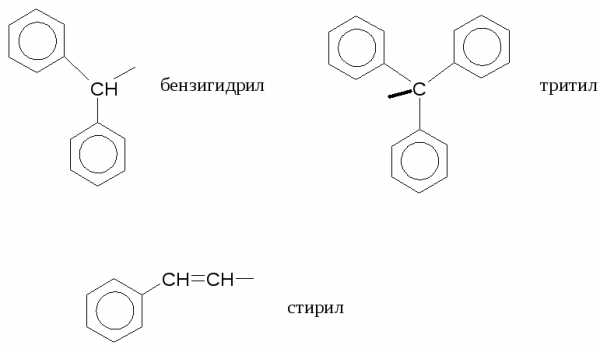
Это правило не действует, если в соединении имеется несколько одинаковых заместителей.
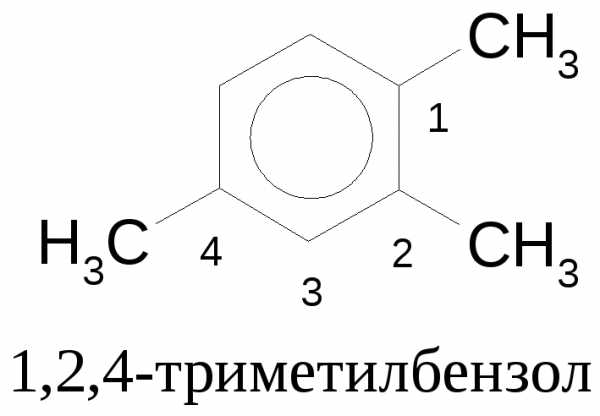
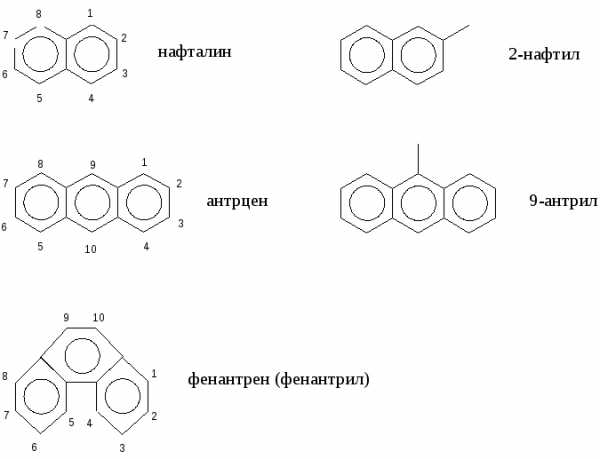
Сложные заместители называют, применяя умножительные приставки «бис», «трис», «тетракис». Пример:
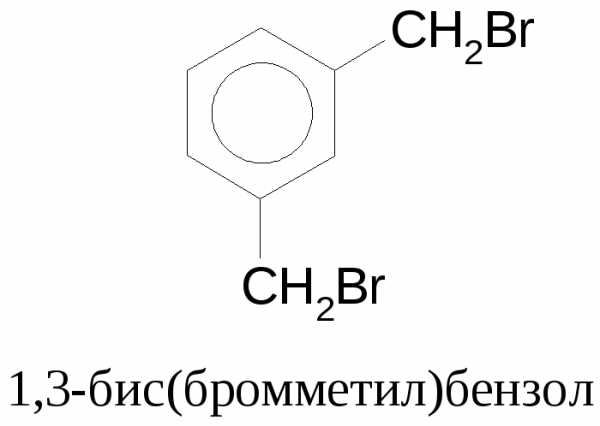
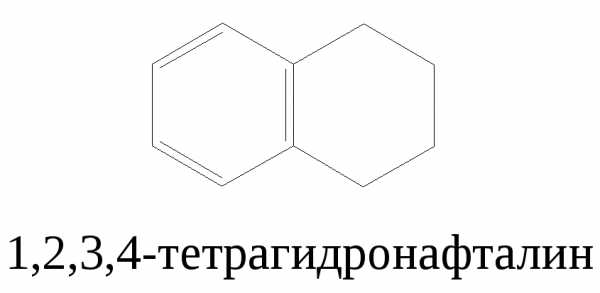
Для частично гидрированных ароматических углеводородов название включает количество присоединенных атомов водорода с применением приставки «гидро-» («пергидро»).
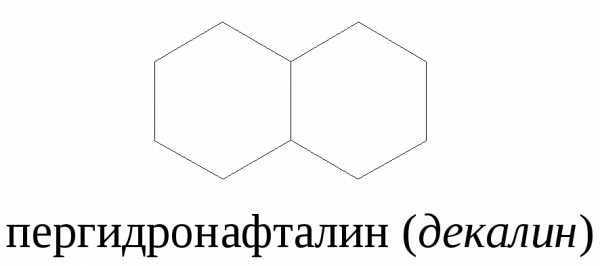
Номенклатура гетероциклических соединений
Соединения, содержащие в цикле один или несколько гетероатомов называют, комбинируя приставку, отражающую природу гетероатома с названием корня, обозначающего число звеньев в кольце.
Приставки:
О – оксо
Sтиа
Nаза
Также учитывается еще несколько факторов, приведенных в таблице.
| число звеньев в кольце | Кольца, содержащие азот | Кольца, не содержащие азот | ||
| ненасыщенные | Насыщенные | ненасыщенные | насыщенные | |
| 3 4 5 6 | -ирин -ет -ол -ил | -иридин -етидин -олидин -пергидро | -ирен -ет -ол -ин | -иран -етан -олан -ан |
Для соединения: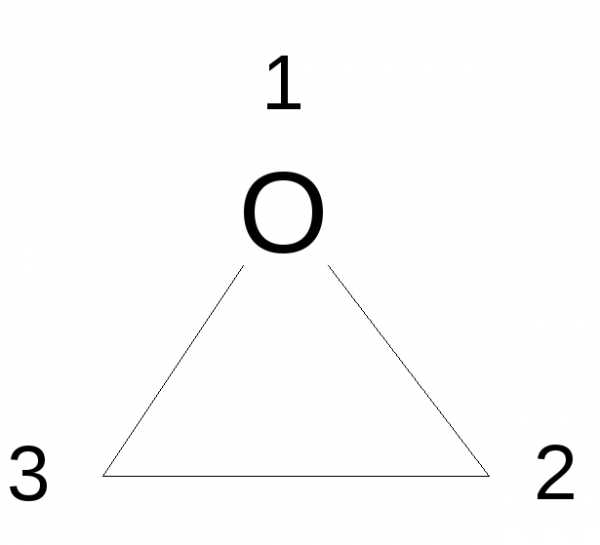 , комбинируют «окса» и «иран» (нет двойной связинасыщенный). Оканчательное название: оксиран.
, комбинируют «окса» и «иран» (нет двойной связинасыщенный). Оканчательное название: оксиран.
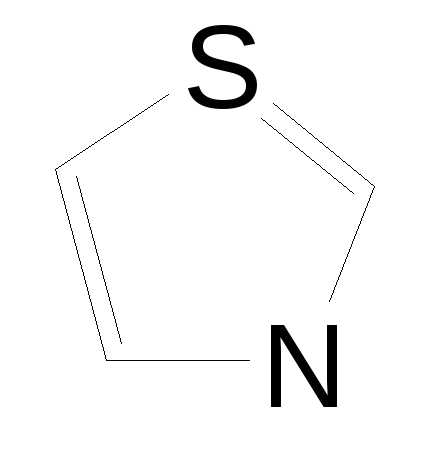 «тиа», «аза», «ол» (ненасыщенный, содержит азот) – 1,3-тиазол-2,4
«тиа», «аза», «ол» (ненасыщенный, содержит азот) – 1,3-тиазол-2,4
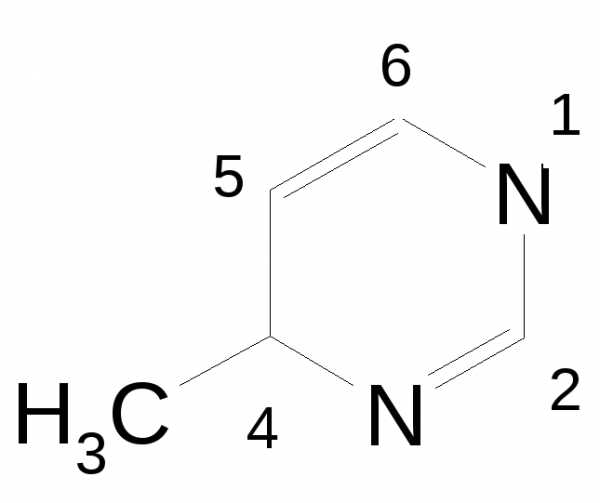 «диаза», «ин»: 4-метил-1,3-диазин-2,5
«диаза», «ин»: 4-метил-1,3-диазин-2,5
Сохраняются тривиальные названия для следующих гетероциклических соединений и радикалов на их основе:
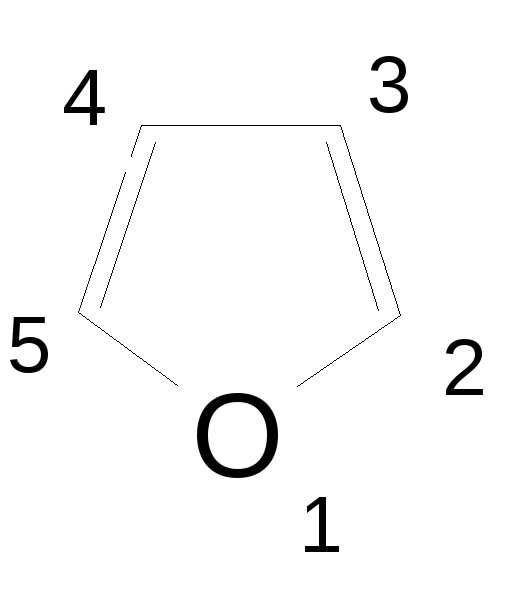 фуран (радикалфурил),
фуран (радикалфурил),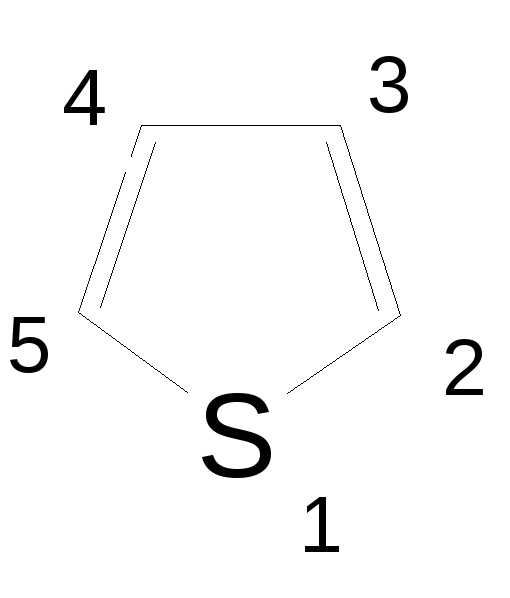 тиофен (радикалтиенил),
тиофен (радикалтиенил),
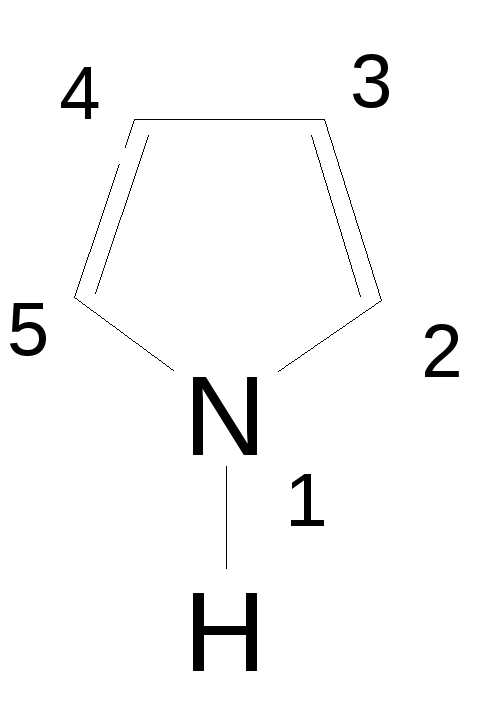 пиррол (пирролил),
пиррол (пирролил),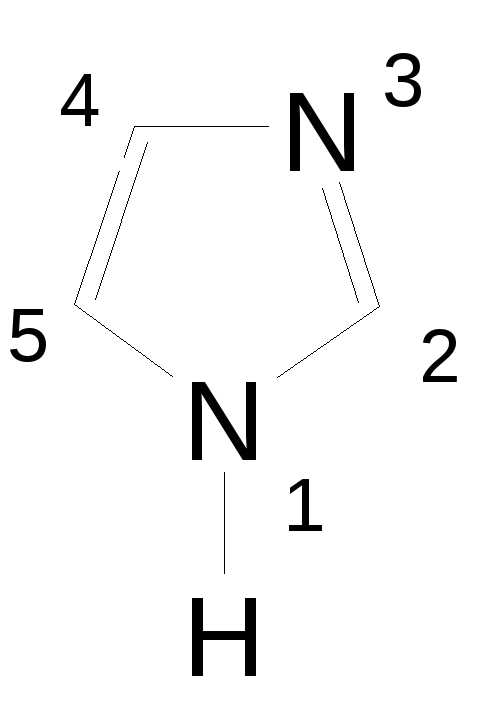 имидазол (имидазолил),
имидазол (имидазолил),
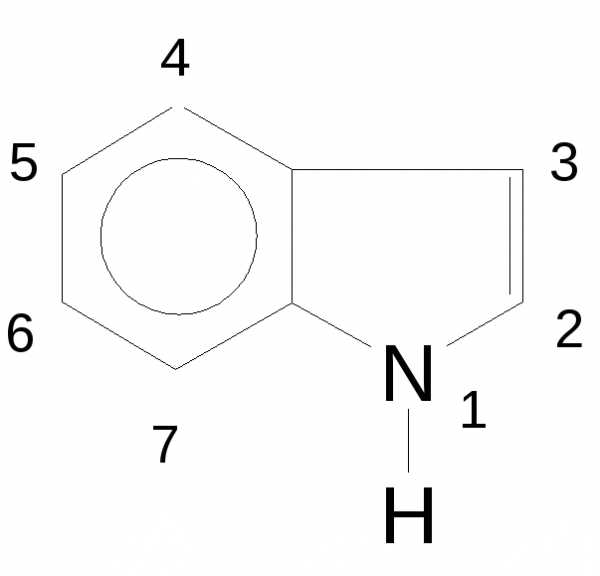 индол (радикал – индолил), например:
индол (радикал – индолил), например:
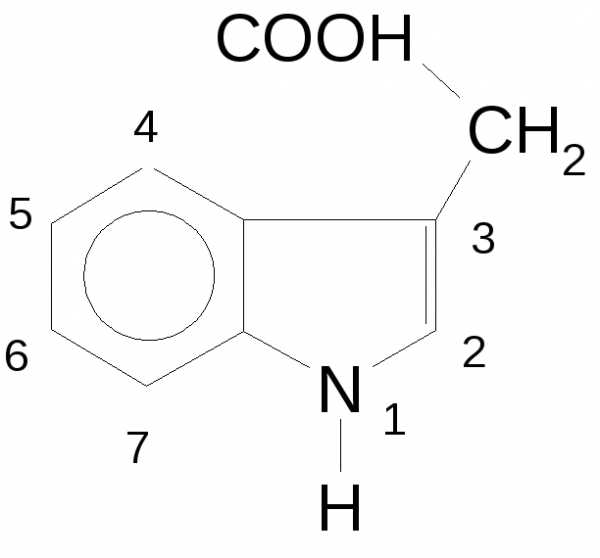 3-индолилэтановая кислота (гетероауксин),
3-индолилэтановая кислота (гетероауксин),
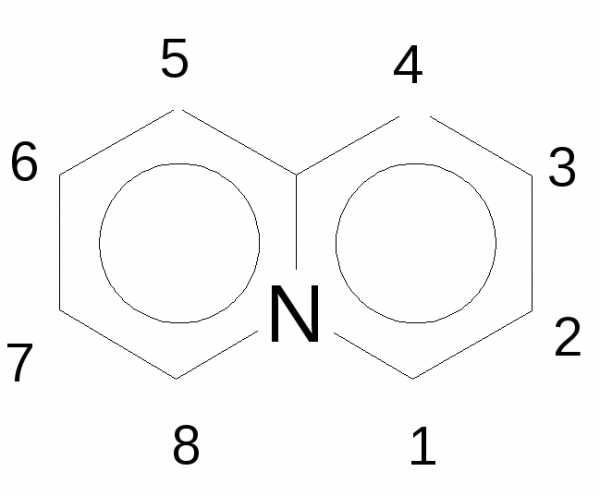 хинолин (радикал – хинолил),
хинолин (радикал – хинолил), 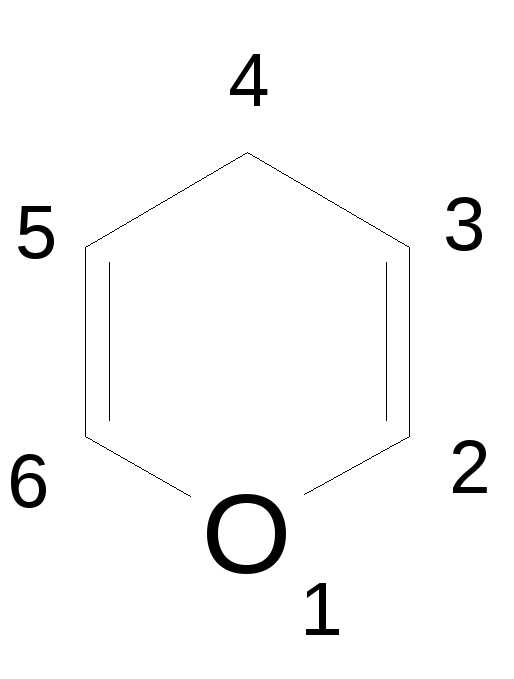 пиран (радикал – пиранил).
пиран (радикал – пиранил).
Номенклатура июпак для производных различных классов органических соединений
В соответствии с современной интерпретацией за основу названия (корень) принимается название основной, как правило, самой длинной углерод-углеродной цепи, цикла или гетероатома (амины, имны). Наличик в соединении других атомов, групп или связей обозначают в зависимости от старшинства приставками или суффиксами, а их положение в основной цепи арабскими цифрами. Для обозначения числа одинаковых незамещенных радикалов применяют приставки ди-, три-, тетра-, а замещенных радикалов бис, трис, тетракис, пентакис.
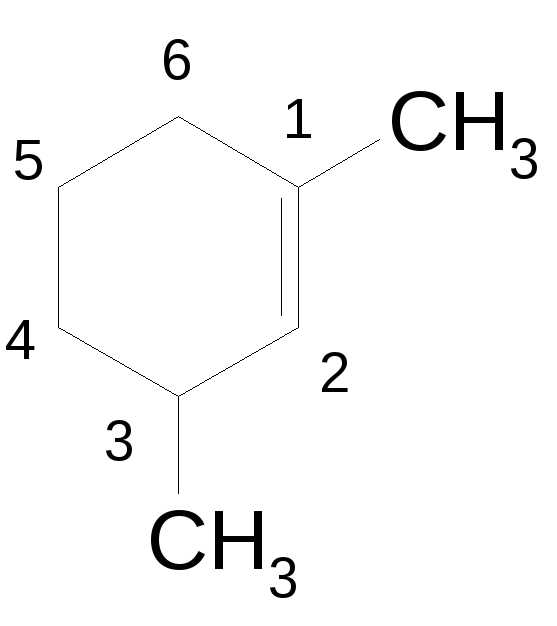 1,3-диметилциклогексен-1,
1,3-диметилциклогексен-1,
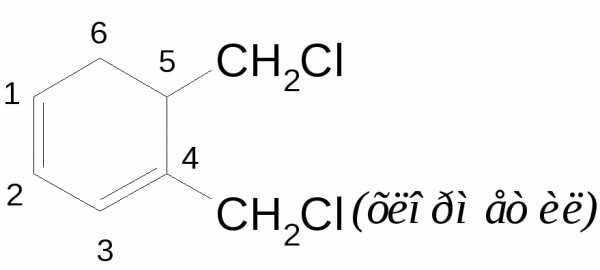 4,5-бис(хлорметил) циклогексадиен-1,3.
4,5-бис(хлорметил) циклогексадиен-1,3.
В номенклатуре заместительного типа (основная часть номенклатуры ИЮПАК) некоторые атомы или группы атомов обозначаются только приставками. К ним относят все нефункциональные заместители, боковые цепи из следующих групп:
Галогены (хлор, бром, йод, фтор)
Нитрозо- и нитрогруппы:
Азо- диазо- и азидогруппы:
Например,
азобензол,
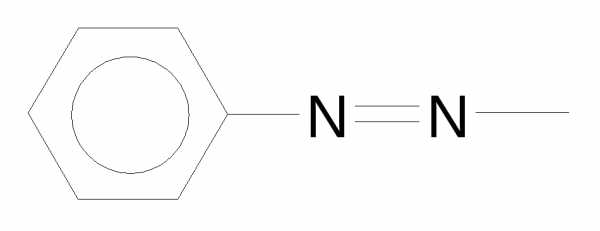 фенилазо- (нефункцианальная приставка),
фенилазо- (нефункцианальная приставка),
азидо
R– окси,R– диокси и гидропироксигруппы (RO,ROO, НOO):
Например,
метокси (метилокси),
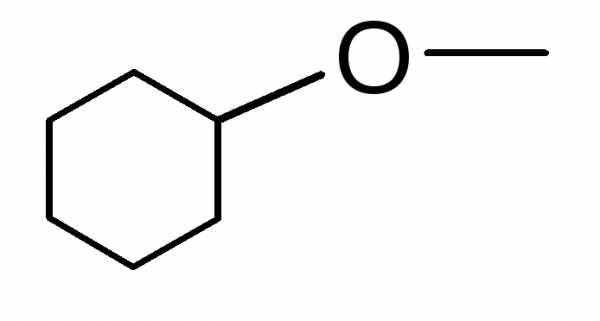 циклогексилокси
циклогексилокси
Серопроизводные:
R-тио,этилтио
Чаще всего функциональные группы могут называться какприставками, так исуффиксами, согласно приведенной ниже таблице (приложение 1):
| Класс соединения | Группа | Приставки | Суффиксы | Пример |
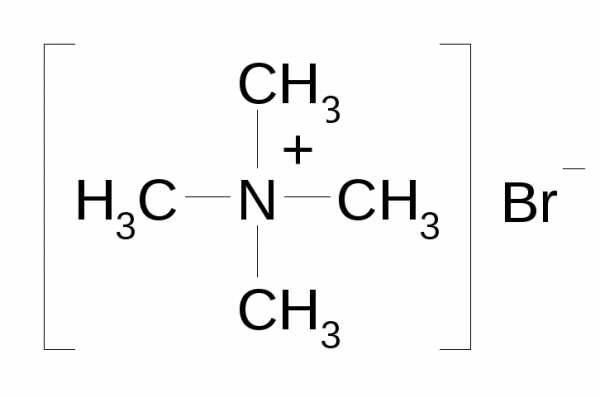
| Катионы |
| онио- | -оний | тетраметиламмонийбромид |
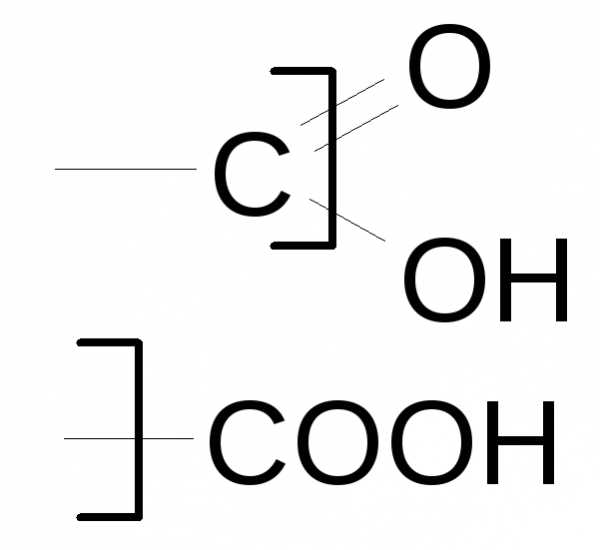
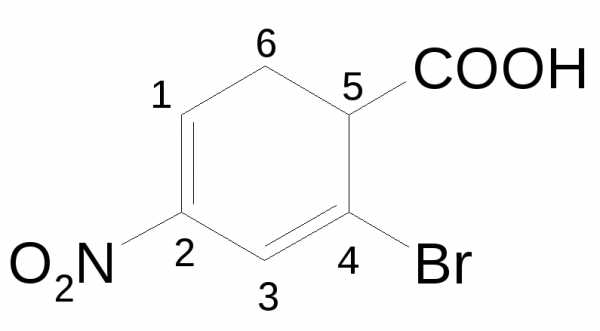
| Карбоновые кислоты |
| карбокси- // | -овая кислота карбоновая кислота | 4-бром-2-нитроциклогексадиен-1,3-карбоновая-5-кислота 2-фторпропановая кислота |
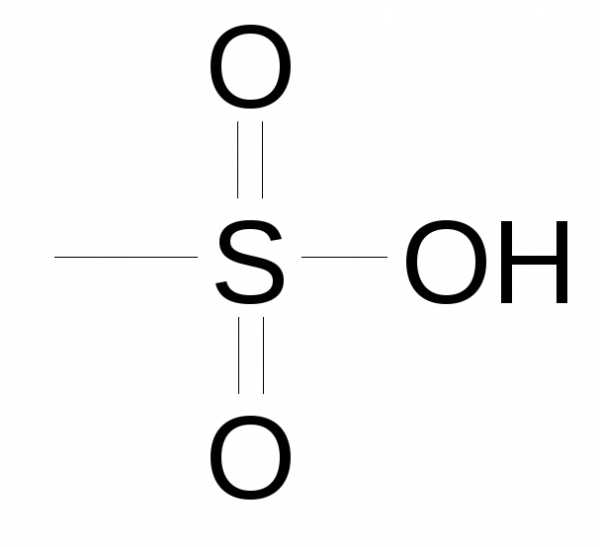
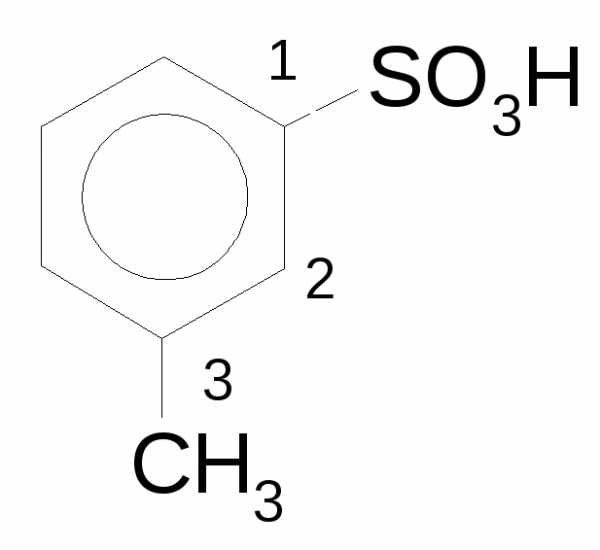
| Сульфокислоты |
| сульфо- | -сульфоновая (сульфо) кислота | м-толуолсульфокислота |
| ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ | ||||
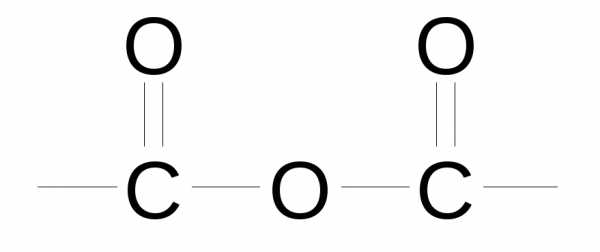
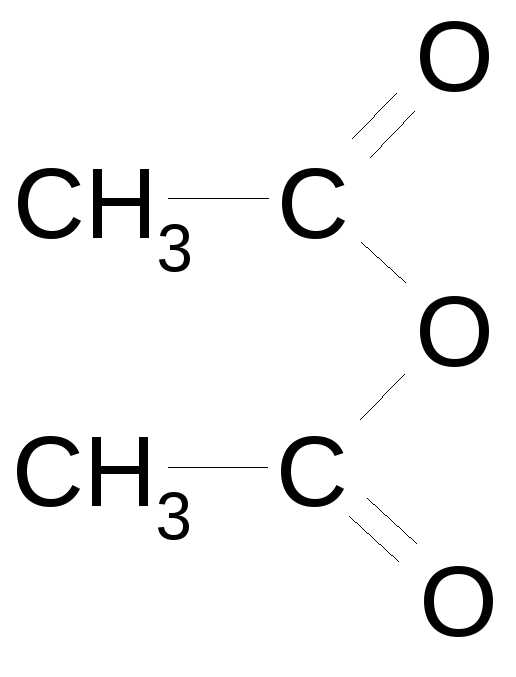
| Ангидриды карбоновых кислот |
| – | Ангидрид овой (карбоновой кислоты) | ангидрид этановой (уксусной) кислоты |
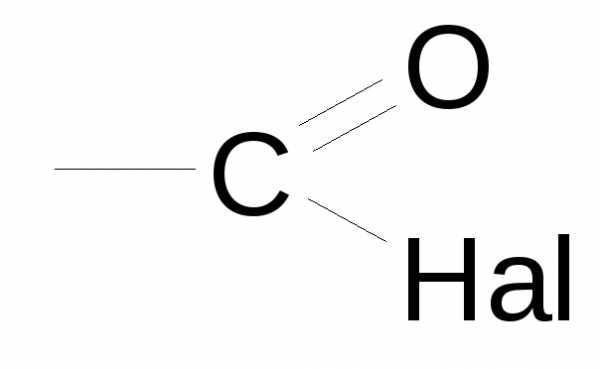
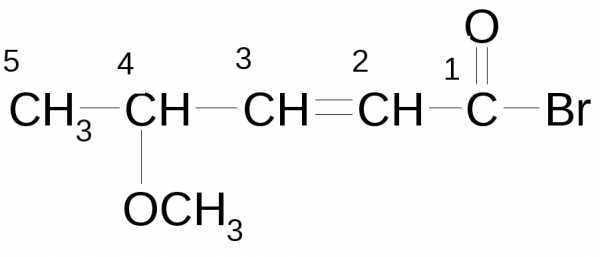
| Галогенангидриды карбоновых кислот |
| галогенформил- | Карбонилгалоген, галогенангидрид -овой (карбоновой) кислоты | бромангидрид-4-метоксипентен-2-овой кислоты |
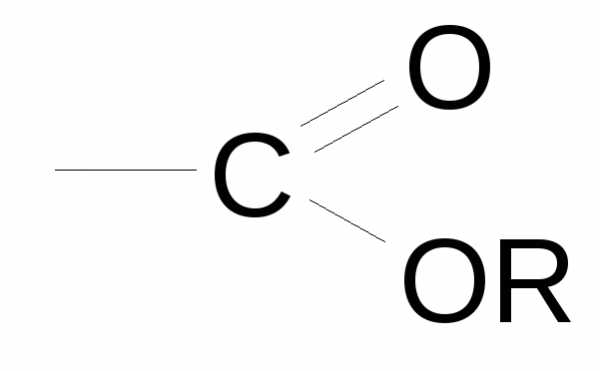
| Сложные эфиры карбоновых кислот |
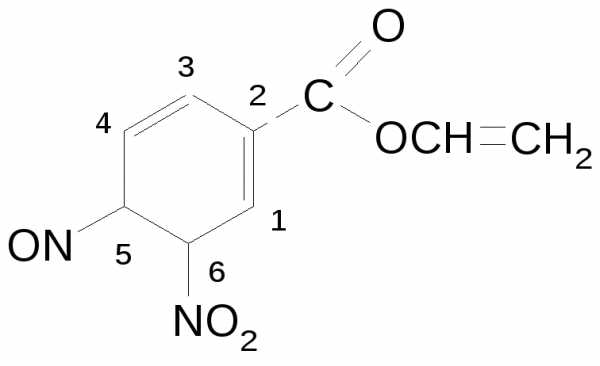
| R-карбокси- | R-карбоксилат, R-ный эфир…-овой (карбоновой) кислоты | 5-нитрозо-6-нитроциклогексадиен-1,3-карбоновой-2 кислоты виниловый эфир |
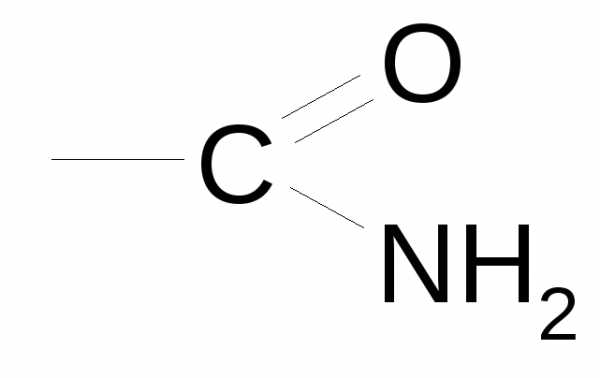
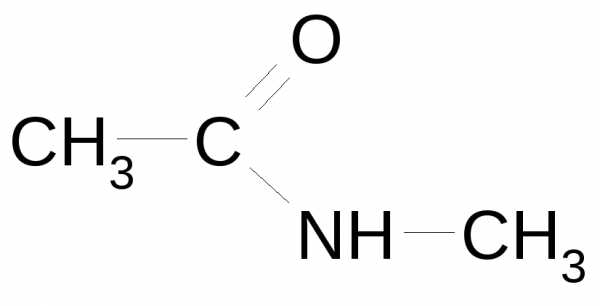
| Амиды карбоновых кислот |
| Карбомоил | Амид…-овой (карбоновой) кислоты | N-метиламид этановой кислоты |
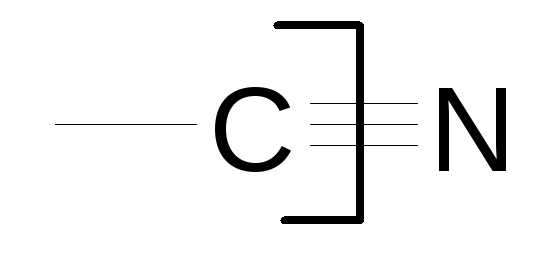
| Нитрилы карбоновых кислот |
| Циано- | Карбонитрил нитрил…–овой (карбоновой) кислоты | 3-бромбензоной кислоты нитрил |
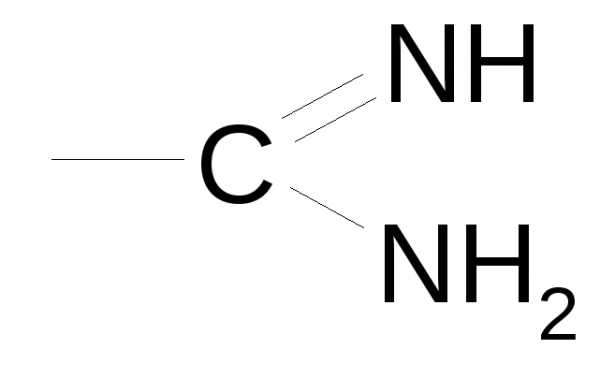
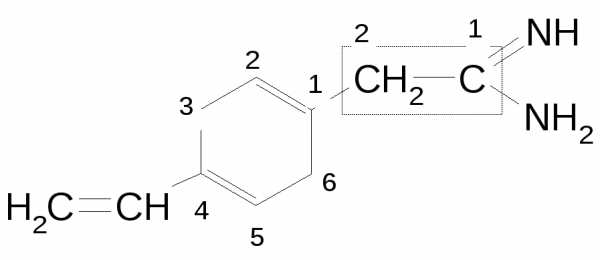
| Амидины |
| амидино- | амидин –овой (карбоновой) кмслоты | 2-(4-винилциклогексадиен-1,4-ил)этановой кислоты амидин |
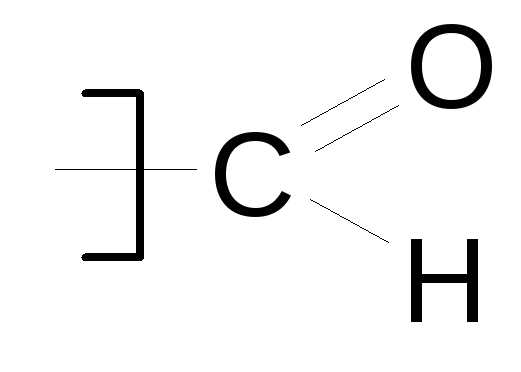
| Адьдегиды |
| формил- оксо- | -карбальдегид -аль | 4-формил-5-(2-хлорвинил) циклопентен-1-карбоновая кислота-1 |
| Кетоны |
| оксо- | -он | 2,5-дихлор-4-оксогексадиен-2,5-аль |
| Спирты, фенолы | OH | гидрокси- (окси) | -ол |
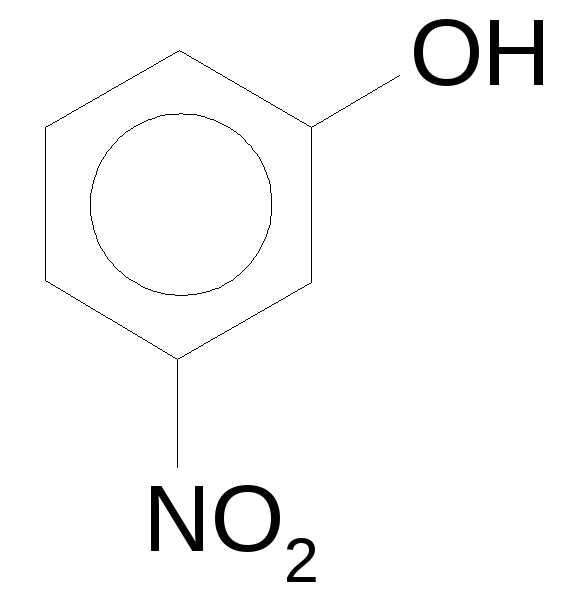
4-бромметил-5-бромпентен-2-ол-1 3-нитрофенол (м-нитрофенол) |
| Тиоспирты | SH | тио- (меркапто-) | -тиол (-меркаптан) |
бутантиол (бутилмеркаптан) |
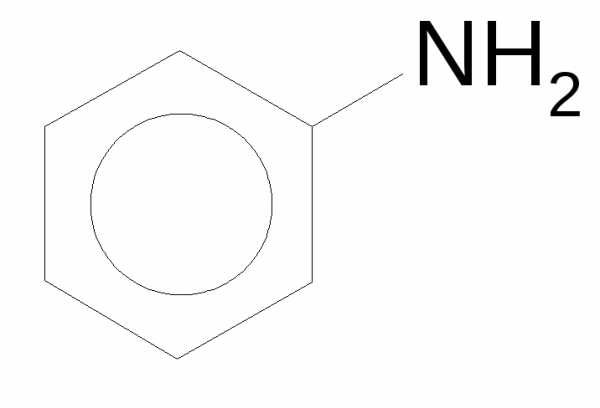
| Амины | Nh3 | амино- | -амин | анилин
диэтиламин |
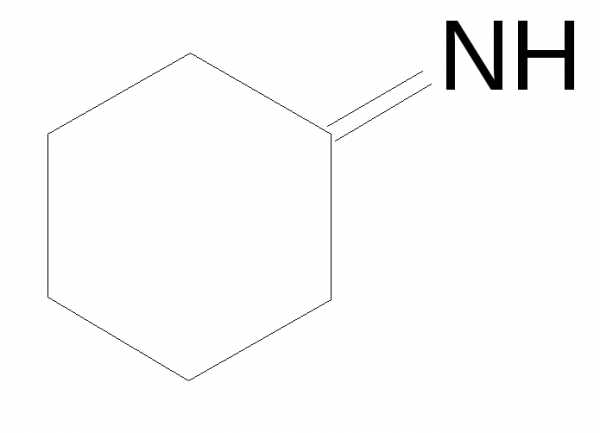
| Имины (альдегидов, кетонов) | =NH | имино- | -имин (альдегида, кетона) | циклогексанимин (имин циклогесанона) |
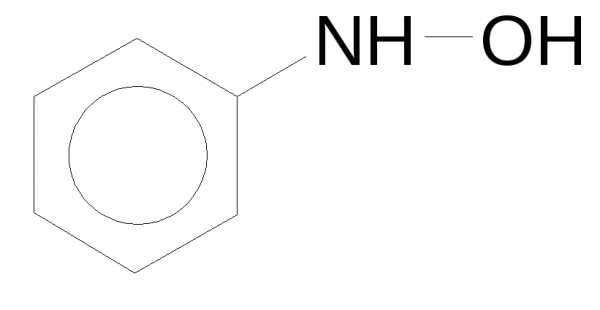
| Гидроксил- амины | NHOH | оксамино- | гидроксиламин | фенилгидроксиламин |
| Оксимы | =N–OH | оксимино- | -оксим (альдегида, кетона) |
пентаноксим-3 оксим диэтилкетона |
| Гидразины | NHNh3 | гидразино- | гидразин | трет-бутилгидразин |
В заместительной номенклатуре ИЮПАК старшая функциональная группа обозначаетсясуффиксом, а все остальные функциональные группы и заместителиприставками.
После перечисления приставок называют корень соответствующий самой длинной углерод-углеродной цепи (или главной структуры). Название заканчивается суффиксом, соответствующим старшей функциональной группе. Суффикс должен быть один (кроме кратных связей).
studfiles.net