Содержание
Борноэтиловый эфир — Википедия — Study in China 2023
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 12 декабря 2020 года; проверки требуют 6 правок.
Не следует путать с триэтилбораном.
Борноэти́ловый эфи́р (триэти́лбора́т, химическая формула — B(C2H5O)3) — сложный эфир ортоборной кислоты и этанола.
При нормальных условиях — бесцветная легкоподвижная жидкость со слабым запахом этилового спирта. Применяется в качестве растворителя, реагента в органическом синтезе, катализатора и для придания пламени зелёного цвета при горении пиротехнических изделий и смесей.
Содержание
Show / Hide
Химические свойства
Горение на воздухе ярким зеленым пламенем с образованием оксида бора:
- 2B(OC2H5)3+18O2→B2O3+12CO2+15h3O{\displaystyle {\mathsf {2B(OC_{2}H_{5})_{3}+18O_{2}\rightarrow B_{2}O_{3}+12CO_{2}+15H_{2}O}}}
Получение
1) Перегонка раствора ортоборной кислоты в этаноле в присутствии кислотного катализатора и водоотнимающего реагента, обычно — серной кислоты[2]:
- B(OH)3+3 C2H5OH⟶B(C2H5O)3↑+3 h3O{\displaystyle {\mathsf {B(OH)_{3}+3\ C_{2}H_{5}OH\longrightarrow B(C_{2}H_{5}O)_{3}\uparrow +3\ H_{2}O}}}
2) Взаимодействие тетрабората натрия и этанола в сернокислой среде:
- Na2B4O7+2h3SO4+12C2H5OH→4B(C2H5O)3↑+2NaHSO4+7h3O{\displaystyle {\mathsf {Na_{2}B_{4}O_{7}+2H_{2}SO_{4}+12C_{2}H_{5}OH\rightarrow 4B(C_{2}H_{5}O)_{3}\uparrow +2NaHSO_{4}+7H_{2}O}}}
Применение
- В качестве катализатора в органическом синтезе при производстве синтетических смол, синтетических восков, красок и лаков;
- В получении борных соединений, например, борогидрида натрия;
- В качестве растворителя;
- Пропитка древесины и тканей для придания им огнеупорности.

- Компонент некоторых флюсов.
- Компонент пиротехнических изделий;
- Поджиг многоразовых ракетных двигателей[источник не указан 694 дня].
Предосторожности при использовании
Является легковоспламеняемой жидкостью, поэтому при работе с веществом следует применять меры безопасности при работе с огнеопасными веществами.
Примечания
Ссылки
- National Pollutant Inventory — Бор и его соединения
Литература
- Лидин Р. А., Молочко В. А., Андреева Л. Л. Химические свойства неорганических веществ. — М.: Химия, 1996. — С. 77. — 479 с. — 5000 экз. — ISBN 5-7245-0948-2.
#Wikipedia® is a registered trademark of the Wikimedia Foundation, Inc. Wiki (Study in China) is an independent company and has no affiliation with Wikimedia Foundation.
This article uses material from the Wikipedia article Борноэтиловый эфир, which is released under the Creative Commons Attribution-ShareAlike 3.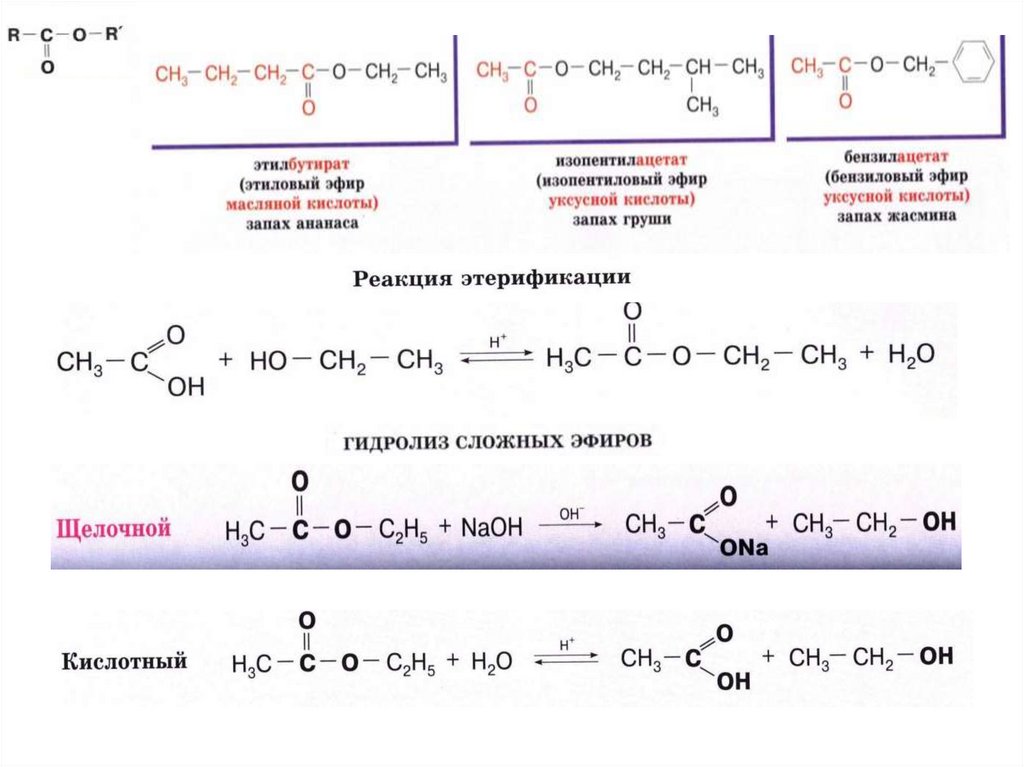 0 license («CC BY-SA 3.0»); additional terms may apply. (view authors). Если не указано иное, содержание доступно по лицензии CC BY-SA 3.0. Images, videos and audio are available under their respective licenses.
0 license («CC BY-SA 3.0»); additional terms may apply. (view authors). Если не указано иное, содержание доступно по лицензии CC BY-SA 3.0. Images, videos and audio are available under their respective licenses.
🌐 Wiki languages: 1,000,000+ articlesEnglishРусскийDeutschItalianoPortuguês日本語Français中文العربيةEspañol한국어NederlandsSvenskaPolskiУкраїнськаمصرى粵語DanskفارسیTiếng ViệtWinaraySinugboanong Binisaya
🔥 Top trends keywords Русский Wiki:
Заглавная страницаСлужебная:ПоискYouTubeСоединённые Штаты АмерикиКузнецов, Сергей БорисовичВторжение России на Украину (2022)РоссияВыборы в Сенат США (2022)Группа ВагнераВКонтактеКалифорнияGoogle (компания)PythonGoСан-БруноПригожин, Евгений ВикторовичВыборы в Палату представителей США (2022)Список игроков НХЛ, забросивших 500 и более шайбБольшая двадцаткаVK (компания)Список умерших в 2022 годуПенн, ШонСаммит G-20 на Бали (2022)Республиканская партия (США)Лунное затмениеПушкин, Александр СергеевичЧемпионат мира по футболу 2022Путин, Владимир Владимирович2021 год8 ноябряМоскваУкраинаTelegramПереводчикПервая мировая войнаДамер, ДжеффриТрамп, ДональдПотери сторон в период вторжения России на УкраинуБайден, ДжоСанкт-ПетербургRobloxМаккаферти, Уильям ДэниелЯндексRuTracker.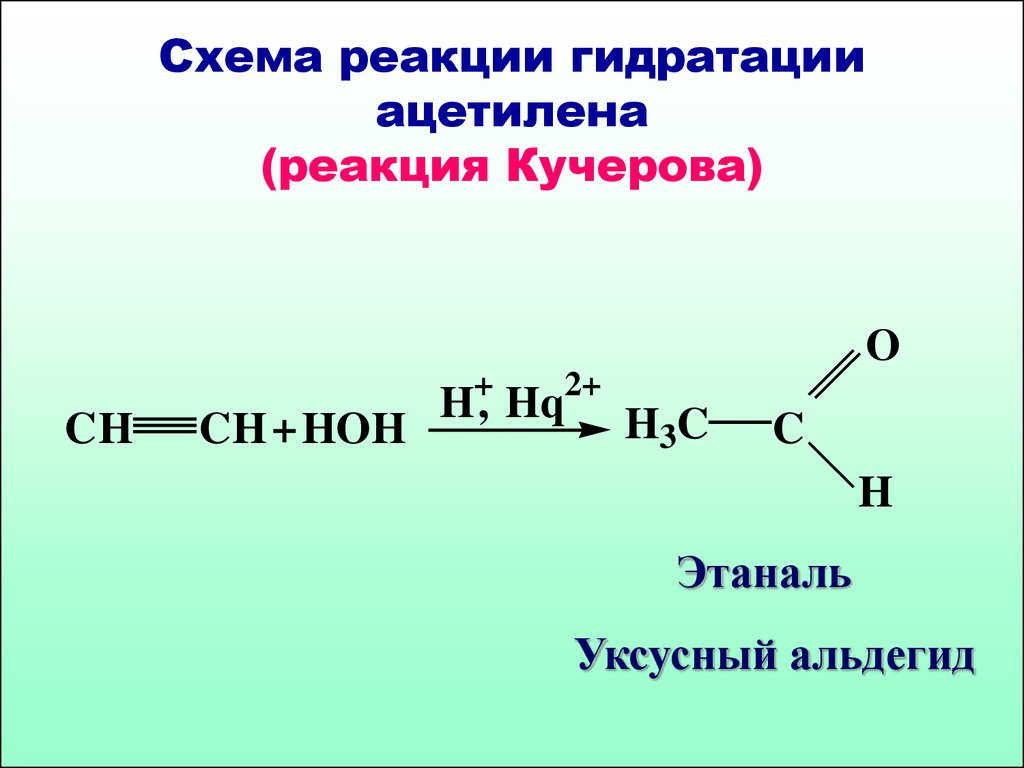 orgGoogle ПереводчикЗеленский, Владимир АлександровичОднопользовательская играХерсонСоюз Советских Социалистических РеспубликМаск, ИлонБРИКСДом ДраконаGod of War: RagnarökЛермонтов, Михаил ЮрьевичСталин, Иосиф ВиссарионовичАн-225Вторая мировая войнаZALA ЛанцетАнглийский языкРоссийско-украинская войнаПётр IМногопользовательская играРусский языкСписок президентов СШАЗнаки зодиакаЕкатерина IIДёмушкин, Дмитрий НиколаевичДень Великой Октябрьской социалистической революцииШатунов, Юрий Васильевич155-я отдельная гвардейская бригада морской пехотыДемократическая партия (США)Ласковый майОвечкин, Александр МихайловичВикипедия:ФорумWindows2020 годДень народного единстваОктябрьская революцияФокин, Валерий Владимирович🡆 More
orgGoogle ПереводчикЗеленский, Владимир АлександровичОднопользовательская играХерсонСоюз Советских Социалистических РеспубликМаск, ИлонБРИКСДом ДраконаGod of War: RagnarökЛермонтов, Михаил ЮрьевичСталин, Иосиф ВиссарионовичАн-225Вторая мировая войнаZALA ЛанцетАнглийский языкРоссийско-украинская войнаПётр IМногопользовательская играРусский языкСписок президентов СШАЗнаки зодиакаЕкатерина IIДёмушкин, Дмитрий НиколаевичДень Великой Октябрьской социалистической революцииШатунов, Юрий Васильевич155-я отдельная гвардейская бригада морской пехотыДемократическая партия (США)Ласковый майОвечкин, Александр МихайловичВикипедия:ФорумWindows2020 годДень народного единстваОктябрьская революцияФокин, Валерий Владимирович🡆 More
Related topics
Сложные эфиры — Госстандарт
Среди функциональных производных кислот особое место занимают сложные эфиры — производные кислот, у которых кислотный водород заменён на алкильные (или вообще углеводородные) радикалы.
Сложные эфиры делятся в зависимости от того, производной какой кислоты они являются (неорганической или карбоновой).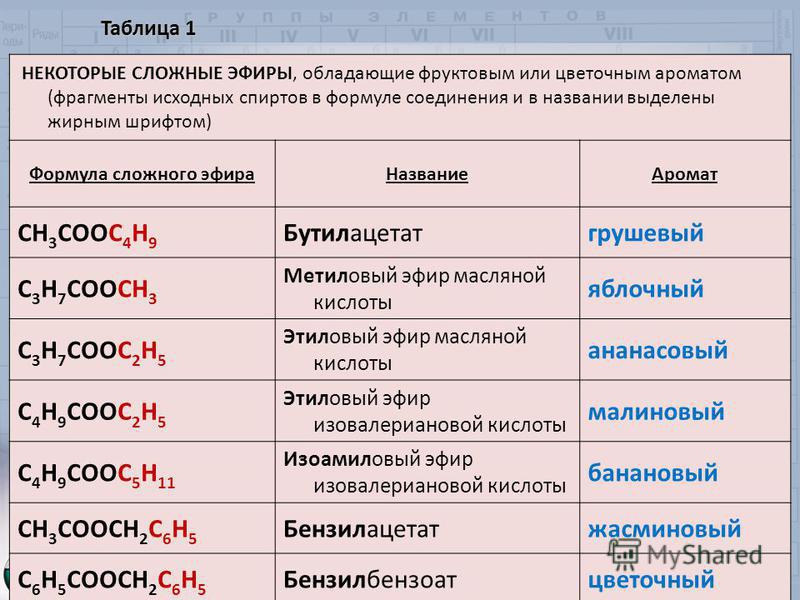
Среди сложных эфиров особое место занимают природные эфиры — жиры и масла, которые образованы трехатомным спиртом глицерином и высшими жирными кислотами, содержащими четное число углеродных атомов. Жиры входят в состав растительных и животных организмов и служат одним из источников энергии живых организмов, которая выделяется при окислении жиров.
Цель моей работы заключается в подробном ознакомлении с таким классом органических соединений, как сложные эфиры и углублённом рассмотрении области применения отдельных представителей этого класса.
Строение
Общая формула сложных эфиров карбоновых кислот:
где R и R’ — углеводородные радикалы (в сложных эфиpax муравьиной кислоты R — атом водорода).
Общая формула жиров:
гдеR’, R», R»‘ — углеродные радикалы.
Жиры бывают “простыми” и “смешанными”. В состав простых жиров входят остатки одинаковых кислот (т. е. R’ = R» = R'»), в состав смешанных — различных.
В жирах наиболее часто встречаются следующие жирные кислоты:
Алкановые кислоты
- Масляная кислота СН3 — (CH2 )2 — СООН
- Капроновая кислота СН3 — (CH2 )4 — СООН
- Пальмитиновая кислота СН3 — (CH2 )14 — СООН
- Стеариновая кислота СН3 — (CH2 )16 — СООН
Алкеновые кислоты
- Олеиновая кислота С17 Н33 СООН
СН3 —(СН2 )7 —СН === СН—(СН2 )7 —СООН
Алкадиеновые кислоты
- Линолевая кислота С17 Н31 СООН
СН3 —(СН2 )4 —СН = СН—СН2 —СН = СН—СООН
Алкатриеновые кислоты
- Линоленовая кислота С17 Н29 СООН
СН3 СН2 СН = CHCH2 CH == CHCH2 CH = СН(СН2 )4 СООН
Номенклатура и изомерия
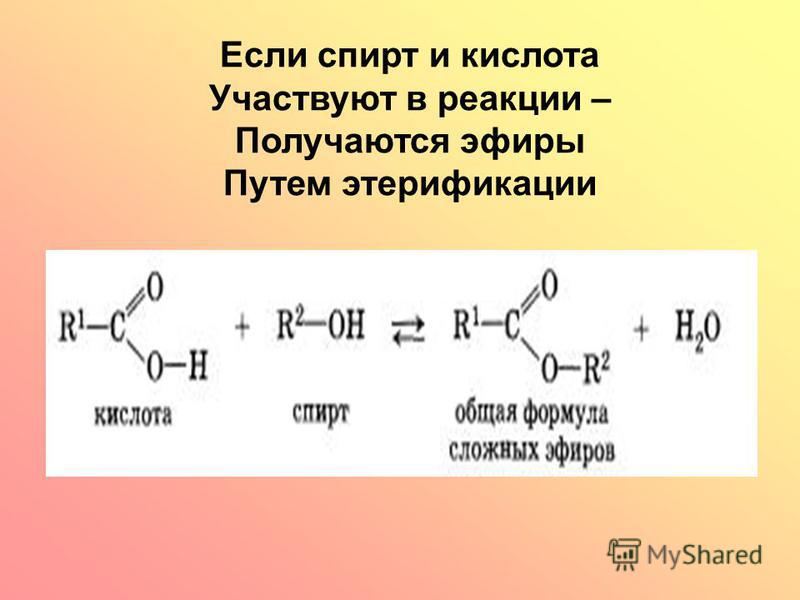
Названия сложных эфиров производят от названия углеводородного радикала и названия кислоты, в котором вместо окончания -овая используют суффикс — ат, например:
Для сложных эфиров характерны следующие виды изомерии:
- Изомерия углеродной цепи начинается по кислотному остатку с бутановой кислоты, по спиртовому остатку — с пропилового спирта, например, этилбутирату изомерны этилизобутират, пропилацетат и изопропилацетат.

- Изомерия положения сложноэфирной группировки —СО—О—. Этот вид изомерии начинаетсясо сложных эфиров, в молекулах которых содержится не менее 4 атомов углерода, например этилацетат и метилпропионат.
- Межклассовая изомерия, например, метилацетату изомерна пропановая кислота.
Для сложных эфиров, содержащих непредельную кислоту или непредельный спирт, возможны еще два вида изомерии: изомерия положения кратной связи и цис-, транс-изомерия.
Физические свойства и нахождение в природе
Сложные эфиры низших карбоновых кислот и спиртов представляют собой летучие, нерастворимые в воде жидкости. Многие из них имеют приятный запах. Так, например, бутилбутират имеет запах ананаса, изоамилацетат — груши и т. д.
Сложные эфиры высших жирных кислот и спиртов — воскообразные вещества, не имеют запаха, в воде не растворимы.
Приятный аромат цветов, плодов, ягод в значительной степени обусловлен присутствием в них тех или иных сложных эфиров.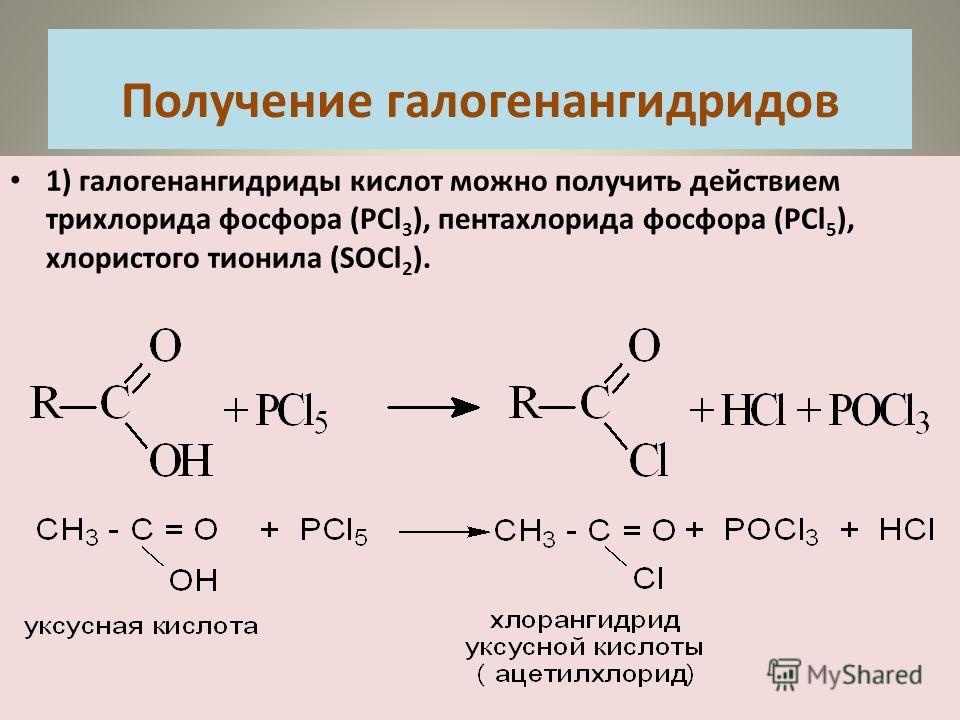
Жиры широко распространены в природе. Наряду с углеводородами и белками они входят в состав всех растительных и животных организмов и составляют одну из основных частей нашей пищи.
По агрегатному состоянию при комнатной температуре жиры делятся на жидкие и твердые. Твердые жиры, как правило, образованы предельными кислотами, жидкие жиры (их часто называют маслами) — непредельными. Жиры растворимы в органических растворителях и нерастворимы в воде.
Химические свойства
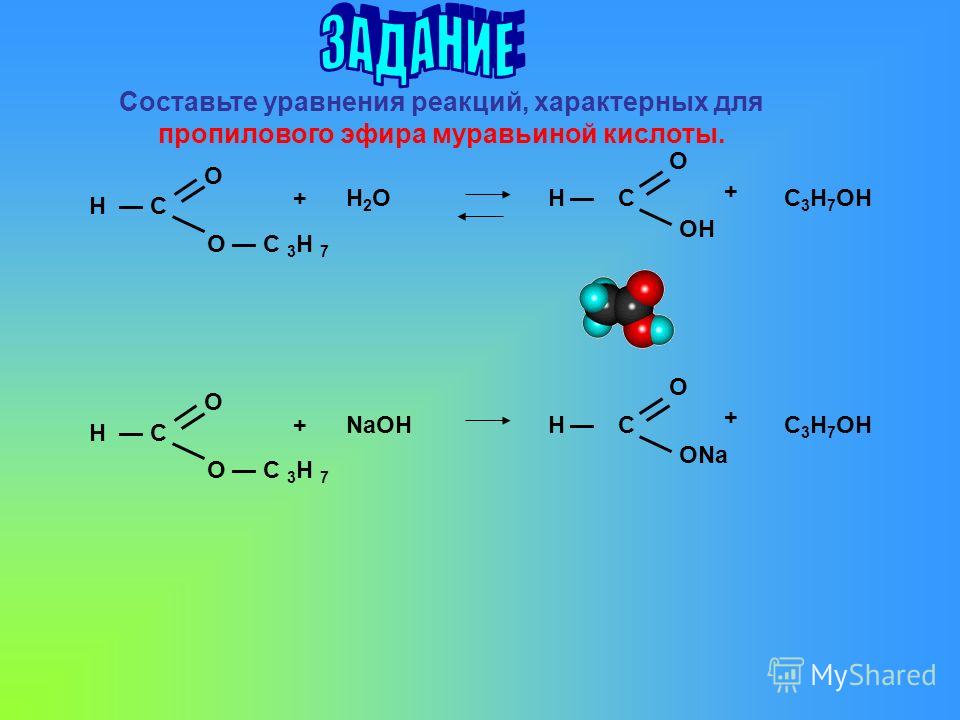
1. Реакция гидролиза, или омыления. Так, как реакция этерификации является обратимой, поэтому в присутствии кислот протекает обратная реакция гидролиза:
Реакция гидролиза катализируется и щелочами; в этом случае гидролиз необратим, так как получающаяся кислота со щелочью образует соль:
2. Реакция присоединения. Сложные эфиры, имеющие в своем составе непредельную кислоту или спирт, способны к реакциям присоединения.
3. Реакция восстановления. Восстановление сложных эфиров водородом приводит к образованию двух спиртов:
4. Реакция образования амидов. Под действием аммиака сложные эфиры превращаются в амиды кислот и спирты:
Реакция образования амидов. Под действием аммиака сложные эфиры превращаются в амиды кислот и спирты:
Получение
1. Реакция этерификации:
Спирты вступают в реакции с минеральными и органическими кислотами, образуя сложные эфиры. Реакция обратима (обратный процесс – гидролиз сложных эфиров).
Реакционная способность одноатомных спиртов в этих реакциях убывает от первичных к третичным.
2. Взаимодействием ангидридов кислот со спиртами:
3. Взаимодействием галоидангидридов кислот со спиртами:
Применение
Применение сложных эфиров неорганических кислот
Эфиры борной кислоты — триалкилбораты — легко получаются нагреванием спирта и борной кислоты с добавкой концентрированной серной кислоты. Борнометиловый эфир (триметилборат) кипит при 65° С, борноэтиловый (триэтилборат) — при 119° С. Эфиры борной кислоты легко гидролизуются водой.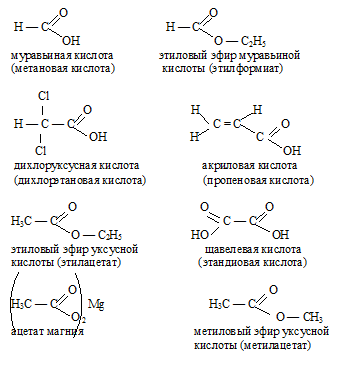
Реакция с борной кислотой служит для установления конфигурации многоатомных спиртов и была неоднократно использована при изучении Сахаров.
Ортокремневые эфиры — жидкости. Метиловый эфир кипит при 122° С, этиловый при 156° С. Гидролиз водой проходит легко уже на холоду, но идет постепенно и при недостатке воды приводит к образованию высокомолекулярных ангидридных форм, в которых атомы кремния соединены друг с другом через кислород (силоксановые группировки):
Эти высокомолекулярные вещества (полиалкоксисилоксаны) находят применение в качестве связующих, выдерживающих довольно высокую температуру, в частности для покрытия поверхности форм для точной отливки металла.
Аналогично SiCl4 реагируют диалкилдихлорсиланы, например ((СН3 )2 SiCl2 , образуя диалкоксильные производные
Их гидролиз при недостатке воды дает так называемые полиалкилсилоксаны:
Они обладают разным (но очень значительным) молекулярным весом и представляют собой вязкие жидкости, используемые в качестве термостойких смазок, а при еще более длинных силоксановых скелетах — термостойкие электроизоляционные смолы и каучуки.
Эфиры ортотитановой кислоты. ИХ получают аналогично ортокремневым эфирам по реакции:
Это жидкости, легко гидролизующиеся до метилового спирта и TiO2 применяются для пропитки тканей с целью придания им водонепроницаемости.
Эфиры азотной кислоты. Их получают действием на спирты смеси азотной и концентрированной серной кислот. Метилнитрат СН3 ONO2 , (т. кип. 60° С) и этилнитрат C2 H5 ONO2 (т. кип. 87° С) при осторожной работе можно перегнать, но при нагревании выше температуры кипения или при детонации они очень сильно взрывают.
Нитраты этиленгликоля и глицерина, неправильно называемые нитрогликолем и нитроглицерином, применяются в качестве взрывчатых веществ. Сам нитроглицерин (тяжелая жидкость) неудобен и опасен в обращении.
Пентрит — тетранитрат пентаэритрита С(CH2 ONO2 )4 , получаемый обработкой пентаэритрита смесью азотной и серной кислот, — тоже сильное взрывчатое вещество бризантного действия.
Нитрат глицерина и нитрат пентаэритрита обладают сосудорасширяющим эффектом и применяются как симптоматические средства при стенокардии.
Эфиры фосфорной кислоты — высококипящие жидкости, лишь очень медленно гидролизуемые водой, быстрее щелочами и разбавленными кислотами. Эфиры, образованные этерификацией высших спиртов (и фенолов), находят применение как пластификаторы пластмасс и для извлечения солей уранила из водных растворов.
Известны эфиры типа (RO)2S═O, но они не имеют практического значения.
Из алкилсульфатов — солей сложных эфиров высших спиртов и серной кислоты производят моющие средства. В общем виде образование таких солей можно изобразить уравнениями:
Эти соли содержат в молекуле от 12 до 14 углеродных атомов и обладают очень хорошими моющими свойствами. Кальциевые и магниевые соли растворимы в воде, а потому такие мыла моют и в жесткой воде. Алкилсульфаты содержатся во многих стиральных порошках.
Они и обладают прекрасными моющими способностями.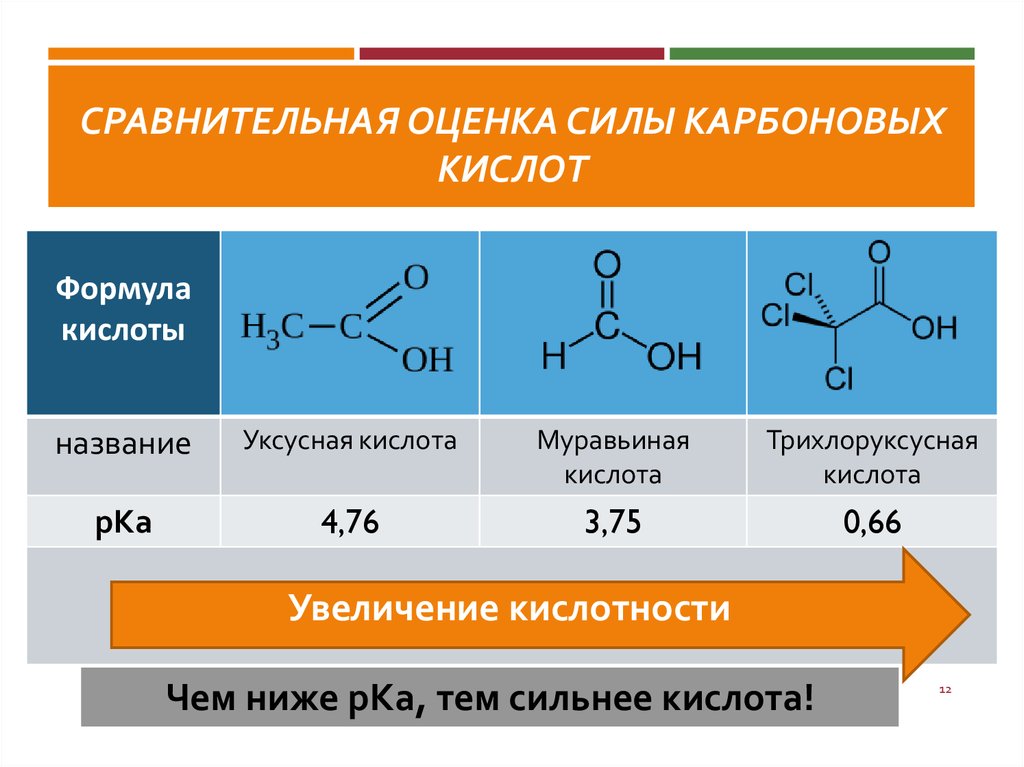 Принцип их действия тот же, что и у обычного мыла, только кислотный остаток серной кислоты лучше адсорбируется частицами загрязнения, а кальцевые соли алкилсерной кислоты растворимы в воде, поэтому это моющее средство стирает и в жесткой, и в морской воде.
Принцип их действия тот же, что и у обычного мыла, только кислотный остаток серной кислоты лучше адсорбируется частицами загрязнения, а кальцевые соли алкилсерной кислоты растворимы в воде, поэтому это моющее средство стирает и в жесткой, и в морской воде.
Применение сложных эфиров органических кислот
Наибольшее применение в качестве растворителей получили эфиры уксусной кислоты — ацетаты. Прочие эфиры (кислот молочной — лактаты, масляной — бутираты, муравьиной — формиаты) нашли ограниченное применение. Формиаты из-за сильной омыляемости и высокой токсичности в настоящее время не используются. Определенный интерес представляют растворители на основе изобутилового спирта и синтетических жирных кислот, а также алкиленкарбонаты. Физико-химические свойства наиболее распространенных сложных эфиров приведены в таблице (см. приложение).
Метилацетат СН3 СООСН3 . Отечественной промышленностью технический метилацетат выпускается в виде древесно-спиртового растворителя, в котором содержится 50% (масс. ) основного продукта. Метилацетат также образуется в виде побочного продукта при производстве поливинилового спирта. По растворяющей способности метилацетат аналогичен ацетону и применяется в ряде случаев как его заменитель. Однако он обладает большей токсичностью, чем ацетон.
) основного продукта. Метилацетат также образуется в виде побочного продукта при производстве поливинилового спирта. По растворяющей способности метилацетат аналогичен ацетону и применяется в ряде случаев как его заменитель. Однако он обладает большей токсичностью, чем ацетон.
Этилацетат С2 Н5 СООСН3 . Получают методом этерификации на лесохимических предприятиях при переработке синтетической и лесохимической уксусной кислоты, гидролизного и синтетического этилового спирта или конденсацией ацетальдегида. За рубежом разработан процесс получения этилацетата на основе метилового спирта.
Этилацетат подобно ацетону растворяет большинство полимеров. По сравнению с ацетоном его преимущество в более высокой температуре кипения (меньшей летучести). Добавка 15-20 % этилового спирта повышает растворяющую способность этилацетата в отношении эфиров целлюлозы, особенно ацетилцеллюлозы.
Пропилацетат СН3 СООСН2 СН2 СН3 . По растворяющей способности подобен этилацетату.
По растворяющей способности подобен этилацетату.
Изопропилацетат СН3СООСН(СН3 )2 . По свойствам занимает промежуточное положение между этил- и пропилацетат.
Амилацетат CH3 COOCH2 CH2 CH2 CH2 CH3 , т. кип. 148° С, иногда называют «банановым маслом» (которое он напоминает по запаху). Он образуется в реакции между амиловым спиртом (часто – сивушным маслом) и уксусной кислотой в присутствии катализатора. Амилацетат широко применяется как растворитель для лаков, поскольку он испаряется медленнее, чем этилацетат.
Фруктовые эфиры. Характер многих фруктовых запахов, таких, как запахи малины, вишни, винограда и рома, отчасти обусловлен летучими эфирами, например этиловым и изоамиловым эфирами муравьиной, уксусной, масляной и валериановой кислот. Имеющиеся в продаже эссенции, имитирующие эти запахи, содержат подобные эфиры.
Винилацетат CH2 =CHOOCCH3 , образуется при взаимодействии уксусной кислоты с ацетиленом в присутствии катализатора. Это важный мономер для приготовления поливинилацетатных смол, клеев и красок.
Это важный мономер для приготовления поливинилацетатных смол, клеев и красок.
Мыла — это соли высших карбоновых кислот.Обычные мыла состоят главным образом из смеси солей пальмитиновой, стеариновой и олеиновой кислот. Натриевые соли образуют твердые мыла, калиевые соли — жидкие мыла.
Мыла получаются при гидролизе жиров в присутствии щелочей:
Обычное мыло плохо стирает в жесткой воде и совсем не стирает в морской воде, так как содержащиеся в ней ионы кальция и магния дают с высшими кислотами нерастворимые в воде соли:
Ca2+ + 2C17 H35COONa→Ca(C17 H35 COO)2 ↓ + 2Na+
В настоящее время для стирки в быту, для промывки шерсти и тканей в промышленности используют синтетические моющие средства, которые обладают в 10 раз большей моющей способностью, чем мыла, не портят тканей, не боятся жесткой и даже морской воды.
Физико-химические свойства сложных эфиров
| Название | Давление пара при 20°С, кПа | Молекулярная масса | Температура кипения при 101,325 кПа. °С °С | Плотность при 20°С. г/см3 | Показатель переломления n20 | Поверхностное натяжение 20°С. мН/м |
| Метилацетат | 23,19 | 74,078 | 56,324 | 0,9390 | 1,36193 | 24,7625,7 |
| Этилацетат | 9,86 | 88,104 | 77,114 | 0,90063 | 1,37239 | 23,75 |
| Пропилацетат | 3,41 | 102,13 | 101,548 | 0,8867 | 1,38442 | 20,53 |
| Изопропилацетат | 8,40 | 102,13 | 88,2 | 0,8718 | 1,37730 | 22,1022 |
| Бутилацетат | 2,40 | 116,156 | 126,114 | 0,8813 | 1,39406 | 25,2 |
| Изоиутилацетат | 1,71 | 116,156 | 118 | 0,8745 | 1,39018 | 23,7 |
| Втор-Бутилацетат | — | 116,156 | 112,34 | 0,8720 | 1,38941 | 23,3322,1 |
| Гексилацетат | — | 114,21 | 169 | 0,890 | — | — |
| Амилацетат | 2,09 | 130,182 | 149,2 | 0,8753 | 1,40228 | 25,8 |
| Изоамилацетат | 0,73 | 130,182 | 142 | 0,8719 | 1,40535 | 24,6221,1 |
| Ацетат монометилового эфира этиленгликоля (метилцеллозольвацетат) | 0,49 | 118,0 | 144,5 | 1,007 | 1,4019 | — |
| Ацетат моноэтилового эфира этиленгликоля (этилцеллозольвацетат) | 0,17 | 132,16 | 156,4 | 0,9748 | 1,4030 | — |
| Этиленгликольмоноацетат | — | 104 | 181-182 | 1,108-1,109 | — | — |
| Этиленгликольдиацетат | 0,05 | 146 | 186-190 | 1,106 | — | — |
| Циклогексилацетат | 0,97 | 142 | 175 | 0,964 | 1,4385 | — |
| Этиллактат | 0,13 | 118,13 | 154,5 | 1,031 | 1,4118 | 28,917,3 |
| Бутиллактат | 0,05 | 146,0 | 185 | 0,97 | — | — |
| Пропиленкарбонат | — | 102,088 | 241,7 | 1,206 | 1,4189 | — |
Не нашли что искали? Вы можете оставить заявку, в форме обратной связи.
Портал Gosstanart.info не осуществляет коммерческой деятельности, не сотрудничает с рекламодателями, производителями товаров и компаниями предоставляющими услуги. Просьба, не обращаться с коммерческими предложениями! Вся информация, представленная на портале, результат независимых исследований и является свободно распространяемой информацией.
Главная Новости портала Черный список Архив Обратная связь
Диэтиловый эфир трифторида бора | AMERICAN ELEMENTS®
РАЗДЕЛ 1. ИДЕНТИФИКАЦИЯ. БО-ТДЭ-02
, БО-ТДЭ-03
, БО-ТДЭ-04
, BO-TDE-05
Номер CAS: 109-63-7
Соответствующие установленные области применения вещества: Научные исследования и разработки
Сведения о поставщике:
American Elements
10884 Weyburn Ave.
Los Angeles, CA
Тел.: +1 310-208-0551
Факс: +1 310-208-0351
Телефон службы экстренной помощи в Северной Америке: 7 900: 1 800-424-9300 Классификация вещества или смеси Маркировка СГС элементы, включая меры предосторожности Сигнальное слово Вещества Описание мер первой помощи Средства пожаротушения Меры предосторожности для персонала, защитное снаряжение и порядок действий в чрезвычайных ситуациях Меры предосторожности для безопасного обращения параметры контроля рабочего места Информация об основных физических и химических свойствах Информация о токсикологическом воздействии Токсичность Методы обработки отходов скруббер, но проявляйте особую осторожность при воспламенении, так как этот материал легко воспламеняется. Предложите излишки и неперерабатываемые решения лицензированной компании по утилизации. Обратитесь в лицензированную профессиональную службу по утилизации отходов, чтобы утилизировать этот материал. DOT (US) SARA 302 Компоненты Паспорт безопасности (ЕС) № 1907/2006 (ДОСТИГАЕМОСТЬ). Приведенная выше информация считается верной, но не претендует на полноту и должна использоваться только в качестве руководства. Информация в этом документе основана на современном уровне наших знаний и применима к продукту с учетом соответствующих мер предосторожности. Это не является гарантией свойств продукта. American Elements не несет ответственности за любой ущерб, возникший в результате обращения или контакта с вышеуказанным продуктом. Перейти в конец галереи изображений Перейти к началу галереи изображений
Международный: +1 703-527-3887 РАЗДЕЛ 2.
 ИДЕНТИФИКАЦИЯ ОПАСНОСТИ
ИДЕНТИФИКАЦИЯ ОПАСНОСТИ
Классификация СГС в соответствии с 29 CFR 1910 (OSHA HCS)
Горючий 3), h326
Острая токсичность, Оральное (категория 4), h402
Острая токсичность, Вдыхание (Категория 2), h430
Разъедание кожи (Категория 1A), h414
Серьезное повреждение глаз (Категория 1), h418
Специфическая токсичность для органа-мишени — многократное воздействие, Вдыхание (Категория 1), h472
Пиктограмма
Опасность
Краткая(ые) характеристика(я) опасности
h326
Воспламеняющаяся жидкость и пар.
h402
Вреден при проглатывании.
h414
Вызывает серьезные ожоги кожи и повреждения глаз.
h418
Вызывает серьезное повреждение глаз.
h430
Смертельно при вдыхании.
h472
Вызывает поражение органов при длительном или многократном воздействии при вдыхании.
Меры предосторожности
P210
Хранить вдали от источников тепла/искр/открытого огня/горячих поверхностей. — Не курить.
— Не курить.
P233
Держите контейнер плотно закрытым.
P240
Заземлить/склеить контейнер и приемное оборудование.
P241
Использовать взрывозащищенное электрическое/вентиляционное/осветительное/оборудование.
P242
Используйте только искробезопасный инструмент.
P243
Примите меры предосторожности против статического разряда.
P260
Не вдыхать пыль/дым/газ/туман/пары/аэрозоль.
P264
Тщательно вымыть кожу после работы.
P270
Не ешьте, не пейте и не курите при использовании этого продукта.
P271
Использовать только на открытом воздухе или в хорошо проветриваемом помещении.
P280
Пользоваться защитными перчатками/ защитной одеждой/ средствами защиты глаз/ средствами защиты лица.
P284
Использовать средства защиты органов дыхания.
P301 + P312 + P330
ПРИ ПРОГЛАТЫВАНИИ: При плохом самочувствии обратитесь в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР или к врачу. Прополоскать рот.
P301 + P330 + P331
ПРИ ПРОГЛАТЫВАНИИ: Прополоскать рот. Не вызывает рвоту.
Не вызывает рвоту.
P303 + P361 + P353
ПРИ ПОПАДАНИИ НА КОЖУ (или волосы): Немедленно снять всю загрязненную одежду. Промойте кожу водой/душем.
P304 + P340 + P310
ПРИ ВДЫХАНИИ: Вынести пострадавшего на свежий воздух и обеспечить ему покой в удобном для дыхания положении. Немедленно позвоните в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР или к врачу/врачу.
P305 + P351 + P338 + P310
ПРИ ПОПАДАНИИ В ГЛАЗА: Осторожно промыть глаза водой в течение нескольких минут. Снимите контактные линзы, если они есть и это легко сделать. Продолжайте полоскать. Немедленно позвоните в ТОКСИКОЛОГИЧЕСКИЙ ЦЕНТР или к врачу/врачу.
P314
При плохом самочувствии обратитесь к врачу.
P363
Стирать загрязненную одежду перед повторным использованием.
P370 + P378
В случае пожара: Для тушения использовать сухой песок, сухой химикат или спиртостойкую пену.
P403 + P233
Хранить в хорошо проветриваемом месте. Держите контейнер плотно закрытым.
P403 + P235
Хранить в хорошо проветриваемом месте. Сохранять хладнокровие.
Сохранять хладнокровие.
P405
Хранить под замком.
P501
Утилизировать содержимое/контейнер на утвержденном предприятии по утилизации отходов
Опасности, не классифицированные иначе (HNOC) или не охваченные GHS
Бурно реагирует с водой. РАЗДЕЛ 3. СОСТАВ/ИНФОРМАЦИЯ О КОМПОНЕНТАХ
Синонимы: Трифторид бора этиловый эфир
Формула: BF3·C4h20O
Молекулярная масса: 141,93 г/моль
7-9-0: 30-9-0: 30-9-0: 30-9-0: 30-9-0: 309-024 CAS-Номер. .: 203-689-8 РАЗДЕЛ 4. МЕРЫ ПЕРВОЙ ПОМОЩИ
Общие рекомендации
Обратиться к врачу. Покажите этот паспорт безопасности лечащему врачу. Выйти из опасной зоны
При вдыхании
При вдыхании вывести пострадавшего на свежий воздух. Если человек не дышит, сделайте ему искусственно дыхание. Проконсультируйтесь с врачом.
При попадании на кожу
Немедленно снять загрязненную одежду и обувь. Смыть большим количеством воды с мылом. Немедленно доставьте пострадавшего в больницу. Проконсультируйтесь с врачом.
Немедленно доставьте пострадавшего в больницу. Проконсультируйтесь с врачом.
При попадании в глаза
Тщательно промыть большим количеством воды в течение не менее 15 минут и обратиться к врачу.
Продолжайте промывать глаза во время транспортировки в больницу.
При проглатывании
НЕ вызывать рвоту. Никогда не давайте ничего в рот человеку, находящемуся без сознания. Прополоскать рот водой. Проконсультируйтесь с врачом.
Наиболее важные симптомы и эффекты, как острые, так и замедленные
Наиболее важные известные симптомы и эффекты описаны на этикетке (см. раздел 2.2) и/или в разделе 11
Указание на необходимость немедленной медицинской помощи и специального лечения
Нет доступных данных РАЗДЕЛ 5. ПРОТИВОПОЖАРНЫЕ МЕРЫ
Подходящие средства пожаротушения
Сухой порошок
Особые опасности, исходящие от вещества или смеси
Оксиды углерода, Фторид водорода, Боран/оксиды бора
Рекомендации для пожарных
При тушении пожара надевайте автономный дыхательный аппарат, если это необходимо.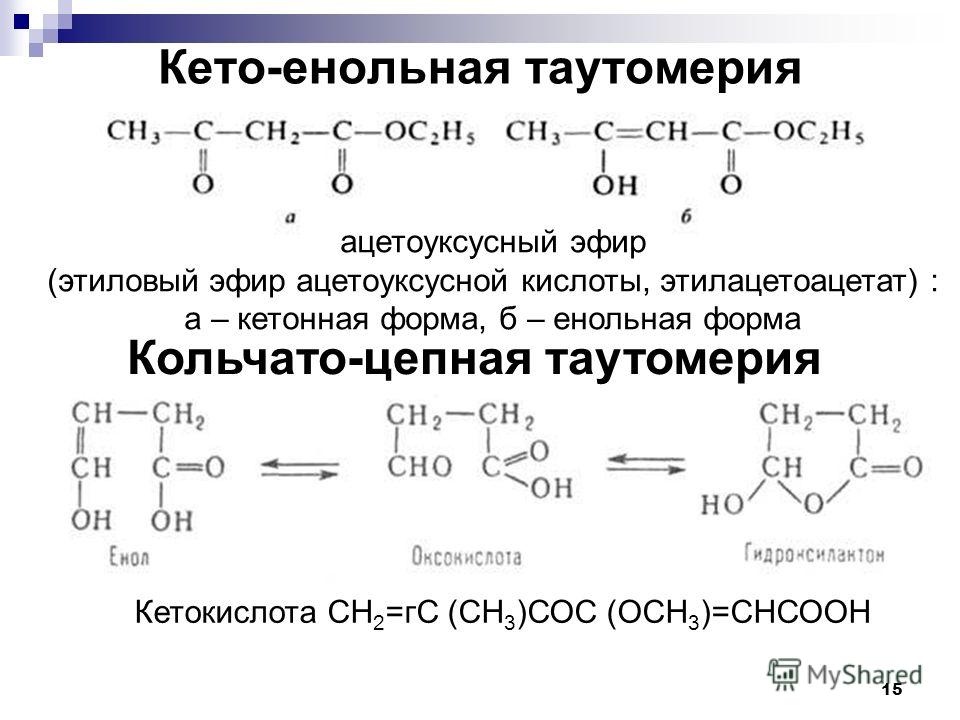
Дополнительная информация
Вода гидролизует материал с выделением кислого газа, который при контакте с металлическими поверхностями может образовывать горючий и/или взрывоопасный водород. РАЗДЕЛ 6. МЕРЫ ПРИ СЛУЧАЙНОМ ВЫБРОСЕ
Носить средства защиты органов дыхания. Избегайте вдыхания паров, тумана или газа. Обеспечьте достаточную вентиляцию. Удалить все источники возгорания. Эвакуируйте персонал в безопасные зоны. Остерегайтесь накопления паров с образованием взрывоопасных концентраций.
Пары могут скапливаться в низинах.
Индивидуальную защиту см. в разделе 8
Меры предосторожности по охране окружающей среды
Предотвратите дальнейшую утечку или разлив, если это безопасно. Не допускайте попадания продукта в канализацию.
Методы и материалы для локализации и очистки
Соберите утечку, а затем соберите пылесосом с электрозащитой или влажной щеткой и поместите в контейнер для утилизации в соответствии с местными правилами (см.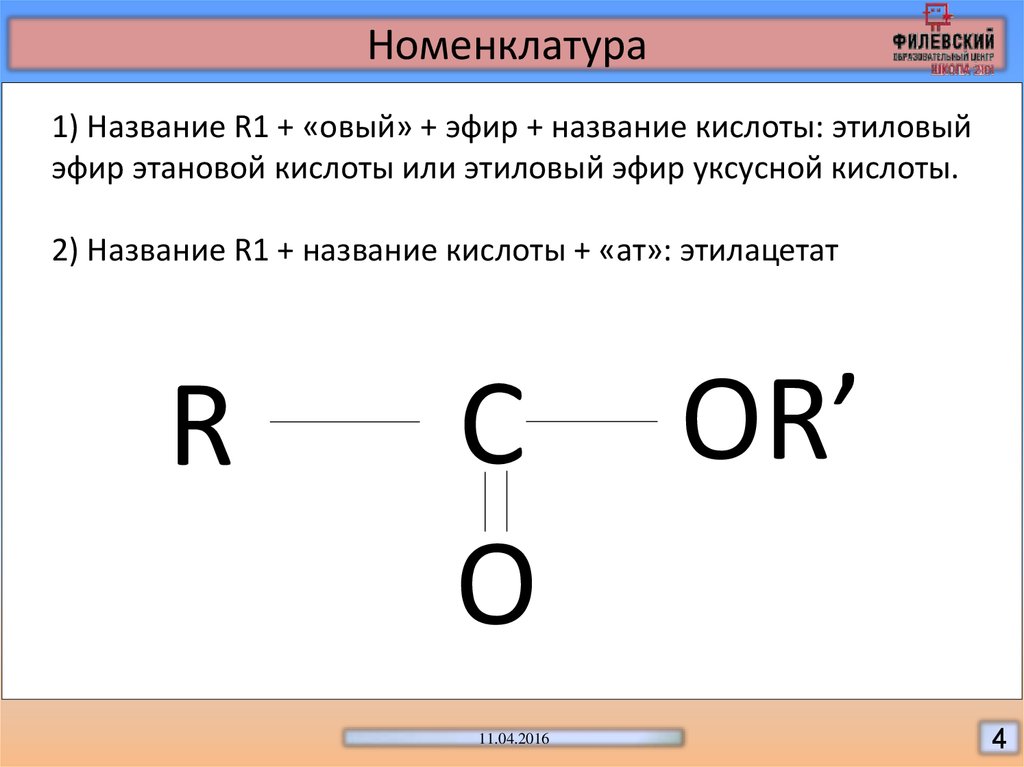 раздел 13). Не смывать водой.
раздел 13). Не смывать водой.
Ссылка на другие разделы
Информацию об утилизации см. в разделе 13 РАЗДЕЛ 7. ОБРАЩЕНИЕ И ХРАНЕНИЕ
Избегать контакта с кожей и глазами. Избегайте вдыхания паров или тумана.
Хранить вдали от источников воспламенения. Не курить. Принять меры для предотвращения накопления электростатического заряда.
Меры предосторожности см. в разделе 2.2.
Условия для безопасного хранения, включая любые несовместимости.
Хранить в атмосфере азота.
Хранить контейнер плотно закрытым в сухом и хорошо проветриваемом месте.
Контейнеры, которые открываются, должны быть тщательно запечатаны и храниться в вертикальном положении, чтобы предотвратить утечку.
Хранить вдали от воды. Никогда не допускайте контакта продукта с водой во время хранения.
Рекомендуемая температура хранения
2 — 8 °C
Хранить в атмосфере инертного газа.
Класс хранения (TRGS 510): Воспламеняющиеся жидкости
Конкретное конечное использование
Помимо использования, указанного в разделе 1. 2, никакие другие специальные применения не предусмотрены
2, никакие другие специальные применения не предусмотрены
Не содержит веществ с предельно допустимыми значениями воздействия на рабочем месте.
Контроль воздействия
Соответствующие технические средства контроля
Избегать контакта с кожей, глазами и одеждой. Мойте руки перед перерывами и сразу после работы с продуктом.
Средства индивидуальной защиты
Средства защиты глаз/лица
Плотно прилегающие защитные очки. Маска для лица (минимум 8 дюймов). Используйте средства защиты глаз, проверенные и одобренные в соответствии с соответствующими государственными стандартами, такими как NIOSH (США) или EN 166 (ЕС).
Защита кожи
Работать в перчатках. Перчатки должны быть проверены перед использованием. Используйте правильную технику снятия перчаток (не касаясь внешней поверхности перчатки), чтобы избежать контакта этого продукта с кожей. Утилизируйте загрязненные перчатки после использования в соответствии с применимыми законами и передовой лабораторной практикой. Вымойте и высушите руки.
Вымойте и высушите руки.
Защита тела
Полный костюм для защиты от химикатов, Огнестойкая антистатическая защитная одежда. Тип защитного снаряжения должен выбираться в соответствии с концентрацией и количеством опасного вещества на конкретном рабочем месте.
Защита органов дыхания
Если оценка риска показывает, что воздухоочистительные респираторы целесообразны, используйте полнолицевой респиратор с многоцелевым комбинированным (США) или респираторным картриджем типа ABEK (EN 14387) в качестве резерва средств технического контроля.
Если респиратор является единственным средством защиты, используйте полнолицевой респиратор с подачей воздуха. Используйте респираторы и компоненты, проверенные и одобренные в соответствии с соответствующими государственными стандартами, такими как NIOSH (США или CEN (ЕС).
Контроль воздействия окружающей среды
Предотвратите дальнейшую утечку или разлив, если это безопасно. Не допускайте попадания продукта в канализацию РАЗДЕЛ 9 ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА
а) Внешний вид
Форма: жидкость
b) Запах
Данные отсутствуют
c) Порог восприятия запаха
Данные отсутствуют
d) pH
Данные отсутствуют
e) Температура плавления/замерзания
Температура плавления/диапазон: -58 °C (-72 °F)
f) Начальная точка кипения и интервал кипения
126 -129 °C (259 -264 °F)
г) Температура вспышки
48 °C (118 °F) — закрытый тигель
ч) Скорость испарения
Нет данных имеется
i) Воспламеняемость (твердое вещество, газ)
Данные отсутствуют
j) Верхний/нижний пределы воспламеняемости или взрываемости
Верхний предел взрываемости: 36 %(V)
Нижний предел взрываемости: 1,9 %(V)
k) Давление пара
5,6 гПа (4,2 мм рт. ст.) при 20 °C (68 °F)
ст.) при 20 °C (68 °F)
л) Плотность пара
4,90-( Воздух = 1,0)
m) Относительная плотность
1,15 г/мл
n) Растворимость в воде
Нет данных
o) Коэффициент распределения: н-октанол/вода
Нет данных
p) Температура самовоспламенения
Нет данных
q) Температура разложения
Нет данных
r) Вязкость
Нет данных
s) Взрывоопасные свойства
Нет данных
t) Окислительные свойства
Нет данных
Другая информация по технике безопасности
Относительная плотность паров
4,90 — (Воздух = 1,0)
Химическая стабильность
Стабилен при соблюдении рекомендуемых условий хранения
Возможность опасных реакций
Бурно реагирует с водой.
Условия, которых следует избегать
Вода гидролизует материал с выделением кислого газа, который при контакте с металлическими поверхностями может образовывать легковоспламеняющийся и/или взрывоопасный газообразный водород. Не допускайте попадания воды в контейнер из-за бурной реакции.
Тепло, пламя и искры. Воздействие влаги.
Несовместимые материалы
Металлы, кислоты, Основания, Спирты, Щелочные металлы, Окислители, Вода
Опасные продукты разложения
Другие продукты разложения — Нет данных
В случае пожара: см. раздел 5
Острая токсичность
Нет данных
LC50 Вдыхание — Крыса — 4 часа — 1,2 мг/л
Кожный: Нет данных
Нет данных
Разъедание/раздражение кожи
Серьезное повреждение/раздражение глаз
Глаза — кролик
Результат: Разъедающее действие на глаза
Респираторная или кожная сенсибилизация
Нет данных
Мутагенность зародышевых клеток компонент этого продукта, присутствующий на уровне выше или равном 0,1%, идентифицируется IARC как
вероятный, возможный или подтвержденный канцероген для человека.
ACGIH:
Ни один из компонентов этого продукта, присутствующий на уровне выше или равном 0,1%, не идентифицирован как
канцероген или потенциальный канцероген ACGIH.
NTP:
Ни один из компонентов этого продукта, присутствующий в количествах, превышающих или равных 0,1%, не идентифицирован NTP как известный или ожидаемый канцероген.
OSHA:
Ни один компонент этого продукта, присутствующий в концентрациях выше или равных 0,1%, не идентифицирован OSHA как канцероген или потенциальный канцероген.
Репродуктивная токсичность
Нет данных
Нет данных
Специфическая токсичность для затронутого органа — однократное воздействие
Нет данных
Специфическая токсичность для органа-мишени — многократное воздействие
Вдыхание — Вызывает повреждение органов при длительном или многократном воздействии.
Опасность при аспирации
Нет данных
Дополнительная информация
RTECS: нет данных
Материал чрезвычайно разрушительно действует на ткани слизистых оболочек и верхних дыхательных путей, глаз и кожи., ощущение жжения, Кашель, свистящее дыхание, ларингит, Затрудненность дыхания, Головная боль, тошнота, рвота
Насколько нам известно, химические, физические и токсикологические свойства тщательно не исследовались.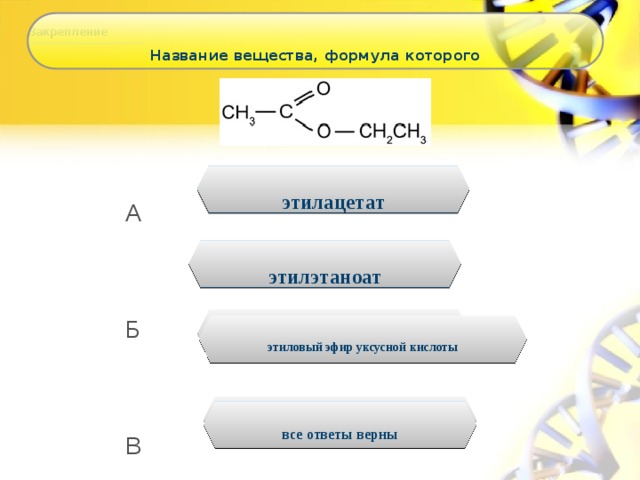 9
9 РАЗДЕЛ 12. ЭКОЛОГИЧЕСКАЯ ИНФОРМАЦИЯ
Токсичность для рыб Полевые исследования LC50 — Leuciscus idus (Golden orfe) — 22 —
Стойкость и способность к разложению
Способность к биоразложению
Результат: — Частично биоразлагаемый
Потенциал биоаккумуляции
Нет данных
Мобильность в почве
Нет данных
Результаты оценки PBT и vPvB
Оценка PBT/vPvB недоступна, так как оценка химической безопасности не требуется/не проводилась
Другие неблагоприятные воздействия
Нет данных РАЗДЕЛ 13. СООБРАЖЕНИЯ ПО УТИЛИЗАЦИИ
Загрязненная упаковка
Утилизировать как неиспользованный продукт.
РАЗДЕЛ 14. ИНФОРМАЦИЯ О ТРАНСПОРТИРОВКЕ
Номер ООН: 2604
Класс: 8(3)
Группа упаковки: I
Надлежащее отгрузочное наименование: Трифторид бора диэтилэфират
Вдыхание Poison Отчетное количество (R24): 90 Опасность: №
IMDG
Номер ООН: 2604
Класс: 8(3)
Группа упаковки: I
EMS-No: F-E, S-C
Надлежащее отгрузочное наименование: BORON TRIFTORIDE DIETHYL ETHERATE
IATA
Номер ООН: 2604
Класс: 8(3)
Группа упаковки: I
Надлежащее отгрузочное наименование: Трифторид бора диэтиловый эфир РАЗДЕЛ 15. НОРМАТИВНАЯ ИНФОРМАЦИЯ
Никакие химические вещества в этом материале не подпадают под действие отчетности. требованиям SARA, Раздел III, Раздел 302.
Компоненты SARA 313
Этот материал не содержит химических компонентов с известными номерами CAS, которые превышают пороговые (De Minimis) уровни отчетности, установленные SARA, Раздел III, Раздел 313.
SARA 311/312 Опасности
Опасность пожара, острая опасность для здоровья, хроническая опасность для здоровья
Массачусетс/Пенсильвания/Нью-Джерси Право знать компоненты
Диэтиловый эфир-трифторид бора
CAS-No.109-63-7 04-24
California Prop. 65 Component
Этот продукт не содержит каких-либо химических веществ, которые, как известно штату Калифорния, вызывают рак, врожденные дефекты или любое другое нарушение репродуктивной функции РАЗДЕЛ 16. ПРОЧАЯ ИНФОРМАЦИЯ
 Дополнительные условия продажи см. на обратной стороне счета-фактуры или упаковочного листа. АВТОРСКОЕ ПРАВО 1997-2022 АМЕРИКАНСКИЕ ЭЛЕМЕНТЫ. ПРЕДОСТАВЛЯЕТСЯ ЛИЦЕНЗИЯ НА ИЗГОТОВЛЕНИЕ НЕОГРАНИЧЕННОГО БУМАЖНОГО КОПИЯ ТОЛЬКО ДЛЯ ВНУТРЕННЕГО ИСПОЛЬЗОВАНИЯ.
Дополнительные условия продажи см. на обратной стороне счета-фактуры или упаковочного листа. АВТОРСКОЕ ПРАВО 1997-2022 АМЕРИКАНСКИЕ ЭЛЕМЕНТЫ. ПРЕДОСТАВЛЯЕТСЯ ЛИЦЕНЗИЯ НА ИЗГОТОВЛЕНИЕ НЕОГРАНИЧЕННОГО БУМАЖНОГО КОПИЯ ТОЛЬКО ДЛЯ ВНУТРЕННЕГО ИСПОЛЬЗОВАНИЯ. Комплекс трехфтористого бора и этилового эфира | КАС 109-63-7 | TCI-B0527
Трифторид бора – комплекс этилового эфира
Молекулярная формула:
BF3•C4h20O
Номер каталога:
ТКИ-B0527
Производитель:
ОТК Америка
Количество CAS:
109-63-7
Услуги и сборы Spectrum Freight
Пожалуйста, ознакомьтесь с нашими 16 марта 2020 г. ВАЖНОЕ ОБНОВЛЕНИЕ и 2 апреля 2020 г. ВАЖНОЕ ОБНОВЛЕНИЕ о получении отправлений во время кризиса, связанного с коронавирусом.