Ацетоуксусный эфир. Ацетоуксусный эфир формула
Ацетоуксусный эфир — Википедия
Материал из Википедии — свободной энциклопедии
Перейти к навигации Перейти к поиску| Ацетоуксусный эфир | |
 | |
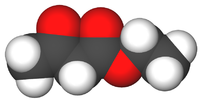 | |
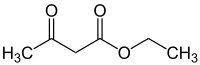
| Этил-3-оксобутаноат | |
| Этилацетоуксусный эфир,этиловый эфир ацетоуксусной кислоты,этилацетоацетат | |
| Ch4COCh3COOС2Н5 | |
| C6h20O3 | |
| бесцветная жидкость с фруктовым запахом | |
| 130,1418 ± 0,0064 г/моль | |
| 1,0284 г/см³ | |
| -45 °C | |
| 180,8 °C | |
| 84 °C | |
| 304 °C | |
| 9,5 % | |
| 100 Па при 20 °С | |
| 10,68 (в воде), 14,2 (в ДМСО) | |
| 2,86 г/100 мл | |
| 1,4198 | |
ru.bywiki.com
Ацетоуксусный эфир - WikiVisually
1. Химическая формула – These are limited to a single typographic line of symbols, which may include subscripts and superscripts. A chemical formula is not a name, and it contains no words. Although a chemical formula may imply certain simple chemical structures, it is not the same as a full chemical structural formula. Chemical formulas can fully specify the structure of only the simplest of molecules and chemical substances, the simplest types of chemical formulas are called empirical formulas, which use letters and numbers indicating the numerical proportions of atoms of each type. Molecular formulas indicate the numbers of each type of atom in a molecule. For example, the formula for glucose is Ch3O, while its molecular formula is C6h22O6. This is possible if the relevant bonding is easy to show in one dimension, an example is the condensed molecular/chemical formula for ethanol, which is Ch4-Ch3-OH or Ch4Ch3OH. For reasons of structural complexity, there is no condensed chemical formula that specifies glucose, chemical formulas may be used in chemical equations to describe chemical reactions and other chemical transformations, such as the dissolving of ionic compounds into solution. A chemical formula identifies each constituent element by its chemical symbol, in empirical formulas, these proportions begin with a key element and then assign numbers of atoms of the other elements in the compound, as ratios to the key element. For molecular compounds, these numbers can all be expressed as whole numbers. For example, the formula of ethanol may be written C2H6O because the molecules of ethanol all contain two carbon atoms, six hydrogen atoms, and one oxygen atom. Some types of compounds, however, cannot be written with entirely whole-number empirical formulas. An example is boron carbide, whose formula of CBn is a variable non-whole number ratio with n ranging from over 4 to more than 6.5. When the chemical compound of the consists of simple molecules. These types of formulas are known as molecular formulas and condensed formulas. A molecular formula enumerates the number of atoms to reflect those in the molecule, so that the formula for glucose is C6h22O6 rather than the glucose empirical formula. However, except for very simple substances, molecular chemical formulas lack needed structural information, for simple molecules, a condensed formula is a type of chemical formula that may fully imply a correct structural formula. For example, ethanol may be represented by the chemical formula Ch4Ch3OH
2. Агрегатное состояние – In physics, a state of matter is one of the distinct forms that matter takes on. Four states of matter are observable in everyday life, solid, liquid, gas, some other states are believed to be possible but remain theoretical for now. For a complete list of all states of matter, see the list of states of matter. Historically, the distinction is based on qualitative differences in properties. Matter in the state maintains a fixed volume and shape, with component particles close together. Matter in the state maintains a fixed volume, but has a variable shape that adapts to fit its container. Its particles are close together but move freely. Matter in the state has both variable volume and shape, adapting both to fit its container. Its particles are close together nor fixed in place. Matter in the state has variable volume and shape, but as well as neutral atoms, it contains a significant number of ions and electrons. Plasma is the most common form of matter in the universe. The term phase is used as a synonym for state of matter. In a solid the particles are packed together. The forces between particles are strong so that the particles move freely but can only vibrate. As a result, a solid has a stable, definite shape, solids can only change their shape by force, as when broken or cut. In crystalline solids, the particles are packed in a regularly ordered, there are various different crystal structures, and the same substance can have more than one structure. For example, iron has a cubic structure at temperatures below 912 °C. Ice has fifteen known crystal structures, or fifteen solid phases, glasses and other non-crystalline, amorphous solids without long-range order are not thermal equilibrium ground states, therefore they are described below as nonclassical states of matter
3. Плотность – The density, or more precisely, the volumetric mass density, of a substance is its mass per unit volume. The symbol most often used for density is ρ, although the Latin letter D can also be used. Mathematically, density is defined as mass divided by volume, ρ = m V, where ρ is the density, m is the mass, and V is the volume. In some cases, density is defined as its weight per unit volume. For a pure substance the density has the numerical value as its mass concentration. Different materials usually have different densities, and density may be relevant to buoyancy, purity, osmium and iridium are the densest known elements at standard conditions for temperature and pressure but certain chemical compounds may be denser. Thus a relative density less than one means that the floats in water. The density of a material varies with temperature and pressure and this variation is typically small for solids and liquids but much greater for gases. Increasing the pressure on an object decreases the volume of the object, increasing the temperature of a substance decreases its density by increasing its volume. In most materials, heating the bottom of a results in convection of the heat from the bottom to the top. This causes it to rise relative to more dense unheated material, the reciprocal of the density of a substance is occasionally called its specific volume, a term sometimes used in thermodynamics. Density is a property in that increasing the amount of a substance does not increase its density. Archimedes knew that the irregularly shaped wreath could be crushed into a cube whose volume could be calculated easily and compared with the mass, upon this discovery, he leapt from his bath and ran naked through the streets shouting, Eureka. As a result, the term eureka entered common parlance and is used today to indicate a moment of enlightenment, the story first appeared in written form in Vitruvius books of architecture, two centuries after it supposedly took place. Some scholars have doubted the accuracy of this tale, saying among other things that the method would have required precise measurements that would have been difficult to make at the time, from the equation for density, mass density has units of mass divided by volume. As there are units of mass and volume covering many different magnitudes there are a large number of units for mass density in use. The SI unit of kilogram per metre and the cgs unit of gram per cubic centimetre are probably the most commonly used units for density.1,000 kg/m3 equals 1 g/cm3. In industry, other larger or smaller units of mass and or volume are often more practical, see below for a list of some of the most common units of density
4. Температура плавления – The melting point of a solid is the temperature at which it changes state from solid to liquid at atmospheric pressure. At the melting point the solid and liquid phase exist in equilibrium, the melting point of a substance depends on pressure and is usually specified at standard pressure. When considered as the temperature of the change from liquid to solid. Because of the ability of some substances to supercool, the point is not considered as a characteristic property of a substance. For most substances, melting and freezing points are approximately equal, for example, the melting point and freezing point of mercury is 234.32 kelvins. However, certain substances possess differing solid-liquid transition temperatures, for example, agar melts at 85 °C and solidifies from 31 °C to 40 °C, such direction dependence is known as hysteresis. The melting point of ice at 1 atmosphere of pressure is close to 0 °C. In the presence of nucleating substances the freezing point of water is the same as the melting point, the chemical element with the highest melting point is tungsten, at 3687 K, this property makes tungsten excellent for use as filaments in light bulbs. Many laboratory techniques exist for the determination of melting points, a Kofler bench is a metal strip with a temperature gradient. Any substance can be placed on a section of the strip revealing its thermal behaviour at the temperature at that point, differential scanning calorimetry gives information on melting point together with its enthalpy of fusion. A basic melting point apparatus for the analysis of crystalline solids consists of an oil bath with a transparent window, the several grains of a solid are placed in a thin glass tube and partially immersed in the oil bath. The oil bath is heated and with the aid of the melting of the individual crystals at a certain temperature can be observed. In large/small devices, the sample is placed in a heating block, the measurement can also be made continuously with an operating process. For instance, oil refineries measure the point of diesel fuel online, meaning that the sample is taken from the process. This allows for more frequent measurements as the sample does not have to be manually collected, for refractory materials the extremely high melting point may be determined by heating the material in a black body furnace and measuring the black-body temperature with an optical pyrometer. For the highest melting materials, this may require extrapolation by several hundred degrees, the spectral radiance from an incandescent body is known to be a function of its temperature. An optical pyrometer matches the radiance of a body under study to the radiance of a source that has been previously calibrated as a function of temperature, in this way, the measurement of the absolute magnitude of the intensity of radiation is unnecessary. However, known temperatures must be used to determine the calibration of the pyrometer, for temperatures above the calibration range of the source, an extrapolation technique must be employed
5. Температура кипения – The boiling point of a substance is the temperature at which the vapor pressure of the liquid equals the pressure surrounding the liquid and the liquid changes into a vapor. The boiling point of a liquid varies depending upon the environmental pressure. A liquid in a vacuum has a lower boiling point than when that liquid is at atmospheric pressure. A liquid at high pressure has a boiling point than when that liquid is at atmospheric pressure. For a given pressure, different liquids boil at different temperatures, for example, water boils at 100 °C at sea level, but at 93.4 °C at 2,000 metres altitude. The normal boiling point of a liquid is the case in which the vapor pressure of the liquid equals the defined atmospheric pressure at sea level,1 atmosphere. At that temperature, the pressure of the liquid becomes sufficient to overcome atmospheric pressure. The standard boiling point has been defined by IUPAC since 1982 as the temperature at which boiling occurs under a pressure of 1 bar, the heat of vaporization is the energy required to transform a given quantity of a substance from a liquid into a gas at a given pressure. Liquids may change to a vapor at temperatures below their boiling points through the process of evaporation, evaporation is a surface phenomenon in which molecules located near the liquids edge, not contained by enough liquid pressure on that side, escape into the surroundings as vapor. On the other hand, boiling is a process in which molecules anywhere in the liquid escape, a saturated liquid contains as much thermal energy as it can without boiling. The saturation temperature is the temperature for a corresponding saturation pressure at which a liquid boils into its vapor phase, the liquid can be said to be saturated with thermal energy. Any addition of energy results in a phase transition. If the pressure in a system remains constant, a vapor at saturation temperature will begin to condense into its liquid phase as thermal energy is removed, similarly, a liquid at saturation temperature and pressure will boil into its vapor phase as additional thermal energy is applied. The boiling point corresponds to the temperature at which the pressure of the liquid equals the surrounding environmental pressure. Thus, the point is dependent on the pressure. Boiling points may be published with respect to the NIST, USA standard pressure of 101.325 kPa, at higher elevations, where the atmospheric pressure is much lower, the boiling point is also lower. The boiling point increases with increased pressure up to the critical point, the boiling point cannot be increased beyond the critical point. Likewise, the point decreases with decreasing pressure until the triple point is reached
6. Температура вспышки – The flash point is the lowest temperature at which vapours of a volatile material will ignite, when given an ignition source. The flash point may sometimes be confused with the autoignition temperature, the fire point is the lowest temperature at which the vapor will keep burning after being ignited and the ignition source removed. The fire point is higher than the point, because at the flash point the vapor may be reliably expected to cease burning when the ignition source is removed. The flash point is a characteristic that is used to distinguish between flammable liquids, such as petrol, and combustible liquids, such as diesel. It is also used to characterize the fire hazards of liquids, all liquids have a specific vapor pressure, which is a function of that liquids temperature and is subject to Boyles Law. As temperature increases, vapor pressure increases, as vapor pressure increases, the concentration of vapor of a flammable or combustible liquid in the air increases. Hence, temperature determines the concentration of vapor of the liquid in the air. The flash point is the lowest temperature at which there will be enough flammable vapor to induce ignition when a source is applied. There are two types of flash point measurement, open cup and closed cup. In open cup devices, the sample is contained in a cup which is heated and, at intervals. The measured flash point will vary with the height of the flame above the liquid surface and, at sufficient height. The best-known example is the Cleveland open cup, in both these types, the cups are sealed with a lid through which the ignition source can be introduced. Closed cup testers normally give lower values for the point than open cup and are a better approximation to the temperature at which the vapour pressure reaches the lower flammable limit. The flash point is an empirical measurement rather than a physical parameter. The measured value will vary with equipment and test protocol variations, including temperature ramp rate, time allowed for the sample to equilibrate, sample volume, methods for determining the flash point of a liquid are specified in many standards. For example, testing by the Pensky-Martens closed cup method is detailed in ASTM D93, IP34, ISO2719, DIN51758, JIS K2265 and AFNOR M07-019. Determination of flash point by the Small Scale closed cup method is detailed in ASTM D3828 and D3278, EN ISO3679 and 3680, cEN/TR15138 Guide to Flash Point Testing and ISO TR29662 Guidance for Flash Point Testing cover the key aspects of flash point testing. Gasoline is a used in a spark-ignition engine
7. Константа диссоциации кислоты – An acid dissociation constant, Ka, is a quantitative measure of the strength of an acid in solution. It is the constant for a chemical reaction known as dissociation in the context of acid–base reactions. In the example shown in the figure, HA represents acetic acid, and A− represents the acetate ion, the chemical species HA, A− and h4O+ are said to be in equilibrium when their concentrations do not change with the passing of time. The definition can then be more simply H A ⇌ A − + H +, K a = This is the definition in common usage. A weak acid has a pKa value in the approximate range −2 to 12 in water, pKa values for strong acids can, however, be estimated by theoretical means. The definition can be extended to non-aqueous solvents, such as acetonitrile and dimethylsulfoxide. Denoting a solvent molecule by S H A + S ⇌ A − + S H +, K a = When the concentration of solvent molecules can be taken to be constant, K a =, as before. The value of pKa also depends on structure of the acid in many ways. For example, Pauling proposed two rules, one for successive pKa of polyprotic acids, and one to estimate the pKa of oxyacids based on the number of =O and −OH groups. Other structural factors that influence the magnitude of the dissociation constant include inductive effects, mesomeric effects. Hammett type equations have frequently applied to the estimation of pKa. The quantitative behaviour of acids and bases in solution can be only if their pKa values are known. These calculations find application in different areas of chemistry, biology, medicine. Acid dissociation constants are essential in aquatic chemistry and chemical oceanography. In living organisms, acid–base homeostasis and enzyme kinetics are dependent on the pKa values of the acids and bases present in the cell. According to Arrheniuss original definition, an acid is a substance that dissociates in solution, releasing the hydrogen ion H+. The equilibrium constant for this reaction is known as a dissociation constant. Brønsted and Lowry generalised this further to an exchange reaction
8. Растворимость – Solubility is the property of a solid, liquid, or gaseous chemical substance called solute to dissolve in a solid, liquid, or gaseous solvent. The solubility of a substance depends on the physical and chemical properties of the solute and solvent as well as on temperature, pressure. The solubility of a substance is a different property from the rate of solution. Most often, the solvent is a liquid, which can be a substance or a mixture. One may also speak of solid solution, but rarely of solution in a gas, the extent of solubility ranges widely, from infinitely soluble such as ethanol in water, to poorly soluble, such as silver chloride in water. The term insoluble is often applied to poorly or very poorly soluble compounds, a common threshold to describe something as insoluble is less than 0.1 g per 100 mL of solvent. Under certain conditions, the solubility can be exceeded to give a so-called supersaturated solution. Metastability of crystals can also lead to apparent differences in the amount of a chemical that dissolves depending on its form or particle size. A supersaturated solution generally crystallises when seed crystals are introduced and rapid equilibration occurs, phenylsalicylate is one such simple observable substance when fully melted and then cooled below its fusion point. Solubility is not to be confused with the ability to dissolve a substance, for example, zinc dissolves in hydrochloric acid as a result of a chemical reaction releasing hydrogen gas in a displacement reaction. The zinc ions are soluble in the acid, the smaller a particle is, the faster it dissolves although there are many factors to add to this generalization. Crucially solubility applies to all areas of chemistry, geochemistry, inorganic, physical, organic, in all cases it will depend on the physical conditions and the enthalpy and entropy directly relating to the solvents and solutes concerned. By far the most common solvent in chemistry is water which is a solvent for most ionic compounds as well as a range of organic substances. This is a factor in acidity/alkalinity and much environmental and geochemical work. According to the IUPAC definition, solubility is the composition of a saturated solution expressed as a proportion of a designated solute in a designated solvent. Solubility may be stated in units of concentration such as molarity, molality, mole fraction, mole ratio, mass per volume. Solubility occurs under dynamic equilibrium, which means that solubility results from the simultaneous and opposing processes of dissolution, the solubility equilibrium occurs when the two processes proceed at a constant rate. The term solubility is used in some fields where the solute is altered by solvolysis
9. SMILES – The simplified molecular-input line-entry system is a specification in form of a line notation for describing the structure of chemical species using short ASCII strings. SMILES strings can be imported by most molecule editors for conversion back into two-dimensional drawings or three-dimensional models of the molecules, the original SMILES specification was initiated in the 1980s. It has since modified and extended. In 2007, a standard called OpenSMILES was developed in the open-source chemistry community. Other linear notations include the Wiswesser Line Notation, ROSDAL and SLN, the original SMILES specification was initiated by David Weininger at the USEPA Mid-Continent Ecology Division Laboratory in Duluth in the 1980s. The Environmental Protection Agency funded the project to develop SMILES. It has since modified and extended by others, most notably by Daylight Chemical Information Systems. In 2007, a standard called OpenSMILES was developed by the Blue Obelisk open-source chemistry community. Other linear notations include the Wiswesser Line Notation, ROSDAL and SLN, in July 2006, the IUPAC introduced the InChI as a standard for formula representation. SMILES is generally considered to have the advantage of being slightly more human-readable than InChI, the term SMILES refers to a line notation for encoding molecular structures and specific instances should strictly be called SMILES strings. However, the term SMILES is also used to refer to both a single SMILES string and a number of SMILES strings, the exact meaning is usually apparent from the context. The terms canonical and isomeric can lead to confusion when applied to SMILES. The terms describe different attributes of SMILES strings and are not mutually exclusive, typically, a number of equally valid SMILES strings can be written for a molecule. For example, CCO, OCC and CC all specify the structure of ethanol, algorithms have been developed to generate the same SMILES string for a given molecule, of the many possible strings, these algorithms choose only one of them. This SMILES is unique for each structure, although dependent on the algorithm used to generate it. These algorithms first convert the SMILES to a representation of the molecular structure. A common application of canonical SMILES is indexing and ensuring uniqueness of molecules in a database, there is currently no systematic comparison across commercial software to test if such flaws exist in those packages. SMILES notation allows the specification of configuration at tetrahedral centers, and these are structural features that cannot be specified by connectivity alone and SMILES which encode this information are termed isomeric SMILES
10. International Chemical Identifier – Initially developed by IUPAC and NIST from 2000 to 2005, the format and algorithms are non-proprietary. The continuing development of the standard has supported since 2010 by the not-for-profit InChI Trust. The current version is 1.04 and was released in September 2011, prior to 1.04, the software was freely available under the open source LGPL license, but it now uses a custom license called IUPAC-InChI Trust License. Not all layers have to be provided, for instance, the layer can be omitted if that type of information is not relevant to the particular application. InChIs can thus be seen as akin to a general and extremely formalized version of IUPAC names and they can express more information than the simpler SMILES notation and differ in that every structure has a unique InChI string, which is important in database applications. Information about the 3-dimensional coordinates of atoms is not represented in InChI, the InChI algorithm converts input structural information into a unique InChI identifier in a three-step process, normalization, canonicalization, and serialization. The InChIKey, sometimes referred to as a hashed InChI, is a fixed length condensed digital representation of the InChI that is not human-understandable. The InChIKey specification was released in September 2007 in order to facilitate web searches for chemical compounds and it should be noted that, unlike the InChI, the InChIKey is not unique, though collisions can be calculated to be very rare, they happen. In January 2009 the final 1.02 version of the InChI software was released and this provided a means to generate so called standard InChI, which does not allow for user selectable options in dealing with the stereochemistry and tautomeric layers of the InChI string. The standard InChIKey is then the hashed version of the standard InChI string, the standard InChI will simplify comparison of InChI strings and keys generated by different groups, and subsequently accessed via diverse sources such as databases and web resources. Every InChI starts with the string InChI= followed by the version number and this is followed by the letter S for standard InChIs. The remaining information is structured as a sequence of layers and sub-layers, the layers and sub-layers are separated by the delimiter / and start with a characteristic prefix letter. The six layers with important sublayers are, Main layer Chemical formula and this is the only sublayer that must occur in every InChI. The atoms in the formula are numbered in sequence, this sublayer describes which atoms are connected by bonds to which other ones. Describes how many hydrogen atoms are connected to each of the other atoms, the condensed,27 character standard InChIKey is a hashed version of the full standard InChI, designed to allow for easy web searches of chemical compounds. Most chemical structures on the Web up to 2007 have been represented as GIF files, the full InChI turned out to be too lengthy for easy searching, and therefore the InChIKey was developed. With all databases currently having below 50 million structures, such duplication appears unlikely at present, a recent study more extensively studies the collision rate finding that the experimental collision rate is in agreement with the theoretical expectations. Example, Morphine has the structure shown on the right, as the InChI cannot be reconstructed from the InChIKey, an InChIKey always needs to be linked to the original InChI to get back to the original structure
wikivisually.com
34.Понятие о кетокислотах на примере ацетоуксусной кислоты. Ацетоуксусный эфир, кето-енольная таутомерия. Кетонное расщепление ацетоуксусного эфира.
Ацетоуксусная кислота (формула СН3·CO·СН2СООН) — органическая кетокислота; промежуточный продукт обменажирных кислотиаминокислот. Ацетоуксусная кислота — органическое соединение из группы β-кетокислот.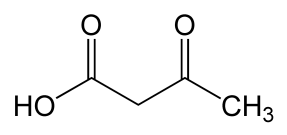
Для ацетоуксусной кислоты характерна кето-енольная таутомерия. В результатеиндуктивного эффектакетогруппыацетоуксусная кислота является более «кислой», чем её основа -масляная кислота.
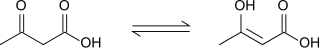
Ацетоуксусная кислота реагирует с галогенами(хлоромилибромом), которые разлагают её до соответствующегогалогеноводорода,углекислого газаи галоидацетона (хлор- или бромацетона):
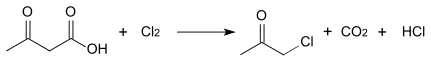
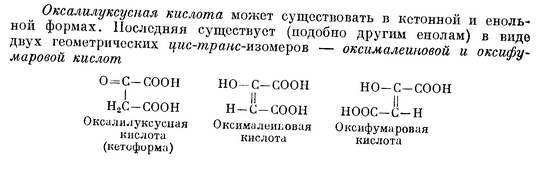
Реакции кетонного расщепления ацетоуксусного эфира
35.Гетерофункциональные производные бензольного ряда как лекарственные средства. Салициловая кислота и ее производные (ацетилсалициловая кислота, фенилсалицилат, метилсалицилат).
Среди монофункциональных производных бензола особое место занимает производное с карбоксильной группой — бензойная кислота͵ применяемая в медицине в виде натриевой соли (натрия бензоат) как отхаркивающее средство.
Бензойная кислота в свободном виде встречается в некоторых смолах и бальзамах, а также клюкве, бруснике, но чаще содержится в связанном виде. Как гетерофункциональное соединение п- аминофенол образует производные по каждой функциональной группе в отдельности и одновременно по двум функциональным группам. п-Аминофенол ядовит. Интерес для медицины представляют его производные – парацетамол, фенацетин, оказывающие анальгетическое (обезболивающее) и жаропонижающее действие.
Парацетамол является N-ацетильным производным п-аминофенола. Фенацетин получается при ацетилировании этилового эфира п-аминофенола, называемого фенетидином.
Эфиры ароматических аминокислот обладают общим свойством – способностью в какой-либо степени вызывать местную анестезию, ᴛ.ᴇ. потерю чувствительности. Особенно заметно это свойство выражено у пара- производных. В медицине используют анестезин и новокаин. Новокаин применяют в виде соли (гидрохлорида), что связано с крайне важно стью повышения его растворимости в воде.
п-Аминобензойная кислота является фактором роста микроорганизмов и участвует в синтезе фолиевой кислоты, при недостатке или отсутствии которой микроорганизмы погибают. Название кислоты связано с выделением ее из листьев шпината (от лат. folium – лист). Фолиевая кислота играет важную роль в метаболизме нуклеиновых кислот и белков; в организме человека не синтезируется.
Фолиевая кислота (витамин В) включает три структурных фрагмента — ядро птеридина, п-аминобензойную и L-глутаминовую кислоты. Обе функциональные группы п- аминобензойной кислоты участвуют в образовании связей с двумя другими компонентами.
Салициловая кислота относится к группе гидроксибензойных кислот. Как о-гидроксибензойная кислота она легко декарбоксилируется при нагревании с образованием фенола.
Салициловая кислота растворима в воде, дает интенсивное окрашивание с хлоридом железа(III) (качественное обнаружение фенольной гидроксильной группы). Она оказывает антиспазматическое, жаропонижающее и антигрибковое действие, но как сильная кислота (рКа 2,98) вызывает раздражение пищеварительного тракта и в связи с этим применяется только наружно. Внутрь применяют ее производные – соли или эфиры. Салициловая кислота способна образовывать производные по любой функциональной группе. Практическое значение имеют салицилат натрия, сложные эфиры по СООН-группе (метилсалицилат, фенилсалицилат (салол)) и ОН-группе – ацетилсалициловая кислота (аспирин). Перечисленные производные (кроме салола) оказывают анальгетическое, жаропонижающее и противовоспалительное действие. Метилсалицилат из-за раздражающего действия используется наружно в составе мазей. Салол применяется как дезинфицирующее средство при кишечных заболеваниях и примечателен тем, что в кислой среде желудка не гидролизуется, а распадается только в кишечнике, в связи с этим используется также в качестве материала для защитных оболочек некоторых лекарственных средств, которые не стабильны в кислой среде желудка.
Из других производных салициловой кислоты большое значение имеет п- аминосалициловая кислота (ПАСК) как противотуберкулезное средство. ПАСК является антагонистом п-аминобензойной кислоты, крайне важно й для нормальной жизнедеятельности микроорганизмов. Другие изомеры таким действием не обладают. м-Аминосалициловая кислота является высокотоксичным веществом.
фенилсалицилат
Антисептическое средство, расщепляясь в щелочном содержимом кишечника, высвобождает салициловую кислоту и фенол. Салициловая кислота оказывает жаропонижающее и противовоспалительное действие, фенол активен в отношении патогенной микрофлоры кишечника.Оказывает некоторое уроантисептическое действие.По сравнению с современными противомикробными ЛС фенилсалицилат менее активен, но малотоксичен, не раздражает слизистую оболочку желудка, не вызывает дисбактериоза и др.осложнений противомикробной терапии.
метилсалицилат представляет собой жидкость, обладающую противовоспалительным, обезболивающим, раздражающим и отвлекающим действием. Препарат назначают при ревматизме, радикулите, артрите, экссудативном плеврите.
studfiles.net
Ацетоуксусный эфир Википедия
| Ацетоуксусный эфир | |
 | |
 | |
| Этил-3-оксобутаноат | |
| Этилацетоуксусный эфир,этиловый эфир ацетоуксусной кислоты,этилацетоацетат | |
| Ch4COCh3COOС2Н5 | |
| C6h20O3 | |
| бесцветная жидкость с фруктовым запахом | |
| 130,1418 ± 0,0064 г/моль | |
| 1,0284 г/см³ | |
| -45 °C | |
| 180,8 °C | |
| 84 °C | |
| 304 °C | |
| 9,5 % | |
| 100 Па при 20 °С | |
| 10,68 (в воде), 14,2 (в ДМСО) | |
| 2,86 г/100 мл | |
| 1,4198 | |
| 141-97-9 | |
| 8868 | |
| 205-516-1 | |
| AK5250000 | |
| 4893 | |
| 13865426 | |
| 3895 мг/кг (крысы, перорально) | |
| Слаботоксичен, высокотоксичен при действии на кожу, ирритант  | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Ацетоуксусный эфир , также этиловый эфир ацетоуксусной кислоты, этилацетоацетат — органическое соединение, сложный эфир, бесцветная подвижная жидкость со своеобразным нерезким запахом. Растворяется в воде (14,3 % при 16,5 °C), смешивается с этанолом и диэтиловым эфиром.
Свойства[ | код]
Для ацетоуксусного эфира, как и для других 1,3-дикарбонильных соединений характерна
ru-wiki.ru
Ацетоуксусный эфир — википедия орг
Для ацетоуксусного эфира, как и для других 1,3-дикарбонильных соединений характерна кето-енольная таутомерия:
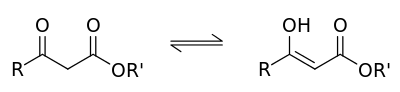 ,
,Согласно правилу Эльтекова енольные формы карбонильных соединений неустойчивы. Однако в ряде случаев енольные формы могут быть достаточно стабильными. Например, енольный таутомер стабилизирован за счет образования сопряжённой системы ( (H):О—C(Ch4)=C(H) —C(:OC2H5)=O: ; см. 2-ю формулу енольной формы на рис., R — Ch4, R’ — C2H5) и внутримолекулярной водородной связи между протоном и соседним карбонильным кислородом. Положение равновесия и, соответственно, соотношение таутомеров зависит от растворителя и температуры. Так, в чистом ацетоуксусном эфире при комнатной температуре концентрация енольной формы составляет 7,5 % (кетонной — 92,5 %). Равновесие сдвигается в сторону енольной формы при уменьшении полярности растворителя, так, при 18 °C доля енольной формы в водном растворе составляет 0,4 %, в диэтиловом эфире — 27,1 %, в циклогексане — 46,4 %.
Кетонная форма ацетоуксусного эфира может быть выделена из равновесной смеси вымораживанием, енольная - вакуумной перегонкой в кварцевой посуде. Скорость установления кето-енольного равновесия зависит от температуры и материала сосуда, чистые таутомеры хранятся в кварцевой посуде при низких температурах (-80°C - охлаждение сухим льдом).
Содержание енольной формы определяется бромометрически: бром практически мгновенно присоединяется по двойной связи енола, что сопровождается исчезновением желто-оранжевой окраски молекулярного брома.
Реакциями енольной формы также обусловлено O-ацилирование ацетоуксусного эфира хлорангидридами карбоновых кислот в пиридине, при этом образуются сложные эфиры β-гидроксикротоновой кислоты:
Ch4(HO)C=CHCOOC2H5 + ROCl →{\displaystyle \to } Ch4(ROO)C=CHCOOC2H5 + HClПри взаимодействии с пентахлоридом фосфора гидроксил енольной формы ацетоуксусного эфира замещается на хлор с образованием этилового эфира β-хлоркротоновой кислоты:
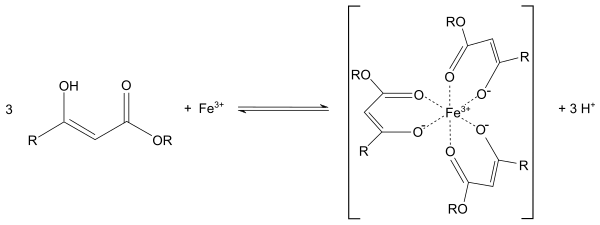
Ch4(HO)C=CHCOOC2H5 + PCl5→{\displaystyle \to } Ch4ClC=CHCOOC2H5 + POCl3 + HClС металлами ацетоуксусный эфир образует хелаты, в которых ацетилацетат-анион выступает в роли бидентантного лиганда, так, с солями трехвалентного железа ацетоуксусный эфир образует окрашенный в пурпурный цвет комплекс:
Под действием сильных оснований и щелочных металлов ацетоуксусный эфир депротонируется с образованием резонансно стабилизированного аниона:
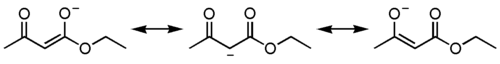
Образование натриевой соли ацетилацетата (натрийацетоуксусного эфира) под действием алкоголята натрия - в том числе и под действием этилата натрия, образующегося in situ при действии металлического натрия на ацетоуксусный эфир - широко используется в синтетической практике вследствие высокой нуклеофильности аниона.
Ацетилацетат натрия в реакциях с мягкими электрофилами выступает в роли C-нуклеофила. Так, он легко алкилируется галогеналкилами с образованием соответствующих алкилацетоуксусных эфиров, из которых, в свою очередь, могут быть получены и затем проалкилированы натриевые производные:
Ch4COCh3COOC2H5 + EtONa →{\displaystyle \to } Ch4COCH-COOC2H5 Na+ + EtOH Ch4COCH-COOC2H5 Na+ + RHal →{\displaystyle \to } Ch4COCHRCOOC2H5 + NaHalВ безводных условиях в присутствии бикарбоната натрия ацетоуксусный эфир самоконденсируется с образованием дегидроацетовой кислоты[1]:
2 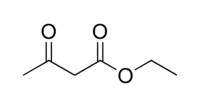 | → 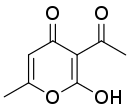 |
| Ацетоуксусный эфир | Дегидроацетовая кислота |
Под действием серной кислоты на ацетоуксусный эфир происходит самоконденсация двух молекул эфира с замыканием α-пиронового цикла, ведущая к образованию изодегидроацетовой кислоты[2].
Под действием водных кислот или разбавленных растворов щелочей ацетоуксусный эфир омыляется с образованием нестабильной ацетоуксусной кислоты, которая в мягких условиях декарбоксилируется с образованием ацетона:
Ch4COCh3COOC2H5 + h3O →{\displaystyle \to } Ch4COCh3COOH + C2H5OH Ch4COCh3COOH →{\displaystyle \to } Ch4COCh4 + CO2 + h3OАналогичным образом ведут себя и моно- и дизамещенные ацетоуксусные эфиры, полученные алкилированием натрийацетоуксусного эфира (кетонное расщепление), эта реакция используется для синтеза замещенных метилкетонов.
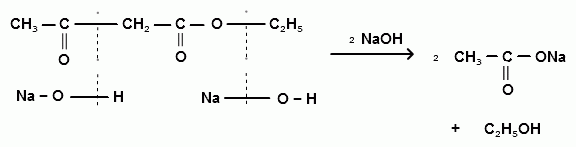
Иначе протекает взаимодействие ацетоуксусного эфира с концентрированными растворами щелочей: в этом случае протекает отщепление ацетильной группы с образованием двух молекул уксусной кислоты (кислотное расщепление), эта реакция идет и с замещенными ацетоуксусными эфирами и используется для синтеза гомологов уксусной кислоты через алкилпроизводные ацетоуксусного эфира:
Ch4COCHRCOOC2H5 + OH- + h3O →{\displaystyle \to } Ch4COO- + RCh3COOH + C2H5OHАцетоуксусный эфир широко применяется в органическом синтезе.
Алкилирование натрийацетоуксусного эфира 2 с последующим кетонным либо кислотным расщеплением моно- и дизамещенных ацетоуксусныых эфиров 3 используется как препаративный метод синтеза метилкетонов 4 и замещенных уксусных кислот 5:
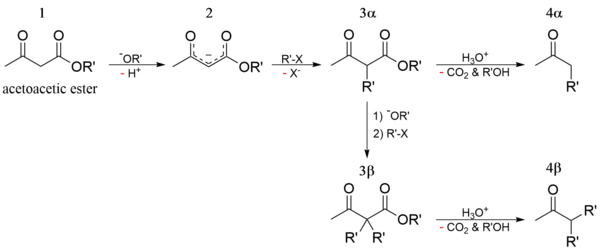
Будучи 1,3-дифункциональным реагентом, он применяется для синтеза гетероциклических соединений. В промышленности применяется в производстве фармацевтических препаратов (пирамидона, акрихина, витамина B1), ряда органических веществ.
В фотографии использовался как жёлтая диффундирующая цветообразующая компонента, образующая краситель в процессе цветного фотографического проявления[4].
www-wikipediya.ru
| Ацетоуксусный эфир | |
 | |
 | |
| Этил-3-оксобутаноат | |
| Этилацетоуксусный эфир,этиловый эфир ацетоуксусной кислоты,этилацетоацетат | |
| Ch4COCh3COOС2Н5 | |
| C6h20O3 | |
| бесцветная жидкость с фруктовым запахом | |
| 130,1418 ± 0,0064 г/моль | |
| 1,0284 г/см³ | |
| -45 °C | |
| 180,8 °C | |
| 84 °C | |
| 304 °C | |
| 9,5 % | |
| 100 Па при 20 °С | |
| 10,68 (в воде), 14,2 (в ДМСО) | |
| 2,86 г/100 мл | |
| 1,4198 | |
| 141-97-9 | |
| 8868 | |
| 205-516-1 | |
| AK5250000 | |
| 4893 | |
| 13865426 | |
| 3895 мг/кг (крысы, перорально) | |
| Слаботоксичен, высокотоксичен при действии на кожу, ирритант  | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
ruwikiorg.ru
Ацетоуксусный эфир - это... Что такое Ацетоуксусный эфир?
Ацетоуксусный эфир(этиловый эфир ацетоуксусной кислоты, этилацетоацетат) - бесцветная подвижная жидкость со своеобразным нерезким запахом.
Растворяется в воде (14,3 % при 16,5 °C), смешивается с этанолом и диэтиловым эфиром.Свойства
Для ацетоуксусного эфира, как и для других 1,3-дикарбонильных соединений характерна кето-енольная таутомерия:
 ,
, Енольный таутомер стабилизирован за счет образования внутримолекулярной водородной связи между протоном и соседним карбонильным кислородом. Положение равновесия и, соответственно, соотношение таутомеров зависит от растворителя и температуры. Так, в чистом ацетоуксусном эфире при комнатной температуре концентрация енольной формы составляет 7,5 %. Равновесие сдвигается в сторону енольной формы при уменьшении полярности растворителя, так, при 18 °C доля енольной формы в водном растворе составляет 0,4 %, в диэтиловом эфире — 27,1 %, в циклогексане — 46,4 %.
Кетонная форма ацетоуксусного эфира может быть выделена из равновесной смеси вымораживанием, енольная - вакуумной перегонкой в кварцевой посуде. Скорость установления кето-енольного равновесия зависит от температуры и материала сосуда, чистые таутомеры хранятся в кварцевой посуде при низких температурах (-80°C - охлаждение сухим льдом).
Содержание енольной формы определяется бромометрически: бром практически мгновенно присоединяется по двойной связи енола, что сопровождается исчезновением желто-оранжевой окраски молекулярного брома.
Реакциями енольной формы также обусловлено O-ацилирование ацетоуксусного эфира хлорангидридами карбоновых кислот в пиридине, при этом образуются сложные эфиры β-гидроксикротоновой кислоты:
Ch4(HO)C=CHCOOC2H5 + ROCl Ch4(ROO)C=CHCOOC2H5 + HCl
Ch4(ROO)C=CHCOOC2H5 + HCl При взаимодействии с пентахлоридом фосфора гидроксил енольной формы ацетоуксусного эфира замещается на хлор с образованием этилового эфира β-хлоркротоновой кислоты:
Ch4(HO)C=CHCOOC2H5 + PCl5 Ch4ClC=CHCOOC2H5 + POCl3 + HCl
Ch4ClC=CHCOOC2H5 + POCl3 + HCl С металлами ацетоуксусный эфир образует хелаты, в которых ацетилацетат-анион выступает в роли бидентантного лиганда, так, с солями трехвалентного железа ацетоуксусный эфир образует окрашеный в пурпурный цвет комплекс:
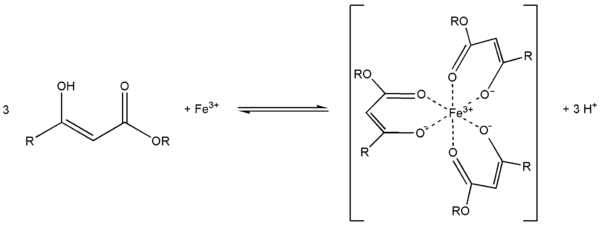
Под действием сильных оснований и щелочных металлов ацетоуксусный эфир депротонируется с образованием резонансно стабилизированный аниона:

Образование натриевой соли ацетилацетата (натрийацетоуксусного эфира) под действием алкоголята натрия - в том числе и под действием этилата натрия, образующегося in situ при действии металлического натрия на ацетоуксусный эфир - широко используется в синтетической практике вследствие высокой нуклеофильности аниона.
Ацетилацетат натрия в реакциях с мягкими электрофилами выступает в роли C-нуклеофила. Так, он легко алкилируется галогеналкилами с образованием соответствующих алкилацетоуксусных эфиров, из которых, в свою очередь, могут быть получены и затем проалкилированы натриевые производные:
Ch4COCh3COOC2H5 + EtONa Ch4COCH-COOC2H5 Na+ + EtOH Ch4COCH-COOC2H5 Na+ + RHal
Ch4COCH-COOC2H5 Na+ + EtOH Ch4COCH-COOC2H5 Na+ + RHal  Ch4COCHRCOOC2H5 + NaHal
Ch4COCHRCOOC2H5 + NaHal Под действием кислот или разбавленных растворов щелочей ацетоуксусный эфир омыляется с образованием нестабильной ацетоуксуслой кислоты, которая м мягких условиях декарбоксилируется с образованием ацетона:
Ch4COCh3COOC2H5 + h3O Ch4COCh3COOH + C2H5OH Ch4COCh3COOH
Ch4COCh3COOH + C2H5OH Ch4COCh3COOH  Ch4COCh4 + CO2 + h3O
Ch4COCh4 + CO2 + h3O Аналогичным образом ведут себя и моно- и дизамещенные ацетоуксусные эфиры, полученные алкилированием натрийацетоуксусного эфира (кетонное расщепление), эта реакция используется для синтеза замещенных метилкетонов.
Иначе протекает взаимодействие ацетоуксусного эфира с концентрированными растворами щелочей: в этом случае протекает отщепление ацетильной группы с образованием двух молекул уксусной кислоты (кислотное расщепление), эта реакция идет и с замещенными ацетоуксусными эфирами и используется для синтеза гомологов уксусной кислоты через алкилпроизводные ацетоуксусного эфира:
Ch4COCHRCOOC2H5 + OH- + h3O Ch4COO- + RCh3COOH + C2H5OH
Ch4COO- + RCh3COOH + C2H5OH Синтез
Классическим методом синтеза ацетоуксусного эфира является сложноэфирная конденсации этилацетата в присутствии этанола под действием металлического натрия, катализатором конденсации является образующийся in situ этилат натрия. Образующийся натрийацетоуксусный эфир действием разбавленной минеральной кислоты переводят в ацетоуксусный эфир[1]:

Ацетоуксусный эфир также может быть синтезирован ацилированием этанола дикетеном, этот метод является промышленным методом синтеза:
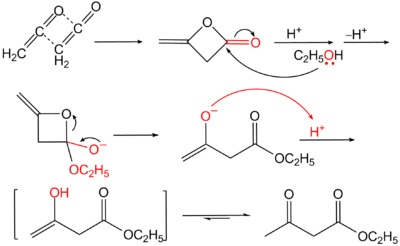
Применение
Ацетоуксусный эфир широко применяется в органическом синтезе. Будучи 1,3-дифункциональным реагентом, он применяется для синтеза гетероциклических соединений. В промышленности применяется в производстве фармацевтических препаратов (пирамидона, акрихина, витамина B1), а также красителей для цветной фотографии, ряда органических веществ.
Биологическое действие
Обладает кожнораздражающим действием. Всасывается через кожу. ПДК 1 мг/м³
Примечания
- ↑ С.В.Пономарев, А.С.Золотарева, Л.Г.Сагинова, В.И.Теренин "Практикум по органической химии"
Ссылки
3dic.academic.ru

 Ch4(ROO)C=CHCOOC2H5 + HCl
Ch4(ROO)C=CHCOOC2H5 + HCl