СЛОЖНЫЕ ЭФИРЫ. Воска это сложные эфиры
4.6.2. Воски
Воски (воска) – это сложные эфиры жирных кислот и одноатомных высокомолекулярных (высших) спиртов. Это жироподобные вещества растительного и животного происхождения. Только вместо глицерина в состав восков входят высшие спирты.
По внешнему виду, физическим свойствам и источникам происхождения жиры и воска имеют много общего, однако воски очень устойчивы к воздействию химических реагентов и не изменяются при длительном хранении.
Существует простой способ, помогающий их различить. При сильном нагревании жир издает резкий неприятный запах акролеина, а воск при этом имеет приятный запах.
Воски бывают растительные, животные, ископаемые и синтетические.
Растительные воски
Карнаубский воск покрывает листья бразильской пальмы Copernicia cerifera. Представляет собой сложный эфир триаконтанола СН3(СН2)29ОН и тетракозановой кислоты СН3(СН2)22СООН. Для получения карнаубского воска листья пальмы высушивают, из них выколачивают порошок, который вываривают в воде и выливают в формы. 2000 листьев дают около 16 кг воска. Используют карнаубский воск для изготовления мастик, кремов для обуви.
Пальмовый воск находится в углублениях кольчатого ствола восковой пальмы, откуда его соскабливают. Одно дерево дает 12 кг воска.
Японский воск добывают из лакового дерева, произрастающего в Японии и Китае.
Растительными восками покрыты фрукты, овощи и ягоды (например, черника).
Животные воски
Пчелиный воск – наиболее известный из этого вида восков – представляет собой пальмитиномирициловый эфир.
С15Н31– С = О
О – С31Н63
Шерстяной (шерстный) воск – ланолин – обильно покрывает шерсть животных.
Спермацет содержится в костных черепных углублениях некоторых видов китов, особенно кашалотов. На 90 % состоит из пальмитиноцетилового эфира:
С15Н31– С = О
О – С16Н33
Китайский воск вырабатывается червецом, который обитает на китайском ясене и образует на нем восковой покров. Содержит сложный эфир гексакозановой кислоты СН3(СН2)24СООН и гексадеканового спирта СН3(СН2)15ОН.
К воскам относятся кожное сало и ушная сера.
Воск бактерий покрывает поверхность кислотоупорных бактерий, например, туберкулезных, обеспечивая их устойчивость к внешним воздействиям. Содержит сложные эфиры миколевой кислоты С88Н172О2 и октадеканола С20Н42О.
Ископаемые воски
Торфяной воск получают экстракцией бензином при 800С верхового битуминозного торфа.
Буроугольный воск (монтан-воск) извлекают бензином из бурого битуминозного угля.
Горный воск – озокерит – минерал из группы нефтяных битумов.
Синтетические воски получают на основе нефтяных и смоляных парафинов и их производных.
Воски применяют более чем в 200 отраслях народного хозяйства. Они входят в состав политур, защитных композиций для металлов, тканей, бумаги, кож, дерева; как изолирующий материал; компоненты мазей в косметике и медицине.
Тема 5. Органические соединения, содержащие серу и азот
studfiles.net
Натуральные воски.
Косметическая химия
Натуральные воски.
Воск, название, применяемое для обозначения группы жироподобных твердых веществ природного или синтетического происхождения.
В зависимости от происхождения они делятся на:
1. Животные (пчелиный воск, ланолин, спермацет),
2. Растительные (карнаубский, канделильский, японский, воск розы, лаванды, жожоба и др).
Растительные и животные воски состоят, главным образом, из сложных эфиров жирных кислот и одноатомных спиртов, а также свободных жирных спиртов, жирных кислот и углеводородов.
Эти воски называют натуральными.
Кроме них существуют:
3. Воски минерального происхождения. Это ископаемый или горный воск (озокерит), церезин (очищенный озокерит) и парафин (продукт перегонки нефти).
Минеральные воски — это смесь предельных углеводородов.
4. Синтетические воски.
Свойства и применение восков в косметике
Воски обладают химической устойчивостью, не подвержены окислению, водостойки, имеют достаточную твердость и высокую температуру плавления.
В косметике воски, чаще всего, выполняют роль структурообразующих компонентов, влияющих на плотность и термостойкость изделий. Отдельные виды восков содержат биологически активные вещества, что усиливает их полезное воздействие на кожу.
1. Воски животного происхождения
Пчелиный воск
Пчелиный воск - продукт жизнедеятельности пчёл, из которого они строят соты.
По химическому составу пчелиный воск - сложное органическое соединение, состоящее из более чем 50 компонентов. Основу пчелиного воска составляют сложные эфиры жирных кислот и высших одноатомных спиртов.
Пчелиный воск представляет собой нерастворимое в воде твёрдое вещество от белого до жёлто-бурого цвета с характерным медовым запахом.
Применение
Пчелиный воск обладает сильными антимикробными свойствами. По этой причине он нашёл своё применение в медицине.
Его используют для лечения простудных заболеваний, ангины, кашля.
Хорошо известно его смягчающее, ранозаживляющее воздействие на кожу.
Он применяется в составе лекарственных средств для лечения воспалительных заболеваний, кожи и слизистых оболочек, при лечении ран, ожогов, язв.
В косметике пчелиный воск используют в качестве загустителя для кремов, мазей, как основу губных помад.
Пчелиный воск используют в составе масок для лица. Такие маски очищают кожу, придают ей мягкость эластичность, препятствуют появлению морщин.
Маски на основе пчелиного воска используют для лечения юношеских угрей, удаления чёрных точек на кожи и пр.
Ланолин
Ланолин (от лат. lana — шерсть и лат. oleum — масло) — шерстяной воск, получаемый при вываривании шерсти овец.
Внешне Ланолин это густая, вязкая масса жёлтого или жёлто-бурого цвета.
Состав
Химический состав ланолина сложен и на сегодня не достаточно изучен. В основном он представляет собой смесь сложных эфиров высокомолекулярных спиртов с высшими жирными кислотами (миристиновой, пальмитиновой, церотиновой и д.р.) и свободных высокомолекулярных спиртов.
Свойства
По свойствам ланолин близок к кожному салу человека.
В химическом отношении достаточно инертен, нейтрален, устойчив при хранении.
Важнейшим качеством ланолина является его способность эмульгировать с водой, образуя эмульсию типа вода/масло. При добавлении небольшого количества ланолина к жирам и углеводородам резко увеличивают их способность смешиваться с водой и водными растворами.
Применение
В косметике Ланолин применяется в качестве основы для кремов.
Он хорошо всасывается в кожу, обладает смягчающим действием, способствует хорошему увлажнению и питанию кожи.
Ланолин делает кожу мягкой и эластичной. Его применение способствует регенерации клеток кожи.
Использование Ланолина в чистом виде не рекомендуется, поскольку он может закупоривать поры кожи и препятствовать её дыханию.
В отдельных случаях Ланолин может вызывать аллергию, покраснения, сыпь.
Спермацет
Спермацет – воскоподобное вещество животного происхождения. Его получают при помощи охлаждения животного жира кашалота и некоторых других китообразных.
Раньше спермацет ошибочно принимали за сперму кашалота (отсюда название).
Жир, используемый для получения Спермацета, находится, главным образом, в голове животного, в, так называемых, спермацетовых мешках. Спермацет содержится также в сале кашалота.
В связи с тем, что добыча кашалотов сегодня сведена к минимуму или, вообще, запрещена, спермацет таким способом больше не производится. Он обычно заменяется искусственно синтезированным главным компонентом спермацета — цетилпальмитатом.
Состав
Основной компонент спермацета – цетилпальмитат. Это сложный эфир цетилового спирта и пальмитиновой кислоты. Другой эфир пальмитиновой кислоты – мирицилпальмитат – содежится в пчелином воске:
Кроме цетилпальмитата, в спермацете присутствуют свободные спирты — цетиловый, октадециловый и эйкозиловый.
Применение
В медицине спермацет применяется в качестве заживляющего, противоожогового средства.
Употребляется внутрь против кашля, легочных заболеваний, поносов.
В косметике спермацет применяется в качестве основы для кремов и мазей.
2. Воски растительного происхождения
Многие растения обладают способностью продуцировать восковидные вещества. Воск создаёт защитную плёнку и покрывает ей различные части растений: стебли, листья, цветы, плоды.
Восковая плёнка – это один из видов защиты растений от неблагоприятных факторов внешней среды, например, болезнетворных бактерий и вирусов.
Состав
Растительный воски, как и воски животные, состоят, прежде всего, из эфиров одноатомных жирных спиртов и жирных кислот. Так же в их состав входят свободные жирные спирты и жирные кислоты.
Из жирных кислот больше всего растительные воски содержит пальмитиновой кислоты. В меньшем количестве найдены стеариновая, олеиновая и миристиновая.
Почти всегда растительный воск содержит небольшие количества красящих, пахучих и смолистых веществ.
Растительные воски в природе
Обыкновенно воск покрывает тончайшим слоем наружную ткань растения — эпидерму. Мы можем наблюдать этот налёт на зрелых плодах сливы.
В случаях тех растений, отложение воска на которых достигает значительной величины, их используют для добывания этого продукта.
Способ добывания при поверхностном отложении очень прост: корки воска снимают механическим путем, сплавляют и либо прямо пускают в продажу, или предварительно очищают. При отложении воска внутри клеток его добывают, подобно маслу, дроблением и прессованием растения.
Примеры растительных восков
В продаже известны главным образом следующие сорта:
- Карнаубский воск, добываемый с карнаубской пальмы Copernicia cerifera в Бразилии. Состоит на 80% из сложного эфира мирицилового спирта и церотовой кислоты. Содержит также лактоны, жирные кислоты, смолистые вещества. Используется в губной помаде, туши для ресниц, румянах, жидкой пудре, шариковых дезодорантах как структурообразующий компонент, повышающий их твердость и температуру плавления. “Запирает” влагу в коже, придает вязкую приятную консистенцию косметическим средствам.
- Пальмовый воск получается с Ceroxylon andicola, растущего в Кордильерах Новой Гранады. На стволах и листьях этого растения восковой налет образует корки до 6 мм толщиной; с каждого дерева получают около 10 кг воска. Пальмовый воск имеет желтовато-белый цвет. Температура его плавления 72°.
- Японский воск добывается преимущественно из семян двух видов Rhus — R. vernicifera и R. succedanea, растущих в Японии, Китае и культивируемых в Ост-Индии. Полутвердый продукт с жирным запахом и вкусом, содержащий триглицериды пальмитиновой, линолевой и линоленовой кислот. Этот воск следует отнести скорее к растительным маслам. В косметических препаратах может заменять пчелиный воск. Используется для производства помад и косметических карандашей.
- Воск жожоба (хохобы) (Wax Jojoba) - восковая фракция масла жожоба, вырабатываемого из вечнозеленого кустарникового растения Simmondsia chinensis. Полутвердый продукт, содержащий эйкозановую, докозановую, олеиновую кислоты, природные антиоксиданты (витамин F). В косметике применяется, как правило, гидрогенизированный воск жожоба, обладающий хорошими смягчающими и гелеобразующими свойствами, имеющий достаточно высокую температуру плавления. Широко используется в современных косметических препаратах: увлажняющих и питательных кремах, губных помадах и других декоративных изделиях. В шампуни, бальзамы, лаки для волос вводится в качестве специальной добавки, придающей волосам мягкость и блеск. Может служить заменой спермацету.
- Воск розы - получают из отходов производства розового эфирного масла. Твердый продукт темно-желтого цвета с приятным запахом розы. Обладает структурообразующими свойствами, близкими к пчелиному воску. Проявляет легкое бактерицидное и противовоспалительное действие. Используется в составе губных помад и других декоративных изделий.
xn----7sbb4aandjwsmn3a8g6b.xn--p1ai
Воски - Гидрофобные мазевые основы - Аптечная технология приготовления лекарственных форм - Справочник фармацевта - Medkurs.ru
Воски — это сложные эфиры жирных кислот и высших одноатомных спиртов. В качестве мазевых основ наибольшее распространение получили ланолин, спермацет и пчелиный воск.
Ланолин (Lanolinum). Представляет собой сложную природную смесь эфиров, спиртов и свободных жирных кислот (более 70 разновидностей). Очищенный ланолин буро-желтого цвета, густой, вязкой, мазеобразной консистенции со своеобразным слабым запахом. Температура плавления 36—42 °С. В воде не растворяется, однако при растирании смешивается с ней, при этом не теряя своей мазеобразной консистенции (поглощает до 150 % воды).
С помощью безводного ланолина (Lanolinum anhydricum) в мази можно вводить большое количество водных жидкостей. Ланолин труднорастворим в спирте, но может воспринять (в виде грубой дисперсии) до 40 частей (на 100 частей безводного ланолина) 70%-ного спирта. Глицерина безводный ланолин воспринимает до 120—140 частей.
Ланолин легкорастворим в эфире и хлороформе. Это вещество прекрасно всасывается кожей за счет сходства по составу с жироподобными веществами, покрывающим кожу человека; не раздражает кожи и слизистых оболочек. Достаточно стоек к химическим воздействиям, несмотря на возможность окислительных процессов и связанное с этим изменение цвета его поверхности. Обладает высокой вязкостью и клейкостью, поэтому практически всегда применяется в смеси с другими основами. Если в рецепте врачом прописан ланолин, то отпускают Lanolinum hydricum (ланолин водный), который получают при смешивании 7 частей безводного ланолина с 3 частями воды, которую добавляют небольшими порциями (содержание воды в водном ланолине составляет 32 %). При плавлении водного ланолина на водяной бане эмульсия разрушается.
Спермацет (Cetaceum, Spermacetum) — это сложный эфир спирта и высших жирных кислот (пальмитиновой, стеариновой и др.). Получают из спермацетового жира черепа кашалота. Представляет собой массу жирную на ощупь, твердую, белую, пластинчато-кристаллического строения, без запаха с температурой плавления 45—54 °С. Обладает эмульгирующими свойствами, сплавляется с жирами, углеводородами. При добавлении к мазевой основе спермацет придает ей большую плотность, приятную скользкость и способность впитывать водные жидкости, образуя грубые эмульсии. При натирании бумаги не оставляет жирных следов. Спермацет нерастворим в воде и холодном спирте; растворим в кипящем 95%-ном спирте, эфире и хлороформе. Стоек при хранении. Кислотное число не более 2,0. Применяется чаще всего в мазях для массажа, косметических препаратах для придания им скользкости и большей плотности.
Воск (Cera). Представляет собой смесь сложных эфиров высокомолекулярных спиртов с пальмитиновой кислотой. Температура плавления составляет 63—65 °С. За счет содержания небольшого количества свободных спиртов способен эмульгировать небольшое количество воды. Нерастворим в воде и спирте, частично растворим в кипящем спирте, эфире, хлороформе, жирных и эфирных маслах. Химически стоек. В чистом виде никогда не употребляется для изготовления мазей, применяется для уплотнения мазевых основ, повышает вязкость жиров и углеводородов, улучшает впитываемость водных жидкостей. Существует две разновидности воска — пчелиный желтый и белый (отбеленный) (Cera alba, Cera flava). Пчелиный воск представляет собой темно-желтую, белую или желтовато-белую зернистую в изломе массу, которая плавится при температуре 63—65 °С. Белый воск получают отбеливанием желтого на солнечном свете. В аптечном производстве предпочтительнее использовать желтый воск, так как белый более склонен к прогорканию. Основа, состоящая из сплава 30 % воска желтого и 70 % масла оливкового, является фармакопейной гидрофобной основой.
Далее по теме:
www.medkurs.ru
Омыляемые липиды
Простые и сложные липиды легко омыляются. При действии кислот и щелочей на них происходит расщепление сложноэфирной связи – омыление жира. При этом выделяются свободный спирт и свободные жирные кислоты или их соли.
Простые липиды
Простые липиды – соединения, состоящие только из жирных кислот и спиртов. Они делятся на две группы: 1) нейтральные ацилглицеролы и 2) воски.
Триацлглицеролы (жиры)
Нейтральные ацилглицеролы представляют собой сложные эфиры трехатомного спирта глицерина и высших жирных кислот. Простые ацилглицеролы не содержат ионных групп, являются нейтральными липидами, относятся к L-ряду.
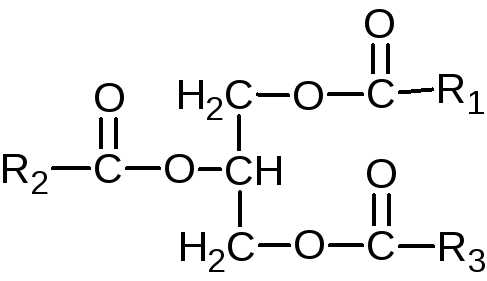
Если жирными кислотами этерифицированы все три гидроксильные группы глицерина, то такое соединение называют триацилглицеролом (триглицерид), если две – диацилглицеролом (диглицерид) и, наконец, если этерифицирована одна группа – моноацилглицеролы( моноглицерид).
Триацилглицеролы различаются природой и расположением трех остатков жирных кислот. В зависимости от типа остатков жирных кислот нейтральные жиры делятся на простые и смешанные. Если во всех трех положениях стоят остатки одной и той же жирной кислоты, то их относят к простым триацилглицеролам, название которых определяется названием соответствующей жирной кислоты (например, трипальмитин, тристеарин, триолеин и т.д.), если остатки разных жирных кислот, то их относят к смешанным триацилглицеролам (например, 1-олео-2-пальмито-3-стеарин).
Нейтральные ацилглицеролы служат главными составными частями природных жиров и масел, чаще всего это смешанные триацилглицеролы. По происхождению природные жиры делят на животные и растительные. В зависимости от жирно-кислотного состава жиры и масла по консистенции бывают жидкими и твердыми. Животные жиры (баранье, говяжье, свиное сало, молочный жир) обычно содержат значительное количество насыщенных жирных кислот (пальмитиновой, стеариновой и др.), благодаря чему при комнатной температуре они твердые.
Жиры, в состав которых входит много ненасыщенных кислот (олеиновая, линолевая, линоленовая и др.), при обычной температуре жидкие и называются маслами.
Жиры, как правило, содержатся в животных тканях, масла – в плодах и семенах растений. Особенно высоко содержание масел (20-60 %) в семенах подсолнечника, хлопчатника, сои, льна. Семена этих культур используются в пищевой промышленности для получения пищевых масел.
По способности высыхать на воздухе масла подразделяются: на высыхающие (льняное, конопляное), полувысыхающие (подсолнечное, кукурузное), невысыхающие (оливковое, касторовое). Это свойство масел определяется их жирно - кислотным составом.
Триацилглицеролы способны вступать во все химические реакции, свойственные сложным эфирам. Наибольшее значение имеет реакция омыления, она может происходить как при ферментативном гидролизе, так и при действии кислот и щелочей. Жидкие растительные масла превращают в твердые жиры при помощи гидрогенизации. Этот процесс широко используется для изготовления маргарина и кулинарного жира.
Жиры при сильном и продолжительном взбалтывании с водой образуют эмульсии – дисперсные системы с жидкой дисперсной фазой (жир) и жидкой дисперсионной средой (водой). Однако эти эмульсии нестойки и быстро разделяются на два слоя – жир и воду. Жиры плавают над водой, поскольку их плотность меньше плотности воды (от 0,87 до 0,97).
Для получения стойких эмульсий жира в воде необходимо присутствие третьего вещества – эмульгатора, легко адсорбирующегося на поверхности раздела двух фаз. Молекула эмульгатора состоит из двух частей: из углеводородной цепи (гидрофобный хвост) и какой-либо полярной или ионной группы (гидрофильная головка). К таким соединениям относятся мыла, белки, фосфолипиды, соли желчных кислот. При взбалтывании жира с водой в присутствии эмульгатора происходит дробление жира на капли, на которых появляется тончайшая пленка, состоящая из адсорбированных молекул эмульгатора, гидрофобный конец которых погружен в капельку жира, а гидрофильный – в водную фазу (см. рис. 3).
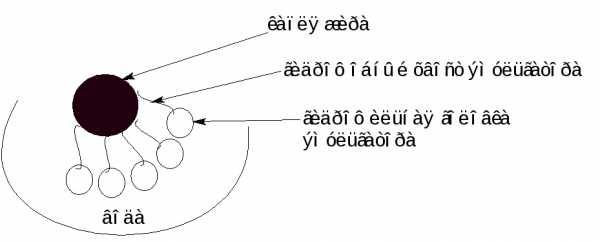
Рисунок 3 – Схема действия эмульгатора
Таким образом, эмульгатор формирует гидрофильную оболочку вокруг капель жира, образуя мелкодисперсную смесь с водой или эмульсию, которая приобретает свойство стабильности.
Эмульгирование имеет большое физиологическое значение при всасывании и усвоении организмом жиров, а также при образовании биологических мембран. Эмульсии широко используются в пищевой промышленности при приготовлении шоколада, майонеза, маргарина, мыловарении, при изготовлении косметических средств, в производстве красителей.
Воски
Это сложные эфиры высших жирных кислот и высших одноатомных спиртов жирного (реже ароматического) ряда.
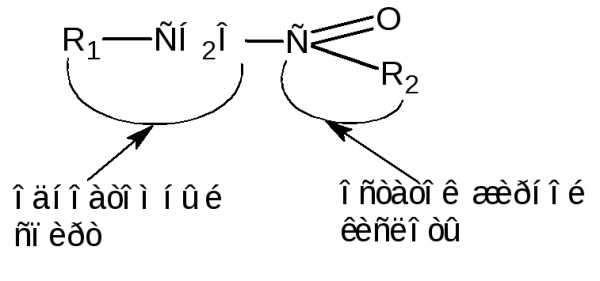
Воски являются твердыми соединениями с ярко выраженными гидрофобными свойствами. Природные воски содержат также некоторое количество свободных жирных кислот и высокомолекулярных спиртов. В состав восков входят как обычные, содержащиеся в жирах, – пальмитиновая, стеариновая, олеиновая и др., так и жирные кислоты, характерные для восков, имеющие гораздо большие молекулярные массы, – карноубовая С24Н48О2, церотиновая С27Н54О2, монтановая С29Н58О2 и др.
Среди высокомолекулярных спиртов, входящих в состав восков, можно отметить цетиловый – СН3–(СН2)14–СН2ОН, цериловый – СН3–(СН2)24–СН2ОН, мирициловый СН3–(СН2)28–СН2ОН.
Воски встречаются как в животных, так и в растительных организмах и выполняют, главным образом, защитную функцию.
В растениях они покрывают тонким слоем листья, стебли и плоды, тем самым, предохраняя их от смачивания водой, высыхания, механических повреждений и поражения микроорганизмами. Нарушение этого налета приводит к быстрой порче плодов при их хранении.
Например, значительное количество воска выделяется на поверхности листьев пальмы, произрастающей в Южной Америке. Этот воск, называемый карноубским, является, в основном, церотиново-мирициловым эфиром:
,
имеет желтый или зеленоватый цвет, очень тверд, плавится при температуре 83-900С, идет на выделку свечей.
Среди животных восков наибольшее значение имеет пчелиный воск, под его покровом хранится мед и развиваются личинки пчелы. В пчелином воске преобладает пальмитиново-мирициловый эфир:
,
а также высокое содержание высших жирных кислот и различных углеводородов, плавится пчелиный воск при температуре 62-700С.
Другими представителями воска животных является ланолин и спермацет. Ланолин предохраняет волосы и кожу от высыхания, очень много его содержится в овечьей шерсти.
Спермацет – воск, добывающий из спермацетового масла черепных полостей кашалота, состоит, в основном, (на 90%) из пальмитиново-цетилового эфира:
твердое вещество, его температура плавления 41-490С.
Различные воска широко применяют для изготовления свечей, помад, мыла, разных пластырей.
studfiles.net
Глава II. Липиды
Глава II. ЛИПИДЫ
§ 4. КЛАССИФИКАЦИЯ И ФУНКЦИИ ЛИПИДОВ
Липиды представляют собой неоднородную группу химических соединений, нерастворимых в воде, но хорошо растворимых в неполярных органических растворителях: хлороформе, эфире, ацетоне, бензоле и др., т.е. общим их свойством является гидрофобность (гидро – вода, фобия – боязнь). Из-за большого разнообразия липидов дать более точное определение им невозможно. Липиды в большинстве случаев являются сложными эфирами жирных кислот и какого-либо спирта. Выделяют следующие классы липидов: триацилглицерины, или жиры, фосфолипиды, гликолипиды, стероиды, воска, терпены. Различают две категории липидов – омыляемые и неомыляемые. К омыляемым относятся вещества, содержащие сложноэфирную связь (воска, триацилглицерины, фосфолипиды и др.). К неомыляемым относятся стероиды, терпены.
Триацилглицерины, или жиры
Триацилглицерины являются сложными эфирами трехатомного спирта глицерина
и жирных (высших карбоновых) кислот. Общая формула жирных кислот имеет вид: R-COOH, где R – углеводородный радикал. Природные жирные кислоты содержат от 4 до 24 атомов углерода. В качестве примера приведем формулу одной из наиболее распространенной в жирах стеариновой кислоты:
Ch4-Ch3-Ch3-Ch3-Ch3-Ch3-Ch3-Ch3-Ch3-Ch3-Ch3-Ch3-Ch3-Ch3-Ch3-Ch3-Ch3-COOH
В общем виде молекулу триацилгицерина можно записать так:
Если в состав триациоглицерина входят остатки различных кислот (R1 R2 R3), то центральный атом углерода в остатке глицерина становится хиральным.
Триацилглицерины неполярны и вследствие этого практически нерастворимы в воде. Основная функция триацилглицеринов – запасание энергии. При окислении1 гжира выделяется 39 кДж энергии. Триацилглицерины накапливаются в жировой ткани, которая, кроме депонирования жира, выполняет термоизолирующую функцию и защищает органы от механических повреждений. Более подробную информацию о жирах и жирных кислотах вы найдете в следующем параграфе.
Интересно знать! Жир, которым заполнен горб верблюда, служит, в первую очередь, не источником энергии, а источником воды, образующейся при его окислении.
Фосфолипиды
Фосфолипиды содержат гидрофобную и гидрофильную области и поэтому обладают амфифильнымы свойствами, т.е. они способны растворяться в неполярных растворителях и образовывать стойкие эмульсии с водой.
Фосфолипиды в зависимости от наличия в их составе спиртов глицерина и сфингозина делятся на глицерофосфолипиды и сфингофосфолипиды.
Глицерофосфолипиды
В основе строения молекулы глицерофосфолипидов лежит фосфатидная кислота, образованная глицерином, двумя жирными и фосфорной кислотами:
В молекулах глицерофосфолипидов к фосфатидной кислоте сложноэфирной связью присоединена НО-содержащая полярная молекула. Формулу глицерофосфолипидов можно представить так:
где Х – остаток НО-содержащей полярной молекулы (полярная группировка). Названия фосфолипидов образуются в зависимости от наличия в их составе той или иной полярной группировки. Глицерофосфолипиды, содержащие в качестве полярной группировки остаток этаноламина,
HO-Ch3-Ch3-Nh3
носят название фосфатидилэтаноламинов, остаток холина
– фосфатидилхолинов, серина
– фосфатидилсеринов.
Формула фосфатидилэтаноламина выглядит так:
Глицерофосфолипиды отличаются друг от друга не только полярными группами, но и остатками жирных кислот. В их состав входят как насыщенные (состоящие обычно из 16 – 18 атомов углерода), так и ненасыщенные (содержащие чаще 16 – 18 атомов углерода и 1 – 4 двойные связи) жирные кислоты.
Сфингофосфолипиды
Сфингофосфолипиды по составу сходны с глицерофосфолипидами, но вместо глицерина содержат аминоспирт сфингозин:
или дигидросфингазин:
Наиболее распространенными сфингофосфолипидами являются сфингомиелины. Они образованы сфингозином, холином, жирной кислотой и фосфорной кислотой:
Молекулы как глицерофосфолипидов, так и сфингофосфолипидов состоят из полярной головы (образована фосфорной кислотой и полярной группировкой) и двух углеводородных неполярных хвостов (рис.1). У глицерофосфолипидов оба неполярных хвоста являются радикалами жирных кислот, у сфингофосфолипидов – один хвост является радикалом жирной кислоты, другой – углеводородной цепочкой спирта сфингазина.
Рис. 1. Схематическое изображение молекулы фосфолипида.
При встряхивании в воде фосфолипиды спонтанно формируют мицеллы, в которых неполярные хвосты собираются внутри частицы, а полярные головы располагаются на ее поверхности, взаимодействуя с молекулами воды (рис. 2а). Фосфолипиды способны образовывать также бислои (рис. 2б) и липосомы – замкнутые пузырьки, окруженные непрерывным бислоем (рис. 2в).
Рис. 2. Структуры, образуемые фосфолипидами.
Способность фосфолипидов, образовывать бислой, лежит в основе формирования клеточных мембран.
Гликолипиды
Гликолипиды содержат в своем составе углеводный компонент. К ним относятся гликосфинголипиды, содержащие, кроме углевода спирт, сфингозин и остаток жирной кислоты:
Они так же, как и фосфолипиды, состоят из полярной головы и двух неполярных хвостов. Гликолипиды располагаются на внешнем слое мембраны, являются составной частью рецепторов, обеспечивают взаимодействие клеток. Их особенно много в нервной ткани.
Стероиды
Стероиды являются производными циклопентанпергидрофенантрена (рис. 3). Один из важнейших представителей стероидов – холестерин. В организме он встречается как в свободном состоянии, так и в связанном, образуя сложные эфиры с жирными кислотами (рис. 3). В свободном виде холестерин входит в состав мембран и липопротеинов крови. Сложные эфиры холестерина являются его запасной формой. Холестерин является предшественником всех остальных стероидов: половых гормонов (тестостерон, эстрадиол и др.), гормонов коры надпочечников (кортикостерон и др.), желчных кислот (дезоксихолевая и др.), витамина D (рис. 3).
Интересно знать! В организме взрослого человека содержится около 140 г холестерина, больше всего его находится в нервной ткани и надпочечниках. Ежедневно в организм человека поступает 0,3 – 0,5 г холестерина, а синтезируется – до 1 г.
Воска
Воска – это сложные эфиры, образованные длинноцепочечными жирными кислотами (число атомов углерода 14 – 36) и длинноцепочечными одноатомными спиртами (число атомов углерода 16 – 22). В качестве примера рассмотрим формулу воска, образованного олеиновым спиртом и олеиновой кислотой:
Воска выполняют главным образом защитную функцию, находясь на поверхности листьев, стеблей, плодов, семян они защищают ткани от высыхания и проникновения микробов. Они покрывают шерсть и перья животных и птиц, предохраняя их от намокания. Пчелиный воск служит строительным материалом для пчел при создании сот. У планктона воск служит основной формой запасания энергии.
Терпены
В основе терпеновых соединений лежат изопреновые остатки:
К терпенам относятся эфирные масла, смоляные кислоты, каучук, каротины, витамин А, сквален. В качестве примера приведем формулу сквалена:
Сквален является основным компонентом секрета сальных желез.
ebooks.grsu.by
Ответы@Mail.Ru: Какие температуры плавления воска?
Здесь <a rel="nofollow" href="http://www.krugosvet.ru/articles/41/1004162/1004162a1.htm" target="_blank">www.krugosvet.ru/articles/41/1004162/1004162a1.htm</a> найдете всю информацию о всех восках и их температуре плавления в том числе, смотрите что там есть - "ВОСК. название, применяемое для обозначения группы жироподобных твердых веществ природного или синтетического происхождения; по химической природе это, как правило, сложные эфиры высших одноосновных жирных кислот и высших одноатомных жирных спиртов; ископаемые воски – насыщенные углеводороды...." и далее : " Разновидности и использование. Минеральные воски. Парафины. Озокерит. Церезин. Горный воск. Растительные воски. Карнаубский (бразильский) воск. Канделила (травяной воск) . Японский воск, воск лавра, мирта и восковницы. Воски насекомых. Пчелиный воск. Китайский воск. Воски животных. Спермацет (цетин). Шерстяной воск (ланолин). Литература. " Из этого же источника - "...Товарный очищенный парафин подразделяется на три сорта по температуре плавления (48–49° C, 50–51° C, 54–56° C). Очищенный озокерит плавится при температуре (от 65° C до 80° C), Товарный церезин плавится при температурах от 54° C до 77° C. Карнаубский воск плавится при 85–90° C...." Удачи!
воск плавится при температуре около от 50 до 100° C смотря какой!!!
Хм, воск и парафин - разные вещи. Воски есть продукты секреции особых желез пчел и по химическому составу представляют собой сложные эфиры высших разветвленных спиртов (в основном миристилового и цетилового) с высшими жирными кислотами. Тпл лежит в области 60-120 гр Ц в зависимости от состава - разные пчелы делают разный воск в разное время года. Также восками называют продукты растительного происхождения, как правило гидрофобные, покрывающие листья, стебли итп в целях защиты от насекомых, грибов, тлей или уменьшения испарения воды. По химсоставу такие воски аналогичны пчелиным. Парафины. Это общее название высших насыщенных углеводородов, с восками ничего общего не имеющих, к тому же технические парафины есть как правило сложная смесь. Т пл напрямую зависит от строения молекулы, точнее просто от длины цепи и варьируется от 10-20 гр. Ц (вазелин к примеру) до 200 (с разложением) - это уже полиэтилены высокого давления. Просто так Т пл и тех и других не рассчитать. Одна и та же марка может плавиться в совершенно различных диапазонах температур - они медленно кристаллизуются и собственно Т пл одной и той же смеси зависит от степени кристалличности.
Озокерит (перенаправление с Горный воск) как гипс. Удельный вес — от 0.85 до 0.97, чаще от 0.91 до 0.95, температура плавления — от 58 до 100 °C. Озокерит растворяется в эфире, нефти, бензоле 8 КБ (492 слова) - 14:13, 15 января 2016 Парафин (категория Воски) строения состава от С18Н38 (октадекан) до С35Н72 (пентатриоконтан). Температура плавления от 45°С до 65°С; плотность 0,880–0,915 г/см³ (15 °C). Получают главным 16 КБ (1002 слова) - 23:59, 28 апреля 2016 Карнаубский воск углеводороды (1—3 %). Карнаубский воск — самый твёрдый и тугоплавкий (температура плавления +83…+91 °С) из восков растительного и животного происхождения 5 КБ (322 слова) - 10:58, 25 февраля 2016 Свеча Пальмовый воск — производится из плодов пальмового дерева. Он достаточно твёрд, а потому температура его плавления несколько выше, чем у пчелиного воска, и составляет 36 КБ (2372 слова) - 07:23, 2 мая 2016 Гексоген объём газообразных продуктов взрыва — 908 л/кг. Температура вспышки — 230 °C, температура плавления — 204,1°C. Теплота взрыва — 1370 ккал/кг, теплота 11 КБ (609 слов) - 11:16, 18 апреля 2016 Аморфные тела имеют определённой точки плавления: при повышении температуры стабильно-аморфные вещества постепенно размягчаются и выше температуры стеклования (Tg) переходят 11 КБ (605 слов) - 09:16, 2 мая 2016 Мелиссовая кислота монтанового воска. Содержится в форме глицерида в корнях одуванчика (Taráxacum officinále). Выделяется также из сахарно-тростникового воска (Saccharum 6 КБ (169 слов) - 17:54, 11 августа 2013 Лимонная кислота трёхосновная карбоновая кислота. Кристаллическое вещество белого цвета, температура плавления 153 °C. Хорошо растворима в воде, растворима в этиловом спирте, 14 КБ (686 слов) - 23:19, 3 апреля 2016 Растительное масло насыщенных жирных кислот с 16 и особенно 18 атомами углерода, тем больше температура плавления масла или жира. Кроме триглицеридов, в состав природных масел входят 24 КБ (1224 слова) - 10:31, 18 апреля 2016 Суппозитории эмульгатор № 1, эмульгатор Т-1, эмульгатор Т-2, твин-80, спирты шёрстного воска, аэросил и другие вспомогательные вещества, разрешённые для медицинского 12 КБ (735 слов) - 12:21, 6 октября 2015 Литьё легкоплавкого материала: парафин, стеарин и др., (в простейшем случае — из воска) путём его запрессовки в пресс-форму изготавливается точная модель изделия 37 КБ (2393 слова) - 23:59, 28 апреля 2016 Неорганические тиосульфаты К2S2O3·3Н2О — температура плавления 56,1 °C K2S2O3·h3О — температура плавления 78,3 °C, плотность 2,590 г/см3 MgS2O3·6h3O — температура плавления выше 82 °C 20 КБ (936 слов) - 10:36, 24 июня 2015 Этилацетат с резким запахом эфира. Молярная масса 88,11 г/моль, температура плавления −83,6 °C, температура кипения 77,1 °C, плотность 0,9001 г/см³, n204 1,3724 9 КБ (453 слова) - 13:09, 17 февраля 2016 Спермацет (категория Воски) растворим в эфире, ацетоне, горячем спирте, но нерастворим в воде. Температура плавления 53—54° С, иодное число 4—9, число омыления 125—136. В XVIII веке 8 КБ (499 слов) - 00:00, 29 апреля 2016 Унуноктий расчётная температура кипения составляет 80 ± 30 °C (довольно широкий диапазон вследствие вариации влияния релятивистских эффектов). Температура плавления его 22 КБ (1355 слов) - 15:48, 10 февраля 2016 Сера выкачивать её на поверхность. Сравнительно невысокая (113 °C) температура плавления серы подтверждала реальность идеи Фраша. В 1890 г. начались испытания 62 КБ (3907 слов) - 23:29, 28 апреля 2016 Пластмассы пластмасс 1 кг) углубится в пластмассу на 1 мм. Температура хрупкости (морозостойкость) — температура, при которой пластичный или эластичный материал 37 КБ (1980 слов) - 11:40, 7 мая 2016 Мазевые основы Температура плавления 50-65 °C. Применяется как уплотнитель. Церезин — Ceresinum Очищенный озокерит. Аморфная бесцветная ломкая масса с температурой плавления 31
300 гр по заебанию
touch.otvet.mail.ru
СЛОЖНЫЕ ЭФИРЫ
Сложными эфирами называются органические соединения, молекулы которых состоят из углеводородных радикалов (остатков спирта) и кислотных остатков, соединенных атомом кислорода.
Сложные эфиры можно рассматривать как производные кислот, у которых атом водорода в карбоксиле замещен радикалом:
R – C – O – R/
ll
O
Общая формула сложных эфиров такая же, как и у карбоновых кислот Сnh3nO2.
Сложные эфиры могут быть образованы как органическими, так и неорганическими кислотами:
OH
½
СН3 – С – О – С2Н5 О = S – O – C2H5 О = N – O – C2H5
ll ll ll
О O O
этиловый эфир этиловый эфир этиловый эфир
уксусной кислоты серной кислоты азотной кислоты
Номенклатура сложных эфиров
Сложные эфиры в большинстве своем называют по тем кислотам и спиртам, остатки которых участвуют в их образовании. По систематической номенклатуре сложные эфиры называют, прибавляя в качестве приставки название спиртового радикала к названию кислоты, в котором окончание “- овая” заменяется на “- оат”.
Н – С = О СН3 – С = О СН3 – СН2 – С = О С3Н7 – С = О
½ ½ ½ ½
О – СН3 О – С2Н5 О – С2Н5 О – СН3
метиловый эфир этиловый эфир этиловый эфир метиловый эфир
муравьиной уксусной пропионовой масляной
кислоты кислоты кислоты кислоты
метиловый эфир этиловый эфир этиловый эфир метиловый эфир
метановой этановой пропановой бутановой
кислоты кислоты кислоты кислоты
метилметаноат этилэтаноат этилпропаноат метилбутаноат
метилформиат этилацетат метилпропионат метилбутират
Изомерия сложных эфиров
Изомерия сложных эфиров определяется изомерией радикалов кислот и спиртов, участвующих в их образовании.
Сложные эфиры являются межклассовыми изомерами с карбоновыми кислотами, имея одинаковую общую формулу.
Физические свойства сложных эфиров
Сложные эфиры простейших и средних представителей кислот и спиртов - жидкости, легче воды, летучие, в большинстве случаев обладающие приятным запахом фруктов. Температуры кипения и плавления сложных эфиров ниже температур кипения и плавления исходных органических кислот. В воде растворимы лишь сложные эфиры с наименьшим числом углеродных атомов. Большинство сложных эфиров плохо растворяется в воде, но хорошо растворяется в органических растворителях.
Таблица 16.6.
Показатели пожарной опасности сложных эфиров
| Кислоты | Плотность r, кг/м3 | tкип | tвспышки | tсамовосп | НТПР | ВТПР |
| Метилацетат СН3СООСН3 | 57,3 | – 15 | – 15 | |||
| Этилацетат СН3СООС2Н5 | 77,1 | |||||
| Бутилацетат СН3СООС4Н9 | 126,1 | |||||
| Амилацетат СН3СООС5Н11 | 148,4 |
Этилацетат – жидкость с приятным запахом, легко испаряется, плохо растворяется в воде. С воздухом этилацетат образует взрывоопасные смеси. Эфир способен к электризации. При контакте с сильными окислителями (перманганатом калия КMnO4, хромовым ангидридом CrO3, перекисью натрия Na2O2) самовозгорается.
Способы получения сложных эфиров
Важнейший способ получения сложных эфиров – реакция этерификации – кислота + спирт.
Н2SO4 конц.
СН3 – С – ОН + НО – СН2 – СН2 –СН3 ¾¾® СН3 – С – О– СН2 – СН2 –СН3 + Н2О
ll ll
О О
уксусная кислота пропанол-1 пропиловый эфир уксусной кислоты
(этановая) (пропилэтаноат)
С помощью метода меченых атомов доказано, что при этерификации от молекулы кислоты отщепляется гидроксил, а от молекулы спирта – водород.
Химические свойства сложных эфиров
1. Реакция этерификации
Основное химическое свойство – гидролиз сложных эфиров – расщепление сложных эфиров под действием воды. Эта реакция обратна реакции этерификации. Реакция протекает как в кислой (катализаторы реакции – протоны Н+), так и в щелочной среде (катализаторы реакции – гидроксид-ионы ОН–).
Н+,(Н2SO4 разб.)
СН3 – С – О– СН2 – СН2 –СН3 + Н2О ¾¾® СН3 – С – ОН + ОН – СН2 – СН2 –СН3
ll ll
О О
пропиловый эфир уксусной кислоты уксусная пропанол-1
(пропилэтаноат) кислота
ОН–,(NaОН)
СН3 – С – О– СН2 – СН2 –СН3 + Н2О ¾¾® СН3 – С – ОNa + ОН – СН2 – СН2 –СН3
ll ll
О О
пропиловый эфир уксусной кислоты ацетат пропанол-1
(пропилэтаноат) натрия
В присутствии щелочи реакция необратима, т.к. происходит омыление – образование солей карбоновых кислот.
В растворах разбавленных минеральных кислот соли карбоновых кислот вновь превращаются в исходную карбоновую кислоту:
2СН3СООNa + h3SO4 разб. ® 2СН3СООН + Na2SO4
ацатат натрия уксусная кислота
2. Реакция восстановления
При восстановлении сложных эфиров образуется смесь двух спиртов:
С2Н5 – С = О + 2 Н2 ® С2Н5 – СН2 – ОН + НО – СН – СН3
½ пропиловый спирт ½
О – СН – СН3 СН3
½ изопропиловый спирт
СН3
изопропиловый эфир
пропановой кислоты
3. Взаимодействие с аммиаком
При взаимодействии сложных эфиров с аммиаком образуются амиды:
СН3 – С = О + Nh4 ® СН3 – С = О + СН3 – ОН
½ ½ метанол
О – СН3 Nh3
метилацетат амид уксусной кислоты
Применение сложных эфиров
Многие сложные эфиры обладают приятным запахом. Так, амиловый эфир муравьиной кислоты имеет запах вишни, изоамиловый эфир уксусной кислоты – запах груш. Эти эфиры идут на изготовление искусственных эссенций, используемых в производстве фруктовых вод и т.п., а также в парфюмерии.
Этилацетат используется в качестве растворителя, а также при изготовлении лекарственных средств.
Жиры
Жиры – это смеси сложных эфиров, образованных трехатомным спиртом глицерином и высшими жирными кислотами. Строение жиров было выяснено в 1811 г французским химиком Шеврелем. В 1854 г Бертло доказал строение жиров, получив их нагреванием глицерина с ВЖК.
Общее название этих эфиров – глицериды. Они могут содержать как одинаковые, так и разные кислотные остатки. Чаще всего встречаются кислоты с числом атомов углерода 12 – 18.
Как правило, все сложные эфиры, входящие в состав жиров, являются полными эфирами, т.е. производными глицерина, остаток которого связан с тремя остатками ВЖК; такие полные эфиры глицерина называются триглицеридами.
Реакция получения триглицерида олеодистеарина, состоящего из остатка олеиновой кислоты и двух остатков стеариновой кислоты может быть записана следующим образом:
СН2 – ОН + НООС – С17Н35 СН2 – О – ОС – С17Н35
½ ½
СН – ОН + НООС – С17Н33 ® СН – О – ОС – С17Н33 + 3Н2О
½ ½
СН2 – ОН + НООС – С17Н35 СН2 – О – ОС – С17Н35
глицерин ВЖК олеодистеарин
Глицерин – постоянная составная часть жиров, т.е. входит во все природные жиры. Кислоты же, входящие в состав жиров весьма разнообразны. Из жиров выделено около 50 различных кислот. Формулы некоторых насыщенных и ненасыщенных ВЖК приведены в разделе 16.5.3.
Получение жиров
В настоящее время практическое значение имеет лишь получение жиров из природных источников – животных и растений; синтез жиров пока экономически невыгоден.
Физические свойства жиров
Жиры бывают животного и растительного происхождения. Некоторые жиры при обычной температуре – твердые вещества (например, баранье и говяжье сало), другие – мягкие или даже жидкие. Жидкие жиры обычно называют маслами.
Жиры не имеют постоянной температуры плавления или застывания, т.к. представляют собой многокомпонентные смеси. Температура плавления жиров зависит от того, какие жирные кислоты в них входят. Жиры, в молекулах которых преобладают остатки насыщенных кислот (например, пальмитиновой и стеариновой), – твердые, в молекулах которых преобладают остатки ненасыщенных кислот (олеиновой, линолевой, линоленовой), – жидкие. Поэтому определение температуры плавления жиров дает некоторое представление о его составе. Ниже других застывает ореховое масло (– 270С), выше - баранье сало (+550С).
Для характеристики различных жиров помимо определения температуры плавления большое значение имеет определение иодного числа. Иодное число – это число граммов иода, присоединяющегося к 100 г жира. Иодное число служит показателем ненасыщенности жира (т.е. наличия кратных связей). Чем выше иодное число масла, тем больше способно масло к самовозгоранию. Установлено, что самовозгораться способны масла с иодным числом больше 50.
Таблица 16.7.
Иодные числа некоторых жиров и масел
| Жиры | Масла | ||
| Бараний | 31 – 46 | Касторовое | 82 – 86 |
| Свиной | 42 – 66 | Хлопковое | 100 – 120 |
| Олеиновая кислота | 80 – 115 | Соевое | 114 – 139 |
| Тюлений | 122 – 162 | Подсолнечное | 145 – 167 |
| Моржовый | Льняное | 175 – 192 |
Все жиры легче воды (их плотность 900 – 950 кг/м3) и нерастворимы в ней. Жиры растворяются во многих органических растворителях (бензине, эфире, сероуглероде, четыреххлористом углероде и др.) Растворимость их в органических соединениях используют, например, при извлечении масла из семян.
Химические свойства жиров
1. Гидролиз (омыление) жиров
В результате омыления жиров щелочами образуются соли ВЖК – мыла и глицерин:
СН2 – О – ОС – С17Н35 СН2 – ОН
½ ½
СН – О – ОС – С17Н35 + 3NaOH ® СН – ОН + 3 С17Н35СООNa
½ ½
СН2 – О – ОС – С17Н35 СН2 – ОН
триглицерид глицерин стеарат натрия
стеариновой кислоты (мыло)
2. Гидрогенизация (гидрирование) жиров
Гидрогенизацией жиров называется процесс присоединения водорода к остаткам непредельных кислот, входящих в состав жиров, в результате чего эти остатки переходят в остатки предельных кислот.
Например, остатки олеиновой, линолевой и линоленовой кислот, присоединяя два, четыре или шесть атомов водорода, превращаются в остатки стеариновой кислоты.
СН2 – О – ОС – С17Н33 + Н2 СН2 – О – ОС – С17Н35
½ Ni ½
СН – О – ОС – С17Н31 + 2Н2 ® СН – О – ОС – С17Н35
½ ½
СН2 – О – ОС – С17Н29 + 3Н2 СН2 – О – ОС – С17Н35
Твердые гидрогенизованные жиры используются не только для технических целей (мыловарение), но и как пищевые жиры (маргарин).
Название “маргарин” происходит от греческого слова “маргарон”, т.е. жемчуг. Впервые метод получения маргарина путем гидрогенизации растительных жиров был предложен французский химиком Меж-Мурье. Маргарин принес ему славу – он выиграл приз, назначенный Наполеоном III за изобретение заменителя сливочного масла.
При более значительной гидрогенизации жиров жирные кислоты превращаются в высокомолекулярные спирты, применяющиеся для производства синтетических заменителей мыла.
3. Окисление жиров
Характерным свойством жиров, как и других органических веществ, является окисление. Эта реакция сопровождается выделением 39 кДж энергии на 1 г жира, что более чем в два раза превосходит тепловой эффект окисления углеводов или белков.
Другая особенность окисления жиров состоит в том, что в результате окисления из 1 г жира образуется до 1, 4 г воды. Это существенный вклад в поддержание общего водного баланса организма. Отдельные виды обитающих в пустынях животных (например, верблюды) такой эндогенной водой полностью удовлетворяют свои потребности во влаге.
Окислению могут подвергаться и остатки непредельных жирных кислот по месту их кратных связей. Этот процесс называется прогорганием жиров. В результате образуются кислоты с более короткими цепями типа масляной кислоты, обладающие неприятным запахом.
От количества кратных связей зависит и способность масел к высыханию. Растительные масла, содержащие в своем составе ненасыщенные связи, при окислении образуют твердую тонкую прозрачную пленку, которая носит название “линоксин”. Масло высыхает тем легче, чем больше двойных связей имеют кислотные остатки.
| Масла, по способности к высыханию делятся на | ||
| высыхающие | полувысыхающие | Невысыхающие |
| льняное, ореховое, маковое, конопляное | подсолнечное, хлопковое | оливковое, кокосовое |
Чтобы ускорить процесс высыхания, высыхающие масла варят и прибавляют к ним так называемые сиккативы – катализаторы, ускоряющие высыхание. В качестве сиккативов используются соли марганца, кобальта, свинца. Высыхающее масло, подвергнутое нагреванию (варке) в присутствии сиккативов, называется олифой.
Процесс высыхания олифы очень сложен и еще полностью не изучен. Известно, что в основе высыхания лежит процесс полимеризации остатков непредельных кислот, образующих высыхающие масла, а также, возможно, их окисления. Кислород воздуха, так же как и сиккативы, является катализатором полимеризации.
Олифа применяется для приготовления масляных красок, для приготовления клеенки, линолеума и т.д.
Воски
Воски (воска) – это сложные эфиры жирных кислот и одноатомных высокомолекулярных (высших) спиртов. Это жироподобные вещества растительного и животного происхождения. Только вместо глицерина в состав восков входят высшие спирты.
По внешнему виду, физическим свойствам и источникам происхождения жиры и воска имеют много общего, однако воски очень устойчивы к воздействию химических реагентов и не изменяются при длительном хранении.
Существует простой способ, помогающий их различить. При сильном нагревании жир издает резкий неприятный запах акролеина, а воск при этом имеет приятный запах.
Воски бывают растительные, животные, ископаемые и синтетические.
Растительные воски
Карнаубский воск покрывает листья бразильской пальмы Copernicia cerifera. Представляет собой сложный эфир триаконтанола СН3(СН2)29ОН и тетракозановой кислоты СН3(СН2)22СООН. Для получения карнаубского воска листья пальмы высушивают, из них выколачивают порошок, который вываривают в воде и выливают в формы. 2000 листьев дают около 16 кг воска. Используют карнаубский воск для изготовления мастик, кремов для обуви.
Пальмовый воск находится в углублениях кольчатого ствола восковой пальмы, откуда его соскабливают. Одно дерево дает 12 кг воска.
Японский воск добывают из лакового дерева, произрастающего в Японии и Китае.
Растительными восками покрыты фрукты, овощи и ягоды (например, черника).
Животные воски
Пчелиный воск – наиболее известный из этого вида восков – представляет собой пальмитиномирициловый эфир.
С15Н31 – С = О
½
О – С31Н63
Шерстяной (шерстный) воск – ланолин – обильно покрывает шерсть животных.
Спермацет содержится в костных черепных углублениях некоторых видов китов, особенно кашалотов. На 90 % состоит из пальмитиноцетилового эфира:
С15Н31 – С = О
½
О – С16Н33
Китайский воск вырабатывается червецом, который обитает на китайском ясене и образует на нем восковой покров. Содержит сложный эфир гексакозановой кислоты СН3(СН2)24СООН и гексадеканового спирта СН3(СН2)15ОН.
К воскам относятся кожное сало и ушная сера.
Воск бактерий покрывает поверхность кислотоупорных бактерий, например, туберкулезных, обеспечивая их устойчивость к внешним воздействиям. Содержит сложные эфиры миколевой кислоты С88Н172О2 и октадеканола С20Н42О.
Ископаемые воски
Торфяной воск получают экстракцией бензином при 800С верхового битуминозного торфа.
Буроугольный воск (монтан-воск) извлекают бензином из бурого битуминозного угля.
Горный воск – озокерит – минерал из группы нефтяных битумов.
Синтетические воски получают на основе нефтяных и смоляных парафинов и их производных.
Воски применяют более чем в 200 отраслях народного хозяйства. Они входят в состав политур, защитных композиций для металлов, тканей, бумаги, кож, дерева; как изолирующий материал; компоненты мазей в косметике и медицине.
Дата добавления: 2015-07-12; просмотров: 125 | Нарушение авторских прав
mybiblioteka.su - 2015-2018 год. (0.032 сек.)mybiblioteka.su



















