Содержание
Химия — 11
3.3.2. Получение и свойства
• Вспомните пройденное •
— Чем отличается функциональная группа сложных эфиров от карбоксильной группы?
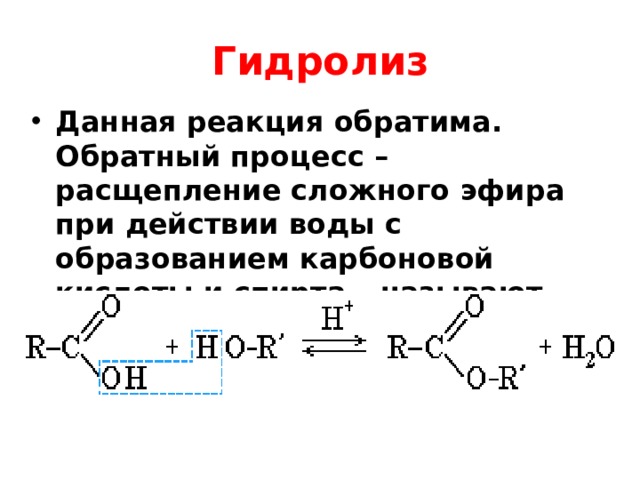
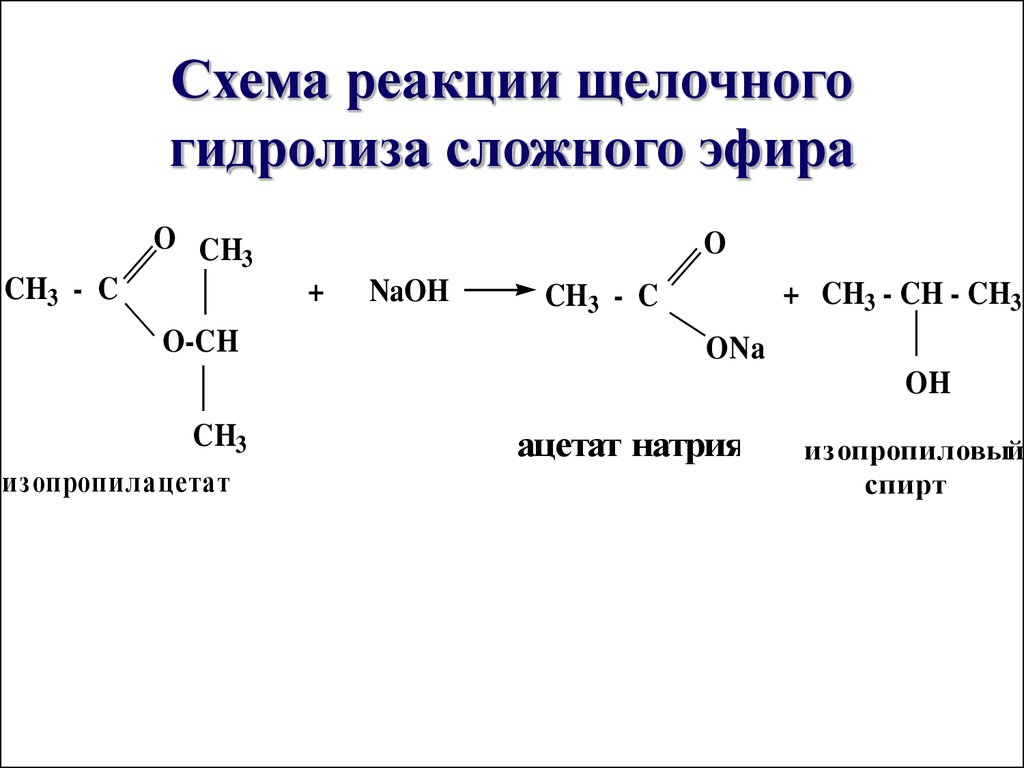
— В каких условиях сложные эфиры подвергаются гидролизу?
|
|
| Деятельность • | Реакции этерификации. Завершите схему реакции и назовите сложный эфир. Установите, какой фактор способствует протеканию реакции. В таблице укажите, как надо изменять количество реагентов и продуктов реакции, чтобы сместить равновесие вправо. Установите, какой фактор способствует протеканию реакции. В таблице укажите, как надо изменять количество реагентов и продуктов реакции, чтобы сместить равновесие вправо.
|
Обсудите: — Почему реакция этерификации является обратимой?
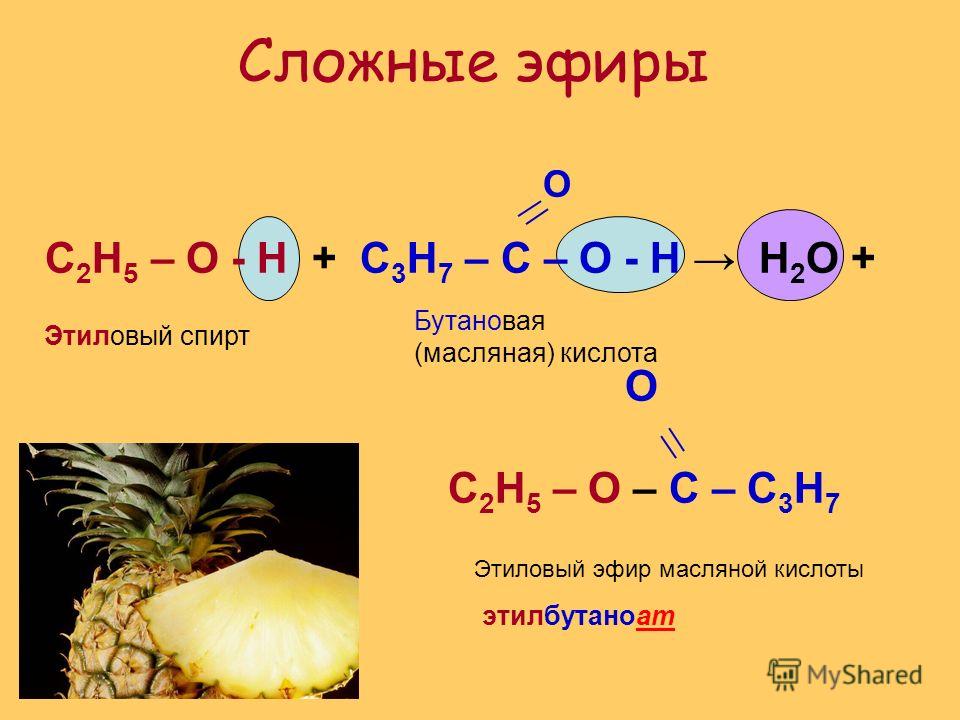
Природные сложные эфиры выделяют из растений методом экстракции органическими растворителями. Однако, большинство из них получают реакцией этерификации:
Некоторые особенности реакции этерификации:
1) В реакции вода образуется из -ОН группы карбоновой кислоты и атома водорода -ОН группы спирта; 2)
реакция этерификации — обратимая реакция.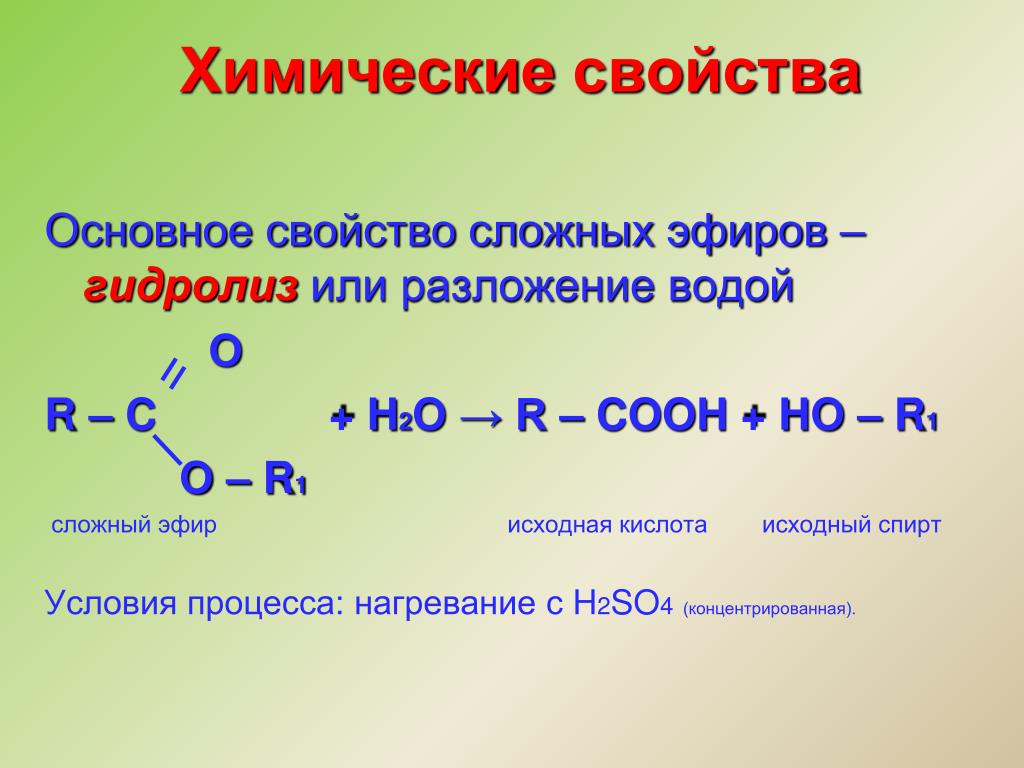 3) реакция проводится в присутствии концентрированной серной кислоты.
3) реакция проводится в присутствии концентрированной серной кислоты.
Для смещения равновесия в сторону образования эфира согласно принципу Ле Шателье надо выполнить следующее:
(a) в реакции спирт или кислоту следует взять в избытке;
(b) удалить эфир из реакционной среды методом дистилляции или образующуюся воду связать посредством водоотнимающих веществ;
Сложные эфиры получают также взаимодействием спиртов с ангидридами кислот (a) и спиртов со сложными эфирами
(b):
Последняя реакция (b) называется переэтерификацией сложных эфиров.
Солнечный свет сдвинул равновесие реакции в сторону продуктов
Химики из Китая и США использовали фототермический катализатор на основе оксида графена, чтобы увеличить эффективность этерификации. В каталитическом процессе продукт реакции быстро переходил в газовую фазу за счет нагрева поверхности катализатора с помощью солнечного света, таким образом авторам удалось преодолеть теоретическое значение конверсии исходных реагентов.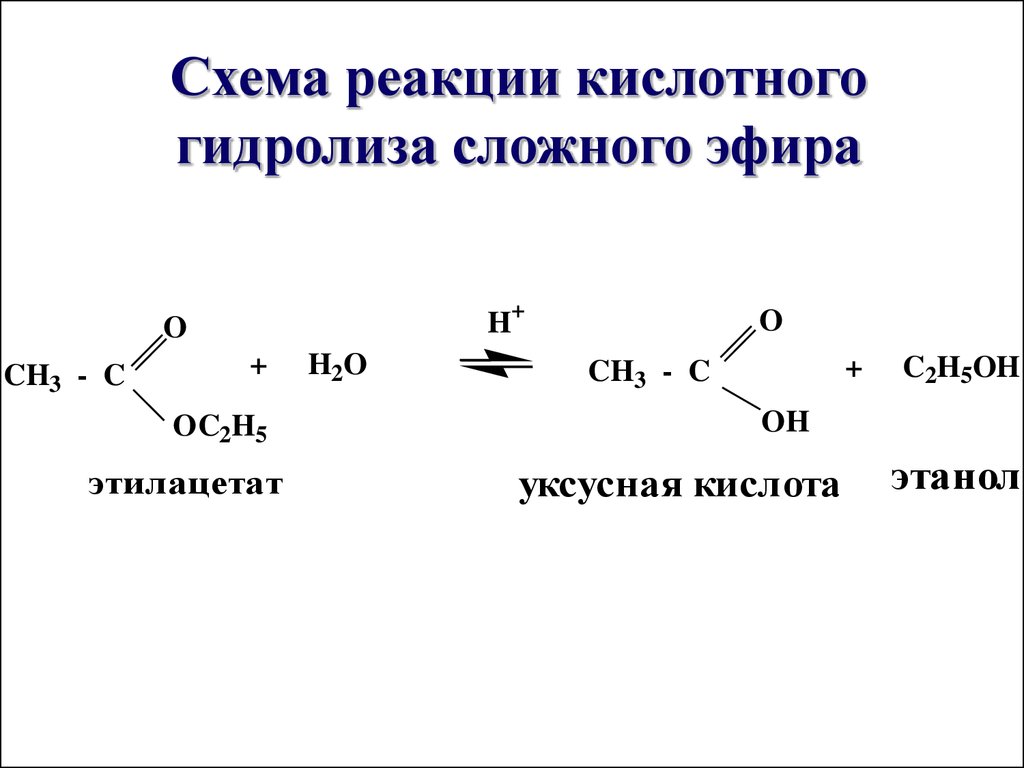 Исследование опубликовано в журнале Nature Sustainability.
Исследование опубликовано в журнале Nature Sustainability.
Реакцию этерификации применяют в промышленности для синтеза пигментов, лекарств и других полезных химических соединений. В ней органическая карбоновая кислота объединяется со спиртом, при этом образуется сложный эфир и вода. Эта реакция равновесная, то есть ее выход определяется константой равновесия. Так, из равных количеств уксусной кислоты и этилового спирта можно получить только около 60 процентов сложного эфира этилацетата (для интервала температур 20–90 градусов Цельсия).
Чтобы преодолеть равновесное значение, химики используют разные подходы. Например, можно добавлять в смесь избыток одного из реагентов и таким образом смещать равновесие в сторону продуктов. Также положение равновесия зависит от температуры, в частности, охлаждение приводит в большим выходам реакции этерификации (но при этом уменьшается ее скорость).
Еще один часто применяемый способ — удаление продукта реакции из реакционной смеси.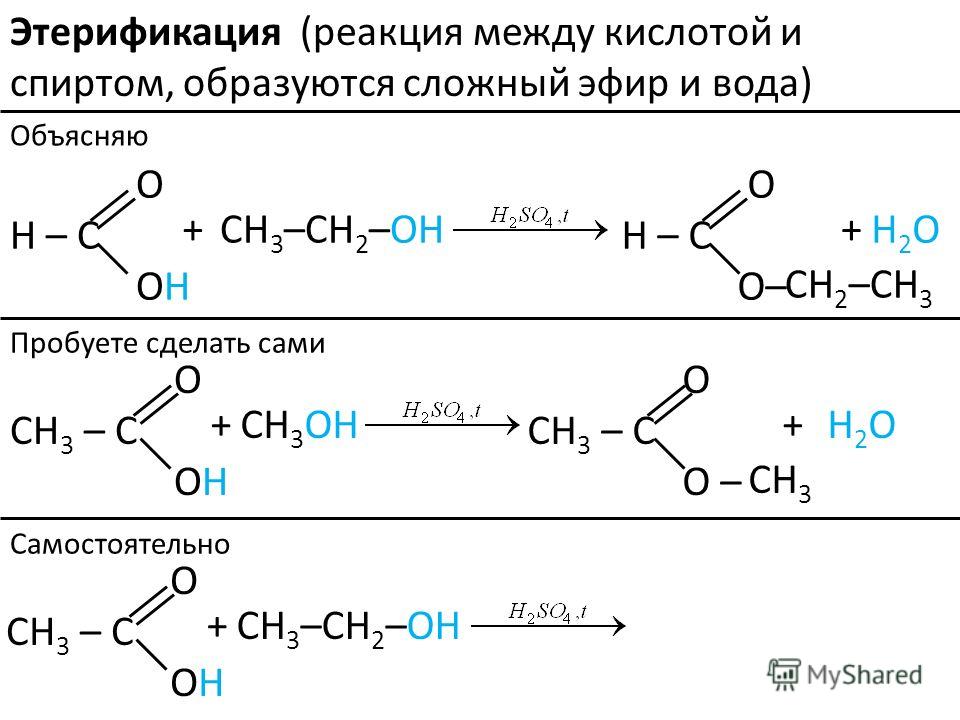 Часто в процессе этерификации связывают получающуюся воду, из-за этого выход реакции тоже повышается. Но группа химиков под руководством Чжу Биня (Zhu Bin) и Чжу Цзя (Zhu Jia) из Нанкинского университета решила попробовать удалять не воду, а сам этилацетат из реакционной смеси. Они предположили, что, подобрав нужный катализатор, им удастся применить солнечную энергию для испарения этилацетата и сдвига равновесия реакции в сторону продуктов.
Часто в процессе этерификации связывают получающуюся воду, из-за этого выход реакции тоже повышается. Но группа химиков под руководством Чжу Биня (Zhu Bin) и Чжу Цзя (Zhu Jia) из Нанкинского университета решила попробовать удалять не воду, а сам этилацетат из реакционной смеси. Они предположили, что, подобрав нужный катализатор, им удастся применить солнечную энергию для испарения этилацетата и сдвига равновесия реакции в сторону продуктов.
Авторам было известно, что для точечного нагревания можно использовать катализаторы на основе графена, так как они обладают фототермическим эффектом (эффективно преобразуют энергию излучения в тепло). Поэтому химики решили взять аэрогель из модифицированного кислотными группами оксида графена. Такой катализатор мог бы одновременно ускорять реакцию с помощью кислотного катализа и смещать равновесие в сторону продуктов за счет точечного нагревания окружающего раствора.
Чтобы модифицировать оксид графена, химики ввели его в реакцию с хлорсульфоновой кислотой HSO3Cl, затем несколько раз промыли водой и высушили.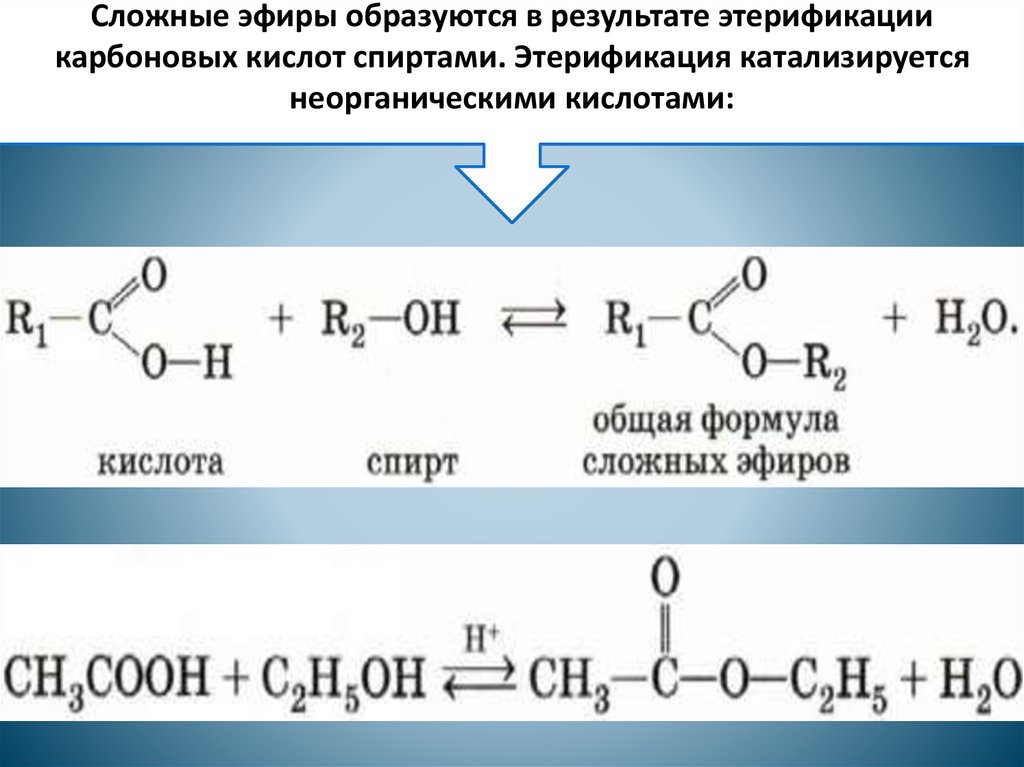 Для изучения каталитических свойств полученного вещества, авторы разработали специальной реактор. Его верхнюю часть они смонтировали из кварцевого стекла, чтобы свет мог проникать внутрь, а чуть ниже сделали дополнительное выпускное отверстие, чтобы испаряющийся этилацетат мог свободно уходить из реакционной массы.
Для изучения каталитических свойств полученного вещества, авторы разработали специальной реактор. Его верхнюю часть они смонтировали из кварцевого стекла, чтобы свет мог проникать внутрь, а чуть ниже сделали дополнительное выпускное отверстие, чтобы испаряющийся этилацетат мог свободно уходить из реакционной массы.
Затем ученые провели несколько экспериментов по получению этилацетата с разной интенсивностью света и, соответственно, с разной температурой, а этанол и уксусную кислоту они взяли в соотношении один к одному. Оказалось, что при интенсивности света 3000 ватт на квадратный метр и более графеновый катализатор становится эффективнее обычной серной кислоты (ее часто применяют в качестве кислотного катализатора). Кроме того, данные ЯМР-спектров полученной смеси продуктов показали, что доля этилацетата в ней составляла 86,15 процента, то есть, несмотря на очень близкие температуры кипения этанола и этилацетата, испарялся только последний. Авторы объяснили это тем, что этанол может образовывать водородные связи с частицами катализатора, а это замедляет его испарение.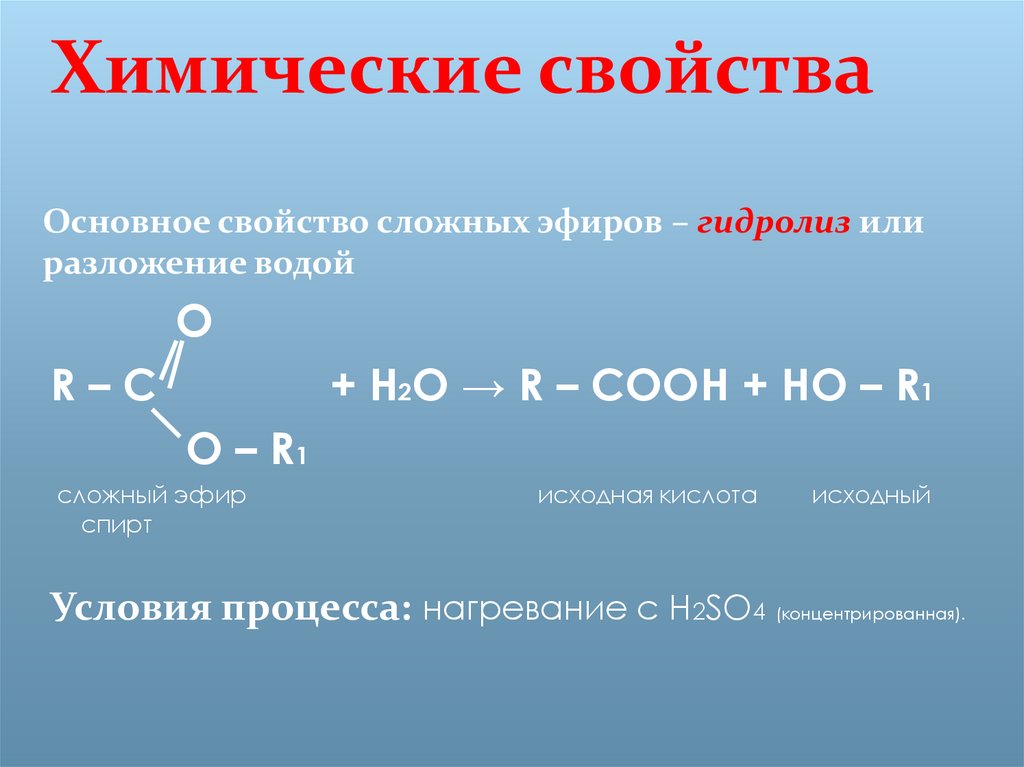
В результате химики разработали процесс, в котором конверсия исходных превзошла равновесную (62,5 процента) и достигла 77 процентов при интенсивности излучения 4000 ватт на квадратный метр. А полученный авторами фототермический катализатор не терял эффективности даже при последовательном проведении шести синтезов (у химиков это заняло примерно 56 часов).
Солнечный свет химики используют не только для нагревания растворов, но и для активации фотохимических катализаторов. Ранее мы рассказывали о том, как фотохимическая реакция позволила легко получать контрастные агенты для томографии.
Михаил Бойм
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Реакции дегидратации в воде. Комбинированный катализатор Бренстеда кислота-ПАВ для образования сложных эфиров, эфиров, тиоэфиров и дитиоацеталей в воде
. 2002 г. 9 октября; 124 (40): 11971-8.
doi: 10.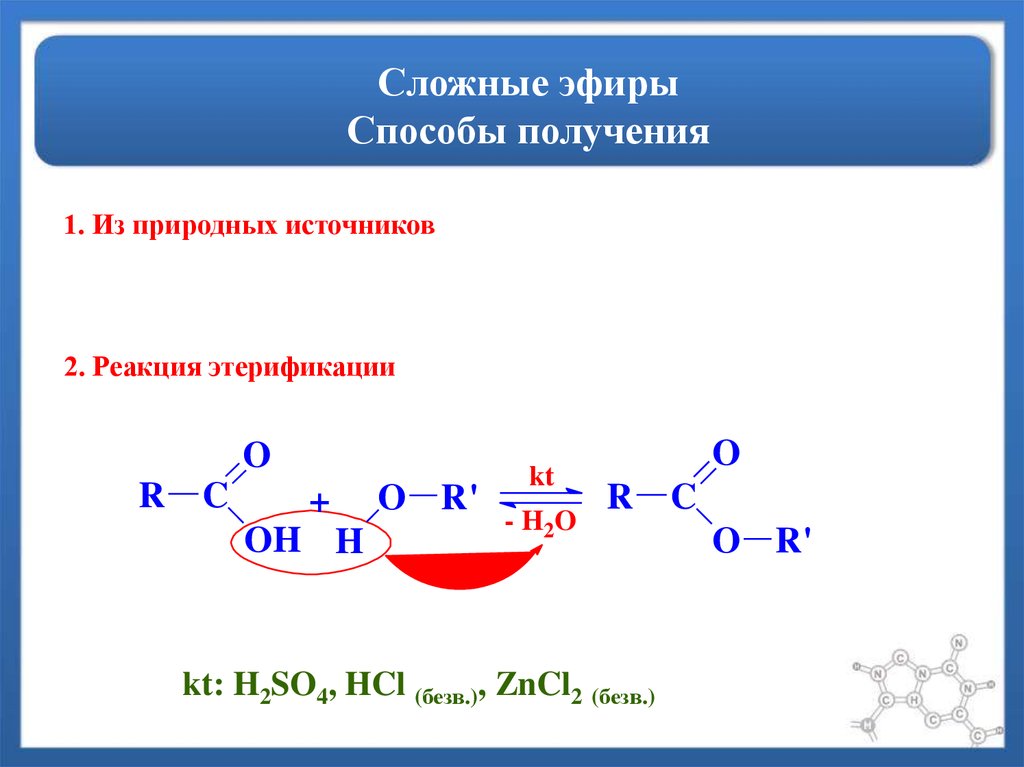 1021/ja026241j.
1021/ja026241j.
Кей Манабэ
1
, Шинья Иимура, Сян-Мин Сун, Шу Кобаяши
принадлежность
- 1 Высшая школа фармацевтических наук, Токийский университет, CREST, Японская научно-техническая корпорация (JST), Хонго, Бункё-ку, Токио 113-0033, Япония.
PMID:
12358542
DOI:
10.1021/ja026241j
Кей Манабэ и др.
J Am Chem Soc.
.
. 2002 г. 9 октября; 124 (40): 11971-8.
doi: 10.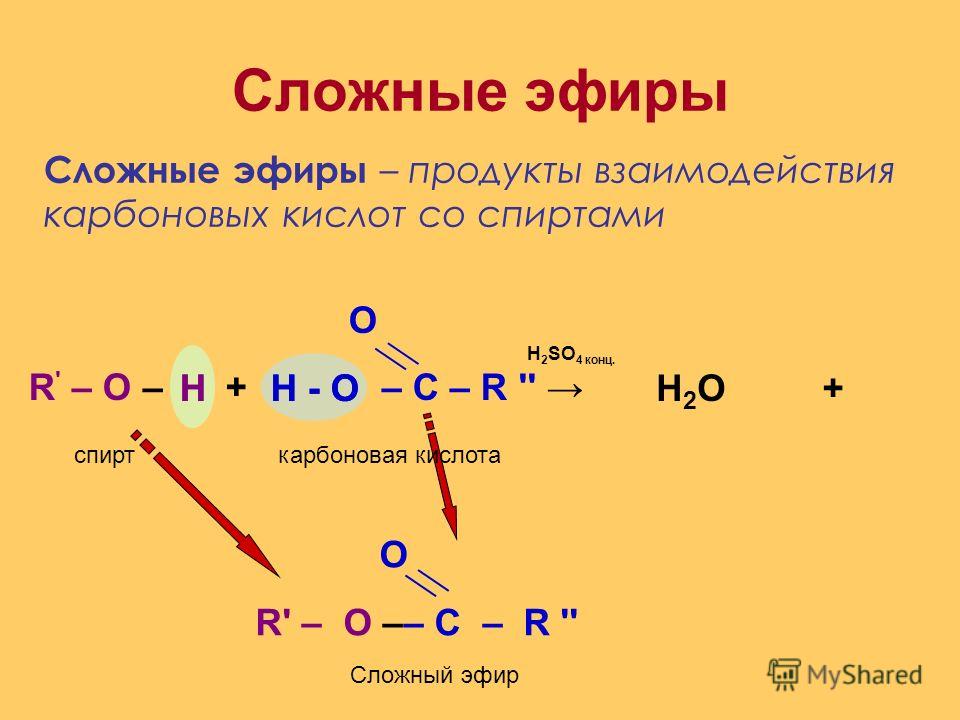 1021/ja026241j.
1021/ja026241j.
Авторы
Кей Манабэ
1
, Шинья Иимура, Сян-Мин Сун, Шу Кобаяши
принадлежность
- 1 Высшая школа фармацевтических наук, Токийский университет, CREST, Японская научно-техническая корпорация (JST), Хонго, Бункё-ку, Токио 113-0033, Япония.
PMID:
12358542
DOI:
10.1021/ja026241j
Абстрактный
Реакции дегидратации в воде осуществляются с помощью катализатора типа поверхностно-активного вещества додецилбензолсульфокислоты (ДБСК). Эти реакции включают дегидратационную этерификацию, этерификацию, тиоэтерификацию и дитиоацетализацию. В этих реакциях ДБСК и субстраты образуют капли эмульсии, внутренняя часть которых достаточно гидрофобна, чтобы исключить образование молекул воды во время реакций. Подробные исследования этерификации показали, что на выход сложных эфиров влияли температура, количество используемого DBSA и субстраты. Эфиры были получены с высокими выходами для высокогидрофобных субстратов. На основе разницы в гидрофобности субстратов была достигнута уникальная селективная этерификация и этерификация в воде. Кроме того, было обнаружено, что хемоспецифические трехкомпонентные реакции в условиях, катализируемых DBSA, также протекают гладко. Эта работа может не только привести к экологически безвредным системам, но и обеспечит новый аспект органической химии в воде.
В этих реакциях ДБСК и субстраты образуют капли эмульсии, внутренняя часть которых достаточно гидрофобна, чтобы исключить образование молекул воды во время реакций. Подробные исследования этерификации показали, что на выход сложных эфиров влияли температура, количество используемого DBSA и субстраты. Эфиры были получены с высокими выходами для высокогидрофобных субстратов. На основе разницы в гидрофобности субстратов была достигнута уникальная селективная этерификация и этерификация в воде. Кроме того, было обнаружено, что хемоспецифические трехкомпонентные реакции в условиях, катализируемых DBSA, также протекают гладко. Эта работа может не только привести к экологически безвредным системам, но и обеспечит новый аспект органической химии в воде.
Похожие статьи
Синтез эфиров фитостерола и линолевой кислоты без растворителей при низкой температуре.
Лю В, Сяо Б, Ван Х, Чен Дж, Ян Г.

Лю В. и др.
RSC Adv. 2021 12 марта; 11 (18): 10738-10746. doi: 10.1039/d1ra00798j. Электронная коллекция 2021 10 марта.
RSC Adv. 2021.PMID: 35423575
Бесплатная статья ЧВК.Опосредованное поверхностно-активными веществами тиогликозилирование 1-гидроксисахаров в воде.
Раттачаг Т., Бунтасана С., Вилайван Т., Падунгрос П.
Раттахаг Т. и др.
Орг Биомол Хим. 2021 28 января; 19 (4): 822-836. doi: 10.1039/d0ob02246b. Epub 2021 6 января.
Орг Биомол Хим. 2021.PMID: 33403378
Кислота Бренстеда поверхностно-активного типа катализирует дегидратационное нуклеофильное замещение спиртов в воде.
Ширакава С., Кобаяси С.
Ширакава С. и соавт.
Орг. лат. 2007 18 января; 9 (2): 311-4. doi: 10.1021/ol062813j.
Орг. лат. 2007.PMID: 17217292
Рекуперация осадка жирных сточных вод скотобойни путем преобразования в бутиловые эфиры жирных кислот путем кислотно-катализируемой этерификации.
Уоллис С., Черни М., Лакру Э., Мулунги З.
Уоллис С. и др.
Управление отходами. 2017 Февраль;60:184-190. doi: 10.1016/j.wasman.2016.07.003. Epub 2016 28 августа.
Управление отходами. 2017.PMID: 27577749
Реакции дегидратации в воде. Катализируемая кислотой Бренстеда прямая этерификация карбоновых кислот спиртами в эмульсионной системе поверхностно-активного типа.
Манабэ К., Сан Х.М., Кобаяши С.
Манабе К. и др.
J Am Chem Soc. 2001 17 октября; 123 (41): 10101-2. дои: 10.1021/ja016338q.
J Am Chem Soc. 2001.PMID: 11592891
Аннотация недоступна.

Посмотреть все похожие статьи
Цитируется
Синтез эфиров фитостерола и линолевой кислоты без растворителей при низкой температуре.
Лю В, Сяо Б, Ван Х, Чен Дж, Ян Г.
Лю В. и др.
RSC Adv. 2021 12 марта; 11 (18): 10738-10746. doi: 10.1039/d1ra00798j. Электронная коллекция 2021 10 марта.
RSC Adv. 2021.PMID: 35423575
Бесплатная статья ЧВК.Селективное гидродеоксигенирование сложных эфиров в несимметричные эфиры на катализаторе Pt-Mo, нанесенном на оксид циркония.
Сакода К., Ямагучи С., Мицудоме Т., Мизугаки Т.
Сакода К. и др.
JACS Au. 2022 г., 24 февраля; 2(3):665-672. doi: 10.1021/jacsau.1c00535. Электронная коллекция 2022 28 марта.
JACS Au. 2022.
2022.PMID: 35373194
Бесплатная статья ЧВК.Гетерогенный катализ в воде.
Линь Л., Гэ Ю., Чжан Х., Ван М., Сяо Д., Ма Д.
Лин Л. и др.
JACS Au. 2021 15 сентября; 1(11):1834-1848. doi: 10.1021/jacsau.1c00319. Электронная коллекция 2021 22 ноября.
JACS Au. 2021.PMID: 34841403
Бесплатная статья ЧВК.Обзор.
Протонная диссоциация биопротонных ионных жидкостей: ионные жидкости [AAE]X аминокислот.
He T, Hong CB, Jiao PC, Xiang H, Zhang Y, Cai HQ, Wang SL, Tao GH.
Он Т и др.
Молекулы. 2020 25 декабря; 26 (1): 62. doi: 10.3390/молекулы26010062.
Молекулы. 2020.PMID: 33375527
Бесплатная статья ЧВК.Конденсация Пикеринга на границе раздела фаз-Кнёвенагеля в эмульсии Пикеринга, стабилизированной оксидом магния.

Садгар А.Л., Деоре Т.С., Джаярам Р.В.
Садгар А.Л. и соавт.
АСУ Омега. 2020 19 мая;5(21):12224-12235. doi: 10.1021/acsomega.0c00819. электронная коллекция 2020 2 июня.
АСУ Омега. 2020.PMID: 32548405
Бесплатная статья ЧВК.
Просмотреть все статьи «Цитируется по»
Преобразование карбоновых кислот в сложные эфиры с использованием кислоты и спиртов (этерификация по Фишеру) – Магистр органической химии
dasdas
Описание: При обработке карбоновой кислоты спиртом и кислотным катализатором образуется сложный эфир (вместе с водой). Эта реакция называется этерификацией Фишера.
Примечания: Реакция фактически является равновесной. Спирт обычно используется в качестве растворителя, поэтому присутствует в большом избытке. Можно использовать множество различных кислот; обычно встречается просто «H+», хотя также часто используются h3SO4 (серная кислота) и TsOH (тозиновая кислота).
Примеры:
Примечания: Побочным продуктом каждой из этих реакций является вода. Обратите внимание, что третий и четвертый примеры представляют собой внутримолекулярные реакции с образованием циклического сложного эфира. Циклические сложные эфиры также называются лактоны .
Пятый пример показывает, что без добавления спирта происходит только протонирование карбонила!
Шестой пример представляет собой двойную этерификацию по Фишеру.
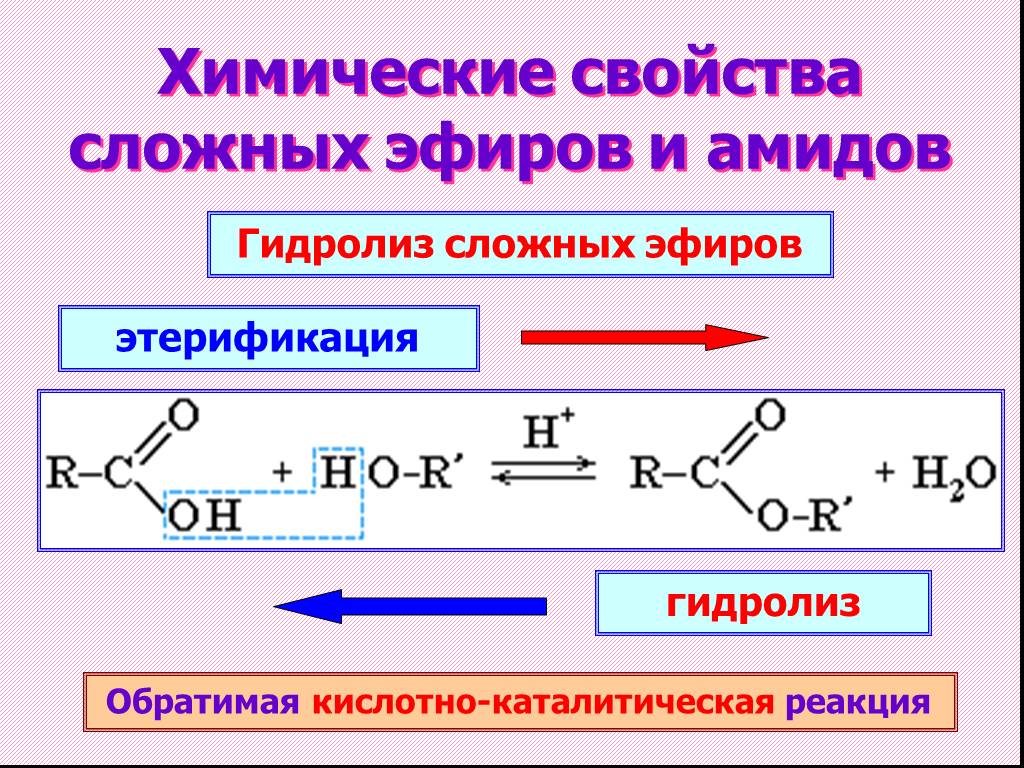
Механизм:
Для такой, казалось бы, простой реакции (замена ОН на ОР) на самом деле нужно много стадий. Протонирование карбонильного кислорода кислотой (этап 1, стрелки A и B) делает карбонильный углерод гораздо лучшим электрофилом. Он подвергается 1,2-присоединению со спиртом (Стадия 2, стрелки C и D), после чего протон от спирта переносится на одну из групп ОН (Стадия 3, стрелки E и F). Последующее 1,2-отщепление воды (Стадия 4, стрелки G и H) приводит к протонированному эфиру, который затем депротонируется (Стадия 5, стрелки I и J).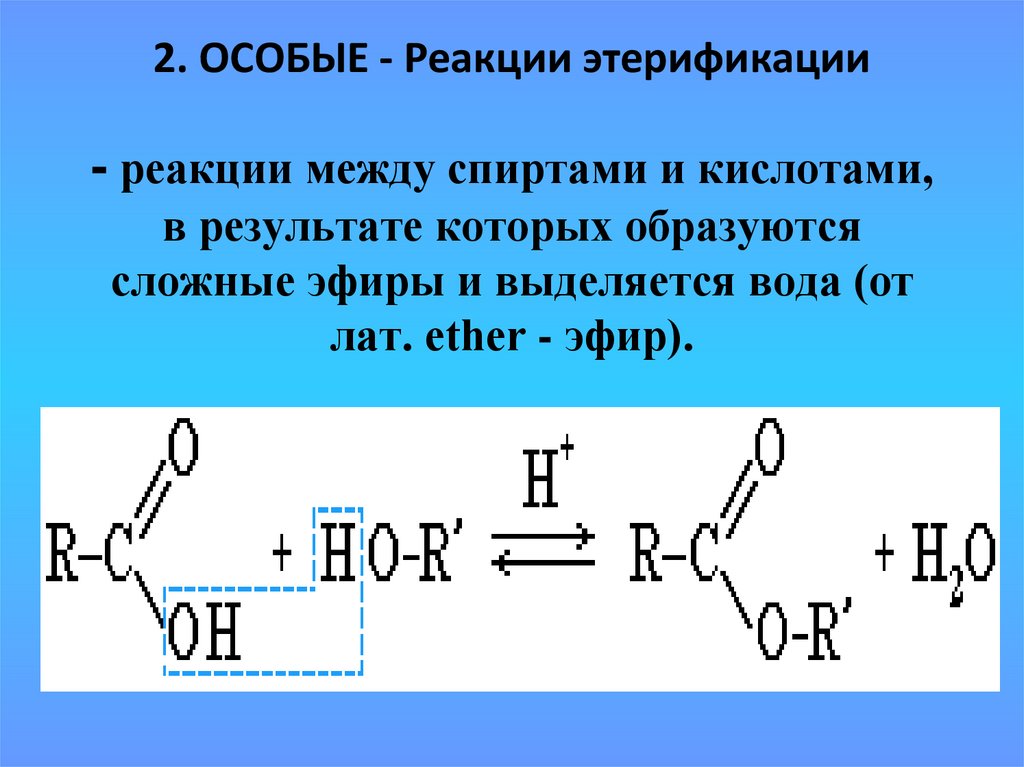
Примечания:
- Все эти стадии находятся в равновесии
Обратите внимание, что кислота здесь является катализатором (регенерируется в конце) и служит двум целям. Во-первых, это делает карбонильный углерод лучшим электрофилом (шаг подготовки 2), а также допускает потерю h3O в качестве уходящей группы (гораздо лучше уходящей группы, чем HO–)
(дополнительно)
- Первый пример
Эмиль Фишер, Артур Шпейер ( 1895 ). «Дарстеллунг дер Эстер».
Chemische Berichte . 28: 3252–3258
DOI: 1002/cber.189502803176
Оригинальная статья Эмиля Фишера и Артура Шпейера, описывающая катализируемую кислотой этерификацию карбоновых кислот и спиртов. - Протонные состояния и механизм кислотно-катализируемой этерификации
Dr. H. Zimmermann Dr. J. Rudolph
Angewandte Chemie Int.


 2022.
2022.