Содержание
Сложные эфиры. Жиры — презентация онлайн
Похожие презентации:
Сложные эфиры. Жиры
Физические, химические свойства предельных и непредельных карбоновых кислот, получение
Газовая хроматография
Хроматографические методы анализа
Искусственные алмазы
Титриметрические методы анализа
Биохимия гормонов
Антисептики и дезинфицирующие средства. (Лекция 6)
Клиническая фармакология антибактериальных препаратов
Биохимия соединительной ткани
1. Сложные эфиры жиры
3. Номенклатура. Изомерия.
Сокращенный вариант
первым указывается название радикала R,
присоединенного к кислоте, затем – название кислоты
(корень слова) с суффиксом «оат» (по аналогии с
суффиксом «ат» в названиях неорганических солей:
карбонат натрия, нитрат хрома).
5. Полный вариант. К названию радикала R (по систематической номенклатуре) добавляется суффикс «овый», затем вставляется
Полный вариант.
К названию радикала R (по
систематической
номенклатуре)
добавляется
суффикс «овый», затем вставляется слово «эфир» и
указывается название кислоты, например, этиловый эфир
этановой кислоты или этиловый эфир уксусной кислоты.
Название сложного эфира бутилпропионат в полном
варианте будет выглядеть следующим образом: бутиловый
эфир пропановой (пропионовой) кислоты.
6. 2. Тривиальное название: к названию радикала R добавляется тривиальное название остатка кислоты (используется суффикс «ат»): —
2. Тривиальное название:
к названию радикала R добавляется тривиальное название
остатка кислоты (используется суффикс «ат»):
— формиат — эфир муравьиной кислоты (НСОО-R),
— ацетат — эфир уксусной кислоты (Ch4COO-R)
— бутират — эфир масляной (бутановой) кислоты
(C3H7COO- R).
Для сложных эфиров карбоновых кислот характерны следующие виды
изомерии:
1. Изомерия углеродной цепи (углеродного скелета) например,
этилбутирату изомерны этилизобутират, пропилацетат и изопропилацетат.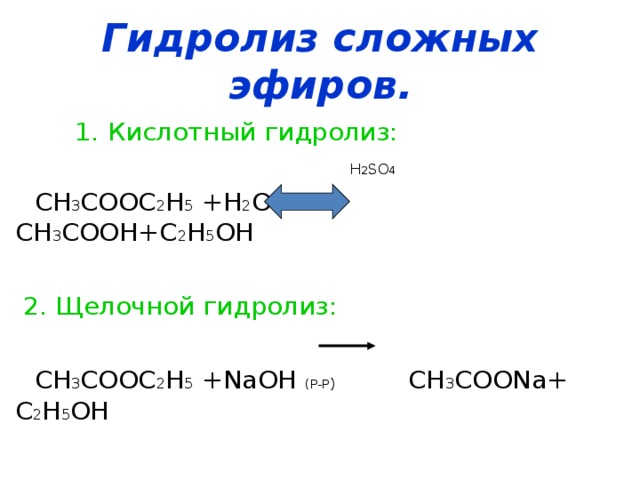
2. Изомерия положения сложноэфирной группировки —С(О)—О—. Этот
вид изомерии начинается со сложных эфиров, в молекулах которых
содержится не менее 4 атомов углерода, например этилацетат и
метилпропионат.
3. Межклассовая изомерия с карбоновыми кислотами,
например, СН3СООСН3 и СН3СН2СООН. Общая формула С3Н6О2 .
Для сложных эфиров, содержащих непредельную кислоту или непредельный
спирт, возможны еще два вида изомерии: изомерия положения кратной
связи и геометрическая (цис-, транс-) изомерия.
9. Физические свойства
Сложные эфиры низших карбоновых кислот и
спиртов представляют собой летучие жидкости, многие
из которых обладают приятным цветочным или
фруктовым запахом. Они практически нерастворимы в
воде и имеют более низкие температуры кипения, чем
изомерные им карбоновые кислоты. Это связанно с тем,
что в молекулах сложных эфиров отсутствуют
межмолекулярные водородные связи.
Сложные эфиры высших жирных кислот и спиртов –
воскообразные вещества, не имеют запаха, в воде не
растворимы,
хорошо
растворяются
в
органических
растворителях.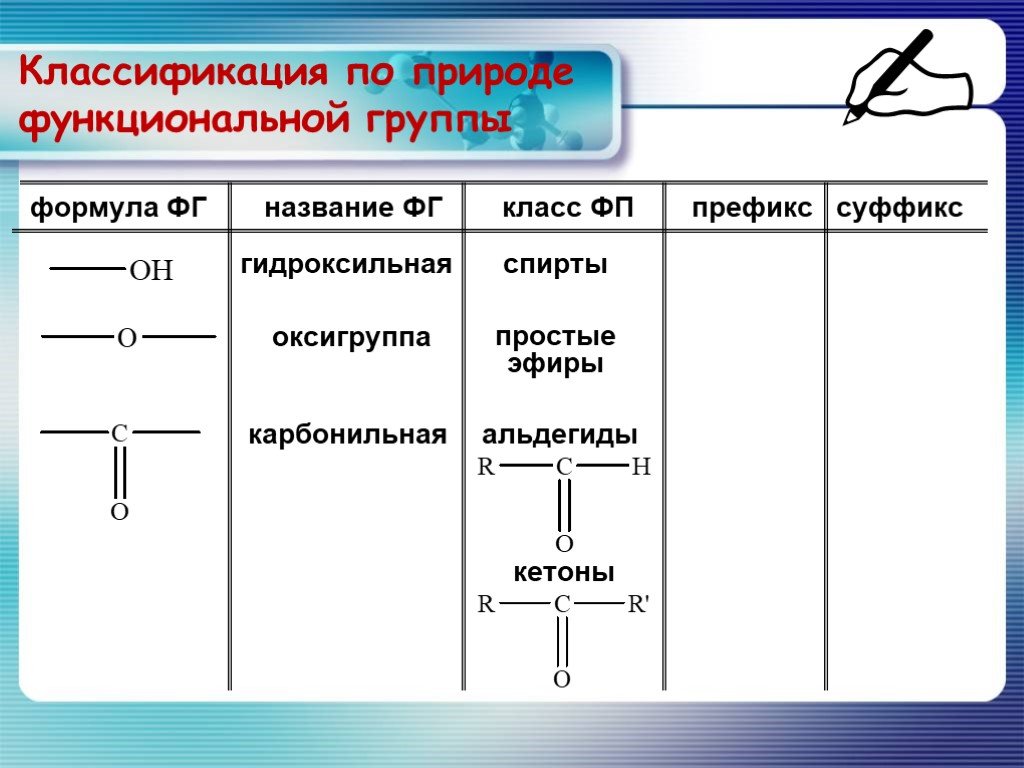
Воски бывают растительные, животные, ископаемые и
синтетические.
Пчелиный воск наиболее известный из этого вида
восков.
Он
содержит
сложный
эфир
пальмитиновой кислоты и мирицилового спирта
(мирицилпальмитат,
пальмитиномирициловый
эфир):
Ch4(Ch3)14–CO–O–(Ch3)29Ch4
12. Химические свойства
1. Реакция гидролиза (омыления)
2. Реакция присоединения
Сложные эфиры, имеющие в своем составе непредельную
кислоту или спирт, способны к реакциям присоединения.
3. Реакция гидрирования (восстановления)
4. Реакция образования амидов
Под действием аммиака сложные эфиры превращаются в
амиды кислот и спирты:
5. Реакция горения
16. ПОЛУЧЕНИЕ
17. 1 способ
Cложные эфиры могут быть получены при взаимодействии
карбоновых кислот со спиртами (реакция этерификации).
Катализаторами являются минеральные кислоты.
видео
19. 2 способ
20. 3 способ
21. 4 способ
22.
 5 способ
5 способ
23. ЖИРЫ относятся к большой химически разнородной группе соединений — ЛИПИДАМ (группа природных нерастворимых в воде соединений)
Классификация липидов
Глицерин-содержащие Не содержащие
глицерин
Связанные с другими
органическими
веществами
Нейтральные жиры,
триацилглицерины
Фосфоглицериды
Сфингоипиды
Липопротеины
Алифатические
спирты и воска
Терпены
Липополисахариды
Стероиды
Гликолипиды
Молекулы
липидов
обладают
двойственным
сродством к полярной среде (гидрофильность) и к
неполярной
среде
(гидрофобность)
амфифильностью
25. ЖИРЫ ИЛИ ТРИАЦИЛГЛИЦЕРИНЫ
ЭТО СЛОЖНЫЕ ЭФИРЫ
ГЛИЦЕРИНА
И КАРБОНОВЫХ
КИСЛОТ
26. Схема получения жиров
27. Простые и смешанные жиры
28. Условные знаки для обозначения жиров
• Известно более 70 карбоновых кислот, входящих в состав жиров
• Большая часть из них имеет неразветвленную углеродную цепь из
четного числа атомов С от 14 до 24
• Двойные связи имеют изолированный характер и имеют цисконфигурацию
• Обозначение в биохимии: 12:0 , где 12- число атомов С в кислоте
0 – число двойных связей.
• Для пальмитолеиновой кислоты С15Н29СООН — 16:1, ∆9
Наиболее важные незаменимые
полиненасыщенные жирные кислоты:
• линолевая 18:2, ∆9, 12 омега – 6
С17Н31СООН
• линоленовая 18:3, ∆9, 12,15 омега – 3
С17Н29СООН
• арахидоновая 20:4, ∆5,8,11,14 омега – 6 С19Н31СООН
30. Физические свойства
• Растительные жиры – масла, имеют температуру плавления ниже
0о С : оливковое масло -6о С, подсолнечное -17о С , льняное 24о С.
• Животные жиры — твердые вещества; температура плавления
свиного жира 38-44о С, говяжьего 44-50о С
• Не растворяются в воде
31. Химические свойства
1 . Гидролиз
33. 2 . Гидрирование
34. 3 . Окисление
English
Русский
Правила
Классификация и состав сложных эфиров.
Среди
изученных и широко применяемых сложных
эфиров большинство представляют
соединения, полученные на основе
карбоновых кислот. Сложные эфиры на
основе минеральных (неорганических)
кислот не столь разнообразны, т.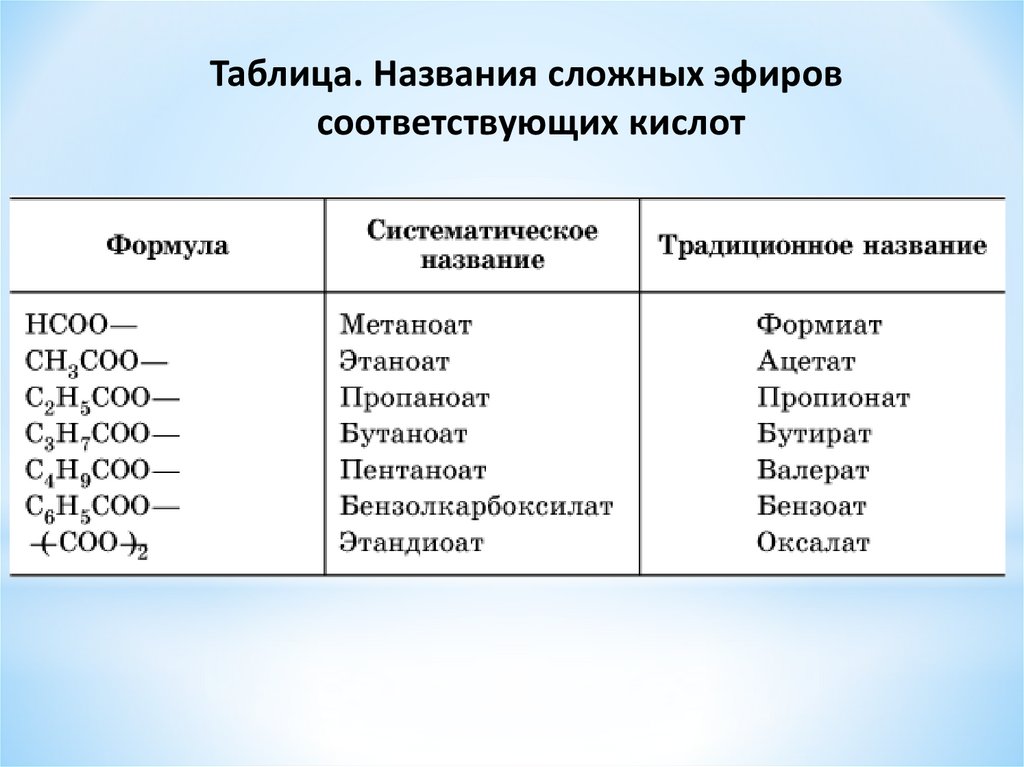 к. класс
к. класс
минеральных кислот менее многочисленен,
чем карбоновых (многообразие соединений
– один из отличительных признаков органической
химии).
Когда
число атомов С в исходных карбоновой
кислоте и спирте не превышает 6–8,
соответствующие сложные эфиры представляют
собой бесцветные маслянистые жидкости,
чаще всего с фруктовым запахом. Они
составляют группу фруктовых эфиров.
Если в образовании сложного эфира
участвует ароматический спирт (содержащий
ароматическое ядро), то такие соединения
обладают, как правило, не фруктовым, а
цветочным запахом. Все соединения этой
группы практически нерастворимы в воде,
но легко растворимы в большинстве
органических растворителей. Интересны
эти соединения широким спектром приятных
ароматов (табл. 1), некоторые из них
вначале были выделены из растений, а
позже синтезированы искусственно.
При
увеличении размеров органических групп,
входящих в состав сложных эфиров, до
С15–30 соединения
приобретают консистенцию пластичных,
легко размягчающихся веществ.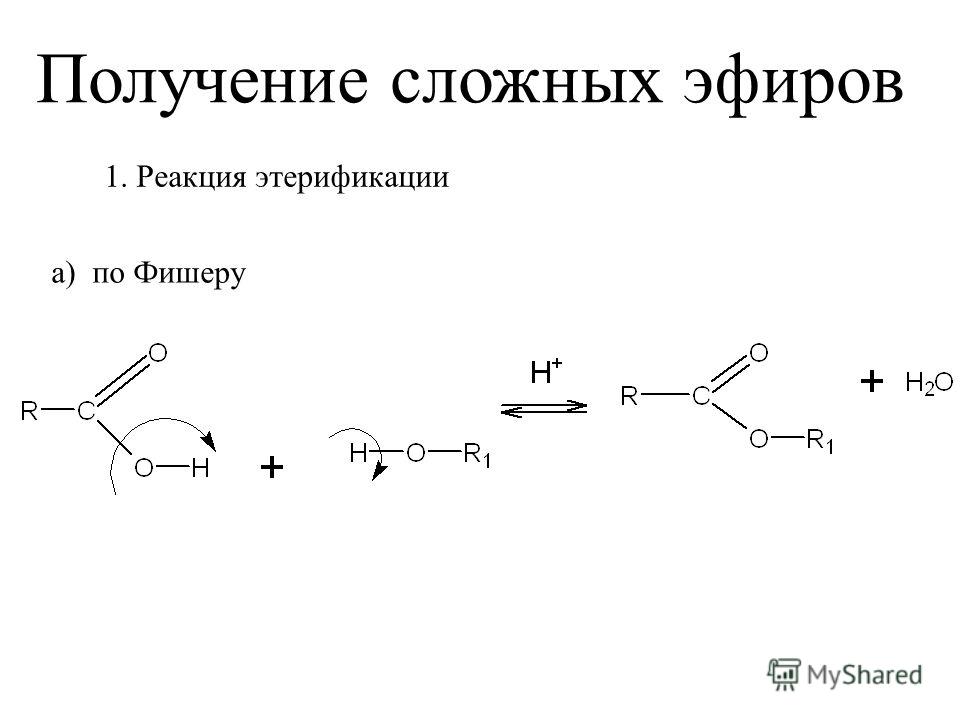 Эту группу
Эту группу
называют восками, они, как правило, не
обладают запахом. Пчелиный воск содержит
смесь различных сложных эфиров, один
из компонентов воска, который удалось
выделить и определить его состав,
представляет собой мирициловый эфир
пальмитиновой кислоты С15Н31СООС31Н63.
Китайский воск (продукт выделения
кошенили – насекомых Восточной Азии)
содержит цериловый эфир церотиновой
кислоты С25Н51СООС26Н53.
Кроме того, воски содержат и свободные
карбоновые кислоты и спирты, включающие
большие органические группы. Воски не
смачиваются водой, растворимы в бензине,
хлороформе, бензоле.
Среди функциональных
производных карбоновых кислот особое
место занимают сложные эфиры —
соединения, представляющие карбоновые
кислоты, у которых атом водорода в
карбоксильной группе заменен углеводородным
радикалом. Общая формула сложных эфиров
R — C — O — R’ |
|| |
O |
где R и R’
— углеводородные радикалы (в сложных
эфирах муравьиной кислоты R —
атом водорода).
Названия сложных
эфиров производят от названия,
углеводородного радикала и названия
кислоты, в котором вместо окончания
«-овая кислота» используют суффикс «ат»,
например:
|
| |||||||||||||||||||||||||
Часто сложные эфиры
называют по тем остаткам кислот и спиртов,
из которых они состоят.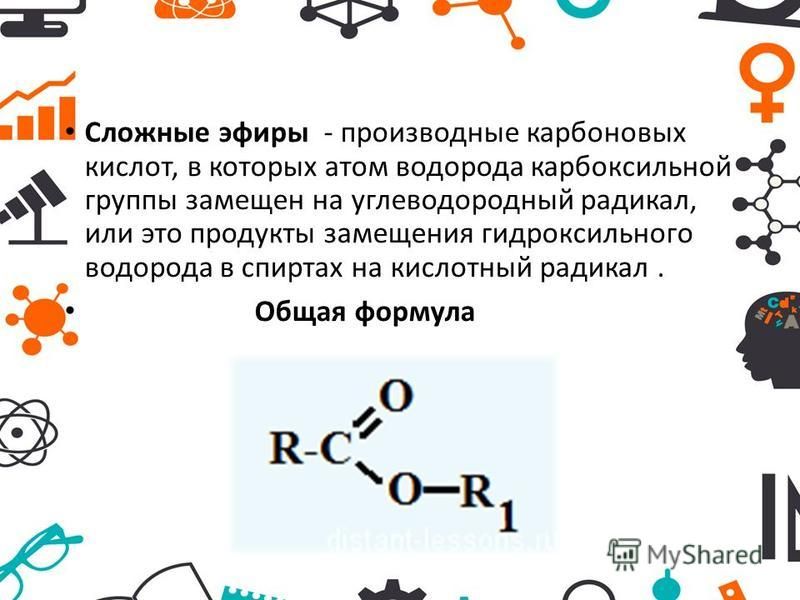 Так, рассмотренные
Так, рассмотренные
выше сложные эфиры могут быть названы:
этановоэтиловый эфир, кротоновометиловый
эфир.
Номенклатура
простых эфиров.
Если
группы R и R’ в простом эфире одинаковы,
то его называют симметричным, если
разные – несимметричным. В название
эфира включают названия органических
групп, упоминая их в алфавитном порядке,
и добавляют слово эфир, например,
C2H5OC3H7 –
пропилэтиловый эфир. Для симметричных
эфиров перед названием органической
группы вводят приставку «ди», например,
C2H5OC2H5 –
диэтиловый эфир. Для многих эфиров часто
используют тривиальные (упрощенные)
названия, сложившиеся исторически. К
простым эфирам иногда относят соединения,
которые содержат эфирный фрагмент С–О–С
в составе циклической молекулы (рис.
1), одновременно их причисляют к другому
классу соединений – гетероциклическим
соединениям.
Есть также соединения (см. АЛЬДЕГИДЫ
И КЕТОНЫ),
в состав которых входит фрагмент С–О–С,
но к классу эфиров их не относят, это
полуацетали – соединения, содержащие
одновременно алкокси- и гидрокси-группу
у одного атома углерода: >C(OH)OR, а также
ацетали – соединения, где у одного атома
углерода находятся одновременно две
RО-группы: >C(OR)2(рис.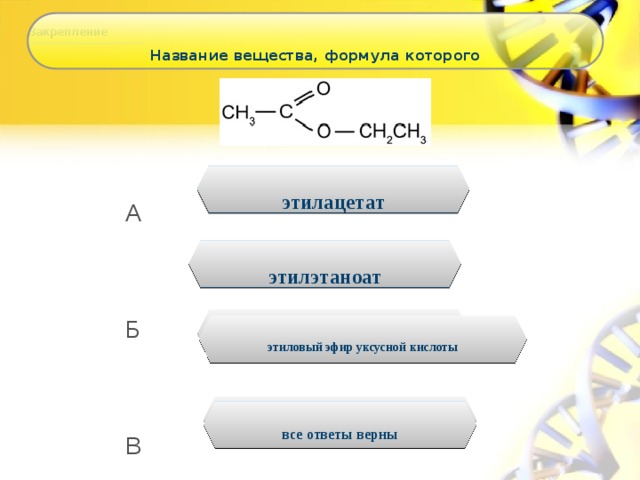
1). Наличие у одного атома углерода сразу
двух химически связанных атомов О делает
эти соединения непохожими по химическим
свойствам на простые эфиры.
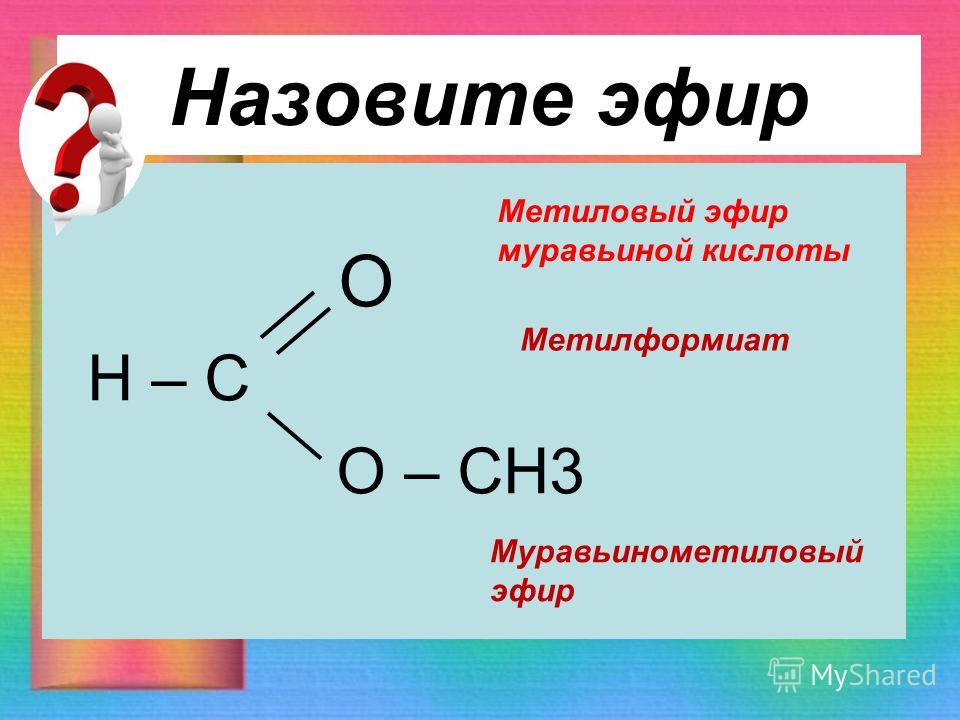
какой суффикс сложного эфира?
Ответ
Проверено
216,3 тыс.+ просмотров
Подсказка: Система номенклатуры ИЮПАК состоит из трех частей: корня слова, суффикса и префикса. Суффикс связан с корнем слова. Эфиры являются производными кислоты. Таким образом, сложные эфиры можно разделить на две части: кислотную часть и спиртовую часть. Общая номенклатура сложного эфира IUPAC — алкилалканоат.
Полное решение:
Сложные эфиры имеют характерный запах. Они обычно используются для характерного аромата и аромата. Сложные эфиры являются производными карбоновой кислоты. Его получают реакцией кислоты и спирта с последующим удалением молекулы воды. Общее представление сложного эфира: $\text{ R}-\text{COO}-\text{R }\!\!’\!\!\text{ }$ .
Для присвоения названия сложному эфиру можно использовать следующую стадию. Эти этапы следующие:
Шаг 1) во-первых, определить атом кислорода непрерывной цепи, которая связана с атомом углерода с обеих сторон. (С одной стороны это карбонильный углерод).
Шаг 2) давайте начнем нумеровать углеродную цепь по обе стороны от идентифицированного атома кислорода. Число будет дано таким образом, что углерод по обе стороны от кислорода будет иметь 1 позицию.
Шаг 3) Назвать соединение, используя простой формат.
(Алкил на стороне без карбонильной группы) (Алкан на стороне с карбонильной группой)
Стадия 4) на последней стадии конец алкана (который находится на той же стороне, что и карбоксильная или карбонилсодержащая цепь) меняется с -e на -oate.
$\text{ Алкилалканы -е + оат = Алкилалканоаты }$
Таким образом, сложные эфиры имеют суффикс «-оат».
Рассмотрим пример:
Соединение имеет название IUPAC как метилметаноат.
Примечание: Помните, что сложный эфир состоит из двух частей: кислоты и спирта. Алкогольная часть всегда заканчивается на «ил». Однако окончания названия IUPAC записываются таким образом, что «ойевая кислота» кислоты заменяется на «оат». Точно так же амиды также являются производными кислоты. В амидах ойевая кислота заменена названием «амид».
Недавно обновленные страницы
Большинство эубактериальных антибиотиков получены из биологии ризобия класса 12 NEET_UG
Биоинсектициды саламин были извлечены из класса 12 Biology NEET_UG
Какое из следующих утверждений, касающихся Baculovirussess, Neet_ug
. Какое из следующих утверждений, касающихся Baculoviruses, Neet_ug
. муниципальные канализационные трубы не должны быть непосредственно 12 класса биологии NEET_UG
Очистка сточных вод выполняется микробами A B Удобрения 12 класса биологии NEET_UG
Иммобилизация фермента – это конверсия активного фермента класса 12 биологии NEET_UG
Большинство эубактериальных антибиотиков получают из биологического класса Rhizobium 12 NEET_UG
Саламиновые биоинсектициды были извлечены из биологического класса А 12 NEET_UG
12 класс биологии NEET_UG
Канализационные или городские канализационные трубы не должны быть напрямую 12 класс биологии NEET_UG
Очистка сточных вод выполняется микробами A B Удобрения 12 класс биологии NEET_UG
Иммобилизация фермента – это Превращение активного фермента класса 12 биологии NEET_UG
Актуальные сомнения
12.
 3. Названия альдегидов, кетонов, карбоновых кислот, сложных эфиров, а также общие названия
3. Названия альдегидов, кетонов, карбоновых кислот, сложных эфиров, а также общие названия
Альдегиды
Основная статья: Альдегиды
Альдегиды (R-CHO) имеют суффикс «-al». Если присутствуют другие функциональные группы, цепь нумеруют так, чтобы альдегидный углерод находился в положении «1», если только не присутствуют функциональные группы с более высоким приоритетом.
Если требуется форма префикса, используется «оксо-» (как для кетонов), с номером позиции, указывающим конец цепи: CHOCH 2 COOH – 3-оксопропановая кислота. Если углерод в карбонильной группе не может быть включен в присоединенную цепь (например, в случае циклических альдегидов), используется префикс «формил-» или суффикс «- карбальдегид »: C 6 H 11 CHO представляет собой циклогексанкарбальдегид. Если альдегид присоединен к бензолу и является основной функциональной группой, суффикс становится бензальдегидом.
Если альдегид присоединен к бензолу и является основной функциональной группой, суффикс становится бензальдегидом.
Кетоны
Основная статья: Кетоны
Обычно кетоны (R-CO-R) имеют суффикс «-one» (произносится как собственный , а не выиграл ) с инфиксным номером позиции: CH 3 CH 2 CH 2 COCH 3 представляет собой пентан-2-он. Если используется суффикс более высокого приоритета, используется префикс «оксо-»: CH 3 CH 2 CH 2 COCH 2 CHO представляет собой 3-оксогексаналь.
Карбоновые кислоты
Основная статья: Карбоновые кислоты
Обычно карбоновые кислоты называются с суффиксом -ойная кислота (этимологически обратное образование из бензойной кислоты). Подобно альдегидам, они занимают положение «1» в исходной цепи, но их номер положения не указан. Например, CH 3 CH 2 CH 2 CH 2 COOH (валериановая кислота) называется пентановой кислотой. Для обычных карбоновых кислот некоторые традиционные названия, такие как уксусная кислота, настолько широко используются, что считаются сохраненными названиями IUPAC, хотя «систематические» названия, такие как этановая кислота, также приемлемы. Карбоновые кислоты, присоединенные к бензольному кольцу, такие как Ph-COOH, называются бензойной кислотой или ее производными.
Для обычных карбоновых кислот некоторые традиционные названия, такие как уксусная кислота, настолько широко используются, что считаются сохраненными названиями IUPAC, хотя «систематические» названия, такие как этановая кислота, также приемлемы. Карбоновые кислоты, присоединенные к бензольному кольцу, такие как Ph-COOH, называются бензойной кислотой или ее производными.
Если в одной исходной цепи имеется несколько карбоксильных групп, можно использовать суффикс «-карбоновая кислота» (например, -дикарбоновая кислота, -трикарбоновая кислота и т. д.). В этих случаях углерод в карбоксильной группе , а не считается частью основной цепи алкана. То же самое верно и для префиксной формы «карбоксил-». Лимонная кислота является одним из примеров; она называется 2-гидроксипропан-1,2,3-трикарбоновой кислотой, а не 3-карбокси-3-гидроксипентандиовой кислотой.
Сложные эфиры
Основная статья: Сложные эфиры
Сложные эфиры (R-CO-O-R’) называются алкилпроизводными карбоновых кислот. Алкильная группа (R’) названа первой. Затем часть R-CO-O называется отдельным словом на основе названия карбоновой кислоты с изменением окончания с -oic acid на -oate . Например, CH 3 CH 2 CH 2 CH 2 COOCH 3 IS Метил пентаноат и (CH 3 ) 2 CHCH 2 CH ) 2 CHCH 2 CH ) 2 CHCH 2 CH ) 2 CHCH 2 CH
Алкильная группа (R’) названа первой. Затем часть R-CO-O называется отдельным словом на основе названия карбоновой кислоты с изменением окончания с -oic acid на -oate . Например, CH 3 CH 2 CH 2 CH 2 COOCH 3 IS Метил пентаноат и (CH 3 ) 2 CHCH 2 CH ) 2 CHCH 2 CH ) 2 CHCH 2 CH ) 2 CHCH 2 CH
084 2 COOCH 2 CH 3 представляет собой этил 4-метилпентаноат . Для сложных эфиров, таких как этилацетат (CH 3 COOCH 2 CH 3 ), этилформиат (HCOOCH 2 CH 3 ) или диметилфталат, которые основаны на обычных кислотах, IUPAC рекомендует использовать эти установленные названия. , называемые сохраненными именами. -oate меняется на -ate . Некоторые простые примеры, названные в обоих направлениях, показаны на рисунке выше.
