Содержание
Простые эфиры,
Простые эфиры являются производными
спиртов, енолов и фенолов, в которых
атом водорода гидроксильной группы
замещен углеводородным остатком.
Простые эфиры подразделяют на соединения
алифатического, ароматического и
смешанного рядов.
Для названия простых эфиров используется
радикально-функциональная
номенклатура, согласно которой название
образуют из названий радикалов следующих
в алфавитном порядке и слова эфир,
например, диметиловый эфир С2Н5
– О – С2Н5; винилметиловый
эфир СН3 – О – СН=СН2
; диизопропиловый эфир (СН3)2СН
– О – СН(СН3)2.
Более сложные по составу простые эфиры
называют по правилам заместительной
номенклатуры, в соответствии с которой
к названию более старшего углеводорода
добавляют название радикала R
– O – в качестве приставки,
например, СН3СН2 — О – С6Н5
этоксибензол. Полиэфиры линейной
Полиэфиры линейной
структуры называют по заместительной
номенклатуре, например,
1,2-диметоксиэтан (глим) СН3 – О –
СН2СН2 – О – СН3.
Правила номенклатуры IUPAC
сохраняют некоторые тривиальные
названия эфиров
Циклические простые эфиры называют как
гетероциклические соединения. Насыщенные
кислородсодержащие гетероциклы называют:
оксиран (трехчленный), оксолан
(пятичленный), диоксан (шестичленный
с двумя атомами кислорода). Оксолан чаще
называют тетрагидрофураном
как производное ненасыщенного аналога
– фурана.
Для оксирана прочно
сохраняется название этиленоксид.
Оксираны часто называют эпоксидами,
хотя префикс эпокси-означает атом
кислорода, связанный с двумя любыми
атомами углерода в циклической системе,
и не обязательно соседними.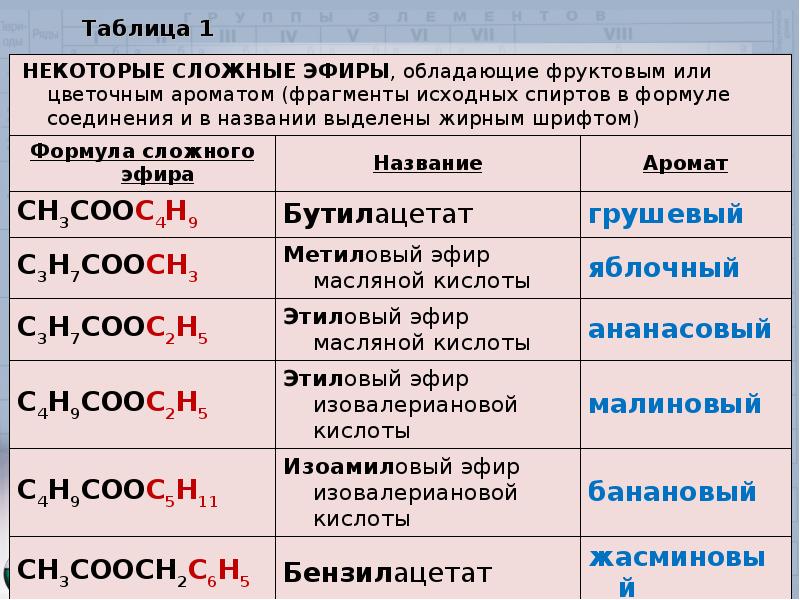
Физические свойства.
Простые эфиры, как правило, представляют
собой бесцветные жидкости со своеобразным
запахом и довольно низкими температурами
кипения. Только диариловые эфиры являются
твердыми веществами. Простые эфиры
легче воды и плохо в ней растворимы.
Простые эфиры фенолов имеют своеобразный
цветочный запах и используются в
парфюмерии. Наиболее важными в этом
отношении являются анизол и фенетол,
которые, кроме того, применяются в
синтезе лекарственных препаратов и
красителей.
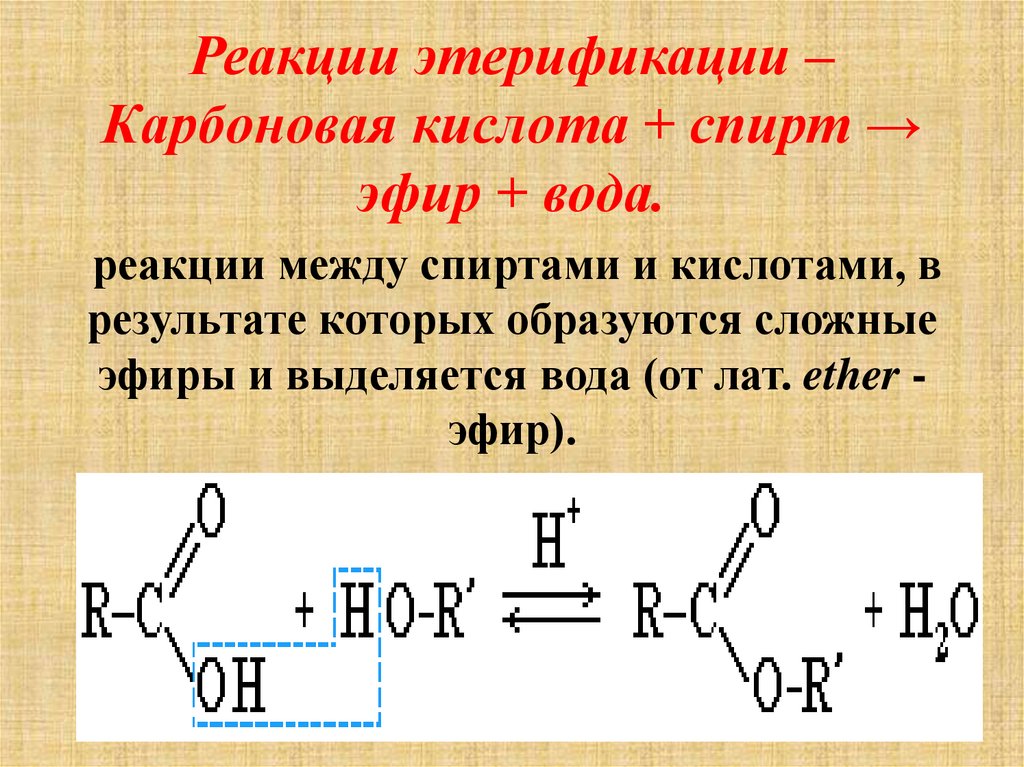
Способы получения.
Простые эфиры могут быть получены из
галогенопроизводных, спиртов, фенолов.
Получение из галогенопроизводных
(синтез Вильямсона). Реакция
протекает по механизму SN2,
поэтому хороший выход достигается лишь
в случае первичных алкилирующих
реагкнтов, в качестве которых могут
выступать алкилгалогениды, алкилсульфаты
и алкилсульфонаты.
Дегидратация спиртов.

Превращение первичных спиртов под
действием минеральных кислот – старейший
и до настоящего времени важнейший
способ образования симметричных простых
эфиров. Однако этот способ мало пригоден
для синтеза смешанных алифатических
эфиров и не годится для получения
ароматических эфиров.
Н2SO4
2 СН3СН2СН2-ОН
СН3СН2СН2 —
О – СН2СН2СН3
Пропанол-1
дипропиловый эфир
(1-пропоксипропан)
Вторичные и третичные спирты в этих
условиях превращаются не в простые
эфиры, а в алкены. Третичные спирты дают
хорошие выходы смешанных эфиров в
реакциях с первичными спиртами. В случае
диолов реакция дегидратации может
протекать как межмолекулярно, так и
внутримолекулярно с образованием
циклических эфиров.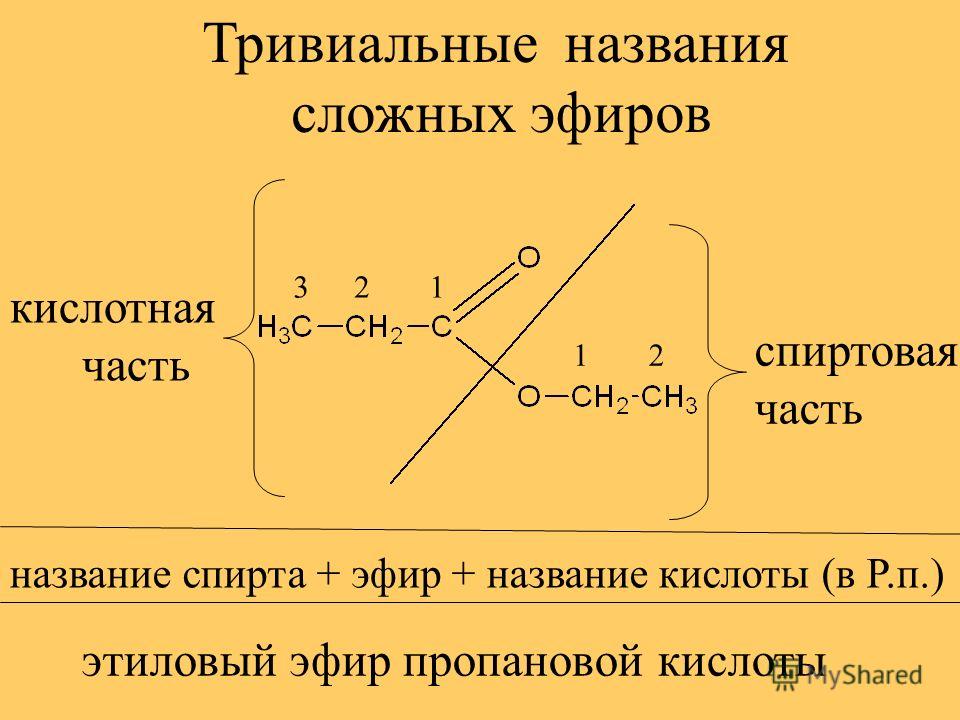
Конспект урока «Сложные эфиры» по химии
Муниципальное бюджетное образовательное учреждение
«Вечерняя (сменная) общеобразовательная школа №1»
Рузаевского муниципального района
Подготовила и провела:
Фоменкова Н.И.
Тема урока: «Сложные эфиры»
Цели урока:
Образовательные — дать учащимся понятие о составе и строении сложных эфиров; отработать умение выделять общие существенные свойства, на основе которых вещества объединяются в класс сложных эфиров, рассмотреть получение и применение сложных эфиров; дать понятие о реакции этерификации.
Развивающие — формирование умений составлять формулы сложных эфиров и называть их, умений составлять уравнения реакций гидролиза и этерификации, развить знания учащихся о закономерностях химических реакций, об условиях смещения химического равновесия; развитие логического мышления, внимания, памяти.
Воспитательные — воспитание познавательной активности, доброже-
лательности, уважения друг к другу, умения слушать и верно оценивать ответы товарищей, воспитание культуры общения, самостоятельности в приобретении знаний.
Оборудование: Образцы сложных эфиров, образцы фруктовых эссенций, карточки для самостоятельной работы учащихся
Тип урока: изучение нового материала.
Метод урока: словесный и сопутствующий ему наглядный.
Дидактическое оснащение: Рудзитис Г.Е., Фельдман Ф.Г., Химия: Органическая химия: Учебник для 10 класса средней школы. М.: Просвещение.
Ход урока
I. Организационной момент:
Сообщение темы и плана урока, постановка цели.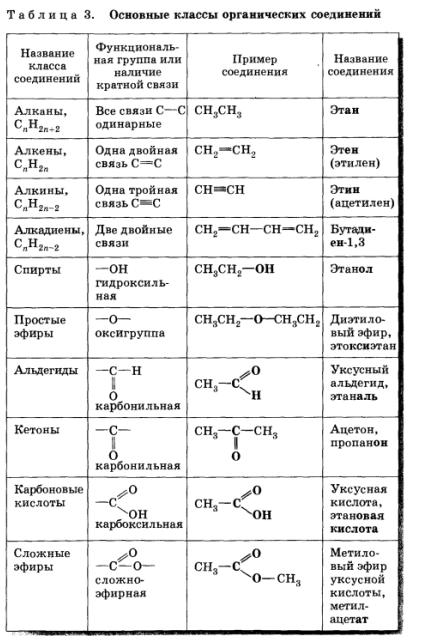
Цель: подготовка обучающихся к восприятию нового материала.
Тема и цели урока сообщаются устно, план урока также сообщается устно.
II. Контроль и актуализация опорных знаний обучающихся:
Цель: выяснение уровня знаний, умений навыков, необходимых для восприятия нового материала.
Предварительная проверка знаний учащихся об кислородосодержащих соединениях в органической химии.
? Перечислите классы органических веществ, содержащих кислород или кислородсодержащие органические вещества. С какими из них вы знакомы? Приведите примеры.
Области применения сложных эфиров
Сложные эфиры применяют для изготовления приятно пахнущих так называемых искусственных фруктовых эссенций.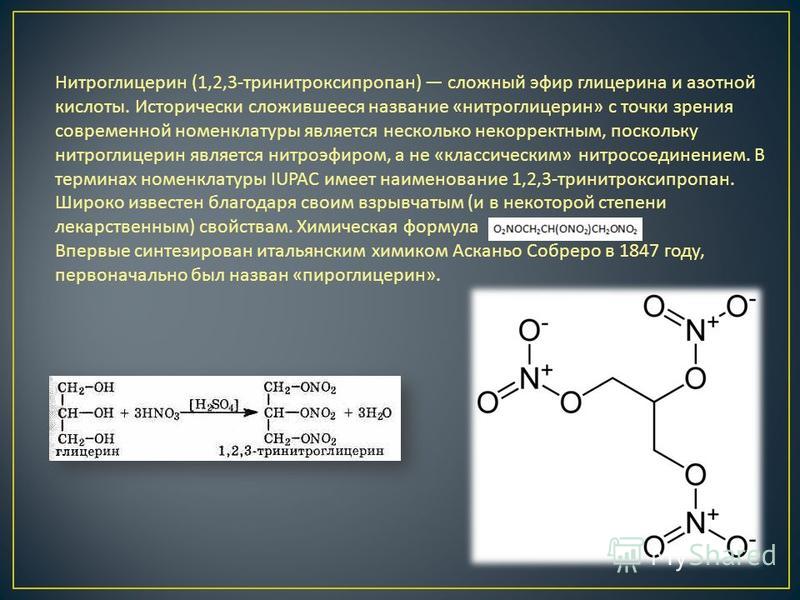
Их широко используют в производстве фруктовых вод и шипучих фруктовых порошков, кондитерских изделий, а также в парфюмерии.
Многие сложные эфиры используются в производстве пластмасс, взрывчатых веществ, лекарственных препаратов, лаков и синтетических волокон – лавсана и т. д.
Сложные эфиры широко распространены в природе, находят применение в технике и различных отраслях промышленности. Они являются хорошими растворителями органических веществ, их плотность меньше плотности воды, и они практически не растворяются в ней.
Схема. Применение сложных эфиров:
Сложные эфиры с относительно небольшой молекулярной массой представляют собой легковоспламеняющиеся жидкости с невысокими температурами кипения, имеют запахи различных фруктов. Их применяют как растворители лаков и красок, ароматизаторы изделий пищевой промышленности.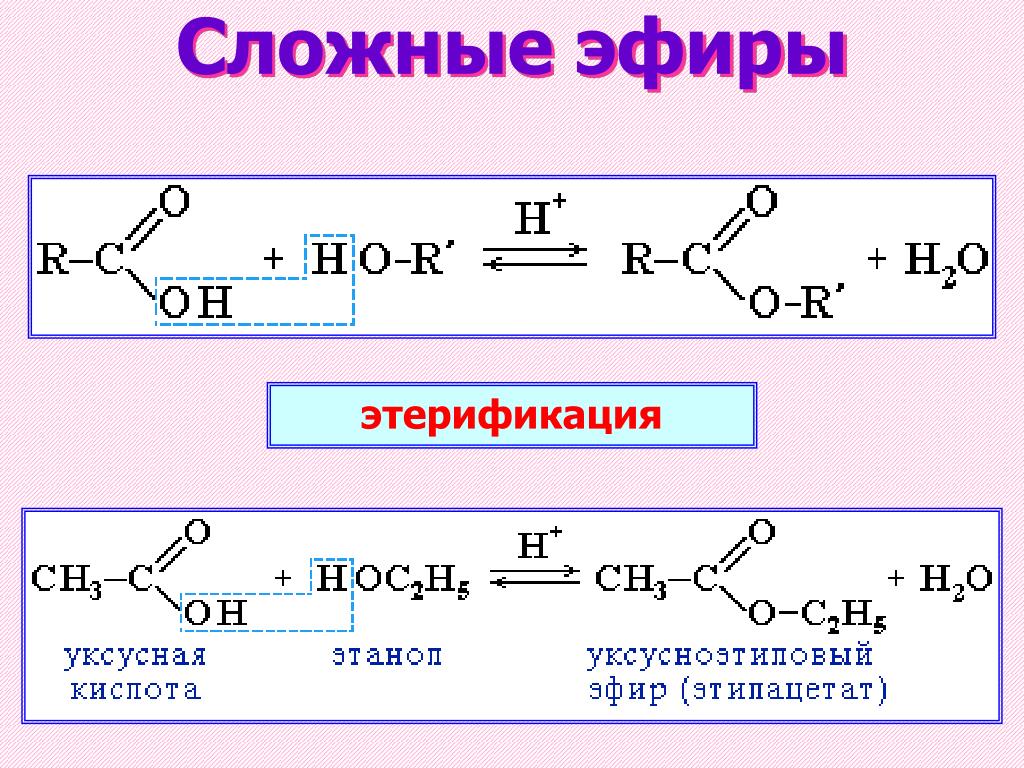
Например, метиловый эфир масляной кислоты имеет запах яблок, этиловый эфир этой кислоты — запах ананасов, изобутиловый эфир уксусной кислоты запах бананов.
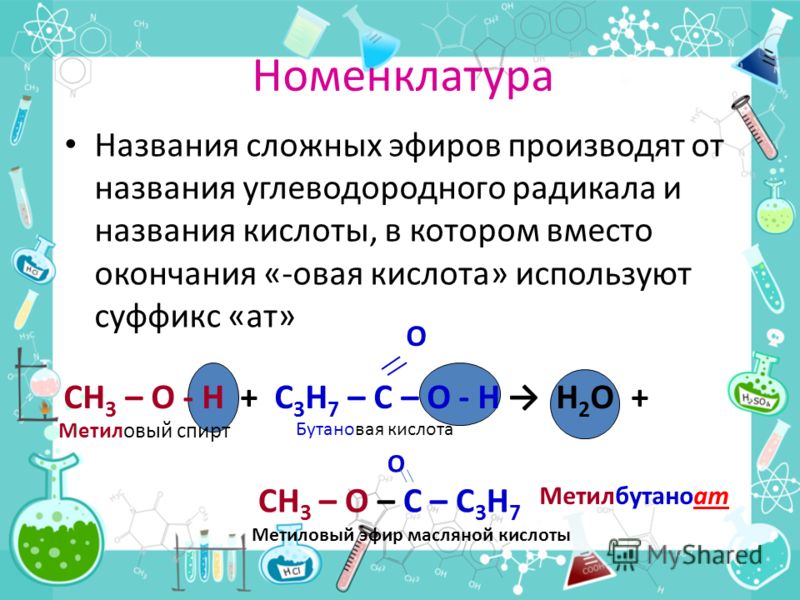
Сложные эфиры высших карбоновых кислот и высших одноосновных спиртов называют во скажи.
Так, пчелиный воск состоит, главным образом, из эфира пальмитиновой кислоты и мирицилового спирта С15Н31СООС31Н63;
Кашалотовый воск —
спермацет – сложный
эфир той же пальмити-
новой кислоты и
цетилового спирта
С15Н31СООС16Н33.
Сложные эфиры часто служат исходными веществами в производстве многих фармацевтических препаратов.
В завершение урока для закрепления изученного материала предлагается осуществить несколько заданий:
Составить уравнения реакций, при помощи которых можно осуществить следующие превращения:
Приведите уравнения реакций получения:
а) этилового эфира муравьиной кислоты;
б) пентилового эфира уксусной кислоты;
в) метилового эфира азотной кислоты.
Итоги урока:
Общая характеристика работы группы, анализ урока: успешность и недостатки, пути их устранения.
Выставление оценок за работу наиболее активных обучающихся.
Задание на дом.
Здесь представлен конспект к уроку на тему «Сложные эфиры», который Вы можете бесплатно скачать на нашем сайте. Предмет конспекта: Химия Также здесь Вы можете найти дополнительные учебные материалы и презентации по данной теме, используя которые,
Предмет конспекта: Химия Также здесь Вы можете найти дополнительные учебные материалы и презентации по данной теме, используя которые,
Вы сможете еще больше заинтересовать аудиторию и преподнести еще больше полезной информации.
органическая химия — Как называется этот сложный эфир?
спросил
Изменено
6 лет, 3 месяца назад
Просмотрено
671 раз
$\begingroup$
Не подскажете название этого эфира? Он представляет собой сложный эфир двух $\ce{C8}$ жирных кислот, связанных между собой молекулой 1,3-бутандиола. хотелось бы сказать ( R )-бутандиол-1,3-диилдигексаноат, но я действительно не уверен.
- органическая химия
- номенклатура
- сложные эфиры
$\endgroup$
$\begingroup$
Согласно действующей версии Номенклатуры органической химии – Рекомендации ИЮПАК и предпочтительные названия 2013 (Синяя книга), названия сложных эфиров обычно образуются путем помещения спиртового компонента перед названием в виде отдельного слова. Отдельные подразделы, касающиеся сложных эфиров из одного спиртового компонента и нескольких кислотных компонентов, гласят следующее:
Отдельные подразделы, касающиеся сложных эфиров из одного спиртового компонента и нескольких кислотных компонентов, гласят следующее:
P-65.6.3.3.3 Полиэфиры, образованные из одного «спиртового» компонента
Сложные эфиры, полученные из одного «полигидроксильного» компонента, называются путем размещения названия «полигидроксильного» компонента, обозначаемого поливалентной органильной группой (алкильной, арильной и т. д.), перед названием(ями) кислотного компонента, обозначаемого названия анионов, полученные от соответствующих кислот (кислот) (…).
P-65.6.3.3.3.1 Когда анионы идентичны, используется мультипликативная номенклатура функционального класса. Имена формируются путем указания мультивалентной группы, мультипликативного префикса и названия умноженного анионного компонента. Мультипликативные приставки «ди», «три» и т. д. используются, когда анионы незамещены; при замене используются префиксы «бис», «трис» и т.
д.
В этом случае полигидроксильный компонент обозначается многовалентной органильной группой «бутан-1,3-диил». Кислотный компонент обозначается названием аниона «гексаноат», которое происходит от соответствующей кислоты «гексановая кислота». Поскольку оба кислотных компонента идентичны и незамещены, мультипликативная приставка «ди» используется в мультипликативной номенклатуре функционального класса. Поэтому предпочтительным названием IUPAC для соединения, указанного в вопросе, является (3 R )-бутан-1,3-диилдигексаноат 9.0037 .
$\endgroup$
0
Зарегистрируйтесь или войдите в систему
Зарегистрируйтесь с помощью Google
Зарегистрироваться через Facebook
Зарегистрируйтесь, используя электронную почту и пароль
Опубликовать как гость
Электронная почта
Требуется, но никогда не отображается
Опубликовать как гость
Электронная почта
Требуется, но не отображается
Нажимая «Опубликовать свой ответ», вы соглашаетесь с нашими условиями обслуживания, политикой конфиденциальности и политикой использования файлов cookie
.
Понимание названий органических соединений
Сложные эфиры
Сложные эфиры являются одним из ряда соединений, известных под общим названием кислотные производные . В них кислотная группа каким-то образом модифицирована. В сложном эфире водород в группе -COOH заменен алкильной группой (или, возможно, какой-либо более сложной углеводородной группой).
Пример 1: Напишите структурную формулу метилпропаноата .
Название сложного эфира состоит из двух частей: часть, которая происходит от кислоты (пропаноат), и часть, которая показывает алкильную группу (метил).
Начните с размышлений о пропановой кислоте — трехуглеродной кислоте без двойных углерод-углеродных связей.
Водород в группе -COOH заменен алкильной группой, в данном случае метильной группой.
Имена сложных эфиров сбивают с толку, потому что они написаны задом наперёд по сравнению с тем, как нарисована структура. Обойти это невозможно — к этому нужно просто привыкнуть!
Обойти это невозможно — к этому нужно просто привыкнуть!
В сокращенной версии эта формула будет записана как CH 3 CH 2 COOCH 3 .
Пример 2: Напишите структурную формулу этилового спирта .
Вероятно, это наиболее часто используемый пример сложного эфира. В его основе лежит этановая кислота (отсюда и этаноат) — 2-углеродная кислота. Водород в группе -COOH заменен этильной группой.
Убедитесь, что вы правильно нарисовали этильную группу. Довольно распространенная ошибка — пытаться присоединиться к CH 9.0115 3 группа к кислороду. Если вы посчитаете связи, то обнаружите, что и углерод CH 3 , и углерод CH 2 имеют неправильное количество связей.
Ацилхлориды (хлорангидриды)
Ацилхлорид является еще одним производным кислоты. В этом случае группа -ОН кислоты заменяется на -Cl. Все ацилхлориды содержат группу -COCl:
Пример: Напишите структурную формулу числа 9.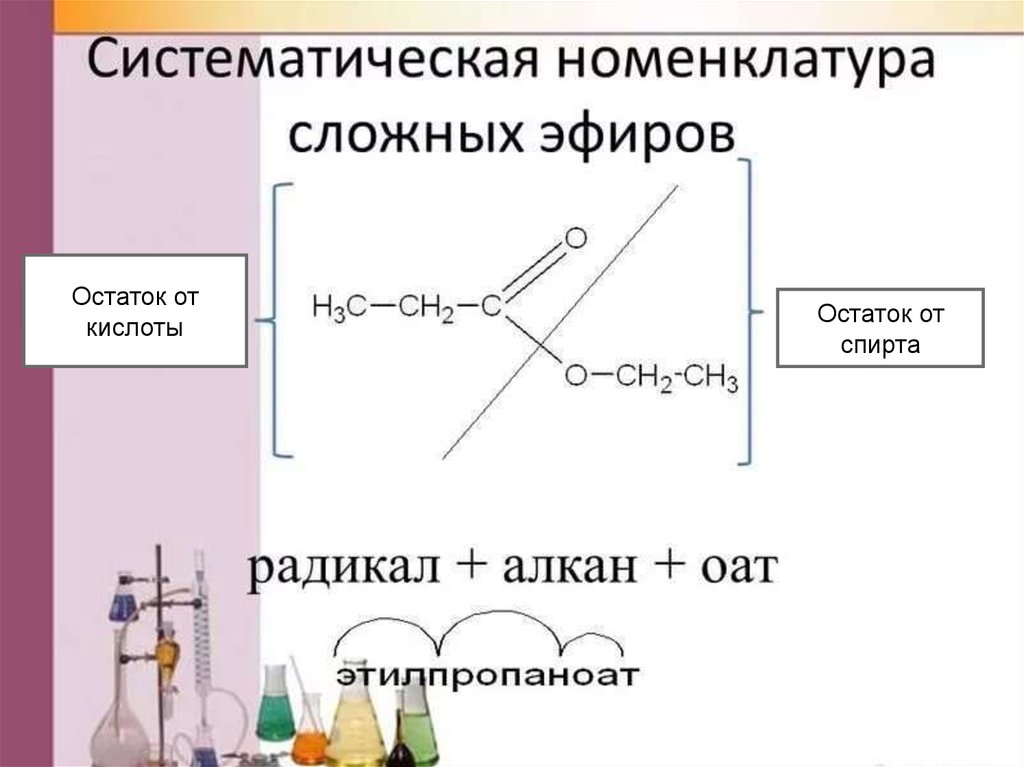 0085 этанолилхлорид .
0085 этанолилхлорид .
Ацилхлориды обозначаются окончанием ойлхлорид . Таким образом, этанолилхлорид основан на 2-углеродной цепи без углерод-углеродных двойных связей и группе -COCl. Углерод в этой группе считается частью цепи. В более длинной цепи с присоединенными боковыми группами углероду -COCl отводится положение номер 1.
ангидриды кислот
Еще одно производное кислоты! Кислотный ангидрид — это то, что получится, если обезвожить кислоту, то есть удалить из нее воду.
Пример: Напишите структурную формулу пропанового ангидрида .
Легче всего их вычислить, записав на клочке бумаги следующим образом:
Изобразите две молекулы кислоты, расположенные так, чтобы группы -ОН находились рядом друг с другом. Выделите молекулу воды, а затем соедините то, что осталось. В этом случае, поскольку вам нужен пропановый ангидрид, вы рисуете две молекулы пропановой кислоты.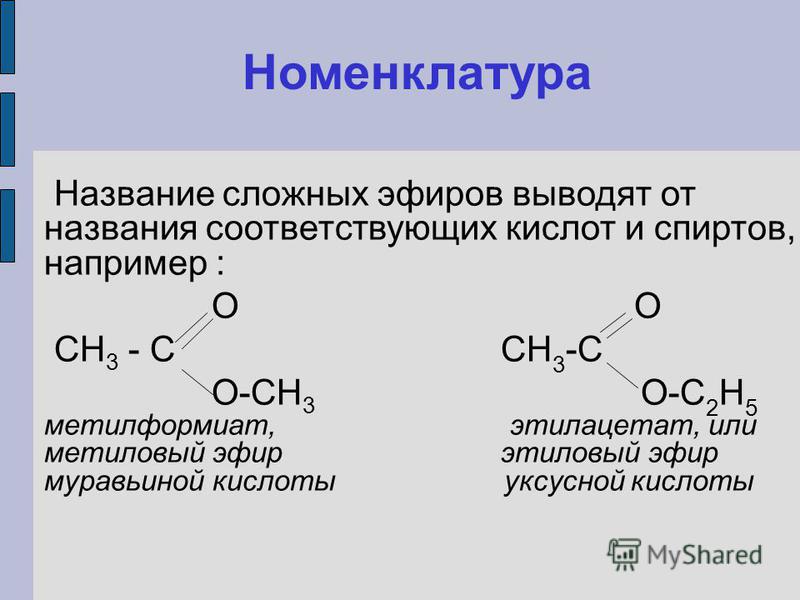
Амиды
Еще одно производное кислоты! Амиды содержат группу -CONH 2 , где -ОН кислоты заменен на -NH 2 .
Пример: Напишите структурную формулу пропанамида .
Основан на цепочке из 3 атомов углерода без двойных углерод-углеродных связей. В конце цепи находится группа -CONH 2 . Углерод в этой группе считается частью цепи.
Нитрилы
Нитрилы содержат группу -CN и раньше назывались цианидами.
Пример 1: Напишите структурную формулу этанитрила .
Название показывает цепочку из 2 атомов углерода без двойной углерод-углеродной связи. нитрил показывает группу -CN на конце цепи. Как и в предыдущих примерах с кислотами и их производными, не забывайте, что углерод в группе -CN считается частью цепи.
Старое название для этого было бы метилцианид .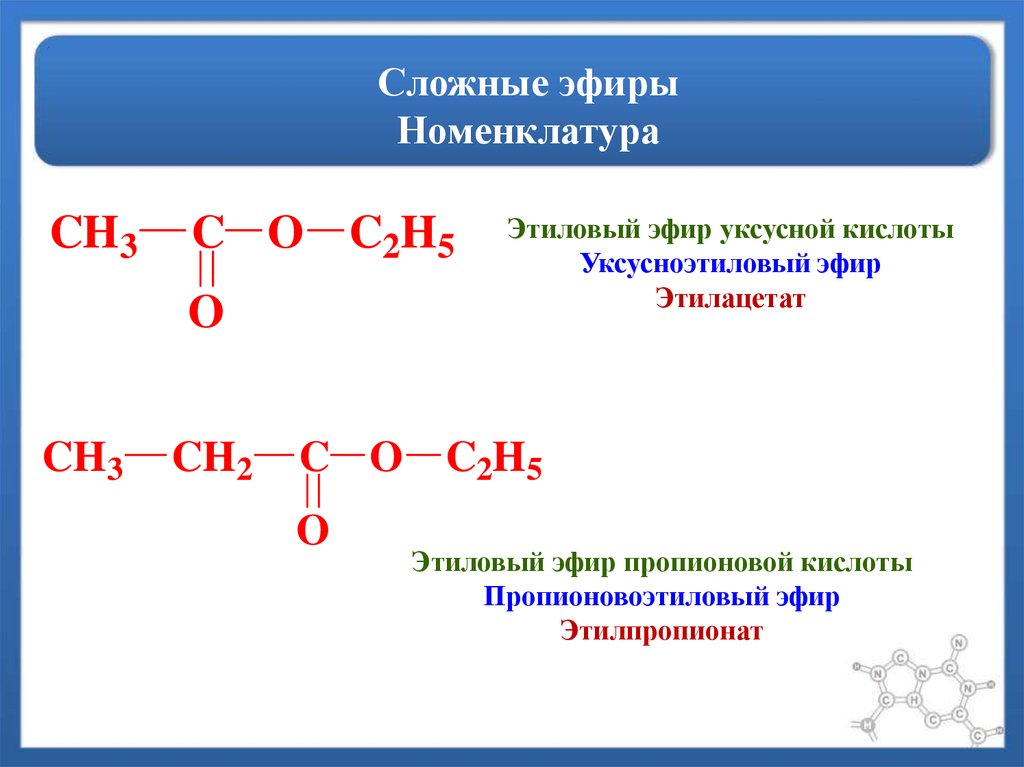 Вы можете подумать, что так проще, но как только цепочка усложняется, она не работает — как показывает следующий пример.
Вы можете подумать, что так проще, но как только цепочка усложняется, она не работает — как показывает следующий пример.
Пример 2: Напишите структурную формулу 2-гидроксипропаннитрила .
Здесь у нас есть цепочка из 3 атомов углерода, нет двойных углерод-углеродных связей и есть группа -CN на конце цепи. Углерод в группе -CN считается углеродом номер 1. На углероде номер 2 находится группа -ОН ( гидрокси ). Обратите внимание, что вы не можете использовать окончание ol , потому что у вас уже есть окончание нитрил .
Первичные амины
Первичный амин содержит группу -NH 2 , присоединенную к углеводородной цепи или кольцу. Вы можете думать об аминах в целом как о производных от аммиака, NH 3 . В первичном амине один из атомов водорода заменен углеводородной группой.
Пример 1: Напишите структурную формулу этиламина .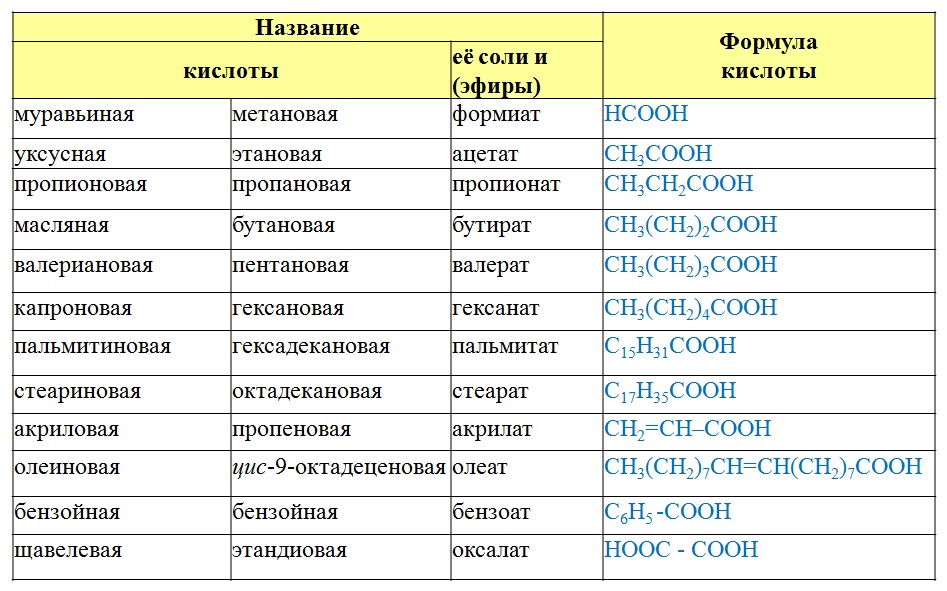
В этом случае этильная группа присоединена к группе -NH 2 .
Это название (этиламин) подходит, если у вас есть только короткая цепь, где нет никакой двусмысленности относительно того, где находится группа -NH 2 . Но предположим, что у вас есть цепочка из 3 атомов углерода — в этом случае группа -NH 2 может находиться на конце атома углерода или на среднем атоме углерода. Как обойти эту проблему, показано в следующем примере.
Пример 2: Напишите структурную формулу 2-аминопропана .
Название показывает цепочку из 3 атомов углерода с аминогруппой, присоединенной ко второму атому углерода. амино показывает группу -NH 2 .
Этиламин (пример 1 выше) с таким же успехом можно было бы назвать аминоэтаном.
Вторичные и третичные амины
Скорее всего, вы встретите только простые примеры.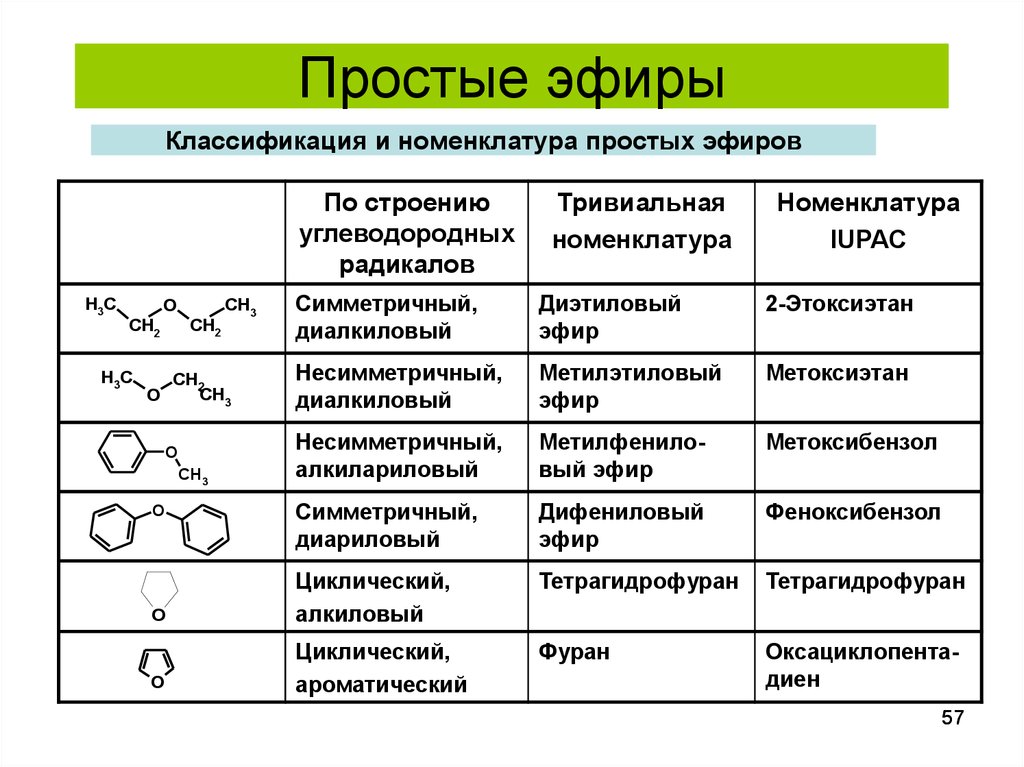 Во вторичном амине два атома водорода в молекуле аммиака заменены углеводородными группами. В третичном амине заменены все три атома водорода.
Во вторичном амине два атома водорода в молекуле аммиака заменены углеводородными группами. В третичном амине заменены все три атома водорода.
Пример 1: Напишите структурную формулу диметиламина .
В этом случае два атома водорода в аммиаке заменены метильными группами.
Пример 2: Напишите структурную формулу триметиламина .
Здесь все три атома водорода в аммиаке заменены метильными группами.
Аминокислоты
Аминокислота содержит аминогруппу -NH 2 и карбоксильную группу -COOH в одной и той же молекуле. Как и во всех кислотах, углеродная цепь пронумерована так, что углерод в группе -COOH считается номером 1.
Пример: Напишите структурную формулу 2-аминопропановой кислоты .
Имеет цепочку из 3 атомов углерода без двойных углерод-углеродных связей.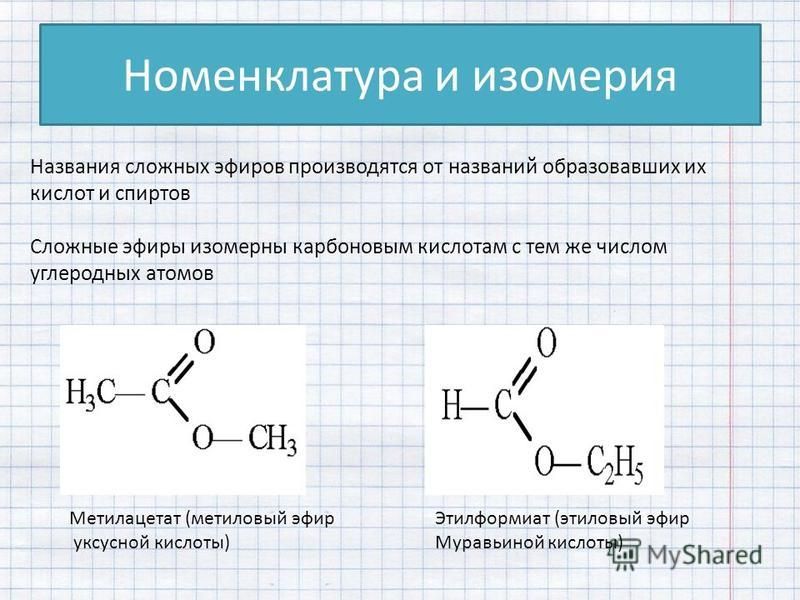


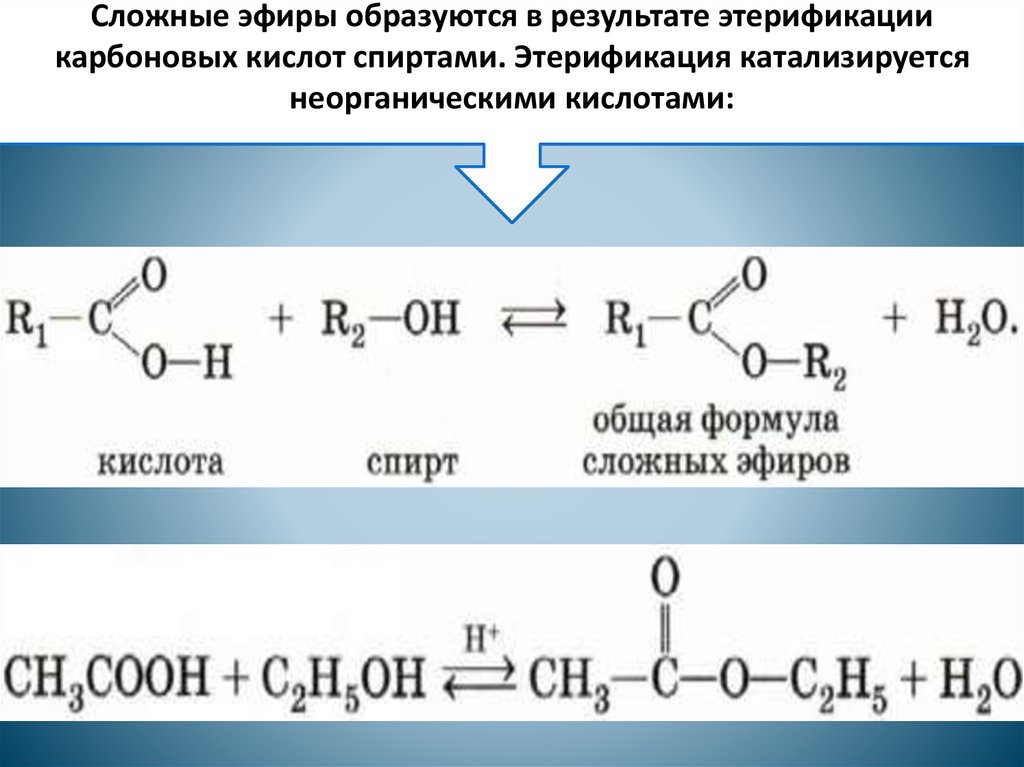 Приятные ароматы цветов, плодов и ягод в значительной степени обусловлены присутствующими в них сложными эфирами.
Приятные ароматы цветов, плодов и ягод в значительной степени обусловлены присутствующими в них сложными эфирами.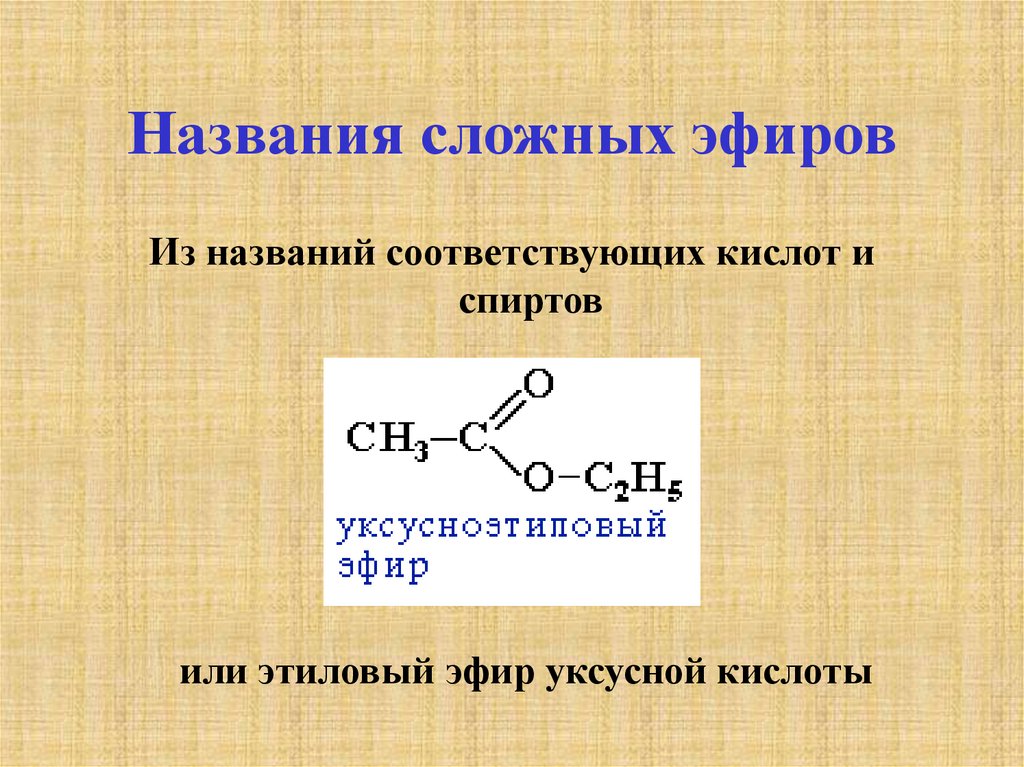 д.
д.