Содержание
Задание 11 ЕГЭ по химии 2023: теория и практика
Русский язык
Математика (профиль)
Математика (база)
Обществознание
История
Биология
Физика
Химия
Английский язык
Информатика
Литература
Задание 1
Задание 2
Задание 3
Задание 4
Задание 5
Задание 6
Задание 7
Задание 8
Задание 9
Задание 10
Задание 11
Задание 12
Задание 13
Задание 14
Задание 15
Задание 16
Задание 17
Задание 18
Задание 19
Задание 20
Задание 21
Задание 22
Задание 23
Задание 24
Задание 25
Задание 26
Задание 27
Задание 28
Задание 29
Задание 30
Задание 31
Задание 32
Задание 33
Задание 34
За это задание ты можешь получить 1 балл. На решение дается около 2 минут. Уровень сложности: базовый.
На решение дается около 2 минут. Уровень сложности: базовый.
Средний процент выполнения: 51.7%
Ответом к заданию 11 по химии может быть последовательность цифр, чисел или слов. Порядок записи имеет значение.
Разбор сложных заданий в тг-канале
Посмотреть
Задачи для практики
Задача 1
Из предложенного перечня выберите два класса веществ, в молекулах которых присутствует функциональная группа
- спирты
- кетоны
- простые эфиры
- фенолы
- пептиды
Запишите в поле ответа номера выбранных классов веществ.
Решение
Функциональная группа -С(О)- (карбонильная группа) присутствует в кетонах в составе кетогруппы, в альдегидах в составе альдегидной группы -СНО и в кислотах в составе карбоксильной группы -СООН. Среди предложенных классов есть кетоны а также пептиды — производные аминокислот, тоже несущие карбонильную группу — в составе пептидной связи -С(О)-NH-.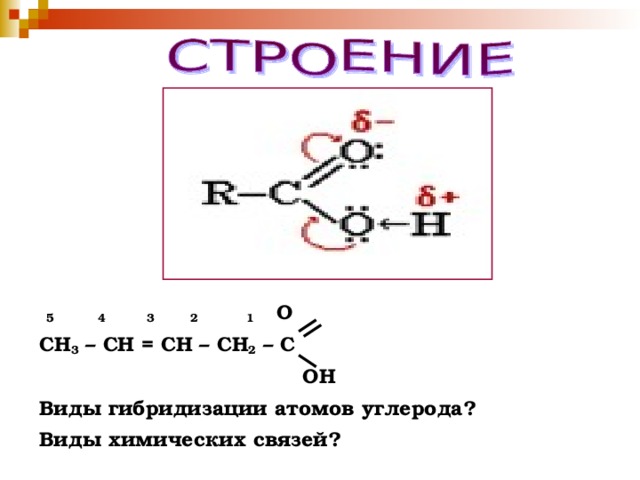 2$-гибридизацию.
2$-гибридизацию.
Ответ: 12
Показать решение
Бесплатный интенсив
Задача 4
Из предложенного перечня выберите два ряда веществ, которые являются гомологами.
- $CH_3NO_2$ и $CH_3NH_2$
- $CH_3OH$ и $CH_3COOH$
- $CH_3CH_2CH_2OH$ и $CH_3OH$
- $CH_3Cl$ и $CH_3Br$
- $CH_3CHO$ и $C_2H_5CHO$
Запишите в поле ответа номера выбранных рядов веществ.
Решение
Гомологическим рядом называют ряд веществ, которые имеют общую формулу, похожее строение, закономерно изменяющиеся физические свойства, общие способы получения и общие химические свойства и отличаются по составу на одну или несколько групп $CH_2$, которая называется гомологической разностью. Гомологи — вещества, принадлежащие к одному гомологическому ряду.
1) $CH_3NO_2$ — нитрометан, класс нитросоединений; $CH_3NH_2$ — метиламин (аминометан), класс предельных первичных аминов. Вещества принадлежат к разным классам.
Вещества принадлежат к разным классам.
2) $CH_3OH$ — метанол (метиловый спирт), класс предельных одноатомных спиртов; $CH_3COOH$ — уксусная кислота. Вещества принадлежат к разным классам.
3) $CH_3CH_2CH_2OH$ — пропанол-1, $CH_3OH$ — метанол. Оба вещества относятся к классу спиртов, отличаются по составу на две группы $–CH_2$, имеют похожее строение (линейная цепь углеродных атомов, группа –OH находится у крайнего атома углерода) и общую формулу $C_{n}H_{2n+2}O (C_{n}H_{2n+1}OH$), т. е. являются гомологами.
4) $CH_3Cl$ — хлорметан и $CH_3Br$ — бромметан. Вещества отличаются качественным составом.
5) $CH_3CHO$ — этаналь, класс альдегидов предельного ряда; $C_2H_5CHO$ — пропаналь, класс альдегидов предельного ряда. Оба вещества относятся к классу альдегидов, отличаются по составу на группу $–CH_2$, имеют похожее строение (линейная цепь углеродных атомов) и общую формулу $C_{n}H_{2n}O$, т. е. являются гомологами.
Ответ: 35
Показать решение
Бесплатный интенсив
Задача 5
Из предложенного перечня выберите два вещества, в молекулах которых имеется две π-связи.
- акриловая кислота
- пропен
- бутан
- бутен
- ацетилен
Запишите в поле ответа номера выбранных веществ.
Решение
Двойная связь состоит из одной σ-связи и одной π-связи.
Тройная связь состоит из одной σ-связи и двух π-связей.
1) Акриловая (пропеновая) кислота $CH_2=CH–C(O)–OH$. В молекуле имеется одна двойная C=C связь и одна двойная C=O связь. Ответ правильный.
2) Пропен $CH_2=CH–CH_3$. В молекуле имеется одна двойная С=С связь. Ответ неверный.
3) Бутан $CH_3–CH_2–CH_2–CH_3$. В молекуле нет двойных С=С связей. Ответ неверный.
4) Бутен, $CH_2=CH–CH_2–CH_3$ или $CH_3–CH=CH–CH_3$. В молекуле любого из бутенов имеется только одна двойная C=C связь. Ответ неверный.
5) Ацетилен, или этин, H–C≡C–H. В молекуле имеется тройная C≡C связь. Ответ правильный.
Ответ: 15
Показать решение
Бесплатный интенсив
Задача 6
Из предложенного перечня выберите два вещества, которые относятся к тем же гомологическим рядам, что и вещества, имеющие молекулярную формулу $С_5Н_{10}$.
- метан
- этилен
- бензол
- циклопропан
- ацетилен
Запишите в поле ответа номера выбранных веществ.
Решение
Общую формулу гомологического ряда $C_nH_{2n}$ имеют алкены и циклоалканы. В предложенном списке веществ есть алкен – этилен, и циклоалкан – циклопропан.
Ответ: 24
Показать решение
Бесплатный интенсив
Задача 7
Из предложенного перечня выберите два вещества, которые являются изомерами 2-метилбутана.
- $CH_3–CH_2–CH_2–CH_2–CH_3$
- $CH_3–CH_2–CH_2–CH_3$
Запишите в поле ответа номера выбранных веществ.
Решение
Изомеры — вещества, имеющие одинаковый состав, то есть одинаковую молекулярную формулу, но разное строение. 2-метилбутан $СН_3-СН(СН_3)-СН_2-СН_3$ имеет молекулярную формулу $С_5Н_{12}$. Такую же молекулярную формулу имеют все алканы с пятью атомами углерода, в том числе представленный под номером 1 н-пентан и представленный под номером 2 1,2-диметилпропан.
Ответ: 12
Показать решение
Бесплатный интенсив
Задача 8
Из предложенного перечня выберите два вещества, которые являются структурными изомерами пентена-1.
- циклопентан
- пентадиен-1,3
- 2-метилбутан
- 2-метилбутен-2
- 3-метилбутин-1
Запишите в поле ответа номера выбранных веществ.
Решение
Пентен-1 – алкен, то есть имеет 5 атомов углерода и 10 атомов водорода, его изомерами являются циклопентан, который также теряет два атома водорода из-за кольцевой связи, а также 2-метилбутен-2, который теряет 2 атома водорода в той же двойной связи.
Ответ: 14
Показать решение
Бесплатный интенсив
Задача 9
Из предложенного перечня выберите две пары веществ, которые являются гомологами.
- этилен и метан
- пропен и этен
- циклобутан и бутан
- пропан и бутан
- этин и этен
Запишите в поле ответа номера выбранных пар веществ.
Решение
Гомологи — вещества, принадлежащие к одному классу. В первой паре представлен алкен и алкан, во второй — два алкена, в третьей — циклоалкан и алкан, в четвёртой — два алкана, в пятой — алкин и алкен. Таким образом, гомологи представлены в парах номер 2 и 4.
Ответ: 24
Показать решение
Бесплатный интенсив
Задача 10
Из предложенного перечня выберите два класса органических веществ, к которым может относиться вещество, формула которого $C_4H_{10}O$.
- спирты
- альдегиды
- простые эфиры
- сложные эфиры
- кетоны
Запишите в поле ответа номера выбранных классов веществ.
Решение
Общей формулой гомологического ряда спиртов является $С_{n}H_{2n+1}ОH$, что как раз соответствует данному веществу (его можно переписать как $C_{4}H_{9}OH$). Общей формулой гомологического ряда простых эфиров является $С_{n}H_{2n+2}О$, что также соответствует данному веществу.
Ответ: 13
Показать решение
Бесплатный интенсив
Задача 11
Из предложенного перечня выберите два вещества, между молекулами которых образуются водородные связи.
- этанол
- этан
- этаналь
- ацетон
- этановая кислота
Запишите в поле ответа номера выбранных веществ.
Решение
Водородные связи образуются между молекулами веществ, содержащих атом водорода непосредственно связанным с атомом кислорода. Из органических веществ это спирты, фенолы, карбоновые кислоты, аминокислоты. Среди представленных веществ есть спирт — этанол и карбоновая кислота — этановая.
Ответ: 15
Показать решение
Бесплатный интенсив
Задача 12
Из предложенного перечня выберите два вещества, которые имеют систему сопряжённых связей.
- фенол
- бутадиен-1,3
- циклогексен
- 2-метилбутан
- бутин-1
Запишите в поле ответа номера выбранных веществ.
Решение
Систему сопряжённых связей имеют, прежде всего, сопряжённые диены (две двойных связи разделены одинарной). Но помимо них сопряжённые двойные связи формально присутствуют в бензольном кольце, что наглядно отражает формула Кекуле. Среди предложенных веществ есть сопряжённый диен — бутадиен-1,3 $CH_2=CH-CH=CH_2$ и соединение, имеющее в составе бензольное кольцо — фенол $С_6Н_5ОН$.
Ответ: 12
Показать решение
Бесплатный интенсив
Задача 13
Из предложенного перечня выберите две пары веществ, каждое из которых содержит функциональную группу –ОН.
- фенол и рибоза
- диэтиловый эфир и глюкоза
- сахароза и формальдегид
- фенол и толуол
- пропанол и крезол
Запишите в поле ответа номера выбранных пар веществ.
Решение
Функциональную группу –ОН содержат спирты, фенолы и углеводы. Из предложенных пар веществ эту группу имеют фенол и рибоза (углевод) — номер 1, пропанол (спирт) и крезол (метилфенол).
Ответ: 15
Показать решение
Бесплатный интенсив
Задача 14
Из предложенного перечня выберите два вещества, которые имеют общую формулу СnH2n.
- бензол
- циклогексан
- гексан
- гексен
- гексин
Запишите в поле ответа номера выбранных веществ.
Решение
Общая формула $С_nH_{2n}$ соответствует классу алкенов, а также их изомеров — циклоалканов. Среди предложенных веществ есть циклоалкан — циклогексан ($С_6Н_{12}$) и алкен — гексен ($С_6Н_{12}$).
Ответ: 24
Показать решение
Бесплатный интенсив
Задача 15
Из предложенного перечня выберите два вещества, которые относятся к кетонам.
- формалин
- ацетон
- этилацетат
- бутанон
- фруктоза
Запишите в поле ответа номера выбранных веществ.
Решение
О принадлежности к классу кетонов в названии вещества свидетельствует суффикс -он-. По этому принципу выбираем бутанон, а ацетон — это тривиальное название диметилкетона (пропанона).
Ответ: 24
Показать решение
Бесплатный интенсив
Задача 16
Из предложенного перечня выберите два вещества, которые являются гомологами глицина.
- $CH_3CH_2CONH_2$
- $CH_3CH(NH_2)COOH$
- $CH_3CH_2COOH$
- $CH_3CH_2CH(NH_2)COOH$
- $CH_3CH_2NH_2$
Запишите в поле ответа номера выбранных веществ.
Решение
Гомологи — вещества, относящиеся к одному классу. Глицин $NH_2-СН_2-СООН$ — аминокислота. К этому же классу относятся вещества, имеющие в составе карбоксильну группу -СООН и аминогруппу $-NH_2$. Подходят соединения под номерами 2 и 4.
Подходят соединения под номерами 2 и 4.
Ответ: 24
Показать решение
Бесплатный интенсив
Задача 17
Из предложенного перечня выберите два вещества, которые являются гомологами бензола.
- циклогексан
- толуол
- ацетилен
- винилбензол
- фенилэтан
Запишите в поле ответа номера выбранных веществ.
Решение
Гомологи — вещества, принадлежащие одному классу соединений. Безол — ароматический углеводород, то есть содержит бензольное кольцо и состоит только из углерода и водорода. Его гомологами являются толуол (метилбензол) и фенилэтан. Винилбензол не является гомологом, так как содержит непредельный радикал.
Ответ: 25
Показать решение
Бесплатный интенсив
Показать еще
Для доступа к решениям необходимо включить уведомления от группы Турбо в вк —
это займет буквально 10 секунд.
Никакого спама, только самое важное и полезное для тебя. Ты всегда можешь запретить
уведомления.
Включить уведомления
Бесплатный интенсив по химии
3 огненных вебинара, домашние задания, беседа курса, личный кабинет, связь с преподавателем и многое
другое.
Курс стартует 8 ноября.
Бесплатный интенсив
Для скачивания — Кафедра химии
- Главная
- Университет
- Для скачивания
- Кафедра химии
Лекция. Растворы неэлектролитов
Размер файла:
638.79 kB
Автор:
Апанович, З.В.
Дата:
26.12.2016 12:03
Растворы неэлектролитов. Лекция по курсу «Общая химия» для студентов инженерно-технологического факультета / З.В. Апанович. – Гродно : ГГАУ , 2016. – 33 с.
Учебно-методическое пособие включает лекцию по теме «Растворы неэлектролитов» курса «Общая химия» и предназначено для контролируемой самостоятельной работы студентов инженерно – технологического факультета. Использование пособия, в котором рассмотрены важнейшие теоретические вопросы в доступной и сжатой форме, позволит студентам быстрее и эффективнее изучить материал.
Использование пособия, в котором рассмотрены важнейшие теоретические вопросы в доступной и сжатой форме, позволит студентам быстрее и эффективнее изучить материал.
Скачать
Лекция. Окислительно-восстановительные реакции
Размер файла:
609.98 kB
Автор:
Апанович, З.В.
Дата:
26.12.2016 12:03
Окислительно – восстановительные реакции. Лекция по курсу «Общая химия » для студентов инженерно-технологического факультета / З.В. Апанович. – Гродно : ГГАУ, 2016. – 31 с.
Учебно-методическое пособие включает лекцию по теме «Окислительно – восстановительные реакции» и предназначено для контролируемой самостоятельной работы студентов инженерно–технологического факультета. Использование такого пособия, в котором рассмотрены важнейшие вопросы в доступной и сжатой форме, позволит студентам быстрее и эффективнее изучить материал.
Скачать
Лекция. Комплексные соединения
Размер файла:
531.46 kB
Автор:
Апанович, З.В.
Дата:
26.12.2016 12:03
Лекция «Комплексные соединения» по курсу «Общая химия» для студентов инженерно-технологического факультета / З.В. Апанович. – Гродно : ГГАУ, 2016. – 26 с.
Учебно-методическое пособие включает лекцию по теме «Комплексные соединения» курса «Общая химия». Комплексные соединения играют важную роль в природе и технике, прежде всего, это ферментативные и фотохимические процессы, перенос кислорода в биологических системах, тонкая технология редких металлов, каталитические реакции и т.д. Координационные свойства проявляются всеми элементами периодической системы.
Скачать
Лекция. Кинетика химических реакций. Химическое равновесие
Размер файла:
768.32 kB
Автор:
Апанович, З.В.
Дата:
26.12.2016 12:03
Кинетика химических реакций. Химическое равновесие. Лекции по курсу «Общая химия» для студентов инженерно-технологического факультета / З.В. Апанович. – Гродно : ГГАУ, 2016. – 44 с.
Учебно-методическое пособие включает лекции по отдельным темам курса «Общая химия» и предназначено для контролируемой самостоятельной работы студентов инженерно – технологического факультета.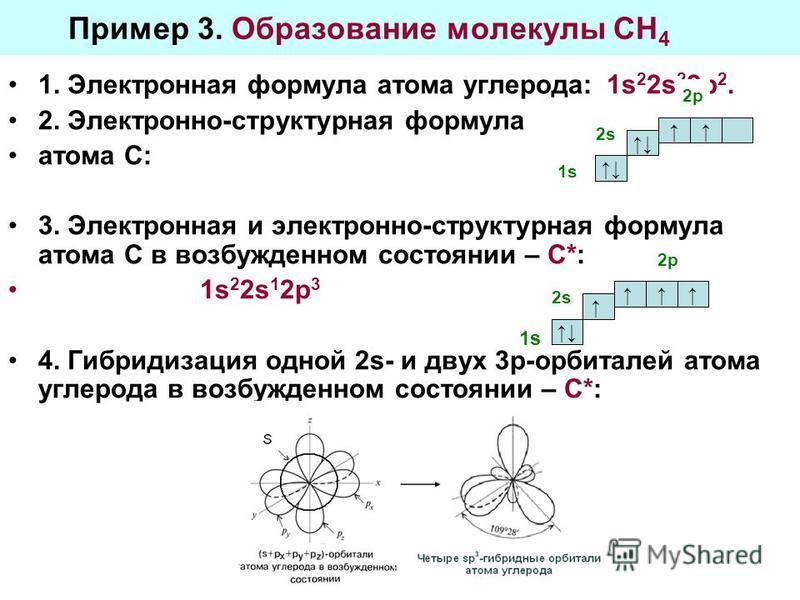 Использование таких пособий, в которых рассмотрены важнейшие теоретические вопросы в доступной и сжатой форме, позволит студентам быстрее и эффективнее изучить материал.
Использование таких пособий, в которых рассмотрены важнейшие теоретические вопросы в доступной и сжатой форме, позволит студентам быстрее и эффективнее изучить материал.
Скачать
Предэкзаменационные тесты по органической и биологической ХИМИИ
Размер файла:
1.30 MB
Автор:
Макарчиков А.Ф., Колос И.К.
Дата:
26.12.2016 12:02
Предэкзаменационные тесты по органической и биоло-гической химии для студентов биотехнологического факультета / А.Ф. Макарчиков, И.К. Колос – Гродно: ГГАУ, 2016. – 205 с.
В пособии приведен перечень вопросов для проведения предэкзаменационного тестирования студентов, обучающихся на биотехнологическом факультете, по предмету «Химия (органическая и биологическая)»
Скачать
Лекция. Электролиз. Коррозия металлов и методы защиты металлов от коррозии
Размер файла:
758.87 kB
Автор:
Апанович, З.В.
Дата:
26.12.2016 12:02
Электролиз. Коррозия металлов и методы защиты металлов от коррозии. Лекция по курсу «Общая химия» для студентов инженерно-технологического факультета / З.В. Апанович. – Гродно : ГГАУ, 2016. – 31 с.
Лекция по курсу «Общая химия» для студентов инженерно-технологического факультета / З.В. Апанович. – Гродно : ГГАУ, 2016. – 31 с.
Учебно-методическое пособие включает лекции по отдельным темам курса «Общая химия» и предназначено для контролируемой самостоятельной работы студентов инженерно – технологического факультета. Использование таких пособий, в которых рассмотрены важнейшие теоретические вопросы в доступной и сжатой форме, позволит студентам быстрее и эффективнее изучить материал.
Скачать
Лекция. Энергетика химических процессов.
Размер файла:
604.00 kB
Автор:
Апанович, З.В.
Дата:
26.12.2016 12:02
Энергетика химических процессов. Лекция по курсу «Общая химия» для студентов инженерно-технологического факультета / З.В. Апанович. – Гродно : ГГАУ, 2016. – 25 с.
Учебно-методическое пособие включает лекцию по теме «Энергетика химических процессов» и предназначено для контролируемой самостоятельной работы студентов инженерно – технологического факультета. Использование такого пособия, в котором рассмотрены важнейшие вопросы в доступной и сжатой форме, позволит студентам быстрее и эффективнее изучить материал.
Использование такого пособия, в котором рассмотрены важнейшие вопросы в доступной и сжатой форме, позволит студентам быстрее и эффективнее изучить материал.
Скачать
Лекция. Строение атомов элементов
Размер файла:
789.90 kB
Автор:
Апанович, З.В.
Дата:
26.12.2016 12:02
Строение атомов элементов. Лекция по курсу «Общая химия» для студентов инженерно-технологического факультета / З.В. Апанович. – Гродно : ГГАУ , 2016. – 23 с.
Учебно-методическое пособие включает лекцию по теме «Строение атомов элементов» курса «Общая химия» и предназначено для контролируемой самостоятельной работы студентов инженерно – технологического факультета. Использование пособия, в котором рассмотрены важнейшие теоретические вопросы в доступной и сжатой форме, позволит студентам быстрее и эффективнее изучить материал.
Скачать
Лекция. Основные понятия и законы химии
Размер файла:
675.23 kB
Автор:
Апанович, З.В.
Дата:
26. 12.2016 12:03
12.2016 12:03
Основные понятия и законы химии. Лекция по курсу «Общая химия» для студентов инженерно-технологического факультета / З.В. Апанович. – Гродно : ГГАУ, 2016. – 30 с.
Учебно-методическое пособие включает лекцию по теме «Основные понятия и законы химии» курса «Общая химия» и предназначено для контролируемой самостоятельной работы студентов инженерно – технологического факультета. Использование студентами распечатки лекционной темы значительно сэкономит время для понимания материала, излагаемого лектором, и конспектирования.
Скачать
Предэкзаменационные тесты по химии
Размер файла:
813.02 kB
Автор:
Макарчиков А.Ф., Колос И.К.
Дата:
14.11.2016 11:47
Предэкзаменационные тесты по химии для студентов, обучающихся на агробиологических специальностях / А.Ф. Макарчиков, И.К. Колос – Гродно: ГГАУ, 2016. – 201 с.
В пособии приведен перечень вопросов для проведения предэкзаменационного тестирования студентов, обучающихся на агробиологических специальностях, по предмету «Химия».
Скачать
Методическое пособие для лабораторных работ по аналитической химии
Размер файла:
544.41 kB
Автор:
Апанович З.В., Тараненко Т.В., Томашева Е.В., Кулеш И.В., Цветницкая Э.В.
Дата:
28.12.2015 12:22
В пособие излагается материал по аналитической химии в объеме соответствующих программ по специальностям: «Ветеринарная медицина», «Аграномия», «Биотехналогия». Содержатся методические указания по технике выполнения лабораторных работ по качественному и количественному анализу.
Скачать
Комментарии для работы с рабочими тетрадями по химии элементов
Размер файла:
655.75 kB
Дата:
28.12.2015 12:22
Комментарии для работы с рабочими тетрадями по химии элементов / З.В. Апанович, Ю.А. Лукашенко.
Учебно-методическое пособие включает лекции по отдельным темам курса «Неорганическая химия» и предназначено для контролируемой самостоятельной работы студентов инженерно – технологического факультета, для которых введен отдельный курс по химии элементов, а также может быть использовано студентами других факультетов.
Скачать
Практикум по физической химии
Размер файла:
1.03 MB
Дата:
01.04.2013 04:24
Учебно-методическое пособие (для проведения лабораторных занятий) для студентов инженерно-технического факультета
Практикум по физической химии: учеб.-мет. пособие / О. И. Валентюкевич.- Гродно: ГГАУ, 2008 – 88с.
Данное пособие предназначено для студентов технологических специальностей аграрного университета. Целью данного пособия является оказание помощи в изучении теоретического материала, а также выработка навыков экспериментальной работы.
Скачать
Коллоидная химия
Размер файла:
834.37 kB
Дата:
01.04.2013 04:09
Учебно-методическое пособие (для проведения лабораторных занятий) для студентов инженерно-технического факультета
К-60 Практикум по физической химии: учеб.-мет. пособие / И. В. Кулеш, О. И. Валентюкевич.- Гродно: ГГАУ, 2013 – 94с.
Данное пособие предназначено для студентов технологических специальностей аграрного университета. Целью данного пособия является оказание помощи в изучении теоретического материала, а также выработка навыков экспериментальной работы.
Целью данного пособия является оказание помощи в изучении теоретического материала, а также выработка навыков экспериментальной работы.
Скачать
Курс лекций по дисциплине «Неорганическая химия»
Размер файла:
1.33 MB
Дата:
28.12.2015 12:22
Лекции по курсу «Неорганическая химия »для студентов инженерно – технологического факультета / З.В. Апанович.
Скачать
Рабочая тетрадь и методические указания по неорганической химии
Размер файла:
701.32 kB
Дата:
28.12.2015 12:23
Рабочая тетрадь и методические указания по неорганической химии. Для студентов технологических специальностей / З.В. Апанович.
Скачать
Ионные равновесия и обменные реакции в растворах электролитов
Скачать
Лабораторные работы по химии элементов для студентов технологических специальностей
Скачать
Университет
Ярлык — Master Organic Chemistry
Ярлык для определения гибридизации атома в молекуле
Вот сокращенный способ определения гибридизации атома в молекуле , который будет работать по крайней мере в 95% случаев. случаи, которые вы видите в Org 1.
случаи, которые вы видите в Org 1.
Для данного атома:
- Подсчитайте количество атомов , связанных с ним (атомы – не связи!)
- Подсчитайте количество 9К нему подключено 0003 одиноких пары .
- Добавьте эти два числа вместе.
- Если это 4 , ваш атом будет sp 3 .
- Если это 3 , ваш атом будет sp 2 .
- Если это 2 , ваш атом равен sp.
(Если это 1, это, вероятно, водород!)
Основное исключение составляют атомы с неподеленными парами, которые примыкают к пи-связям, которые мы подробно обсудим ниже.
Оглавление
- Некоторые простые рабочие примеры ярлыка гибридизации
- Как определить гибридизацию атома: два упражнения
- Есть ли исключения?
- Исключение №1: Одиночные пары, соседние с пи-связями
- Одиночные пары в P-орбиталах (по сравнению с гибридными орбитами) имеют лучшее орбитальное перекрытие с соседними пи-системами
- Исключение №2.
 Геометрические ограничения
Геометрические ограничения - «Геометрия определяет гибридизацию, а не наоборот»
- Notes
1. Some Simple Worked Examples Of The Hybridization Shortcut
sp 3 hybridization : sum of attached atoms + lone pairs = 4
sp 2 гибридизация : сумма присоединенных атомов + неподеленных пар = 3
sp-гибридизация : сумма присоединенных атомов l + 9000 пар0004 = 2
Некоторые сложности могут возникнуть при работе с линейными диаграммами , содержащими неявные («скрытые») атомы водорода и неподеленные пары.
Химики, как и все остальные, любят экономить время, и умение быстро интерпретировать линейные диаграммы так же важно для органической химии, как изучение алфавита для письменного английского языка.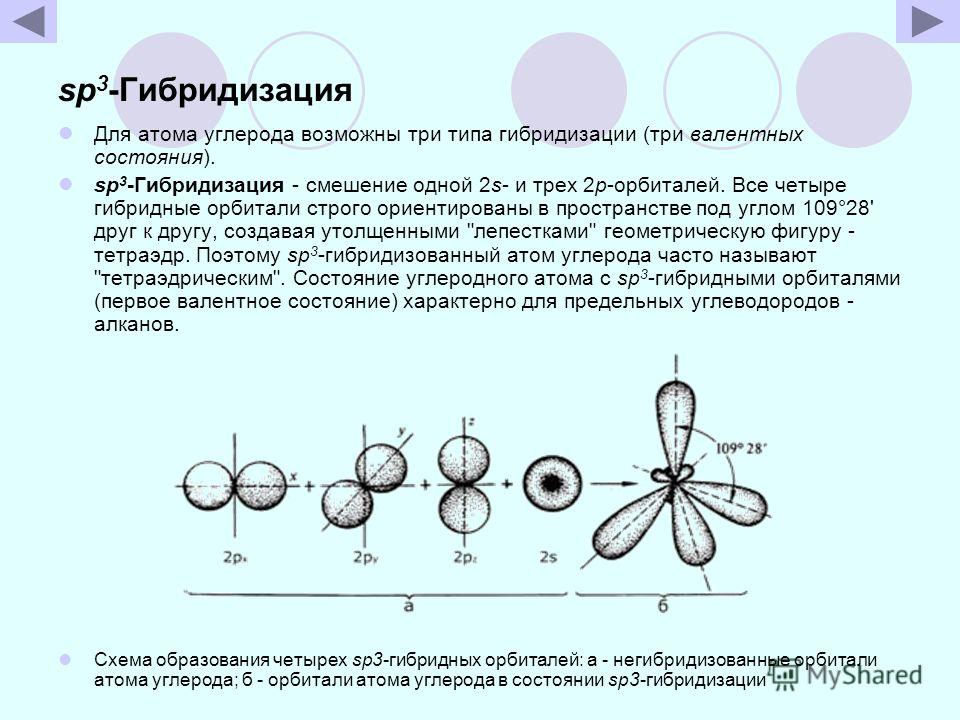
Помните:
- Просто потому, что неподеленные пары не втягиваются в кислород, азот и фтор не означает , что их там нет.
- Предположим, что полный октет для C, N, O и F со следующим одним исключением: положительный заряд углерода означает, что вокруг него находится только шесть электронов. [ Азот и Кислород с формальным зарядом +1 все еще имеют полные октеты].
[ Advanced: Примечание 1 описывает, как определить гибридизацию атомов в некоторых необычных случаях, таких как свободные радикалы, карбены и нитрены]
2. Как определить гибридизацию атома: два упражнения
Вот упражнение. Попробуйте определить гибридизацию атомов в этой очень ядовитой молекуле, созданной лягушкой в причудливой пижаме, справа внизу.
[Не беспокойтесь, если молекула выглядит немного сумасшедшей: просто сосредоточьтесь на отдельных атомах , на которые указывают стрелки (A, B, C, D, E).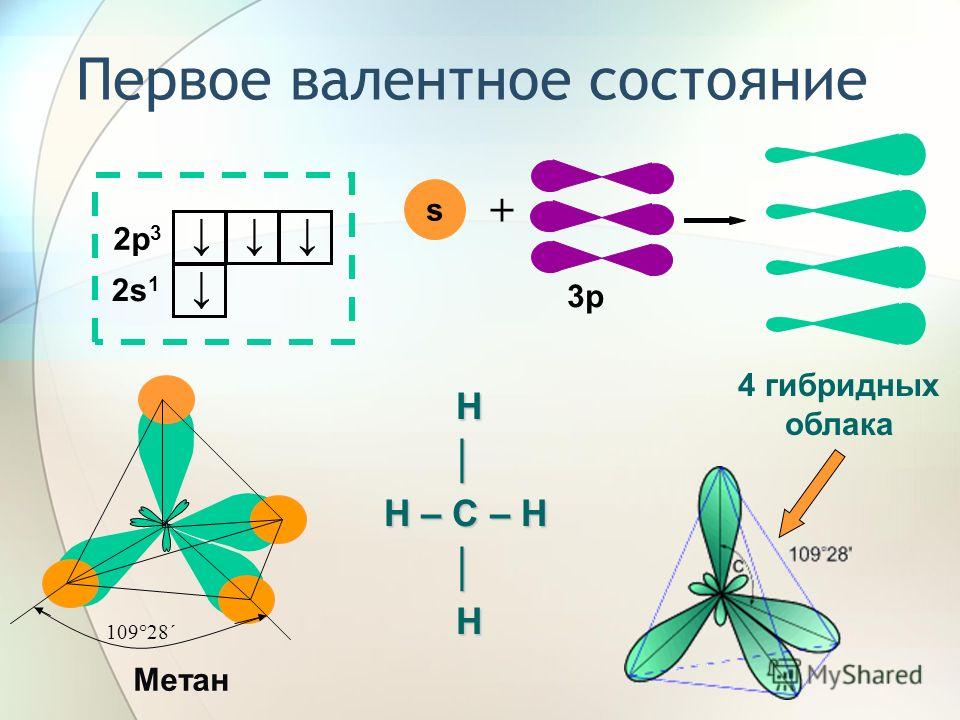 А и Б особенно. Если вы еще не освоили линейные диаграммы (и «скрытые» атомы водорода), возможно, попрактикуйтесь и вернитесь к этому позже.]
А и Б особенно. Если вы еще не освоили линейные диаграммы (и «скрытые» атомы водорода), возможно, попрактикуйтесь и вернитесь к этому позже.]
Вот еще несколько примеров.
Другие практические тесты по гибридизации можно найти здесь (Членство MOC открывает их все)
3. Есть ли исключения?
Конечно. Хотя, как и во многих других случаях, объяснение ярлыка занимает около 2 минут, а объяснение исключений занимает примерно в 10 раз больше времени.
К счастью, эти исключения делятся на две основные категории. Следует отметить, что к тому времени, когда ваш курс объяснит, почему эти примеры являются исключениями, он, скорее всего, продвинется далеко за пределы гибридизации.
Итог: их, вероятно, не найдут на первом промежуточном экзамене.
4. Исключение №1: неподеленные пары, соседние с пи-связями
Основное исключение составляют атомы, несущие неподеленные пары, которые соседствуют с пи-связями.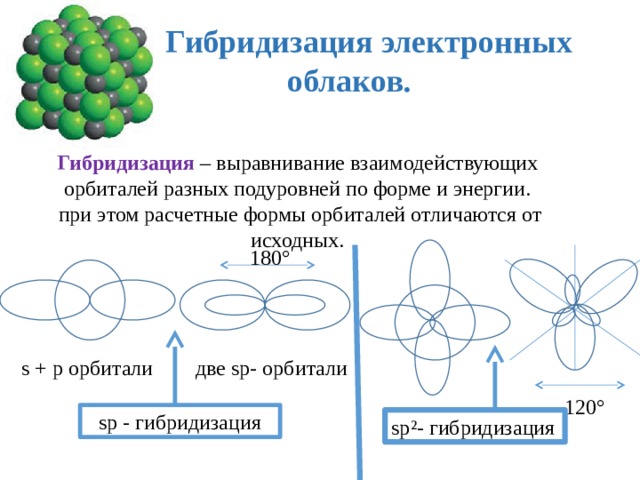
Краткий путь: Одиночные пары, смежные с пи-связями (и пи-системами), как правило, находятся на негибридных p-орбиталях, а не на гибридизированных sp n орбиталях.
Чаще всего используется для азот и кислород .
В приведенных ниже случаях азот или кислород, которые, как мы могли бы ожидать, будут sp 3 гибридизованными, на самом деле являются sp 2 гибридными (тригонально-плоскими).
Почему? Быстрый ответ заключается в том, что снижение энергии от сопряжения p-орбитали с соседней пи-связью более чем компенсирует рост энергии из-за большего отталкивания электронных пар для sp 2 по сравнению с sp 3
[см. этот пост: «Сопряжение и резонанс»]
Какой длинный ответ?
5. Одиночные пары на P-орбиталях (по сравнению с гибридными орбитами) имеют лучшее перекрытие орбит с соседними Pi-системами
Давайте вспомним, почему атомы гибридизуются в первую очередь: минимизация отталкивания электронных пар.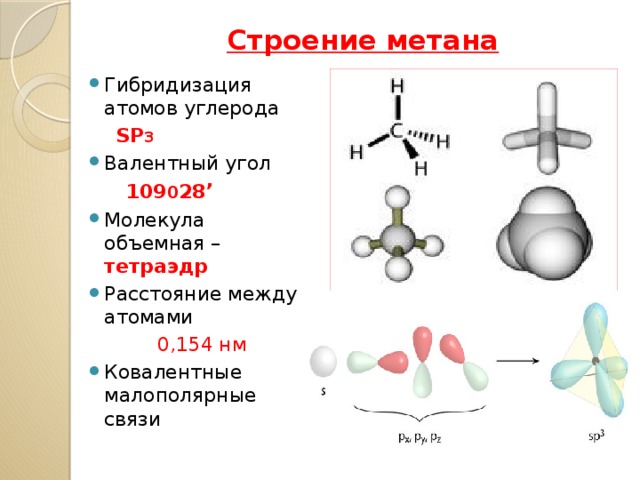
Для первичных аминов, таких как метиламин, принятие тетраэдрической (sp 3 ) геометрии азотом по сравнению с тригональной плоской (sp 2 ) геометрия стоит около 5 ккал/моль [примерно 20 кДж/моль].
Это может показаться не таким уж большим, но для двух видов, находящихся в равновесии, разница в энергии в 5 ккал/моль представляет собой соотношение примерно 4400:1 ]. [Откуда мы это знаем? См. это (расширенное) примечание 2 об инверсии азота]
Что, если бы существовал некоторый компенсирующий эффект, благодаря которому негибридизированная p-орбиталь с неподеленной парой была бы на самом деле более стабильной, чем если бы она находилась на гибридизированной орбитали?
Так происходит во многих ситуациях, когда неподеленная пара находится рядом с пи-связью! Наиболее распространенным и важным примером являются амиды , которые образуют связи между аминокислотами. Азот в амидах плоский (sp 2 ), а не тригонально-пирамидальный (sp 3 ), как доказано рентгеноструктурным анализом.
Разница в энергии варьируется в широких пределах, но типичное значение составляет около 10 ккал/моль в пользу тригонально-плоской геометрии. [Мы знаем это, потому что многие амиды имеют измеримый барьер для вращения, о чем мы также говорили в посте о сопряжении и резонансе]
Почему здесь предпочтение отдается тригональной планарной геометрии? Лучшее перекрытие орбитали p-орбитали с пи-связью по сравнению с (гибридизированной) sp 3 орбиталью .
На приведенном ниже рисунке делается попытка показать, как изменение гибридизации с sp 3 на sp 2 сближает p-орбиталь с соседними p-орбиталями пи-связи, обеспечивая лучшее перекрытие орбиталей. Лучшее перекрытие орбит обеспечивает более прочную пи-связь между неподеленной парой азота и карбонильной п-орбиталью, что приводит к общему снижению энергии.
Вы можете думать об этом как о более прочной «частичной» связи C–N. Двумя важными последствиями этого взаимодействия являются ограниченное вращение в амидах, а также тот факт, что кислота реагирует с амидами по кислороду, а не по неподеленной паре азота (!)
2 гибридизуются, как азот в енаминах и бесчисленное множество других примеров.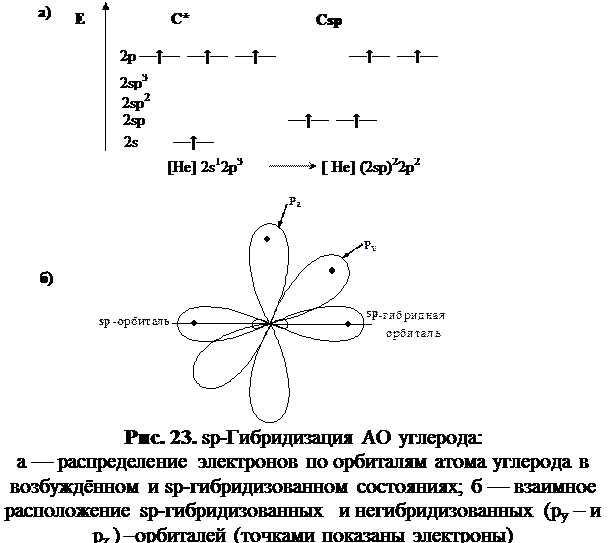
Как вы, вероятно, увидите в Org 2, одними из самых драматичных случаев являются те, где «дегибридизированная» неподеленная пара участвует в ароматической системе. Здесь энергетическая компенсация изменения гибридизации от sp 3 по sp 2 может быть действительно очень большой – в некоторых случаях более 20 ккал/моль.
По этой причине наиболее основным участком пиррола является не неподеленная пара азота, а углерод (С-2) (!).
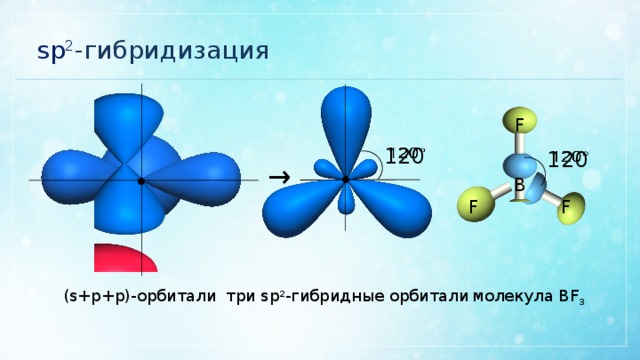
6. Исключение №2. Геометрические ограничения
Другой пример, когда фактическая гибридизация отличается от того, что мы могли бы ожидать от сокращения, — это случаи с геометрическими ограничениями. Например, в приведенном ниже фенильном катионе к указанному углероду присоединены два атома и ноль неподеленных пар.
Что такое гибридизация?
Исходя из нашего ярлыка, мы можем ожидать, что гибридизация будет sp .
На самом деле геометрия вокруг атома намного ближе к sp 2 .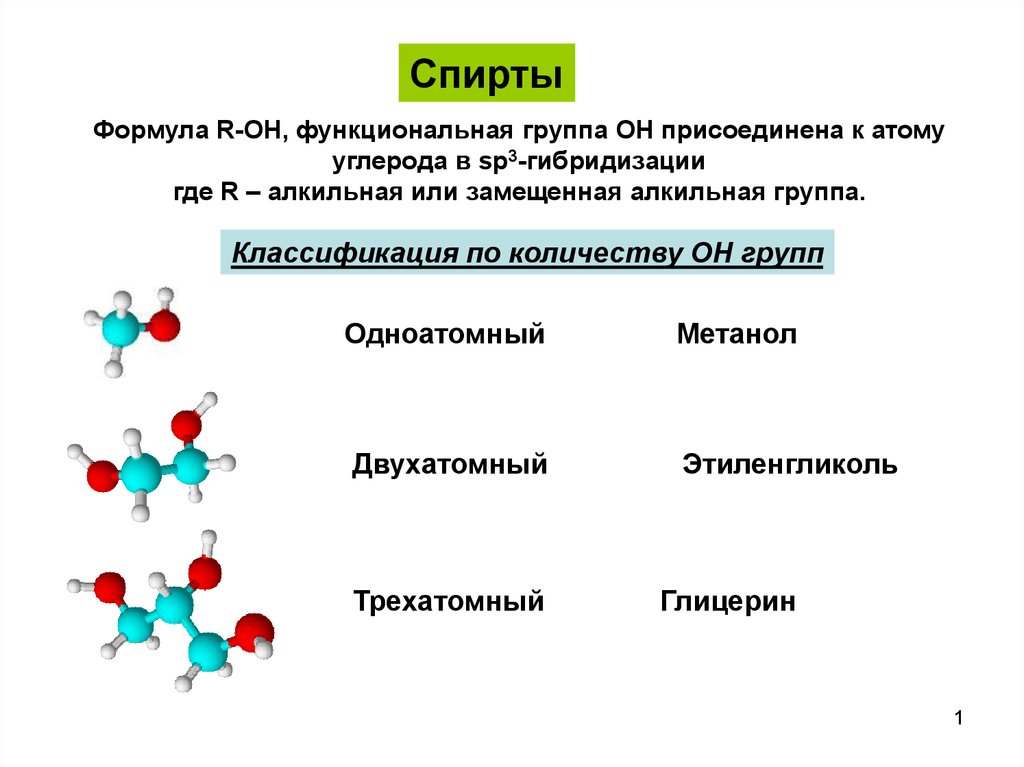 Это связано с тем, что угловая деформация, принимающая линейную (sp) геометрию, привела бы к слишком большой угловой деформации, чтобы быть стабильной молекулой.
Это связано с тем, что угловая деформация, принимающая линейную (sp) геометрию, привела бы к слишком большой угловой деформации, чтобы быть стабильной молекулой.
7. «Геометрия определяет гибридизацию, а не наоборот»
Цитата, переданная мне Мэттом, кажется уместной:
«Геометрия определяет гибридизацию, а не наоборот»
Пожалуй, это больше, чем вы хотели знать о том, как определять гибридизацию атомов.
Достаточно сказать, что любое сообщение с этого сайта, содержащее ярлык в заголовке, наверняка содержит более 1000 слов и >10 цифр.
Спасибо Мэтту Пирсу из компании Organic Chemistry Solutions за важный вклад в этот пост. Спросите Мэтта о расписании сеанса онлайн-репетиторства здесь.
Примечания
Соответствующие сообщения
- Скрытые атомы водорода, скрытые неподеленные пары, скрытые противоионы
- Гибридные орбитали и гибридизация?
- Откуда мы знаем, что метан тетраэдрический?
- Практика гибридизации связей
- Орбитальная гибридизация и прочность связей
- Сопряжение и резонанс в органической химии
Примечание 1. Несколько странных случаев.
Несколько странных случаев.
Иногда вас могут попросить определить гибридизацию свободные радикалы и карбены (или нитрены)
Хотя вы вряд ли столкнетесь с ними, давайте все же посмотрим.
- Свободные радикалы существуют в мелкой пирамидальной геометрии , а не только в sp 2 или sp 3 .
- Однако, если они примыкают к пи-системе (например, двойной или тройной связи С-С), то неглубокая пирамида регибридизирует , чтобы придать ей геометрию sp 2 , которая допускает полные резонансная делокализация свободного радикала.
- Карбены и нитрены дадут нам sp 2 геометрию путем гибридизации. Однако их фактическая структура может варьироваться в зависимости от того, существует ли электронная пара на одной орбитали (синглет карбен ) или разделена на две однократно заполненные орбитали (триплет карбен ).
 Это действительно выходит за рамки вводной органической химии.
Это действительно выходит за рамки вводной органической химии.
А как насчет высших блочных элементов, таких как сера и фосфор?
Элементы третьего ряда, такие как фосфор и сера, могут превышать октет электронов за счет включения d-орбиталей в гибрид. Это больше из области неорганической химии, поэтому я не хочу это обсуждать. Вот пример гибридизации SF 4 из других источников. (sp 3 d-орбитали).
Примечание 2 : Цифру 5 ккал/моль см. здесь. [Тетраэдр Летт, 1971, 37 , 3437]. (Kurt Mislow, RIP.)
Амин, связанный с тремя разными заместителями (R 1 R 2 и R 3 ), должен быть хиральным, поскольку он имеет всего 4 разных заместителя (включая неподеленную пару ). Однако все первые попытки получить энантиомерно чистые амины потерпели неудачу. Позже было обнаружено, что амины претерпевают инверсию при комнатной температуре, как зонтик, вывернутый наизнанку сильным ветром.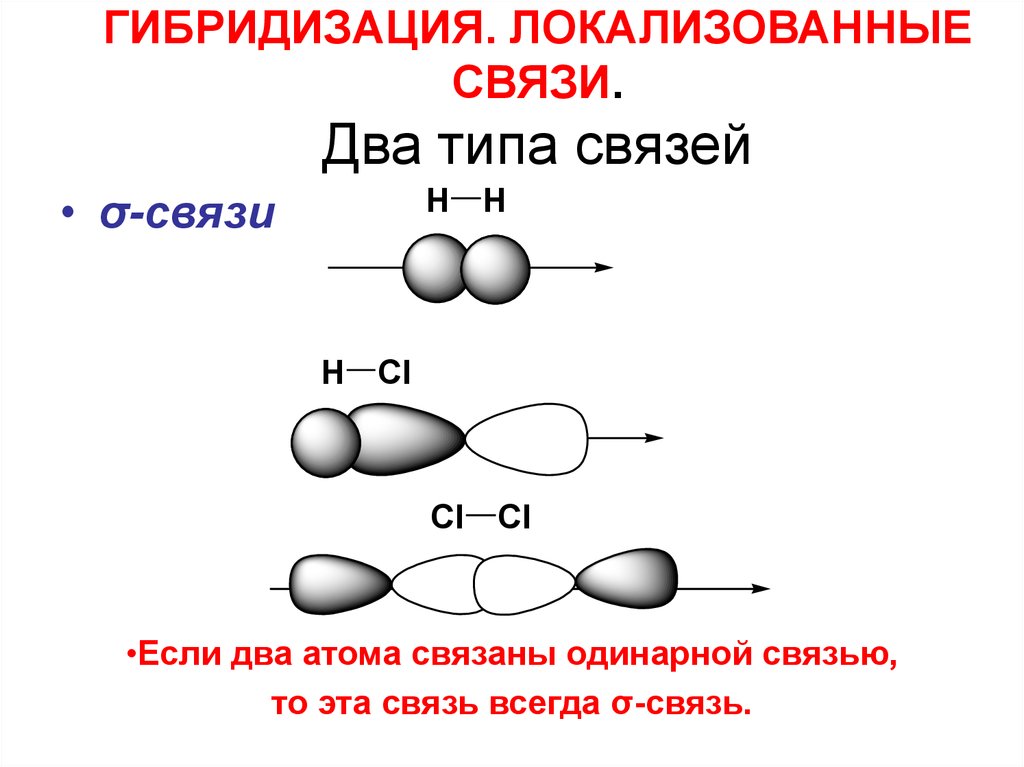
В переходном состоянии для инверсии азот тригонально-плоский. Таким образом, можно рассчитать разницу в энергии между геометриями sp 3 и sp 2 , измерив активационный барьер для этого процесса (см. ссылку).
Примечание 3 : Забавным контрпримером может быть целентеразин.
Нельзя ожидать, что оба атома азота будут sp 2 гибридизированы, потому что это привело бы к циклической, плоской, сопряженной системе с 8 пи-электронами: другими словами, антиароматической. Я не могу найти кристаллическую структуру основной молекулы для подтверждения (но буду рад любой дополнительной информации!)
ПРИМЕЧАНИЕ. – (добавлено позже) Если вы нарисуете резонансную форму, в которой неподеленная пара азота образует пи-связь с карбонильным углеродом, тогда кольцевая система имеет 10 электронов и, следовательно, будет «ароматической».
- Барьер для пирамидальной инверсии азота у дибензилметиламина
Майкл Дж. С. Дьюар и В. Брайан Дженнингс
С. Дьюар и В. Брайан Дженнингс
Журнал Американского химического общества 1971 93 (2) 1971 93 (2) 1971 93 (2) 1971 93 (2) 1971 93 (2) 1971 93 (2). 10.1021/ja00731a016 Pyramidal inversion barriers: the significance of ground state geometry
Joseph Stackhouse, Raymond D.Baechler, Kurt Mislow
Tetrahedron Letters Volume 12, Issue 37, 1971 , Pages 3437-3440
DOI: doi.org/10.1016/S0040-4039(01)97199-0
Эфиры
Диметиловый эфир
Функциональная группа эфира представляет собой атом кислорода, связанный с двумя атомами углерода.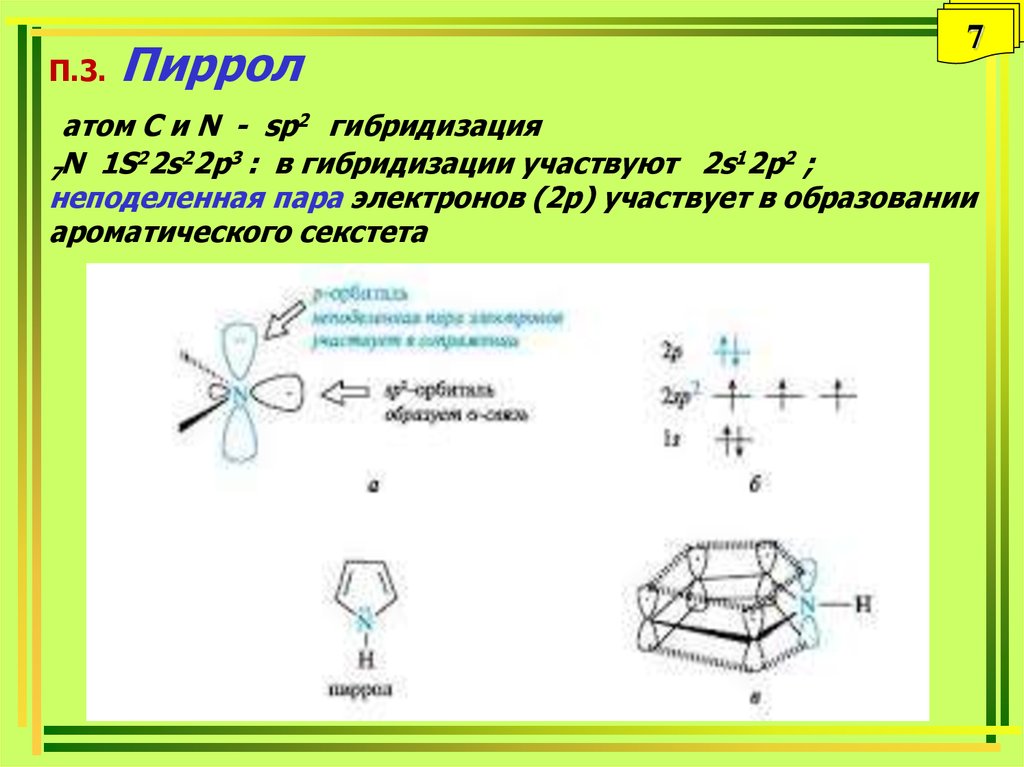 В диметиловом эфире два
В диметиловом эфире два
сп 3 гибридные орбитали кислорода образуют сигма-связь с двумя атомами углерода.
Две другие sp 3 гибридные орбитали атома кислорода содержат по неподеленной паре электронов.
Валентный угол C–O–C в диметиловом эфире равен 110,3°, что близко к тетраэдрическому углу 109,5°. В до сих пор
в других эфирах кислород эфира связан с sp 2 гибридизированными атомами углерода. В этоксиэтилене (этилвиниловом эфире), например
эфирный кислород связан с одним sp 3 и один sp 2 гибридизированный углерод.
Синтез эфира Вильямсона
Общие методы получения эфиров:
Сернокислотный процесс (или) синтез эфиров из спиртов:
Этот метод используется для получения стерически затрудненных симметричных эфиров.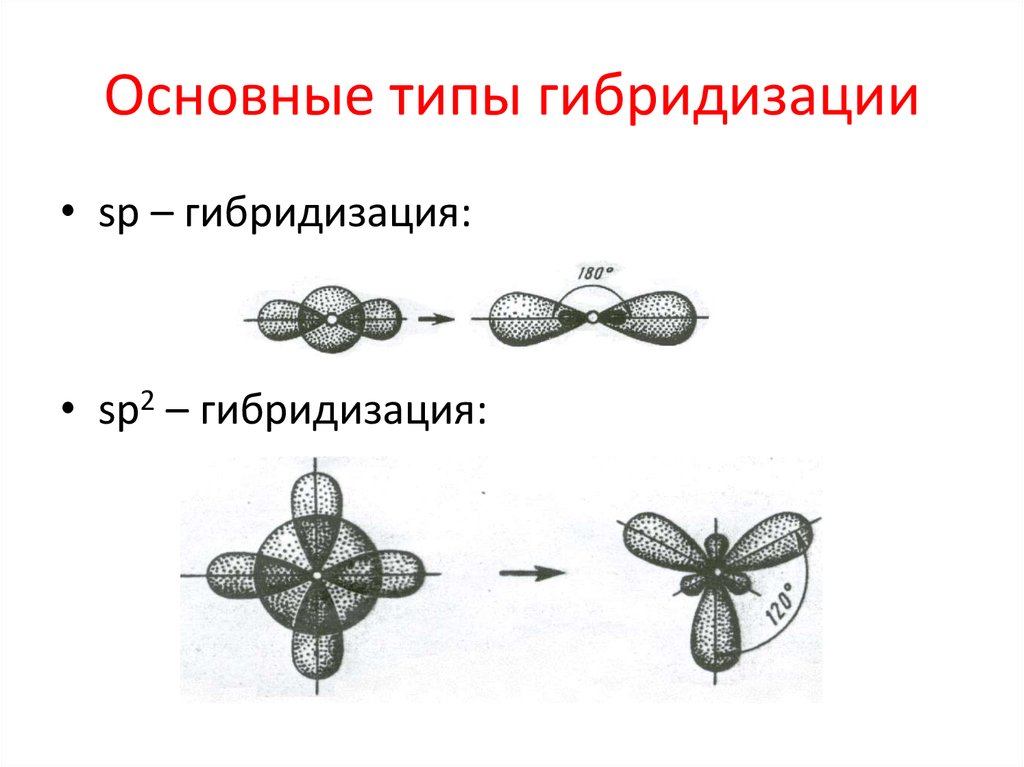
Метод Вильямсона:
Синтез эфира Вильямсона протекает по механизму SN 2 , в котором ион алкоксида замещает ион галогена.
При нагревании галогеналкенов с сухим оксидом серебра:
Галогеналканы при нагревании с Ag 2 O дают эфир. Этим методом можно получать как простые, так и смешанные эфиры.
Реакция с кислотами
Химические свойства эфира:
Эфиры – достаточно устойчивые соединения. Они плохо поддаются воздействию щелочей, разбавленных минеральных кислот, активных металлов, восстановителей.
агенты или окислители в обычных условиях.
Реакция с кислотами:
Будучи основаниями Льюиса, простые эфиры образуют комплексы с кислотами Льюиса, такими как BF 3 , AlCl 3 , FeCl 3 и т.д.
комплексы называются эфираты.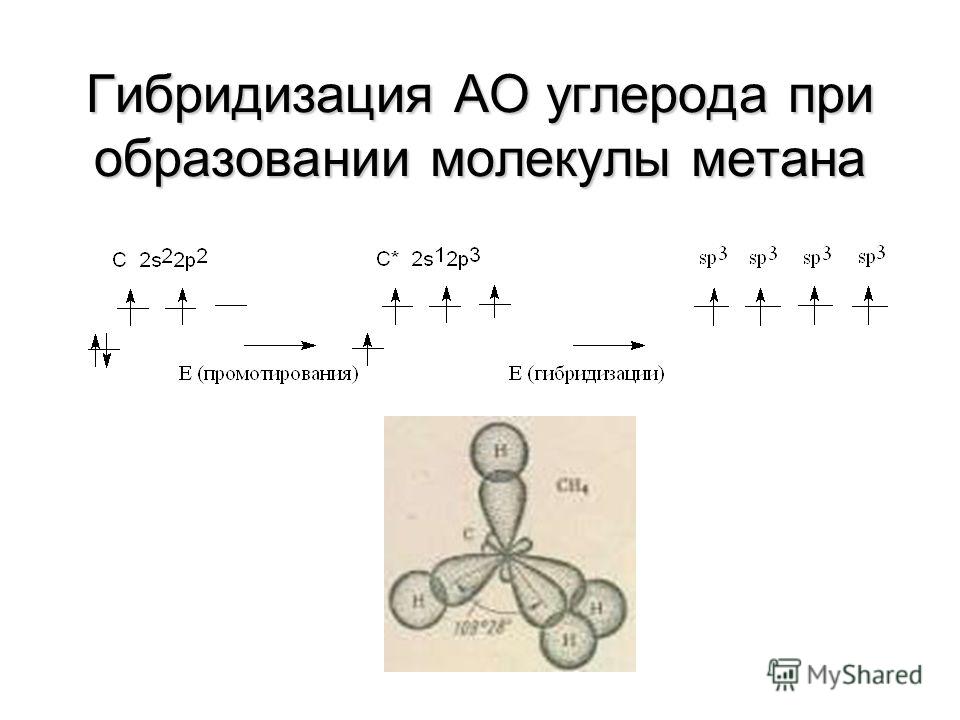
Аналогичным образом диэтиловый эфир реагирует с реактивом Гриньяра, образуя эфират реактива Гриньяра. Благодаря образованию эфирата,
Реактивы Гриньяра растворяются в эфире. Поэтому реактивы Гриньяра обычно готовят в эфирах. Однако они не могут быть
получают в бензоле, так как бензол не имеет неподеленной пары электронов и, следовательно, не может образовывать с ними комплексы.
метод Зейзеля
Метод Зейзеля, используемый для обнаружения и оценки алкоксигруппы в соединении.
Действие иодистоводородной кислоты:
С холодным HI:
С горячим HI:
Иодид серебра, образующийся таким образом в вышеуказанной реакции, может быть обнаружен и оценен методом Цейзеля.
Реакция с монооксидом углерода:
Эфиры используются в качестве анестезии.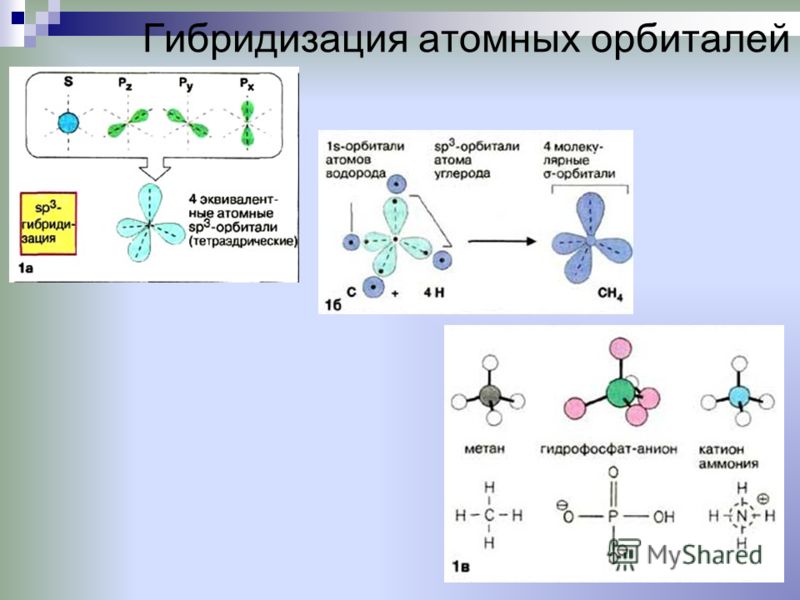

 Геометрические ограничения
Геометрические ограничения Это действительно выходит за рамки вводной органической химии.
Это действительно выходит за рамки вводной органической химии. С. Дьюар и В. Брайан Дженнингс
С. Дьюар и В. Брайан Дженнингс