Содержание
КРАУН-ЭФИРЫ | Энциклопедия Кругосвет
Содержание статьи
- Номенклатура краун-эфиров.
- Свойства краун-эфиров.
- Получение краун-эфиров.
КРАУН-ЭФИРЫ (от англ. crown – корона) – крупные циклические молекулы (макроциклы), которые состоят из чередующихся этиленовых мостиков –СН2–СН2– и атомов кислорода. В некоторых случаях часть атомов О заменена атомами N или S. Форма таких молекул напоминает корону, что и определило их название (англ. crown – корона).
Номенклатура краун-эфиров.
Рис. 1. СОСТАВЛЕНИЕ НАЗВАНИЙ ДЛЯ КРАУН-ЭФИРОВ
Свойства краун-эфиров.
Формально все краун-эфиры можно отнести к классу гетероциклических соединений, однако необычные свойства таких соединений позволили выделить их в самостоятельный класс, в связи с чем для составления названий были предложены специальные правила. Название содержит слово «краун», цифра перед этим словом обозначает общее число атомов в цикле, а цифра в конце названия указывает на количество гетероатомов O, N и S (рис. 1). В названии не указывают наличие в цикле атомов О (это подразумевается), но если в цикле есть иные гетероатомы (кроме кислорода), например, азот или сера, то их количество указывают, добавляя к названию приставки ди- или три-, а положение в цикле – с помощью числовых индексов, предварительно нумеруются все атомы в цикле.
1). В названии не указывают наличие в цикле атомов О (это подразумевается), но если в цикле есть иные гетероатомы (кроме кислорода), например, азот или сера, то их количество указывают, добавляя к названию приставки ди- или три-, а положение в цикле – с помощью числовых индексов, предварительно нумеруются все атомы в цикле.
Краун-эфиры содержат фрагмент С–О–С, характерный для простых эфиров, а также могут включать фрагменты амина C–NH–C, или тиоэфира C–S–C (см. СЕРАОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ). Характерное свойство этих классов соединений – образовывать комплексы за счет неподеленных электронных пар кислорода, азота и серы. Это свойство многократно усилено в краун-эфирах из-за большого числа гетероатомов в цикле, к тому же неподеленные электронные пары ориентированы внутрь цикла. В результате ионы щелочных и щелочноземельных металлов входят внутрь цикла, образуя прочные комплексы. Меняя величину цикла и, соответственно, размер внутренней полости, можно точно настроить краун-эфир на удерживание катиона определенного размера, например, 12-краун-4 (рис. 1) наиболее прочно захватывает катион лития, 15-краун-5 соответствует по размеру катиону натрия, а 18-краун-6 «подходит по размеру» катиону калия (рис. 2).
1) наиболее прочно захватывает катион лития, 15-краун-5 соответствует по размеру катиону натрия, а 18-краун-6 «подходит по размеру» катиону калия (рис. 2).
Рис. 2. КОМПЛЕКСЫ КРАУН-ЭФИРОВ с катионами щелочных металлов (пунктирными линиями показаны координационные связи)
Более наглядно взаимосоответствие внутренней полости цикла и размера катиона можно показать с помощью объемных моделей (рис. 3).
У краун-эфиров склонность к «захвату» катионов выражена настолько сильно, что даже если катион не соответствует по размеру внутренней полости цикла, то все равно оказываются возможными варианты, при которых катион все же удерживаеся. Например, если катион по размеру много больше внутренней полости, то он может окружить себя двумя молекулами краун-эфира, образуя подобие бутерброда (рис. 4А) если же ситуация обратная, то внутрь молекулы краун-эфира может поместиться два катиона (рис. 4Б).
Подобные комплексы менее устойчивы, чем те, у которых размер катиона точно соответствует величине внутренней полости.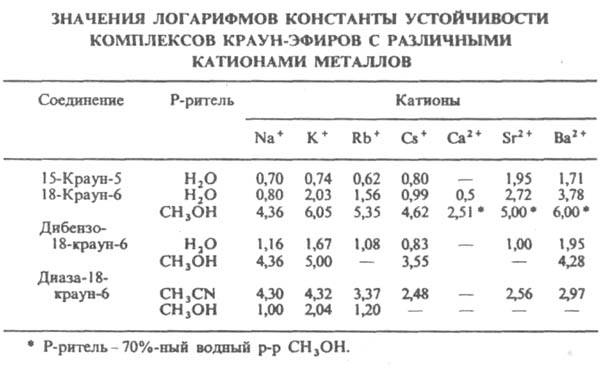
Краун-эфиры открыли новые горизонты в синтетической органической химии, с их помощью оказалось возможным вводить в растворенном виде (т.е. гомогенно), неорганические реагенты в органическую среду. Например, широко применяемый окислитель перманганат калия KMnO4 практически нерастворим в органических растворителях, но в присутствии 18-краун-6 он легко растворяется в бензоле, приобретая при этом высокую окисляющую способность. Причина в том, что в водном растворе анионы MnO4–, осуществляющие окисление, окружены водной сольватной оболочкой, а в бензольном растворе они как бы обнажены и потому высокоактивны.
Получение краун-эфиров.
При конденсации дихлоралкилов, содержащих в цепи простые эфирны группировки С–О–С, с полиэтиленгликолями протекает циклизация, приводящая к образованию краун-эфира (рис. 5А). В зависимости от длины цепочки исходных соединений получают краун-эфиры с различной величиной цикла. Азотсодержащие краун-эфиры получают конденсацией диаминов, содержащих эфирные группировки, с хлорангидридами дикарбоновых кислот. В результате получаются циклические амиды, которые затем восстанавливают, при этом карбонильные группы С=О превращаются в метиленовые СН2 (рис. 5Б). Серосодержащие краун-эфиры получают по схеме А (рис. 5), при этом исходные соединения содержат тиоэфирные группировки С–S–С.
В результате получаются циклические амиды, которые затем восстанавливают, при этом карбонильные группы С=О превращаются в метиленовые СН2 (рис. 5Б). Серосодержащие краун-эфиры получают по схеме А (рис. 5), при этом исходные соединения содержат тиоэфирные группировки С–S–С.
Применение краун-эфиров определяется, прежде всего, их избирательной способностью захватывать катионы определенного размера. Наибольшее распространение получили краун-эфиры, содержащие только гетероатомы О. Их применяют в технологических процессах, связанных с выделением и очисткой солей щелочных и щелочноземельных металлов, в аналитических исследованиях и работах, связанных с синтезом, когда нужно перевести неорганические соединения из водной фазы в органическую среду.
Краун-эфиры обладают противомикробной и противопаразитарной активностью, кроме того, из организма с их помощью выводятся ионы токсичных тяжелых металлов, а также радиоактивных изотопов цезия и стронция.
В радиохимии краун-эфиры помогают решать проблему переработки отходов ядерных производств.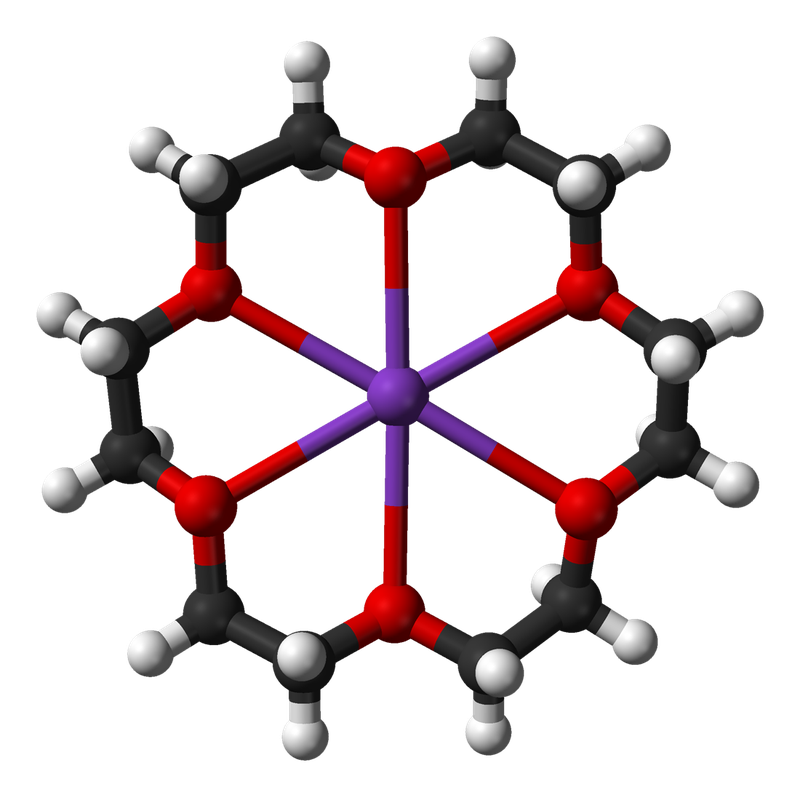 Первый этап – удаление с помощью краун-эфиров из переработанного ядерного горючего наиболее активных изотопов (стронций-90, цезий-137, технеций-99), на этой стадии предпочтительны S-содержащие краун-эфиры, поскольку они обладают повышенной радиационной стойкостью. Извлеченные изотопы используются затем в установках радиодиагностики, заменяющих рентгеновские аппараты, а также при создании долговременных источников тока для метеостанций, метеозондов и космических аппаратов. Следующий этап переработки ядерного топлива – извлечение с помощью краун-эфиров (специально подобранного состава) неизрасходованных урана и плутония, после чего объем подлежащих утилизации отходов становятся заметно меньше и к тому же отходы обладают слабой радиоактивностью.
Первый этап – удаление с помощью краун-эфиров из переработанного ядерного горючего наиболее активных изотопов (стронций-90, цезий-137, технеций-99), на этой стадии предпочтительны S-содержащие краун-эфиры, поскольку они обладают повышенной радиационной стойкостью. Извлеченные изотопы используются затем в установках радиодиагностики, заменяющих рентгеновские аппараты, а также при создании долговременных источников тока для метеостанций, метеозондов и космических аппаратов. Следующий этап переработки ядерного топлива – извлечение с помощью краун-эфиров (специально подобранного состава) неизрасходованных урана и плутония, после чего объем подлежащих утилизации отходов становятся заметно меньше и к тому же отходы обладают слабой радиоактивностью.
На основе краун-эфиров созданы электропроводящие материалы нового типа (см. ЭЛЕКТРИДЫ).
За развитие химии макрогетероциклических соединений американский химик Ч.Педерсен, фактически создавший новый класс соединений – краун-эфиры, в 1987 (совместно Д. Крамом и Ж.Леном) был удостоен Нобелевской премии.
Крамом и Ж.Леном) был удостоен Нобелевской премии.
Михаил Левицкий
Проверь себя!
Ответь на вопросы викторины «Неизвестные подробности»
Какой музыкальный инструмент не может звучать в закрытом помещении?
Пройти тест
Молекулярные контейнеры – аналитический портал ПОЛИТ.РУ
О контейнерной химии впервые заговорили сорок лет назад: именно тогда были открыты краун-эфиры, первые синтетические аналоги природных веществ, осуществляющих перенос ионов металлов через мембрану клетки. Это открытие позволило ученым создать так называемые молекулы-«контейнеры»: искусственные химические соединения, способные захватывать и удерживать уже не только ионы металлов, но и нейтральные молекулы. Сегодня химики синтезируют все новые краун-соединения, применяя их в медицине, технике, науке и сельском хозяйстве. «Полит.ру» публикует статью доктора химических наук Юрия Чиркова, в которой речь пойдет о последних достижениях контейнерной химии, а также об ученых, стоявших у ее истоков.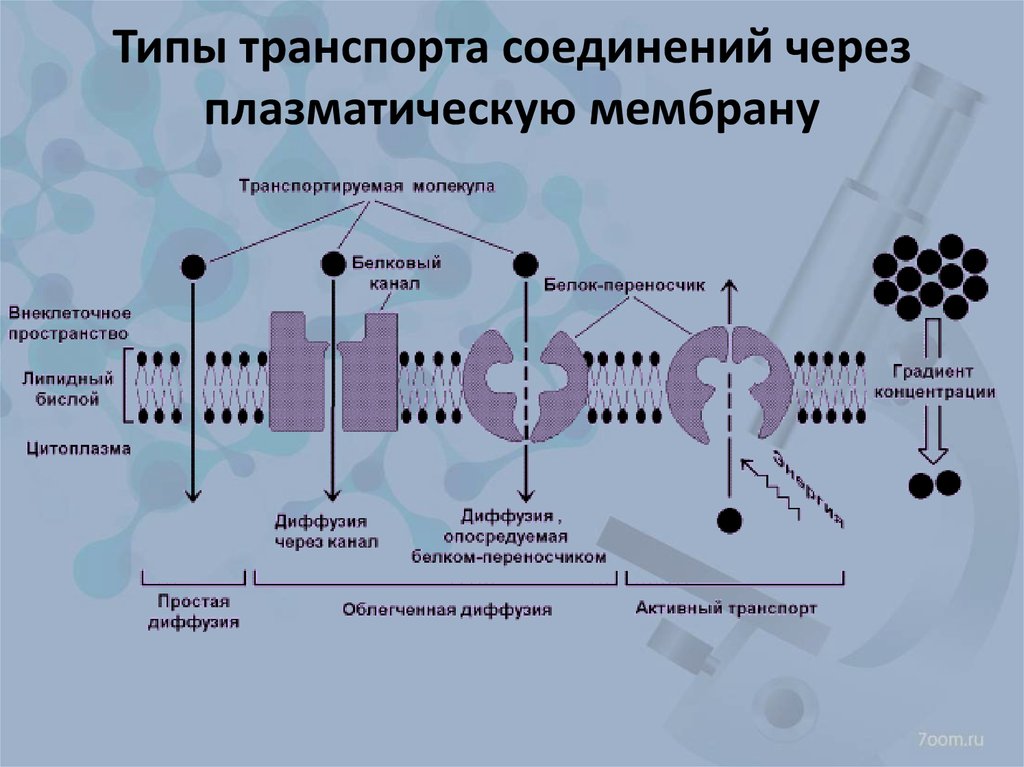 Статья опубликована в новом номере журнала «Наука и жизнь» (2010. №7).
Статья опубликована в новом номере журнала «Наука и жизнь» (2010. №7).
Из всех связей наиприятнейшей является связь между хозяином и гостем.
Эсхил, древнегреческий поэт и драматург
Как здание строится из кирпичей, так ткани живых существ состоят из клеток. К примеру, организм взрослого человека искусно смонтирован из 100 триллионов (!) клеток. Подобно тому как организм состоит из отдельных органов, клетка сконструирована из многих структур, ответственных за питание, размножение, выделение… Она обладает даже «эрудицией» и «умом». Клеточная «эрудиция»? Это хранение большого набора программ целесообразного реагирования на внешние сигналы. А «ум»? Способность включать соответствующие программы по мере надобности. Что это за программы? Какие биомолекулы в клетке их осуществляют?
Хоровод калия с натрием
Когда-то на нашей планете бурлил Первоокеан. В нём возникли и плавали первые биомолекулы. Однако хитроумной Природе этого показалось мало. И она в какой-то момент решила собрать биомолекулы в сгустки и создать для них особые искусственные условия существования. Так, должно быть, и возникла первая живая клетка. Внутри биологической мембраны, которая огораживает пределы клетки, царит особый мир, комфортный для «клеточных» биомолекул.
И она в какой-то момент решила собрать биомолекулы в сгустки и создать для них особые искусственные условия существования. Так, должно быть, и возникла первая живая клетка. Внутри биологической мембраны, которая огораживает пределы клетки, царит особый мир, комфортный для «клеточных» биомолекул.
Что это за условия? В любой клетке ионов калия (К+) всегда гораздо больше, чем ионов натрия (Na+). Вне её всё наоборот: здесь преобладает натрий. Впрочем, вот точные цифры. В клетке, точнее, во внутриклеточной жидкости, например, эритроцитов человека концентрация калия (в условных единицах) К+ — 92, натрия Na+ — 11. А вне клетки (в межклеточной жидкости, скажем в плазме крови) К+ — всего 5, а Na+ — 152 единицы. В нервной же клетке (нейроне) неравенство концентраций ещё более ощутимо: К+ — 300, Na+ — 10. Снаружи нейрона напротив: К+ — 22, Na+ — 440.
Какие преимущества это даёт живой клетке? Такое неоднородное распределение катионов щелочных металлов по обе стороны клеточной мембраны создаёт трансмембранный электрический потенциал, как в батарейке. Эта разность потенциалов, её энергия, используется, среди прочего, при передаче информации по нейронам в нервной системе.
Эта разность потенциалов, её энергия, используется, среди прочего, при передаче информации по нейронам в нервной системе.
Разность концентраций ионов К+ и Na+ по обе стороны мембраны играет ключевую роль не только в проведении нервных импульсов, но и в регуляции клеточного осмотического давления и водно-солевого обмена. Например, с помощью встроенных в мембраны клеток особых ферментов (К+, Na+ — АТФаз) морские птицы умеют опреснять для себя солёную воду. Так что вода, попадающая во внутриклеточное пространство, уже пресная.
Таким образом, биомембраны клеток способны отличать ионы калия от ионов натрия, хотя эти ионы имеют близкие размеры и одинаковый положительный заряд. Более того, в мембрану живой клетки как будто встроен и действует особый «насос»: он непрерывно выкачивает из клетки натрий и накачивает в неё калий, организуя особое действо — калий-натриевый обмен.
Проблема активного переноса ионов через биологические мембраны сотню лет волновала умы исследователей. Разгадка пришла примерно полвека назад. Большой вклад в эти исследования внесли советские учёные.
Разгадка пришла примерно полвека назад. Большой вклад в эти исследования внесли советские учёные.
Ионофоры
В 1959 году в Академии наук СССР был создан Институт химии природных соединений АН СССР, возглавил его академик Михаил Михайлович Шемякин (1908—1970). Сотрудники нового института начали с самого простого — с низкомолекулярных соединений в ткани живого, с изучения того, как антибиотики, витамины и прочие биорегуляторы воздействуют на клетки живого организма, с исследования молекулярных механизмов их действия.
Шемякин раньше других уловил момент оформления новой науки и со свойственным ему темпераментом принялся насаждать её на доступном ему пространстве. В частности, как и учёные других научных учреждений мира, шемякинцы занялись проблемой валиномицина.
Антибиотик валиномицин впервые был выделен из экстракта штамма бактерий Streptomyces fulvissimus австрийским исследователем Г. Брокманом в 1954—1955 годах. А в 1963 году в лаборатории М. М. Шемякина установили химическую структуру этого соединения.
Валиномицин представляет собой депсипептид, свёрнутый в кольцо. Он стал «фирменным блюдом» института, но его успешный синтез доставил советским учёным немало хлопот. Дело в том, что немецкие химики, устанавливая строение валиномицина, ошибочно решили, что его кольцо содержит не 12, а 8 остатков. Следуя их формуле, шемякинцы получили то, что не имело ничего общего с природным антибиотиком. Понадобилась интеллектуальная смелость, чтобы предположить ошибку в размере кольца.
Между тем прошло несколько лет, и слово «валиномицин», ранее известное лишь узкому кругу «пептидчиков», внезапно заполонило страницы биологических журналов. Началось это с открытия способности валиномицина стимулировать перенос ионов калия через биологические мембраны. Вскоре американцы П. Мюллер и Д. Рудин предположили, что валиномицин играет роль контейнера для переноса ионов. Согласно их гипотезе, ион калия переправляется через мембрану, спрятавшись внутри гораздо большей по размеру молекулы антибиотика.
Кристаллическая структура K+-комплекса валиномицина. Этот переносчик ионов проходит сквозь мембрану клетки и на другом её конце отдаёт ион в раствор.
В короткое время Михаилу Шемякину удалось развернуть в Институте химии природных соединений исследования самых разных аспектов этой проблемы. Изучением закономерностей связи между структурой и функцией валиномицина и родственных ему веществ в той же лаборатории занялся и будущий академик и вице-президент Академии наук СССР Юрий Анатольевич Овчинников (1934—1988).
В те годы Юрий Овчинников занимался синтезом тетрациклинов. И был неприятно удивлён, когда Шемякин предложил ему сменить тему и заняться химией пептидов. После сложнейших схем синтеза тетрациклинов пептидная химия, в основе которой лежало наращивание полипептидных цепей однотипными аминокислотами, показалась талантливому учёному пресной, малотворческой. Потребовались долгие уговоры, дискуссии, приведение веских доводов, чтобы убедить Овчинникова и пришедших с ним выпускников МГУ в актуальности, сложности и своеобразии предлагаемой им темы исследований.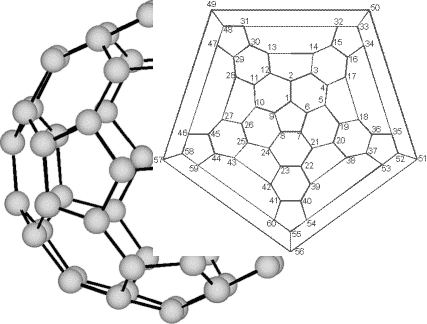
Вскоре вслед за валиномицином удалось обнаружить и другие, подобные ему вещества природного происхождения — вкупе весь этот класс соединений получил в науке название «ионофоры». Благодаря их открытию и изучению был сделан решающий шаг в познании механизмов переноса ионов сквозь биологические мембраны. За большой вклад в эти исследования в 1978 году Ю. А. Овчинников и член-корреспондент АН СССР Вадим Тихонович Иванов были удостоены Ленинской премии.
Итоги работы советских учёных докладывались на многих международных конференциях и были суммированы в обзорах и монографии «Мембранно-активные комплексоны» (валиномицин и вообще все ионофоры называли также комплексонами).
Стоит отметить, что лужайку перед главным входом в Институт биоорганической химии АН СССР (ныне — РАН) украшает не бюст какого-нибудь именитого учёного, а скульптурная композиция, изображающая изящную пространственную структуру калиевого комплекса валиномицина.
Примеры валиномицина и других ионофоров, казалось бы, должны были настроить работу химиков-органиков на определённую волну. Разве не заманчиво было бы тотчас заняться синтезом хитроумных «ловушек» не только катионов, но и анионов, и даже молекул?
Разве не заманчиво было бы тотчас заняться синтезом хитроумных «ловушек» не только катионов, но и анионов, и даже молекул?
Всюду здесь план кольцевой макроструктуры налицо. И в её центре обязательно красуется атом того или иного металла.
Уже знакомый нам валиномицин также представляет собой макроциклическое соединение, скроенное из шести α-аминокислот и шести α-гидроксикислот, соединённых друг с другом попеременно амидными и сложноэфирными связями.
Таким образом, идея макроциклического комплексообразования буквально стучалась в умы исследователей. И, казалось бы, наличествовали научные предпосылки для подобных разработок. Ощущалась и потребность — такие вещества были остро необходимы (об этом мы ещё будем говорить). И всё ж требовался случай, неожиданная находка, которая начала бы лавинообразное развитие исследований в данной области, как позднее и случилось.
Золотая жила Чарльза Педерсена
Сын норвежца и японки Чарльз Педерсен родился 1904 году в Корее.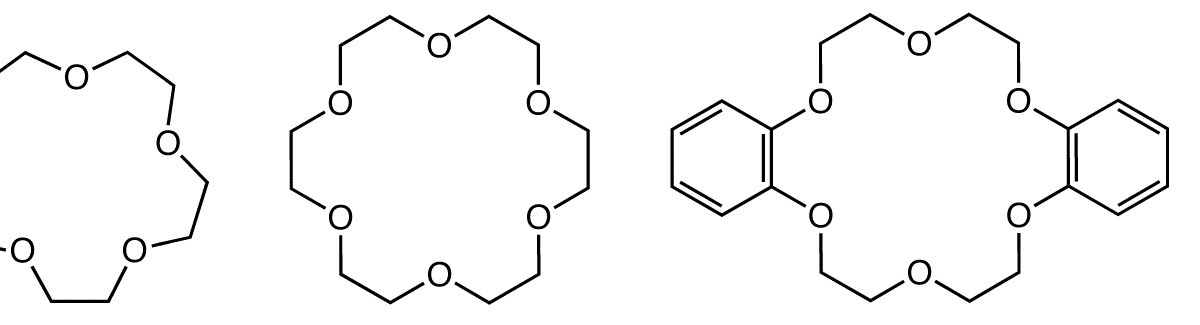 Отучившись четыре года в Дейтоне (США) и год в аспирантуре Массачусетского технологического института (МТИ, США), Педерсен, несмотря на уговоры своего научного консультанта, не остался в МТИ для получения степени доктора философии. Молодому человеку не терпелось начать зарабатывать на жизнь самостоятельно. В 1927 году Педерсен устроился на работу в компанию «Дюпон».
Отучившись четыре года в Дейтоне (США) и год в аспирантуре Массачусетского технологического института (МТИ, США), Педерсен, несмотря на уговоры своего научного консультанта, не остался в МТИ для получения степени доктора философии. Молодому человеку не терпелось начать зарабатывать на жизнь самостоятельно. В 1927 году Педерсен устроился на работу в компанию «Дюпон».
К середине 40-х годов прошлого века Педерсен был уже зрелым специалистом, попробовавшим себя во многих областях. И его ждало дело всей жизни — открытие краун-эфиров — первых синтетических аналогов природных веществ, осуществляющих перенос ионов щелочных металлов через клеточную мембрану. Открытие, сделавшее его не только нобелевским лауреатом (1987 год, вместе с Дональдом Крамом и Жан-Мари Леном), но и родоначальником гигантского пласта исследований и открытий.
Свою эпохальную работу Педерсен сделал в 1962 году, однако целых пять лет не спешил публиковаться, а синтезировал всё новые и новые краун-эфиры. В полученных учёным соединениях фигурировали несколько атомов кислорода, связанных мостиками Ch3Ch3, которые, образуя кольцевую цепь (макроцикл того или иного размера), могут создавать прочные комплексы с ионами щелочных металлов.
В общей сложности Педерсен к 1967 году, моменту первой публикации в журнале Американского химического общества, синтезировал более 60 полиэфиров с числом кислородных атомов от 4 до 20 и размером цикла от 12- до 60-членного.
Похоже, он уже тогда чувствовал, что копает золотую жилу.
Интуитивная прозорливость
Что, собственно, сделал Чарльз Педерсен? Он синтезировал соединение, названное им краун-эфиром за особенность его структуры: она представляла собой пустое внутри и подвижное кольцо из углеродных атомов, связанное через мостики кислородными атомами. Варьируя размер цикла, учёный установил, что краун-эфиры способны избирательно связывать некоторые катионы, помещая их в центр своей «короны».
Тут уместно привести небольшую цитату, она взята из Нобелевской лекции, прочитанной Педерсеном в Стокгольме: «Мои первые действия мотивировались скорее эстетикой, чем наукой. Мне доставляло большое эстетическое наслаждение созерцать построенную компьютером трёхмерную модель структуры… Какой простой, изящный и эффективный способ улавливания доселе непокорённого катиона щелочного металла! Я принял эпитет «crown» («корона») для первого представителя этого класса, потому что его молекулярная модель выглядела именно так, и с ним катион мог быть коронован и декоронован без какого-либо физического ущерба для обоих».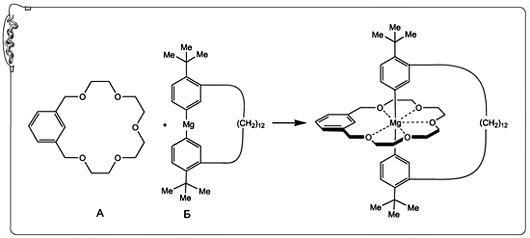
Образование краун-эфира — комплекса 18-краун-6 и иона K+ (в центре). Надо отдать должное искусству Педерсена, сумевшего выделить и изучить свойства побочного продукта, полученного в крайне малом количестве.
Теперь подробности того, как было сделано Педерсеном открытие. Исследователь пытался создать ингибиторы (замедлители) аутоокисления нефтяных масел. Намерение было скромным и чисто прикладным. К разочарованию учёного, в результате произведённого им эксперимента образовался смолистый продукт, а вместо ожидаемого соединения выделилось ничтожное количество (< 1%) кристаллического вещества. Спектральные и аналитические данные свидетельствовали: полученное вещество является макроциклическим полиэфиром.
Что делают в подобных случаях? Неожиданная примесь? Да бог с ней! Не будем тратить времени, выбросим всё это и повторим синтез при более тщательной очистке исходных веществ и более строгом соблюдении необходимых для основной реакции условиях.
«Поступи я таким образом, — рассказывал в Нобелевской лекции Педерсен, — о краун-эфирах не было бы известно ничего до тех пор, пока другой исследователь не прошёл бы по моим следам и в критический момент не принял бы лучшее решение».
Но Педерсен, не колеблясь, стал изучать неизвестное вещество. От его внимания не ускользнули необычные особенности поведения нежданно полученного им соединения. Ему пришла в голову блестящая гипотеза о природе этого вещества, и он стал его тщательно исследовать. Работа учёного в итоге стала примером способности одного химика обеспечить интереснейшими задачами значительную часть химического сообщества.
Чарльзу Педерсену помог случай, это стоит подчеркнуть ещё раз. В английском языке есть слово «serendipity» (серендипити), которое обычно переводится на русский язык как «интуитивная прозорливость». В англоязычных энциклопедиях оно трактуется так: «способность случайно совершать желаемые открытия». История с открытием краун-эфиров — один из удачных примеров роли серендипити в науке.
Сферанды, кавитанды, криптанды
Открытие Чарльза Педерсена получило развитие в работах американца Дональда Крама (1919—2001) и француза Жан-Мари Лена (родился в 1939 году).
Краун-эфиры обладают двухмерной структурой.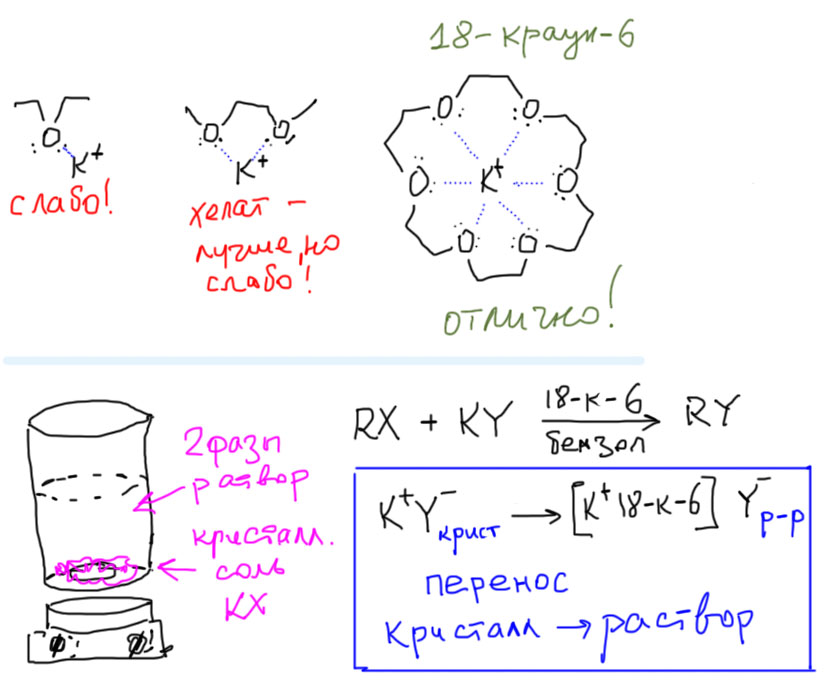 Краму удалось создать аналогичного рода трёхмерные структуры, способные захватывать ионы. В результате сложных многостадийных органических синтезов в начале 1980-х годов он создал так называемые молекулы-«контейнеры» с заранее организованной структурой — сферанды (буквально пустые внутри сферические структуры) и молекулы, обладающие внутренней полостью, — кавитанды (от английского слова «cavity» — полость), своего рода молекулярные чаши с углублениями. В чашах этих, так же как и в молекулах краун-эфиров, могли вольготно размещаться ионы.
Краму удалось создать аналогичного рода трёхмерные структуры, способные захватывать ионы. В результате сложных многостадийных органических синтезов в начале 1980-х годов он создал так называемые молекулы-«контейнеры» с заранее организованной структурой — сферанды (буквально пустые внутри сферические структуры) и молекулы, обладающие внутренней полостью, — кавитанды (от английского слова «cavity» — полость), своего рода молекулярные чаши с углублениями. В чашах этих, так же как и в молекулах краун-эфиров, могли вольготно размещаться ионы.
Крам предположил и доказал, что, в отличие от относительно гибких молекул краун-эфиров в растворе, жёсткие молекулы сферанда или кавитанда, в силу особенностей своей трёхмерной структуры, должны проявлять более сильное связывание с ионами и превосходную катионную селективность.
Кольцевая жёсткая трёхмерная структура сферанда. Это один из сильнейших комплексообразователей, известных для катиона лития. Все другие катионы исключаются, поскольку слишком велики для того, чтобы соответствовать связывающей полости.
Теперь попавший «в лапы» к сферанду или кавитанду катион металла оказывается в очень крепких «объятиях». Однако с той особенностью, что объятия эти открыты лишь для данного рода катионов. Селективность связи сферанда с катионом натрия (Na+) на 10 (!) порядков величины выше его сродства к катиону калия (K+). Отметим и другое: селективность для пары катионов Na+/K+ у сферанда много выше, чем селективность у природных ионофоров, не говоря уж об ионофорах синтетических.
Важное достоинство кавитанда состоит в том, что эта молекула способна принять и прочно удерживать не только ионы металлов, чем отличаются краун-эфиры. Кавитанд «заглатывает» и, так сказать, «держит в зубах» даже небольшие нейтральные молекулы, такие, например, как хлороформ или ацетон.
Другая большая заслуга Дональда Крама — он ввёл в науку новую концепцию «хозяин — гость». Свою Нобелевскую лекцию в Стокгольме Крам так и озаглавил: «Получение молекулярных комплексов типа ″хозяин — гость″ (The Design of Molecular Hosts, Guests, and their Complexes)».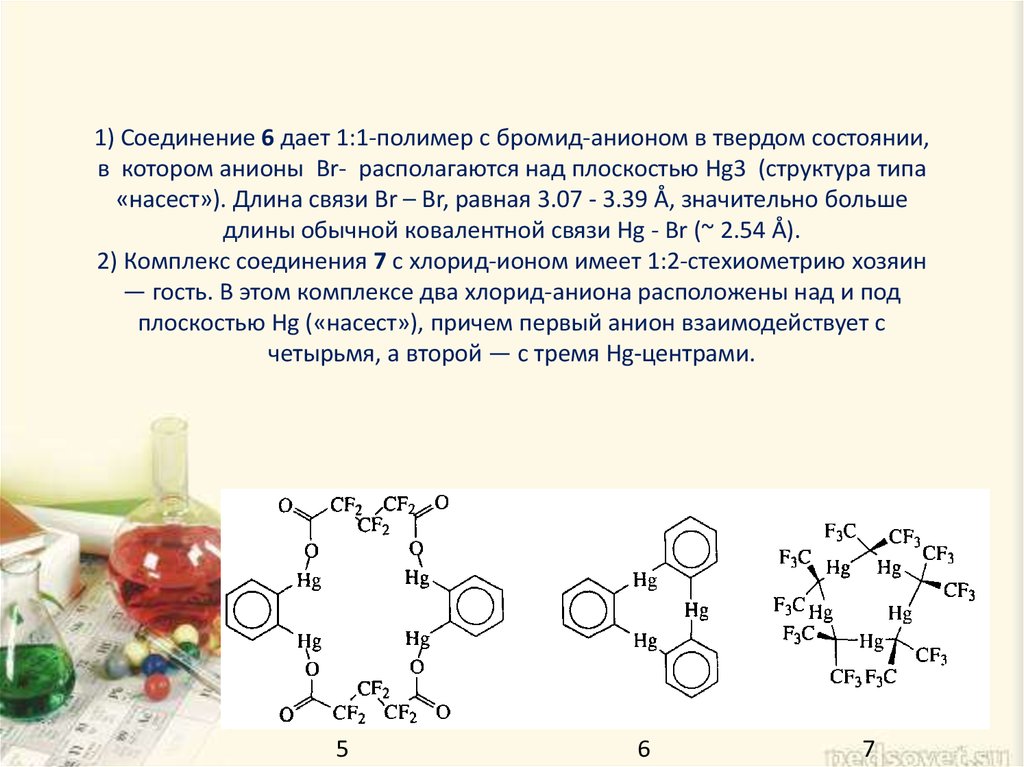 Понятно, что речь идёт всё о том же: о способности большой молекулы («хозяина») специфически «захватывать» и прятать в своём молекулярном «чреве», если можно так выразиться, «гостя» — ион того или иного знака или даже целую небольшую молекулу.
Понятно, что речь идёт всё о том же: о способности большой молекулы («хозяина») специфически «захватывать» и прятать в своём молекулярном «чреве», если можно так выразиться, «гостя» — ион того или иного знака или даже целую небольшую молекулу.
Теперь о вкладе Жан-Мари Лена. Он также был занят попытками создать искусственные химические соединения, обладающие свойствами природных ионофоров. Поиск таких соединений он начал в 1968 году. В результате были синтезированы особые молекулярные структуры — криптанды.
Как и Крам, Лен хотел сконструировать трёхмерный аналог краун-эфиров. Он предвидел, что с помощью таких структур ионы металлов могут быть полностью капсулированы внутри краунподобного «хозяина». Это должно было привести к увеличению катионной селективности молекулы-«хозяина» и к усилению его ионофороподобных транспортных свойств.
Криптанды получили своё название благодаря способности сферически окружать, как бы «погребать в склепе», ионы металлов (греческое «kruptos» означает «скрытый»). Ассоциация со склепом обусловлена наличием у этих соединений внутренней полости, защищённой с трёх сторон атомами кислорода, соединёнными между собой группами Сh3Ch3.
Ассоциация со склепом обусловлена наличием у этих соединений внутренней полости, защищённой с трёх сторон атомами кислорода, соединёнными между собой группами Сh3Ch3.
Было также доказано, что криптанды можно приспособить и для «захватывания» уже не катионов, а анионов.
Химия «хозяин – гость»
Открытие краун-эфиров стимулировало огромную армию химиков-органиков на новые исследования подобного же рода. Была проявлена уйма изобретательности, чтобы придать ожидающей «гостя» внутренней полости макроциклической молекулы-«хозяина» большую организованность и ёмкость.
Ход рассуждений учёных был примерно таков. Если уподобить краун-эфир молекуле-«тарелке», то почему бы не получить ещё, образно выражаясь, молекулы-«чашки», молекулы-«пиалы», молекулы-«кувшины» и прочие мыслимые ёмкости? Ведь тогда «гость», возможно, чувствовал бы себя в них гораздо удобнее.
Концепцию «хозяин — гость» можно иллюстрировать такой простенькой схемой. Маленький «гость» и крупный «хозяин» с полостью, готовой принять «гостя».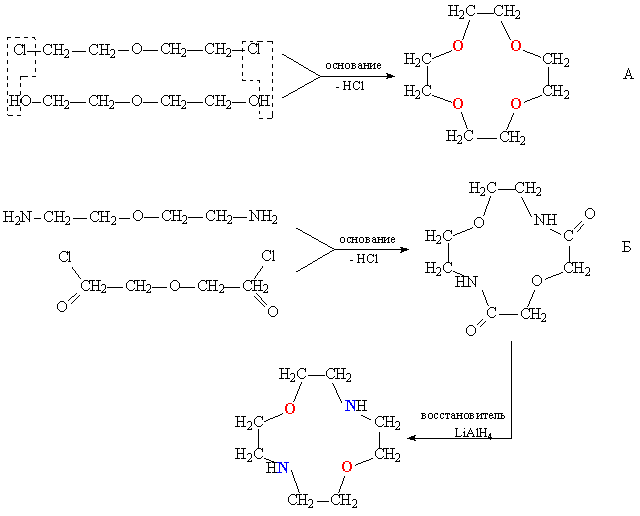 «Гость» прочно удерживается с помощью слабых, нековалентных сил.
«Гость» прочно удерживается с помощью слабых, нековалентных сил.
Так постепенно начала оформляться и претворяться в жизнь идея того, что теперь называется «контейнерная химия». Со времени первой публикации Чарльза Педерсена прошли четыре десятка лет. За это время получены сотни и тысячи новых искусственных ионофоров и их аналогов. Появляются всё более и более сложные структуры. Они подчас имеют замысловатые имена: «корзины», «щётки», «осьминоги». Номенклатура этих диковинных соединений крайне сложна и пока ещё недостаточно разработана. Синтезированное химиками-органиками новое множество хитроумных органических молекул имеет огромное поле применения на практике.
***
Контейнерную химию – в жизнь!
Наука. Соединения, способные образовывать комплексы типа «хозяин — гость» с органическими молекулами, нужны для разделения и очистки органических веществ, их активации и решения множества других научных задач. Сейчас химики-органики пытаются синтезировать «хозяев» для сульфаниламидов, катехоламинов, аминокислот, пептидов, пуриновых и пиримидиновых оснований. И тут возникает возможность создавать лекарственные препараты новых поколений.
И тут возникает возможность создавать лекарственные препараты новых поколений.
Техника. Разрабатываются процессы извлечения ценных цветных и редких металлов из сточных вод промышленных предприятий.
Большая перспектива в использовании краун-соединений открылась в области разделения изотопов. Например, можно отделить кальций-40 от кальция-44, разделить натрий-23 и натрий-24, литий-6 и литий-7, изотопы радиоактивных элементов. Это может иметь огромное значение для создания будущих реакторов термоядерного синтеза.
Синтетические ионофоры широко используют в буровой технике для ликвидации в нефтепроводах пробок, вызванных применением в буровом растворе практически нерастворимого сульфата бария.
На основе краун-соединений созданы специальные противокоррозионные присадки, значительно продлевающие срок службы масел и улучшающие их эксплуатационные свойства.
Иммобилизованные (прикреплённые к подложке-носителю) краун-эфиры являются прекрасными промышленными катализаторами для самых разных химических реакций.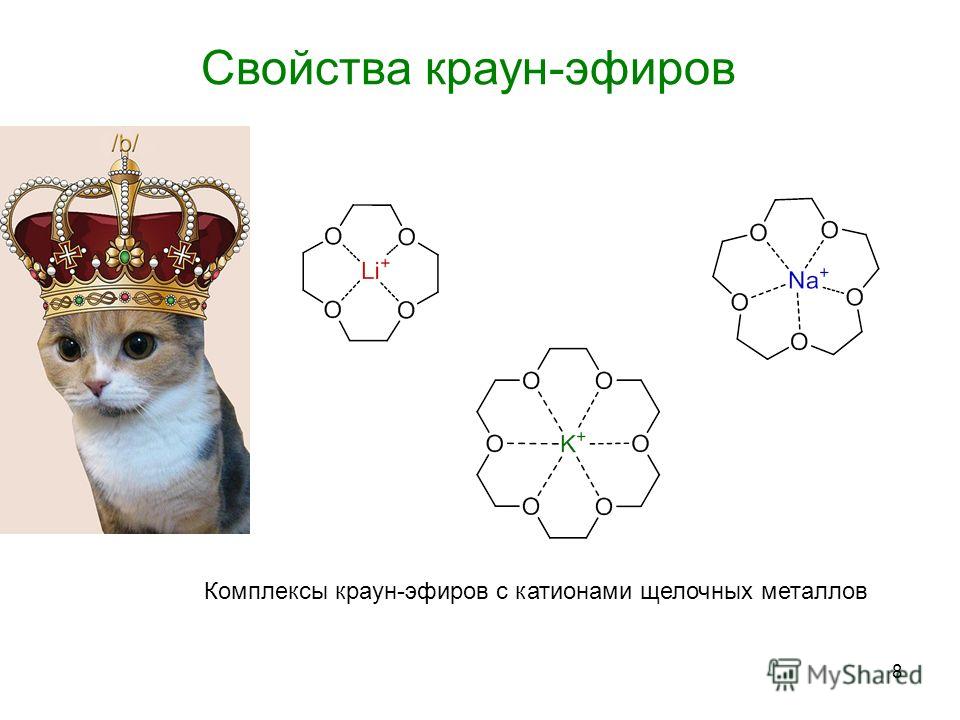
Сельское хозяйство. В животноводстве созданы эффективные добавки к кормам, которые регулируют обмен ионов и, таким образом, значительно улучшают усвоение корма животными. Это, в частности, экономит значительное количество корма для скота.
Некоторые синтезированные ионофоры оказались мощными пестицидами, очень специфичными (то есть действующими избирательно — только на ту или иную мишень) и не загрязняющими окружающую среду.
Медицина. Крауны можно применять как средства для лечения болезней, вызванных избытком или недостатком в организме ионов того или иного металла.
Краун-соединения становятся действенным инструментом регулирования процессов переноса металлов через биологические мембраны. Это создаёт основу и для разработки лекарственных препаратов, направленных на борьбу с заболеваниями, вызванными избытком тяжёлых металлов в организме, или для выведения из организма опасных радиоактивных ионов, таких как цезий -137.
Краун-эфиры: определение, структура, образование и использование
- Автор
Павитра ВГ - Последнее изменение 19-07-2022
Краун Эфиры: Какова общая формула спирта? Да, это \({\rm{R — OH}}\).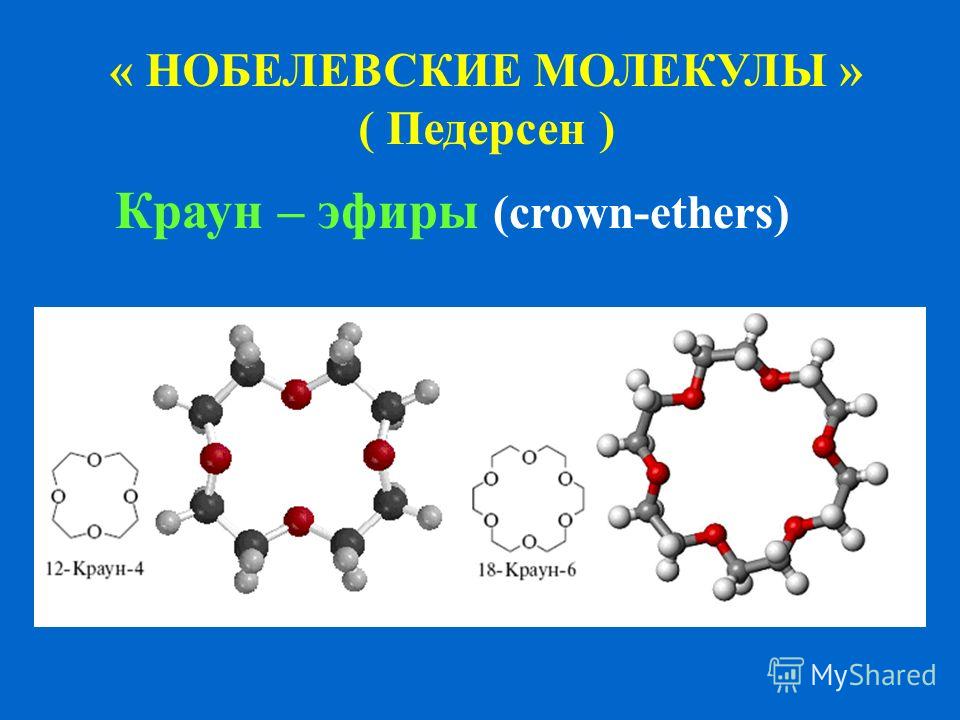 {\rm{3}}}\) гибридизованным. Эфиры полярны, относительно инертны, на них не действуют щелочи, щелочные металлы и разбавленные кислоты, так как они не содержат активной функциональной группы и не имеют двойной или тройной связи.
{\rm{3}}}\) гибридизованным. Эфиры полярны, относительно инертны, на них не действуют щелочи, щелочные металлы и разбавленные кислоты, так как они не содержат активной функциональной группы и не имеют двойной или тройной связи.
Что такое краун-эфиры?
Циклический полиэфир, содержащий четыре или более эфирных связей в кольце из \(12\) или более атомов, называется краун-эфиром. Краун-эфиры получили такое название, потому что их молекулы напоминают кроны.
Примеры: \(15\)-Crown-\(5,{\rm{ }}18\)-Crown-\(6\)
Изучение концепций экзамена на Embibe
Как образуются краун-эфиры ?
Сополимеризация по \({{\rm{S}}_{\rm{N}}}2\) реакции \({\rm{a, 1, 2}}\)-диола и \({\rm{a, 1, 2}}\)-дигалогенид образует простой полиэфир.
Эта реакция заканчивается быстро до образования длинных цепей. Эта реакция имеет большое применение при получении краун-эфиров.
\(18\)-краун-\(6\) имеет восемнадцатичленное кольцо с шестью равномерно расположенными атомами кислорода.
\(18\)-краун-\(6\) — правильный размер для ионов калия, а раствор \({\rm{KMn}}{{\rm{O}}_{\rm{4 }}}\) и \(18\)-краун-\(6\) в бензоле называется фиолетовым бензолом. Это полезный окислитель.
Соединение включения
Краун-эфир особым образом связывает определенные ионы металлов или органические молекулы в зависимости от размера его полости. Коронный эфир называется хозяином, а вид, который он связывает, называется гостем. Комплекс «краун-гость» называется соединением включения.
Пример: \({\rm{Na}}{\rm{.15}}\)-Crown-\(5\)
Практические экзаменационные вопросы
Известно, что краун-эфиры образуют более стабильные комплексы с ионы металлов, чем простые эфиры. Связывание происходит в результате взаимодействия положительно заряженных ионов с несвязывающими электронами атомов кислорода.
Краун-эфиры позволяют неорганическим солям растворяться в неполярных органических растворителях, что позволяет проводить многие реакции в неполярных растворителях.
Пример: \({\rm{KMn}}{{\rm{O}}_{\rm{4}}}\) не растворяется ни в каких неполярных растворителях, но растворяется в неполярном бензоле, если \( \left[ {18} \right]\)-crown-\(6\) добавляется к решению.
Краунэфиры образуют комплексы с положительными ионами, обычно ионами металлов или ионами аммония и замещенными ионами аммония.
Наименование краун-эфиров
Краун-эфиры называются \(\left[ {\rm{X}} \right]\)-crown-\({\rm{Y}}\), где \({\ rm{X}}\) — общее количество атомов в кольце, а \({\rm{Y}}\) — количество атомов кислорода в кольце.
Пример: \(\left[ {15} \right]\)-краун-\(5\) содержит \(15\) атомов в кольце и \(5\) атомов кислорода в кольце.
Попытка имитационных испытаний
Краун-эфиры в качестве катализатора межфазного переноса
Краун-эфиры переносят ионные соединения в органическую фазу. Поэтому краун-эфиры также называют катализаторами межфазного переноса.
Применение краун-эфиров
- Используется в лаборатории в качестве межфазного катализатора.

- Краун-эфиры используются в этерификации, омылении, замещении, реакциях элиминации, образовании карбенов и т. д.
- Он используется при сверхкритической флюидной экстракции микроэлементов металлов из твердых и жидких материалов.
- Применяется при фотоцианировании, разделении керамических смесей, гетероциклизации и т. д.
- Краун-эфир, как и дициклогексил-\(18\)-краун-\(6\), используется при определении золота в геологических пробах.
Криптанды
Молекулярные объекты, содержащие циклический или полициклический набор сайтов связывания, которые содержат три или более сайтов связывания, удерживаемых вместе ковалентными связями, называются криптандами. Образующийся при этом аддукт называется криптатом. Термин криптат обычно ограничивается бициклическими или олигоциклическими молекулярными единицами.
Криптанды широко используются в качестве стационарных фаз благодаря их высокой селективности и более сильной способности связывать катионы, анионы и молекулы. Чем жестче трехмерная структура криптандов, тем выше селективность и специфичность краун-эфиров аналогичного размера.
Чем жестче трехмерная структура криптандов, тем выше селективность и специфичность краун-эфиров аналогичного размера.
Резюме
В статье о краун-эфирах вы получили знания о значении и структуре краун-эфиров на подходящих примерах. Вы также поняли, как называются краун-эфиры, как образуются комплексы включения, что такое криптанды, роль краун-эфира в качестве катализатора межфазного переноса, другие способы использования краун-эфиров и т. д.
Часто задаваемые вопросы (
Часто задаваемые вопросы) Эфиры
Часто задаваемые вопросы, связанные с краун-эфирами, перечислены ниже:
Q.1. Почему их называют краун-эфирами?
Ans : Циклические полиэфиры, содержащие четыре или более эфирных связей в кольце из 12 или более атомов, называются краун-эфирами. Краун-эфиры получили такое название, потому что их молекулярная структура напоминает краун.
Q.2. Как вы делаете краун-эфиры?
Ans : Сополимеризация по \({{{\rm{S}}_{\rm{N}}}2}\) реакции \({{\rm{a,}}\,1 ,\,2}\)-диол и \({{\rm{a,}}\,1,\,2}\)-дигалогенид образуют полиэфир.
Эта реакция заканчивается быстро до образования длинных цепей. Эта реакция имеет большое применение при получении краун-эфиров.
\(18\)-Краун-\(6\) имеет восемнадцатичленное кольцо с шестью равномерно расположенными атомами кислорода.
Q.3. Что такое краун-эфиры и криптаты?
Ans : Циклический полиэфир, содержащий четыре или более эфирных связей в кольце из 12 или более атомов, называется краун-эфиром.
Молекулярные объекты, содержащие ациклический или полициклический набор сайтов связывания, которые содержат три или более сайтов связывания, удерживаемых вместе ковалентными связями, называются криптандами. Образующиеся при этом аддукты называются криптатами.
Q.4. Каковы примеры краун-эфиров?
Ans : Ниже приведены примеры краун-эфиров.
Q.5. Являются ли краун-эфиры плоскими?
Ответ : Да, краун-эфиры представляют собой плоские и жесткие структуры. Краун-эфиры представляют собой циклические полиэфиры, содержащие четыре или более эфирных связей в кольце из 12 или более атомов.
Краун-эфиры представляют собой циклические полиэфиры, содержащие четыре или более эфирных связей в кольце из 12 или более атомов.
Q.6. Являются ли краун-эфиры макроциклами?
Ответ : Да, краун-эфиры являются макроциклами. Он образует соединение включения с щелочными металлами и щелочноземельными металлами.
Если у вас есть какие-либо вопросы по поводу Crown Ethers или в целом по этой статье, отправьте нам сообщение через поле для комментариев ниже, и мы свяжемся с вами как можно скорее.
Биомедицинские возможности краун-эфиров: перспективные противоопухолевые средства
Обзор
. 2008 Октябрь; 3 (10): 1478-92.
doi: 10.1002/cmdc.200800118.
Мариета Краль
1
, Льерка Тусек-Божич, Лео Фрканец
принадлежность
- 1 Отделение молекулярной медицины, Институт Рудера Босковича, Bijenicka cesta 54, 10002 Загреб, Хорватия.
 [email protected]
[email protected]
PMID:
18683175
DOI:
10.1002/cmdc.200800118
Обзор
Marijeta Kralj et al.
ХимМедХим.
2008 Октябрь
. 2008 Октябрь; 3 (10): 1478-92.
doi: 10.1002/cmdc.200800118.
Авторы
Мариета Краль
1
, Льерка Тусек-Божич, Лео Фрканец
принадлежность
- 1 Отделение молекулярной медицины, Институт Рудера Босковича, Bijenicka cesta 54, 10002 Загреб, Хорватия.
 [email protected]
[email protected]
PMID:
18683175
DOI:
10.1002/cmdc.200800118
Абстрактный
Краун-эфиры представляют огромный интерес и значение в химии, биохимии, материаловедении, катализе, процессах разделения, транспорта и инкапсуляции, а также при разработке и синтезе различных синтетических систем со специфическими свойствами, разнообразными возможностями и программируемыми функциями. Классические краун-эфиры представляют собой макроциклические полиэфиры, содержащие от 3 до 20 атомов кислорода, отделенных друг от друга двумя или более атомами углерода. Они исключительно универсальны в селективном связывании ряда ионов металлов и различных органических нейтральных и ионных соединений. В настоящее время краун-эфиры изучаются и используются во множестве приложений, выходящих за рамки их традиционного места в химии. В этом обзоре представлены дополнительные применения и постоянно растущий биомедицинский потенциал этих интригующих соединений с особым акцентом на перспективы их применения в качестве противоопухолевых средств. Мы считаем, что следует поощрять дальнейшие исследования в этом направлении, поскольку краун-соединения могут либо индуцировать токсичность, отличную от токсичности обычных противоопухолевых препаратов, либо дополнять используемые в настоящее время лекарства, обеспечивая тем самым ценное дополнение к терапии.
В настоящее время краун-эфиры изучаются и используются во множестве приложений, выходящих за рамки их традиционного места в химии. В этом обзоре представлены дополнительные применения и постоянно растущий биомедицинский потенциал этих интригующих соединений с особым акцентом на перспективы их применения в качестве противоопухолевых средств. Мы считаем, что следует поощрять дальнейшие исследования в этом направлении, поскольку краун-соединения могут либо индуцировать токсичность, отличную от токсичности обычных противоопухолевых препаратов, либо дополнять используемые в настоящее время лекарства, обеспечивая тем самым ценное дополнение к терапии.
Похожие статьи
Противоопухолевый потенциал краун-эфиров: взаимосвязь структура-активность, нарушения клеточного цикла и исследования гибели клеток ряда ионофоров.
Марьянович М., Краль М., Супек Ф.
 , Фрканец Л., Пьянтанида И., Смук Т., Тусек-Божич Л.
, Фрканец Л., Пьянтанида И., Смук Т., Тусек-Божич Л.
Марьянович М. и соавт.
J Med Chem. 2007 8 марта; 50 (5): 1007-18. дои: 10.1021/jm061162u. Epub 2007, 15 февраля.
J Med Chem. 2007.PMID: 17300184
Разработка металлокомплексов аза-краун-эфира в качестве искусственной гидролазы.
Ю Л., Ли Ф. З., Ву Д. Ю., Се Д. К., Ли С.
Ю Л и др.
Дж. Инорг Биохим. 2016 Январь; 154: 89-102. doi: 10.1016/j.jinorgbio.2015.09.011. Epub 2015 3 октября.
Дж. Инорг Биохим. 2016.PMID: 26460062
Обзор.
Последние достижения в области асимметричного фазового катализа.
Оой Т., Маруока К.
Оои Т. и др.
Angew Chem Int Ed Engl. 2007;46(23):4222-66. doi: 10.1002/anie.200601737.
Angew Chem Int Ed Engl. 2007.
PMID: 17525926
Обзор.
Каликсароматики с мостиками азота и кислорода: синтез, структура, функционализация и молекулярное распознавание.
Ван MX.
Ван МХ.
Acc Chem Res. 2012 21 февраля; 45 (2): 182-95. doi: 10.1021/ar200108c. Epub 2011 11 августа.
Acc Chem Res. 2012.PMID: 21834499
Краун-эфиры: сенсоры для ионов и молекулярные каркасы для материалов и биологических моделей.
Гокель Г.В., Леви В.М., Вебер М.Е.
Гокель Г.В. и др.
Chem Rev. 2004 May; 104(5):2723-50. doi: 10.1021/cr020080k.
Химическая редакция 2004 г.PMID: 15137805
Обзор.
Аннотация недоступна.
Посмотреть все похожие статьи
Цитируется
Циклометаллированные комплексы платины(II) с малыми кольцами краун-эфира: правильный выбор мостикового дифосфана для координации катионов калия.

Лусио-Мартинес Ф., Рейгоса Ф., Бермудес Б., Адамс Х., Перейра М.Т., Вила Х.М.
Лусио-Мартинес Ф. и др.
АСУ Омега. 2022 14 октября; 7 (42): 37256-37263. doi: 10.1021/acsomega.2c03526. Электронная коллекция 2022 25 октября.
АСУ Омега. 2022.PMID: 36312351
Бесплатная статья ЧВК.Флуоресцентные и фосфоресцирующие азотсодержащие гетероциклы и краун-эфиры: применение в биологии и фармацевтике.
Улла Ф., Улла С., Хан МИД, Мустаким М., Парача Р.Н., Рехман МФУ, Канвал Ф., Хассан СГУ, Бунгау С.
Улла Ф. и др.
Молекулы. 2022 6 октября; 27 (19): 6631. doi: 10,3390/молекулы27196631.
Молекулы. 2022.PMID: 36235167
Бесплатная статья ЧВК.Обзор.
Захват атомов щелочных металлов на поверхности краун-эфирами в сверхвысоком вакууме.

Стреданский М., Турко Э., Фэн З., Костантини Р., Комелли Г., Вердини А., Флореано Л., Морганте А., Дри С., Коссаро А.
Стреданский М. и соавт.
Наномасштаб Adv. 2019 2 апр; 1(5):1721-1725. дои: 10.1039/c9na00144a. Электронная коллекция 2019 15 мая.
Наномасштаб Adv. 2019.PMID: 36134236
Бесплатная статья ЧВК.Взаимодействие краун-эфиров с транспортером ABCG2 и их роль в реверсировании множественной лекарственной устойчивости.
Миоч М., Тельбиш А., Радман К., Бертоша Б., Шумановац Т., Саркади Б., Краль М.
Миоч М. и соавт.
Гистохим клеточной биологии. 2022 г., сен; 158 (3): 261–277. doi: 10.1007/s00418-022-02106-z. Epub 2022 1 июня.
Гистохим клеточной биологии. 2022.PMID: 35648291
Комплексообразование биологически важных (моно- и двухвалентных) катионов металлов с кукурбитурилами: оценка DFT/SMD ключевых факторов, управляющих распознаванием «хозяин-гость».

