Содержание
Строение, изомерия и гомологический ряд спиртов
Гидроксисоединения – это органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Гидроксисоединения делят на спирты и фенолы.
Строение, изомерия и гомологический ряд спиртов
Химические свойства спиртов
Способы получения спиртов
| Спирты – это гидроксисоединения, в которых группа ОН соединена с алифатическим углеводородным радикалом R-OH. Если гидроксогруппа ОН соединена с бензольным кольцом, то вещество относится к фенолам. |
Общая формула предельных нециклических спиртов: CnH2n+2Om, где m ≤ n.
По числу гидроксильных групп:
- одноатомные спирты — содержат одну группу -ОН. Общая формула CnH2n+1OH или CnH2n+2O.
- двухатомные — содержат две группы ОН. Общая формула CnH2n(OH)2 или CnH2n+2O2.
- трехатомные спирты — содержат три группы ОН. Общая формула CnH2n-1(OH)3 или CnH2n+2O3.
Двухатомные спирты с двумя и тремя гидроксогруппами у одного атома углерода R‒CH(OH)2 или R-C(OH)3 неустойчивы, от них легко отрывается вода и образуется карбонильное соединение.
Классификация по числу углеводородных радикалов у атома углерода при гидроксильной группе
- Первичные спирты – группа ОН соединена с первичным атомом углерода.
 Например, этанол СН3–СН2–ОН.
Например, этанол СН3–СН2–ОН. - Вторичные спирты – группа ОН соединена с вторичным атомом углерода. Например, пропанол-2: СН3–СН(СН3)–ОН.
- Третичные спирты – группа ОН соединена с третичным атомом углерода. Например, 2-метилпропанол-2: (СН3)3С–ОН.
- Метанол не относится ни к первичным, ни к вторичным, ни к третичным спиртам.
Классификация по строению углеводородного радикала
- Предельные спирты – группа ОН соединена с предельным радикалом. Например, пропанол-1: СН3–СН2–СН2–ОН.
- Непредельные спирты – группа ОН соединена с непредельным радикалом. Например, алкенолы: СН2=СН–СН2–ОН.
Непредельные спирты, в которых гидроксильная группа соединена с атомом углерода при двойной связи (алкенолы), неустойчивы и изомеризуются в соответствующие карбонильные соединения.
- Ароматические спирты – содержат в радикале ароматическое кольцо, не связанное непосредственно с группой ОН. Например, бензиловый спирт.
В молекулах спиртов, помимо связей С–С и С–Н, присутствуют ковалентные полярные химические связи О–Н и С–О.
| Электроотрицательность кислорода (ЭО = 3,5) больше электроотрицательности водорода (ЭО = 2,1) и углерода (ЭО = 2,4). |
Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода:
| Атом кислорода в спиртах находится в состоянии sp3-гибридизации. |
В образовании химических связей с атомами C и H участвуют две 2sp3-гибридные орбитали, а еще две 2sp3-гибридные орбитали заняты неподеленными электронными парами атома кислорода.
Поэтому валентный угол C–О–H близок к тетраэдрическому и составляет почти 108о.
Водородные связи и физические свойства спиртов
Спирты образуют межмолекулярные водородные связи.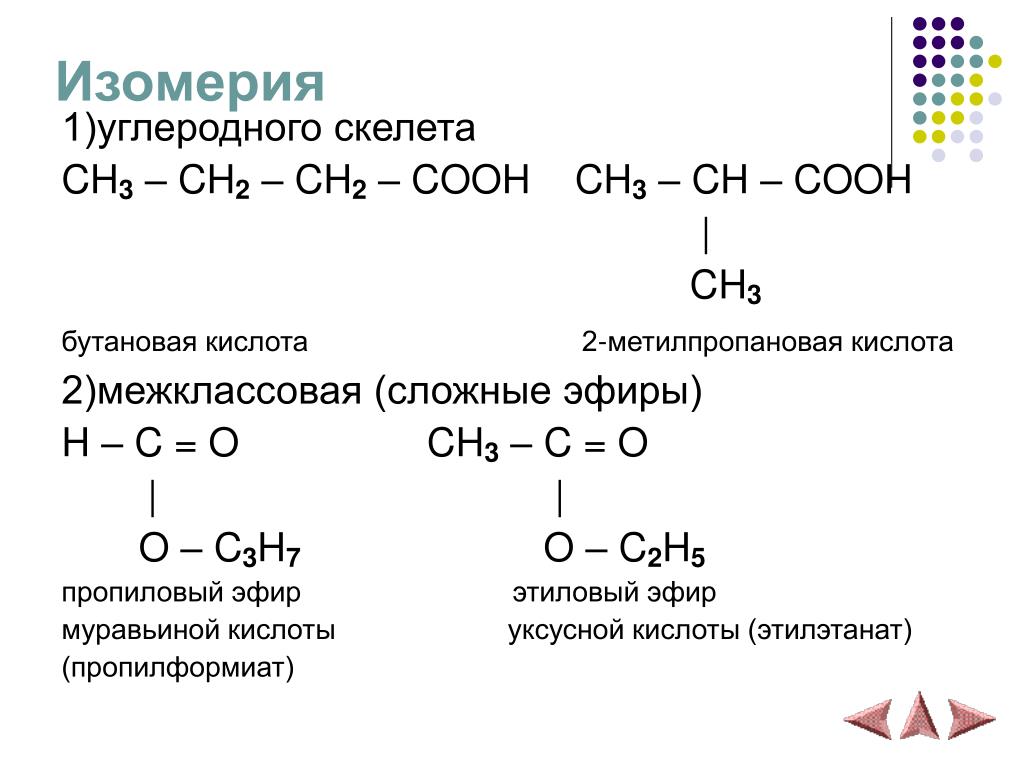 Водородные связи вызывают притяжение и ассоциацию молекул спиртов:
Водородные связи вызывают притяжение и ассоциацию молекул спиртов:
Поэтому спирты – жидкости с относительно высокой температурой кипения (температура кипения метанола +64,5оС). Температуры кипения многоатомных спиртов и фенолов значительно выше.
Таблица. Температуры кипения некоторых спиртов и фенола.
| Название вещества | Температура кипения |
| Метанол | 64 |
| Этанол | 78 |
| Пропанол-1 | 92 |
| Бутанол-1 | 118 |
| Этиленгликоль | 196 |
| Фенол | 181,8 |
Водородные связи образуются не только между молекулами спиртов, но и между молекулами спиртов и воды. Поэтому спирты очень хорошо растворимы в воде. Молекулы спиртов в воде гидратируются:
Чем больше углеводородный радикал, тем меньше растворимость спирта в воде. Чем больше ОН-групп в спирте, тем больше растворимость в воде. Чем больше ОН-групп в спирте, тем больше растворимость в воде. |
Низшие спирты (метанол, этанол, пропанол, изопропанол, этиленгликоль и глицерин) смешиваются с водой в любых соотношениях.
- По систематической номенклатуре к названию углеводорода добавляют суффикс «-ОЛ» и цифру, указывающую номер атома углерода, к которому присоединена гидроксильная группа.
Нумерация ведется от ближайшего к ОН-группе конца цепи.
- По радикально-функциональной номенклатуре названия спиртов составляют от названий углеводородных радикалов, соединенных с группой ОН, с добавлением слова «спирт».
Например: СН3ОН – метиловый спирт, С2Н5ОН – этиловый спирт и т.д.
- В названиях многоатомных спиртов количество групп ОН указывают суффиксами -диол в при наличии двух ОН-групп, -триол при наличии трех ОН-групп и т.
 д. После этого добавляют номера атомов углерода, связанных с гидроксильными группами.
д. После этого добавляют номера атомов углерода, связанных с гидроксильными группами.
Например, пропандиол-1,2 (пропиленгликоль):
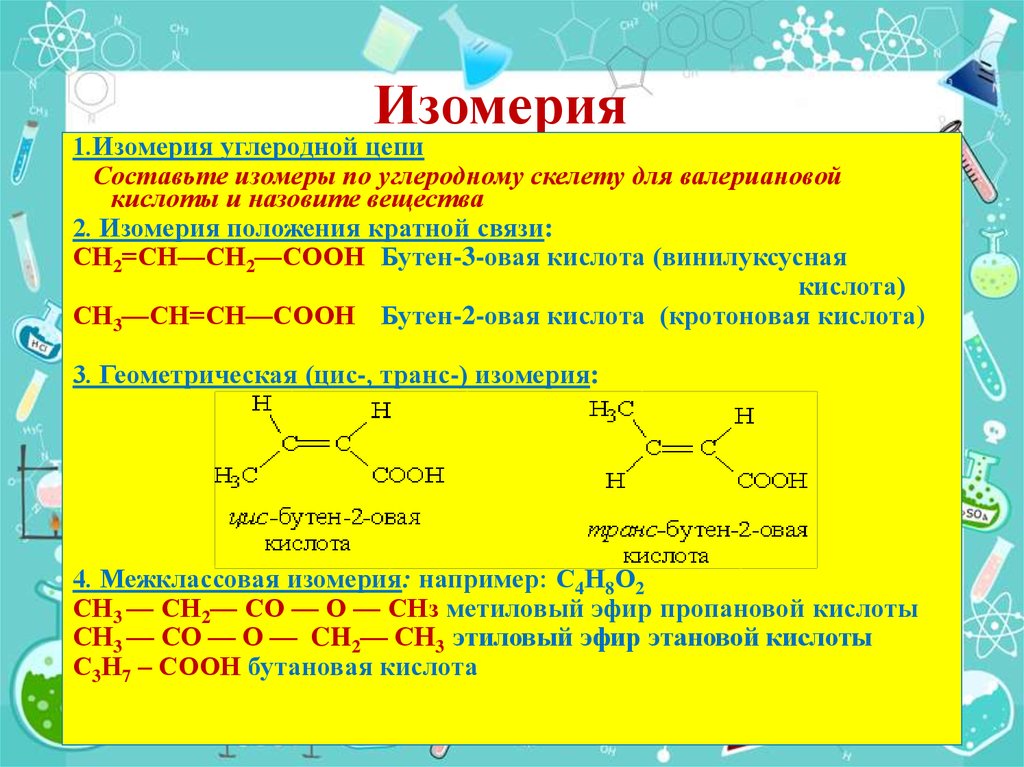
Структурная изомерия
Для спиртов характерна структурная изомерия – изомерия углеродного скелета, изомерия положения гидроксильной группы и межклассовая изомерия.
Структурные изомеры — это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
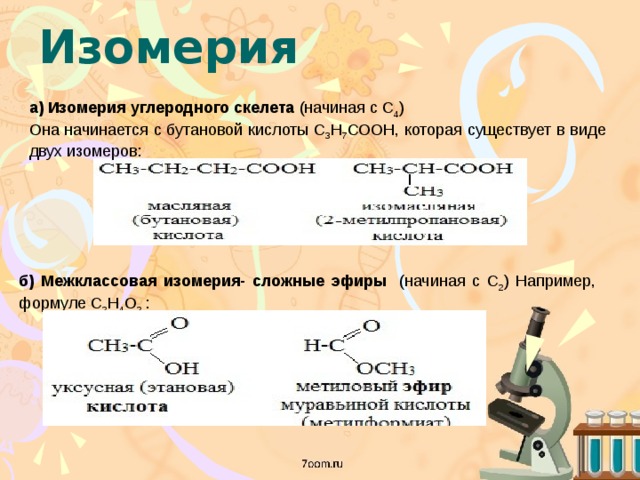
Изомеры углеродного скелета характерна для спиртов, которые содержат не менее четырех атомов углерода.
| Например. Формуле С4Н9ОН соответствуют четыре структурных изомера, из них два различаются строением углеродного скелета |
| Бутанол-1 | 2-Метилпропанол-1 |
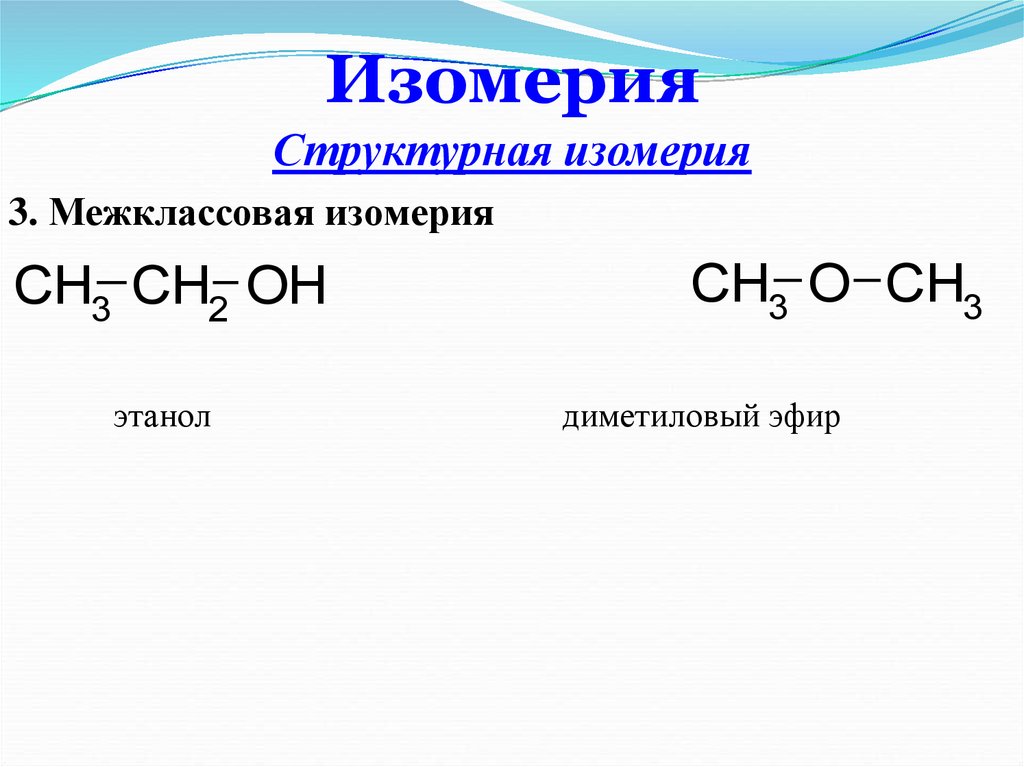
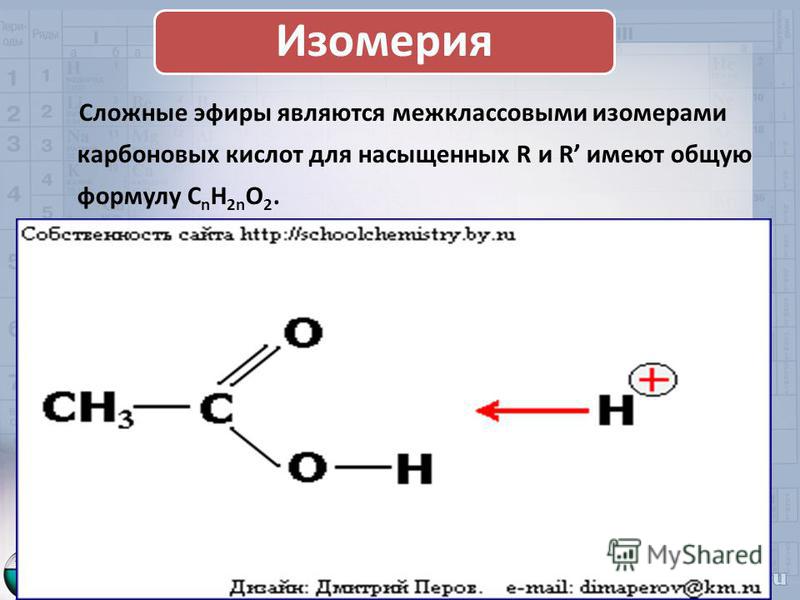
Межклассовые изомеры — это вещества разных классов с различным строением, но одинаковым составом. Спирты являются межклассовыми изомерами с простыми эфирами. Общая формула и спиртов, и простых эфиров — CnH2n+2О.
Спирты являются межклассовыми изомерами с простыми эфирами. Общая формула и спиртов, и простых эфиров — CnH2n+2О.
| Например. Межклассовые изомеры с общей формулой С2Н6О: этиловый спирт СН3–CH2–OH и диметиловый эфир CH3–O–CH3 |
| Этиловый спирт | Диметиловый эфир |
| СН3–CH2–OH | CH3–O–CH3 |
Изомеры с различным положением группы ОН отличаются положением гидроксильной группы в молекуле. Такая изомерия характерна для спиртов, которые содержат три или больше атомов углерода.
| Например. Пропанол-1 и пропанол-2 |
| Пропанол-1 | Пропанол-2 |
Понравилось это:
Нравится Загрузка. ..
..
|
Изомерия эфиров: определение, виды, примеры
- Автор
Сушмита Рут - Последнее изменение 10.11.2022
Изомерия в эфирах: Все те соединения, которые имеют одинаковую молекулярную формулу, но различаются по химическим свойствам, известны как изомеры. Изомерия возникает из-за того, что атомы в молекулярной формуле могут быть организованы несколькими способами с образованием соединений с различными физическими и химическими свойствами, известных как изомеры. В спиртах атомы, связанные с атомом кислорода, включают водород и углерод.
Когда атом водорода заменяется другим набором атомов углерода, спирты образуют изомерные структуры, известные как простые эфиры. Например, диметиловый эфир изомерен с этанолом, а метилэтиловый эфир изомерен с пропанолом.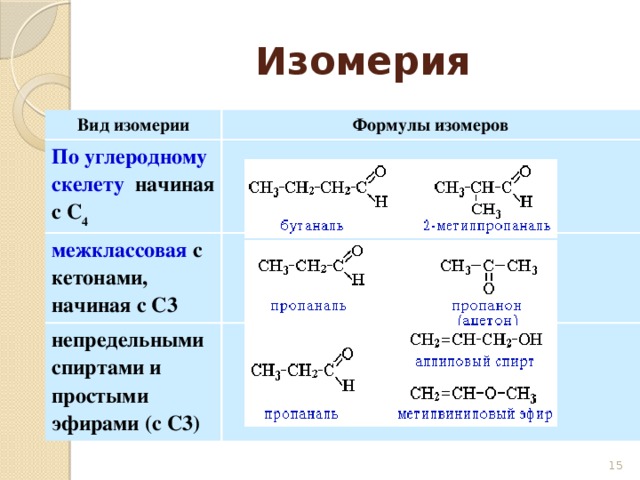 Давайте разберемся, как эфиры проявляют различную изомерию.
Давайте разберемся, как эфиры проявляют различную изомерию.
Простые эфиры представляют собой тип органических молекул, в которых две углеводородные группы (алкильные или арильные) связаны вместе одним атомом кислорода. Он представлен общей формулой \({\rm{R — O — R}}\)’, как показано ниже. 9\circ }}}\)
Типы эфиров
В зависимости от групп в \({\text{R}}\) и \({\text{R}}\)’ эфиры классифицируются на два типа:
1. Простые эфиры или симметричные эфиры: Эти простые эфиры состоят из одной и той же алкильной группы на обоих концах атома кислорода. Например:
2. Смешанные эфиры или асимметричные эфиры: Эти эфиры состоят из разных алкильных групп на обоих концах атома кислорода. Например-
Изомерия в эфире
Изомерия возникает, когда два или более химических соединения имеют одинаковую молекулярную формулу, но отличаются структурным расположением атомов. Соединения, проявляющие явление изомерии, известны как изомеры и различаются по физическим и химическим свойствам.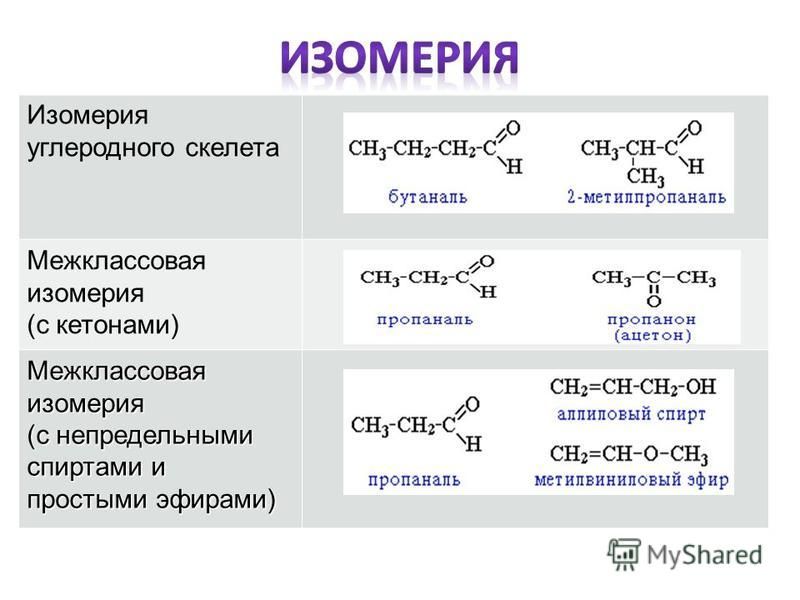 Алифатические эфиры могут иметь два разных типа изомеров. Это:
Алифатические эфиры могут иметь два разных типа изомеров. Это:
1. Цепная изомерия
Простые эфиры, имеющие одинаковую молекулярную формулу, но разные скелеты углеродных цепей по обе стороны от атома кислорода, называются цепными изомерами. Например, \({{\rm{C}}_4}{{\rm{H}}_{10}}{\rm{O}}\) имеет два изомера цепи. Это — этоксиэтан и метоксипропан 9.0011
\({\rm{C}}{{\rm{H}}_3}{\rm{C}}{{\rm{H}}_2}{\rm{OC}}{{\rm{ H}}_2}{\rm{C}}{{\rm{H}}_3}\) и \({\rm{C}}{{\rm{H}}_3}{\rm{C} }{{\rm{H}}_2}{\rm{C}}{{\rm{H}}_2}{\rm{OC}}{{\rm{H}}_3}\)
2. Функциональная изомерия
Соединения с одинаковой молекулярной формулой, но разными функциональными группами проявляют функциональную изомерию. Эфиры изомерны со спиртом.
Пример: диметиловый эфир изомерен с этанолом, а метилэтиловый эфир изомерен с пропанолом
3. Метамерия
Метамеры – это изомеры с одинаковой химической формулой, но разными алкильными группами (вокруг функциональной группы).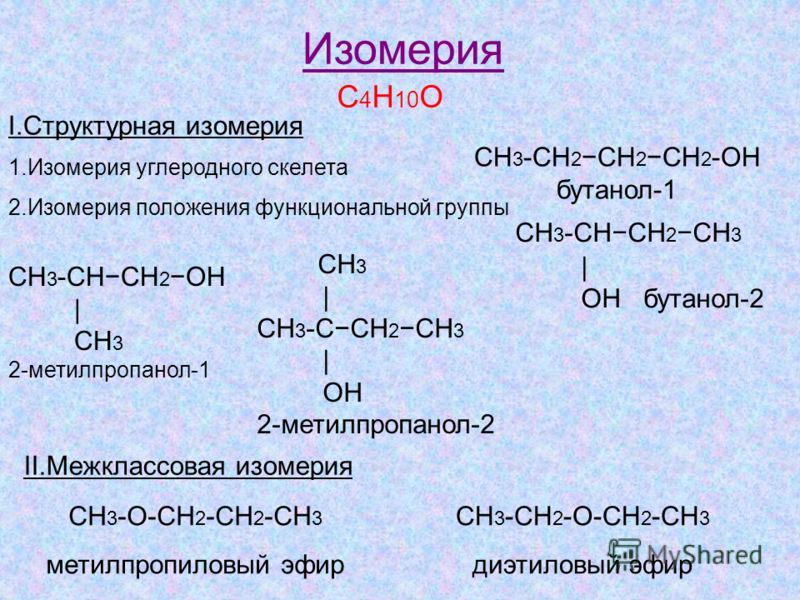 Метамерию проявляют диэтиловый эфир и метилпропиловый эфир. Оба имеют одинаковую химическую формулу; однако алкильные группы по бокам разные.
Метамерию проявляют диэтиловый эфир и метилпропиловый эфир. Оба имеют одинаковую химическую формулу; однако алкильные группы по бокам разные.
Резюме
Структурные формулы этилового спирта и диметилового эфира различны. Однако их молекулярная формула одинакова: \({{\rm{C}}_2}{{\rm{H}}_6}{\rm{O}}.\) Эти соединения не только имеют разные структурные формулы , но и характеристики у них разные. В результате молекулярная формула может представлять несколько соединений. Изомерия — термин для этого явления. Изомерия состоит из двух слов: iso и meros, которые означают «то же самое» и «части».
Простые эфиры представляют собой органические соединения, в которых атом кислорода присутствует между алкильными или арильными группами. Пространственное расположение различных атомов в эфирах приводит к цепной изомерии, функциональной изомерии и метамерии. В этой статье мы обсудили различную изомерию эфиров вместе с их классификацией. Мы также узнали разницу между простыми эфирами и смешанными эфирами.
F AQs
Q.1. Какова общая формула эфиров?
Ответ: Он представлен общей формулой \({\rm{R – O – R}}\)’. \({\text{R}}\)
,’ т. е. углеводородная группа в формуле может быть такой же, как \({\text{R}}\), или другой.
Q.2. Что такое изомерия функциональных групп в эфирах?
Ответ: Простой эфир и одноатомный спирт, содержащие одинаковое количество атомов углерода , являются функциональными изомерами. Пример: \({\rm{C}}{{\rm{H}}_3} — {\rm{O}} — {\rm{C}}{{\rm{H}}_3}\) диметил эфир и \({\rm{C}}{{\rm{H}}_3}{\rm{C}}{{\rm{H}}_2}{\rm{OH}}\) этиловый спирт функциональные изомеры.
Q.3. Какой вид изомерии характерен для диэтилового эфира и метилпропилового эфира?
Ответ: Молекулы диэтилового эфира и метилпропилового эфира имеют одинаковое число атомов (четыре атома углерода, один атом кислорода и десять атомов водорода). Таким образом, их можно было рассматривать как «метамеры» в старой номенклатуре.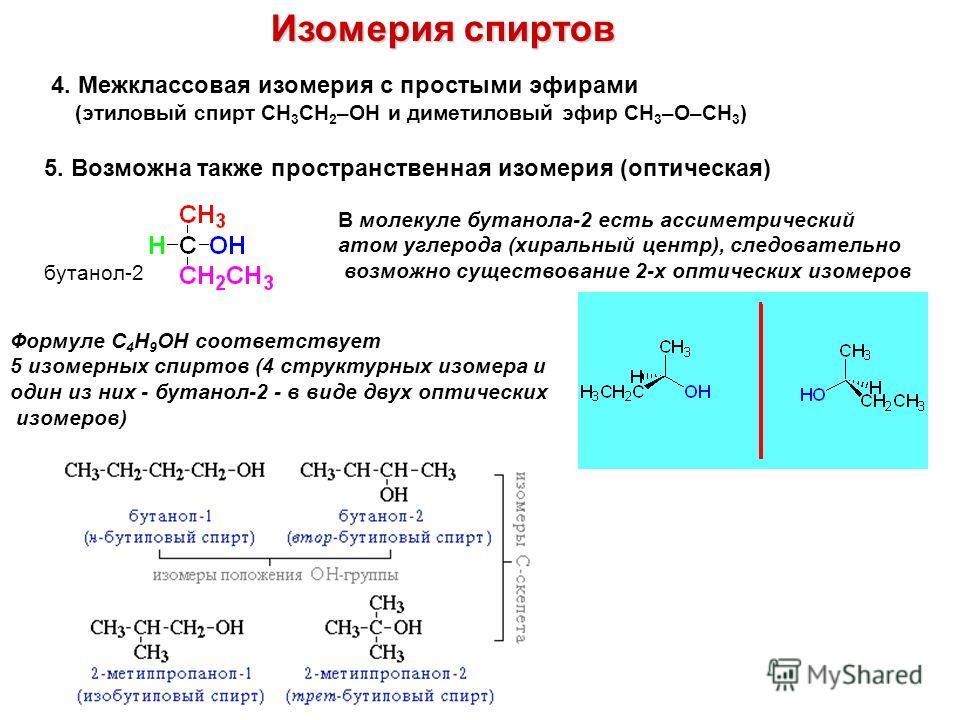 Поскольку положение атома кислорода и разветвление углеродных фрагментов различаются, эти молекулы теперь называются «конституционными изомерами».
Поскольку положение атома кислорода и разветвление углеродных фрагментов различаются, эти молекулы теперь называются «конституционными изомерами».
Вопрос 4. Как связаны диметиловый эфир и этанол?
Ответ: Этанол и диметиловый эфир образуют пару функциональных изомеров.
Q.5. Чем отличается цепная изомерия от метамерии?
Ответ: Основное различие между позиционной изомерией и метамерией состоит в том, что при позиционной изомерии изменяется положение функциональной группы, тогда как при метамерии изменяется тип алкильных групп по бокам функциональной группы.
Изомерия функциональных групп | Творческая химия
Что это такое?
Функциональная изомерия возникает, когда вещества имеют одинаковую молекулярную формулу, но разные функциональные группы. Это означает, что функциональные изомеры принадлежат к разным гомологическим рядам. Вы не встретите их на GCSE Chemistry, но вы столкнетесь с ними на уровне A.
Существуют изомеры трех функциональных групп, о которых вам необходимо знать:
- спирты и простые эфиры
- альдегиды и кетоны
- Карбоновые кислоты и сложные эфиры
Что здесь?
Вы можете увидеть модели:
- этанол и метоксиметан — изомеры функциональных групп C 2 H 6 O
- пропаналь и пропанон — изомеры C по функциональным группам 3 H 6 O
- пропановая кислота и метилэтаноат — изомеры C 3 H 6 O 2 9 по функциональным группам0004
Это типичные молекулы, встречающиеся на уровне A. Вы должны быть готовы идентифицировать изомеры функциональных групп для таких простых органических соединений, как эти, а также уметь давать им названия.
Дважды нажмите, чтобы остановить и перезапустить каждую анимацию.
×
атомные метки
модель шарика и палочки
модель заполнения пространства
вид в перспективе
этанол
CH
3 CH 2 OH
метоксиметан0165
СН 3 ОСН 3
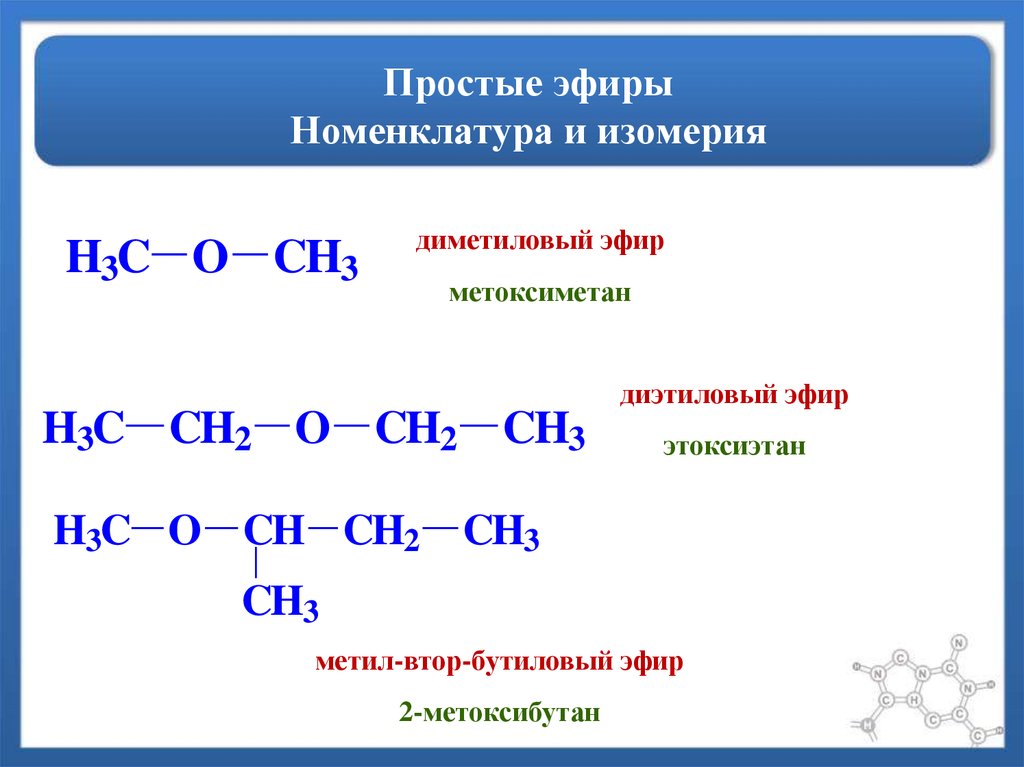
Спирты и эфиры
Функциональной группой спиртов является гидроксильная группа —ОН.
Функциональная группа простых эфиров: R 1 –O–R 2 . Символы R 1 и R 2 обозначают структуры остальной части молекулы:
- они могут быть одинаковыми или разными
- , если один из атомов водорода, соединение содержит гидроксильную группу и не является эфиром.
R 1 и R 2 представляют собой метильные группы -CH 3 в метоксиметане.
пропаналь
CH
3 CH 2 CHO
пропанон
CH
3 COCH 3 12
8
Альдегиды и кетоны
Альдегиды и кетоны имеют карбонильную группу C=O. Эта функциональная группа может находиться в разных положениях:
- в альдегидах присоединен к одному или двум атомам водорода.
- в кетонах присоединяется к двум атомам углерода.
пропановая кислота
CH
3 CH 2 COOH
метилэтаноат
CH
3 COOCH 5
Карбоновые кислоты и сложные эфиры
Имеют разные функциональные группы:
- карбоновые кислоты имеют карбоксильную группу —COOH
- сложные эфиры имеют функциональную группу R 1 COOR 2
Символы R 1 и R 2 обозначают структуру остальной части молекулы:
- они могут быть одинаковыми или разными
- , если один из атомов водорода, соединение содержит карбоксильную группу и не является сложным эфиром.


 Например, этанол СН3–СН2–ОН.
Например, этанол СН3–СН2–ОН. д. После этого добавляют номера атомов углерода, связанных с гидроксильными группами.
д. После этого добавляют номера атомов углерода, связанных с гидроксильными группами.