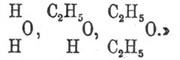3.3 Гидролиз сложных эфиров. Гидролиз сложных эфиров
3.3 Гидролиз сложных эфиров. Реакции ацилирования
Похожие главы из других работ:
Оптимизация методик определения концентрации железа (III) в полиэлектролитных микрокапсулах и магнитоуправляемых липосомах
1. Литературный обзор. Характеристика методов определения концентрации химических элементов в сложных соединениях
В последнее время широко применяются лекарства в виде коллоидов микроскопических капсул и липосом [4,5], которые применяются для лечения определенных заболеваний...
Полимераналогичные превращения хитозана
ГИДРОЛИЗ
Опубликован ряд обзорных работ по гидролизу хитозана, среди них следует отметить работу Мак-Барнея, который рассматривает различие между реакциями, протекающими в растворе и в гетерогенной среде, и кинетику этих реакций[2]...
Понятие и биологическая роль ферментов
1.2 Особенности строения простых и сложных ферментов. Преимущества перед химическими катализаторами
По строению ферменты могут быть однокомпонентными, простыми белками, и двухкомпонентными, сложными белками. Во втором случае в составе фермента обнаруживается не только белковый компонент - апофермент (apoenzyme)...
Проектирование производства фосфорсодержащего вещества
Механизм реакции переэтерификации эфиров кислот трехвалентного фосфора
Механизм реакции переэтерификации эфиров кислот трехвалентного фосфора подробно не изучен. Предполагается, что механизм этой реакции состоит в чередующихся процессах присоединения протона к атому фосфора...
Реакции ацилирования
1.4 Реакции ацилирования сложных эфиров сложными эфирами. Конденсации Кляйзена и Дикмана
При обработке сложных эфиров, сильным основанием (этилат натрия), происходит конденсация, приводящая к кетоэфирам. Эта реакция называется конденсацией Кляйзена: Необходимо отметить...
Реакции ацилирования
3.4 Гидролиз амидов
Незамещенные амиды RCONh3 способны гидролизоваться под действием как кислотных, так и основных катализаторов; при этом образуются соответствующая свободная кислота и ион аммония или соль кислоты и аммиак...
Реакции ацилирования
3.8 Алкоголиз сложных эфиров. Переэтерификация
Переэтерификация катализируется кислотами или основаниями. Это обратимая реакция и равновесие необходимо смещать в желаемую сторону...
Свойства краун-эфиров и фуллеренов
1. Структура и свойства краун-эфиров и фуллеренов
...
Свойства краун-эфиров и фуллеренов
1.1.2 Номенклатура краун-эфиров
Формально все краун-эфиры можно отнести к классу гетероциклических соединений, однако необычные свойства таких соединений позволили выделить их в самостоятельный класс...
Свойства краун-эфиров и фуллеренов
1.1.3 Получение краун-эфиров
Существует множество методов синтеза краун - соединений, однако наиболее важный аспект любого из них заключается в подавлении побочных реакций, приводящих к линейным полимерам, для преимущественного протекания реакции циклизации...
Свойства краун-эфиров и фуллеренов
1.1.4 Применение краун-эфиров
Применение краун-эфиров определяется, прежде всего, их избирательной способностью захватывать катионы определенного размера. Наибольшее распространение получили краун-эфиры, содержащие только гетероатомы О...
Свойства краун-эфиров и фуллеренов
1.3 Монослой на основе фуллеренов и краун-эфиров
Проведенные исследования [3-5] показали, что молекулы С60 при степени покрытия 0,4-0,5 начинают агрегировать уже в газовой фазе, что исключает возможность формирования монослоя и, как следствие...
Сущность метода квазистационарных концентраций
1. Термодинамика и кинетика сложных химических реакций. Метод квазистационарных концентраций
...
Трансформация экополлютантов в окружающей среде
Гидролиз
В ходе гидролиза химиката, имеющего в составе молекул определенные функциональные группы R-X, происходит присоединение воды. Примером таких процессов могут служить реакции омыления сложных эфиров...
Тригалогениды галлия
1.4.1 Гидролиз
Безводный трифторид галлия практически нерастворим в воде и в растворе почти не диссоциирует. Однако гидрат трифторида галлия GaF3·3h3O, образующийся при действии фтороводородной кислоты на оксид или гидроксид галлия...
him.bobrodobro.ru
Сложные эфиры (эстеры)
Эфиры карбоновых кислот широко распространены в природе. Наибольшее значение из них имеют жиры и масла, представляющие собой эфиры глицерина и карбоновых кислот. Циклические сложные эфиры называют лактонами



хиры и масла g-бутиролактон d-валеролактон
Сложные эфиры низших спиртов и карбоновых кислот представляют собой летучие жидкости с приятным запахом.



этилформиат изопентилацетат октилацетат
RumBananaOrangeапельсин



етилбутаноат этилбутаноат метил-2-аминобензоат
(метилантранилат)
ApplePineappleGrape
Упр .27. Напишите формулы следующих эфиров кислот:
(а) метилформиата, (б) этилацетата, (в) пропилбензоата, (г) изопропилпропионата, (д) диэтилмалоната, (е) диизопропилсукцината, (ж) диметилтерефталата.
Упр.28. Репеллент тараканов, выделенный из огурцов, имеет формулу:

Назовите его. Синтетическим репеллентом тараканов является диизопропилфумарат. Напишите его формулу.
Получение сложных эфиров
Эфиры карбоновых кислот, как мы видели в предыдущих разделах, могут быть получены из различных производных кислот. С высоким выходом их получают путем алкилирования солей карбоновых кислот алкилгалогенидами.
 (47)
(47) Этерификация
Карбоновые кислоты реагируют со спиртами с образованием сложных эфиров (эстеров) по реакции конденсации получившей название этерифиация .

Реакция этерификации катализируется кислотами. Без добавления кислоты равновесие достигается очень медленно, но если же смесь спирта и кислоты нагревать в присутствии небольшого количества концентрированной серной кислоты или хлороводорода, равновесие устанавливается за несколько часов.
С помощью меченых атомов было установлено, что гидроксильную группу в этой реакции отдает кислота, а не спирт.
Реакция получения бутилацетата
 (48)
(48) 
проходит по следующему механизму:
 (М 8)
(М 8) 




Упр. 29. Напишите реакцию 1-бутанола с уксусной кислотой в присутствии серной кислоты и опишите ее механизм.
 Упр. 30. Напишите реакции метанола с кислотами: (а) бензойной, (б) пропионовой и опишите их механизм.
Упр. 30. Напишите реакции метанола с кислотами: (а) бензойной, (б) пропионовой и опишите их механизм. Упр. 31. Завершите реакцию
Ацилирование спиртов и фенолов
По реакции этерификации нельзя получить эфиры фенолов. Их можно получать лишь ацилированием фенолов ангидридами и хлорангидридами кислот:
 (49)
(49)
п- нитрофенол п- нитрофенилацетат
Упр. 32.
 Завершите реакции
Завершите реакции (а)(б)
Присоединение карбоновых кислот к алкенам
Алкены, особенно разветвленные, легко присоединяются к карбоновыми кислотам:
 (50)
(50) трет -бутилацетат
В водных растворах кислот легко проходит обратная реакция.
Метилирование кислот диазометаном
Для получения метиловых эфиров карбоновых кислот в аналитических целях используют диазометан.
 (51)
(51)
диазометан метиловые эфиры
 (М 9)
(М 9) 
Восстановление сложных эфиров
Сложные эфиры восстанавливают тетрагидроалюминатом лития до первичных спиртов:

Для получения первичных спиртов из сложных эфиров в промышленности предпочитают гидрирование в присутствии таких катализаторов как Pd, Ni, Ru или Cu-Cr при 150-200 о С под давлением:

диметиладипат 1,6-гексаметилендиамин (52)
Эфиры карбоновых кислот восстанавливаются в альдегиды с помощью диизобутилалюминийгидрида.
i-Bu2 AlH Диизобутилалюминийгидрид (DIBAL-H)
 (53)
(53) Упр. 33. Напишите реакции восстановления диизобутилалюминийгидридом
(а) метилпропионата, (б) этилбензоата, (в) диметилсукцината, (г) диэтилфталата.
Гидролиз сложных эфиров
Гидролиз эфиров представляет собой реакцию обратную этерификации и катализируется кислотами:

Гидролиз сложных эфиров в щелочной среде называют омылением.

Он проходит по следующему механизму:

Омылением жиров получают мыла и глицерин:
 (54)
(54) Упр. 34. Напишите реакции гидролиза (а) метилбензоата и (б) бутилацетата в присутствии кислоты и опишите их механизм.
Упр. 35. Напишите реакции щелочного гидролиза (омыления) (а) метилпальми-тата и (б) этилстеарата и опишите их механизм.
Переэтерификация
Эфиры получают и переэтерификацией более доступных эфиров:

Переэтерификация представляет собой равновесную реакцию.
 (55)
(55) Полиэфиры
Одним из наиболее важных полиэфиров является полиэтилентерефталат (дакрон, терилен, лавсан, милар). Он может быть получен по реакции этерификации из этиленгликоля и терефталевой кислоты:


(56)
терефталевая кислота этиленгликоль полиэтилентерефталат
Другой метод получения полиэтилентерефталата основан на переэтерификации диметилфталата этиленгликолем:
 (57)
(57) 
 (58)
(58) 
Упр. 36. Кодель получают по реакции переэтерификации диметилтерефталата
1,4-диоксиметилциклокексаном - продуктом каталитического гидрирования диметилтерефталата. Напишите реакции превращеня терефталевой кислоты в кодель.

кодель
Упр.37. Напишите реакцию получения кевлара (лексана, мерлона) из бисфенола А и дифенилкарбоната.
Упр.38. Исходя из бензола и пропена, а также фоcгена предложите схему получения кевлара (лексана, мерлона).
Взаимодействие эфиров карбоновых кислот с аммиаком и аминами
При нагревании эфиров карбоновых кислот с аммиаком и аминами образуются амиды:
 (59)
(59) Реакция проходит по следующему механизму:
 (м 10)
(м 10) Синтез амидов из эфиров осуществляется медленнее, чем из ангидридов и хлорангидридов кислот, но зато экспериментально он существенно проще.
Упр.39. Напишите реакции этиловых эфиров кислот: (а) уксусной, (б) пропионовой, (в) масляной и (г) бензойной с аммиаком и опишите их механизм.
Упр.40. Многие пластмассовые бутылки для воды изготовлены из полиэтилен-терефталата. Напишите реакции, которые могут происходить при хранении в таких бутылках (а) водных растворов щелочей, (б) водных растворов кислот, (в) водного раствора аммиака.
mirznanii.com
Сложные эфиры скорости гидролиза - Справочник химика 21
Кинетика гидролиза сложных эфиров очень сложна, так как приходится учитывать и каталитическое действие получающейся при гидролизе кислоты. При кислотном гидролизе реакции не доходят до конца, оставаясь всегда в каком-то состоянии равновесия, и лишь при щелочном гидролизе благодаря образованию солей кислот реакция проходит количественно. Скорость щелочного гидролиза в 3000—4000 раз больше, чем кислотного. [c.530] В работе [10] изучали влияние н-бутаиола на-кинетику реакций гидролиза сложных эфиров, катализируемых карбокси-пептидазой В. На основании зависимости скорости ферментативной реакции от начальной концентрации субстрата (табл. 11) предложить кинетическую схему реакции (приняв двухстадийный механизм действия фермента) и определить константу ингибирования н-бутанолом. [c.91]Сложные эфиры, в отличие от простых, с большей или меньшей скоростью расщепляются водой — подвергаются гидролизу с образованием вновь кислоты и спирта. Поэтому, как показано в схемах приведенных выше реакций, процесс этерификации обратим и доходит до состояния динамического равновесия. Ионы водорода, как и всякий катализатор, ускоряют протекание не только реакции этерификации, но и обратной ей реакции гидролиза таким образом в присутствии минеральной кислоты быстрее достигается равновесие в процессе этерификации. [c.578]
Скорость гидролиза в значительной степени зависит от строения кислоты. Так, например, с большим трудом подвергаются гидролизу эфиры триметилуксусной кислоты и эфиры 2,6-диметилбензойной кислоты, так как благодаря стерическим препятствиям затруднена атака карбонильного углерода сложного эфира молекулами воды. [c.166]
Активным катализатором может быть и ион водорода. Отклонения в каталитической силе кислот в зависимости от изменения их концентрации, различную скорость гидролиза сложных эфиров слабыми и сильными кислотами, действие нейтральных соединений (солевой эффект) и т. д. следует приписать образованию промежуточных соединений. [c.547]
Скорость гидролиза сложного эфира зависит от строения как ацильного, так и спиртового радикалов. При этом сложные эфиры омыляются тем быстрее, чем легче они образуются. Наименее устойчивыми являются сложные эфиры, полученные из кислот с высокой константой диссоциации. Муравьиноэтиловый эфир, метиловый и этиловый эфиры щавелевой кислоты гидролизуются при комнатной температуре. [c.166]
В тех случаях, когда каталитические и субстратные группы принадлежат одной и той же молекуле, может иметь место кардинальное увеличение реакционной способности [24, 25]. В табл. 24.1.2 проиллюстрирован эффект введения карбоксильной группы в ряд ароматических сложных эфиров. Скорости гидролиза этих соединений измеряли при очень низких концентрациях моль-л ). Присутствие карбоксилсодержащих соединений, например ацетата, в таких низких концентрациях не должно в принципе существенно влиять на скорость реакции. Очевидно, что гидролиз сложноэфирной группы катализируется соседней карбоксилатной группой (активна, как обычно, ионизованная форма). Эффективная моль-ность этой группы несомненно много выше ее истинной концентрации в растворе. Этот параметр (последняя колонка в табл. 24.1.2) является наилучшей мерой эффективности данной группы во внутримолекулярном катализе по сравнению с межмолекулярным. Эта величина равна отношению констант первого и второго порядков и имеет в силу этого размерность мольности. Она может быть определена как мольНость внешнего катализатора (в данном случае ацетата), необходимая для протекания реакции с той же скоростью, с какой она идет при наличии катализатора, встроенного в субстрат. Все эффективные мольности в табл. 24.1.2. превышают предел растворимости ацетата в воде, так что эта величина (мольность внешнего катализатора) является гипотетической. Данный параметр учитывает внутреннюю реакционную способность каталитической группы в рассматриваемой системе эффективная мольность хорошего катализатора, по-видимому, совпадает с соответствующей величиной для плохого катализатора (ср. эффективные мольности групп Me,N— и — Oj для номеров 2 и 6, а также 3 и 7, табл. 24.1.2). В связи с этим иногда более показательным параметром эффективности катализа являет- [c.465]
Без катализаторов гидролиз многих эфиров протекает очень медленно, иногда в течение нескольких лет, хотя некоторые сложные эфиры, например метиловый и этиловый эфиры муравьиной кислоты, метиловый и этиловый эфиры щавелевой кислоты, эфиры а-окси- и низших а-аминокислот и др., гидролизуются очень быстро. Скорость реакции значительно увеличивается добавками [c.529]
Кислотно-щелочной катализ. Хорошо известно, что ионы водорода и гидроксила катализируют гидролиз сложных эфиров. Скорость гидролиза сахарозы кислотами была применена для измерения силы кислот прежде, чем были разработаны современные методы определения концентрации водородных ионов. [c.161]
Кинетика гидролиза. Скорость гидролиза кислых эфиров в спир>-ты находится в линейной зависимости от кислотной функции Я,. Это реакции первого порядка по отношению к сложному эфиру. Скорость гидролиза сложных диалкилэфиров не зависит от кислотной функции (до момента образования кислых сложных моноэфиров) реакция также имеет первый порядок по отношению к сложному диалкилэфиру. [c.196]
Реакция этерификации обратима. Это объясняется тем, что получаемый сложный эфир гидролизуется одновременно образующейся при реакции водой, и поэтому процесс идет в обратном направлении с разложением эфира на кислоту и спирт. При этом, чем больше накапливается воды, тем больше скорость обратной реакции последняя ускоряется и при нагревании, а также под влиянием ионов водорода (стр. 181), вводимых для ускорения прямой реакции. Таким образом, реакция этерификации не доходит до конца, а лишь достигает состояния химического равновесия применение же катализаторов и повышение температуры только ускоряют достижение равновесия. Соотношение всех реагирующих веществ в момент равновесия зависит от строения кислоты и спирта, а также от склонности сложного эфира к гидролизу. [c.182]
Реакция этерификации с участием органических кислот протекает очень медленно, но при нагревании и в присутствии катализаторов (минеральные кислоты) скорость ее растет. Эта реакция обратима, поскольку полученный сложный эфир и вода реагируют с образованием кислоты и спирта. А такая реакция вещества с водой, когда составные части воды соединяются с составными частями вещества, называется гидролизом. Скорость обратной реакции, т. е. гидролиза эфиров, к к [c.348]
Этерификация является обратимте реакцией и под действием водн происходит гидролиз молекулы сложного эфира, скорость которого заметно увеличивается в присутствии катализатора. [c.33]
Для превращения галогенопроизводных в спирты иногда прибегают к двухстадийному процессу действием калиевой или серебряной соли органической кислоты на галогенопроизводное получают сложный эфир, который затем подвергают гидролизу или восстановлению. В последнем случае образуется смесь двух спиртов. Добавление Б реакционную массу краун-эфира повышает скорость гидролиза галогенопроизводных. [c.101]
Такое представление согласуется с данными по относительной скорости катализируемого гидролиза сложных эфиров и амидов. Из табл. [c.164]
Относительные скорости катализируемого гидролиза сложных эфиров [c.165]
При параллельном протекании кислотного и-водного гидролиза сложного эфира эффективная константа скорости псевдопервого порядка должна определяться выражением [c.53]
Экстракция трибутилфосфатом (ТБФ). Трибутилфосфат — бесцветная вязкая жидкость (физические свойства см. в табл. 2. 4). Для достижения оптимальных условий проведения процессов непрерывной жидкостной экстракции чистый трибутилфосфат, обладающий некоторыми неблагоприятными свойствами (большая плотность и вязкость и т. п.), всегда разбавляется инертным растворителем. ТБФ — типичный сложный эфир и гидролизуется как в щелочной, так и в кислой среде [40—44]. Гидролиз протекает ступенчато, причем последовательно отщепляется по одной алкильной группе и образуются дибутилфосфорная кислота (ДБФ), монобутилфосфорная кислота (МБФ) и фосфорная кислота. Скорости гидролиза на каждой ступени различны, но все они достаточно малы. Так, скорость образования дибутилфосфата из ТБФ в условиях работы одного из аффинажных заводов составляла, по оценке, менее 0,001 % в час. Скорости гидролиза ДБФ и монобутилфосфата были еще меньше. [c.33]
Если одно из веществ в большом избытке, то его концентрация практически ие меняется во время реакции. Поэтому произведение концентрации его на константу скорости — величина постоянная и уравнение (Х1У.8) переходит в уравнение (Х1У.З). Такие реакции называются п с е в д о м о н о м о л е ку л я р н ы м и, как, например, гидролиз сложных эфиров в кислой среде, где концентрация воды велика. [c.223]
При одинаковых условиях скорость реакции гидролиза зависит от природы как спиртового, так и кислотного остатков в молекуле эфира, но кислотный остаток влияет на скорость значительно сильнее. Скорость гидролиза снижается с увеличением молярной массы кислоты и спирта, составляющих исходный сложный эфир. [c.84]
Резкое понижение скорости может быть связано со стерическим затруднением, прямой преградой нуклеофильной атаке. Другим примером стерического затруднения служат 2,6-диза-мещенные бензойные кислоты, которые с трудом поддаются этерификации независимо от того, проявляют ли заместители в положениях 2 и 6 резонансный эффект или эффект поля. Если же 2,6-дизамещенпую бензойную кислоту удается этерифи-цировать, полученный сложный эфир трудно гидролизовать. [c.362]
Метод основан на определении С-алкильных групп по Куну — Роту (см. выше). Сложный эфир сначала гидролизуют (серной или ге-толуолсульфокислотой, водным или метанольным раствором КОН или NaOH для повышения растворимости вначале можно добавить пиридин). Летучие кислоты (после подкисления, когда это необходимо) отгоняют и титруют так же, как при определении С-алкильных групп. Для соединений с трудногидролизуемыми ацетильными группами проводят окисление, как было описано выше при этом следует обращать внимание на наличие С-алкильных групп. Для образцов, дающих 3—6 мл 0,01 н. кислоты, точность определения составляет 0,3—0,5%. Визенбер-гер [150] усовершенствовал применяемую аппаратуру, приспособив ее для совместного определения С-алкильных и С-ацильных групп. Алицино [151] дифференцировал 0-ацетильные и N-аце-тильные группы но различию в скоростях гидролиза холодным [c.43]
Некоторые сложные эфиры, исключительно устойчивые к основному гидролизу, были успешно гидролизованы кипячением с Л. и. б. в коллидине. Реакция часто идет с низкой скоростью, например, сложный эфир (1) гидролизуется лишь при кипячении в течесгие 72 аде в атмосфере азота, однако выход, соответствующей [c.198]
Скорость этерификации и соотношение веществ в состоянии рэвновесия, т. е. предел этерификации, зависят от природы реагирующих веществ и от склонности образующихся сложных эфиров к гидролизу. Н. А. Меншуткин установил, что скорость и предел этерификации тесно связаны со строением исходных спиртов (стр. 172) наибольшими они являются для первичных спиртов, несколько меньшими для вторичных, а совсем медленно и с низшим пределом в реакцию этерификации вступают третичные спирты и фенолы. С другой стороны, течение реакции этерификации зависит и от строения кислоты кислоты, у которых при смежном с карбоксильной группой углеродном атоме содержатся ответвляющиеся углеводородные радикалы, вступают в реакцию эфирообразования медленнее, чем соответствующие им кислоты нормального строения. [c.343]
Трибутилфосфат (ТБФ) представляет собой сложный эфир он гидролизуется как в кислой, так и в щелочной среде с отщеплением вначале одной молекулы спирта, а затем другой с образованием соответственно длбутил-фосфата и монобутилфосфата. Скорость гидролиза ТБФ определяется многими факторами, но в обычных условиях экстракционно-реэкстрак-ционного процесса она невелика и составляет около 0,001% в 1 ч. Некоторые физико-химические свойства ТБФ, а также дибутилфосфата (ДБФ) и монобутилфосфата (МБФ) приведены в табл. 9.1. [c.206]
Основные стадии производства — абсорбция этилена Н2304, разбавление и гидролиз сложных эфиров серной кислоты, отгонка спирта и, наконец, регенерация Нг504 высокой концентрации. Скорость абсорбции этилена серной кислотой возрастает с увеличением концентрации кислоты, температуры, давления, эффективности катализатора и времени контакта. [c.200]
Скорость гидролиза в идентичных условиях зависит от характера как спиртового, так и кислотного радикалов сложного эфира. Однако было установлено, что спиртовый радикал относительно меньше влияет на скорость гидролиза, чем кислотный, влияние которого весьма сильно. Можно принять, как правило, что для эфиров типа КСООСоНд скорость гидролиза замедляется с увеличением молекулярного веса кислоты. [c.530]
В качестве реакции сравнения, в которой гидролиз сложного эфира (I) проходил бы по тому же механизму, но без дополнительных нековалентных взаимодействий со стероидным фрагментом нуклеофила, выбрана реакция соединений (I, а—ж) со свободным имидазолом. Для незаряженных эфиров (I, а—в) логарифм константы скорости взаимодействия с нуклеофилом (II) gkn прямо пропорционален логарифму константы скорости взаимодействия с имидазолом ghrn (рис. 18). Соединения (I, г—е) реагируют несколько быстрее за счет электростатического взаимодействия разноименных зарядов в молекулах реагентов. Это проявляется положительным отклонением величины lg n от нормировочной прямой, полученной для незаряженных эфиров (рис. 18). В противоположность этому соединение (I, ж) обнаруживает отрицательное отклонение из-за отталкивания одноименных зарядов в молекулах реагентов. [c.73]
При анализе значений наблюдаемых констант скорости второго порядка 2 следует иметь в виду в принципе два возможных эффекта, вызываемых увеличением длины (п) алифатических групп в молекулах реагентов возрастание стерических препятствий, тормозящих реакцию, и, с другой стороны, возрастание свободной энергии гидрофобного взаимодействия реагентов, приводящего к стабилизации переходного состояния реакции и тем самым к ее ускорению. В нуклеофиле (VI) алкильный заместитель отделен от реакционного центра ими-дазольным кольцом. Поэтому при увеличении п в имидазолах (VI) стерические эффекты должны быть выражены в гораздо меньшей степени, чем для сложных эфиров (V), где заместитель расположен непосредственно у атакуемого карбонильного атома углерода. Следовательно, можно допустить в первом приближении, что стерические эффекты зависят только от свойств эфира. И если принять, наконец, что стерический эффект торможения реакции алкильным заместителем в ацильной группе вносит одинаковый вклад как в щелочной, так и в катализируемый имидазолами (VI) гидролиз, то необходимая поправка может быть внесена простым делением величин на соответствующее для данного сложного эфира (V) значение константы скорости щелочного гидролиза н. [c.75]
В последние годы все большее внимание привлекает эффект мицеллярного катализа [28] — ускорение или замедление органических реакций в результате солюбилизации реагентов (Или одного из них) мицеллами коллоидного ПАВ. Таковы, например, реакции гидролиза и сольволиза сложных эфиров, ацеталей, ортоэфиров, некоторые реакции замещения соединений алифатического и ароматического рядов. Увеличение константы скорости реакции при протекании ее в мицеллах может достигать 1—2 порядков по сравнению со скоростью реакции в воде. [c.85]
Константа скорости гидролиза сложного эфира на полимерном катализаторе выше, чем на его низкомолекулярном аналоге толу-олсульфокислоте. [c.57]
Вслед за Ингольдом [33] Тафт предполагал, что в реакциях гидролиза сложных эфиров и стерические и резонансный эффекты должны быть одинаковы независимо от того, катализируется ли гидролиз кислотой или основанием (см. обсуждение механизма гидролиза сложных эфиров, т. 2, реакция 10-11). Поэтому различие в скоростях должно вызываться только эффектами поля групп К и К в молекуле КСООК [34]. Для изучения эффектов поля это вполне подходящая система, поскольку при гидролизе, катализируемом кислотой, переходное состояние (7) имеет больший положительный заряд (и поэтому дестабилизируется —/- и стабилизируется -Ь/-заместителями), чем исходный сложный эфир, тогда как при гидролизе, катализируемом основанием, переходное состояние (8) имеет больший [c.369]
Доказательства этого получены из сравнительного изучения скоростей реакций [196]. Так, субстрат 73 гидролизуется в 10 раз быстрее, чем бензамид (РЬСОЫНг) при примерно одинаковой концентрации ионов водорода. Причиной такого увеличения скорости не являются резонансные эффекты или эффекты поля группы СООН (электроноакцепторной группы), что было показано экспериментами по гидролизу о-нитробензамида и терефта-ламовой кислоты (иара-изомера 73), который для обоих субстратов протекает медленнее, чем для беизамида. Сообщается и о многих других примерах участия соседней группы в реакциях замещения у атома углерода карбонильной группы [197]. Вероятно, что и при ферментативном катализе гидролиза сложных эфиров нуклеофильный катализ играет определенную роль. [c.60]
chem21.info