Содержание
Метоксиэтан Formule полудевелопе Химическая формула Структурная формула Диметиловый эфир, Klingon, угол, текст, логотип png
Метоксиэтан Formule полудевелопе Химическая формула Структурная формула Диметиловый эфир, Klingon, угол, текст, логотип png
теги
- угол,
- текст,
- логотип,
- другие,
- химия,
- структура,
- эфир,
- структурная формула,
- символ,
- метильная группа,
- метоксиэтан,
- метоксигруппа,
- черный и белый,
- линия,
- клингон,
- площадь,
- формула,
- этильная группа,
- диметиловый эфир,
- диэтиловый эфир,
- химическая формула,
- марка,
- юпак Номенклатура органической химии,
- png,
- прозрачный,
- бесплатная загрузка
Об этом PNG
Размер изображения
- 2988x827px
Размер файла
- 24.2KB
MIME тип
- Image/png
Скачать PNG ( 24. 2KB )
2KB )
изменить размер PNG
ширина(px)
высота(px)
Лицензия
Некоммерческое использование, DMCA Contact Us
Химическое соединение Химический синтез Химия Органическое соединение Молекула, химическая формула, угол, белый, текст png
1917x1466px
134.17KBАцетон Химическое соединение Структурная формула Химическая формула Метильная группа, другие, угол, текст, другие png
1920x1141px
40.17KBЭтаноловое топливо Алкоголь Структурная формула Структура, стоимость, организационная структура, угол, белый, текст png
1280x783px
14.72KB org/ImageObject»>Этанол Химическая формула Алкоголь Химия Химическое вещество, другие, угол, белый, текст png
1280x837px
18.88KBЭтанол Структурная формула Алкоголь Скелетная формула Химическое соединение, абсолют, разное, угол, белый png
1200x742px
10.61KBХимический состав Химический состав Химия Химическая номенклатура Амин, другие, химический элемент, угол, текст png
1280x927px
43.85KBХимическая формула Алкоголь Химическое вещество Химия Структурная формула, другие, угол, белый, текст png
800x558px
18. 2KB
2KBЭтанол Спирт Химическое соединение Структурная формула Химия, Растворение, разное, угол, белый png
1208x747px
1.64KBАдреналин Химическая структура Норадреналин Дофамин, дофамин, угол, белый, текст png
1024x647px
17.56KBМолекула Химическое соединение Химическая формула Аминокислота Леводопа, дофамин, угол, белый, текст png
1280x546px
25.57KBшестигранная форма, циклогексановая конформация структурная формула химическое вещество молекула, шестиугольник, разное, угол, белый png
1200x1380px
28.68KBКофеин Кофеин Молекулы Химическая структура Молекулярная геометрия, Кофе, угол, белый, текст png
1200x987px
40. 58KB
58KBХимическая формула Молекула Химическая структура Химия Химические вещества, другие, угол, текст, прямоугольник png
709x616px
8.01KBБензол Химия Химическая структура Структурная формула, каучуки, угол, белый, текст png
880x1040px
38.73KBХолестерин Химическая структура Химия Молекула, липид, угол, белый, текст png
1414x659px
51.73KBУксусная кислота Химическая формула Химическое соединение Химическое вещество Ацетат натрия, другие, угол, текст, другие png
1024x666px
19.42KBХимическая формула Молекула Вода Химия Химическое соединение, вода, угол, текст, логотип png
1280x549px
12. 36KB
36KBПолипропилен Органическая химия Химическое вещество Химическая промышленность, Полимер, угол, белый, текст png
1200x773px
19.32KBМетанол Химическая формула Спирт Метильная группа Химическое соединение, 30 июня, угол, текст, прямоугольник png
679x600px
8.09KBАцетон Скелетная формула Карбонильная группа Структура Кетон, скелет, разное, угол, другие png
787x768px
11.98KBХимическая формула Молекула Йод Структурная формула Химическое вещество, другие, разное, химический элемент, угол png
1200x941px
28.83KBИзофлавоны Химическая структура Химия Химическая субстанция, наука, угол, белый, текст png
1600x1048px
39. 97KB
97KBНапиток с кофеином Кофе Латте Кофеин Состав, формула, угол, белый, текст png
1024x842px
30.07KBНоскапин Молекула Химическое соединение Химическая формула Химия, Структура, угол, белый, текст png
1060x958px
23.77KBМетанол Структурная формула Структура Бутанол Спирт, молекулярная цепь, разное, угол, белый png
1208x747px
1.65KBХимическая структура Структурная формула Химическое соединение Органическая химия, долиходиал, угол, белый, текст png
759x768px
25.77KBгексагональной формы искусства, конформации циклогексана Структурная формула Структура Органическая химия, гексагоно, угол, белый, прямоугольник png
668x768px
14. 61KB
61KBМолекула Химическая структура Тиамин Химическая формула, другие, угол, белый, текст png
1200x420px
22.19KBЭстер Органическое соединение Карбоновая кислота Éster carbónico, Эфир жирных кислот, угол, текст, логотип png
1024x756px
26.09KBСтруктура бензола Льюиса Резонанс Химическая структура, другие, угол, белый, текст png
800x945px
22.86KBХлороформ Химическое соединение Химическое вещество Химическая формула Химия, др., угол, текст, логотип png
1280x1200px
33.53KBКофеин Кофеин Молекула Химия Химическое вещество, Кофе, угол, белый, текст png
748x615px
25. 92KB
92KBСеротонин молекула химия химическая структура мелатонин, другие, угол, белый, текст png
800x587px
16.54KBГексан Скелетная формула Алкан Органическая химия Углеводород, Химическая полярность, угол, текст, треугольник png
1280x318px
10.57KBХлорид натрия Химия Молекула Химическая структура Химическое вещество, вода, угол, белый, текст png
614x1023px
20.99KBСтруктурная формула Пропан Химическая формула Скелетная формула Химическое соединение, другие, угол, белый, текст png
800x470px
8.42KBМелатонин Химическое строение Химическое вещество Химия Химическое соединение, другие, угол, белый, текст png
1232x1024px
30. 73KB
73KBСтруктура Льюиса Аммиак Молекула Химия Аммоний, точечная формула, угол, текст, логотип png
640x462px
4.05KBСеротонин Химическая структура Структурная формула Дофамин, дмт, угол, белый, текст png
928x768px
23.05KBТаурин Молекула Химическое вещество Химическая формула Химия, Мочевой Кальций, угол, текст, треугольник png
1200x640px
22.31KBФормальдегид Химическое строение Химическое вещество, холодная кислота Линг, разное, угол, текст png
1104x1024px
23.69KBФормула Математика Евклидова, математическая формула, угол, текст, монохромный png
3500x3313px
875. 77KB
77KBДиметиловый эфир Диэтиловый эфир Структура скелета, хлорметилметиловый эфир, угол, другие, Wikimedia Commons png
1280x562px
18.24KBХимия Бензол Химическое соединение Химическое вещество Химическая структура, бензольное кольцо, разное, угол, белый png
529x600px
32.96KBСтруктура Льюиса Молекулярная геометрия Метан Молекула Химическая формула, другие, разное, угол, текст png
800x916px
5.7KBАльдегид Функциональная группа Структура Кетон Химия, Альдегид, угол, химия, структура png
657x600px
10.16KBХимическая структура Биохимия Молекулы липидов, глицерин, угол, белый, текст png
1280x874px
31. 32KB
32KBГлюкоза Органическое соединение Химия Химическое соединение Сахароза, сахар, угол, белый, текст png
1920x1280px
58.33KBСтруктура Льюиса Метан Простая связь Химическая связь Валентный электрон, молекулярная цепь, разное, угол, текст png
1041x1079px
10.8KB
Ацетон Химическое соединение Химическая формула Структурная формула Диметилсульфоксид, другие, угол, текст, другие png
1200x713px
22.38KB
Оптические изомеры • Алексей Паевский • Научно-популярные задачи на «Элементах» • Химия
Химикам уже давно известно явление изомерии — когда два вещества имеют одну и ту же брутто-формулу (отражающую только количество разных атомов в веществе), но разные свойства — из-за разного порядка соединения атомов.
Особенно богата изомерами органическая химия. К примеру, этиловый спирт и диметиловый эфир имеют одну и ту же брутто-формулу: C2H6O, но структурная формула спирта — CH3–CH2–OH, а эфира — CH3–O–CH3.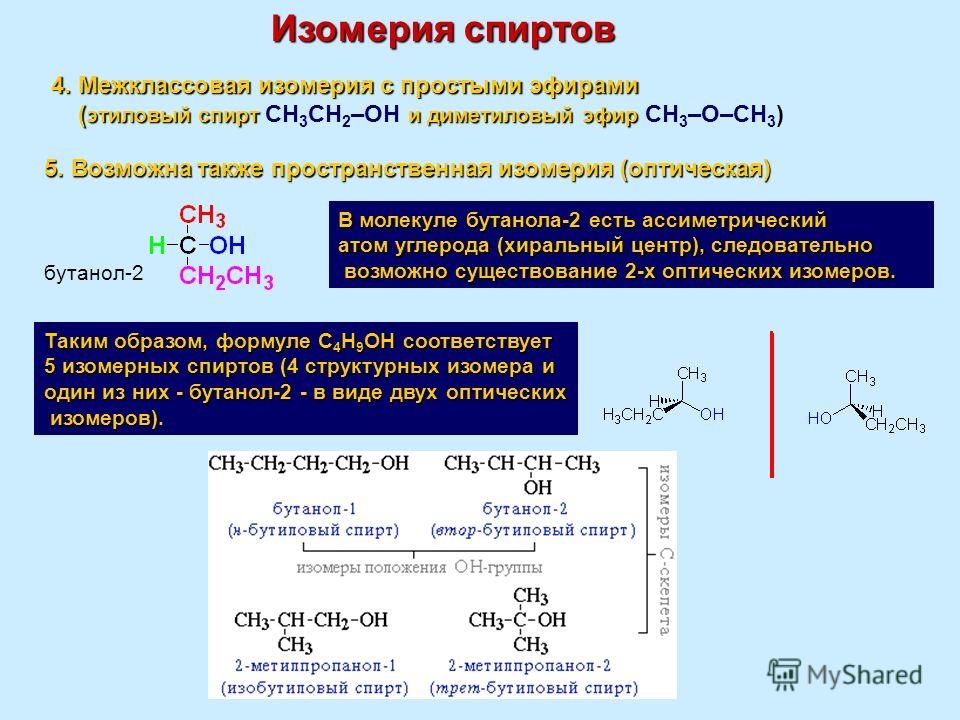 Эти вещества имеют разные свойства — как химические, так и физические (температура плавления, вязкость и т. д.).
Эти вещества имеют разные свойства — как химические, так и физические (температура плавления, вязкость и т. д.).
В органической химии известны и так называемые оптические изомеры — молекулы, имеющие одинаковую структурную формулу, но не совместимые со своим зеркальным отражением. Простейший пример такой молекулы — это атом углерода с четырьмя разными заместителями. К примеру, СHClBrF или аланин CH3CHNH2COOH (рис. 1). Наличие у такой молекулы двух разных конфигураций связано с тем, что у атома углерода, образующего четыре одинарные связи, эти связи направлены к вершинам тетраэдра.
Оптические изомеры имеют одинаковый цвет, температуру кипения, плотность. Однако такие вещества обладают интересным физическим свойством — они вращают плоскость поляризации пропущенного через них поляризованного света. Один изомер будет вращать ее влево, другой — вправо.
Атом углерода с четырьмя разными заместителями называется хиральным атомом (от греческого heiros «ладонь» — тот же корень, что и в слове «хиромантия»).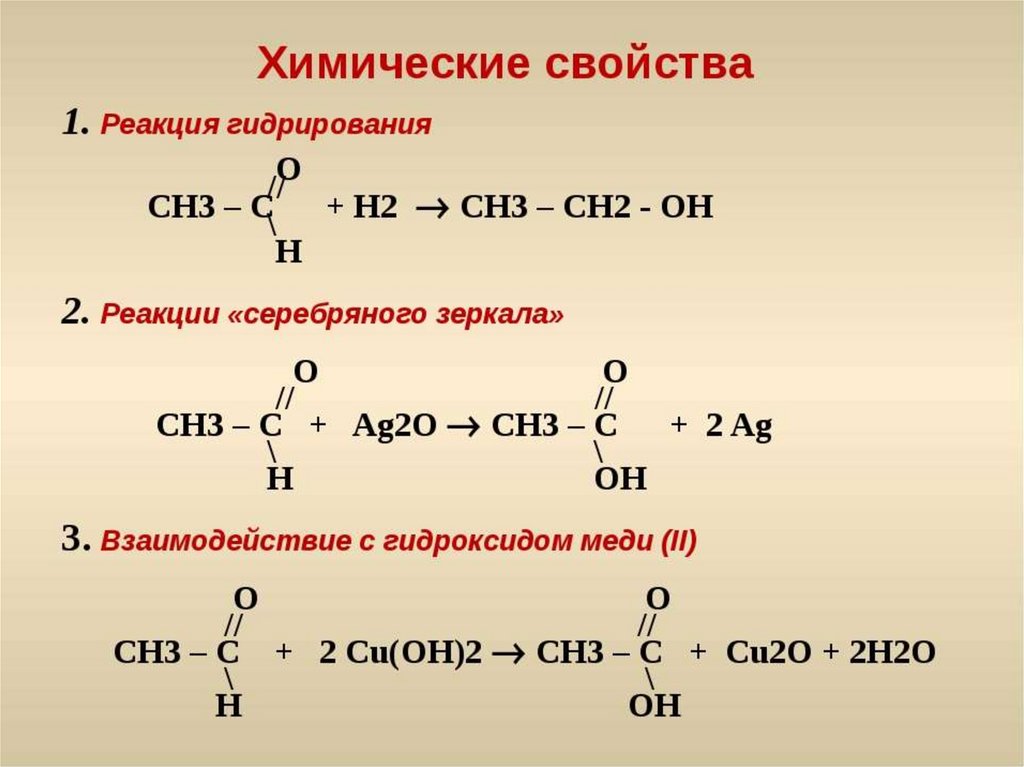 Чем больше хиральных атомов в молекуле, тем больше у вещества может быть оптических изомеров.
Чем больше хиральных атомов в молекуле, тем больше у вещества может быть оптических изомеров.
Интересно, что возможны органические вещества, которые имеют оптические изомеры, хотя в них формально нет ни одного хирального атома — центра изомерии.
Подсказка 1
Для того чтобы молекула некоторого вещества не совпадала со своим зеркальным отражением, совершенно не обязательно, чтобы у нее был хотя бы один хиральный атом. К примеру, любая молекула в форме спирали будет оптически активной.
Подсказка 2
Кроме того, вспомните, к вершинам какой геометрической фигуры направлены четыре связи в хиральном атоме углерода.
Решение
Начнем с того, что для несовместимости со своим зеркальным отражением молекуле недостаточно быть просто несимметричной. Молекула может быть не равна своему отражению «на бумаге», но совместима с ним. Скажем, молекулу HCl мы можем просто повернуть (или посмотреть на нее с другой стороны). Мы можем также вращать части молекулы вокруг одинарных связей — а вот с двойными и тройными связями так поступать нельзя, они при этом рвутся.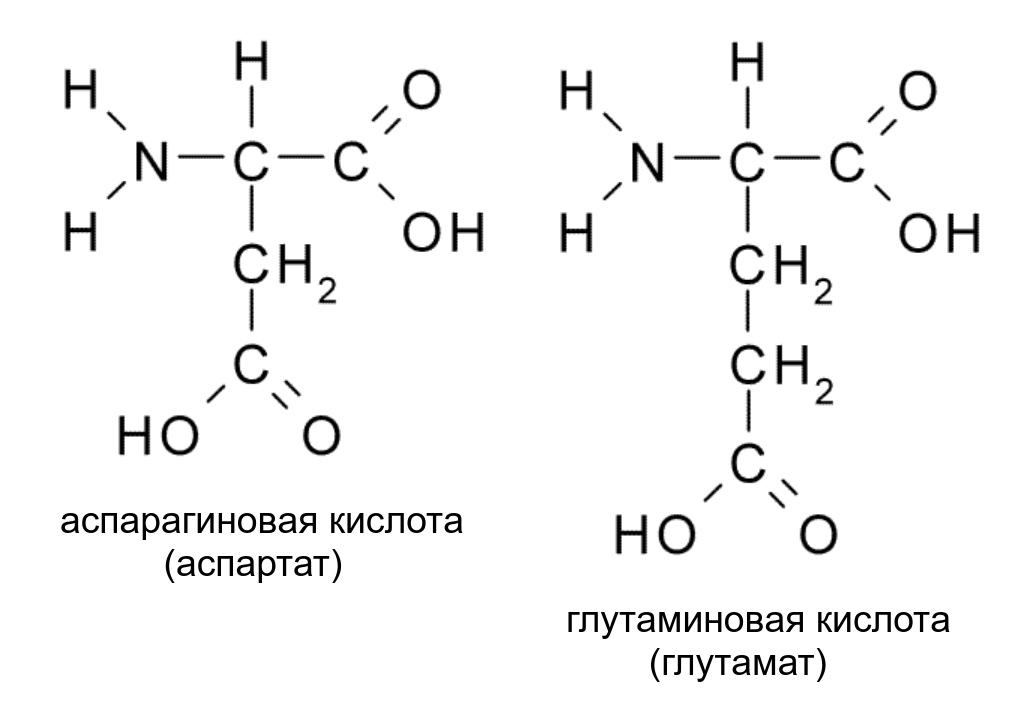
Итак, если структура молекулы имеет такую пространственную асимметрию, что она не совмещается со своим зеркальным отражением, то молекула и ее отражение называются оптическими изомерами. Наша цель — попробовать придумать структуру, которая бы была несовместима со своим зеркальным отражением, имела бы минимальное количество атомов углерода, и при этом сами эти атомы не были бы хиральными центрами молекулы.
На первый взгляд, такой молекулой могли бы быть замещенные этилены, где вместо атомов водорода — четыре разных заместителя:
Однако несмотря на то, что у такого вещества есть изомеры (два произвольно выбранных заместителя у разных атомов углерода могут располагаться по одну сторону двойной связи или по разные), хиральными они не будут, так как молекулы с одной двойной связью — плоские; чтобы совместить их со своим зеркальным отражением, их достаточно просто повернуть на 180° вокруг оси, лежащей в плоскости молекулы и перпендикулярной двойной связи.
Существует вариант с тремя атомами углерода, который формально уже можно назвать решением нашей задачи.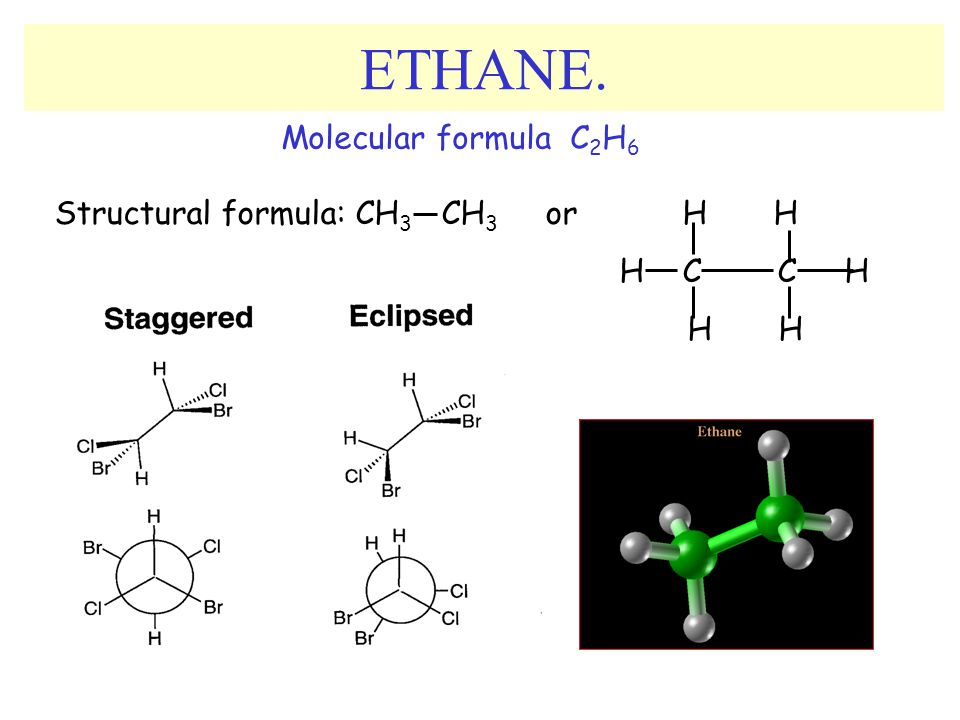 Четырехзамещенные аллены RR’C=C=CR»R»’ тоже содержат двойные связи, но их молекулы уже не плоские. Дело в том, что если у одного атома углерода есть две двойные связи, то их плоскости повернуты друг относительно друга на 90 градусов:
Четырехзамещенные аллены RR’C=C=CR»R»’ тоже содержат двойные связи, но их молекулы уже не плоские. Дело в том, что если у одного атома углерода есть две двойные связи, то их плоскости повернуты друг относительно друга на 90 градусов:
Эта молекула уже хиральна, и можно сказать, что задачу мы решили. Однако в ней есть «хиральный центр» — центральный атом углерода. Попробуем решить задачу другим способом.
Три атома углерода можно расположить по-другому — создав из них треугольник. У нас получится вещество циклопропан, С3H6:
Это хорошо известное вещество, которое до сих пор иногда используется в медицине в качестве средства для наркоза. Атомы углерода образуют жесткую плоскость. Каждый из них связан с двумя атомами водорода — один над плоскостью, другой — под ней.
Теперь заменим у двух атомов углерода по одному атому водорода на два других заместителя — к примеру, хлор и бром — так, чтобы они оказались по разные стороны от плоскости атомов углерода.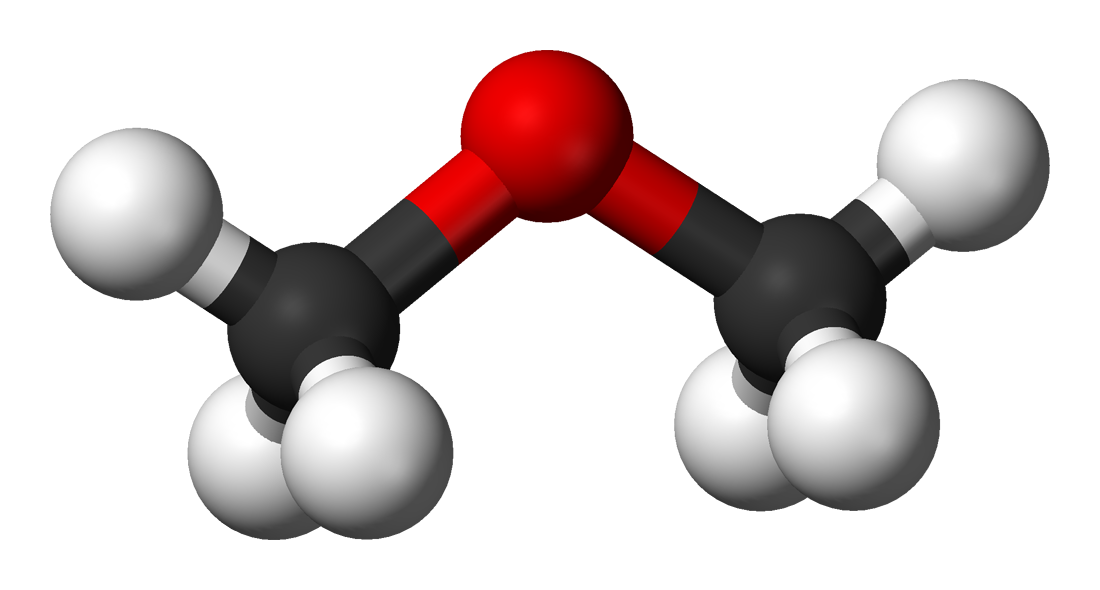 Такое положение заместителей называется транс-изомером 1,2-дизамещенного циклопропана. (Если бы эти заместители располагались по одну сторону от плоскости, у нас получился бы цис-изомер, но он нас сейчас не интересует).
Такое положение заместителей называется транс-изомером 1,2-дизамещенного циклопропана. (Если бы эти заместители располагались по одну сторону от плоскости, у нас получился бы цис-изомер, но он нас сейчас не интересует).
Внимательно посмотрим на получившуюся молекулу и представим себе ее зеркальное отражение:
Обе структуры, как бы мы ни крутили их в пространстве, друг с другом не совмещаются, а атома — хирального центра тут нет.
А теперь попробуем создать полный аналог хирального атома углерода — но без хирального центра. Вернемся к первоначальному атому, с которого мы начали (см. условие задачи). Четыре связи его направлены к вершинам тетраэдра. Давайте попробуем расположить по атому углерода в его вершинах и соединить их связями.
У нас получится углеродный скелет вещества C4H4 — тетраэдрана. Само это вещество еще не получено химиками, но его производные уже существуют в реальности. Если заместить в нём все атомы водорода на разные заместители, то получится вполне себе хиральная молекула, «хиральный центр» которой будет располагаться внутри тетраэдра:
Послесловие
Тема изомерии — одна из самых благодатных тем для игры ума.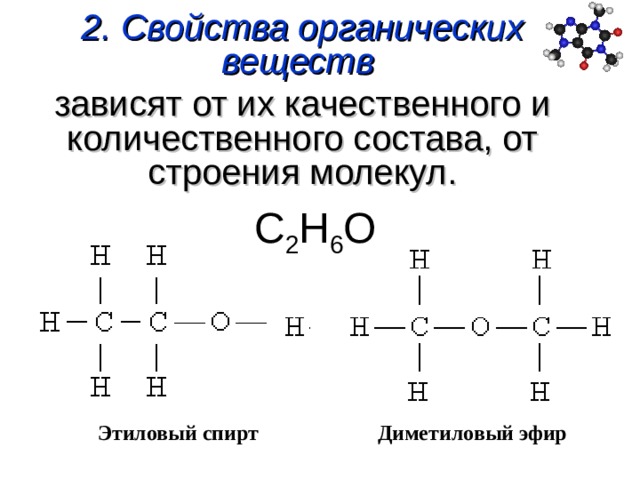 Даже в школьных олимпиадах по химии очень часто можно встретить задания с просьбой написать все изомеры того или иного вещества (иногда сами составители задач чего-то не рассчитывают, и на решение уходит много времени и очень много бумаги; у автора этой задачи на районной олимпиаде как-то ушло полтора часа и целая тетрадка).
Даже в школьных олимпиадах по химии очень часто можно встретить задания с просьбой написать все изомеры того или иного вещества (иногда сами составители задач чего-то не рассчитывают, и на решение уходит много времени и очень много бумаги; у автора этой задачи на районной олимпиаде как-то ушло полтора часа и целая тетрадка).
Оптические изомеры — всего один из вариантов изомерии в органической химии, но очень важный.
К примеру, все основные аминокислоты, которые входят в состав наших белков, имеют формулу H2N–CH(R)–COOH — то есть все (кроме глицина, у которого R тоже представляет собой атом водорода) имеют асимметрический атом углерода и имеют оптические изомеры. И в нашем организме встречаются почти исключительно L-изомеры аминокислот (если не вдаваться в тонкости номенклатуры хиральных атомов, которых существует целых три типа, то можно назвать эти молекулы «левыми»). И биохимики до сих пор гадают, почему природа выбрала именно этот изомер — ведь при всех реакциях, когда из более простых веществ получаются вещества с хиральным атомом (без присутствия специфических катализаторов) образуется смесь двух изомеров в равных частях.
Синтетики тоже любят «поиграть» с оптической изомерией и при этом уже создали множество веществ без хирального атома — но с оптической активностью.
Кстати, можно создать хиральную молекулу вообще без заместителей. И она будет достаточно небольшой. Существуют так называемые ароматические углеводороды. Самый простой из них — бензол, C6H6. Его структуру учат в школе — плоский шестигранник. Вещество посложнее — нафталин. Это уже два соединенных по одной стороне бензольных кольца:
Три кольца можно уже соединять в линию — получится антрацен, а можно — под углом, и тогда у нас получится фенантрен:
Так вот, если продолжать соединять кольца под углом и дойти до шести колец, то крайние кольца упрутся друг в друга, им не хватит места, и плоскость молекулы нарушится. Вещество из шести колец называется гексагелицен, и его молекула уже представляет собой спираль. А значит, эта молекула может быть либо левой спиралью, либо правой, и будет иметь оптические изомеры.
Кстати, химики научились получать такие спирали даже из 12 бензольных колец, в них уже есть пара витков.
Более того, и оптическими изомерами весь ассортимент разнообразия химических веществ, как ни странно, не заканчивается.
Стоит сказать о возможности так называемой топологической изомерии. Что это такое? К примеру, существует вещество в форме кольца. Две молекулы этого вещества изомерны одной, в которой одно кольцо продето в другое. И такие молекулы уже есть. Класс веществ, в которых две или более частей молекул удерживаются механически, как звенья цепи, называются катенанами — от латинского catena «цепь» (см. Catenane). Биохимики научились получать катенаны из молекул ДНК, и более короткие структуры тоже складывали в цепочки.
А если представить себе катенан из четырех колец, то возможна изомерия между молекулой, в которой три кольца продеты в четвертое, и молекулой, в которых кольца соединены последовательно.
диметиловый эфир | КАС №: 115-10-6 | Chemsrc
Дата изменения: 2022-10-27 08:08:39
структура диметилового эфира | Общее имя | диметиловый эфир | ||
|---|---|---|---|---|
| Номер CAS | 115-10-6 | Молекулярный вес | 46. 068 068 | |
| Плотность | 0,7±0,1 г/см3 | Точка кипения | -29,5±3,0 °С при 760 мм рт.ст. | |
| Молекулярная формула | С 2 Н 6 О | Точка плавления | −141 °С (лит.) | |
| MSDS | Н/Д | Температура вспышки | -85,9±5,7 °С | |
- Свойства
- Спектр
Имена
| Имя | диметиловый эфир |
|---|---|
| Синоним | Другие синонимы |
Химические и физические свойства
| Плотность | 0,7±0,1 г/см3 |
|---|---|
| Точка кипения | -29,5±3,0 °С при 760 мм рт.ст. |
| Точка плавления | −141 °С (лит.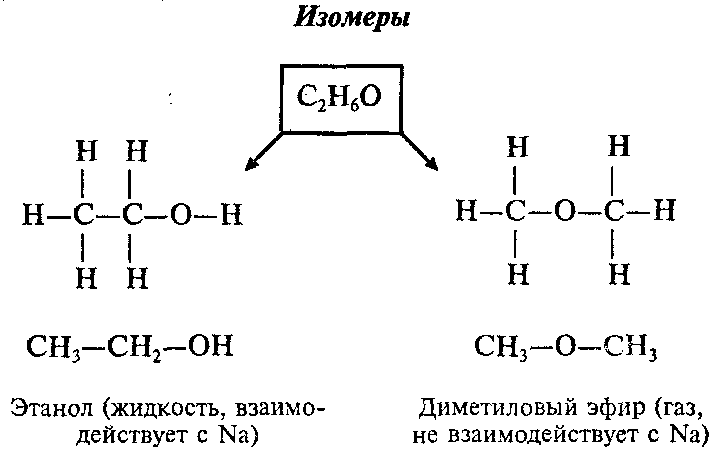 ) ) |
| Молекулярная формула | С 2 Н 6 О |
| Молекулярный вес | 46.068 |
| Температура вспышки | -85,9±5,7 °С |
| Точная масса | 46.041866 |
| СРП | 9.23000 |
| ЛогП | -0,08 |
| Плотность пара | 1,62 (относительно воздуха) |
| Давление паров | 4784,2±0,0 мм рт.ст. при 25°C |
| Показатель преломления | 1.309 |
| Устойчивость | Стабильный. Чрезвычайно легко воспламеняется. Обратите внимание на низкую температуру вспышки. Может образовывать взрывоопасные смеси с воздухом. При длительном хранении может образовывать перекиси. |
| Растворимость в воде | растворимый |
Паспорт безопасности
паспорт безопасности диметилового эфира (китайский) |
Токсикологическая информация
ХИМИЧЕСКАЯ ИДЕНТИФИКАЦИЯ
ДАННЫЕ ОБ ОПАСНОСТИ ДЛЯ ЗДОРОВЬЯДАННЫЕ ОБ ОСТРОЙ ТОКСИЧНОСТИ
|
Информация по технике безопасности
| Коды опасности | F+: легковоспламеняющийся; |
|---|---|
| Фразы риска | R12 |
| Фразы безопасности | С9-С16-С33 |
| РИДАДР | ООН 1033 2. 1 1 |
| ВГК Германия | 1 |
| РТЕКС | PM4780000 |
| Класс опасности | 2.1 |
| Код ТН ВЭД | 2909191000 |
Прекурсор и последующие этапы
| Прекурсор 10 | |
|---|---|
| |
| |
| |
| Нижестоящий 10 | |
| |
| |
| |
Таможня
| Код ТН ВЭД | 2909191000 |
|---|---|
| Резюме | 2909191000 метоксиметан。Условия надзора:Нет。НДС:13,0%。Налоговая скидка:13,0%。Самый низкий тариф:5,5%。Общий тариф:30,0% |
Синонимы
Ч4-О-Ч4 |
диметиловый эфир |
метиловый эфир |
диметиловый эфир |
Метан, 1,1′-оксибис- |
эфир, диметил |
3,4,5-ТРИМЕТОКСИ-2-(МЕТОКСИМЕТИЛ)КОРИЧНИТРИЛ |
ИНЭКС 204-065-8 |
эфир, метил |
Метоксиметан |
монометиловый эфир |
MFCD00008494 |
(Ч4)2О |
ДМЕ |
МЕТАН,1,1′-ОКСИБИС- |
Лучшие поставщики: Я хочу быть здесь
- Dayang Chem (Hangzhou) Co.
 , Ltd.
, Ltd. Китай
- Название продукта: Диметиловый эфир
- Цена:
$Запрос/100г$Запрос/1кг
$Запрос/100кг
$Запрос/1000кг
Чистота: 98,0%
- Период хранения: запрос
- Контактное лицо: г-жа Ван
Получить всех поставщиков и цену по ссылке ниже:
поставщиков диметилового эфира
цена диметилового эфира
Родственные соединения:
Более…
| диметиловый эфир 157621-61-9 |
| диметиловый эфир 149228-22-8 |
| диметиловый эфир-d6 17222-37-6 |
| нудол диметиловый эфир 97399-69-4 |
| диметиловый эфир ТББФА 37853-61-5 |
| Агар, диметиловый эфир 131439-06-0 |
| Хинол диметиловый эфир 150-78-7 |
| Диметиловый эфир гликоля 24991-55-7 |
| диметиловый эфирный радикал 16520-04-0 |
Chemsrc предоставляет паспорт безопасности диметилового эфира (CAS #: 115-10-6), плотность, температуру плавления, температуру кипения, структуру, формулу, молекулярную массу и т. Д. Также включены статьи о диметиловом эфире. >> версия усилителя: диметиловый эфир
Д. Также включены статьи о диметиловом эфире. >> версия усилителя: диметиловый эфир
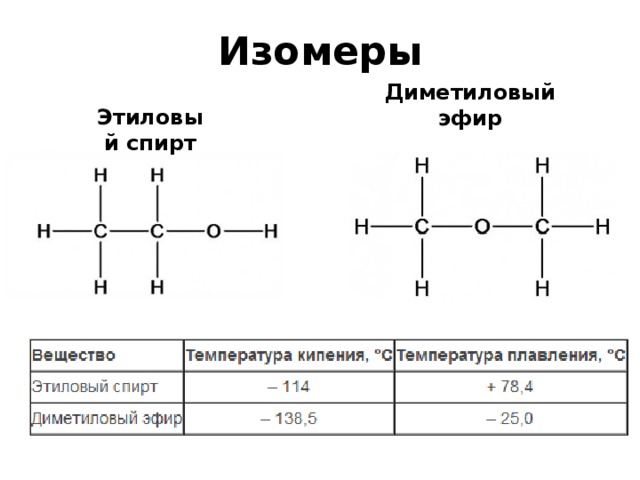
Разница между этанолом и диметиловым эфиром
Основное различие между этанолом и диметиловым эфиром заключается в том, что этанол представляет собой бесцветную жидкость при комнатной температуре, обладающую высокой летучестью, тогда как диметиловый эфир представляет собой бесцветный газ при комнатной температуре. Кроме того, этанол (обычное название — этиловый спирт) представляет собой спирт, а диметиловый эфир — это простой эфир.
Спирт представляет собой органическое соединение, состоящее из гидроксильной группы (-ОН) в качестве функциональной группы. Эфир также является органическим соединением, но он имеет две алкильные группы, присоединенные к одному и тому же атому кислорода.
СОДЕРЖАНИЕ
1. Обзор и ключевые отличия
2. Что такое этанол
3. Что такое диметиловый эфир
4. Сходства между этанолом и диметиловым эфиром
5. Сравнение бок о бок – этанол и диметиловый эфир в табличной форме
Сравнение бок о бок – этанол и диметиловый эфир в табличной форме
6. Резюме
Что такое этанол?
Этанол представляет собой спирт, имеющий химическую формулу C 2 H 5 OH . Общее название этого соединения — этиловый спирт . Функциональной группой этого соединения является гидроксильная группа (-ОН). Этанол легко воспламеняется; таким образом, он также используется в качестве топлива. Кроме того, это очень летучее соединение. Однако при комнатной температуре это бесцветная жидкость с характерным запахом.
Рисунок 1: Химическая структура этанола
Некоторые химические факты об этаноле
- Химическая формула = C 2 H 6 O
- Молярная масса = 07 г/моль
- Температура плавления = -114,1 °C
- Температура кипения = 78,37 °C
- Физическое состояние = при комнатной температуре существует в виде бесцветной жидкости
- Запах = характерный спиртовой запах
- Растворимость в воде = смешивается с водой
Этанол смешивается с водой, поскольку он может образовывать водородные связи с молекулами воды (группы –OH могут образовывать водородные связи с молекулами H 2 O).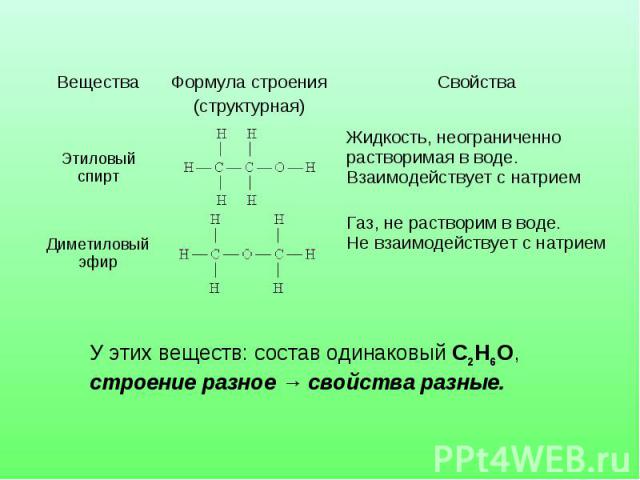 Поэтому используемые растворы имеют высокую вязкость. Кроме того, летучесть снижается при смешивании этанола с водой.
Поэтому используемые растворы имеют высокую вязкость. Кроме того, летучесть снижается при смешивании этанола с водой.
Этанол является полярным соединением, так как он имеет концевую гидроксильную группу. Это делает этанол хорошим растворителем для полярных соединений. Есть два пути производства этанола: химические процессы и биологические процессы. Наиболее распространенным химическим процессом является гидратация этилена. Наиболее распространенным биологическим путем является ферментация сахаров микроорганизмами.
Этанол используется в промышленности, медицине, в качестве топлива, в качестве растворителя и т. д. Этанол также используется в качестве антисептика, поскольку он может убивать некоторые микроорганизмы. Кроме того, этанол является антидотом метанола. Этанол можно использовать непосредственно в качестве топлива или в качестве присадки к топливу.
Что такое диметиловый эфир?
Диметиловый эфир представляет собой эфирное соединение, имеющее химическую формулу C 2 H 6 O .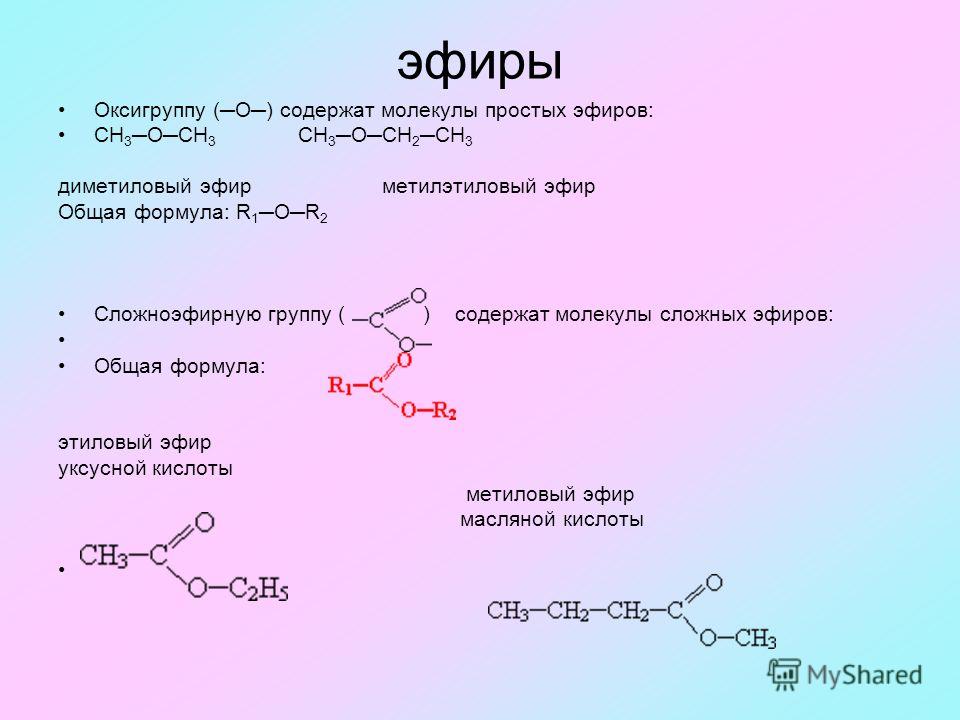 Название этого соединения по классификации ИЮПАК — 9.0597 Метоксиметан . Это соединение хорошо известно своими растворяющими свойствами. Он имеет две метильные группы, связанные через атом кислорода; две метильные группы связаны с одним и тем же атомом кислорода.
Название этого соединения по классификации ИЮПАК — 9.0597 Метоксиметан . Это соединение хорошо известно своими растворяющими свойствами. Он имеет две метильные группы, связанные через атом кислорода; две метильные группы связаны с одним и тем же атомом кислорода.
Рисунок 2: Скелетная структура диметилового эфира
Некоторые химические факты о диметиловом эфире
- Химическая формула = C 2 H 6 O
- Молярная масса = 46,07 г/моль
- Температура плавления = −141 °C
- Температура кипения = −24°C
- Физическое состояние = при комнатной температуре это бесцветный газ
- Запах = запах эфира
- Растворимость в воде = не растворяется в воде
Диметиловый эфир является неполярным соединением. Это означает, что диметиловый эфир не имеет полярности. Это связано с его симметричной молекулярной структурой. Поэтому он является хорошим растворителем для неполярных соединений. Однако он химически неактивен по сравнению с другими органическими соединениями.
Однако он химически неактивен по сравнению с другими органическими соединениями.
Каковы сходства между этанолом и диметиловым эфиром?
- Этанол и диметиловый эфир являются органическими соединениями.
- И этанол, и диметиловый эфир имеют одинаковую молярную массу
- Оба являются хорошими растворителями
- Этанол и диметиловый эфир состоят из атомов C, H и O.
В чем разница между этанолом и диметиловым эфиром?
Этанол против диметилового эфира | |
| Этанол представляет собой спирт, имеющий химическую формулу C 2 H 5 ОХ. | Диметиловый эфир представляет собой эфирное соединение, имеющее химическую формулу C 2 H 6 O. |
| Категория | |
| Этанол представляет собой спирт. | Диметиловый эфир представляет собой эфир. |
| Температура плавления | |
Температура плавления этанола составляет -114,1 °C.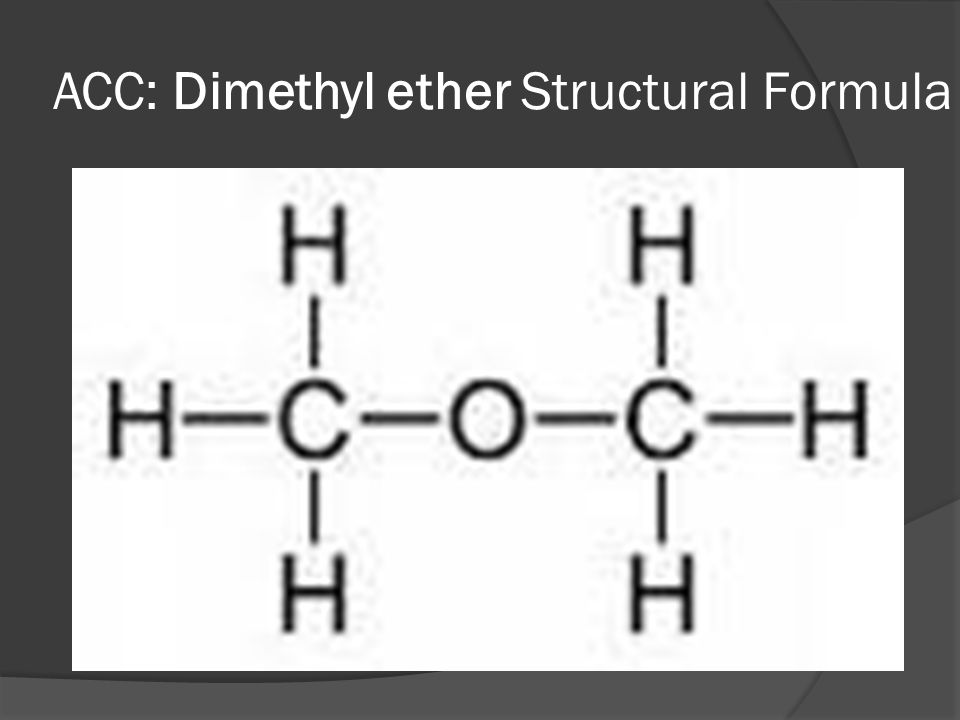 | Температура плавления диметилового эфира составляет -141 °C. |
| Точка кипения | |
| Температура кипения этанола 78,37 °C | Температура кипения диметилового эфира –24°C |
| Физическое состояние | |
| Этанол представляет собой бесцветную жидкость при комнатной температуре с высокой летучестью. | Диметиловый эфир представляет собой бесцветный газ при комнатной температуре. |
| Запах | |
| Этанол имеет характерный спиртовой запах. | Диметиловый эфир имеет типичный запах эфира. |
| Наличие гидроксильной группы | |
| Этанол имеет гидроксильную группу (-ОН). | Диметиловый эфир не имеет гидроксильных групп. |
Резюме – Сравнение этанола и диметилового эфира
Этанол и диметиловый эфир представляют собой органические соединения с одинаковой молекулярной массой, но разной химической структурой.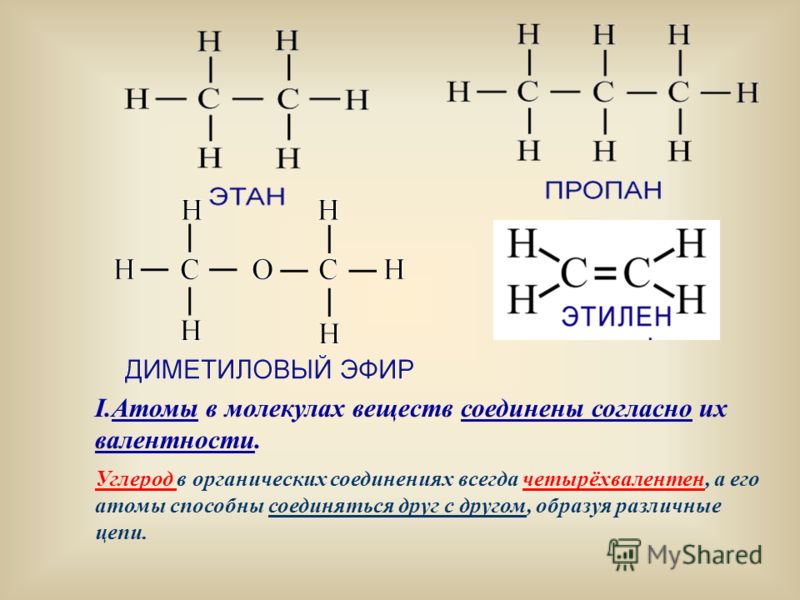

 2KB
2KB 58KB
58KB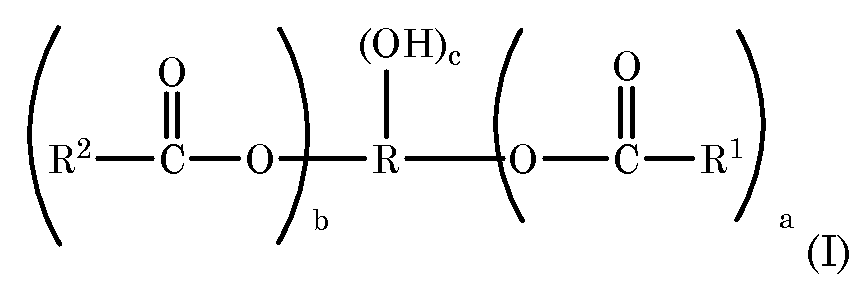 36KB
36KB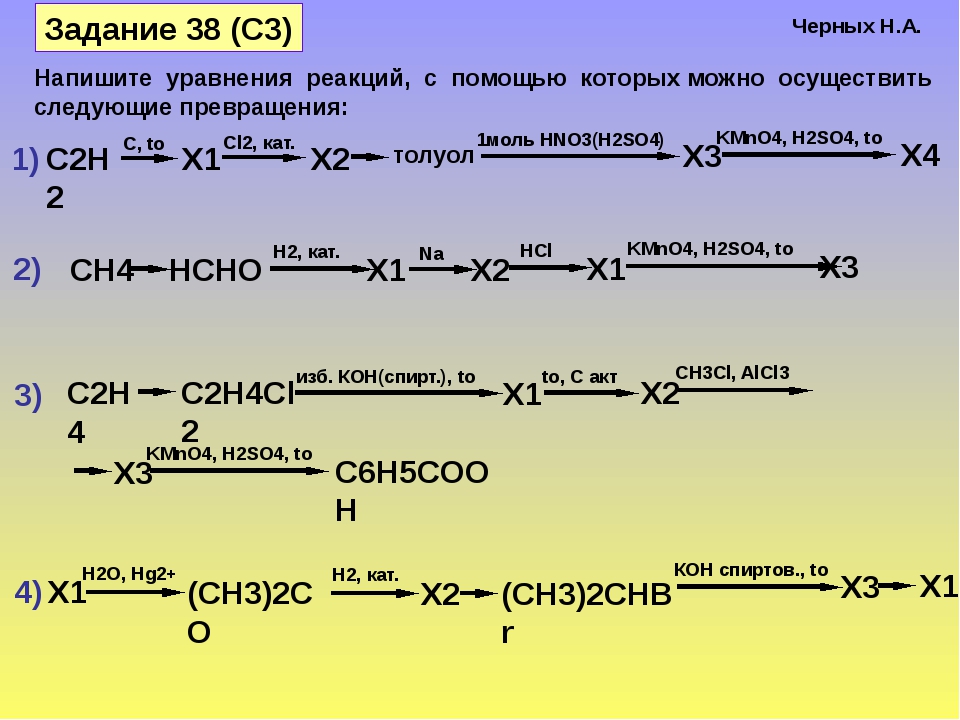 97KB
97KB 61KB
61KB 92KB
92KB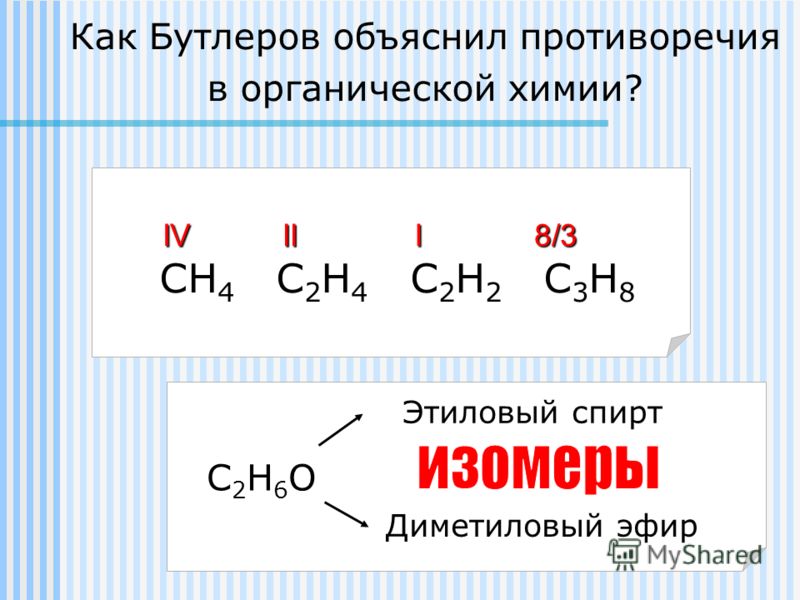 77KB
77KB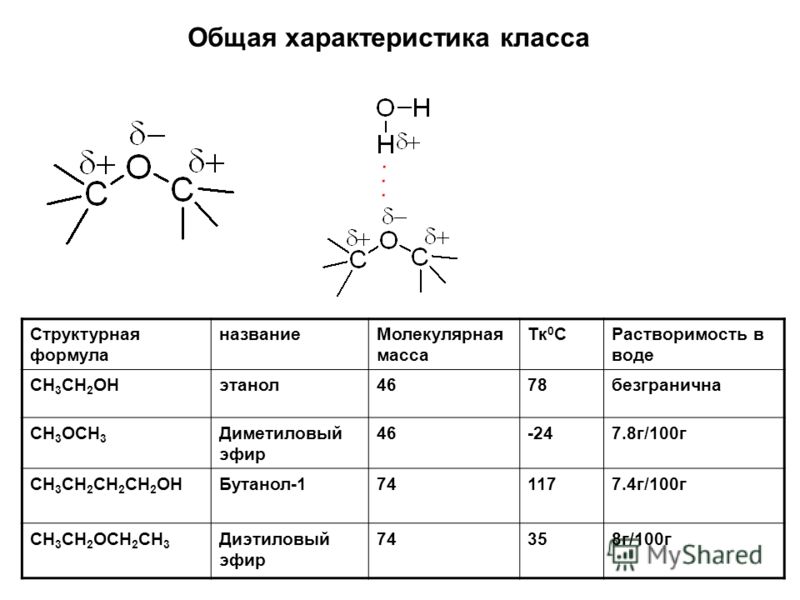 32KB
32KB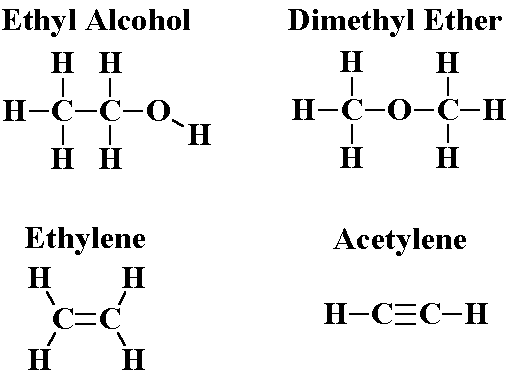 08
08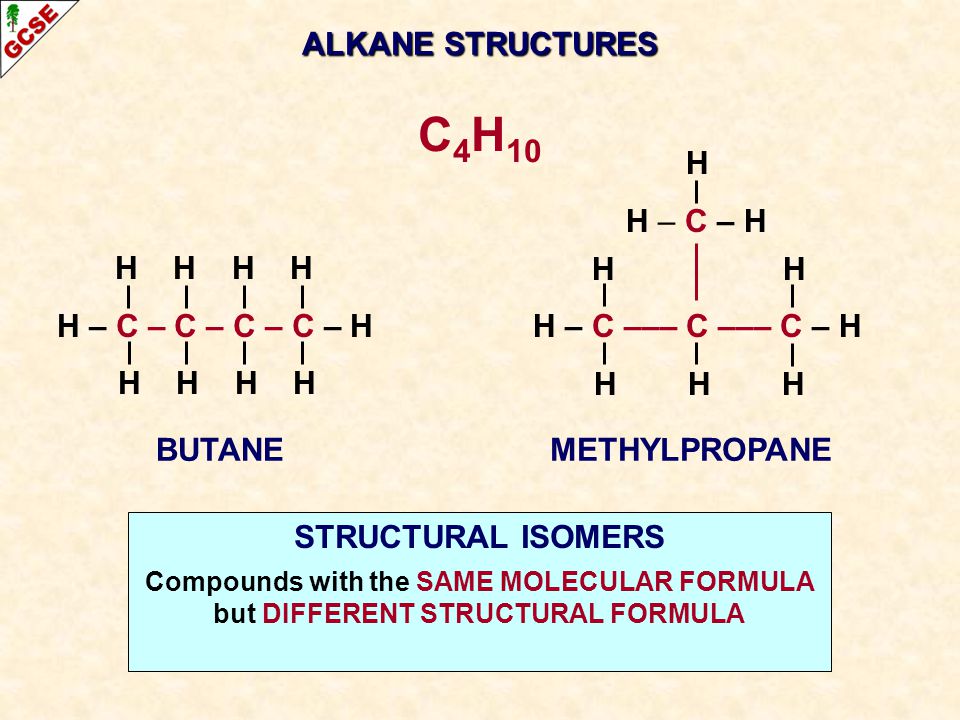 (Elsevier Scientific Pub. Ireland, Ltd., POB 85, Лимерик, Ирландия) V.1- 1973- Том (выпуск)/страница/год: 11,65,1978 *** ПРЕДЕЛЫ ВОЗДЕЙСТВИЯ НА ПРОФЕССИОНАЛЬНОМ ВОЗДЕЙСТВИИ *** OEL-ГЕРМАНИЯ: TWA 1000 частей на миллион (1910 мг/м3) ЯНВАРЬ 1993 *** РАЗРАБОТКА СТАНДАРТОВ NIOSH И ДАННЫЕ НАДЗОРА *** ДАННЫЕ ОБЗОРА НА ПРОФЕССИОНАЛЬНОМ ВОЗДЕЙСТВИИ NIOSH: 1974) Код опасности NOHS — 81811 Количество объектов: 897 (оценка) Количество отраслей: 7 Количество занятий: 12 Количество сотрудников: 50005 (оценка) NOES — Национальное обследование профессионального облучения (1983) NOES Код опасности — 81811 Количество объектов: 223 (оценка) Количество отраслей: 3 Количество занятий: 8 Количество сотрудников: 2282 (оценка) Количество женщин-сотрудников: 75 (оценка)
(Elsevier Scientific Pub. Ireland, Ltd., POB 85, Лимерик, Ирландия) V.1- 1973- Том (выпуск)/страница/год: 11,65,1978 *** ПРЕДЕЛЫ ВОЗДЕЙСТВИЯ НА ПРОФЕССИОНАЛЬНОМ ВОЗДЕЙСТВИИ *** OEL-ГЕРМАНИЯ: TWA 1000 частей на миллион (1910 мг/м3) ЯНВАРЬ 1993 *** РАЗРАБОТКА СТАНДАРТОВ NIOSH И ДАННЫЕ НАДЗОРА *** ДАННЫЕ ОБЗОРА НА ПРОФЕССИОНАЛЬНОМ ВОЗДЕЙСТВИИ NIOSH: 1974) Код опасности NOHS — 81811 Количество объектов: 897 (оценка) Количество отраслей: 7 Количество занятий: 12 Количество сотрудников: 50005 (оценка) NOES — Национальное обследование профессионального облучения (1983) NOES Код опасности — 81811 Количество объектов: 223 (оценка) Количество отраслей: 3 Количество занятий: 8 Количество сотрудников: 2282 (оценка) Количество женщин-сотрудников: 75 (оценка) ..
.. ..
.. , Ltd.
, Ltd.