Содержание
Простые эфиры
Диэтиловый эфир (его часто называют просто эфиром) —один из наиболее широко применяющихся в лабораторной практике растворителей. Он отличается хорошей растворяющей способностью и в то же время низкой температурой кипения, поэтому особенно удобен для извлечения — его легко испарить in вытяжек. При работе с эфиром следует учитывать, что он заметно растворим в воде [примерно 7% (масс.) при 20°C. Вода в небольшом количестве также растворяется в эфире (при 20 °С немногим более 1%).
Тетрагидрофуран и диоксан по растворяющей способности сходны с диэтиловым эфиром, но обладают более высокими температурами кипения и неограниченно смешиваются с водой. Некоторые свойства простых эфиров приведены в табл. 5.
Перечисленные вещества относятся к легковоспламеняющимся жидкостям. Особенно опасен в пожарном отношении диэтиловый эфир: он обладает при комнатной температуре очень высокой летучестью, его пары тяжелее воздуха и способны распространяться по поверхности рабочего стола, образуя с воздухом взрывоопасные смеси.
Простые эфиры и им подобные вещества при хранении, особенно на свету, способны окисляться кислородом воздуха с образованием чрезвычайно взрывоопасных пероксидов. При перегонке таких растворителей пероксиды концентрируются в перегонной колбе, в результате чего часто происходят взрывы. Перед работой с эфирами следует обязательно проверять, не присутствуют ли в них пероксиды. Для этого 2—3 мл эфира встряхивают в пробирке с равным объемом 2%-ного раствора иодида калия и несколькими каплями разбавленной серной или соляной кислоты. Бурое окрашивание (выделяется свободный иод) указывает на присутствие пероксидов.
Для очистки от пероксидов эфиры и их аналоги фильтруют через колонку с прокаленным оксидом алюминия; при этом удаляется также большинство примесей и вода. Фильтрование через колонку можно заменить встряхиванием с несколькими порциями оксида алюминия, общее количество которого должно составлять 10—15% от массы очищаемого растворителя.
Эффективный способ удаления пероксидов заключается в кипячении эфира над небольшим количеством порошкообразного едкого кали или едкого натра с последующей перегонкой. Применяют также встряхивание эфиров на холоду со свежеприготовленным раствором сульфата железа (II) FeS04. После очистки обязательно повторяют проверку на присутствие пероксидов.
Применяют также встряхивание эфиров на холоду со свежеприготовленным раствором сульфата железа (II) FeS04. После очистки обязательно повторяют проверку на присутствие пероксидов.
Основное количество воды удаляют из эфиров с помощью какого-либо дешевого осушителя, например прокаленного хлорида кальция. При необходимости более тщательной осушки растворители перегоняют над металлическим натрием и хранят над натриевой проволокой.
Диоксан и тетрагидрофуран рекомендуется хранить над гранулированной щелочью, чтобы обезвредить от пероксидов. Эффективными осушителями являются свежепрокаленный оксид алюминия и цеолит NaA.
Диоксан является сильным ядом с наркотическим действием, он избирательно влияет на печень и почки, вызывая в них необратимые изменения. Обладает кумулятивными свойствами, т. е. при регулярном вдыхании даже небольших количеств паров накапливается в организме, что усиливает вредное действие. ПДК в воздухе рабочей зоны 10 мг/м3.
Тетрагидрофуран сходно действует на организм, однако менее ядовит.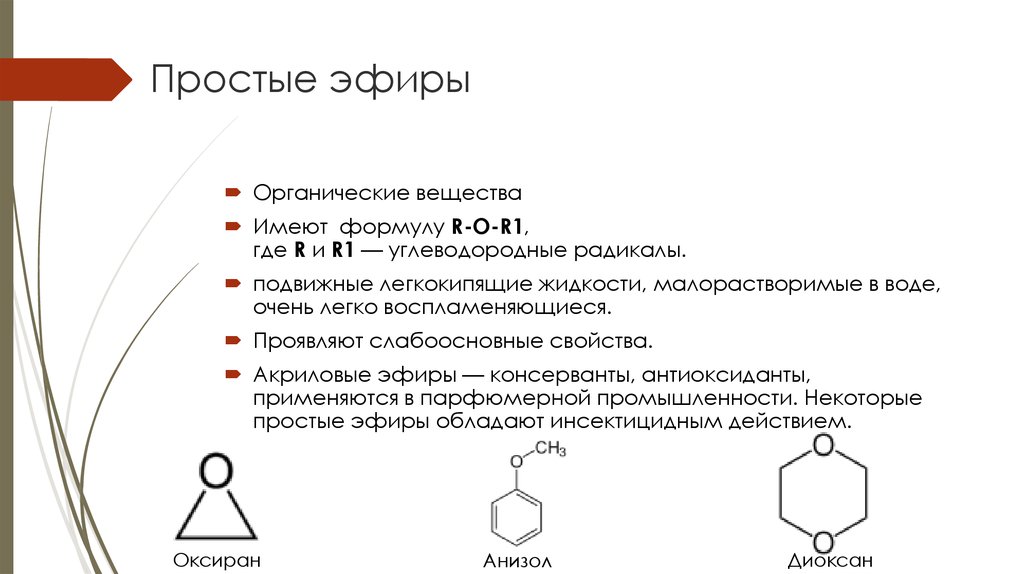 ПДК в воздухе рабочей зоны 100 мг/м3.
ПДК в воздухе рабочей зоны 100 мг/м3.
Пары диэтилового эфира обладают сильным наркотическим действием.
К оглавлению
см. также
- Алициклические углеводороды
- Ароматические углеводороды
- Хлорпроизводные углеводородов
- Простые эфиры
- Сложные эфиры
- Спирты
- Кетоны
- Карбоновые кислоты
- Амиды кислот
Простые эфиры
Читайте также
08.12.2022 в 09:40
Нейросеть Google предсказала запах молекул по их структуре
03.10.2022 в 11:33
Что такое блоттер, и как им правильно пользоваться?
Все статьи рубрики
Лучшие статьи
Моя отдушина: 4 аромата для успокоения и расслабления
8 лучших духов с запахом пиона: Dior, Ella K, Ex Nihilo
Радикальная роза и парижский мускус: знакомимся с ароматами Matiere Premiere
Синтетические джунгли: Encelade от Marc-Antoine Barrois
Дракон, Мисима, деконструкция: 3 японских по духу аромата
A Kiss from a Rose By Kilian: цветы и мускус на малой громкости
Субтропики, акация и звезды 1930-х: цветочные ароматы для летнего экватора
Интересные подборки
Лучшие ароматы для девушек
Духи для секса: самые возбуждающие феромоны и афродизиаки
Ароматы для горячей кожи
Ароматы с горчинкой для женщин
Лучшие сладкие ароматы для женщин
Духи для холодной кожи
Женские ароматы с нотой полыни
Стойкие духи для женщин
Женские ароматы с нотой ванили
Ароматы с нотой ландыша
Комментарии
Пожаловаться на материал
Анна Аскарова
28. 03.2016 в 00:00
03.2016 в 00:00
Ниже рассмотрены простые эфиры, применяемые в парфюмерно-косметическом производстве.
Дифенилоксид – кристаллическое бесцветное вещество, обладающее запахом герани и апельсина. Синтезируют это вещество взаимодействием хлорбензола и фенолята калия. Используют в качестве душистого вещества в приготовлении духов и одеколонов, также дифенилоксид входит в состав мыла и отдушек косметических средств.
Эвгенол – изомер, то есть они одинаковы по своему составу, имеют одну и ту же молекулярную массу. Но в то же время они различаются по своим физическим и химическим свойствам. Они имеют запах гвоздики, причем эвгенол имеет более грубый запах гвоздики. В промышленности предпочитают использовать изоэвгенол. Изоэвгенол содержится в больших количествах в масле мускатного шалфея и т.д. Сейчас изоэвгенол получают из синтетического гваякола.
Гваякол – химическое вещество, в женевской номенклатуре носит название ортометоксифенол.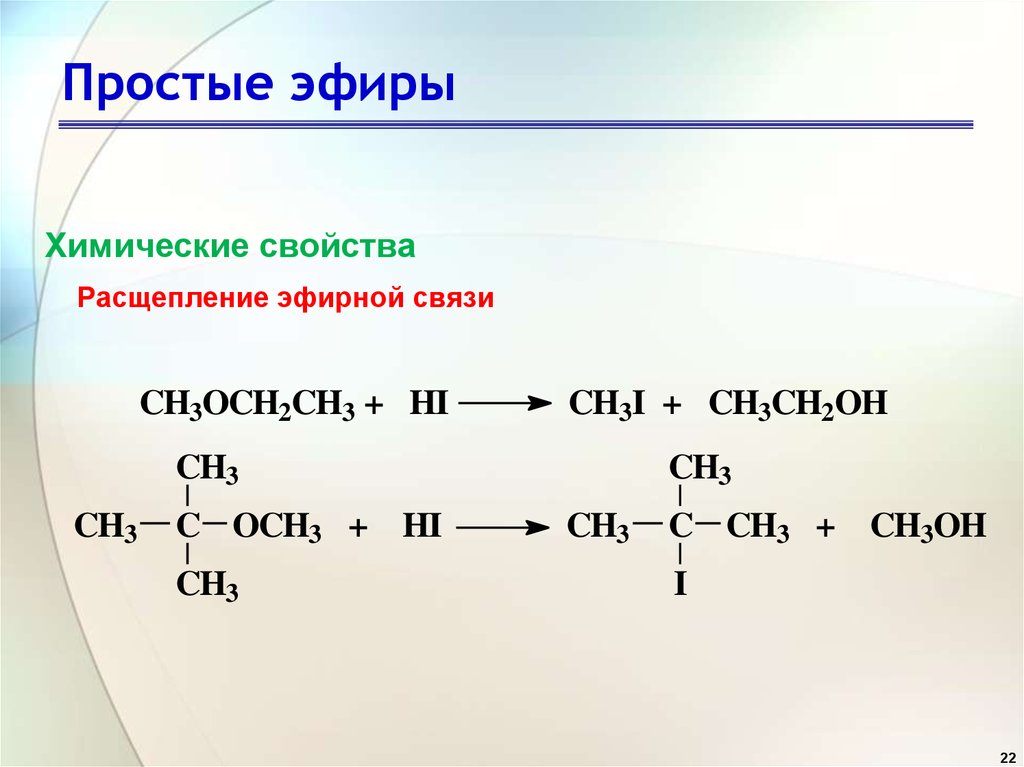
Этиловый и метиловый эфир. Этиловый (неролин — бромелия) спирт обладает фруктовым запахом, метиловый (яра-яра) – запахом черемухи. Оба применяются при изготовлении отдушек для синтетических моющих средств и для мыла. Оба эфира получают взаимодействием р-нафтола с одним из спиртов (метиловым или этиловым) с присутствием серной кислоты и с последующей сублимацией и очисткой.
Предложения от партнеров:
наборы парфюмерных пробников 8 в 1
Биосинтез эфиров: необычные или обычные природные явления?
Обзор
. 2010 март; 27(3):370-92.
дои: 10.1039/b809416k.
Epub 2010 2 февраля.
Пабло Домингес де Мария
1
, Роберт В. ван Гемерт, Адри Дж. Дж. Страатхоф, Ульф Ханефельд
принадлежность
- 1 Отдел технологий производства и производства, AkzoNobel BV, Velperweg 76, Арнем, Нидерланды.
 [email protected]
[email protected]
PMID:
20179877
DOI:
10.1039/b809416k
Обзор
Пабло Домингес де Мария и др.
Представитель Nat Prod.
2010 9 марта0003
. 2010 март; 27(3):370-92.
дои: 10.1039/b809416k.
Epub 2010 2 февраля.
Авторы
Пабло Домингес де Мария
1
, Роберт В. ван Гемерт, Адри Дж. Дж. Страатхоф, Ульф Ханефельд
принадлежность
- 1 Отдел технологий производства и производства, AkzoNobel BV, Velperweg 76, Арнем, Нидерланды.
 [email protected]
[email protected]
PMID:
20179877
DOI:
10.1039/b809416k
Абстрактный
Эфирные связи обнаружены в большом количестве природных продуктов, в основном вторичных метаболитах, включая липиды, оксираны, терпеноиды, флавоноиды, поликетиды и производные углеводов, и это лишь некоторые типичные примеры. Чтобы обеспечить такое биоразнообразие структур, большое количество различных ферментов участвует в нескольких различных путях биосинтеза. В зависимости от соединения и (микро)среды, в которой протекает реакция, простые эфиры образуются в результате очень разных (ферментативных) реакций, что дает впечатляющую демонстрацию того, как Природа объединила эволюцию и термодинамику, чтобы иметь возможность производить огромное количество соединений.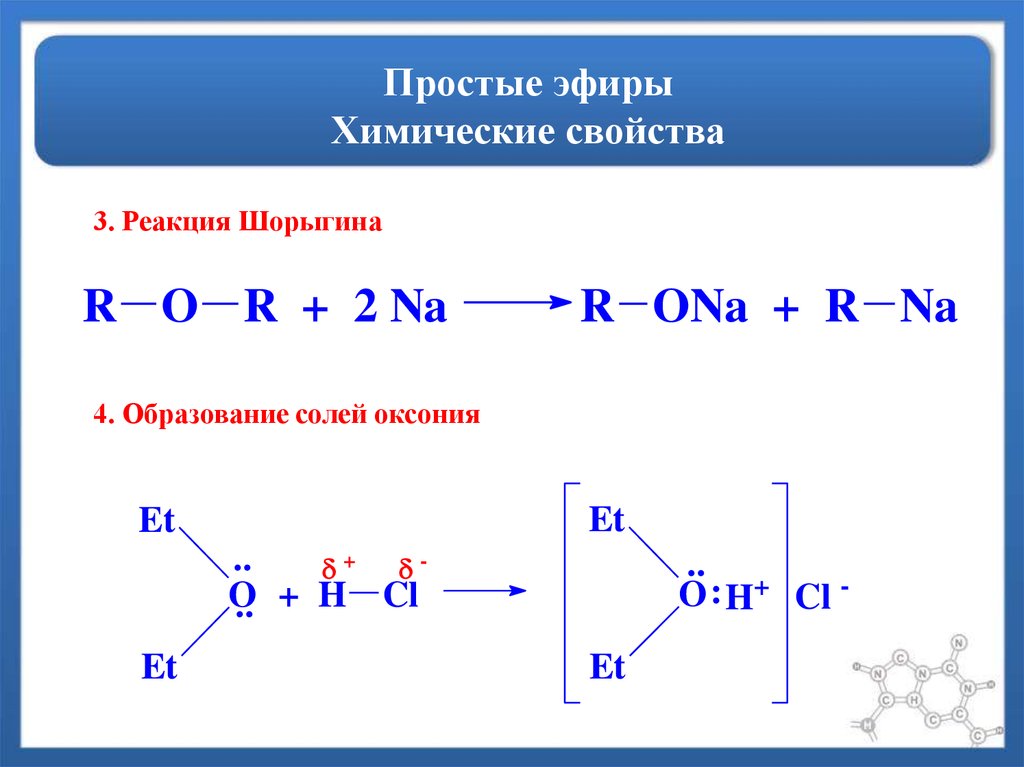 Кроме того, многие из этих соединений обладают различной биологической активностью, представляющей фармакологический интерес. Более того, некоторые из этих простых эфиров (например, эпоксиды) обладают высокой химической активностью и могут быть полезными исходными материалами для дальнейших синтетических процессов. Этот обзор направлен на то, чтобы предоставить обзор различных стратегий, которые встречаются в природе для образования этих «биоэфиров». Будут обсуждаться как фундаментальные, так и практические взгляды на процессы биосинтеза.
Кроме того, многие из этих соединений обладают различной биологической активностью, представляющей фармакологический интерес. Более того, некоторые из этих простых эфиров (например, эпоксиды) обладают высокой химической активностью и могут быть полезными исходными материалами для дальнейших синтетических процессов. Этот обзор направлен на то, чтобы предоставить обзор различных стратегий, которые встречаются в природе для образования этих «биоэфиров». Будут обсуждаться как фундаментальные, так и практические взгляды на процессы биосинтеза.
Похожие статьи
Большие эффекты от небольших изменений: возможные способы изучения химического разнообразия природы.
Боде Х.Б., Бете Б., Хёфс Р., Зик А.
Боде Х.Б. и соавт.
Химбиохим. 2002 г., 2 июля; 3 (7): 619-27. doi: 10.1002/1439-7633(20020703)3:73.0.CO;2-9.
Химбиохим. 2002.PMID: 12324995
Обзор.

Необычный биосинтез сахара и гликодиверсификация натуральных продуктов.
Thibodeaux CJ, Melançon CE, Liu HW.
Тибодо CJ и соавт.
Природа. 2007 г., 26 апреля; 446(7139):1008-16. doi: 10.1038/nature05814.
Природа. 2007.PMID: 17460661
Обзор.
Разработка натуральных продуктов с использованием комбинаторного биосинтеза и биокатализа.
Чжоу Х, Се Х, Тан Ю.
Чжоу Х и др.
Курр Опин Биотехнолог. 2008 Декабрь; 19(6): 590-6. doi: 10.1016/j.copbio.2008.10.012. Epub 2008 18 ноября.
Курр Опин Биотехнолог. 2008.PMID: 18992814
Обзор.
Терпеноиды: возможности биосинтеза лекарственных препаратов природного происхождения с использованием генно-инженерных микроорганизмов.

Аджикумар П.К., Тио К., Карлсен С., Муха О., Фон Т.Х., Стефанопулос Г.
Аджикумар П.К. и др.
Мол Фарм. 2008 март-апрель;5(2):167-90. doi: 10.1021/mp700151b. Epub 2008 21 марта.
Мол Фарм. 2008.PMID: 18355030
Обзор.
Терпеноидные биоматериалы.
Болманн Дж., Килинг С.И.
Болманн Дж. и соавт.
Плант Дж. 2008 г., май; 54 (4): 656-69. doi: 10.1111/j.1365-313X.2008.03449.x.
Завод Дж. 2008.PMID: 18476870
Посмотреть все похожие статьи
Цитируется
На пути к микробной переработке и переработке пластмасс: перспективы и проблемы.
Вершур Дж. А., Кусумавардхани Х., Рам А. Ф. Дж., Де Винд Дж. Х.
Вершуор Дж.А. и соавт.
Фронт микробиол. 2022 23 марта; 13:821629. doi: 10.3389/fmicb.2022.821629. Электронная коллекция 2022.
2022 23 марта; 13:821629. doi: 10.3389/fmicb.2022.821629. Электронная коллекция 2022.
Фронт микробиол. 2022.PMID: 35401461
Бесплатная статья ЧВК.Обзор.
Ферментативный синтез и антимикробная активность олигомерных аналогов лекарственных биополимеров из окопника и других видов семейства бурачковых.
Мерлани М., Шейбель Д.М., Барбакадзе В., Гогилашвили Л., Амиранашвили Л., Героникаки А., Катания В., Скиллачи Д., Галло Г., Гицов И.
Мерлани М. и др.
Фармацевтика. 2022 4 января; 14 (1): 115. doi: 10.3390/фармацевтика14010115.
Фармацевтика. 2022.PMID: 35057011
Бесплатная статья ЧВК.Эпоксидирование, катализируемое негемовой железо(II)- и 2-оксоглутарат-зависимой оксигеназой, AsqJ: механистическое объяснение переноса атома кислорода ферриловым промежуточным звеном.

Li J, Liao HJ, Tang Y, Huang JL, Cha L, Lin TS, Lee JL, Kurnikov IV, Kurnikova MG, Chang WC, Chan NL, Guo Y.
Ли Дж. и др.
J Am Chem Soc. 1 апреля 2020 г.; 142(13):6268-6284. дои: 10.1021/jacs.0c00484. Epub 2020 16 марта.
J Am Chem Soc. 2020.PMID: 32131594
Бесплатная статья ЧВК.Адаптация хемоферментативного окисления с помощью перкислот in situ.
Re RN, Proessdorf JC, La Clair JJ, Subileau M, Burkart MD.
Ре Р.Н. и соавт.
Орг Биомол Хим. 20196 ноября; 17 (43): 9418-9424. doi: 10.1039/c9ob01814j.
Орг Биомол Хим. 2019.PMID: 31650153
Бесплатная статья ЧВК.Катализируемые ферментами перегруппировки катионных эпоксидов в биосинтезе хинолоновых алкалоидов.
Цзоу Ю., Гарсия-Боррас М.
 , Танг М.С., Хираяма Ю., Ли Д.Х., Ли Л., Ватанабэ К., Хоук К.Н., Тан Ю.
, Танг М.С., Хираяма Ю., Ли Д.Х., Ли Л., Ватанабэ К., Хоук К.Н., Тан Ю.
Цзоу Ю и др.
Nat Chem Biol. 2017 март; 13(3):325-332. doi: 10.1038/nchembio.2283. Epub 2017 23 января.
Nat Chem Biol. 2017.PMID: 28114276
Бесплатная статья ЧВК.
Просмотреть все статьи «Цитируется по»
Типы публикаций
термины MeSH
вещества
Что такое эфиры в органической химии? ~ ChemistryGod
Эфиры представляют собой класс органических соединений, которые содержат атом кислорода, связанный с двумя алкильными или арильными группами с помощью одинарной ковалентной связи. В литературе они обозначаются суффиксом «-эфир». Например, диметиловый эфир или этилизопропиловый эфир.
Общее простое химическое представление простых эфиров — R-O-R’, где R и R’ представляют собой алкильные или арильные группы, связанные с атомом кислорода.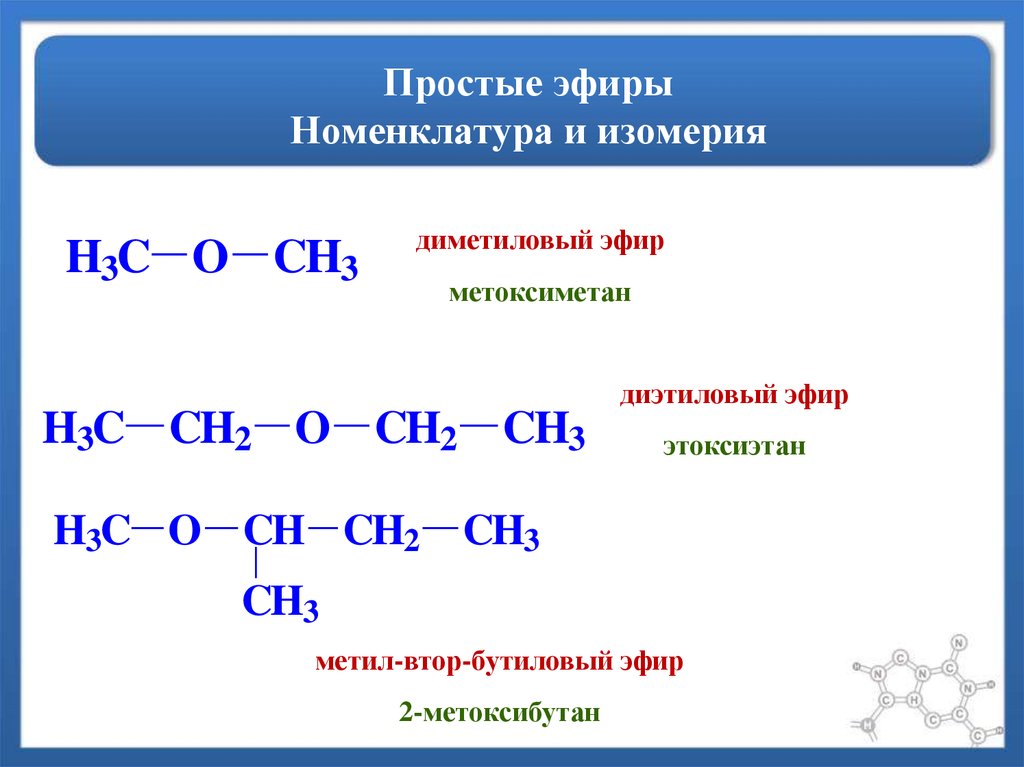 R и R’ могут быть одинаковыми или разными объектами.
R и R’ могут быть одинаковыми или разными объектами.
Примечание: R или R’ не может быть H; в противном случае она станет гидроксильной группой.
Эфирная функциональная группа
Простые эфиры представляют собой интересное химическое соединение, обладающее различными химическими и физическими свойствами по сравнению со спиртами, кетонами, альдегидами и карбоновыми кислотами.
Судя по геометрической форме эфирной группы, центральный атом кислорода находится в состоянии sp3-гибридизации. Таким образом, у нас есть четыре sp3-орбитали. Две из четырех используются для связи с R или R’, а оставшиеся две sp3-орбитали несут неподеленную пару электронов. Валентный угол между R-O-R’ меньше 120°. Это связано с тем, что две неподеленные пары электронов вызывают большее отталкивание, что уменьшает угол R-O-R’. В диметиловом эфире и диэтиловом эфире угол составляет около 110°.
Атом кислорода весит около 16, а углерода около 12. Итак, молекулярная масса любого эфира всегда больше 16 + 12 * 2 = 40 г/моль.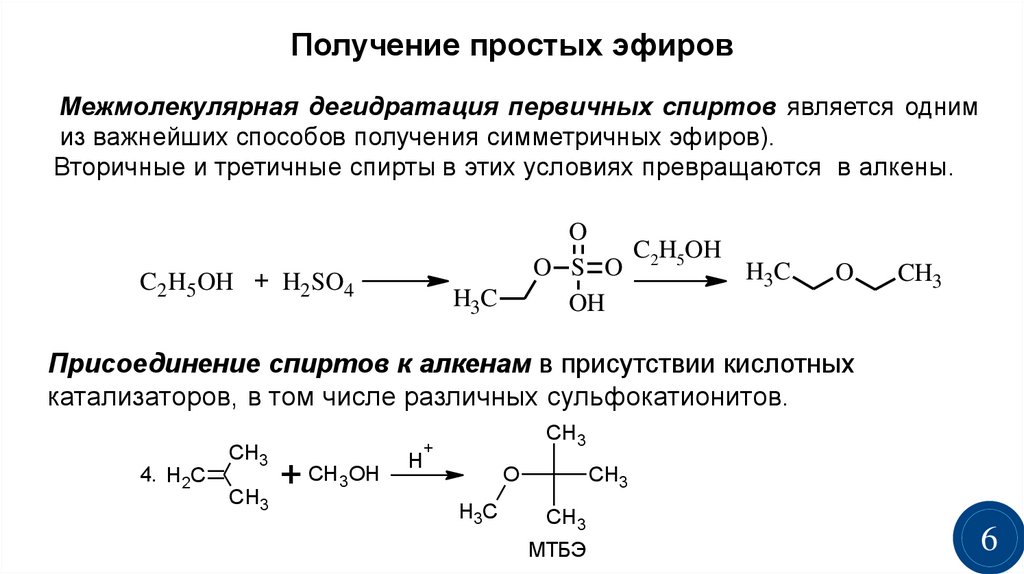 Простейшим эфиром является диметиловый эфир, т. е. две метильные группы, присоединенные к атому кислорода, и он имеет молекулярную массу 46 г/моль.
Простейшим эфиром является диметиловый эфир, т. е. две метильные группы, присоединенные к атому кислорода, и он имеет молекулярную массу 46 г/моль.
Простые эфиры являются основанием Льюиса, поскольку они имеют неподеленные пары на кислороде и имеют слегка щелочные значения pH. С другой стороны, спирты, альдегиды и карбоновые кислоты имеют кислую природу.
В спиртах (–OH), альдегидах (–CHO) и карбоновых кислотах (–COOH) атом кислорода непосредственно связан с водородом. А кислород гораздо более электроотрицательный, чем водород. Как следствие, эти химические группы могут легко потерять протон (ион Н+). В то время как в эфирах водород не находится в прямом контакте с кислородом, что затрудняет удаление протона. Кроме того, альфа-водороды (водороды, присоединенные к альфа-углероду) менее кислые, чем альдегиды и кетоны.
Эфиры – неполярные соединения, и молекулы эфира не образуют прочных водородных связей, как в спиртах и карбоновых кислотах. В результате они имеют более низкую температуру кипения, чем соответствующие спирты и карбоновые кислоты.
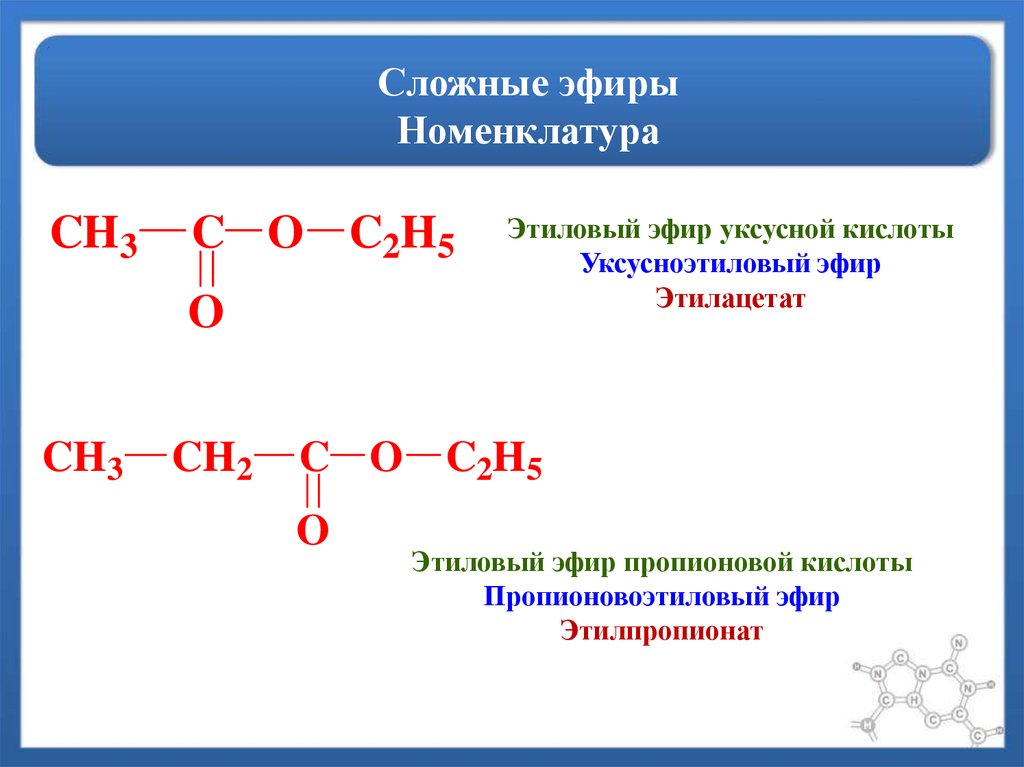
Номенклатура
Простые и меньшие эфиры обычно называют по общепринятой терминологии. Сначала идет алкильная часть с меньшими атомами углерода, например, метилэтиловый эфир. Здесь метил (–Ch4) является одноуглеродной группой, а этил имеет два атома углерода (–Ch3Ch4). Другим примером является метилфениловый эфир. Метил меньше фенила, поэтому ставится первым. Когда R одинаково, мы добавляем префикс di- к группе. Например, диэтилэтил (h4C–h3C–O–Ch3–Ch4) или дифениловый эфир (C6H5–O–C6H5).
Однако эта общепринятая методология не работает, так как сложность молекулы эфира возрастает. Как мы назовем 1,4,7,10-тетраоксациклододекан, используя этот метод?
Он имеет четыре атома кислорода и восемь атомов углерода, и это циклическое соединение. Мы не можем назвать это тривиальными приемами. Итак, мы движемся к номенклатуре IUPAC.
IUPAC
Номенклатура IUPAC делит молекулу эфира на две части: алкокси (–OR) и алкан (–R). Таким образом, метилэтил становится метоксиэтаном, диметиловый эфир становится метоксиметаном и так далее.
В приведенной ниже таблице перечислены некоторые распространенные эфиры с их именами IUPAC.
| Common name | IUPAC name |
| Dimethyl ether | Methoxymethane |
| Methyl ethyl ether | Methoxyethane |
| Diethyl ether | Ethoxyethane |
| Methyl phenyl ether | Methoxybenzene |
| Дифениловый эфир | Феноксибензол |
| Диизопропиловый эфир | 2-[(Пропан-2-ил)окси]пропан |
Производство
Эфиры получают в основном двумя промышленными способами: синтезом Вильямсона и дегидратацией эфирных спиртов.
Дегидратация спиртов
Спирты (R–OH) тесно связаны с простыми эфирами. Гидроксильная группа (-OH) спирта может быть преобразована в эфирную функциональную группу, если мы можем заменить H, присоединенный к O, на -R. Вот чего мы добиваемся обезвоживанием спиртов.
Вот чего мы добиваемся обезвоживанием спиртов.
Общее химическое уравнение:
R–OH + R–OH → R–O–R + h3O
Для реакции требуется кислая среда (серная кислота, h3SO4) и температура (≈125°C). Механизм реакции показан ниже:
Как и в приведенной выше реакции, протон атакует неподеленную пару электронов на кислороде. Это дестабилизирует связь углерод-кислород. Увидев возможность, неподеленная пара на кислороде другой молекулы спирта связывается с образованием промежуточного комплекса. Комплекс распадается на эфир, высвобождая молекулу воды и протон.
Важно отметить, что этот метод лучше всего подходит для получения симметричных эфиров. Когда реагирующая смесь содержит несколько спиртов, в качестве продуктов мы получим смесь простых эфиров. Это связано с тем, что несколько спиртов протонированы. Например, смесь метанола и этанола дает диметиловый эфир, диэтиловый эфир и метилэтиловый эфир.
Ch4–OH + Ch4Ch4–OH + H+ + тепло → h4C–O–Ch4 + h4C–h3C–O–Ch3–Ch4 + h4C–O–Ch3–Ch4
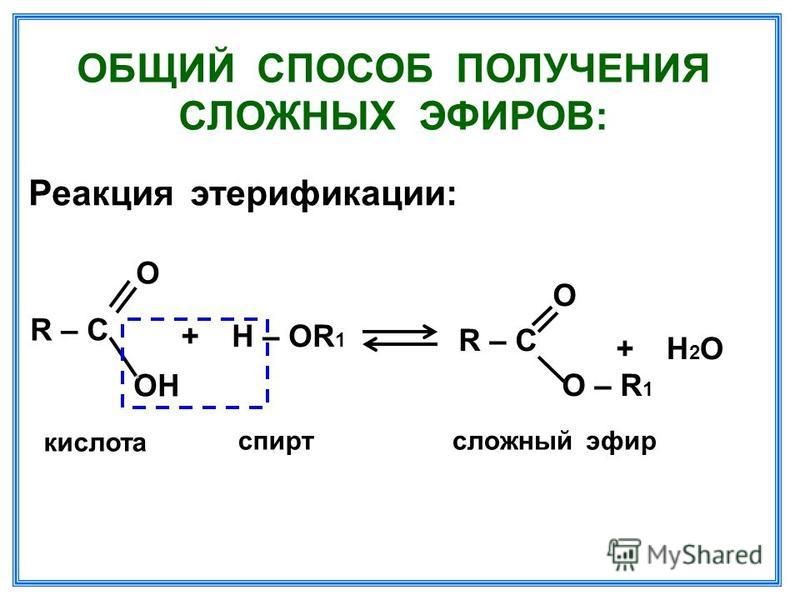
Синтез Вильямсона
Реакция Вильямсона представляет собой нуклеофильное замещение, которое можно использовать для получения асимметричных эфиров.
Реакция включает алкоксид и алкилгалогенид в качестве реагентов, а также эфир и галоидную соль в качестве продуктов.
Выполняется общая реакция:
R–ONa + R’–X → R–O–R’ + NaX
R–ONa – алкоксид натрия, R’X – алкилгалогенид, NaX – натриевая соль.
Алкоксид натрия можно легко получить путем обработки соответствующего спирта натрием.
2 R–OH + 2 Na → 2 R–ONa + h3 (газ)
Возьмем пример метилэтилового эфира:
2 Ch4–OH + 2 Na → 2 Ch4–ONa + h3 (газ)
Ch4–ONa + Ch4Ch3–Cl → Ch4–O–Ch3Ch4 + NaCl
Химическая активность
В отличие от других функциональных групп, простой эфир группа относительно стабильна. Связь C–O эфира стабильна и ее трудно разорвать. Таким образом, эфиры обладают низкой реакционной способностью. Низкая реакционная способность эфиров делает их очень полезными органическими растворителями. Диэтиловый эфир является очень распространенным растворителем, используемым в промышленности для производства различных промежуточных продуктов, фармацевтических препаратов, пластмасс и органических материалов.



 2022 23 марта; 13:821629. doi: 10.3389/fmicb.2022.821629. Электронная коллекция 2022.
2022 23 марта; 13:821629. doi: 10.3389/fmicb.2022.821629. Электронная коллекция 2022.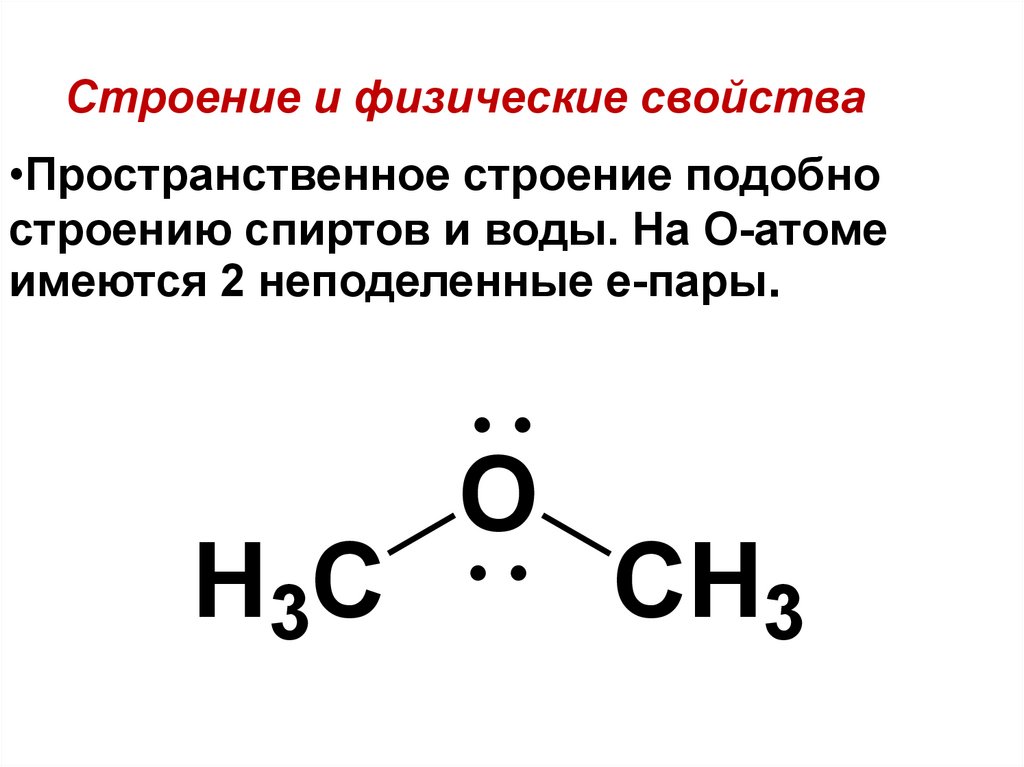
 , Танг М.С., Хираяма Ю., Ли Д.Х., Ли Л., Ватанабэ К., Хоук К.Н., Тан Ю.
, Танг М.С., Хираяма Ю., Ли Д.Х., Ли Л., Ватанабэ К., Хоук К.Н., Тан Ю.